Сравнить физические свойства воды и уксусной кислоты. Физические свойства воды и уксуса
Физические свойства уксусной кислоты, формула
Обычная бутылка пищевого уксуса, которую можно найти на кухне у любой домохозяйки, имеет в составе множество других кислот и витаминов. Добавление пары капель продукта в приготовленную пищу, салаты вызывает естественное усиление вкуса. Но мало кто из нас всерьез задумывался о свойствах и реальных масштабах применения основного компонента – уксусной кислоты.
Что это за вещество?
Формула уксусной кислоты СН3СООН, что относит ее к ряду жирных карбоновых кислот. Присутствие одной карбоксильной группы (СООН) относит ее к одноосновным кислотам. Вещество встречается на земном шаре в органическом виде и получается синтетическим путем в лабораториях. Кислота является самым простым, но не менее важным представителем своего ряда. Легко растворяется в воде, гигроскопична.
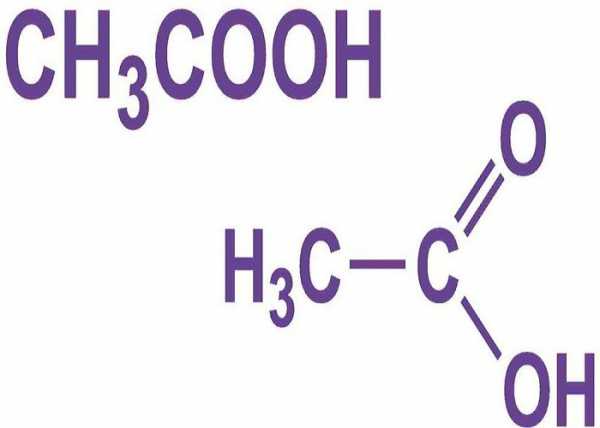
Физические свойства уксусной кислоты и плотность меняются в зависимости от температурного режима. При комнатной температуре в 20оС кислота находится в жидком состоянии, обладает плотностью 1,05 г/см3. Имеет специфический запах и кисловата на вкус. Раствор вещества без примесей твердеет и переходит в кристаллы на температуре ниже 17оС. Процесс кипения уксусной кислоты начинается при температуре свыше 117оС. Метиловая группа (СН3) формулы уксусной кислоты получается при взаимодействии спиртов с кислородом: брожение спиртовых веществ и углеводов, скисание вин.
Немного истории
Открытие уксуса было одним из первых в ряду кислот и совершалось поэтапно. Вначале уксусную кислоту стали добывать путем перегонки арабские ученые 8-го века. Однако еще в древнем Риме это вещество, полученное из скисшего вина, использовалось в качестве универсального соуса. Само название с древнегреческого переводится как "кислый". В 17 веке ученым Европы удалось добыть чистую субстанцию вещества. На тот момент они вывели формулу и обнаружили необычную способность – уксусная кислота в парообразном состоянии воспламенялась голубым огнем.
Вплоть до 19-го века ученые находили присутствие уксусной кислоты только в органическом виде - как часть соединений солей и эфиров. В составе растений и их плодов: яблок, винограда. В организме людей и животных: потовые выделения, желчь. В начале 20-го века русские ученые случайным образом добыли уксусный альдегид из реакции ацетилена с окисью ртути. На сегодня потребление уксусной кислоты на столько велико, что ее основная добыча происходит только синтетическим способом в огромных масштабах.
Способы добычи
Будет ли уксусная кислота чистого вида или с наличием примесей в растворе зависит от метода добычи. Пищевая уксусная кислота получается биохимическим методом в процессе брожения этанола. В промышленности выделяют несколько способов добычи кислоты. Как правило, реакции сопровождаются высокой температурой и наличием катализаторов:
- Метанол в реакции с углеродом (карбонилирование).
- Окислением фракции нефти кислородом.
- Пиролизом древесины.
- Окислением ацетальдегида кислородом.

Промышленный способ эффективнее и экономичнее биохимического. Благодаря промышленному способу, объем производства уксусной кислоты в 20-м и 21-м столетии вырос в сотни раз, по сравнению с 19-м веком. На сегодня синтез уксусной кислоты карбонилированием метанола дает боле 50% от всего производимого объема.
Физические свойства уксусной кислоты и влияние ее на индикатор
В жидком состоянии уксусная кислота бесцветна. Уровень кислотности pH 2,4 легко проверяется лакмусовой бумажкой. Уксусная кислота при попадании на индикатор окрашивает его в красный цвет. Физические свойства уксусной кислоты меняются визуально. Когда температура опускается ниже 16оС, вещество принимает твердую форму и напоминает мелкие кристаллы льда. Она легко растворяется в воде и взаимодействует с широким спектром растворителей, кроме сероводорода. Уксусная кислота снижает общий объем жидкости при разбавлении ее водой. Самостоятельно опишите физические свойства уксусной кислоты, ее цвет и консистенцию, которые вы наблюдаете на следующем изображении.

Вещество воспламеняется при температуре от 455оС с выделением теплоты в 876 кДж/моль. Молярная масса составляет 60,05 г/моль. Физические свойства уксусной кислоты как электролита в реакциях проявляются слабо. Диэлектрическая проницаемость равна 6,15 при комнатной температуре. Давление, как и плотность, – переменная величина физического свойства уксусной кислоты. При давлении 40 мм. рт. ст. и температуре 42оС начнется процесс кипения. Но уже при давлении в 100 мм. рт. ст. кипение произойдет только при 62оС.
Химические свойства
Вступая в реакцию с металлами и оксидами, вещество проявляет свои кислотные свойства. Прекрасно растворяя в себе более сложные соединения, кислота образует соли, которые называются ацетаты: магния, свинца, калия и др. Значение pK кислоты составляет 4,75.
При взаимодействии с газами уксус вступает в реакцию замещения с последующим вытеснением и образованием более сложных кислот: хлоруксусной, йодоуксусной. Растворяясь в воде, кислота диссоциирует с выделением ацетат-ионов и протонов водорода. Степень диссоциации равна 0,4 процента.
Физические и химические свойства молекул уксусной кислоты в кристаллическом виде создают диамеры на водородных связях. Также ее свойства необходимы при создании более сложных жирных кислот, стероидов и биосинтезе стеринов.
Лабораторные испытания
Обнаружить уксусную кислоту в растворе можно за счет выявления ее физических свойств, например запаха. Достаточно добавить в раствор более сильную кислоту, которая начнет вытеснять соли уксуса с выделением ее паров. Путем лабораторной перегонки Ch4COONa и h3SO4 возможно получить уксусную кислоту в сухом виде.
Проведем опыт из школьной программы по химии 8 класса. Физические свойства уксусной кислоты ярко демонстрирует химическая реакция расстворения. Достаточно добавить в раствор к веществу оксид меди и слегка нагреть его. Оксид полностью растворяется, делая раствор голубоватого цвета.
Производные вещества
Качественные реакции вещества со многими растворами образуют: эфиры, амиды и соли. Однако во время производства других веществ, требования к физическим свойствам уксусной кислоты остаются высокими. Она всегда должна иметь высокую степень растворения, а значит, не иметь сторонних примесей.
В зависимости от концентрации уксусной кислоты водного раствора выделяют ряд ее производных. Концентрация вещества более 96% имеет название - ледяная уксусная кислота. Уксусную кислоту в 70-80% можно приобрести в продуктовых магазинах, там она будет называться – уксусная эссенция. Столовый уксус имеет концентрацию 3-9 %.
Уксусная кислота и повседневная жизнь
Помимо пищевых особенностей, уксусная кислота обладает рядом физических свойств, которым человечество нашло свое применение в быту. Раствор вещества невысокой концентрации легко удаляет налет с металлических изделий, поверхности зеркал и окон. Способность впитывать влагу также играет на пользу. Уксус хорошо устраняет запахи в затхлых помещениях, удаляет пятна от овощей и фруктов на одежде.
Как выяснилось, физическое свойство уксусной кислоты – устранять жир с поверхности - может найти применение в народной медицине и косметологии. Слабым раствором пищевого уксуса обрабатывают волосы для придания им блеска. Вещество широко применяется для лечения простудных заболеваний, удаления бородавок и кожных грибков. Набирает темп использование уксуса в составе косметических обертываний для борьбы с целлюлитом.
Использование в производстве
В соединениях солей и других сложных веществ уксусная кислота выступает незаменимым элементом:
- Фармацевтическая отрасль. Для создания: аспирина, антисептических и антибактериальных мазей, фенацетина.
- Производство синтетических волокон. Негорючие пленки, ацетилцеллюлоза.
- Пищевая отрасль. Для успешной консервации, приготовления маринадов и соусов, в качестве пищевой добавки E260.
- Текстильная отрасль. Входит в состав красителей.
- Производство косметики и средств гигиены. Ароматические масла, крема для улучшения тонуса кожи.
- Изготовление протрав. Используется как инсектицид и протрава от сорняков.
- Производство лаков. Технические растворители, производство ацетона.

Ежегодно производство уксусной кислоты увеличивается. На сегодня его объем в мире составляет более 400 тысяч тонн в месяц. Транспортировка кислоты осуществляется в прочных цистернах из стали. Хранение в пластиковой таре на многих производствах в связи с высокой физической и химической активностью уксусной кислоты запрещено либо ограничено сроком до нескольких месяцев.
Безопасность
Уксусная кислота высокой концентрации имеет третью степень воспламенения и выделяет токсичные пары. Рекомендуется надевать специальные противогазы и другие средства индивидуальной защиты в процессе работы с кислотой. Смертельная доза для человеческого организма от 20 мл. В момент попадания вещества внутрь кислота в первую очередь обжигает слизистую оболочку, а затем поражает остальные органы. В таких случаях нужна немедленная госпитализация.
После попадания кислоты на открытые участки кожи рекомендуется сразу промыть их проточной водой. Поверхностный ожог кислотой может вызвать некроз тканей, что также требует госпитализации.
Интересные факты
Ученые физиологии выяснили, что человеку вовсе не обязателен прием уксусной кислоты - без пищевых добавок можно обойтись. Зато людям с непереносимостью кислоты, а также с проблемами желудка, вещество противопоказано.

Уксусная кислота используется в книгопечатании.
Вещество в небольшом количестве было найдено в меде, бананах и пшенице.
Охладив уксусную кислоту и резко взболтав с ней емкость, можно наблюдать ее резкое застывание.
Небольшая концентрация уксусной кислоты может снизить болевой симптом от укуса насекомых, а также мелких ожогов.
Прием в пищу продуктов с малым содержанием уксусной кислоты снижает уровень холестерина в организме. Вещество хорошо стабилизирует уровень сахара у диабетиков.
Употребление белковой и углеводной пищи вместе с небольшим количеством уксусной кислоты повышает их усвояемость организмом.
Если еда пересолена, достаточно добавить пару капель уксуса, чтобы сгладить солоноватость.
Напоследок
Тысячелетия использования уксусной кислоты привели к тому, что ее физические и химические свойства находят свое применение на каждом шагу. Сотни возможных реакций, тысячи полезных веществ, благодаря которым человечество идет дальше. Главное знать все особенности уксусной кислоты, ее положительные и отрицательные качества.
Не стоит забывать о пользе, но всегда надо помнить какой вред может причинить неосторожное обращение с уксусной кислотой высокой концентрации. По своей опасности она стоит рядом с соляной и серной кислотой. Всегда помните о технике безопасности при использовании кислоты. Правильно и осторожно разбавляйте эссенцию водой.
fb.ru
Физические свойства уксусной кислоты и ее соединений – ООО ДХЗ
Растворение уксусной кислоты в воде сопровождается выделением тепла и, следовательно, повышением температуры раствора. Однако выделение тепла происходит только при определенном соотношений уксусной кислоты и воды. При приготовлении значительно разбавленных растворов происходит поглощение тепла, и температура понижается.
Выделение тепла происходит в результате гидратации уксусной кислоты, которая присоединяет две молекулы воды. Теплота гидратации уксусной кислоты равна +0,755 кДж/моль С2Н4О2. При дальнейшем увеличении количества воды наблюдается поглощение тепла, которое при бесконечном разбавлении составляет -1,900 кДж/моль С2Н4О2 (теплота растворения уксусной кислоты). Так как теплота растворения включает в себя теплоту гидратации, то теплота растворения гидрата С2Н4О2 будет равна - 1,145 кДж/моль.

Других соединений уксусной кислоты с водой, по-видимому, не существует, так как кривая имеет только один минимум, отвечающий 62,5% СН3СООН. Впрочем, до концентрации 62,5% кривая имеет некоторую мало заметную выпуклость, а выше 62,5% также мало заметную вогнутость. Это указывает на существование других соединений уксусной кислоты с водой, которые, однако, не являются стабильными и ярко выраженными.
Впервые соединение уксусной кислоты и воды состава С2Н4О2•2Н2О было обнаружено автором и описано им в 1939 г. Образование гидрата СН3СООН•2Н2О подтверждено исследованиями А. А. Глаголевой, а также С.Я. Левитмана и Н.Ф. Ермоленко. Последними авторами по максимуму показателя преломления предположено также существование молекулярного соединения 2СН3СООН•Н2О.
При замораживании растворов, содержащих уксусной кислоты больше 62,5%, вымерзает более концентрированная кислота, а из растворов, содержащих менее 62,5%, вымерзают более разбавленные растворы. Этим свойством иногда пользуются в промышленности для получения более концентрированной уксусной кислоты из разбавленной.
Раствор, содержащий 62,5% уксусной кислоты, при охлаждении замерзает одновременно по всей своей массе (эвтектика). Точка замерзания такого раствора находится около -24°С. Все водные растворы при замерзании уменьшаются в объеме от нуля до 4,7% в зависимости от содержания уксусной кислоты, а при плавлении кристаллов объем соответственно увеличивается.

При перегонке водных растворов уксусной кислоты содержание кислоты в парах всегда меньше, чем в растворе. При этом разница между содержанием уксусной кислоты в парах и в жидкости увеличивается по мере того, как содержание кислоты в растворе приближается к величине, соответствующей гидрату С2Н4О2•2Н2О. Эта разница максимальна, когда содержание уксусной кислоты в растворе равно 62,5%.
Если водные растворы уксусной кислоты перегонять при разных давлениях, разность между содержаниями уксусной кислоты в жидкости и в парах изменяется, а именно; при повышении давления понижается, а при понижении давления - повышается. Поэтому ректификацию выгоднее вести под вакуумом, особенно при высоких концентрациях уксусной кислоты. Однако из практических соображений ректификацию обычно проводят при давлении, несколько превышающем атмосферное.
При высоких давлениях и более высоких концентрациях возможно активное образование азеотропа уксусной кислоты, а также воды. И тогда будет невозможным процесс разделения смеси ректификацией.
Содержание солей в водных растворах уксусной кислоты вызывает повышение содержания уксусной кислоты в парах при перегонке, а при определенной концентрации соли и кислоты возможно даже образование азетропа уксусной кислоты и воды.
www.dcpt.ru
Сравнить физические свойства воды и уксусной кислоты, химия
A) Горение магния cool Плавление льда C) Оседание речного песка в воде D) Смешивание порошков серы и железа E) кипение воды
2. Молярная масса железа равна А) 26 г/моль cool 56 г/моль C) 52 г/моль D) 112 г/моль E) 56
3. В формуле 2Na2S число атомов натрия и серы равны А) 1 и 2 cool 4 и 1 C) 2 и 4 D) 4 и 2 E) 2 и 1
4. Формула оксида Mn (VII) 1. MnO2 cool Mn2O7 C) Mn2O3 D) MnO3 E) MnO
5. В схеме реакции P+O2 ? P2O5 нужно поставить коэффициенты А) 4, 5, 2 cool 2, 1, 1 C) 2, 5, 2 D 5, 4, 2 E) 2, 4, 5
6. Уравнение реакции замещения это – A) 4Na + O2 = 2 Na2O cool CaCO3 = CaO +CO2? C) Zn + CuS = ZnS +Cu D) 2Mg + O2 = 2MgO E) 2h3 + O2 > 2 h3O
7. Железный гвоздь погруженный в раствор хлорида меди (II) покрывается красным налетом меди. Это пример реакции: A) Обмена cool Разложение C) Замещение D) Соединение E) неn такой реакции
8. Символ химического элемента марганца A) ?е cool Mg C) О D) Mn E) Mr
9. О химическом элементе, а не о простом веществе азоте идет речь в выражении A) Азот является составной частью воздуха cool В состав азотной кислоты HNO3 входит азот C) Формула азота N2 D) Жидкий азот иногда используется для замораживания продуктов E) азот инертный газ 10. Для алюминия не характерно физическое свойство A) Электропроводность cool Теплопроводность C) Серебристо-белый цвет D) Способность намагничиваться E) газ при обычных условиях
11. Признак, позволяющий назвать ржавление гвоздя химической реакцией – это:A) Выделение тепла cool Выделение газа C) Изменение окраски D) Появление запаха E) выпадение осадка
12. Сульфид железа – это сложное вещество, а не смесь потому что A) Его можно разделить магнитом на железо и серу cool Его можно разделить дистилляцией на железо и серу C) Состоит из атомов разного химического элемента и его нельзя разделить физическими методами на железо и серу D) Он нерастворим в воде E) газ при обычных условиях
13. 3.01 * 10 23 атомов железа составляют A) 2 моль cool 3 моль C) 1 моль D) 0,5 моль E) 1,5 моль
14. 69 г натрия составляют A) 3 моль cool 1 моль C) 6,3 моль D) 1,5 моль E) 0,5 моль
15.Фильтрованием можно разделить смесь: A) медных и железных стружек cool сахара и воды C) мела и воды D) воды и уксусной кислоты E) воды и бензина
16. Взаимодействие магния с кислородом относятся к реакциям: A) разложения cool обмена C) соединения D) замещения E) неn такой реакции
17. К химическим явлениям относятся: A) измельчение мрамора cool испарение воды C) таянье льда D) плавление меди E) сгорание угля
18. Где содержание железа наибольшее (определить массовую долю железа): A) FeO B)Fe2O3 C)Fe3O4 D) FeS E)FeF2
19.Чему равна валентность алюминия? А) 1 cool 2 C)3 D) 4 E) 5
20.Единицы измерения молярной массы: А) граммы cool грамм/ моль C) моль D) мелограмм E) нет единицы измерения
21. Молярная масса NaHCO3 равна: А) 156 cool 156 г/ моль C) 84 г/ моль D) 84 E) 84 л
22.Укажите реакцию разложения: А) 2h3 + O2 > 2 h3O cool 2Na +2h3O > 2NaOH + h3 C) C + O2 > CO2 D) 2Nh4 > N2 + 3h3 E) AgNO3 + HCl > AgCl +HNO3
23.Массовая доля кислорода в серной кислоте h3SO4 равна приблизительно : А) 16% cool 33% C) 65% D) 2% E) 17%
24.Автор закона сохранения массы вещества: А) Пруст cool Д.И.Менделеев C) Авогадро D) М.В.Ломоносов Е) Лавуазье
25.В каком из данных рядов расположены только металлы? А) K, Zn, Fe cool Si, Ca, Bi C)Al, C, Cr D) W, Os, В E) P, Au, Pb
26.Массовая доля серы в веществе SO2 равна : А)32 % cool 64% C) 50% D) 80% E) 12%
27.Масса сульфида цинка, образовавшегося при нагревании 10 г серы с цинком, равна : A) 12 г cool 30,31 г C) 25,6 г D) 10,5 г E) 32,4 г
28. Символ химического элемента криптона A)Ca cool Kr C) K D) Cd E) C
29. Веществом является A) Воздух B)медь C) Зеркало D) Гранит E) молоко
30. В списке физических свойств лишнее A) Плотность cool горение C) Теплопроводность D) Температура кипения E) температура плавления
himia.neznaka.ru
Урок 63. Муравьиная и уксусная кислоты. Физические свойства. Применение. Высшие карбоновые кислоты. Жиры. Роль жиров в процессе обмена веществ в организме.
Карбоновые кислоты, класс органических соединений, содержащих карбоксильную группу (карбоксил)

1. Простейшие представители карбоновых кислот – муравьиная и уксусная кислоты.
Муравьиная кислота НСООН
Впервые муравьиная кислота была открыта в 1670 г. английским естествоиспытателем Джоном Реем в выделениях муравьев, откуда и пошло это название.
Муравьи дают людям муравьиную кислоту. Около 70% содержимого ядовитой железы рыжего муравья – это муравьиная кислота.

Рыжий муравей


Муравьиная кислота содержится также в листьях крапивы (вызывает ожоги), в хвое ели.
Издавна люди использовали муравьиную кислоту как средство для лечения ревматизма. Использовали весьма своеобразным способом. Люди, страдающие подагрой, засовывали ноги в муравейник и некоторое время терпели укусы его обитателей. Иногда использовали крапиву. В начале XVIII в. ученые научились вовлекать муравьиную кислоту в реакции с различными спиртами, получая вещества с узнаваемыми запахами. Например, в реакции фенилэтилового спирта и муравьиной кислоты получали вещество с запахом хризантем; при нагревании бензилового спирта с муравьиной кислотой получали вещество с запахом жасмина.
Муравьиная кислота находит широкое применение в различных отраслях народного хозяйства. В технике кислоту и ее соли применяют в качестве протравы при крашении тканей, в кожевенном производстве – для отмывания извести, используемой при обработке шкур. В медицине смесь кислоты с водой, так называемый муравьиный спирт, используется как раздражающее кожу, рефлекторно действующее средство при ревматических и неврологических болях. Муравьиная кислота применяется в промышленном органическом синтезе в качестве восстановителя, а также для получения щавелевой кислоты. В пищевой отрасли промышленности ее используют в качестве дезинфицирующего и консервирующего средства.
Сложные эфиры муравьиной кислоты используют в качестве растворителей и душистых веществ. Муравьиная кислота обладает хорошим бактерицидным действием.
Уксусная кислота СН3СООН
Из всех кислот Она, конечно, прима, Присутствует везде И зримо, и незримо. В животных и растениях есть она, С ней техника и медицина навсегда. Ее потомство – ацетаты – Очень нужные «ребята». Всем известный аспирин. Он, как добрый господин, Жар больного понижает И здоровье возвращает. Это – меди ацетат. Он растеньям друг и брат, Убивает их врагов. От кислоты еще есть толк – Нас одевает в ацетатный шелк. А пельмени любит кто, Знает уксус тот давно. Есть еще вопрос кино: Хорошо всем надо знать, Что без пленки ацетатной нам кино не увидать. Конечно, есть и другие применения, И вам они известны, без сомнения. Но главное, что сказано, друзья, «Хлеб промышленности» уксусная кислота.
Уксусная кислота известна с древнейших времен (Китай, Египет, Вавилон) и была, очевидно, первой кислотой, которую узнал человек. Кислоту выделяли из уксуса, а последний получался при скисании вина. В 1648 г. немецкий химик И. Р. Глаубер обнаружил уксусную кислоту в подсмольной воде сухой перегонки дерева. В 1789 г. русский химик Т.Е.Ловиц впервые получил кристаллическую, так называемую ледяную уксусную кислоту. Ее химический состав был определен в 1814 г. шведским химиком Й. Я. Берцелиусом. Первый лабораторный синтез уксусной кислоты был осуществлен в 1845 г. немецким химиком А. В. Г. Кольбе.
Уксусная кислота широко распространена в природе. Она содержится в выделениях животных (моче, желчи, испражнениях), в растениях (в частности, в зеленых листьях). Эта кислота встречается как в свободном виде, так и в виде солей и эфиров, она присутствует в кислом молоке и сыре.
Уксусная кислота – жидкость, кислая на вкус, с резким запахом. Безводная уксусная кислота плавится при +16,6 °С, ее кристаллы прозрачны как лед, отсюда название ледяная уксусная кислота. Обычная техническая уксусная кислота имеет концентрацию 70–80%. Температура кипения 100%-й уксусной кислоты – 118 °C. Смешивается во всех отношениях с водой, спиртом, эфиром, бензолом. Ледяная уксусная кислота хороший растворитель многих органических веществ. Концентрированные растворы уксусной кислоты при попадании на кожу вызывают ожоги.
Уксусную кислоту используют при консервации и как приправу к пище. Из уксусной кислоты синтезируют лекарства, соли, ацетатный шелк, фруктовые эссенции, растворители лаков, красители для тканей, средства борьбы с насекомыми и болезнями растений, стимуляторы роста растений.
Уксусный ангидрид применяется в производстве пластических масс, искусственного шелка, ацетанилида.
Из монохлоруксусной кислоты получают негорючую кинопленку, органическое стекло, пропускающее ультрафиолетовые лучи. В результате применения 2,4-дихлорфеноксиуксусной кислоты и ее солей на полях с зерновыми погибают только широколиственные сорняки, что используется при выращивании зерновых культур.
Подобно минеральным кислотам в водных растворах карбоновые кислоты диссоциируют на ионы и изменяют окраску индикаторов (среда кислая):
СН3СОOН ↔ СН3СОО – + Н+.
Как и минеральные кислоты, они взаимодействуют с металлами, основными оксидами, основаниями и солями слабых летучих кислот:
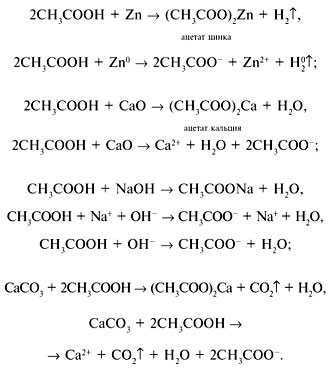
2. Высшие карбоновые кислоты – пальмитиновая и стеариновая кислоты.
СН3(СН2)14СООН, или С15Н31СООН – пальмитиновая кислота,
СН3(СН2)16СООН, или С17Н35СООН – стеариновая кислота.
Эти кислоты в виде сложных зфиров входят в состав жиров, поэтому их называют высшими жирными кислотами.
Мишель Эжен Шеврель совместно с А.Браконно установил, что большинство жиров состоит из стеарина и олеина, выделил стеариновую и пальмитиновую кислоты.
Пальмитиновая кислота – наиболее распространенная в природе жирная кислота, входит в состав глицеридов большинства животных жиров и растительных масел

(например, пальмовое масло содержит 39–47% пальмитиновой кислоты), а также в состав некоторых восков.

Пчелиный воск
Две вот эти кислоты,Словно сестры-близнецы,Вместе как они похожи,И тверды, и белокожи.
Итак, это твердые вещества, белого цвета, нерастворимы в воде, умеренно растворимы в спирте, эфире, хлороформе и других органических растворителях. Температура плавления стеариновой кислоты +69,3 °С, температура кипения от 360 до 370 °С. Химические свойства жирных кислот имеют свои особенности. Окраска водных растворов индикаторов не изменяется при добавлении порошков пальмитиновой и стеариновой кислот.
Эти кислоты растворяются в водных растворах едких щелочей и карбонатов, образуя соли, которые являются спутниками человека всю жизнь. К таким веществам относится мыло. Вспомним с детства знакомые строки:
«Да здравствует мыло душистоеИ полотенце пушистое!»
Натриевые и калиевые соли высших жирных кислот называют мылами. Они хорошо растворяются в воде, обладают моющим действием и составляют основу жидкого мыла (калиевые соли) и твердого мыла (натриевые соли). Водные растворы мыла имеют щелочную реакцию, т. к. соли подвергаются гидролизу.
Смесь пальмитиновой и стеариновой кислот используют для изготовления стеариновых свечей. Жирные кислоты превращают в соли и используют для получения различных мыл. Жидкое мыло (калиевые соли) по сравнению с твердым (натриевые соли) лучше растворимо в воде и поэтому обладает более сильным моющим действием.


Мыла имеют недостаток: они плохо моют в жесткой воде. Кроме того, щелочной характер мыла вреден для некоторых тканей. В связи с этим широко развивается производство синтетических моющих средств. Как и мыло, моющие средства обладают хорошим моющим действием и не утрачивают его в жесткой воде.
3. Другие карбоновые кислоты
Молочная Ch4- CH(OH) – COOH



образуется при скисании молока, квашении капусты, силосовании кормов. Она отличный консервант.
Щавелевая HOOC-COOH содержится в щавеле

При нарушении обмена веществ в организме человека образуются камни в почках,

представляющие собой оксалат кальция – соли щавелевой кислоты.
Щавелевую кислоту используют при производстве красителей и для удаления ржавчины.
4. Сложные эфиры.
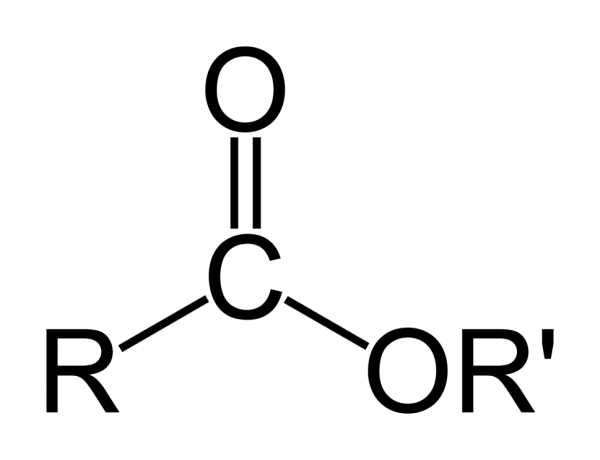
При взаимодействии карбоновых кислот со спиртами образуются сложные эфиры:
Сложные эфиры низших карбоновых кислот и спиртов представляют собой летучие, нерастворимые в воде жидкости. Многие из них имеют приятный запах. Так, например, бутилбутират имеет запах ананаса, изоамилацетат — груши и т. д. Сложные эфиры высших жирных кислот и спиртов — воскообразные вещества, не имеют запаха, в воде не растворимы. Приятный аромат цветов, плодов, ягод в значительной степени обусловлен присутствием в них тех или иных сложных эфиров.
Применение сложных эфиров
Сложные эфиры в природе
5. Жиры – это сложные эфиры глицерина и высших карбоновых кислот.
Жиры широко распространены в природе. Наряду с углеводородами и белками они входят в состав всех растительных и животных организмов и составляют одну из основных частей нашей пищи. По агрегатному состоянию при комнатной температуре жиры делятся на жидкие и твердые. Твердые жиры, как правило, образованы предельными кислотами, жидкие жиры (их часто называют маслами) — непредельными. Жиры растворимы в органических растворителях и нерастворимы в воде.
Классификация жиров
Сложные эфиры используются как растворители, ароматизирующие добавки в парфюмерной, фармацевтической и пищевой отраслях промышленности. Жиры – основной источник энергии в живых организмах. При расщеплении 1 г жира освобождается существенно больше энергии, чем в случае белков и углеводов. Жировые прослойки выполняют структурные и защитные функции (жировые капсулы сердца, печени, почек), теплорегулирующую функцию (у животных – обитателей Севера и Антарктиды очень развита жировая подкожная прослойка). Жиры являются источником эндогенной воды (горб верблюда), выполняют гормональные функции, например жировую природу имеют половые гормоны. Витамины одного из классов называются «жирорастворимые», и жиры пищи способствуют усвоению этих витаминов (к ним относятся, например, витамины А и D). Жиры используются для производства мыла и глицерина.
Применение жидких жиров
sites.google.com