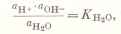Справочник химика 21. Вода разложение
вода разложения - это... Что такое вода разложения?
вода разложенияwater of decomposition
Русско-английский словарь по химии. 2013.
- вода перечной мяты
- вода с сосунов
Смотреть что такое "вода разложения" в других словарях:
ВОДА — ВОДА. I. Физико химические свойства и состав воды. Водные пространства мирового океана и морей составляют 361 млн. кв. км и занимают 71% всей земной поверхности. В свободном состоянии В. занимает самую поверхностную часть земной коры, т. н.… … Большая медицинская энциклопедия
Вода — хим. соединение водорода и кислорода. Весовой состав ее: 11,19% Н и 88,81% О. Молекулярная масса 18,0153. В молекуле В. имеется 10 электронов (5 пар): одна пара внутренних электронов расположена вблизи ядра кислорода, две пары внешних электронов… … Геологическая энциклопедия
ВОДА ПИРОГЕНЕТИЧЕСКАЯ — образуется за счет разложения орг. вещества твердых горючих ископаемых при сухой перегонке. Геологический словарь: в 2 х томах. М.: Недра. Под редакцией К. Н. Паффенгольца и др.. 1978 … Геологическая энциклопедия
Вода — С древнейших времен стали понимать великое значение воды не только для людей и всяких животных и растительных организмов, но и для всей жизни Земли. Некоторые из первых греческих философов ставили воду даже во главе понимания вещей в природе, и… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Вода — окись водорода, h30, простейшее устойчивое в обычных условиях химическое соединение водорода с кислородом (11,19% водорода и 88,81% кислорода по массе), молекулярная масса 18,0160; бесцветная жидкость без запаха и вкуса (в толстых слоях… … Большая советская энциклопедия
ВОДА, ЛЕД И ПАР — соответственно жидкое, твердое и газообразное состояния химического соединения молекулярной формулы Н2О. Историческая справка. Идея древних философов о том, что все в природе образуют четыре элемента (стихии): земля, воздух, огонь и вода,… … Энциклопедия Кольера
КОНСТИТУЦИОННАЯ ВОДА — вода, химически связанная с веществом, в которое она входит (неразличимая в виде «готовых» молекул Н2О). Молекулы Н2О образуются лишь в момент разложения вещества например, при нагревании: Са(ОН)2= СаО+Н2O … Металлургический словарь
Двойные разложения — (хим.). Под таким именем известны химические реакции, которые происходят между двумя веществами при обмене их составных частей, причем результатом взаимодействия получаются два новых соединения. В неорганической химии такими веществами являются,… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Реакции разложения — Реакции разложения химические реакции, в которых из одного, более сложного вещества образуются два или более других, более простых веществ[1]. Фактором, вызывающим разложение, могут являться различные физические воздействия. Соответственно … Википедия
Пресная вода в морском деле* — Испарители, опреснители. П. вода всегда составляла предмет первой необходимости на судах в морском плавании, но, главным образом, лишь для питья. В настоящее время потребление П. воды на новых судах усилилось, благодаря осознанной на практике… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Пресная вода в морском деле — Испарители, опреснители. П. вода всегда составляла предмет первой необходимости на судах в морском плавании, но, главным образом, лишь для питья. В настоящее время потребление П. воды на новых судах усилилось, благодаря осознанной на практике… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
chemistry_ru_en.academic.ru
Вода - разложение - Большая Энциклопедия Нефти и Газа, статья, страница 1
Вода - разложение
Cтраница 1
Вода разложения ( псдсмольная вода) содержит в себе растворенные химические вещества. Так, например, при дальнейшей химической переработке воды, полученной при сухой перегонке древесины и торфа, получают ацетон, уксусную кислоту, метиловый спирт, формалин и другие ценные продукты. [1]
Вода разложения подсмольная вода) содержит в себе растворенные химические вещества. Так, например, при дальнейшей химической переработке воды, полученной при сухой перегонке древесины и торфа, получают ацетон, уксусную кислоту, метиловый спирт, формалин и другие ценные продукты. [2]
Вода разложения, или подсмольная вода, в зависимости от исходного сырья содержит то или иное количество растворенных органических веществ. Особенно богата ими вода сухой перегонки древесины ( лесохимическая промышленность), из которой получают ацетон, уксусную кислоту, метиловый спирт, формалин. В несколько меньшей мере это относится и к воде разложения то ] фа. Сланцевые подсмольные воды содержат в некотором количестве фонол, ацетон и полифенолы ( резорцин, пирокатехин), буроугольная вода - фенолы, аммиак и карбоновые кислоты, угольная - фенолы. [3]
Пирогенетическая вода, или вода разложения, как ее называют в отличие от воды, выделяющейся при сушке топлива. [4]
Как видно из полученных данных, вода разложения в продуктах полукоксования не обнаружена, несмотря на то, что в органической массе смол имеется не менее 10 % кислорода. Нужно полагать, что кислород в смоле находится в формах, которые при термическом распаде не дают воды, образуя окислы углерода и нейтральные кислородные соединения. [5]
ЩГ) нах Дят вес образовавшейся при полукоксовании воды разложения - пирогенетиче-ской. [6]
При окислении углей в условиях комнатной температуры также выделяется большее или меньшее количество воды разложения. Для установления этого1 были проведены следующие опыты. [7]
Сухая перегонка заключается в нагревании топлива без доступа воздуха, благодаря чему из твердого топлива выделяется в парообразном состоянии вода разложения, а затем разлагается органическая часть топлива с выделением газообразных продуктов и смолистых веществ. Горючие газы, торфяной кокс, каменноугольный рыхлый неспекшийся кокс и полукокс используют как энергетическое и промышленное топливо; древесный уголь является хорошим газогенераторным и кузнечным топливом; плотный спекшийся кокс, полученный из коксующихся углей, используют в металлургической промышленности для выплавки металлов из руд. Из древесной и торфяной воды разложения и смолы вырабатывают спирт, парафин, воск и другие материалы. [8]
При нагревании топлива до 150 - 160 С из него выделяется гигроскопическая влага и окклюдированные, заключенные в порах, газы. Вода разложения органического вещества начинает выделяться при температуре - свыше 200 С, и это выделение продолжается до температуры 450 С и выше. [9]
Пает на очистку от примесей, которые могут вызвать коррплию аппаратуры при последующей ректификации алкилата. При очистке алкилат промывают водой дтп разложения комплексных соединений хлористого алюминия, латем отстаивают, смешивают со щелочью, снова отстаивают и промываю - ] водой. Очищенный таким обралом алкилат направляют па ректификацию. [10]
Расчетные кривые ( см. рис. 22) свидетельствуют о возможности дальнейшего повышения калорийности газа путем углубления сушки и предварительного термического разложения в сушилке. При предварительном термическом разложении и удалении части воды разложения и СО2 калорийность газа может быть даже несколько повышена. [11]
Из химических соединений, входящих в органическую массу твердого топлива, наименее устойчивыми являются гуми-новые кислоты. На начальной стадии процесса вследствие отщепления от гуминовых кислот карбоксильных групп ( СООН) выделяются углекислота и вода разложения - пиро-генетическая. [12]
Газовыделение Начинается ори температуре 240 - 260 С, а выделение жидких продуктов ( смолы) - при температуре 270 - 350 С. Критическим интервалом разложения топлива является температура 350 - 450 С, когда интенсивно выделяются смола, пи-рогенетичеокая - вода ( вода разложения) и газы. [13]
Процесс разложения твердого топлива схематически можно представить следующим образом. При нагревании топлива до 150 - 160 С из него выделяются гигроскопическая влага и окклюдированные, заключенные в порах газы. Вода разложения органического вещества начинает выделяться при температуре свыше 200 С, и это выделение продолжается до температуры 450 С и выше. Газовыделение начинается при температуре 240 - 260 С, а выделение жидких продуктов ( смолы) - при температуре 270 - 350 С. Критическим интервалом разложения топлива является температура 350 - 450 С, когда интенсивно выделяются смола, пирогенетическая вода ( вода разложения) и газы. [14]
Вода разложения, или подсмольная вода, в зависимости от исходного сырья содержит то или иное количество растворенных органических веществ. Особенно богата ими вода сухой перегонки древесины ( лесохимическая промышленность), из которой получают ацетон, уксусную кислоту, метиловый спирт, формалин. В несколько меньшей мере это относится и к воде разложения то ] фа. Сланцевые подсмольные воды содержат в некотором количестве фонол, ацетон и полифенолы ( резорцин, пирокатехин), буроугольная вода - фенолы, аммиак и карбоновые кислоты, угольная - фенолы. [15]
Страницы: 1 2
www.ngpedia.ru
Вода, разложение термическое - Справочник химика 21
Объяснение. Когда спираль не накалена, разложение паров воды не наблюдается. По мере усиления нагревания спирали реакция сдвигается в сторону разложения молекул воды. Разложение молекул воды происходит в непосредственной близости от раскаленной поверхности платиновой спирали. За счет процессов диффузии, а также за счет движения вверх молекул пара, продукты термической диссоциации выносятся из зоны реакции в газоизмерительную трубку. Здесь в пневматической ванне пары воды конденсируются, а газообразные кислород и водород поступают в измерительную бюретку. Опыт наглядно показывает зависимость скорости термической диссоциации воды от температуры. Чем выше температура поверхности платины, играющей в данном процессе роль катализатора, тем больше образуется в единицу времени гремучего газа. Следователь- [c.104] Физический смысл гН можно уяснить из следующего. Вода подвергается термическому разложению на водород и кислород [c.71]Гидрирование в эмульсиях, например восстаиовление ароматических динитросоединений в водной эмульсии. При этом улучшаются условия отвода реакционного тепла, облегчается выделение растворимого в воде диамина, предотвращается разложение термически нестабильных динитросоединений. [c.516]
Удаление внешней влаги, называемое сушкой, протекает даже и при комнатной температуре. С повышением температуры этот процесс становится еще интенсивнее и практически заканчивается при 105—110°С. В температурном интервале 100—200 "С из угля выделяются окклюдированные газы и начинаются процессы собственно термической деструкции в наиболее термически нестойких твердых топливах — торфах и некоторых молодых бурых углях. Основным продуктом этого процесса является вода, которая называется пирогенетической водой или водой разложения. Довольно трудно установить, когда заканчивается выделение гигроскопической влаги и начинается образование пирогенетической воды. В большинстве случаев это невозможно и поэтому нельзя с уверенностью определить начало термической деструкции. [c.243]
Для выражения степени окисленности можно использовать а) степень окисленности, вычисляемую на основе элементарного состава б) теплоту сгорания в) выход газа и воды при термическом разложении. [c.15]
Желто-коричневый, плавится без разложения, термически устойчивый. Плохо растворяется в холодной воде. Кристаллогидратов не образует. Не реагирует с разбавленными кислотами. Разлагается кипящей водой, царской водкой , щелочами, гидратом аммиака. Проявляет слабые окислительно-восстановительные свойства. Получение см. 88 , 887 . [c.447]
Белый, плавится без разложения. Термически устойчивый. Безводный порошкообразный К28 пирофорен в сухом воздухе. Хорошо растворяется в воде (сильный гидролиз по аниону). Реакционноспособный во влажном состоянии окисляется кислородом воздуха, присоединяет серу. Разлагается кислотами. Типичный восстановитель. Получение см. 43 , 63 [c.37]
Разложение воды. Процесс термического разложения воды можно описать следующими реакциями [c.330]
Белый, плавится без разложения, термически устойчивый. Хорошо растворяется в воде (гидролиз по аниону), создает сильнощелочную среду, переводит в раствор цинк и алюминий. Частично разлагается концентрированной серной кислотой. Вступает в реакции обмена. Получение см. 28, 29 330, 332. [c.174]
В обычном состоянии этот неметалл с формулой Э2 — бесцветный газ, не имеющий запаха и вкуса, негорючий и малорастворимый в воде, не поддерживающий горение и вообще химически весьма инертный. Только с литием он уже при комнатной температуре образует соединение ЫдЭ, а при нагревании реагирует с магнием, окисляя его до Получить Эд в лаборатории можно из его соединения ЭНд (действуя бромной водой) или термическим разложением соли состава (ЭН )(Э02). Что такое [c.232]
Красно-фиолетовый, плавится и кипит без разложения, термически устойчивый. Не растворяется в холодной воде, не реагирует с разбавленными кислотами. Разлагается кипящей водой. Восстанавливается кальцием, окисляется кислородом. Получение см. 688. [c.345]
Белый, плавится без разложения, термически устойчивый. Хорошо растворяется в холодной воде (гидролиз по аниону). Реагирует с горячей водой, кислотами. Вступает в реакции обмена. Образует изополисоединения. Получение см. 332, 342", 344 [c.179]
Не всегда при добавлении воды разложение сопровождается образованием тетрагалогенида кремния разложение водой может наступить раньше, чем начнется термическое разложение вещества, при этом некоторые вещества переходят в полимерные соединения кремния, которые при термическом разложении образуют Si . Карбид кремния образуется также при сожжении соединений, содержащих у одного атома кремния три атома галогена или атомы галогена и водорода. Такие соединения сжигаются при добавлении к навеске небольшого количества хромированного асбеста, асбеста и воды. [c.53]
Устойчивость к воздействию высоких температур — одно из характерных свойств амфиболовых асбестов. В настоящее время вопрос о поведении амфиболов при нагревании изучен достаточно широко. Термоаналитические исследования как природных, так и искусственных амфиболов химического состава, проведенные в различных газовых средах и в вакууме, в статических и динамических условиях [28], позволили выявить влияние этих параметров на процесс выделения воды, последовательность термических превращений, их механизм и изучить продукты разложения, С привлечением современных методов исследования рассмотрены многие другие вопросы, касающиеся окисления железа, явлений упорядочения и структурных превращений при нагревании. [c.137]
Запах сточных вод населенных мест, представляющий собой смесь запаха фекалий с запахами разложения жиров, белков, мыла и т. д., является довольно характерным. Он зависит от разложения хозяйственно-бытовых стоков и от того, какие в воде преобладают процессы — окислительные или восстановительные. Подобный запах могут иметь также некоторые сточные воды предприятий пищевой промышленности. Сточные воды от термической переработки угля имеют запах фенолов, смолы, сероводорода сточные воды химической промышленности имеют характерные запахи, зависящие от вида производства, например запах органических соединений сероуглерода, сложных и простых эфиров, спиртов, органических кислот, азотсодержащих соединений, меркаптанов, ацетилена и т. д. [c.38]
Нельзя считать, что пероксид водорода в данном процессе является лишь поставщиком кислорода в воде. Разложение пероксида водорода с образованием кислорода в воде протекает лишь при температуре выше 70 °С. Есть основание полагать,, что пероксид водорода образует с соединениями железа комплекс, термически разлагающийся с формированием на поверхности стали защитных пленок магнетита. В результате содержание соединений железа в воде, характеризующее интенсивность коррозии стали, после введения пероксида водорода уменьшается в 4,5—7 раз по сравнению с необработанной водой и достигает 20—30 мкг/л. [c.124]
Угли более высокой степени обуглероживания, имея меньшее содержание кислорода, чем менее обуглероженные, образуют меньше воды при термическом разложении и, отсюда, меньше пара, защищающего аммиак от разложения до элементарного [c.128]
Способы получения. Наибольшее промышленное значение из алкинов имеет ацетилен, получаемый в технике разложением карбида кальция водой или термической деструкцией углеводородов. [c.49]
Котуинит. Белый, плавится и кипит без разложения, термически устойчивый. Плохо растворяется в воде, еще меньше — в разбавленных хлороводородной и азотной кислотах. Кристаллогидратов ие образуег. Разлагается водяным паром, концентрированными кислотами, щелочами, гидратом аммиака. Окис ляется хлором, восстанавливается водородом. Вступает в реакции обмена и комплексообразования. Получение см. 258, 259. 262. 263. [c.134]
Начало и продолжительность реакций дегидратации зависят от парциального давления паров воды. Разложение карбонатов определяется парциальным давлением СОг и Ог в печи, обусловливающим окислительные реакции. В термоанализе веществ, склонных в процессе нагревания окисляться, необходимо соблюдать однородную степень окисления. При исследовании карбонатных пород пространство печи обычно заполняется инертным газом, препятствующим реакции окисления, которая способствует возникновению достаточно длительного и сильного экзотермического эффекта, накладывающегося на другие термические реакции в образце. Требуемая среда в пространстве печи создается за счет нагнетания в нее соответствующего газа. [c.21]
При дальнейшем движении парогазовой смеси ввер1Х соприкасающееся с ней топливо подвергается термическому разложению, в условиях отсутствия кислорода, т. е. топлива подвер-гаетоя сухой, перегонке с образованием газа, паров омолы н воды разложения. [c.302]
Указанные величины получены при относительной влажности щепы перед шахтой 8—11%. Расчетные кривые (см. рис. 22) свидетельствуют о возможности дальнейшего повышения калорийности газа путем углубления сушки и предварительного термического разложения в сушилке. График показывает, что при полном удалении влаги теплотворная способность газа может возрасти примерно до 3000 ккал1нм . При предварительном термическом разложении и удалении части воды разложения и СО2 калорийность газа может быть даже несколько повышена. [c.79]
Белый, плавится без разложения. Термически устойчивый. Безводный порошкообразный RbjS пирофорен в сухом воздухе. Хорошо растворяется в воде [c.44]
Снижение температуры разложения дитиофосфатов металлов отмечается в присутствии органических кислот, хлорированного парафина, пятисернистого фосфора, нефтяного сульфоната кальция [32]. Слеиновая кислота, так же как и вода, ускоряет термическое разложение дитиофосфатов, в то время как сверхщелочной сульфонат магния способствует реакциям окисления [зз]. [c.47]
М-р Хаукес приводит результаты, полученные в тех случаях, когда предполагалось наличие кислорода. Как указывается в его статье, если присутствует кислород или вода, наступает термическое разложение. В дальнейшем мы обнаружили, что при нагревании эластомера Е301 до 350° в течение 200 час конечная потеря неподвижной фазы составляет около 20%, дополнительно к потере в 50% при нагревании до 300°. Однако колонка после этого остается пригодной для последующей работы. [c.282]
Это уравнение получают из уравнений (2) и (7) следующим образом. Предположим, что при р1асчетах исходят из чистой вбды. Пусть ее количество до диссоциации будет 2а моля. После нагревания до той температуры, при которой измеряется диссоциация, количество недиссоциированной водй, если подверглось диссоциации 2а а молей, будет, очевидно, 2а(1—а). Так как из каждых двух разложенных термически олекул Н2О получаются 2 молекулы Н2 и 1 молекула О2, то количество присутствующего в равновесном состоянии водорода будет 2а-а, а количество кислорода — а-а. Таким образом, общее количество молекул или молей будет теперь [c.75]
chem21.info
вода разложения - это... Что такое вода разложения?
вода разложенияOil: water of decomposition
Универсальный русско-английский словарь. Академик.ру. 2011.
- вода разлившегося водоёма
- вода размыла берега
Смотреть что такое "вода разложения" в других словарях:
ВОДА — ВОДА. I. Физико химические свойства и состав воды. Водные пространства мирового океана и морей составляют 361 млн. кв. км и занимают 71% всей земной поверхности. В свободном состоянии В. занимает самую поверхностную часть земной коры, т. н.… … Большая медицинская энциклопедия
Вода — хим. соединение водорода и кислорода. Весовой состав ее: 11,19% Н и 88,81% О. Молекулярная масса 18,0153. В молекуле В. имеется 10 электронов (5 пар): одна пара внутренних электронов расположена вблизи ядра кислорода, две пары внешних электронов… … Геологическая энциклопедия
ВОДА ПИРОГЕНЕТИЧЕСКАЯ — образуется за счет разложения орг. вещества твердых горючих ископаемых при сухой перегонке. Геологический словарь: в 2 х томах. М.: Недра. Под редакцией К. Н. Паффенгольца и др.. 1978 … Геологическая энциклопедия
Вода — С древнейших времен стали понимать великое значение воды не только для людей и всяких животных и растительных организмов, но и для всей жизни Земли. Некоторые из первых греческих философов ставили воду даже во главе понимания вещей в природе, и… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Вода — окись водорода, h30, простейшее устойчивое в обычных условиях химическое соединение водорода с кислородом (11,19% водорода и 88,81% кислорода по массе), молекулярная масса 18,0160; бесцветная жидкость без запаха и вкуса (в толстых слоях… … Большая советская энциклопедия
ВОДА, ЛЕД И ПАР — соответственно жидкое, твердое и газообразное состояния химического соединения молекулярной формулы Н2О. Историческая справка. Идея древних философов о том, что все в природе образуют четыре элемента (стихии): земля, воздух, огонь и вода,… … Энциклопедия Кольера
КОНСТИТУЦИОННАЯ ВОДА — вода, химически связанная с веществом, в которое она входит (неразличимая в виде «готовых» молекул Н2О). Молекулы Н2О образуются лишь в момент разложения вещества например, при нагревании: Са(ОН)2= СаО+Н2O … Металлургический словарь
Двойные разложения — (хим.). Под таким именем известны химические реакции, которые происходят между двумя веществами при обмене их составных частей, причем результатом взаимодействия получаются два новых соединения. В неорганической химии такими веществами являются,… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Реакции разложения — Реакции разложения химические реакции, в которых из одного, более сложного вещества образуются два или более других, более простых веществ[1]. Фактором, вызывающим разложение, могут являться различные физические воздействия. Соответственно … Википедия
Пресная вода в морском деле* — Испарители, опреснители. П. вода всегда составляла предмет первой необходимости на судах в морском плавании, но, главным образом, лишь для питья. В настоящее время потребление П. воды на новых судах усилилось, благодаря осознанной на практике… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Пресная вода в морском деле — Испарители, опреснители. П. вода всегда составляла предмет первой необходимости на судах в морском плавании, но, главным образом, лишь для питья. В настоящее время потребление П. воды на новых судах усилилось, благодаря осознанной на практике… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
universal_ru_en.academic.ru
Вода, разложение - Справочник химика 21
Озон образуется в процессах, сопровождающихся выделением атомарного кислорода (радиолиз воды, разложение перекисей и др.), а также при действии на молекулярный кислород потока электронов, протонов, коротковолнового излучения, т. е. за счет радиохимических и фотохимических реакций. Цепную реакцию образования озона из кислорода можно представить схемой [c.321] Объяснение. Когда спираль не накалена, разложение паров воды не наблюдается. По мере усиления нагревания спирали реакция сдвигается в сторону разложения молекул воды. Разложение молекул воды происходит в непосредственной близости от раскаленной поверхности платиновой спирали. За счет процессов диффузии, а также за счет движения вверх молекул пара, продукты термической диссоциации выносятся из зоны реакции в газоизмерительную трубку. Здесь в пневматической ванне пары воды конденсируются, а газообразные кислород и водород поступают в измерительную бюретку. Опыт наглядно показывает зависимость скорости термической диссоциации воды от температуры. Чем выше температура поверхности платины, играющей в данном процессе роль катализатора, тем больше образуется в единицу времени гремучего газа. Следователь- [c.104]Электрохимическая очистка [5.18, 5.24, 5.36, 5.45, 5.55]. Метод основан на электролизе промышленных сточных вод путем пропускания через них постоянного электрического тока. В настоящее время существуют следующие основные направления электрохимической очистки сточных вод разложение примесей за счет анодного окисления и катодного восстановления удаление растворенных неорганических соединений с использованием полупроницаемых мембран (электродиализ) разложение примесей путем электролиза с использованием растворимых анодов и получением нерастворимых соединений, выпадающих в осадок. [c.495]
Удаление внешней влаги, называемое сушкой, протекает даже и при комнатной температуре. С повышением температуры этот процесс становится еще интенсивнее и практически заканчивается при 105—110°С. В температурном интервале 100—200 "С из угля выделяются окклюдированные газы и начинаются процессы собственно термической деструкции в наиболее термически нестойких твердых топливах — торфах и некоторых молодых бурых углях. Основным продуктом этого процесса является вода, которая называется пирогенетической водой или водой разложения. Довольно трудно установить, когда заканчивается выделение гигроскопической влаги и начинается образование пирогенетической воды. В большинстве случаев это невозможно и поэтому нельзя с уверенностью определить начало термической деструкции. [c.243]
Сколько литров водорода и сколько литров кислорода образуются при нормальных условиях, если подвергнуть 18 г воды разложению при помощи постоянного тока [c.151]
Разложение мыльного клея. В реактор 35, куда непрерывно поступает мыльный клей, одновременно подаются 92%-ная серная кислота и холодная вода. Разложение идет при температуре около 100° и сильном перемешивании. В результате разложения получаются жирные кислоты и сульфат натрия. Из реактора смесь жирных кислот и сульфата натрия спускается в аппарат 36, где при сильном перемешивании заканчивается реакция разложения. Смесь сырых жирных кислот с раствором сульфата натрия перекачивается в отстойник 38, в котором происходит отстаивание раствора сульфата натрия. [c.468]
Выход воды разложения на абсолютно сухую древесину О Выход кокса [c.35]
Смола. . . Кислота. . Швельгаз. . Вода разложения. . . . Кокс. . . [c.98]
Qв p — тепло испарения и нагрева воды разложения, ккал кг с. т. [c.104]
Тепло испарения и нагрева воды разложения ДИСП [c.117]
Образующиеся озониды — в высшей степени неустойчивые взрывчатые вещества, которые тотчас по получении (обычно в хлороформе) разлагаются водой. Разложение протекает по типу [c.270]
При нагревании древесины до 150,..160°С происходит главным образом сушка древесины, т.е. удаление содержащейся в древесине воды. Разложение компонентов древесины идет очень медленно, и на этой стадии химический состав древесины практически не изменяется и летучих продуктов не образуется. [c.354]
Не всегда при добавлении воды разложение сопровождается образованием тетрагалогенида кремния разложение водой может наступить раньше, чем начнется термическое разложение вещества, при этом некоторые вещества переходят в полимерные соединения кремния, которые при термическом разложении образуют Si . Карбид кремния образуется также при сожжении соединений, содержащих у одного атома кремния три атома галогена или атомы галогена и водорода. Такие соединения сжигаются при добавлении к навеске небольшого количества хромированного асбеста, асбеста и воды. [c.53]
Начало и продолжительность реакций дегидратации зависят от парциального давления паров воды. Разложение карбонатов определяется парциальным давлением СОг и Ог в печи, обусловливающим окислительные реакции. В термоанализе веществ, склонных в процессе нагревания окисляться, необходимо соблюдать однородную степень окисления. При исследовании карбонатных пород пространство печи обычно заполняется инертным газом, препятствующим реакции окисления, которая способствует возникновению достаточно длительного и сильного экзотермического эффекта, накладывающегося на другие термические реакции в образце. Требуемая среда в пространстве печи создается за счет нагнетания в нее соответствующего газа. [c.21]
Метод заключается в следующем [188]. Измельченный до 200— 325 меш поллуцит смешивают с водой до пастообразного состояния. Пасту обрабатывают 96%-ной h3SO4, расходуя на 1 кг поллуцита 0,73 кг h3SO4 и 0,25 кг воды. Разложение проводят в реакторе, нагревая 4 ч до 120—150° и перемешивая сжатым воздухом. Во время разложения в реактор вносят еще 0,17 кг воды на 1 кг поллуцита. Прекратив нагревание, твердые продукты реакции оставляют в аппарате на 1—2 ч для вызревания (за этот период дополнительно разлагается 2—3% поллуцита). Затем в реактор порциями заливают воду (11,7 л на 1 кг поллуцита). Непрерывно перемешивая воздухом, нагревают до кипе- [c.122]
Газовыдатение начинается три темшературе 240—260° С, а выделение жидких продуктов (смолы)—при темшературе 270— 350° С. Критическим интервалом разложения топлива является темлература 350—450° С, когда интенсивно. выделяются смола, пирогенетичеокая вода (вода разложения) и газы. [c.271]
При дальнейшем движении парогазовой смеси ввер1Х соприкасающееся с ней топливо подвергается термическому разложению, в условиях отсутствия кислорода, т. е. топлива подвер-гаетоя сухой, перегонке с образованием газа, паров омолы н воды разложения. [c.302]
Затем заменяют газоприводную трубку капельной воронкой и прн сильном охлаждении и размешивании прибавляют по каплям раствор 10 г концентрированной соляной кислоты [й 1,19) в 20 М.Л воды. Разложение заканчивают, когда реакционная смссь разделится на два прозрачных раствора. [c.293]
Обычно железную руду сначала обжигают (нагревают на воздухе) с целью удаления воды, разложения карбонатов и окисления сульфидов. Затем руду восстанавливают коксом в специальных печах — доменных печах (рис. 19.1). Руды, содержащие известняк или карбонаг магния, смешивают с кислым флюсом, содержащим избыток кремнезе- [c.546]
Из химических соединений, входящих в органическую массу твердого топлива, наименее устойчивыми являются гуми-новые кислоты. Так, разложение гуминовых ислот торфа и молодых бурых углей начинается при температурах, лежащих около 100° С [Л. 38, 99]. Однако, до 150—180° С для торфа и 200—230° С для углей разложение идет в весьма малой степени [Л. 100, 101]. На начальной стадии процесса вследствие отщепления от гуминовых кислот карбоксильных групп (СООН) выделяются углекислота и вода разложения — пиро-генетическая. Почти исключительное выделение только их продолжается до 200—250° С, когда вследствие более глубокого разложения органической массы топлива появляются СО, углеводородные газы и первые капли смолы (или дегтя). [c.268]
В опытах производился ряд замеров, позволивших судить о работе установки. Средняя продолжительность опытов составляла около 6 час. Влажность исходного топлива менялась от 10,3 до 37,0%. Выход лесохимикатов составлял (табл. 6) из лиственной древесины (смешанной) 3,7— 4,1% кислоты, 14—16% смолы из хвойной древесины 2,5—2,7% кислоты, 10—12% смолы. Количество выделяющейся воды разложения достигало 21,5%. Полученные данные указывают на достаточно полное разложение древесины в условиях работы топки-генератора. Благодаря тому, что расход греющего газа в топке-генераторе значительно [c.53]
Указанные величины получены при относительной влажности щепы перед шахтой 8—11%. Расчетные кривые (см. рис. 22) свидетельствуют о возможности дальнейшего повышения калорийности газа путем углубления сушки и предварительного термического разложения в сушилке. График показывает, что при полном удалении влаги теплотворная способность газа может возрасти примерно до 3000 ккал1нм . При предварительном термическом разложении и удалении части воды разложения и СО2 калорийность газа может быть даже несколько повышена. [c.79]
Из нитрила молочной кислоты. Нитрил молочной кислоты является а-оксинитрилом, изомерным этиленвдтангидрину. Однако при нагревании в присутствии катализатора он разлагается не на акрилонитрил и воду, а на ацетальдегид и воду. Разложение с образованием акрилонитрила проводили посредством предварительной этерификапии гидроксильной группы органической кислотой, летучей при температуре пиролиза (400—600°) [c.13]
После прибавления всего бромбензола реакционную колбу нагревают на водяной бане 1—1,5 ч до полного растворения магния. Затем хорошо охлаждают колбу снегом с солью, прибавляют еш е 30 мл абсолютного эфира и, заменив капельную воронку газопроводной трубкой, доходяш ей до дна колбы (примечание 3), пропускают 3—4 ч не слишком быстрый ток углекислого газа (из аппарата Киппа или из баллонов), высушив его предварительно пропусканием через две промывалки с серной кислотой (примечание 4). Затем заменяют газопроводную трубку капельной воронкой и, продолжая сильно охлаждать колбу, прибавляют по каплям раствор 24 мл концентрированной соляной кислоты в 24 мл воды. Разложение считают законченным, когда образуются два прозрачных раствора — эфирный и водный. Эфирный раствор отделяют, а водный дважды экстрагируют зфиром (по 20 мл эфира). Соединенные зфирные вытяжки повторно обрабатывают в делительной воронке 10%-ным раствором едкого натра. Щелочную вытяжку подкисляют разбавленной соляной кислотой (по конго) и выделившуюся бензойную кислоту отсасывают, промывают небольшим количеством холодной воды [c.325]
В тех случаях, ко -да требуется определить лишь скорость разложения озонида, можно каждые полчаса брать одинаковые количества свежей воды. Разложение протекает тогда несколько более гладко. Если найденные количества неразложившегося озопида нанести на ординаты, а соответствующее время — на абсциссы координатной системы, то получаются кривые, характеризующие различную степень разложения различных озонидов. > [c.84]
chem21.info
Вода, разложение электролитическое - Справочник химика 21
При этом водород необходимо отделить от диоксида углерода и других продуктов конверсии. Эту проблему еще нельзя считать разрещенной. Одним из основных методов получения водорода в недалеком будущем рассматривается электролиз на атомных электростанциях. Кроме водорода выделяется и кислород, который также может быть использован в промыщленности и быту. Кроме электролитического рассматриваются термохимические и фотохимические методы получения водорода. Термохимический метод получения может быть особенно перспективен при разработке термоядерных энергоустановок. Однако для применения этого метода необходимо рещить задачу разделения водорода и кислорода. Большой интерес вызывает фотохимический способ разложения воды с использованием биологических катализаторов. [c.392] Развитие отечественной электрохимии началось с выдающихся исследований В. В. Петрова по электролитическому разложению воды и других жидкостей (1801 г.). Он же впервые получил металлы электролизом их окислов. Вскоре (1805 г.) Ф. Ф. Гротгус разработал теорию электропроводности растворов (переход протонов от ионов к молекулам воды). Наряду с этим он заметил, что ... расщепление молекул. .. происходит до всякого действия электрического тока (1818 г.). В этом предположении содержится предвидение основных идей теории электролитической диссоциации. [c.7]Получение водорода (потребляемого в больших количествах при синтезе аммиака) осуществляется во многих случаях путем электролитического разложения воды. Ввиду очень малой электропроводности воды, для уменьшения расхода электроэнергии электролизу подвергают не чистую воду, а раствор такого электролита, ионы которого, отличные от и ОН", разряжаются много труднее, чем ионы Н+ и 0Н . В результате этот электролит практически полностью сохраняется, а вода разлагается на водород и кислород. К таким электролитам принадлежат, в частности, едкий натр, серная кислота. [c.447]
Изучение водородного перенапряжения позволяет выяснить механизм этой реакции и представляет большой интерес с теоретической точки зрения. Установленные при этом закономерности можно частично распространить и на другие электрохимические реакции, что значительно повышает теоретическую значимость работ по водородному перенапряжению. Изучение водородного перенапряжения имеет также большое практическое значение, потому что современная промышленная электрохимия является преимущественно электрохимией водных растворов, и процессы электролитического разложения воды могут накладываться на любые катодные и анодные реакции. Водородное перенапряжение составляет значительную долю напряжения на ваннах по электролизу воды и растворов хлоридов. Знание природы водородного перенапряжения позволяет уменьшить его, а следовательно, снизить расход электроэнергии и улучшить экономические показатели этих процессов. В других случаях (электролитическое выделение металлов, катодное восстановление неорганических и органических веществ, эксплуатация химических источников тока) знание природы водородного перенапряжения позволяет успешно решать обратную задачу — нахождение рациональных путей его повышения. Все эти причины обусловили то, что изучение процесса катодного выделения водорода и природы водородного перенапряжения всегда находилось и находится в центре внимания электрохимиков. [c.397]
Воды разложилось 2100 — 1575 = 525 (г), или 525 18 = = 29,17 моля (18 — грамм-моль Н2О). При этом, согласно уравнению электролитического разложения воды, выделяется 29,17 моля, или 58,34 г (2 29,17) водорода и 14,585 лю 7Я, или 466,72 г (32 14,585) кислорода. [c.159]
Одним из путей утилизации стоков ЭЛОУ может быть их использование в качестве сырья для получения активного хлора путем электролитического разложения хлористого натрия. Электролиз растворов поваренной соли известен давно, а полученный активный хлор применяется для обеззараживания воды, отбеливания тканей, бумаги и т.д. Для электролиза используют растворы поваренной соли, морскую воду и подземные высокоминерализованные воды. [c.96]
Аналогично, электролизом растворов ряда солей, щелочей и кислот получают кислород и водород вследствие электролитического разложения воды, хотя для реакции [c.300]
Слабые и сильные электролиты. Кислоты, основания и соли являются электролитами, т. е., будучи растворенными в каком-нибудь растворителе с высокой диэлектрической постоянной, и прежде всего, следовательно, в воде, они проводят электрический ток, сами одновременно подвергаясь разложению (электролитическое разложение). Некоторые из названных веществ обнаруживают электропроводность также в расплавленном, а иные даже и в твердом состоянии. [c.86]
В обычной речной воде тяжелая вода содержится в количестве около 1 5000. Немного более ее в морской воде. Для разделения обоих изотопных вод пользуются обычно тем, что при электролизе водных растворов скорость разложения НаО примерно в 5 раз больше скорости разложения ОдО. Поэтому при электролизе остаток постепенно обогащается тяжелой водой. Такое обогащение впервые наблюдали Юри и Осборн (1932) в старом электролите долго работавших технических электролизеров для получения водорода. Содержание 0 0 в нем обычно составляет /гвоо — /зооо- Из такого электролита Льюис и Макдональд (1933) получили первую порцию чистой тяжелой воды. Сейчас электролитическое обогащение тяжелой водой осуществлено в ряде лабораторий, в том числе у автора этой книги при ближайшем участии В. А. Александровича [c.46]
Рассчитайте теоретическое значение напряжения разложения электролита процесса хромирования [сернокислый раствор оксида хрома (VI) СгОз1, пользуясь термодинамическими функциями компонентов электрохимической реакции (не учитывать побочный процесс электролитического разложения воды). [c.201]
Азот для синтеза аммиака получают при разделении воздуха методом глубокого охлаждения. Водород получают различными методами конверсией метана, содержащегося в природном газе, попутных нефтяных газах, газах нефтепереработки и остаточных газах производства ацетилена методом термоокислительного пиролиза конверсией окиси углерода глубоким охлаждением коксового газа электролитическим разложением воды газификацией твердого и жидкого топлива. [c.33]
В то время как относительное различие в массе изотопов для всех элементов, кроме самых легких, невелико, основные изотопы водорода различаются по массе в два раза. Это обусловливает относительно большее различие их свойств и облегчает их разделение. Влияние различия изотопов более сильно проявляется в физических свойствах, но обусловливает также и некоторое различие химических свойств. Так, при электролизе несколько легче подвергаются разложению молекулы воды, содержащие легкий изотоп, а молекулы, содержащие тяжелый изотоп, постепенно накапливаются в электролитической ванне. Это дает возможность, проводя процесс, многократно полностью разделить изотопы во-п.орода. [c.48]
Поскольку на, практике электролитическое разложение воды осуществляется при напряжении, значительно превышающем 1,48 В. электролизеры всегда работают с выделением тепла. [c.114]
Характер процессов на электродах электролитической ячейки может быть различным. При пропускании электрического тока через ячейку, состоящую из платиновых электродов, опущенных в водный раствор серной кислоты, идет разложение воды. На аноде образуется кислород, а на катоде — водород. [c.326]
В современной промышленности электролитическое производство хлора и каустической соды основано на использовании двух различных методов электролиза с твердым катодом (диафраг-менный) и с ртутным катодом. Эти методы различаются по реакциям, протекающим на катодах. На твердом катоде в процессе электролиза происходит разряд ионов водорода, а в электролите образуется щелочь. На ртутном катоде разряжаются ионы натрия, в результате образуется амальгама натрия, которую выводят из электролизера и разлагают водой при этом выделяется водород и образуется щелочь. Освобождающуюся при разложении амальгамы ртуть возвращают в электролизер. [c.131]
Открыты три изотопа водорода — протий, обозггачается символом Н,, Н — дейтерий — символом D, IH — тритий — символом Т. Протий и дейтерий встречаются в природе, тритий синтезирован. В природном водороде содержание дейтерия достигает 0,02%. Дейтерий впервые был получен при электролизе природной воды в виде тяжелой воды D2O. В процессе электролитического разложения большого количества природной воды D2O концентрируется в остатке, так как при электролизе воды разряжение ионов происходит значительно быстрее, чем ионов D+. [c.246]
Таким путем определяют медь, свинец, висмут, кадмий и некоторые др. металлы. В качестве катода удобно брать металлическую ртуть, так как образование амальгам облегчает электролитическое выделение многих металлов. С другой стороны, на металлической ртути сильно затруднено выделение водорода, и поэтому легко избежать побочной реакции разложения воды под действием электрического тока. [c.221]
Электролиз водного раствора гидроксида натрия приводит к электролитическому разложению воды. Из уравнения (1) видно, что при выделении на аноде. 56 л Оз разложению подвергается 5 молей воды (90 г). [c.180]
На электролитической диссоциации воды и в других случаях на полярной структуре ее молекул основана значительная часть реакций разложения веществ действием воды (реакций гидролиза). [c.38]
Как видно из схемы, электролиз нитрата калия сводится к электролитическому разложению воды. Электролизу подвергаются только электролиты с подвижными ионами. Свободной подвижности ионы достигают либо при растворении электролита в воде, либо при переводе его в расплавленное состояние. [c.212]
Электрохимический способ получения водорода основан на электролитическом разложении воды Этот метод может иметь преимущества перед другими методами там, где по условиям технологии требуется газ высокой чистоты, не содержащий каталитических ядов, либо при наличии дешевой электроэнергии. Малые количества водорода, требуемые постоянно или периодически, целесообразно во всех случаях получать электролизом, как наиболее простым из известных способов. [c.337]
Водород всегда получают из воды. В частности, наиболее чистый водород получают для полупроводниковых целей электролитическим разложением воды в электролизерах, заполненных раствором КОН [c.313]
В любом кулонометрическом определении необходимо создать такие условия электролиза, при которых превращение определяемого вещества происходило бы со 100 %-ным выходом по току. В этом состоит одно из главных отличий кулонометрического анализа от обычного электрогравиметрического. Приложенное внешнее напряжение должно обеспечивать электролиз анализируемого вещества и в то же время быть недостаточным для возникновения побочных химических реакций, нарушающих 100 %-ный выход по току. Необходимо, в частности, полностью устранить возможность электролитического разложения воды. [c.512]
Водород для синтеза аммиака получают из водяного газа, электролитическим разложением воды, разложением водяного пара посредством раскаленного железа, которое при этом окисляется в закись железа. Процесс проводят в генераторах, нагретых до 700 —900". Железо востанановляется посредством водяного газа. После того, как в печи устанавливается подходящая температура, в нее пропускают водяной газ лля вытеснения воздуха. Затем вводится водяной пар, который выгоняет из печи последние следы воздуха и, реагируя с раскаленным железом, дает водород. Водород, полученный этим способом, содержит небольшие количества двуокиси углерода и сернистого водорода, от которых его освобождают с помощью извести. [c.139]
Кислород В чистом виде получают нагреванием марганцевокалиевой или бертолетовой соли или путем электролитического разложения воды. При электролитическом получении кислорода берут дестиллированную воду, кипятят ее для удаления растворенного воздуха, добавляют несколько процентов (10—15%) чистой серной кислоты и наливают ее в прибор для электролиза. Сила тока не должна превышать 0,1 й на 1 см электрода. 1 а дает в течение часа около 2 л [c.74]
Электрохимический способ получения водорода и кислорода основан на электролитическом разложении воды. Впервые этот способ был использован в 1789 г. Труствиком и Диманном. Первый электролизер для электрохимического разложения воды был. разработан Д. А. Лачиновым в 1888 г., причем в его патентах [c.108]
Так как перенапряжение выделения дейтерия на катоде примерно на 0,1 В выше, чем протия, при электролитическом разложении Природной воды происходит постепенное обогащение жидкой фазы дейтерием. Электролитическим путем тяжелая вода впервые была получена в 1932 г. в США Льюисом, а в СССР в 1934 г. Бродским. [c.127]
В принципе можно выбрать такую силу тока в электролитической цепи, чтобы она составляла менее 1 % величины диффузионного предельного тока. В этом случае мешающие реакции начинают протекать только после того, как прореагировало 99% определяемого вещества. Попрешность составляет, таким образом, менее —1%. Но проведение анализа при небольшой силе тока требует больших затрат времени. Поэтому обычно поступают по-другому в анализируемый раствор вво-.дят довольно большую концентрацию вспомогательного ре-.агента, окислительно-восстановительный потенциал которого немного больше окислительно-восстановительного потенциала определяемого иона. К началу электролиза определяемый ион опять восстанавливается или окисляется. В соответствии с уменьшением концентрации определяемого иона у поверхности электродов электродный потенциал снова возрастает, но только -ДО тех пор, пока его значение ие станет равным значению потенциала иона вспомогательного реагента. После этого окисляется или восстанавливается реагент. Поскольку его концентрация намного больше концентрации определяемого иона, обеспечивается дополнительная подача вещества путем диффузии к поверхности электродов. Электродные потенциалы остаются постоянными (не происходит разложения воды 100%-ный выход ло току), остается постояиным значение Яг, а следовательно, и г. Диффундирующий от электродов вспомогательный реагент, являющийся окислителем или восстановителем, реагирует в растворителе с определяемым ионом, и, таким образом, действует только как посредник. [c.274]
Для промышленных целей кислород получают фракционной перегонкой жидкого воздуха. Нормальная температура кипения О, равна — 183 С, тогда как для N3, второго основного компонента атмосферы, она равна — 196°С. Кислород высокой степени чистоты получают путем электролиза воды. Хотя вода недорогое и распространенное сырье для такого процесса, высокая стоимость электрической энергии делает электролитический способ получения элементного кислорода довольно дорогим. При выборе промышленного способа получения всякого вещества экономические соображения играют очень важную роль. В отличие от этого при выборе способа получения небольших количеств какого-либо вещества в лабораторных условиях главную роль играют соображения удобства. Обычным лабораторным способом получения О2 является термическое разложение хлората калия КСЮ3 с добавлением в качестве катализатора МПО2 [c.302]
Потенциал поляризованного электрода, когда начинается пе-тферывное разряжение ионов, называют потенциалом разряжения (выделения, растворения) катода или анода соответственно. По-тенццал разложения, перенапряжение и потенциал разряжения зависят от концентрации раствора, его pH, материала, формы, размеров и характера поверхности электродов, температуры, плотности тока и других факторов. С увеличением площади катода (анода) прн прочих равных условиях уменьщаются плотность тока и перенапряжение. Перенапряжение вызывает увеличение расхода электроэнергии при электролизе и нагревание электролитической ванны. Перенапряжение имеет максимальное значение, когда продукты электролиза — газообразные вещества, например при электролизе воды с использованием 30%-ного раствора КОН шод действием тока протекает реакция Н2(ж) = Нг(г)+7202(г). которая является сум- мой катодной и анодной реакций 2Н20(ж)+2е = Н2(г) + 20Н- и 20Н- = Н20(ж) +7202(г)+2е. В биполярной ванне с железными катодом и анодом при 0° С и давлении газов 760 мм рт. ст. и плотности тока 1000 А/м2 электролиз идет при напряжении 2,31 В. В этих условиях °г.э= 1,233 В Т1к = 0,2 В т]а = 0,22 В падение напряжения. в электролите, диафрагме и проводниках первого рода 0,65 В. Следовательно, к. п. д. напряжения около 53%. Если принять, что на выделение 1 г-экв водорода, занимающего в газообразном состоянии при давлении 760 мм рт. ст. и 0°С 11,2 л, требуется 96 487 КлХ 202 [c.202]
В результате взаимодействия между ионами воды и соли один из ионов поды связывается ионом соли в слабо-диссоциирующую частицу или труднорастворимое вещество, а другой нон воды накапливается в растворе, сообщая ему кислую или щелочную реакцию. Процесс обменного взаимоде11СТЕИя нонов соли с молекулами воды, в результате которого смещается равновесие электролитическо диссоциации воды, называется гидролизом (от греческих слов гидро — вода, лизис — разложение). [c.78]
В производстве хлора электролитическим разложением водного раствора хлорида натрия из электролизера выделяются хлор и водород — соответственно на аноде и катоде. При этом от анода отводится смесь хлора и водяных паров. Из этой смеси сначала конденсируют влагу при 20—30 °С, затем хлор полностью осушают купоросным маслом и применяют его как в газообразном, так и в ожиженном виде. Ожижают хлор или при Т 293 К, но после повышения давления до 1,4н-1,6 МПа, или при атмосферном (иногда пониженном) давлении с охлаждением до 223 К или при промежуточных условиях Т = 248-н268 К и Р = 0,3- -0,6 МПа. В первом случае для охлаждения применяют промышленную воду, во втором — хладон-30 (дихлорметан, Гдл = 176 К, 7 кип = 313 К), в третьем — водный раствор СаС1з. [c.60]
При предельном токе поляризация становится сколь угодно большой. На самом деле при увеличении напряжения на электродах начинаются новые процессы, например, разложение воды или выделение других ионов, если они присутствуют в растворе. Ток снова начинает расти. Это используется в полярографии. Поля-рограф — это электролитическая ячейка, в которой один из электродов (например, катод) представляет собой вытекающие в раствор из капилляра капельки ртути. Анод имеет большую по- [c.385]
Для получения электролитического марганца из карбонатных руд использованы электролизеры нагрузкой / -= 4000 А. Обогащенный нейтральный электролит, содержащий ГМп504 ач = 96 г/л, Г(МН4)25041 ач = 160 г/л ( ач = = = 1,144 г/см ), поступает в катодное пространство, где на титановых катодах осаждается металлический марганец с выходом по току В " 60 %. Обедненный по марганцу электролит протекает через диафрагму в анодное пространство, где на свинцово-серебряных анодах выделяется кислород и частично диоксид марганца 5,5%). Обедненный электролит, выходящий из ванны, содержит сульфата марганца Рмпзо. = 3,3% (мае.). Некоторое подщелачивание католита при выделении водорода приводит к частичному разложению сульфата аммония с выделением ЫН,, в количестве р н, = = 0,35 кг/кг Мп. Испарение воды с зеркала электролита принять рн.о = 0,90 кг/кг Мп. Разбрызгивание раствора и другие потери составляют р = 2,0 % от начального количества обогащенного электролита. [c.249]
Для определения числа переноса ионов гидроксила в растворе NaOH служит та же схема, что и в предыдущем случае (см. рис. 23). В электролитическую ячейку заливают 0,02 н. раствор NaOH, а титрование ведут с метиловым оранжевым раствором НС1. При электролизе в ячейке идет разложение воды. Расчеты производятся так же, как в предыдущем случае. [c.39]
Величины перенапряжения газов п особенно перенапряжение водорода приходится учитывать в теоретических расчетах и при проведении электролиза в водных кислых средах. В большинстве случаев высокие величины перенапряжения нежелательны (наиример, при электролитическом получении металлов, водорода), так как вызывают повышенный расход электроэнергии. Иногда повышенное перенапряжение оказывается полезным, поскольку оно препятствует протеканию нежелательных побочных процессов и создает благоприятт е условия для проведения других, практически цешилх электрохимических процессов. Так, например, благодаря высокому перенапряжению водорода на олове, свинце и цинке возможно выделение этих металлов из водных растворов соответствующих солей при помощи электролиза. Только благодаря высокому перенапряжению водорода на свинце возможна зарядка кислотных аккумуляторов (гл. VI, 86). Иначе на катоде выделялся бы водород и весь ток заряда расходовался бы на разложение воды. [c.322]
Выдающийся литовский физик и химик Т. Гроттус (Христиан Иоганн Дитрих) в 1805 г. впервые дал правильное теоретическое обоснование процессов разложения воды электрическим током и прохождения тока через растворы элек1 ролитов, что заложило основы теории электролитической диссоциации, основные положения которой сформулированы шведским химиком С. Аррениусом. Теория электролитической диссоциации Аррениуса была разработана применительно к водным растворам электролитов. По Аррениусу, кислоты — это электролиты, диссоциирующие в водных растворах с образованием ионов водорода, основания — электролиты, образующие в водных растворах ионы гидроксила [c.85]
Таким способом определяют медь, свинец, кадмий, висмут и другие металлы. В качестве катода удобно применять металлическую ртуть, так как образование амальгам облегчает электролитическое выделение многих металлов. С другой стороны, на металлической ртути сильно затруднено выделение водорода, поэтому легко избежать разложения воды электрическим током. Данным методом можно анализировать и смесь катионов нескольких металлов, выделяя из раствора электролизом сначала более электрополо- [c.512]
chem21.info