Способы умягчения воды. Умягчение воды
Термический способ умягчения воды — Всё самое интересное!
Чтобы закончить подраздел «Умягчение воды» раздела «Вода» и перейти дальше, осталось разобраться с одним-единственным оставшимся способом умягчения воды как такового. Он называется «термический способ умягчения воды«. Естественно, останутся другие технологии, например, технология обратного осмоса или нанофильтрации, которые также работают с жёсткостью воды. Но именно на специфических способах борьбы именно с жёсткой водой мы закончим подраздел Умягчение воды.
Термический способ умягчения воды — это интересный способ, при котором из воды удаляетя временная жёсткость (подробнее про временную жёсткость — в статьях «Жёсткая вода» и «Подробнее про жёсткость воды«) с помощью нагрева воды. То есть, для умягчения применяются именно те процессы, которые приводят к образованию накипи в обычных условиях. Другими словами, образование накипи тут — желательное явление.
На самом деле термическим способом умягчения воды вы пользуетесь почти что с детства — как раз с того возраста, когда вы научились ставить чайник на огонь. Другими словами, когда вы кипятите воду в чайнике, вы делаете так, чтобы часть солей жёсткости выпадала в осадок в виде накипи на чайнике. В результате вы пьёте чай с более мягкой водой, чем течёт из крана.

Соответственно, может возникнуть вопрос: «А сколько нужно времени кипятить воду, чтобы достичь нужного уровня мягкости воды?» Для того, чтобы ответить на него, нужно немного подумать.
Так, растворимость солей жёсткости падает с ростом температуры. Соответственно, чем выше температура, тем быстрее они выпадут в осадок. И чем дольше происходит обработка, тем полнее будет термическое умягчение воды. Соли жёсткости выпадают в осадок при нагревании по реакции (на примере гидрокарбоната кальция):
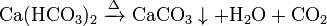
С точки зрения химического равновесия, чем быстрее будет улетучиваться углекислый газ, тем быстрее будут выпадать в осадок соли жёсткости. То есть, первый практический совет:
При термическом способе умячгения воды не полностью закрывайте крышку чайника (кастрюли), чтобы углекислый газ мог свободно улетучиваться.
Соответственно, если вы оставляете крышку закрытой, то углекислый газ не может свободно улетучиваться и замедляет скорость выпадения солей жёсткости в осадок. С другой стороны, полностью открытая ёмкость при кипячении приведёт к быстрому испарению воды, что не очень хорошо, поскольку при этом растёт общее содержание солей и вкус воды ухудшается.
Таким образом, нужно найти оптимальное положение крышки на чайнике для вашей собственной жёсткой воды.
Далее, второе следствие из реакции термического осаждения солей жёсткости с точки зрения химического равновесия — чем больше солей жёсткости (т.е. чем выше жёсткость воды), тем быстрее будет происходить выпадение в осадок. То есть, практический вывод таков:
если у ваша вода имеет жёсткость меньше 4 мг-экв/л (4 ммоль/л), то термически умягчать такую воду не стоит.
Всё потому, что осаждение солей жёсткости будет происходить слишком медленно, и испариться слишком много воды, отчего вкус её может ухудшиться (что для себя определяет каждый отдельно взятый человек, поскольку на вкус и цвет товарища нет).
Конечно, мы обещали назвать точное время, за которое все соли жёсткости выпадут в осадок. К сожалению, так просто называть это время нельзя, потому что очень сложно учесть все параметры — и температуру воды, и жёсткость воды, и то, насколько открыта крышка, и как много в воде углекислого газа и т.д.
Кстати, помимо этих химических параметров важен ещё один — площадь поверхности.
Так, чем больше площадь поверхности, на которой может образовываться накипь, тем полнее произойдёт термическое умягчение воды.
И, если вы пользуетесь чайником, и площадь его стенок и дна, контактирующая с водой, составляет 30 квадратных сантиметров, то вы получите минимально возможное при остальных усовиях умягчение. Но если вы увеличите площадь поверхности, контактирующей с водой, вдвое — примерно так же вырастет эффективность умягчения воды, а, значит, и времени обработки.
Также нужно учитывать, что если вы только начали умягчать воду термически в новом чайнике, то за счёт того, что на гладкой поверхности солям жёсткости менее «удобно» кристаллизоваться, то по-началу умягчение будет происходить не так эффективно, как в последствии, когда на стенках образуется хороший слой накипи.
Мы можем назвать примерное время термического умягчения воды для жёсткости в районе 7 мг-экв/л. Это время составляет 2-3 минуты (без учёта дополнительной площади поверхности и с толстым слоем накипи).
Соответственно, должен возникнуть вопрос: «А как можно самостоятельно определить, сколько нужно кипятить воду для её умягчения?» Ответ на этот вопрос прост:
для определения длительности термического умягчения воды нужно провести эксперимент.
Эксперимент будет состоять в том, что вы одинаковый обЪём воды (например, стакан) будете кипятить разное время (в чайнике с примерно одинаковым слоем накипи и площадью поверхности). И оценивать вкус получившейся кипячёной и охлаждённой воды. Охладить воду до комнатной температуры перед пробой нужно обязательно, поскольку вкус горячей воды человек распознаёт очень плохо.
Также нужно учесть, что кипевшая определённое время вода, разлитая в последствии по ёмкостям для охлаждения, должна быть закрыта! Иначе в воде растворится кислород, что изменит вкус воды — будет ощущаться вкус кислорода (сладковатый), а не собственно мягкой воды.
При дегустации нужно иметь контрольный стакан — с исходной, некипячёной водой. Воду глотать необязательно, достаточно её подержать во рту, а потом выплюнуть. После каждой пробы воды полощите рот исходной, термически не умягчённой водой. Свои ощущения записывайте — разница может быть настолько тонка, что будет теряться после нескольких повторов.
Например, процедура дегустации воды после термического умягчения для определения оптимального времени воздействия такова:
- Попробовать воду из одного стакана и записать баллы вкуса для этого стакана.
- Прополоскать рот исходной неумягчённой термически водой.
- Попробовать второй стакан и записать баллы вкуса для него.
- Прополоскать рот неумягчённой водой
И т.д., сделав минимум по три повтора. В итоге каждая умягчённая проба будет иметь минимум по три оценки. Выводится среднее значение и выбирается оптимальное время!
Определение времени термического умягчения воды можно сделать более точным. Для этого понадобится прибор — TDS-метр, или солемер. Этот прибор измеряет, каково общее содержание солей в воде (в том числе солей жёсткости). Соотвественно, если после термического способа умягчения воды соли жёсткости частично выпали в осадок, то прибор покажет уменьшение общего содержания солей.
Кроме того, поскольку прибор меряет не жёсткость воды, а именно общее содержание солей, то можно определить тот момент, когда кипячение не сколько убирает временную жёсткость воды, сколько увеличивает общее содержание солей за счёт испарения воды.
Естественно, показания прибора лучше всего проверить на вкус — а то мало ли что он показывает 🙂
При покупке солемера нужно приобретать прибор с температурным компенсатором. Иначе в воде разной температуры, но одинакового содержания солей он будет давать разные значения. Ну и вообще солемер — это полезный прибор, им можно определять не только эффективность термического умягчения воды, но и эффективность работы фильтров для воды вообще.
Кстати, важное замечание: если вы пользуетесь фильтром для питься с ионообменной смолой или фильтром, работающим по технологии нанофильтрации или обратного осмоса, или дистиллятором или ещё каким-нибудь фильтром, значительно уменьшающим общее содержание солей или жёсткость воды, то в термическом способе умягчения воды нет необходимости.
Итак, термический способ умягчения воды доступен каждому — остаётся лишь выбрать оптимальную длительность умягчения.

interesko.info
Умягчение воды, фильтры умягчения воды
Умягчение воды - это процесс удаления из воды солей жесткости.
Процессы извлечения из воды солей Ca2+ и Mg2+ в водоподготовке называют умягчением воды. Относительно селективное удаление солей жесткости из воды может производиться тремя методами:
- реагентным умягчением воды;
- ионным обменом;
- нанофильтрацией.
Жесткая питьевая вода горьковата на вкус и оказывает отрицательное влияние на органы пищеварения. По нормам ВОЗ оптимальная жесткость питьевой воды составляет 1,0–2,0 мг-экв/л. В бытовых условиях избыток солей жесткости приводит к зарастанию нагревающихся поверхностей в бойлерах, чайниках, трубах, отложению солей на сантехарматуре и выводу ее из строя, а также оставляет налет на волосах и коже человека, создавая неприятное ощущение их «жесткости». При стирке, взаимодействуя с ПАВами мыла или стиральных порошков, соли жесткости связывают их и требуют большего расхода.
В пищевой промышленности жесткая вода ухудшает качество продуктов, вызывая выпадение солей при хранении. Это характерно для бутилированной питьевой воды, пива, соков, водки. Даже при мытье бутылок она оставляет несмываемые потеки. Поэтому жесткость воды, используемой для приготовления различных продуктов, четко регламентирована и находится на уровне 0,1–0,2 мг-экв/л.
В энергетике случайное кратковременное попадание жесткой воды с систему очень быстро выводит из строя теплообменное оборудование, трубопроводы. Даже небольшой слой отложений солей на поверхности теплообменного оборудования приводит к резкому снижению коэффициента теплопередачи и увеличению расхода топлива. Трубопроводы зарастают настолько, что их производительность падает в несколько раз. Поэтому в тех процессах, где допустимо использование воды с некоторым содержанием солей, ее жесткость ограничивается еще меньшими значениями – 0,03–0,05 мг-экв/л.
Реагентное умягчение воды
Многие соли жесткости имеют низкую растворимость. При введении в раствор некоторых реагентов увеличивается концентрация анионов, которые образуют малорастворимые соли с ионами жесткости Ca2+ и Mg2+. Такой процесс называют реагентным умягчением воды.
Различают умягчение воды известкованием и содо-известкованием.
При известковании в раствор добавляют гашеную известь Ca(OH)2 до рН около 10. В результате протекают реакции:
Ca(HCO3)2 + Ca(OH)2 = 2 CaCO3 + 2Н2O ;
Mg(HCO3)2 + 2 Ca(OH)2 = Mg(OH)2 + 2СaCO3 + 2Н2O .
Данный способ используют при высокой карбонатной и низкой некарбонатной жесткости воды, когда требуется одновременное снижение жесткости и щелочности. Остаточная жесткость на 0,4–0,8 мг-экв/л превышает некарбонатную жесткость. Обычно используется совместно с ионообменным умягчением воды.
При содо-известковании в воду добавляют гашеную известь Ca(OH)2 и соду Na2CO3 до рН около 10. В результате протекают реакции:
Ca(HCO3)2 + Ca(OH)2 + Na2CO3 = 2 CaCO3+ 2 NaOH + Н2СО3;
Mg(HCO3)2 + 2NaOH = Mg(OH)2 + 2NaHCO3.
Как следует из уравнений реакций, в процессе образования и осаждения осадка из воды извлекаются соли жесткости . Вместе с ними удаляются коллоидные и взвешенные частицы с ассоциированными на них загрязнениями. На хлопьях осадка частично сорбируются органические загрязнения воды.
При содо-известковании за счет избытка ионов HCO3 достигается бoльшая полнота удаления из воды солей жесткости. Повышение температуры до 70–80 ° С позволяет довести остаточную жесткость до 0,35–1,0 мг-экв/л. Того же результата можно достигнуть увеличением доз реагентов.
Процессы осаждения осуществляются в отстойниках и осветлителях со взвешенным слоем осадка.
Отстойники малопроизводительны, и получаемая в них гидроксидная пульпа имеет высокую влажность – 97–99%. Поэтому они в настоящее время практически не применяются.
В практике используются различные варианты осветлителей со взвешенным слоем осадка. В них очищаемый раствор подается снизу и проходит через слой осадка. Это увеличивает коэффициент очистки воды. Для уменьшения объема шлама используются дополнительные зоны и камеры шламоуплотнения. Увеличение степени осветления достигается введением дополнительных секций тонкослойного отстаивания.
Реагентные методы умягчения в подготовке питьевой воды не используются. После них вода имеет сильнощелочную реакцию. Они широко применяются в энергетике и промышленности как первая ступень очистки до механических фильтров. При совместной работе они позволяют умягчить воду, удалить взвешенные вещества, включая коллоиды, и частично очистить воду от органических веществ.
Поскольку осаждение образовавшихся хлопьев происходит очень медленно, производительность оборудования низка и оно имеет большие габариты. В результате образуются отходы в виде трудно утилизируемых шламов. Процесс требует тщательного контроля, причем в основном ручного, поскольку зависит от многих факторов: температуры воды, точности дозировки реагентов, исходной мутности воды и т. п.
Новые технологические решения (тонкослойное отстаивание, контактная коагуляция, ввод флокулянтов) позволяют достигнуть тех же показателей умягчения воды при меньших расходе реагентов, габаритах установок и их полной автоматизации.
Нанофильтрационное умягчение воды
При использовании мембран с определенным размером пор обеспечивается их селективность к многозарядным и крупным ионам. Одновалентные ионы (катионы и анионы) в основном не задерживаются мембраной. Реально при селективности по MgSO4 на уровне 98–99% селективность по NaCl для различных нанофильтрационных мембран составляет 20–70%. При пропускании воды через такую нанофильтрационную мембрану удаляются все взвеси, коллоиды, бактерии и вирусы, катионы тяжелых металлов и часть органических загрязнений. Происходит достаточно глубокая очистка от солей жесткости – в 10–50 раз. Концентрация солей натрия уменьшается незначительно. В результате вода умягчается и частично обессоливается.
Для умягчения используются установки с тангенциальной фильтрацией и с рулонными элементами, которые аналогичны установкам обессоливания обратным осмосом. Па раметры такие установоки водоподготовки близки к установкам низконапорного осмоса. Рабочее давление находится в пределе 7–16 атм. Для малогабаритных бытовых фильтров очистки воды производятся мембраны, работающие даже при 3 атм.
Степень умягчения воды определяется характеристиками применяемых мембран и, поскольку селективность нанофильтрационных мембран к катионам Ca2+ и Mg2+ различна (см. табл. 3.3), зависит от состава воды. В любом случае, степень извлечения солей жесткости ниже, чем при обратном осмосе и тем более чем при ионообменном умягчении.
Умягчение воды мембраной типа NF -70 ( Filmtec )
Ион | Концентрация в исходной воде, мг/л | Задержание, % |
Ca2+ | 90 | 86 |
Mg2+ | 2 | 92 |
Na+ | 19 | 50 |
HCO3 – | 270 | 84 |
SO42 – | 6 | 55 |
Эффективность очистки раствора по различным компонентам показана в следующей таблице.
Кондиционирование воды на мембране типа NF -70 ( Filmtec )
Содержание | Исходная вода | Пермеат |
Хлориды, мг/л | 64 | 22 |
Сульфаты, мг/л | 20 | 8 |
Солесодержание, мг/л | 396 | 134 |
Общий органический углерод, мг/л | 15,4 | 1,5 |
Органические галогены, мкг/м3 | 2000 | 51 |
Тригалогенометаны, мкг/м3 | 630 | 56 |
Щелочность, мг/л | 283 | 85 |
Жесткость карбонатная, мг/л | 284 | 22 |
Жесткость общая, мг/л | 316 | 24 |
Цветность, градусы | 38 | 2 |
Наибольшим достоинством нанофильтрации воды является снижение не только жесткости воды, но и щелочности, солесодержания, а также удаление механических, органических и биологических загрязнений воды при отсутствии необходимости использования реагентов и проблем с солевыми стоками при относительно простой схеме.
Промышленная установка для получения питьевой воды с производительностью 2800 м3 в сутки состоит из 2 включенных параллельно установок производительностью 60 м3/ч. Каждая из них содержит 4 ступени из параллельно включенных 8, 4, 2 и 1 модуля, последовательно соединенных по концентрату. Предподготовка состоит из последовательных блоков микрофильтров с рейтингом 10 и 5 мкм. После установки нанофильтрации вода поступает в декарбонизатор для удаления избытка углекислоты и в узел коррекции рН.
В очищенной нанофильтрационной установкой воде отсутствуют бактерии и вирусы, микрозагрязнения и хлорорганика, уменьшены жесткость воды и содержание сульфатов, имеется возможность сокращения в воде дозы хлора. Установка, базирующаяся на традиционных технологиях очистки воды, для получения близкого эффекта должна включать несколько стадий очистки.
Недостатком нанофильтрации является меньшая возможная глубина умягчения воды, необходимость более тщательной предподготовки воды, чем при ионном обмене, и существенно большие потребление воды, электроэнергии и объем отходов. Правда, поскольку последние являются малосолевыми, их сброс существенно легче согласовать с экологическими органами.
Размеры и конструкция рулонных элементов и установок для нанофильтрации и обратного осмоса идентичны.
Электрохимическое умягчение воды
Электрохимический метод умягчения воды является относительно новым. Ранее он предлагался для переработки солевых отходов, включая регенераты установок умягчения, для их последующего повторного использования. В РХТУ им. Д. И. Менделеева разработана технология, включающая электрохимическую коррекцию рН очищаемой воды и электрофлотационное отделение твердой фазы. При прохождении воды через межэлектродное пространство происходят процессы электролиза, поляризации, электрофореза, окислительно-восстановительные реакции с деструкцией органических веществ и инактивацией биологических загрязнений воды. Продукты электролиза взаимодействуют друг с другом с образованием нерастворимых солей.
Принципиальная схема процесса электрохимическогог умягчения воды показана на рисунке. Вода поступает в отстойник 1 , где удаляются грубодисперсные вещества. Затем она подается в катодную камеру электрокорректора 2а . Поскольку между камерами 2а и 2б установлена анионообменная мембрана 4 , при наложении постоянного тока в катодной камере 2а рН поднимается до 10–11, а в анодной 2б опускается до 3–4. В катодной камере происходит образование частиц гидроксидов и карбонатов смешанного состава. Вода со взвесями поступает в камеры грубой 3а и тонкой 3б очистки электрофлотатора. В электрофлотаторе в результате электролиза воды происходит выделение водорода и кислорода, которые поднимаясь флотируют частицы взвесей, органики, эмульсии, образуя пенный слой – флотшлам, который удаляется специальным устройством. После осветления умягченная вода подается в анодную камеру электрокорректора 2б , где происходит ее нейтрализация до рН, близкого к исходной воде.

Схема работы электрокорректора:
1 – отстойник; 2а – катодная камера электрокорректора, 2б – анодная камера электрокорректора; 3а – камера грубой очистки электрофлотатора, 3б – камера тонкой очистки электрофлотатора; 4 – анионообменная мембрана
По данным авторов, качество умягчения воды достаточно высокое – жесткость ниже 0,1 мг-экв/л. Установка умягчения воды производительностью 5 м3 /ч занимает площадь 10 м2 и потребляет 2–3 кВт-ч/м3 электроэнергии.
Наряду с умягчением происходит очистка воды от органических и биологических загрязнений.
www.mediana-filter.ru
Умягчение воды - процесс, в результате которого из воды удаляются соли жесткости. Умягчение сегодня может осуществляться с использованием ряда способов. Это может быть:
- Умягчение с реагентами
- Умягчение ионным обменом
- Умягчение нанофильтрацией
Каждый из способов не универсален и может быть применён в тех или иных случаях. Как правило, для умягчения используется система фильтров, каждый из которых направлен на удаление примесей того или иного типа (крупных взвесей и т.д.).
В нашем ассортименте представлен широкий спектр оборудования для осуществления такой процедуры, как умягчение. Всё оборудование прошло тестирование и имеет высокое качество. Вы можете использовать его длительный период времени. В выборе, установке и планировании систем Вы всегда сможете воспользоваться помощью специалистов.
Процесс удаления из воды солей жесткости называют умягчением.
Жесткая питьевая вода горьковата на вкус и оказывает отрицательное влияние на органы пищеварения. По нормам ВОЗ оптимальная жесткость питьевой воды составляет 1,0-2,0 мг-экв/л. В бытовых условиях избыток солей жесткости приводит к зарастанию нагревающихся поверхностей в бойлерах, чайниках, трубах, отложению солей на сантехарматуре и выводу ее из строя, а также оставляет налет на волосах и коже человека, создавая неприятное ощущение их «жесткости». При стирке, взаимодействуя с ПАВами мыла или стиральных порошков, соли жесткости связывают их и требуют большего расхода.
В пищевой промышленности жесткая вода ухудшает качество продуктов, вызывая выпадение солей при хранении. Это характерно для бутилированной питьевой воды, пива, соков, водки. Даже при мытье бутылок она оставляет несмываемые потеки. Поэтому жесткость воды, используемой для приготовления различных продуктов, четко регламентирована и находится на уровне 0,1-0,2 мг-экв/л.
В энергетике случайное кратковременное попадание жесткой воды с систему очень быстро выводит из строя теплообменное оборудование, трубопроводы. Даже небольшой слой отложений солей на поверхности теплообменного оборудования приводит к резкому снижению коэффициента теплопередачи и увеличению расхода топлива. Трубопроводы зарастают настолько, что их производительность падает в несколько раз. Поэтому в тех процессах, где допустимо использование воды с некоторым содержанием солей, ее жесткость ограничивается еще меньшими значениями - 0,03-0,05 мг-экв/л.
Процессы извлечения из воды солей Са2+ и Mg2+ в водоподготовке называют умягчением. Относительно селективное удаление солей жесткости может производиться 3 методами:
- реагентным умягчением;
- ионным обменом;
- нанофильтрацией.
Кроме того, для защиты нагревательных элементов водонагревательного оборудования применяют магнитные преобразователи воды, которые на химический состав воды не влияют и не снижают ее жесткость. Они лишь предотвращают отложение солей жесткости на нагревательные элементы оборудования.
Реагентное умягчение воды.
Многие соли жесткости имеют низкую растворимость. При введении в раствор некоторых реагентов увеличивается концентрация анионов, которые образуют малорастворимые соли с ионами жесткости Са2+ и Mg2+. Такой процесс называют реагентным умягчением.
Различают умягчение известкованием и содо-известкованием.
При известковании в раствор добавляют гашеную известь Са(ОН)2 до рН около 10. В результате протекают реакции:
Са(НСО3)2 + Са(ОН)2 = 2СаСО3 + 2Н2О;
Mg(HCО3)2 + 2Са(ОН)2 = Mg(OH)2 + 2CaCО3 + 2Н2О.
Данный способ используют при высокой карбонатной и низкой некарбонатной жесткости, когда требуется одновременное снижение жесткости и щелочности. Остаточная жесткость на 0,4-0,8 мг-экв/л превышает некарбонатную жесткость. Обычно используется совместно с ионообменным умягчением.
При содо-известковании в раствор добавляют гашеную известь Са(ОН)2 и соду Na2C03 до рН около 10. В результате протекают реакции:
Са(НСО3)2 + Са(ОН)2 + Na2CО3 = 2CaCО3i+ 2NaOH + h3CО3;
Mg(HCО3)2 + 2NaOH = Mg(OH)2 + 2NaHCО3.
Как следует из уравнений реакций, в процессе образования и осаждения осадка из раствора извлекаются соли жесткости. Вместе с ними удаляются коллоидные и взвешенные частицы с ассоциированными на них загрязнениями. На хлопьях осадка частично сорбируются органические загрязнения.
При содо-известковании за счет избытка ионов НСО3- достигается большая полнота извлечения солей жесткости. Повышение температуры до 70-80°С позволяет довести остаточную жесткость до 0,35-1,0 мг-экв/л. Того же результата можно достигнуть увеличением доз реагентов.
Процессы осаждения осуществляются в отстойниках и осветлителях со взвешенным слоем осадка.
Отстойники малопроизводительны, и получаемая в них гидроксидная пульпа имеет высокую влажность - 91-99%. Поэтому они в настоящее время практически не применяются.
В практике используются различные варианты осветлителей со взвешенным слоем осадка. В них очищаемый раствор подается снизу и проходит через слой осадка. Это увеличивает коэффициент очистки. Для уменьшения объема шлама используются дополнительные зоны и камеры шламоуплотнения. Увеличение степени осветления достигается введением дополнительных секций тонкослойного отстаивания.
Реагентные методы в подготовке питьевой воды не используются. После них вода имеет сильнощелочную реакцию. Они широко применяются в энергетике и промышленности как первая ступень очистки до механических фильтров. При совместной работе они позволяют умягчить воду, удалить взвешенные вещества, включая коллоиды, и частично очистить ее от органических веществ.
Поскольку осаждение образовавшихся хлопьев происходит очень медленно, производительность оборудования низкая и оно имеет большие габариты. В результате образуются отходы в виде трудно утилизируемых шламов. Процесс требует тщательного контроля, причем в основном ручного, поскольку зависит от многих факторов: температуры воды, точности дозировки реагентов, исходной мутности и т. п.
Новые технологические решения (тонкослойное отстаивание, контактная коагуляция, ввод флокулянтов) позволяют достигнуть тех же показателей при меньших расходе реагентов, размерах установок и их полной автоматизации.
Ионный обмен в умягчении воды.
В соответствии с современными воззрениями, для питьевой и хозяйственно-бытовой воды оптимальной является жесткость на уровне 1,5 мг-экв/л.
Практически для всех пищевых производств требуется мягкая вода. Для водочного производства установлена предельная жесткость 0,2 мг-экв/л, для производства соков - 0,7 мг-экв/л. для питания паровых котлов - 0,05 мг-экв/л и менее. Многие производители стараются использовать воду еще более высокого качества.
Наиболее просто снижение жесткости до практически любых значений обеспечивается ионным обменом. Производительность метода практически не ограничена.
Умягчение воды может производиться методами:
- Na-катионирования.
- H-Na-катионирования (параллельное или последовательное)
- Н-катионирования с голодной регенерацией на сильно- или слабокислотном катионите.
Как отмечалось выше, в соответствии с уравнением реакции, умягчение воды производится путем ее контактирования с сильнокислотным катионитом в Na-форме, в результате чего из воды извлекаются катионы Са2+ и Mg2+ и замещаются ионом Na+. Солесодержание воды при этом практически не меняется, поскольку катионы Са2+, имеющие вес 1 мг-экв равный 20, замещаются катионом Na+ с весом 1 мг-экв, равным 23. Поскольку анионный состав не меняется, раствор остается практически нейтральным. Щелочность воды и рН может увеличиться на 0,1-0,2 единицы, в зависимости от содержания солей жесткости.
Интересным решением вопроса умягчения со снижением щелочности воды является Na-Cl-ионирование. Оно основано на применении для очистки воды катионита в Na-форме и анионита в С1-форме. Регенерация обоих ионитов производится одним и тем же раствором NaCI. В этом процессе протекают следующие суммарные реакции:
на катионите:
2R-Na + Ca(Mg)(HCO3)2 <-> R2-Ca(Mg) + 2NaHCO3 (1)
2R-Na + Ca(Mg)SО4 <-> R2-Ca(Mg) + Na2S04 (2)
2R-Na + Ca(Mg)(NО3)2 <->R2-Ca(Mg) + 2NaNО3 (3)
на анионите:
R-Cl + NaHCО3<-> R-НСОз + NaCl: (4)
2R-C1 + Na2SО4<-> R2-SO4 + 2NaCl; (5)
R-Cl + NaNО3<-> R-NO3 + NaCI. (6)
В результате реакций (1-3) с сильнокислотным катионитом обрабатываемая вода умягчается до заданного уровня, и в ней остаются только соли натрия. При их контактировании с сильноосновным анионитом в С1-форме происходит замена бикарбонатных, сульфатных и нитратных анионов на С1 (реакции 4-6). При сорбции бикарбонатного иона уменьшается щелочность воды, которая минимальна в начале цикла, а затем постепенно увеличивается. Время работы анионитного фильтра определяется повышением щелочности до заданного предела.
Метод Na-Cl-ионирования применяют при соотношении концентраций анионов в исходной воде НСО3-/ SО42- + NО3- > 1 при суммарном содержании сульфатов и нитратов не более 3 мг-экв/л.
Поскольку регенерация катионита и анионита производится последовательно одним и тем же раствором соли, необходимо исключить образование осадка карбонатов кальция в слое катионита. Для этого регенерат после анионита подкисляют, разрушая бикарбонат-ионы. Также трудно сбалансировать объемы ионитов, чтобы они насыщались одновременно. При близких значениях жесткости и щелочности в исходной воде и вдвое-втрое большей емкости катионита, чем анионита, объем последнего должен быть в 2-3 раза больше.
Другими путями являются умягчение воды методами H-Na-катионирования (параллельным или последовательным), Н-катионирования с нейтрализацией, Н-катионирования с голодной регенерацией на сильно- или на слабокислотном катионите.
Эти способы позволяют свести щелочность к минимуму, а также уменьшить солесодержание воды. Их недостатком является потребность в больших количествах кислоты и специальном кислотостойком оборудовании. Для удаления образовавшейся углекислоты в буферных баках желательно установить распылительные головки или эжекторы-декарбонизаторы.
Н-катионирование воды позволяет полностью удалить жесткость и щелочность, а также снизить солесодержание. При контакте с катионитом в Н-форме из воды извлекаются все катионы, которые замещаются ионом водорода, рН раствора становится равным 2,5-4,0, в зависимости от исходного солесодержания. Во время очистки в воду выделяются катионы водорода, которые реагируют с бикарбонат-ионами по реакции:
HCО3- + Н+ -> Н2О + СО2 (7)
Кислотность воды велика, все бикарбонаты полностью переходят в растворенный углекислый газ, который отдувается в декарбонизаторе - ДКБ. Вода после декарбонизатора содержит только анионы сильных кислот и имеет кислую реакцию. Для ее нейтрализации в воду дозируют раствор щелочи. В результате очищенная вода имеет минимальную щелочность и жесткость, а содержание катионов соответствует первоначальному содержанию анионов сильных кислот. Снижение солесодержания соответствует исходной щелочности.
При необходимости поддерживать щелочность на определенном уровне при минимальной жесткости применяют параллельное или последовательное H-Na-катионирование (рис. 3.3, г, Э). Оба этих режима обеспечивают и некоторое снижение солесодержания воды.
При параллельном H-Na-катионирование часть раствора очищается Н-катионированием на сильнокислотном катионите, а другая часть умягчается Na-катионированием на таком же ионите. В воде, прошедшей через катионит в Н-форме, удаляются все катионы и вместо них в воду поступает катион водорода, рН раствора становится равным 2,5-4,0 в зависимости от солесодержания. Бикарбонаты полностью разрушаются и присутствуют в виде растворенной углекислоты. В воде, прошедшей через катионит в Na-форме, катионы солей жесткости заменены на натрий, рН не меняется. Обработанные растворы смешиваются в расчетных соотношениях и подаются на декарбонизатор, где удаляют углекислоту. Очищенная вода может иметь остаточную щелочность Щост менее 0,35 мг-экв/л.
Параллельное H-Na-катионирование используется тогда, когда необходимо иметь остаточную щелочность Щост менее 0,35 мг-экв/л; в исходной воде карбонатная жесткость составляет более 50%, а сумма концентраций солей сильных кислот - менее 5-7 мг-экв/л.
Последовательное H-Na-катионирование заключается в пропускании части питающего раствора через катионит в Н-форме, смешении подкисленного раствора с исходным, декарбонизации и умягчении всего потока на катионите в Na-форме. При подкислении воды при Н-катионировании частично разрушается бикарбонат-ион, и связанная с ним жесткость становится некарбонатной. Щелочность перед Na-катионированием поддерживается на уровне 0,7-1,0 мг-экв/л. Поскольку степень извлечения жесткости на Н-катионировании особого значения не имеет, регенерация кислотой может осуществляться без избытка. Такой способ умягчения используется для сильноминерализованных вод с солесодержанием более 1 г/л, когда карбонатная жесткость менее 50% от общей, а щелочность 0,7-1,0 устраивает потребителя.
Магнитное проеобразование воды:
В последние десятилетия, как в России, так и за рубежом, для борьбы с образованием накипи и отложений на внутренней поверхности труб и теп- лообменного оборудования применяют магнитную обработку воды. Ее широко используют в конденсаторах паровых турбин, парогенераторах низкого давления и малой производительности, тепловых сетях и системах горячего водоснабжения, в различных теплообменных аппаратах. Эффект, последствия обработки воды в магнитном поле известны давно. Еще в XIII в. были отмечены лечебные свойства «омагниченной» воды. Но только в ХХ в. началось использование магнитов в технике водоподготовки.
Первый патент на аппарат магнитной обработки воды был выдан в 1946 г. бельгийскому инженеру Т. Вермейрену, еще за 10 лет до этого обнаружившего, что при нагреве воды, пересекшей силовые линии магнитного поля, на поверхности теплообмена накипь не образуется.
Магнитная обработка воды в аппаратах с постоянными магнитами и электромагнитами применяется уже несколько десятилетий. Замечено, что при воздействии магнитного поля на солевые кристаллы последние меняют свою структуру: кристаллы становятся гораздо мельче, и кристаллы кальцита приобретают орагонитную форму. В целом кристаллы карбоната кальция вместо обычной накипи образуют рыхлую массу, легко вымываемую из трубопровода. Кроме того, образовавшаяся большая поверхность множества мелких кристаллов «конкурирует» за отложения с нагретой поверхностью. Более 70% частиц имеют размер менее 0,5 мкм.
Механизм воздействия магнитного поля на воду и содержащиеся в ней примеси окончательно не выяснен, но имеется ряд гипотез.
Современные воззрения объясняют механизм воздействия магнитного поля на воду и ее примеси поляризационными эффектами и деформацией ионов солей. Гидратация ионов при обработке уменьшается, ионы сближаются, образуя кристаллическую форму соли. В основу одной из теорий положено влияние магнитного поля на коллоидные примеси воды, другой - изменение структуры воды. При наложении магнитного поля в массе воды формируются центры кристаллизации, вследствие чего выделение нерастворимых солей жесткости происходит не на теплопередающей поверхности (нагрева или охлаждения), а в объеме воды. Таким образом, вместо твердой накипи в воде появляется мигрирующий тонкодисперсный шлам, легко удаляемый с поверхности теплообменников и трубопроводов. В аппаратах магнитной обработки вода должна двигаться перпендикулярно магнитным силовым линиям.
www.terrawater.ru
Умягчение воды
Умягчение воды
Вода обладает исключительно высокой растворяющей способностью. Выпадая в виде атмосферных осадков, она растворяет находящиеся в атмосфере газы, в том числе и углекислый газ. В дальнейшем просачиваясь в землю, вода захватывает дополнительное количество углекислого газа как продукта разложения объектов живой и не живой природы. Взаимодействуя с водой, углекислый газ образует угольную кислоту, увеличивая потенциал для растворения минералов и других примесей. Проходя через слой известняка, она насыщается ионами кальция и магния, ответственными за жесткость. Железо и марганец в источниках находятся в меньших концентрациях, чем ионы кальция и магния. Поскольку вода является растворителем, она захватывает растворимые хлориды, сульфаты, нитраты кальция и магния. Похожим образом она поглощает карбонатные, бикарбонатные, хлоридные, сульфатные соединения натрия, а также некоторое количество кремнезёма.
В общем случае, при подробном анализе в ней могут быть обнаружены в большей или меньшей концентрации практически все элементы таблицы Менделева.
Жесткость подразделяется на гидрокарбонатную, называемую еще временной, и некарбонатную (хлоридную, сульфатную, нитратную) – постоянную. Временная жесткость устраняется при кипячении (налет на нагревательном элементе), постоянная жесткость при нагревании не устраняется.
Очистка от солей жесткости называется умягчением. Жесткость воды на территории РФ измеряется в единицах мг-экв/литр и, в зависимости от отрасли использования, требования к уровню жесткости изменяются от 7 мг-экв/л (хозяйственно-бытовые цели) до единиц мг-экв/литр и менее в медицине, электронике, энергетике, атомной промышлености. Допустимая жесткость воды 7 мг-экв/л не несет серьезной опасности здоровью, но создает целый ряд бытовых проблем. Жесткая вода вызывает образование осадков и налетов на поверхности трубопроводов и рабочих элементах бытовой техники. Эта проблема особенно актуальна для приборов с нагревательными элементами – водогрейных и паровых котлов, бойлеров и другого теплообменного оборудования.
Устранение жесткости - умягчение осуществляется с помощью ионнообменной смолы. Ионнообменная смола представляет собой полимер, состоящий из полимерной матрицы и функциональных групп. Полимерная матрица синтезируется из мономера стирола в присутствии связывающего дивинилбензола. В процессе синтеза используется спирт, который в определенный момент испаряется, и выходя из матрицы, формирует в ней поры. Затем в матрицу вводятся функциональные группы. Функциональная группа состоит из двух частей: неподвижной, прикрепленной к матрице, и подвижной части. Если подвижной частью функциональной группы служит катион, а неподвижной – анион, то смола называется катионообменной, а если подвижная часть анион – то анионообменной. Катионообменная смола может быть в натриевой форме (Na- катионообменная смола) или в водородной форме (H-катионнообменная смола).
Процесс умягчения ионнообменной смолой
Очистка ионообменными смолами
Ионообменная смола засыпается в колонну, заполняя 60-65% общего объема фильтра. Жесткая вода поступает в колонну и, так как ионообменный материал имеет большее химическое сродство с кальцием и магнием, чем с ионами натрия, последние вытесняются ими со смолы. Замена катионов кальция и магния на катионы натрия происходит в эквивалентных соотношениях. Вода, содержащая на входе ионы бикарбоната кальция и магния, на выходе из него будет содержать эквивалентное количество бикарбонатов натрия. Количество ионов натрия на смоле ограничено,поэтому наступает момент, когда смола перестает умягчать воду, то есть исчерпана обменная емкость смолы. Для перезарядки смолы или ее регенерации запускается процесс обратного ионного обмена, в ходе которого ионообменная смола подвергается воздействию концентрированным раствором исходного вида катионов. Для регенерации Na-катионообменной смолы используют относительно крепкий раствор хлорида натрия. Натрий из раствора вытесняет кальций и магний из смолы, перезаряжая её.
Установка умягчения, очистка ионообменными смолами:Конструктивно установка умягчения состоит из трех частей: баллоны с ионообменной смолой и водоподъемной трубкой, клапана управления с электронным контроллером и ёмкости для солевого раствора. Контроллеры бывают двух видов: регенерация происходит по времени и регенерация происходит по объему. При регенерации по времени контроллер переводит установку в режим регенерации через определенное количество часов, дней или в определенный день недели. При регенерации по объему клапан управления имеет встроенный счетчик воды, и через определенное количество воды, прошедшей через установку воды, контроллер переводит ее в режим регенерации. Этот объем называется фильтроциклом установки и рассчитывается контроллером на основе жесткости воды, объема и емкости загрузки, которые вводятся в контроллер на стадии программирования.
В тех случаях, когда требуется бесперебойное обеспечение мягкой водой, могут применяться два одинаковых фильтра, функционирующих в режиме TWIN или DUPLEX. В режиме «твин» один контроллер управляет двумя клапанами управления. Когда один фильтр умягчает воду, находится в рабочем режиме, второй с отрегенерированной смолой находится в режиме ожидания. Когда фильтроцикл первого фильтра исчерпан, клапан управления переводит второй фильтр в рабочий режим фильтрации, а первый – в режим регенерации. После завершения регенерации первый фильтр переходит в режим ожидания, и находится в нем до тех пор, пока не кончится фильтроцикл второго. Процесс очистки циклично повторяется, фильтры работают попеременно.
В режиме «дуплекс» фильтры функционируют одновременно и поочередно переводятся по заданной программе в режим регенерации со сдвигом по времени её начала на длительность цикла регенерации.
Умягчение воды известкованием
В тех случаях, когда необходимо умягчать воду с высокой карбонатной жесткостью (более 30 мг-экв/л) нецелесообразно применять ионообменную смолу. Следует предварительно понизить жёсткость, используя технологию известкования. Умягчение воды известью и кальцинированной содой предусматривает дозирование гашеной извести Сa(OH)2 в жесткую воду для удаления карбонатной жесткости путем осаждения и последующего фильтрования осадка. Некарбонатная жесткость, в свою очередь, уменьшается добавлением кальцинированной соды Na2CO3 для формирования нерастворимого осадка, который также удаляется фильтрованием.
Данный метод используется на водоканалах и предприятиях с большим потреблением воды. Это достаточно эффективный метод уменьшения жесткости воды, однако, он не позволяет полностью удалить все минералы.
Гашеная известь применяется для удаления бикарбоната кальция из воды. Там, где кальций и магний содержатся в форме хлоридов или сульфатов, такая обработка заметно менее эффективна.
Уменьшение жесткости воды известью и кальцинированной содой становится чрезвычайно дорогостоящим, если жесткость надо снизить до уровня менее 2 мг-экв/л. Для бытовых целей умягчение воды известью и кальцинированной содой является непрактичным. С одной стороны - имеются трудности в подаче извести и кальцинированной соды, с другой стороны – требуетсястрогий контроль процесса отстаивания и фильтрации. Еще одним сдерживающим фактором использования данного процесса являются размеры необходимого оборудования и большое количество выбрасываемого известкового шлама.
gostvoda.ru
Способы умягчения воды. Основные способы умягчения жесткой воды
АкваЩит - Умягчение воды
Разбирать проблемы излишней жесткости современной воды невозможно без детального изучения многообразия способов умягчения воды. Обилие фильтров на полках магазинов и рынков заставляет задуматься над тем, что выбор прибора для квартиры не так прост. И чтобы выбрать нужный вариант умягчителя нужно ознакомиться хотя бы с разными видами способов умягчения воды. Не зная основ, невозможно разбираться в теме.
Хотя о накипи у нас знают достаточно много, до сих пор существует слишком много предубеждений в отношении фильтрующих приборов, а также мифов о бесполезности промышленных систем водоподготовки, по крайне мере для бытовых условий. Излишняя жесткость воды приводит к большому количеству нежелательных явлений. Цена образования накипи и плохой растворимости жестковатой некачественной водой любых моющих средств слишком дорога, чтобы сегодня пренебрегать вопросами умягчения воды.
 У нас почему-то считается, что излишняя жесткость в воде это миф, и что использование фильтров, это выкачка денег из доверчивых граждан. При этом все прекрасно видели и знают, что такое накипь и насколько трудно бороться с ней, как непросто ее удалять, постоянно из месяца в месяц. Если у вас есть сомнения в степени жесткости вашей воды, вы всегда можете провести химический анализ воды. Он всегда поможет вам не только определить, на сколько вода у вас чистая, и пригодная в пищу. На основе ее результатов вы сможете составить правильную, то есть грамотную водоподготовку котельных установок.
У нас почему-то считается, что излишняя жесткость в воде это миф, и что использование фильтров, это выкачка денег из доверчивых граждан. При этом все прекрасно видели и знают, что такое накипь и насколько трудно бороться с ней, как непросто ее удалять, постоянно из месяца в месяц. Если у вас есть сомнения в степени жесткости вашей воды, вы всегда можете провести химический анализ воды. Он всегда поможет вам не только определить, на сколько вода у вас чистая, и пригодная в пищу. На основе ее результатов вы сможете составить правильную, то есть грамотную водоподготовку котельных установок.
О том, что вы пользуетесь некачественной водой, вы узнаете по многим признаком, столь нам всем хорошо знакомым. Излишняя жесткость проявит себя даже при варке. Такая вода заставляет мясо становится более жестким. Овощи при варке в такой воде разваливаются. И извечная кромка осадка солей жесткости. Если у вас уже есть такие чайники или кастрюли с извечной твердой кромкой внутри на поверхностях, то сто процентов жесткость в вашей воде давно превысила допустимые пределы. О наличии подобной воды в квартире вы узнаете не только по известковому налету внутри чайника, оставит свой след вода и даже при мытье посуды в посудомоечной машине. Казалось бы, бокалы и тарелки после мытья в такой машинке должны выходить скрипящими и идеально чистыми, но не в случае с жестковатой водой. Об использовании подобной воды можно будет узнать по предательским белым разводам на бокалах, по едва заметному белому налету на тарелках.
Сказывается жесткость и на качестве приготовленных блюд, и чая с кофе. У настоящего натурального кофе, заваренного на хорошей воде совсем другой вкус, и если вы настоящий кофеман, то вопрос создания системы очистки от жесткости вас ни разу не смутит. Стоит только попробовать хороший кофе на правильной воде.
О присутствии в воде излишков солей кальция с магнием скажет и плохо выстиранная одежда. Образование накипи – это далеко не все к чему приводит работа с подобной водой. Есть у нее еще такая особенность – как плохая растворимость, что порошка, что мыла с моющим средством для посуды. Работая с жестковатой водой, сэкономить никак не удастся. Вот эта особенность приводит к быстрому износу тканей, они начинают трещать и рваться буквально на глазах. И стоит установить перед стиральной машинкой один электромагнитный умягчитель воды АкваЩИт и проблема с повышенной жесткостью воды будет решена. Но многие считают, что прибор на магнитах не может чистить воду. Пока они же на собственном примере не убеждаются, как рационально и экономно работают способы умягчения воды.
И еще один момент - использование некачественной воды для личного употребления, в конце концов, негативно отразиться на нашем здоровье. Нельзя безнаказанно пить такую воду. И ваш организм вам ответит различными хроническими заболеваниями, ранним старением кожи и выпадением волос. Только не все люди могут сразу идентифицировать причину таких болезней в жесткости воды.
Способы умягчения воды подразумевают применение специальных приборов. Их задача устранить из воды излишек двух карбонатных солей. Но есть и более примитивные способы. Их почти не используют сегодня, но когда-то до изобретения фильтров для воды, их применяли наши предки в стремлении хоть как-то оградить себя от пагубного влияния кальция и магния.
Таким самым простым способом умягчения воды является применение простого кусочка кремния. Все, что вам нужно для получения мягкой воды, это купить кусочек кремния размером где-то 5х5 см и положить его в бутыль (3-литровый) с водопроводной водой. Через недели вы сможете пить «заряженную» воду и она будет не плесневелая, а мягкая и вкусная, еще и с лекарственными свойствами. Таково влияние кремния на соли кальция и магния. Очень часто в древности облицовывали колодец кремнием, чтобы получить хорошую воду.
На сегодня использование такого кремниевого способа умягчения воды имеет право на жизнь, но очистить с его помощью большое количество воды вряд ли удастся. Поэтому только лечебное, лекарственное применение такого способа.
Для промышленности использование примитивных способов умягчения воды невозможно. В этой ситуации даже применение тщательно продуманной, сделанной на основе химического анализа воды, системы подготовки воды не является полной защитой от образования накипи. Так в теплоэнергетике, все равно придется проводить очистку от известкового налета. И разница состоит в том, что после работы электромагнитного умягчителя воды Акващит, налет образуется слабенький, а нарастает медленнее и что немаловажно достаточно легко устраняется. Вам даже не придется покупать под него специальные средства. Достаточно обычной промывки водой.
Образование накипи не хуже плохой растворимости в воде вредит бытовым приборам и оборудованию. Проблема еще в том, что если накипь не убирать своевременно, то она начинает нарастать еще быстрее, и еще увереннее. И в след за ней, начинает потихоньку развивать свою деятельность коррозия. Эти два явления неразрывно связаны между собой.
Мало того, что накипь, это не эстетично, некрасиво, мало полезно, но еще и вместе с образованием накипи возрастает угроза потерять технику и дорогостоящее оборудование. Проблемы с накипью особенно в промышленности – это всегда очень большие расходы. Способы умягчения воды. как реагентные, так и безреагентные не могли проявиться просто так. Должны были быть веские причины для их создания. Вот такой причиной и является накипь.
В котельных, особенно паровых, установка умягчения воды непрерывного действия – это целая история. Для того, чтобы паровая котельная работала, качество пара должно быть очень высоким и за время очистки, что вода, что пар проходят огромное количество инстанций, что помогает в дальнейшем паровым электростанциям прослужить гораздо дольше, чем при работе с неочищенной водой.
К чему же приводит плохая вода? Ее разогревают. Соли жесткости в процессе нагрева образуют малорастворимый осадок, то есть накипь, которая при нагреве оседает именно на нагреваемую поверхность. Образованный слой, хоть и образовался в процессе нагрева, но сам по себе тепло не поглощает ,и не передает. И мы помним, отложился он как раз на нагревательной поверхности. Со временем плотность слоя накипи достигает таких пределов, что тепло абсолютно перестает передаваться в воду.
За этот отрезок времени расход топлива растет просто невообразимо. Ведь прибор или оборудование пытается работать. А их работа – это греть воду. И чтобы это сделать, нужно попытаться так нагреть накипь, чтобы она хотя бы 10 процентов переданного ей тепла отдала в воду. Для этого приходится расходовать очень много топлива. Это занимает много времени и поверхности при этом терпят бешенные перегрузки. Естественно вечно это продолжаться не может. Металлы, как будь то попадают в мартеновскую печь, если они покрыты слоем накипи.
Вот и получается, что бытовой прибор может отключиться, чтобы не перегореть, а котел на твердом топливе этого сделать не может. Его только может разорвать от подобного эффекта. Здесь и человеческие жертвы возможны. Поэтому к тому, что такое умягчение воды нужно относиться очень правильно и внимательно. Упускать очистки от накипи особенно в промышленности категорически нельзя.
Любая очистка от накипи промышленного оборудования подразумевает под собой обязательную остановку системы. Это простои, это снова недопоставленная вовремя продукция, это расходы. Сделать очистку от накипи при работающем оборудовании не представляется возможным. Только остановка и очистка. И чаще всего разборная очистка, т.к. оборудование, что в котельных, что в металлургии сложное. Добраться до самых отдаленных мест сразу не получится. Вот и считайте, так ли уж дешево удаление. Бригады по монтажу оборудования, бригады по чистке поверхностей, время на простои, оплата за чистящие средства. На удалении накипи сэкономить точно не получится.
И как бы вы не старались, бесследно провести какую либо противонакипную очистку точно не удастся. Всегда будут царапины, механическая очистка снимает не только защитное покрытие, она заденет и основной слой. Ну а любая испорченная поверхность – любимое место отложения накипи. Вот и получается, что устраняя одну накипь, мы стимулируем быстрое образование других слоев. Так, что невыгодно постоянно удалять накипь, совсем не выгодно.
Способы умягчения жесткой воды
 Теперь, что касается способов умягчения жесткой воды. Хоть и может показаться на первый взгляд, что приборов для умягчения много, и, тем не менее, способов умягчения жесткой воды не так уж много, хотя выбор какой-никакой есть. Способы можно смело поделить на химические и физические. Химическая очистка воды подразумевает использование разнообразных реагентов, в процессе работы которых соли жесткости становятся малорастворимыми, выпадают в осадок и легко выводятся из систем, где используют воду. Давайте подробнее узнаем про эти способы умягчения жесткой воды. Их виды и преимущества.
Теперь, что касается способов умягчения жесткой воды. Хоть и может показаться на первый взгляд, что приборов для умягчения много, и, тем не менее, способов умягчения жесткой воды не так уж много, хотя выбор какой-никакой есть. Способы можно смело поделить на химические и физические. Химическая очистка воды подразумевает использование разнообразных реагентов, в процессе работы которых соли жесткости становятся малорастворимыми, выпадают в осадок и легко выводятся из систем, где используют воду. Давайте подробнее узнаем про эти способы умягчения жесткой воды. Их виды и преимущества.
Физические способы умягчения воды
Группа же физических способов умягчения воды работает без применения каких-либо химикатов. Эта группа идеальна для очистки водопроводной воды, то есть той воды, которая в том числе идет для личного использования – пить и есть. Там вода должна быть мягкой по умолчанию.
Мембранные способы умягчения воды
 Еще можно выделить группу мембранных способов умягчения воды. Сюда входят очень популярный в промышленности обратный осмос. Это метод тонкой очистки с помощью давления. Внутри такого прибора располагается тонкая мембрана, выполненная из дорогостоящих материалов. Вся поверхность такой мембраны испещрена отверстиями. Диаметр таких дырочек не превышает размера молекулы воды. Такая полупроницаемая поверхность дает возможность устранить из воды практически любые примеси, которые имеют размер более молекулы воды.
Еще можно выделить группу мембранных способов умягчения воды. Сюда входят очень популярный в промышленности обратный осмос. Это метод тонкой очистки с помощью давления. Внутри такого прибора располагается тонкая мембрана, выполненная из дорогостоящих материалов. Вся поверхность такой мембраны испещрена отверстиями. Диаметр таких дырочек не превышает размера молекулы воды. Такая полупроницаемая поверхность дает возможность устранить из воды практически любые примеси, которые имеют размер более молекулы воды.
С таким прибором вы легко сможете получить воду идеальную для той же фармакологии или для производства питьевой воды. Дистиллят получают с помощью нанофильтрации. Это еще один вид обратного осмоса, только низконапорного.
Главный козырь этого способа умягчения воды – высочайшая степень очистки, возможность получить воду с заданными признаками, только сменив мембрану. Но есть у обратного осмоса, как и у других мембранных способов очистки воды, свои минусы. Когда прибор работает, очень много воды находится внутри прибора. Так происходит по нескольким причинам. Во-первых, скорость просачивания через мембрану далеко не такая высокая, плюс прибор включает в себя не один фильтр. В установку могут входить обратный осмос, механический фильтр и кондиционер. Последний в обязательном порядке ставят на установках для производства питьевой воды. Такой способ умягчения воды очень хорошо устраняет любые примеси вплоть до бактерий с вирусами, что для питьевой воды немаловажно. Потом без кондиционирования такая вода становится непригодной для личного использования. Ну и потом использование обратного осмоса значительно ограничивает стоимость установки. Далеко не все в быту пока могут дозволить себе, использовать такую установку.
Химический способ умягчения воды
Химический способ умягчения воды как мы уже говорили, подразумевает использование химических веществ. Сюда относят и натрий хлор, и фосфаты. Для такого умягчения чаще всего используют дозаторы, которые монтируют на трубу водопровода. Такие способы плохи тем, что химикаты могут образовывать другие примеси в воде и получается все тот же осадок. Только он еще и очень плохо устраняется. При этом к химическому способу умягчения воды относится и химическое восстановление фильтрующих частей приборов. Поэтому самым известной системой очистки и умягчения воды такого способа является ионный обмен. Здесь картридж восстанавливают с помощью очень соленого раствора. После восстановления картридж сможет снова работать.
Ионообменный способ умягчения воды
Ионный обмен, как способ умягчения воды один из самых простых. Каких-то особых конструкций он не требует. Основа, как понятно из названия ионный обмен. Работает внутри такого прибора гелеобразная смола. В ней содержится большое количество натрия, который очень быстро при контакте с жестковатой водой сменяется на кристаллы солей кальция и магния. Вот и получается простой и быстрый процесс очистки, без каких либо усилий. Спустя определенный период времени, весь натрий из картриджа вымывается.
В промышленности картридж восстанавливают, промывая раствором, а вот в быту просто меняют, т.к. питьевая вода не терпит реагентов. Скорость очистки отличная, только вот расходы на картриджи или их восстановление довольно большие. Да и в быту фильтр-кувшин в состоянии от силы очистить вам пару тройку литров. Для полной защиты от накипи и жесткости придется в обязательном порядке использовать еще один фильтр.
Безреагентный способ умягчения воды
Ярким представителем безреагентного способа умягчения воды является магнитное силовое воздействие. Основу таких приборов составляют мощные магниты. Обязательно постоянные. Такой прибор еще только монтируешь, а магнитное поле уже работает. При этом прибор легко установить, легко снять. Обслуживания он не требует, не нужны ему картриджи и очистки. Он работает. Магнитное силовое поле, таким образом, пронизывает воду, что находящиеся в ней соли жесткости теряют прежнюю форму. Теперь это острые иголочки. Они натирают поверхности со старой накипью, очень качественно при этом ее удаляя. Но магнитное воздействие очень придирчиво к воде. Ему нужна вода комнатной температуры, текущая в одном направлении и с определенной скоростью. Убрать все минусы магнитного способа умягчения воды получилось только путем добавления электрического тока. Так и изобрели электромагнитную установку.
Ознакомившись со всеми способами умягчения воды, нужно сделать вывод, что сегодня отказаться от умягчения означает рисковать здоровьем своей семьи и полное отсутствие дальновидности. Поэтому все больше народу, сегодня выбирает именно такой путь водоподготовки питьевой воды.
vodopodgotovka-vodi.ru
Умягчение воды: бытовые и промышленные технологии
Зачем нужно умягчение воды?
Умягчение воды – процесс удаления солей жесткости. Это один из важнейших этапов промышленной водоподготовки. Но и при бытовом использовании жесткая вода может стать серьезной проблемой.
- жесткая вода сокращает срок службы бытовой техники и сантехнического оборудования;
- не рекомендуется использовать воду с повышенным содержанием солей жесткости для приготовления пищи, так как это небезопасно для здоровья;
- жесткая вода, используемая для купания, делает волосы тусклыми и сушит кожу;
- повышенная жесткость воды приводит к перерасходу моющих средств при стирке и мытье посуды.
Вода в системах централизованного водоснабжения, естественно, проходит предварительную очистку. Но практически повсеместно требуется дополнительное смягчение воды.
Жесткой воду делают катионы (положительно заряженные ионы) кальция и магния. Влияние других металлов на жесткость воды незначительно. Поэтому, снижение жесткости воды подразумевает в первую очередь удаление этих примесей.
Заметим также, что жесткость вода воды зависит от содержания ионов щелочноземельных металлов на площади водосбора. Вот почему в одних регионах проблем с жесткостью воды практически нет, в других же они очень серьезны.
Существуют технологии определения жесткости воды. Но в домашних условиях можно обойтись и без лабораторных исследований. Если на стенках и нагревательных элементах чайника образуется накипь, а на посуде невооруженным глазом виден белый налет, и даже после кипячения вода имеет неприятный, горький или солоноватый привкус, значит, умягчение воды необходимо.
Жесткая вода вредна не только для чайника. Водонагреватели и газовые колонки, стиральные и посудомоечные машины, словом, любая техника, в которой происходит нагрев воды, страдает от ее излишней жесткости.
Образование накипи снижает и эффективность систем отопления. Причем, влияние может быть очень значительным. Накипь не только повышает расход энергии на отопление, но и быстро приводит в негодность элементы системы.
Технологии умягчения воды
Для умягчения воды используются различные методы, химические и физические.
В промышленной водоочистке распространены реагентные методы умягчения воды: известкование и содо-известк ование. Суть методов – в добавлении в воду реагентов: негашеной извести в первом случае или смеси негашеной извести и соды.
ование. Суть методов – в добавлении в воду реагентов: негашеной извести в первом случае или смеси негашеной извести и соды.
Эти технологии используются только для получения технической воды, для питьевой воды они не приемлемы.
Еще один промышленный способ смягчения воды – нанофильтрация. К нанотехнологиям этот термин, к счастью, никакого отношения не имеет. Под нанофильтрацией понимается использование мембранных фильтров. Технология сходна с обратноосмотической фильтрацией, но уступает ей по степени очистки и обессоливания.
В квартирах и коттеджах высокий уровень очистки и умягчения воды обеспечивают системы обратного осмоса. Но для очистки воды для бытовых нужд эта система может оказаться слишком затратной.
Поэтому, фильтры обратного осмоса в домах и квартирах обычно применяются для очистки питьевой воды. А смягчение воды для бытовых нужд производится магнитными, электромагнитными, полифосфатными или ионообменными фильтрами.
Технологии магнитного и электромагнитного умягчения воды заслуживают отдельного упоминания. В их основе лежит тот факт, что под воздействием магнитного поля структура воды изменяется так, что соли жесткости уже не способны осаживаться на трубах и нагревательных элементах в виде накипи. Удаления солей из воды при этом не происходит, эта задача перекладывается на фильтр грубой очистки.
Отношение к магнитному умягчению воды неоднозначное. В одних источниках его объявляют чуть ли не панацеей, в других – называют шарлатанством. Для получения питьевой воды эти фильтры не используются. А вот для защиты от накипи газовых колонок, отопительных котлов, стиральных и посудомоечных машин многие мастера советуют использовать именно такие фильтры-умягчители.
Фильтры на основе ионообменных смол жарких споров не вызывают. Это недорогая и достаточно эффективная технология умягчения воды, которая используется и в промышленности, и в быту.
Основные способы снижения жесткости воды представлены в этом видеоролике.
ofiltrah.ru
Умягчение воды. Умягчение воды в домашних условиях. Что такое умягчение воды
АкваЩит - Умягчение воды
Вода - неотьемлемая часть нашей жизни. Сегодня ее, где только не используют. Это и промышленность, и быт, и непосредственно использование в еду и питье. Естественно, что вопросам ее очистки уделяется очень много внимания. Каждый из нас видел, в каком состоянии у нас реки, протекающие через города и села. И даже если они прозрачны, то тут, то там возникают обьявления о холерной палочке и тому подобных болезнях. То есть вода из любого первичного источника, в том числе из артезианской скважины будет жесткой. А значит, умягчение воды станет необходимостью, если вы хотите сократить свои расходы и заодно защитить себя от влияния повышенной жесткости воды.

Умягчению воды и его видам мы и посвятим эту статью. Но сперва разберемся, что собой представляет жесткая вода, в чем ее вред и почему умягчение воды считается единственным качественным способом снизить жесткость воды. Итак, жесткой воду делают две соли. Причем это не просто включение солей кальция и магния, это превышение допустимых пределов жесткости воды. Вода может быть мягкой, жесткой и очень жесткой. Умягчение воды необходимо всем тем, у кого показатель жесткости колеблется от просто жесткой воды до очень жесткой.
Казалось бы, воду забирают не просто из первичного источника, а из артезианской скважины. Откуда там могут взяться соли кальция и магния? Откуда вообще вода появляется в артезианской скважине? Здесь несколько вариантов. Это вода из подземных рек, или вода, прошедшая сквозь почву, после таяния ледников. Нужно помнить, что вода является одним из самых лучших естественных растворителей. И вот когда вода течет, пропитывает почву и по пути к скважине встречает залежи полезных ископаемых там, и она и набирает свой состав, становится железистой или чересчур жесткой. Так или иначе, но вода из источника - это всегда вода с определенным составом примесей. Причем для здоровья такой состав может быть полезным в малых дозах, а вот для промышленного оборудования может быть губительным.
Что касается воды не из скважины, то там все намного печальнее. В воде, что только не встретишь, и на высокую степень прозрачности воды также рассчитывать не приходится. Когда вода поступает к нам из централизованной системы очистки воды, то там она уже прошла определенные стадии чистки. К сожалению, водоподготовке с помощью АкваЩит у нас не уделяют много внимания, из-за устаревших систем и из-за дороговизны системы очистки и умягчения воды. Да и с хлоркой в качестве дезинфектора часто усердствуют. В результате имеем жесткую воду, которая образует накипь.
Зачем нам так нужно понимать умягчение воды, что это такое? Здесь вся проблема состоит в том, что жесткая вода имеет недостатки и это не только накипь. Из-за этих проблем и пришли к изобретению умягчителей воды. Поэтому разбираться будем постепенно. Определимся сперва с жесткой водой.
Она негативно влияет еще до того, как образуется известковый налет. Ваше здоровье и вещи ощутят влияние повышенной жесткости воды по полной программе. Они, по сути, и будут поверхностями, куда соли жесткости выпадут, образуя нерастворимый осадок. В бытовых приборах, это нагревательные элементы и поверхности. В человеческом организме – кожа, волосы и внутренние органы. В тканях, поры тканей при стирке.
Соли жесткости оседают на любых поверхностях. Постоянное употребление жесткой воды в пищу стимулирует образование язвы, камней в почках и т.п. болезней не хуже употребления соленого и острого в больших количествах. Да и кожу очень сильно сушит. Все эти причины и вызвали так сказать развитие технической мысли. Ведь для человеческого организма любое удаление накипи безразлично. Ведь оно проходит уже после использования жесткой воды в пищу. В данном разделе мы рассмотрели информацию про умягчение воды. Надеемся, вы все поняли.
Цены на умягчение воды
 Теперь, что касается цен на умягчение воды и быстрой изнашиваемости вещей, из-за высокой жесткости. Такая вода крайне плохо растворяет любые моющие вещества. Даже голову помыть в такой воде проблематично. Думаю, каждый замечал, насколько плохо мылится любой шампунь в жесткой воде. Тот же примерно эффект происходит и при стирке. Соли жесткости застревают в порах тканей, не давая и грязи вымываться и порошку. В результате на поверхностях образуется белое пятно. Многим кажется, что это плохо выстиранный порошок. Но пятно так просто не удаляется, т.к. кроме порошка там еще и соли жесткости находятся. В результате и ткани быстрее изнашиваются, и вещи выглядят блекло и некрасиво. Поэтому, не стоит экономить на цене на умягчение воды. Потом будете платить вдвойне.
Теперь, что касается цен на умягчение воды и быстрой изнашиваемости вещей, из-за высокой жесткости. Такая вода крайне плохо растворяет любые моющие вещества. Даже голову помыть в такой воде проблематично. Думаю, каждый замечал, насколько плохо мылится любой шампунь в жесткой воде. Тот же примерно эффект происходит и при стирке. Соли жесткости застревают в порах тканей, не давая и грязи вымываться и порошку. В результате на поверхностях образуется белое пятно. Многим кажется, что это плохо выстиранный порошок. Но пятно так просто не удаляется, т.к. кроме порошка там еще и соли жесткости находятся. В результате и ткани быстрее изнашиваются, и вещи выглядят блекло и некрасиво. Поэтому, не стоит экономить на цене на умягчение воды. Потом будете платить вдвойне.
Но кроме этого у накипи есть еще такой недостаток, как плохая проводимость тепла. То есть она полностью блокирует нормальную работу любого бытового прибора. В то время, как умягчение воды устраняет из нее излишек солей жесткости до того, как жесткая вода поступит в бытовой прибор или к вам в чашку. Потому оно сегодня так стремительно набирает популярность. Хотя цены на умягчение воды и высокие, но тем не менее оно пользуется популярностью у предприятий и у владельцев коттеджей.
Из-за плохой теплопроводимости, в любом бытовом приборе или оборудовании на предприятии начнет резко расти расход топлива. Увеличится время нагрева воды, причем это произойдет довольно резко. И чем больше будет слой накипи, тем хуже будет нагрев и тем дольше он будет. Закрывая нагревательный элемент плотным слоем, накипь не дает ему отдать тепло воде. Но кроме этого, сама поверхность будет находиться в условиях практически экстремальных. Температура нагрева ведь не будет оставаться на месте. Разогреваться вечно, поверхность не сможет. И в результате прибор перегорит.
В промышленности последствия отложения накипи выливаются в куда более худшие последствия. Там трубы стираются в буквальном смысле. А котлы в котельной могут взорваться от перегрузок. Поэтому единственным правильным решением для промышленности или дома, когда есть острая необходимость устранить повышенную жесткость воды, это расчет и цены на умягчитель воды. Надеюсь, вы поняли, что цены на умягчение воды хоть и высокие, но экономить тут не стоит.
Умягчение воды в домашних условиях
Чтобы защитить себя со всех сторон, запомните, что качественное умягчение воды в домашних условиях или в квартире ли, на предприятии ли не может состоять из одного умягчителя воды. Вам все равно придется, либо проводить полный цикл очистки воды, либо устанавливать один умягчитель воды для парового и водогрейного котла, и один для производства питьевой воды.
Кроме того, что накипь стимулирует повышенный расход топлива, а также может привести к поломке прибора, она также способствует развитию коррозии. Потом нельзя удалять накипь вечно. Поверхности тоже страдают. Вы снимаете с них защитных слой, царапаете поверхность, нарушаете целостность. От этого приборы будут хуже работать. И это все последствия только от удаления накипи и не во время выполненного удаления накипи. Это отнюдь не самая полезная и главное дешевая процедура. Вот все эти факты и заставили задуматься человечество о путях избежания появления такого последствия, как накипь. Так изобрели умягчение воды в домашних условиях.
 Итак, умягчение воды, что это такое? Это устранение из воды излишка солей жесткости, путем химического воздействия или естественных физических процессов. На сегодня умягчение воды в домашних представлено двумя большими группами. Это реагентные способы, которые работают с помощью различных химикатов и реакций с ними. И группа безреагентных фильтров для воды. Последние используют в работе исключительно естественные процессы и расхода реагентов не требуют.
Итак, умягчение воды, что это такое? Это устранение из воды излишка солей жесткости, путем химического воздействия или естественных физических процессов. На сегодня умягчение воды в домашних представлено двумя большими группами. Это реагентные способы, которые работают с помощью различных химикатов и реакций с ними. И группа безреагентных фильтров для воды. Последние используют в работе исключительно естественные процессы и расхода реагентов не требуют.
К реагентным фильтрам для воды относят ионообменные установки, потом озонаторы, фосфатирование, хлорирование. Все это варианты умягчения воды в домашних условиях с помощью химических веществ. Во время очистки воды или восстановления могут использоваться различные реагенты. Они вступают в реакцию с солями жесткости, образуя новые вещества. Тогда умягчение воды в домашних называется реагентным.
Безреагентное умягчение воды в домашних условиях, что это такое? Тот же самый процесс устранения излишка жесткости путем преобразования формы кристаллов солей жесткости, которое позволяет не прилипать им к поверхностям оборудования. В качестве примера подобных умягчителей можно упомянуть – магнитную установку, электромагнитный умягчитель воды АкваЩит, ультразвуковой прибор. Работают они на одном принципе. Только силы используют в работе разные. Разве только магнитные и электромагнитные силовые поля являются родственными.
Итак, умягчение воды, что это такое? Мы постарались ответить на этот вопрос более подробно. Ниже рассмотрим самые популярные фильтры для воды, их достоинства и недостатки, как варианты умягчения воды в домашних условиях. И еще один вопрос, который заботит, пожалуй, каждую хозяйку, в сегодняшних реалиях. Умягчение воды своими руками, возможно ли сегодня подобное?
Что вам сказать на этот вопрос… Пока не изучили полезные свойства магнитов, пока не знали, как работает ионообменная смола с солями жесткости, к очистке воды тоже старались подходить по мере своих возможностей. Делали простейшие фильтры из разнообразных засыпок. Применяли и уголь, и песок, и гравий. Правда, к умягчению воды это имело отдаленное отношение. Впрочем, воздействие магнита на воду так и открыли, путем проб и ошибок.
С уверенностью можно сказать, что в современных условиях умягчение воды в домашних условиях практически невозможно. Единственный наиболее подходящий к этому понятию вариант – это применение кремния в качестве очистителя. Если вы слышали когда-нибудь про кремниевую воду, то вот она обладает как раз не только свойствами лечебной воды. Это еще и мягкая вода. И очистку от излишка солей жесткости здесь производит именно кусочек кремния. Все, что вам для этого нужно, это бросить небольшой кусок кремния(чистого!) в трехлитровый бутыль воды и подержать его там несколько дней. После этого вода станет мягкой, и ее можно будет использовать просто для питья, и для готовки.
Что такое умягчение воды
Теперь узнаем, что такое умягчение воды. Мы знаем, что большое содержание солей жесткости, это вредно. Но что это такое умягчение воды? Как мы понимаем, скорость подобной очистки воды очень медленная. Поэтому такую очистку можно использовать просто для лечения, но не в качестве постоянного очистителя воды. Есть для домашних условий специальные порошки – умягчители воды своими руками. Но отнести их к понятию что такое умягчение воды своими руками вряд ли возможно. Так, что сегодня умягчить воду можно только путем установки фильтра для воды.
Какие же способы умягчения воды используют в основе фильтров для воды? Химический способ как было сказано выше, является основой для ионообменного умягчителя. Такой вид фильтров в быту практически не встречается, за исключением фильтра-кувшина. Любое использование химикатов при производстве мягкой воды сразу же пресекает ее применение в качестве питьевой.
 Почему же тогда можно использовать ионообменный фильтр-кувшин? И что такое умягчение воды? Здесь вся разница с другими подобными установками состоит в том, что фильтр не восстанавливают в конкретной модели, а меняют. В промышленности же в водоподготовке использовать сменные фильтры – большая роскошь. И там их восстанавливают и снова пускают в ход. На восстановление тоже тратят немалые деньги. Хоть и регенератором является обычная соль. Но ее обьемы в промышленных масштабах, выливаются в крупные суммы. И восстановление приходится проводить чаще. Правда у подобных ионообменных установок есть и свои плюсы. Понижать степень жесткости воды, можно чуть ли не до нуля. Но тогда вода будет слишком натриевой. И еще такой вид очистки воды один из самых быстрых. Другие фильтры так быстро не работают.
Почему же тогда можно использовать ионообменный фильтр-кувшин? И что такое умягчение воды? Здесь вся разница с другими подобными установками состоит в том, что фильтр не восстанавливают в конкретной модели, а меняют. В промышленности же в водоподготовке использовать сменные фильтры – большая роскошь. И там их восстанавливают и снова пускают в ход. На восстановление тоже тратят немалые деньги. Хоть и регенератором является обычная соль. Но ее обьемы в промышленных масштабах, выливаются в крупные суммы. И восстановление приходится проводить чаще. Правда у подобных ионообменных установок есть и свои плюсы. Понижать степень жесткости воды, можно чуть ли не до нуля. Но тогда вода будет слишком натриевой. И еще такой вид очистки воды один из самых быстрых. Другие фильтры так быстро не работают.
Теперь, что касается непосредственно процесса очистки. Внутри фильтра-кувшина располагается картридж с ионообменной смолой. Она специально обогащена натрием, который внутри структуры очень плохо держится. Когда в такой фильтр поступает жесткая вода, происходит смена одних ионов на другие. Фильтр постепенно забивается. Когда он полностью отдаст свой натрий, приходит время его менять. Это тоже расходы. И немалые. Т.к. стоит картридж как треть самой установки, хоть она и дешевая. Однако постоянно возиться с заменами вряд ли кому то захочется. Да и воды очищенной хватит только на личное потребление.
Следующий бытовой фильтр для умягчения воды – безреагентный. Пример – магнитный или электромагнитный умягчитель воды АкваЩит. У магнитного основа, как вы понимаете мощные постоянные магниты. Делают их из качественных редкоземельных металлов. Они почти не теряют магнитных свойств за годы работы. Это позволяет использовать магнитную установку в течение четверти века без всяких замен и восстановлений. Кстати большая простота использования, отсутствие обслуживания является одним из главных козырей что магнитного, что электромагнитного умягчителя. Вы поняли, что такое умягчение воды и цена на него.
Такой прибор не требует врезания в трубу, он просто одевается на трубу, работать начинает мгновенно. Ему не нужны чистки, восстановления и промывки. Это прибор, который можно поставить и забыть о нем на 25 лет. Он занимает мало места, а магистральные модели в состоянии очищать большие обьемы воды.
Устанавливая такой прибор, обязательно проверьте свою трубу. Внутри не должно быть старой накипи, если она есть, ее нужно убрать, но только на этом отрезке трубы, куда вы будете монтировать устройство. Через старую накипь магнитное поле не сработает.
К огромным плюсам магнитного прибора относят и тот факт, что он позволяет не только умягчать воду. Под воздействием магнитных силовых полей, кристаллы солей жесткости начинают меняться. Из удобных плоских прямоугольников, они превращаются в тонкие, острые иглы. Прилипать к поверхностям не получается. Неудобно, да и нечем. Но иголки продолжают тереться о поверхности. При этом они очень качественно устраняют старую накипь, не оставляя после себя следов. Чистка происходит на молекулярном уровне. Такие приборы из-за такого двойного эффекта в работе получили большую популярность в теплоэнергетике и быту. Но используют больше электромагнитный умягчитель воды АкваЩит, а не его магнитный аналог.
Выбор падает на электромагнитное устройство потому, что требований к воде у него намного меньше. Он работает и с горячей водой, и водой, текущей в двух направлениях. Также ему неважно, с какой скоростью течет вода. Так, что это такое умягчение воды с помощью электромагнитного прибора всегда предпочтительнее.
То есть, умягчение воды предназначено для защиты нашего здоровья и бюджета от вредных последствий повышенной жесткости воды. Установив водоподготовку в квартире или на производстве, мы сознательно выбираем качественную чистку воды, которая поможет нам сохранить здоровье и гарантирует нам качество продукции, которую мы будем производить. Из данной статьи мы знали, что такое умягчение воды и почему так важно его делать.
vodopodgotovka-vodi.ru



















