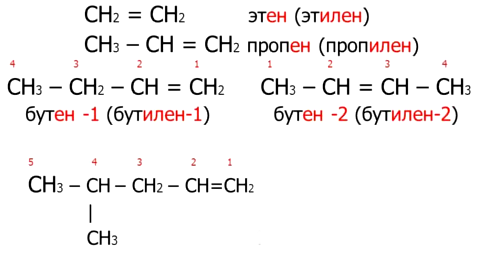
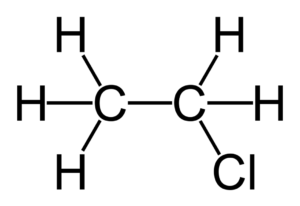
Пять удивительных фактов о воде. Стекловидная вода
Загадочная h3O: 5 нераскрытых тайн простой воды
В старой доброй формуле h3O, казалось бы, не заключено никаких тайн. Но на самом деле вода – источник жизни и самая известная жидкость в мире – таит в себе множество загадок, неподвластных даже ученым. Пять самых известных “странностей” воды – перед вами.1. Горячая вода замерзает быстрее холодной
Возьмем две емкости с водой: в один нальем горячую, а в другой — холодную воду. Поместим их в морозильную камеру. Емкость с горячей водой замерзнет быстрее, чем с холодной, хотя по логике вещей, первой должна была превратиться в лед емкость с холодной водой: ведь горячей надо сначала остыть до температуры холодной, а потом уже превращаться в лед, а холодной остывать не надо. Почему же так происходит?
 В 1963 году ученик старших классов Эрасто Б. Мпемба заметил, что горячая смесь застывает в морозильной камере быстрее, чем холодная. Учитель физики, с которым юноша поделился открытием, поднял его на смех. К счастью, ученик оказался настырным и убедил учителя провести эксперимент, который и подтвердил его правоту. Теперь феномен горячей воды, замерзающей быстрее холодной, носит название “эффект Мпемба”. Ученые так до конца и не понимают природу этого явления, объясняя его разницей в переохлаждении, испарении, формировании льда и т.д.
В 1963 году ученик старших классов Эрасто Б. Мпемба заметил, что горячая смесь застывает в морозильной камере быстрее, чем холодная. Учитель физики, с которым юноша поделился открытием, поднял его на смех. К счастью, ученик оказался настырным и убедил учителя провести эксперимент, который и подтвердил его правоту. Теперь феномен горячей воды, замерзающей быстрее холодной, носит название “эффект Мпемба”. Ученые так до конца и не понимают природу этого явления, объясняя его разницей в переохлаждении, испарении, формировании льда и т.д.2. “Сверхохлаждение” предотвращает формирование льда
Все знают, что вода всегда превращается в лед при охлаждении ее до нуля градусов по Цельсию… за исключением тех случаев, когда этого не происходит! “Сверхохлаждение” – это склонность воды оставаться жидкой, даже будучи охлажденной до температуры ниже точки замерзания. Это явление становится возможным благодаря тому, что окружающая среда не содержит центров или ядер кристаллизации, которые могли бы спровоцировать образование кристаллов льда. Именно поэтому вода остается в жидкой форме, даже будучи охлажденной до температуры ниже нуля градусов по Цельсию. Когда процесс кристаллизации запускается, можно наблюдать, как “сверхохлажденная” вода в одно мгновение превращается в лед. Убедитесь сами — смотрите ролик на нашем сайте.
3. “Стекловидная” вода
Быстро, не задумываясь, скажите, сколько различных состояний есть у воды? Вы сказали, три? Твердое, жидкое, газообразное? А вот и нет. Ученые выделяют как минимум 5 состояний “жидкой” воды и 14 состояний льда. Помните разговор про сверхохлажденню воду? Так вот, что бы вы ни делали, при температуре -38 °C самая сверхохлажденная вода внезапно превратится в лед. А ВТО же произойдет при дальнейшем понижении температуры? При -120 °C лед становится тягучим, как патока, а при -135 °C и ниже он превращается в “стеклянную” или “стекловидную” воду – твердое вещество с отсутствием кристаллов.
4. Квантовое число воды
На молекулярном уровне воде есть чем удивить ученых. В 1995 году проводимый учеными эксперимент по рассеянию нейтронов дал неожиданный результат: было обнаружено, что нейтроны, направленные на молекулы воды, “видят” на 25% меньше протонов водорода. Оказалось, что на скорости одной аттосекунды (10 в минус 18 степени секунд) имеет место необычный квантовый эффект, и химическая формула воды из привычной Н2О превращается в Н1,5О!Что такое одна аттосекунда, спросите вы? Это время, за которое свет проходит расстояние, сравнимое с размерами молекулы воды.
5. Есть ли у воды память?
Альтернативная официальной медицине гомеопатия утверждает, что слабый раствор лекарственного препарата может оказывать лечебный эффект на организм и сохранить свойства раствора первоначальной концентрации, даже если коэффициент разбавления настолько велик, что в растворе уже не остается ничего, кроме молекул воды. Приверженцы гомеопатии как метода лечения объясняют этот парадокс коцепцией под названием “память воды”. В 2002 году международная группа ученых во главе с профессором Мэдлин Эннис из Королевского университета в Белфасте, ранее критиковавшая принципы гомеопатии, заявила о том, что ей удалось доказать реальность эффекта “памяти воды” Однако опыты, проведенные под наблюдением независимых экспертов, результатов не принесли. Дискуссия о феномене “памяти воды” продолжается.
papyrus-net.livejournal.com
Вода - пять удивительных фактов
 Вода... Ее можно называть как угодно – от романтического "источник жизни" до сухого и научного "h3O"… Многим вода кажется самым простой субстанцией, которую только можно себе представить. Однако в действительности вода – тот самый источник жизни, чаще всего встречающийся на Земле в жидком виде – является крайне таинственным веществом.
Вода... Ее можно называть как угодно – от романтического "источник жизни" до сухого и научного "h3O"… Многим вода кажется самым простой субстанцией, которую только можно себе представить. Однако в действительности вода – тот самый источник жизни, чаще всего встречающийся на Земле в жидком виде – является крайне таинственным веществом.Достаточно сказать, что ученые до сих пор не могут внятно обосновать все свойства воды. Если вы сомневаетесь в ее таинственности, предлагаем вашему вниманию пять наиболее удивительных фактов о свойствах воды.
Горячая вода замерзает быстрее, чем холодная вода
Возьмите две емкости с водой (можно небольшие). Наполните одну горячей водой, а другую – холодной. Поставьте их в морозилку (только не испортите ее!). Горячая вода замерзнет быстрее холодной. Подождите, скажете вы! Это же противоречит здравому смыслу! Разве не должна горячая вода вначале остыть до температуры холодной, а уж затем подвергнуться замерзанию, в то время как холодной воде требуется гораздо меньше времени для замерзания?В 1963-ем году танзанийский студент по имени Эрасто Мпемба, экспериментируя на кулинарном поприще, замораживал горячее мороженое, когда вдруг заметил, что горячая смесь замерзла быстрее, чем обычное подтаявшее мороженое. Когда он поинтересовался у своего преподавателя о причине данного феномена, тот высмеял студента, заявив, что данное явление не имеет никакого отношения к классической физике, а является частью "физики Мпемба".
К счастью, Мпемба был не из обидчивых. Он настоял на проведении эксперимента, который, в конечном итоге, подтвердил наблюдения студента: при определенных условиях горячая вода действительно замерзала быстрее холодной воды! Мпембо повезло, так как он прославился, и с тех пор данный феномен стали называть эффектом Мпембы. Впрочем, данное явление было замечено еще такими великими учеными, как Аристотель, Рене Декарт и некоторыми другими.
Однако как же ученые объясняют данный странный феномен? На самом деле, однозначного ответа не может дать ни один профессор, хотя существует несколько возможных объяснений данного явления. При этом многие из объяснений весьма сложны, так как учитывают такие сложные процессы, как переохлаждение, испарение, образование центров кристаллизации, конвекцию, а также эффект растворенных газов для горячей и холодной воды.
Сверхохлаждение и "мгновенное" замерзание
Казалось бы, каждому ребенку известно, что для того, чтобы вода превратилась в лед, ее необходимо охладить до нуля градусов Цельсия. Однако в некоторых случаях этого не происходит! К примеру, вы можете попытаться заморозить сверхочищенную воду, охладив ее много ниже нуля градусов (естественно, при соответствующем давлении!), однако она даже не подумает твердеть.Ученым известно достаточно много о сверхохлаждении. Данное явление происходит тогда, когда кристаллам льда для начала формирования необходима своеобразная точка образования. Данной точкой может быть все, что угодно, начиная от пузырька воздуха и заканчивая плавающей соринкой в воде. Если ничего этого не наблюдается, вода будет продолжать оставаться сверхохлажденной жидкостью без превращения в лед.
Однако если такая отправная точка имеется (для этого достаточно встряхнуть бутылку с сверхохлажденной водой, чтобы возникли пузырьки), вода начинает мгновенно превращаться в лед. В Интернете сейчас можно найти бесчисленное количество видеороликов, демонстрирующих нам именно такое явление. Примечательно, что аналогичным образом и перегретая очищенная вода "не желает" превращаться в пар, даже если ее температура превышает температуру кипения воды.
Стекловидная вода
Ответьте-ка не раздумывая долго: сколько агрегатных состояний воды вы знаете? Если вы припомните только три фазы – жидкость, газ и твердое состояние – то вы ошиблись. На самом деле, существует, по крайней мере, пять различных фаз жидкой воды и целых 14 различных фаз (это те, что ученым удалось открыть!) льда.Взять хотя бы тот же эффект сверхохлаждения. Оказывается, как бы вы ни старались, но даже идеально очищенная вода немедленно превратится в лед при температуре -38°C. Однако что произойдет в том случае, если мы продолжим опускать температуру воды? Как только вы дойдете до отметки в -120°C, начнет происходить нечто очень странное: вода станет чрезвычайно вязкой и густой, как патока. А при температуре в -135°C вода превратится в так называемую стекловидную воду, то есть, станет твердой, но не будет иметь кристаллическую структуру.
Количественные характеристики воды
На молекулярном уровне поведение воды еще более таинственное! В 1995-ом году эксперимент по рассеиванию нейронов принес ученым неожиданные результаты: физики обнаружили, что когда нейроны нацелены на молекулы воды, им удается "различить" лишь 25 процентов протонов водорода.Иными словами, не вдаваясь в сложные научные объяснения, можно сказать, что в какую-то долю секунды (точнее говоря, 10-18 секунды) возникает загадочный количественный эффект и химическая формула воды на это время перестает быть h3O, а становится h2,5O!
Обладает ли вода памятью?
Один из разделов гомеопатии – альтернативной медицины – основан на том, что разбавленные растворы веществ способны оказывать исцеляющий эффект. Причем, этот эффект наблюдается даже тогда, когда коэффициент разбавления настолько велик, что невозможно в растворе обнаружить ни единой молекулы растворенного вещества, кроме молекул самой воды. Сторонники гомеопатии объясняют данный парадокс тем, что существует такое понятие, как "память воды". Мол, молекулы воды просто "запоминают" информацию о тех частицах вещества, которое было растворено в воде.Впрочем, данное заявление лишено всякого здравого смысла для подавляющего большинства сторонников традиционной медицины. Не верила в подобные свойства воды и некая Маделейн Эннис, фармаколог и профессор Королевского университета в Белфасте, Северная Ирландия. Эннис, которая всегда была ярым критиком гомеопатии, даже решила провести специальный эксперимент, чтобы доказать, что никакой памяти у воды нет. Эксперимент был проведен, однако результаты его оказались совсем не те, что ожидала профессор Эннис.
В своем недавнем отчете Эннис детально описала процесс наблюдения за тем, какой эффект оказывает сверхрастворенный раствор гистамина на лейкоциты, которые борются с воспалительным процессом. Лейкоциты, которые называют базофилами, высвобождают гистамин тогда, когда клетка подвергается атаке. Однако гистамин не способен вырабатываться неоднократно. Исследование, проведенное в четырех разных лабораториях, выявило, что гомеопатические жидкости (растворенные настолько, что в них невозможно обнаружить ни одной молекулы гистамина) выполняют функции гистамина!
Скорее всего, Эннис не обрадовалась, когда получила подобный результат, однако отрицать сам факт эффекта памяти она более не могла. Так почему же так произошло? Как известно, гомеопаты приготавливают свои растворы, разводя в них различные вещества (к примеру, древесный уголь, белладонну, яд паука в этаноле и так далее) . Затем полученный раствор снова и снова многократно разбавляют водой, пока не остается лишь своеобразный отпечаток молекул растворенного вещества на молекулах воды. При этом полученная жидкость сохраняет свойства лекарства.
На самом деле, скептицизм Эннис можно понять. Более того: в некоторых испытаниях вместо гомеопатических средств применялось плацебо (в данном случае обычная питьевая вода) при лечении пациентов. На многих такое "лечение" действовало благотворно. Однако совсем иная ситуация сложилась при эксперименте в Белфасте. Профессор Эннис признала, что официальная наука не в состоянии объяснить обнаруженный учеными феномен, а посему требуются дополнительные исследования. Однако если данный феномен подтвердится, следует пересмотреть всю физику и химию!
Известно, что ученые пока не смогли повторить эксперимент Эннис. В то же время, сама Эннис не готова признать наличие памяти у воды, а лишь подтверждает факт наблюдения необычного эффекта. Однако совсем недавно группа ученых из Торонтского университета, Канада, исследовала динамические свойства воды, используя так называемую многоразмерную нелинейную инфракрасную спектроскопию. Как оказалось, молекулы воды действительно продемонстрировали то, что можно назвать памятью. Однако, к несчастью для гомеопатов, длился данный эффект всего 5 на 10-14 секунды! Мистика, да и только...
russiahousenews.info
Пять удивительных фактов о воде
Вода… Ее можно называть как угодно – от романтического "источник жизни" до сухого и научного "h3O"… Многим вода кажется самым простой субстанцией, которую только можно себе представить. Однако в действительности вода – тот самый источник жизни, чаще всего встречающийся на Земле в жидком виде – является крайне таинственным веществом.
Достаточно сказать, что ученые до сих пор не могут внятно обосновать все свойства воды. Если вы сомневаетесь в ее таинственности, предлагаем вашему вниманию пять наиболее удивительных фактов о свойствах воды.
Возьмите две емкости с водой (можно небольшие). Наполните одну горячей водой, а другую – холодной. Поставьте их в морозилку (только не испортите ее!). Горячая вода замерзнет быстрее холодной. Подождите, скажете вы! Это же противоречит здравому смыслу! Разве не должна горячая вода вначале остыть до температуры холодной, а уж затем подвергнуться замерзанию, в то время как холодной воде требуется гораздо меньше времени для замерзания?
В 1963-ем году танзанийский студент по имени Эрасто Мпемба, экспериментируя на кулинарном поприще, замораживал горячее мороженое, когда вдруг заметил, что горячая смесь замерзла быстрее, чем обычное подтаявшее мороженое. Когда он поинтересовался у своего преподавателя о причине данного феномена, тот высмеял студента, заявив, что данное явление не имеет никакого отношения к классической физике, а является частью "физики Мпемба".
К счастью, Мпемба был не из обидчивых. Он настоял на проведении эксперимента, который, в конечном итоге, подтвердил наблюдения студента: при определенных условиях горячая вода действительно замерзала быстрее холодной воды! Мпембо повезло, так как он прославился, и с тех пор данный феномен стали называть эффектом Мпембы. Впрочем, данное явление было замечено еще такими великими учеными, как Аристотель, Рене Декарт и некоторыми другими.
Однако как же ученые объясняют данный странный феномен? На самом деле, однозначного ответа не может дать ни один профессор, хотя существует несколько возможных объяснений данного явления. При этом многие из объяснений весьма сложны, так как учитывают такие сложные процессы, как переохлаждение, испарение, образование центров кристаллизации, конвекцию, а также эффект растворенных газов для горячей и холодной воды.
Казалось бы, каждому ребенку известно, что для того, чтобы вода превратилась в лед, ее необходимо охладить до нуля градусов Цельсия. Однако в некоторых случаях этого не происходит! К примеру, вы можете попытаться заморозить сверхочищенную воду, охладив ее много ниже нуля градусов (естественно, при соответствующем давлении!), однако она даже не подумает твердеть.
Ученым известно достаточно много о сверхохлаждении. Данное явление происходит тогда, когда кристаллам льда для начала формирования необходима своеобразная точка образования. Данной точкой может быть все, что угодно, начиная от пузырька воздуха и заканчивая плавающей соринкой в воде. Если ничего этого не наблюдается, вода будет продолжать оставаться сверхохлажденной жидкостью без превращения в лед.
Однако если такая отправная точка имеется (для этого достаточно встряхнуть бутылку с сверхохлажденной водой, чтобы возникли пузырьки), вода начинает мгновенно превращаться в лед. В Интернете сейчас можно найти бесчисленное количество видеороликов, демонстрирующих нам именно такое явление. Примечательно, что аналогичным образом и перегретая очищенная вода "не желает" превращаться в пар, даже если ее температура превышает температуру кипения воды.
Ответьте-ка не раздумывая долго: сколько агрегатных состояний воды вы знаете? Если вы припомните только три фазы – жидкость, газ и твердое состояние – то вы ошиблись. На самом деле, существует, по крайней мере, пять различных фаз жидкой воды и целых 14 различных фаз (это те, что ученым удалось открыть!) льда.
Взять хотя бы тот же эффект сверхохлаждения. Оказывается, как бы вы ни старались, но даже идеально очищенная вода немедленно превратится в лед при температуре -38°C. Однако что произойдет в том случае, если мы продолжим опускать температуру воды? Как только вы дойдете до отметки в -120°C, начнет происходить нечто очень странное: вода станет чрезвычайно вязкой и густой, как патока. А при температуре в -135°C вода превратится в так называемую стекловидную воду, то есть, станет твердой, но не будет иметь кристаллическую структуру.
На молекулярном уровне поведение воды еще более таинственное! В 1995-ом году эксперимент по рассеиванию нейронов принес ученым неожиданные результаты: физики обнаружили, что когда нейроны нацелены на молекулы воды, им удается "различить" лишь 25 процентов протонов водорода.
Иными словами, не вдаваясь в сложные научные объяснения, можно сказать, что в какую-то долю секунды (точнее говоря, 10-18 секунды) возникает загадочный количественный эффект и химическая формула воды на это время перестает быть h3O, а становится h2,5O!
Один из разделов гомеопатии – альтернативной медицины – основан на том, что разбавленные растворы веществ способны оказывать исцеляющий эффект. Причем, этот эффект наблюдается даже тогда, когда коэффициент разбавления настолько велик, что невозможно в растворе обнаружить ни единой молекулы растворенного вещества, кроме молекул самой воды. Сторонники гомеопатии объясняют данный парадокс тем, что существует такое понятие, как "память воды". Мол, молекулы воды просто "запоминают" информацию о тех частицах вещества, которое было растворено в воде.
Впрочем, данное заявление лишено всякого здравого смысла для подавляющего большинства сторонников традиционной медицины. Не верила в подобные свойства воды и некая Маделейн Эннис, фармаколог и профессор Королевского университета в Белфасте, Северная Ирландия. Эннис, которая всегда была ярым критиком гомеопатии, даже решила провести специальный эксперимент, чтобы доказать, что никакой памяти у воды нет. Эксперимент был проведен, однако результаты его оказались совсем не те, что ожидала профессор Эннис.
В своем недавнем отчете Эннис детально описала процесс наблюдения за тем, какой эффект оказывает сверхрастворенный раствор гистамина на лейкоциты, которые борются с воспалительным процессом. Лейкоциты, которые называют базофилами, высвобождают гистамин тогда, когда клетка подвергается атаке. Однако гистамин не способен вырабатываться неоднократно. Исследование, проведенное в четырех разных лабораториях, выявило, что гомеопатические жидкости (растворенные настолько, что в них невозможно обнаружить ни одной молекулы гистамина) выполняют функции гистамина!
Скорее всего, Эннис не обрадовалась, когда получила подобный результат, однако отрицать сам факт эффекта памяти она более не могла. Так почему же так произошло? Как известно, гомеопаты приготавливают свои растворы, разводя в них различные вещества (к примеру, древесный уголь, белладонну, яд паука в этаноле и так далее) . Затем полученный раствор снова и снова многократно разбавляют водой, пока не остается лишь своеобразный отпечаток молекул растворенного вещества на молекулах воды. При этом полученная жидкость сохраняет свойства лекарства.
На самом деле, скептицизм Эннис можно понять. Более того: в некоторых испытаниях вместо гомеопатических средств применялось плацебо (в данном случае обычная питьевая вода) при лечении пациентов. На многих такое "лечение" действовало благотворно. Однако совсем иная ситуация сложилась при эксперименте в Белфасте. Профессор Эннис признала, что официальная наука не в состоянии объяснить обнаруженный учеными феномен, а посему требуются дополнительные исследования. Однако если данный феномен подтвердится, следует пересмотреть всю физику и химию!
Известно, что ученые пока не смогли повторить эксперимент Эннис. В то же время, сама Эннис не готова признать наличие памяти у воды, а лишь подтверждает факт наблюдения необычного эффекта. Однако совсем недавно группа ученых из Торонтского университета, Канада, исследовала динамические свойства воды, используя так называемую многоразмерную нелинейную инфракрасную спектроскопию. Как оказалось, молекулы воды действительно продемонстрировали то, что можно назвать памятью. Однако, к несчастью для гомеопатов, длился данный эффект всего 5 на 10-14 секунды! Мистика, да и только…
www.kabanik.ru
Вода стеклообразная - Справочник химика 21
Предложен механизм сорбции воды стеклообразными сахарами, по которому поглощение воды идет через плавление сахаров, когда диффузия молекул воды и достижение термодинамического равновесия становятся практически возможными. [c.277]Для затворения сухой смеси применяют жидкое стекло. Получают его растворением в воде стеклообразной массы — силикат-глыбы, которая представляет собой сплав кварцевого песка и соды (или сульфата натрия), взятых в определенных соотношениях. По внешнему виду силикат-глыба представляет собой прозрачные куски синевато-зеленоватого или желтоватого цвета. [c.66]
Метафосфорная кислота — стеклообразная масса, легко растворяющаяся в воде. Пирофосфорная кислота — бесцветное кристаллическое вещество, легко растворяющееся в воде с разогреванием. Ортофосфорная кислота — бесцветный кристаллический продукт плотность ее 1,83 т. пл. 42,35° С. [c.537]Сила полифосфорных кислот возрастает с увеличением числа атомов фосфора в цепочке. При недостатке воды образуется полимерная метафосфорная кислота в виде стеклообразной массы, хорошо растворимой в воде [c.127]
Растворы сульфатов титана в воде обладают рядом свойств, которые отличают их от истинных и коллоидных растворов. Все они дают эффект Тиндаля. В большинстве случаев при их упаривании образуется стеклообразная масса, а не кристаллический осадок. В то же время титан проходит через перегородку, проницаемую только для ионов. Противоречивые свойства растворов сульфатов титана объясняются тем, что титан в них находится как в ионном, так и в коллоидном состояниях, находящихся в равновесии между собой. В концентрированных сильнокислых растворах преобладает ионное состояние, характеризуемое многообразием ионных форм, а в разбавленных и слабокислых растворах — коллоидное состояние. Сложность и метастабильность ионных равновесий в растворах сульфата титана обусловлена одновременным протеканием гидролиза, диссоциации, комплексообразования и гидролитической полимеризации. Все это затрудняет их изучение и является причиной противоречивости данных различных авторов. [c.224]
В качестве методически важных сведений, полученных в рассматриваемом цикле работ, следует отметить достижение высокой (96—99%) степени сгорания для всех исследовавшихся веществ (причем в большинстве случаев не употреблялись вспомогательные горючие вещества) и образование оксида бора в виде мелкодисперсного сублимата (а не в виде труднорастворимой в воде стеклообразной его формы, как при сожжении свободного бора), что создает возможность достижения полноты его гидратации до борной кислоты в главном периоде калориметрического опыта. [c.15]
Метафосфаты натрия, имеющие общую формулу (NaPOg) , получаются при термическом обезвоживании мононатрийфосфата Nah3P04. Соль, известная под названием гексаметафосфат натрия (соль Грэма) представляет собой высокополимерное растворимое в воде стеклообразное вещество (фосфатное стекло). Промышленное название гексаметафосфат совершенно не соответствует структуре этого соединения и является ошибочным. [c.120]
Метафосфаты натрия, имеющие общую формулу (НаРОз),,, получаются при термическом обезвоживании мононатр и йфосфата ЫаН2Р04- Соль, известная под названием гексаметафосфат натрия, представляет собой высокополимерное растворимое в воде стеклообразное вещество (фосфатное стекло). [c.98]
Большое влияние на качество кислотоупорных цементов оказывает жидкое стекло — основная часть кислотоупорных силикатныл вяжущих составов. Жидкое стекло, которое называют также растворимым стеклом, получают растворением в воде стеклообразной массы— силикат-глыбы. Последняя представляет собой сплав кварцевого песка и соды, взятых в определенных соотношениях. В некоторых случаях вместо соды используют сульфат натрия. По внешнему виду силикат-глыба представляет собой прозрачные куски синеватозеленоватого или желтого цветов. [c.46]
Жидкое стекло получают шугем растворения в воде стеклообразной массы — силикат-глыбы (содовая, содово-сульфатная или суль- [c.48]
Сульфид бора B2S3 — стеклообразное вещество, водой полностью разлагается. [c.440]Извлечение плава из тигля. Раскаленный тигель с расплавленной массой нельзя опускать в холодную воду, как это иногда рекомендуется, или применять другие способы быстрого охлаждения плава, не учитывающие необходимости равномерного распределения плава по стенкам тигля (см. ниже). Коэффициент расширения платины значительно больше, чем коэффициент расширения стеклообразной сплавленной массы. При быстром охлаждении в нижней части тигля образуется плотный королек стекловидной массы, которая не дает возможности платине сокращаться в данном месте. Между тем, выше уровня сплава платина сжимается, и в результате, после нескольких операций, тигель нормальной формы де( )ор-мируется, а нередко дает и трещину. Поэтому очень важно перед охлаждением распределить расплавленную массу по возможности равномерно по стенкам тигля. Кроме того, необходимо при извлечении плава из тигля водой лишь очень слабо нажимать палочкой на приставшие к тиглю частицы сплава следует добиваться растворения путем нагревания, обрг.бот-кой кислотой и т. д. [c.463]
Получение триметафосфата. Прв получении метафосфатов исходят из дигидрофосфатов. NaHaPO, нагревают несколько часов в сушильном шкафу при 60 "С для удаления кристаллизационной воды. В неглазурованном тигле медленно нагревают обезвоженную соль до температуры красного каления., причем в результате должен образоваться прозрачный расплав соли Грэма. По охлаждении тигель разбивают, а его содержимое переносят в другой фарфоровый тигель. Стеклообразный пек отжигают в течение 24 ч при 480 °С в электрической печи и получают кристаллический трициклофосфат, [c.552]
На захоронение радиоактивных отходов было затрачено много исследовательских усилий, и работа в этом направлении продолжается до сих пор. В настоящее время наиболее перспективной возможностью связывания радиоактивных отходов считается превращение их в стеклообразную, керамическую или каменную массу. Такие твердые материалы можно затем захоронить глубоко под землей. Поскольку они еще долгое время будут радиоактивны, необходимо иметь уверенность в том, что захороненные материалы не будут растрескива ься в результате выделения тепла при ядерном распаде, так как тогда радиоактивные вещества могли бы проникнуть в грунтовые воды. К сожалению, в настоящее время не существует полньк ответов на все трудные и важные вопросы, связанные с захоронением радиоактивных отходов. [c.272]
Мышьяковая кислота h4ASO4 при обычных условиях находится в твердом состоянии она хорошо растворима в воде. По силе мышьяковая кислота почти равна фосфорной. Соли ее — арсенаты — очень похожи на соответствующие фосфаты. Известны также мета- и димышьяковая кислоты. При прокаливании мышьяковой кислоты получается оксид мышьяка Y), или мышьяковый ангидриду AS2O5 в виде белой стеклообразной массы. [c.447]
КАНИФОЛЬ — твердая, хрупкая, стеклообразная прозрачная смола свет-ло-желтого (иногда темно-красного) цвета, составная часть смолообразных веществ хвойных растений, остающаяся после отгонки из них скипидара. К. нерастворима в воде, растворяется в органических растворителях, состоит из смоляных кислот и группы не омыляющихся веществ. К- применяют для проклеива-ния бумаги, для изготовления мыла, лаков, сургуча, линолеума, мазей, замазок, пластырей, масел, пластмасс, фунгицидов, изоляционных материалов, при пайке и лужении металлов и др. Широко применяются соли смоляных кислот, изготовляемых из К. (абиетиновая, лево-пимаровая и др.) канифольное мыло (натриевая или калиевая соль) применяют в мыловаренной промышленности, для изготовления клеев, в производстве каучуков, для проклеивания бумаги и др. [c.118]
Изучение состава и строения поверхностных пленок на разных стадиях их формирования проводят на основе анализа экспериментальных спектров МНПВО и табличных значений абсорбционных максимумов, характерных для различных модификаций оксидов германия (моноокиси и двуокиси, аморфной, стеклообразной, гексагональной пли тетрагональной), германа-тов, гидридных (GeH), гидроксильных (GeOH) и других функциональных групп, а также молекул физически адсорбированной воды. Кроме того, на всех этапах исследования структурных особенностей поверхностных пленок желательно проводить эллипсометрнческий контроль за толщиной и показателем преломления пленки (см. главу 9). [c.145]
Разбирается значение радиоактивности для геохимии и геохронологии, возможность использования ее закономерностей для определения абсолютного возраста минералов и горных пород. Рассматриваются вопросы о полиморфизме и изоморфизме, о силикатах, показана сущность стеклообразного состояния, значение вязкости при кристаллизации магмы. Подчеркнута роль воды для геохимических и гидрогеологических процессов, ее значение в образовании и разру шении минералов, дано представление о природ ных растворах. Рассматривается минералогиче ское правило фаз, а также ряд других вопросов Табл. 19, иллюстраций 116, библиографий 86 [c.2]
Если окончательный химический состав окисных пленок при упомянутых выше условиях не зависит от применявшегося травителя, то их структура и толщина могут быть весьма различными. Это различие, однако, является не столько качественным, сколько количественным. Так, даже компактные окисные пленки, образующиеся при травлении в смеси НР + HNOз, обладают мелкопористой структурой и не могут надежно изолировать поверхность кристалла от воздействия окружающей атмосферы. В связи с этим заметим, что окисные слои, используемые специально для защиты поверхности, вообще не должны содержать химически связанной воды, а их толщина должна составлять несколько тысяч ангстрем ( 1 Л1к). Такие слои могут быть получены путем высокотемпературного окисления (Т 1300° К) в атмосфере сухого кислорода. По своей структуре и химическим свойствам они соответствуют стеклообразным соединениям типа кварца. [c.117]
Силикат натрия (растворимое стекло) Ма25Юз — стеклообразные куски зеленоватого цвета (от присутствия солей железа), трудно растворимые в воде. Водные растворы растворимого стекла вязки и имеют щелочную реакцию вследствие гидролиза. [c.491]
При нагревании буры Na2B407-10h30 в пламени газовой горелки она теряет воду и превращается в боратный плав. Этот плав, взаимодействуя при высокой температуре с соединениями металлов, содержащимися в анализируемом образце, дает бесцветные или окрашенные стеклообразные метаборатные перлы, включающие, например, Си(В02)2, Сг(В02)з, Ni(B02)2 и т. д. Соединения металлов могут образовывать также растворы в стеклообразной боратной массе. [c.505]
Известно несколько стеклообразных модификаций В2О3. На воздухе он поглощает влагу, взаимодействуя с водой, образует борную [c.309]
Водный раствор силиката натрия называется жидкое стекло. После испарения воды он превращается в стеклообразную массу, состоящую из NajSiOa. Жидкое стекло используется, например, для закупорки трещин. [c.383]
Силикаты щелочных металлов, полученные в результате сплавления кремнезема со щелочами, представляют собой стеклообразную массу и вследствие растворимости в воде называются растворимым стеклом. В промышленности силикат натрия Na2SiOз получают сплавлением песка с содой [c.365]
На Палемонском керамическом заводе (Литовская ССР) эти шламы с 1983 г применяют при производстве глиняной черепицы. Для этого специально оборудован участок приема отходов. Гальванические отходы загружают в контейнеры вместимостью 2 т и централизованно доставляют на завод. Выгрузка контейнеров механизирована. После выгрузки отходов контейнеры и помещение промывают водой, которая стекает в резервуары с отходами. Количество шлама в глиняной смеси 5 % (об.). Подготовка сырьевой смеси шликерная. Формовка изделий пластическая, с предварительной сушкой шликерной шихты во вращающейся сушилке при 600—700 °С. За год принимается 1200 т гальванических отходов. Исследование образцов черепицы, полученных в промышленных условиях, показало, что при повышении температуры начинаются реакции между твердыми веществами и образуются кристаллические силикаты и стекло [45]. При 950 °С часть Na, Са, Zn, d, Ni, Си находятся в форме силикатов, а другая часть растворяется в стеклообразных сплавах. Силикат Сг (III) не образовывается. После прокаливания при 950 °С оксид Сг становится устойчивым, поэтому особое внимание было уделено созданию условий, при которых Сг (III) не переходит в Сг (VI). Оказалось, что ионы Fe , которыми обогащается осадок при очистке сточных вод, предотвращают переход хрома в шестивалентную форму. Кроме того, на определенной стадии создается восстановительная атмосфера в печи. [c.211]
chem21.info
Места с самой чистой водой на Земле
Когда соберётесь в путешествие к местам с самой чистой водой в мире, захватите с собой камеру получше: отличные подводные снимки и фотографии лучших пляжей гарантированы.
1. Долина реки Верзаски, Швейцария
 d.aniela/Flickr.com
d.aniela/Flickr.comЧистые воды 30-километровой реки Верзаски текут в каменистой долине на юге Швейцарии. Плотина с таким же названием, снятая в фильме о Джеймсе Бонде «Золотой глаз», перекрывает речной поток и образует искусственное озеро Лаго-ди-Вогорно (Lago di Vogorno). А ниже по течению река впадает в озеро Маджоре.
2. Сабах, Малайзия
 MEMANG RIZALIS ENT./Flickr.com
MEMANG RIZALIS ENT./Flickr.comУдалённый штат Малайзии, расположенный в северной части острова Борнео, окружён коралловыми рифами. Любимое место встречи дайверов — курорт Семпорна.
3. Пупу Спрингс, Новая Зеландия
 Sarah/Flickr.com
Sarah/Flickr.comНа краю Южного острова, на берегу бухты Голден-Бей, источники ежесекундно выбрасывают 1 400 литров кристально чистой воды.
4. Остров Панари, Окинава, Япония
 rurinoshima/Flickr.com
rurinoshima/Flickr.comПанари, один из островов в группе Яэяма, находится в самом отдалённом районе Японии. Эти острова — одно из лучших направлений для дайвинга. Местные коралловые рифы не уступают в количестве флоры и фауны Большому Барьерному рифу: вокруг Окинавы водится больше 400 видов кораллов, пять видов морских черепах, скаты, китовые акулы и множество тропических рыб.
5. Долина Цзючжайгоу, Сычуань, Китай
 Wilson Loo Kok Wee/Flickr.com
Wilson Loo Kok Wee/Flickr.comНа севере провинции Сычуань в Китае расположен Национальный парк «Цзючжайгоу», заповедник, объявленный ЮНЕСКО всемирным наследием. В этом районе есть и кристальные озёра, и многоступенчатые водопады, и снежные горы. Туризм пришёл в эти края недавно, но активно развивается. Купание в долине запрещено, но любители поплавать без одежды часто нарушают запрет по ночам.
6. Озеро Кёнигсзее, Германия
 Reham Alhelsi/Flickr.com
Reham Alhelsi/Flickr.comЕсли хотите сделать фотографию в лодке, словно парящей воздухе, отправляйтесь в Германию. Подходящий фон найдётся на озере Кёнигсзее в южной Баварии, на границе с Австрией.
7. Пляж Бак Бак, Борнео, Малайзия
 Imran Kadir/Flickr.com
Imran Kadir/Flickr.comПляж Бак Бак находится на севере штата Сабах в Малайзии, неподалёку от Кудата. До пляжа с абсолютно прозрачной водой можно добраться за три с половиной часа от города Кота-Маруду.
8. Озеро Марджори, Калифорния, США
 Steve Dunleavy/Flickr.com
Steve Dunleavy/Flickr.comУ горных озёр может быть множество цветов. Аквамариновое озеро Марджори похоже на бассейн — настолько синяя и чистая в нём вода. Вокруг озера тоже есть на что посмотреть: в небо упираются горы, с которых открывается потрясающий вид.
9. Мальдивы
 Mohamed Iujaz Zuhair/Flickr.com
Mohamed Iujaz Zuhair/Flickr.comМальдивы образованы из 26 атоллов, расположенных на 400 километров южнее полуострова Индостан. Богатая фауна рифов (там даже китовые акулы водятся) и невероятно чистая вода привлекают туристов. Кроме того, на Мальдивах можно встретить редкие виды исчезающих животных.
10. Рио-Сукури, Бразилия
 Roberto Hungria/Flickr.com
Roberto Hungria/Flickr.comРасположенная в районе Национального парка «Пантанал» в Бразилии Рио-Сукури — одна из самых чистых родниковых рек на нашей планете. Местные турфирмы предлагают проехать на автомобиле до реки, чтобы поплавать с трубкой.
11. Озеро Тахо, Невада, США
 Don Graham/Flickr.com
Don Graham/Flickr.comНа границе Калифорнии и Невады расположилось ледниковое озеро Тахо. Прозрачная вода и растущие на скалах бонсай — что ещё нужно для прекрасных фотографий?
12. Провинция Палаван, Филиппины
 Andy Enero/Flickr.com
Andy Enero/Flickr.comВ удалённой части Филиппин, в провинции Палаван, часто встречаются пляжи с невероятно прозрачной водой.
13. Бухта Д’Эн-Во, Франция
 Koen/Filckr.com
Koen/Filckr.comНебольшая бухта на южном побережье Франции, связанная с морем только узким каналом. Атмосфера уединения подчёркивает красоту и чистоту воды в заливе.
14. Озеро Дженни, штат Вайоминг, США
 JayVeeAre/Flickr.com
JayVeeAre/Flickr.comОзеро Дженни расположено у подножия хребта Гранд-Титон. Это цель пеших походов, горных маршрутов и приключенческих туров. Несмотря на то что по озеру разрешено передвигаться на моторных лодках, вода в нём всё ещё считается безупречной.
15. Остров Бора-Бора, Французская Полинезия
 Alquiler de Coches/Flickr.com
Alquiler de Coches/Flickr.comДорога скатов — самое популярное место среди дайверов на Бора-Бора. В воде можно увидеть даже гигантских морских дьяволов.
16. Архипелаг Сан-Блас, Панама
 BORIS G/Flickr.com
BORIS G/Flickr.comВ Панаме на архипелаге, окружённом чистейшей водой, живёт независимое племя индейцев куна. Острова ещё не испорчены цивилизацией, хотя туристы всё чаще приезжают сюда ради дайвинга и рыбалки.
17. Озеро Крейтер, штат Орегон, США
 Mark Stevens/Flickr.com
Mark Stevens/Flickr.comОзеро Крейтер — одно из самых глубоких и чистых в мире, вода такая прозрачная, что видимость не пропадает на глубине 43 метров. В озере можно купаться, но чтобы попасть на пляж, нужно пройти полтора километра по крутой тропе. Иначе придётся прыгать, но это не самое приятное занятие: вода в озере холодная.
18. Кайо-Коко, Куба
 innoxiuss/Flickr.com
innoxiuss/Flickr.comКурортный остров на северном побережье Кубы, связанный с основной частью страны 27-километровой искусственной дорогой. Расположенный в чистых водах коралловый риф превратил Кайо-Коко в признанный во всём мире курорт для дайвинга.
19. Примоштен, Хорватия
 Tobwie/Flickr.com
Tobwie/Flickr.comГород Примоштен на берегу Адриатического моря известен двумя достопримечательностями: виноградниками и пляжами.
20. Кала Макареллета, Менорка, Испания
 Cristina E/flickr.com
Cristina E/flickr.comДо пляжа Кала Макареллета в южной части Менорки можно добраться только пешком или на лодке. Это самый пустынный и чистый пляж в Испании.
21. Голубое озеро, Новая Зеландия
 Chris Gin/Flickr.com
Chris Gin/Flickr.comГолубое озеро претендует на звание самого чистого на планете. Оно расположено в Национальном парке «Нельсон Лейк» в Новой Зеландии, в горах на Южном острове.
lifehacker.ru