Поверхностное натяжение: общие сведения и биологическое значение. Натяжение воды
Поверхностное натяжение жидкостей, воды и водных растворов (Таблица)
Поверхностное натяжение обуславливается направлением внутрь притяжением молекул жидкости, находящихся в поверхностном слое. Это притяжение вызывает искривление свободной поверхности жидкости и создает некоторую разность давлений:
∆p = δ (1/R1 + 1/R2) $
Здесь ∆p обозначает разность давлений, а R1 и R2 – главные радиусы кривизны поверхности жидкости. Величина δ обозначает коэффициент поверхностного натяжения на границе жидкость – газ, δ обычно измеряется в дин/см (эквивалентно свободной поверхности энергии в эрг/см2). При соприкосновении двух (взаимно не растворяющихся) жидкостей говорят о поверхностном натяжении на границе двух жидкостей; при соприкосновении жидкости и твердого тела говорят о явлениях смачивания и не смачивания (капиллярных явлениях).
Зависимость от температуры. Натяжение уменьшается при возрастании температуры жидкости и при ее критической температуре становится равным нулю. Для многих жидкостей применима формула:
-d/dt [δ (M/p)2/3 = 2,12
( M – молекулярный вес, р – плотность, t – температура).
Таблица поверхностное натяжение воды на границе с воздухом
| T, °C | 0 | 10 | 15 | 20 | 25 | 30 | 40 | 50 | 60 | 70 | 80 | 100 |
| Поверхностное натяжение δ | 75,7 | 74,2 | 73,5 | 72,75 | 72,0 | 71,2 | 69,6 | 67,9 | 66,2 | 64,4 | 62,6 | 58,8 |
Таблица поверхностное натяжение различных жидкостей
(в – на границе с воздухом, п – на границе с парами этой же жидкости)
| Жидкость | На границе | Температура, 0С | δ | Жидкость | На границе | Температура 0С | δ |
| Неорганические вещества | |||||||
| Алюминий | в | 700 | 840 | Натрий йодистый | N2 | 861 | 776 |
| Азот | п | -183 | 6,2 | Натрий сернокислый | N2 | 900 | 195 |
| Золото | в | 1130 | 1102 | Натрий фтористый | N2 | 1010 | 200 |
| Кадмий | N2 | 320 | 630 | Натрий хлористый | N2 | 908 | 106 |
| Калий | CO2 | 64 | 410 | Ртуть | п | 20 | 472 |
| Калий хлористый | N2 | 909 | 88 | Ртуть | п | 100 | 456 |
| Кислород | в | -183 | 13,1 | Свинец | CO2 | 350 | 453 |
| Натрий | CO2 | 90 | 290 | Свинец хлористый | в | 490 | 138 |
| Органические вещества | |||||||
| Анилин | п | 20 | 42,9 | Спирт н-пропиловый | п | 20 | 23,8 |
| Ацетон | п | 20 | 23,7 | Спирт этиловый | в | 0 | 24,1 |
| Ацетон | п | 50 | 20,0 | Спирт этиловый | п | 10 | 23,6 |
| Бензол | в | 10 | 30,22 | Спирт этиловый | п | 20 | 22,8 |
| Бензол | в | 20 | 28,88 | Спирт этиловый | п | 30 | 21,9 |
| Бромоформ | п | 20 | 41,5 | Толуол | п | 20 | 28,4 |
| Н-Гексан | в | 20 | 18,4 | Углерод 4-хлористый | п | 20 | 27,0 |
| Глицерин | в | 20 | 63,4 | Углерод 4-хлористый | п | 100 | 17,3 |
| Н-Кислота масляная | в | 20 | 26,8 | Фенол | в | 20 | 40,9 |
| Кислота олеиновая | в | 20 | 32,5 | Хлороформ | в | 20 | 27,14 |
| Кислота уксусная | п | 20 | 27,8 | Этил бромистый | п | 20 | 24,2 |
| Н-Октан | в | 20 | 21,8 | Этилацетат | п | 20 | 23,6 |
| Сероуглерод | п | 20 | 32,3 | Эфир этиловый | п | 20 | 16,96 |
| Н-Спирт бутиловый | в | 20 | 24,6 | Эфир этиловый | п | 50 | 13,4 |
| Спирт метиловый | в | 0 | 24,5 |
|
|
|
|
| Спирт метиловый | в | 20 | 22,6 |
|
|
|
|
| Спирт метиловый | п | 50 | 20,2 |
|
|
|
|
Таблица поверхностное натяжение водных растворов солей
| Соль | δ при 200С | Соль | δ при 200С |
| KCI | 1,4 | NaNO3 | 1,2 |
| NaCI | 1,64 | Na2SO4 | 2,7 |
| Na2CO3 | 2,7 |
|
|
Таблица поверхностное натяжение на границе двух жидкостей при 200С
| Жидкости | Поверхностное натяжение δ, дин/см | Жидкости | Поверхностное натяжение δ, дин/см |
| ВОДА И | Хлороформ | 28 | |
| Бензол | 35 | Эфир этиловый | 10 |
| Н-Гептан | 51 | РТУТЬ И | |
| Кислота гептоловая | 7 | Ацетон | 390 |
| Масло парафиновое | 48 | Бензол | 357 |
| Масло прованское | 20 | Н-Гептан | 379 |
| Н-Октан | 51 | Кислота олеиновая | 322 |
| Углерод | 45 | Хлороформ | 357 |
infotables.ru
Поверхностное натяжение. Видеоурок. Физика 10 Класс
Для начала, обсудим особые свойства, которыми обладают молекулы приповерхностного слоя жидкости по сравнению с молекулами, находящимися в объеме.
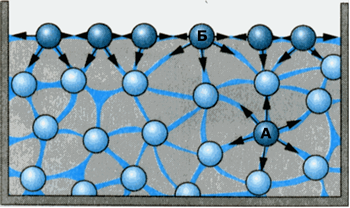
Рис. 1. Отличие молекул приповерхностного слоя от молекул, находящихся в объеме жидкости
Рассмотрим две молекулы А и Б. Молекула А находится внутри жидкости, молекула Б – на ее поверхности (Рис. 1). Молекула А окружена другими молекулами жидкости равномерно, поэтому силы, действующие на молекулу А со стороны молекул, попадающих в сферу межмолекулярного взаимодействия, скомпенсированы, или их равнодействующая равна нулю.
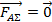
Что же происходит с молекулой Б, которая находится у поверхности жидкости? Напомним, что концентрация молекул газа, который находится над жидкостью, значительно меньше, чем концентрация молекул жидкости. Молекула Б с одной стороны окружена молекулами жидкости, а с другой стороны – сильно разреженными молекулами газа. Поскольку со стороны жидкости на нее действует гораздо больше молекул, то равнодействующая всех межмолекулярных сил будет направлена внутрь жидкости.
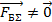
Таким образом, для того чтобы молекула из глубины жидкости попала в поверхностный слой, нужно совершить работу против не скомпенсированных межмолекулярных сил.
Вспомним, что работа – это изменение потенциальной энергии, взятое со знаком минус.
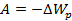
Значит, молекулы приповерхностного слоя, по сравнению с молекулами внутри жидкости, обладают избыточной потенциальной энергией.
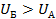
Эта избыточная энергия является составляющей внутренней энергии жидкости и называется поверхностной энергией. Обозначается она, как 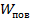 , и измеряется, как и любая другая энергия, в джоулях.
, и измеряется, как и любая другая энергия, в джоулях.
Очевидно, что чем больше площадь поверхности жидкости, тем больше таких молекул, которые обладают избыточной потенциальной энергией, а значит тем больше поверхностная энергия. Этот факт можно записать в виде следующего соотношения:
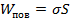 ,
,
где 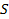 – площадь поверхности, а
– площадь поверхности, а 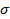 – коэффициент пропорциональности, который мы назовем коэффициентом поверхностного натяжения, этот коэффициент характеризует ту, или иную жидкость. Запишем строгое определение этой величины.
– коэффициент пропорциональности, который мы назовем коэффициентом поверхностного натяжения, этот коэффициент характеризует ту, или иную жидкость. Запишем строгое определение этой величины.
Поверхностное натяжение жидкости (коэффициент поверхностного натяжения жидкости) – это физическая величина, которая характеризует данную жидкость и равна отношению поверхностной энергии к площади поверхности жидкости
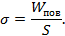
Измеряется коэффициент поверхностного натяжения в ньютонах, деленных на метр.
Обсудим, от чего зависит коэффициент поверхностного натяжения жидкости. Для начала, вспомним, что коэффициент поверхностного натяжения характеризует удельную энергию взаимодействия молекул, а значит факторы, изменяющие эту энергию, изменят и коэффициент поверхностного натяжения жидкости.
Итак, коэффициент поверхностного натяжения 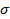 зависит от:
зависит от:
1. Природы жидкости (у «летучих» жидкостей, таких как эфир, спирт и бензин, поверхностное натяжение меньше, чем у «нелетучих» – воды, ртути и жидких металлов).
2. Температуры (чем выше температура, тем меньше поверхностное натяжение).
3. Наличие поверхностно активных веществ, уменьшающих поверхностное натяжение (ПАВ), например мыла или стирального порошка.
4. Свойства газа, граничащего с жидкостью.
Отметим, что коэффициент поверхностного натяжения не зависит от площади поверхности, так как для одной отдельно взятой приповерхностной молекулы абсолютно неважно, сколько таких же молекул вокруг. Обратите внимание на таблицу, в которой приведены коэффициенты поверхностного натяжения различных веществ, при температуре 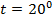 :
:
Таблица 1. Коэффициенты поверхностного натяжения жидкостей на границе с воздухом, при 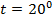
Итак, молекулы приповерхностного слоя обладают избыточной потенциальной энергией по сравнению с молекулами в объеме жидкости. В курсе механики было показано, что любая система стремится к минимуму потенциальной энергии. Например, тело, брошенное с некоторой высоты, будет стремиться упасть вниз. Кроме того, вы чувствуете себя намного комфортнее лёжа, поскольку в этом случае максимально низко расположен центр масс вашего тела. К чему приводит стремление уменьшить свою потенциальную энергию в случае жидкости? Поскольку поверхностная энергия зависит от площади поверхности, значит, любой жидкости энергетически невыгодно иметь большую площадь поверхности. Иными словами, в свободном состоянии жидкость будет стремиться сделать свою поверхность минимальной.
В этом легко убедиться, экспериментируя с мыльной пленкой. Если окунуть в мыльный раствор некий проволочный каркас, то на нем образуется мыльная пленка, при чем пленка приобретет такую форму, чтобы площадь ее поверхности была минимальной (Рис. 2).


Рис. 2. Фигуры из мыльного раствора
Убедиться в существовании сил поверхностного натяжения можно при помощи простого эксперимента. Если к проволочному кольцу в двух местах привязана нить, причем так, чтобы длина нити была несколько больше длины хорды, соединяющей точки крепления нити, и обмакнуть проволочное кольцо в мыльный раствор (Рис. 3а), мыльная пленка затянет всю поверхность кольца и нить будет лежать на мыльной пленке. Если теперь порвать пленку с одной стороны нити, мыльная пленка, оставшаяся с другой стороны нити, сократится и натянет нить (Рис. 3б).

Рис. 3. Эксперимент по обнаружению сил поверхностного натяжения
Почему же так произошло? Дело в том, что оставшийся сверху мыльный раствор, то есть жидкость, стремится сократить площадь своей поверхности. Таким образом, нить вытягивается вверх.
Итак, в существовании силы поверхностного натяжения мы убедились. Теперь научимся ее рассчитывать. Для этого проведем мысленный эксперимент. Опустим в мыльный раствор проволочную рамку, одна из сторон которой подвижна (Рис. 4). Будем растягивать мыльную пленку, действуя на подвижную сторону рамки силой 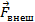 . Таким образом, на перекладину действуют три силы – внешняя сила
. Таким образом, на перекладину действуют три силы – внешняя сила 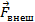 и две силы поверхностного натяжения
и две силы поверхностного натяжения 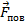 , действующие вдоль каждой поверхности пленки. Воспользовавшись вторым законом Ньютона, можем записать, что
, действующие вдоль каждой поверхности пленки. Воспользовавшись вторым законом Ньютона, можем записать, что
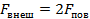
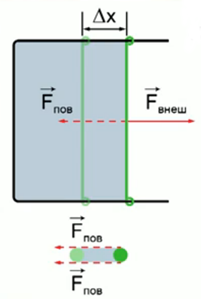
Рис. 4. Вычисление силы поверхностного натяжения
Если под действием внешней силы перекладина переместится на расстояние 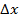 , то эта внешняя сила совершит работу
, то эта внешняя сила совершит работу
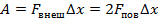 . (*).
. (*).
Естественно, что за счет совершения этой работы площадь поверхности пленки увеличится, а значит, увеличится и поверхностная энергия, которую мы можем определить через коэффициент поверхностного натяжения:
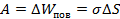 .
.
Изменение площади, в свою очередь можно определить следующим образом:
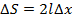 ,
,
где 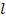 – длина подвижной части проволочной рамки. Учитывая это, можно записать, что работа внешней силы равна
– длина подвижной части проволочной рамки. Учитывая это, можно записать, что работа внешней силы равна
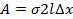 . (**).
. (**).
Приравнивая правые части в (*) и (**), получим выражение для силы поверхностного натяжения:
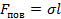 .
.
Таким образом, коэффициент поверхностного натяжения численно равен силе поверхностного натяжения, которая действует на единицу длины линии, ограничивающей поверхность
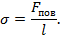
Итак, мы еще раз убедились в том, что жидкость стремится принять такую форму, чтобы площадь ее поверхности была минимальной. Можно показать, что при заданном объеме площадь поверхности будет минимальной у шара. Таким образом, если на жидкость не действуют другие силы или их действие мало, жидкость будет стремиться принимать сферическую форму. Так, например, будет вести себя вода в невесомости (Рис. 5) или мыльные пузыри (Рис. 6).

Рис. 5. Вода в невесомости

Рис. 6. Мыльные пузыри
Наличием сил поверхностного натяжения также можно объяснить то, почему металлическая иголка «лежит» на поверхности воды (Рис. 7). Иголка, которую аккуратно положили на поверхность, деформирует ее, увеличивая тем самым площадь этой поверхности. Таким образом, возникает сила поверхностного натяжения, которая стремится уменьшить подобное изменение площади. Равнодействующая сил поверхностного натяжения будет направлена вверх, и она скомпенсирует силу тяжести.
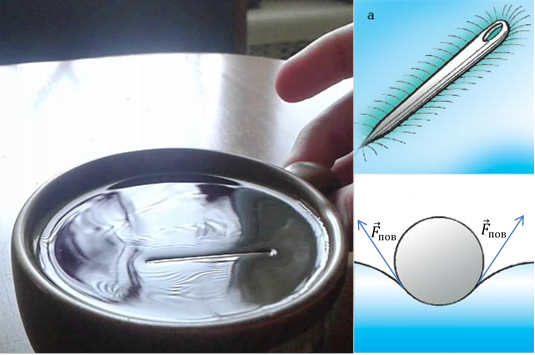
Рис. 7. Иголка на поверхности воды
Таким же образом можно объяснить принцип действия пипетки. Капелька, на которую действует сила тяжести, вытягивается вниз, тем самым увеличивая площадь своей поверхности. Естественно, возникают силы поверхностного натяжения, равнодействующая которых противоположна направлению силы тяжести, и которые не дают капельке растягиваться (Рис. 8). Когда вы нажимаете на резиновый колпачок пипетки, вы тем самым создаете дополнительное давление, которое помогает силе тяжести, и в результате, капля падает вниз.
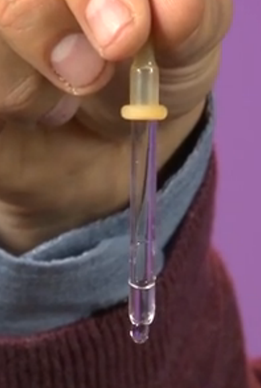
Рис. 8. Принцип работы пипетки
Приведем еще один пример из повседневной жизни. Если опустить кисточку для рисования в стакан с водой, то ее волоски распушатся. Если теперь вынуть эту кисточку из воды, то вы заметите, что все волоски прилипли друг к другу. Это связано с тем, что площадь поверхности воды, налипшей на кисточку, в таком случае будет минимальной.
И еще один пример. Если вы захотите построить замок из сухого песка, это у вас вряд ли получится, поскольку песок будет рассыпаться под действием силы тяжести. Однако если вы намочите песок, то он будет сохранять свою форму благодаря силам поверхностного натяжения воды между песчинками.
Наконец, отметим, что теория поверхностного натяжения помогает найти красивые и простые аналогии при решении более сложных физических задач. Например, когда нужно построить лёгкую и в то же время прочную конструкцию, на помощь приходит физика того, что происходит в мыльных пузырях. А построить первую адекватную модель атомного ядра удалось, уподобив это атомное ядро капле заряженной жидкости.
Список литературы
- Г. Я. Мякишев, Б. Б. Буховцев, Н. Н. Сотский. «Физика 10». – М.: Просвещение, 2008.
- Я. Е. Гегузин «Пузыри», Библиотека Квант. – М.: Наука, 1985.
- Б. М. Яворский, А. А. Пинский «Основы физики» т. 1.
- Г. С. Ландсберг «Элементарный учебник физики» т. 1.
Дополнительные рекомендованные ссылки на ресурсы сети Интернет
- Nkj.ru (Источник).
- Youtube.com (Источник).
- Youtube.com (Источник).
- Youtube.com (Источник).
Домашнее задание
- Решив задачи к данному уроку, вы сможете подготовиться к вопросам 7,8,9 ГИА и вопросам А8, А9, A10 ЕГЭ.
- Гельфгат И.М., Ненашев И.Ю. «Физика. Сборник задач 10 класс» 5.34, 5.43, 5.44, 5.47 (Источник)
- Опираясь на задачу 5.47, определите коэффициент поверхностного натяжения воды и мыльного раствора.
Список вопросов-ответов
Вопрос: Почему поверхностное натяжение меняется с изменением температуры?
Ответ: При увеличении температуры, молекулы жидкости начинают двигаться быстрее, и следовательно, молекулы легче преодолевают потенциальные силы притяжения. Что и приводит к уменьшению сил поверхностного натяжения, являющихся потенциальными силами, которыми связываются молекулы приповерхностного слоя жидкости.
Вопрос: Зависит ли коэффициент поверхностного натяжения от плотности жидкости?
Ответ: Да, зависит, поскольку от плотности жидкости зависит энергия молекул приповерхностного слоя жидкости.
Вопрос: Какие существуют способы определения коэффициента поверхностного натяжения жидкости?
Ответ: В школьном курсе изучаютдва способа определениякоэффициента поверхностного натяжения жидкости. Первый – это метод отрыва проволочки, его принцип описан в задаче 5.44 из домашнего задания, второй – метод счета капель, описанный в задаче 5.47.
Вопрос: Почему через некоторое время мыльные пузыри разрушаются?
Ответ: Дело в том, что через некоторое время, под действием силы тяжести пузырь становится толще внизу, чем вверху, и затем под влиянием испарения разрушается в какой-либо точке. Это приводит к тому, что весь пузырь, подобно воздушному шарику, схлопывается под действием не скомпенсированных сил поверхностного натяжения.
interneturok.ru
Вода-основа жизни - Натяжение воды
Поверхностное натяжение воды
Вы видите его проявление всякий раз, когда наблюдаете, как вода медленно капает из водопроводного крана. Из крана появляется водяная пленка и начинает растягиваться, словно тонкая резиновая оболочка, под тяжестью заключенной в ней жидкости. Эта пленка, прикрепленная к отверстию крана, постепенно удлиняется, пока ее вес не станет вдруг слишком большим. Пленка, однако, не рвется, как порвалась бы резника при перегрузке. Вместо этого она "соскальзывает" с копчика крана и, как бы охватив небольшое количество воды, образует свободно падающую капельку. Несомненно, вы не раз наблюдали, что падающие капельки принимают почти шарообразную форму. Если бы не было внешних сил, они были бы строго шарообразны. То, что вы наблюдаете, является одним из проявлений необычной способности воды "стягиваться", "самоуплотняться", или, другими словами, ее способность к сцеплению (когезии). Капля воды, капающая из крана, стягивается в крошечный шар, а шар из всех возможных геометрических тел обладает наименьшей поверхностью при данном объеме.
Поверхностное натяжение воды
Вследствие сцепления на поверхности воды образуется натяжение, и для того, чтобы разорвать поверхность воды, требуется физическая сила, причем, как это ни странно, довольно значительная. Ненарушенная водная поверхность может удерживать на себе предметы, которые значительно "тяжелее" воды, например стальную иголку или лезвие бритвы, или некоторых насекомых, которые скользят по воде, словно это не жидкость, а твердое тело.

Из всех жидкостей, кроме ртути, у воды самое большое поверхностное натяжение.
Внутри жидкости притяжение молекул друг к другу уравновешено. А на поверхности нет. Молекулы воды, которые лежат глубже, тянут вниз самые верхние молекулы. Поэтому капля воды как бы стремится максимально сжаться. Стягивают ее силы поверхностного натяжения.
Физики точно рассчитали, какую гирю надо подвесить к столбику воды толщиной в три сантиметра, чтобы разорвать его. Гиря потребуется огромная - больше ста тонн! Но это когда вода исключительно чистая. В природе такой воды нет. Всегда в ней что-то растворено. Пусть хоть немного, но чужеродные вещества разрывают звенья в прочной цепи молекул воды, и силы сцепления между ними уменьшаются.
Если нанести на стеклянную пластинку капли ртути, а на парафиновую - капли воды, то очень маленькие капельки будут иметь форму шара, а более крупные окажутся слегка сплюснутыми под действием силы тяжести.

Подобное явление объясняется тем, что между ртутью и стеклом, а также между парафином и водой возникают силы притяжения (адгезия) меньшие чем между самими молекулами (когезия). При соприкосновении воды с чистым стеклом, а ртути с металлической пластинкой мы наблюдаем почти равномерное распределение того и другого вещества на пластинках, так как силы притяжения между стеклом и молекулами воды, металлом и молекулами ртути больше, чем притяжение между отдельными молекулами воды и ртути. Такое явление, когда жидкость равномерно располагается на поверхности твёрдого тела, называется смачиванием. Значит, вода смачивает чистое стекле, но не смачивает парафин. Смачиваемость в частном случае может показать степень загрязнённости поверхности. Например, на чисто вымытой тарелке (фарфоровой, фаянсовой) вода растекается ровным слоем, в чисто вымытой колбе стенки равномерно покрываются водой, если же вода на поверхности принимает форму капель, то это указывает, что поверхность посуды покрыта тонким слоем вещества, которое не смачивает вода, чаще всего жиром.
Опыт с водой: иголка в воде не тонет Закон Архимеда дает ясный ответ: стальная иголка тяжелее равного объема воды почти в 8 раз — она обязательно должна утонуть, упасть на дно. Однако потрем сухую иглу между пальцами (т.е. покроем ее поверхность тонким слоем жира, который не смачивается водой) и осторожно положим ее на поверхность чистой воды в тарелке. Класть надо горизонтально. Для этого можно положить иголку сначала на кусочек промокашки, а затем на воду. Бумажка промокнет и потонет, а игла будет плавать. Ее удерживает поверхностное натяжение воды. Если подлить в воду концентрированный раствор смачивателя (мыла, шампуни), понижающего поверхностное натяжение воды, игла вскоре потонет, т. к. слой жира нейтрализуется. |
voda922.ucoz.ru
общие сведения и биологическое значение
Между молекулами жидкости существуют силы сцепления, разные для поверхностных и глубинных (внутренних) слоев. Молекулы, находящиеся на поверхностном слое, получают одностороннее притяжение со стороны глубинных слоев, а в глубинных слоях силы притяжения между молекулами взаимно уравновешиваются. Молекулы поверхностного слоя притягиваются молекулами воздуха и пара меньше, их равнодействующая сила направлена вниз, и поверхностный слой молекул как бы втягивается глубинными слоями. Поверхностное натяжение в свою очередь зависит от природы жидкости и граничных сред, окружающей температуры, наличия в жидкостях примесей и т. д.
Чтобы увеличить поверхность жидкости, следует проделать определенную работу, направленную против сил поверхностного натяжения. От значения коэффициента поверхностного натяжения зависит размер капель, мениск, величина пузырьков газа, проходящего через жидкость, смачиваемость и несмачиваемость жидкостью поверхности твердого тела и др.
Сила поверхностного натяжения также зависит от давления пара над жидкостью: чем больше пара, тем меньше величина внутреннего давления жидкости. Если жидкость граничит с воздухом, то молекулы ее поверхностного слоя почти не подвергаются силам притяжения со стороны газообразной фазы. В тех случаях, когда давление пара над жидкостью возрастает, ее поверхностное натяжение будет меньшим. Таким образом, молекулы поверхностного слоя не уравновешены, а поэтому система на поверхности раздела фаз всегда имеет определенный излишек свободной энергии. При всех других одинаковых условиях этот излишек тем больше, чем большая поверхность. Согласно второму закону термодинамики, система стремится уменьшить внутреннюю энергию. Поэтому процесс уменьшения поверхности раздела является процессом самостоятельным. Именно поэтому жидкость, на которую не действуют никакие силы, образует форму шара, поскольку такая форма при определенном объеме имеет наименьшую поверхность.
На величину поверхностного натяжения влияет и величина углеводородного радикала вещества. Так, если взять несколько карбоновых кислот одного и того же гомологического ряда (НСООН,СН3СООН, С2Н5СООН, С3Н7СООН), то поверхностное натяжение их уменьшается по мере удлинения карбоновой цепи – в 3,2 раза на каждую группу СН2.
Наличие примесей различных веществ в жидкостях влияет на величину поверхностного натяжения. Многие вещества, главным образом органические, понижают поверхностное натяжение. Такие соединения называются поверхностно-активными (белки, желчные кислоты, мыла, спирты, альдегиды, сложные эфиры, кетоны, танниды и др.). Вещества, наличие которых существенно не влияет на поверхностное натяжение, называются поверхностно-инактивными (фруктоза, глюкоза, крахмал и др.). Уменьшение поверхностного натяжения имеет большое значение в процессах всасывания жидких питательных веществ эпителием слизистой оболочки кишок. Так, жиры и другие липиды в пищевой канал поступают в виде капель. Эти капли эмульгируются желчью в тонкой кишке и после этого становятся доступными для гидролитического расщепления липазой и другими липолитическими ферментами. Добавление к жидкостям поверхностно-активных веществ увеличивает их способность смачивать обрабатываемую поверхность. При использовании инсектицидов часто добавляются мыла, что позволяет им хорошо контактировать с поверхностью тела насекомых и оказывать инсектицидное действие.
Поверхностное натяжение жидкости: методы его определения
Существует ряд методов определения поверхностного натяжения: сталагмометрический, по высоте поднятия жидкости в капилляре, наибольшего давления в пузырьках, по отрыву кольца.
Чаще всего используется сталагмометрический метод, основанный на использовании особого прибора — сталагмометра. Он представляет собой капиллярную трубку с верхней и нижней метками и расширением. В сталагмометр набирается вода до метки, после чего она выпускается и подсчитывается число капель. После чего тоже самое проделывается и с исследуемой жидкостью. При действии сил поверхностного натяжения вытекающая жидкость и вода принимают вид шаровидных капель.
Поверхностное натяжение в жизни организмов
Поверхностное натяжение является одним из факторов, определяющих форму клетки и ее частей. Клетка - элементарная частица живой материи, из которой состоит организм человека, животных и растений. Для клеток, у которых прочная и жесткая поверхность (растения, микроорганизмы), значение поверхностного натяжения невелико. Большинство клеток организма животного имеет форму, близкую к сферической. Малое поверхностное натяжение позволяет клеткам легко изолироваться одна от другой. Форма клеток, прикрепленных к другим клеткам или к субстрату, зависит от других факторов — их цитоскелета, образованного комплексом мембран, контактных структур и др. Отдельные виды клеток (например, лейкоциты и яйцеклетки) при освобождении от действия поверхностного натяжения приобретают форму шара и теряют активность. Локальным изменениям поверхностного натяжения принадлежит важная роль в процессах восприятия и передачи нервных импульсов, в фагоцитозе, пиноцитозе, гаструляции, амебоидном движении и, особенно, в проницаемости клеточных мембран.
fb.ru
Поверхностное натяжение - это... Что такое Поверхностное натяжение?

 Монета, лежащая на воде благодаря силе поверхностного натяжения
Монета, лежащая на воде благодаря силе поверхностного натяжения Пове́рхностное натяже́ние — термодинамическая характеристика поверхности раздела двух находящихся в равновесии фаз, определяемая работой обратимого изотермокинетического образования единицы площади этой поверхности раздела при условии, что температура, объём системы и химические потенциалы всех компонентов в обеих фазах остаются постоянными.
Поверхностное натяжение имеет двойной физический смысл — энергетический (термодинамический) и силовой (механический). Энергетическое (термодинамическое) определение: поверхностное натяжение — это удельная работа увеличения поверхности при её растяжении при условии постоянства температуры. Силовое (механическое) определение: поверхностное натяжение — это сила, действующая на единицу длины линии, которая ограничивает поверхность жидкости[1].
Сила поверхностного натяжения направлена по касательной к поверхности жидкости, перпендикулярно к участку контура, на который она действует и пропорциональна длине этого участка. Коэффициент пропорциональности  — сила, приходящаяся на единицу длины контура — называется коэффициентом поверхностного натяжения. Он измеряется в ньютонах на метр. Но более правильно дать определение поверхностному натяжению, как энергии (Дж) на разрыв единицы поверхности (м²). В этом случае появляется ясный физический смысл понятия поверхностного натяжения.
— сила, приходящаяся на единицу длины контура — называется коэффициентом поверхностного натяжения. Он измеряется в ньютонах на метр. Но более правильно дать определение поверхностному натяжению, как энергии (Дж) на разрыв единицы поверхности (м²). В этом случае появляется ясный физический смысл понятия поверхностного натяжения.
В 1983 году было доказано теоретически и подтверждено данными из справочников (Журнал физической химии. 1983, № 10, с. 2528—2530), что понятие поверхностного натяжения жидкости однозначно является частью понятия внутренней энергии (хотя и специфической: для симметричных молекул близких по форме к шарообразным). Приведенные в этой журнальной статье формулы позволяют для некоторых веществ теоретически рассчитывать значения поверхностного натяжения жидкости по другим физико-химическим свойствам, например, по теплоте парообразования или по внутренней энергии (подробнее о физической природе поверхностного натяжения жидкости см.соотв. статью на викиучебнике или [2] , [3])
В 1985 году аналогичный взгляд на физическую природу поверхностного натяжения, как части внутренней энергии, при решении другой физической задачи был опубликован В. Вайскопфом (Victor Frederick Weisskopf) в США (V.F.Weisskopf, American Journal of Physics 53 (1985) 19-20.; V.F.Weisskopf, American Journal of Physics 53 (1985) 618—619.).
Поверхностное натяжение может быть на границе газообразных, жидких и твёрдых тел. Обычно имеется в виду поверхностное натяжение жидких тел на границе «жидкость — газ». В случае жидкой поверхности раздела поверхностное натяжение правомерно также рассматривать как силу, действующую на единицу длины контура поверхности и стремящуюся сократить поверхность до минимума при заданных объёмах фаз.
В общем случае прибор для измерения поверхностного натяжения называется тензиометр.
Проявления

 Водомерка на поверхности воды.
Водомерка на поверхности воды. Так как появление поверхности жидкости требует совершения работы, каждая среда «стремится» уменьшить площадь своей поверхности:
- в невесомости капля принимает сферическую форму (сфера имеет наименьшую площадь поверхности среди всех тел одинакового объёма).
- струя воды «слипается» в цилиндр.
- маленькие объекты с плотностью, большей плотности жидкости, способны «плавать» на поверхности жидкости, так как сила тяготения меньше силы, препятствующей увеличению площади жидкости.
- некоторые насекомые (например, водомерки) способны передвигаться по воде, удерживаясь на её поверхности за счёт сил поверхностного натяжения.
- На многих поверхностях, именуемых несмачиваемыми, вода (или другая жидкость) собирается в капли.
Математическая теория
Площадь поверхности
С поверхностью жидкости связана свободная энергия

где  — коэффициент поверхностного натяжения,
— коэффициент поверхностного натяжения,  — полная площадь поверхности жидкости[4]. Так как свободная энергия изолированной системы стремится к минимуму, то жидкость (в отсутствие внешних полей) стремится принять форму, имеющую минимальную площадь поверхности. Таким образом задача о форме жидкости сводится к изопериметрической задаче при заданных дополнительных условиях (начальное распределение, объём и т. п.). Свободная капля принимает форму шара, однако при более сложных условиях задача о форме поверхности жидкости становится исключительно сложной.
— полная площадь поверхности жидкости[4]. Так как свободная энергия изолированной системы стремится к минимуму, то жидкость (в отсутствие внешних полей) стремится принять форму, имеющую минимальную площадь поверхности. Таким образом задача о форме жидкости сводится к изопериметрической задаче при заданных дополнительных условиях (начальное распределение, объём и т. п.). Свободная капля принимает форму шара, однако при более сложных условиях задача о форме поверхности жидкости становится исключительно сложной.
Формула Лапласа
Рассмотрим тонкую жидкую плёнку, толщиной которой можно пренебречь. Стремясь минимизировать свою свободную энергию, плёнка создаёт разность давления с разных сторон. Этим объясняется существование мыльных пузырей: плёнка сжимается до тех пор, пока давление внутри пузыря не будет превышать атмосферное на величину добавочного давления плёнки. Добавочное давление в точке поверхности зависит от средней кривизны в этой точке и даётся формулой Лапласа:

Здесь  — радиусы главных кривизн в точке. Они имеют одинаковый знак, если соответствующие центры кривизны лежат по одну сторону от касательной плоскости в точке, и разный знак — если по разную сторону. Например, для сферы центры кривизны в любой точке поверхности совпадают с центром сферы, поэтому
— радиусы главных кривизн в точке. Они имеют одинаковый знак, если соответствующие центры кривизны лежат по одну сторону от касательной плоскости в точке, и разный знак — если по разную сторону. Например, для сферы центры кривизны в любой точке поверхности совпадают с центром сферы, поэтому


Для случая поверхности кругового цилиндра радиуса  имеем
имеем


Обратите внимание, что  должно быть непрерывной функцией на поверхности плёнки, так что выбор «положительной» стороны плёнки в одной точке локально однозначно задаёт положительную сторону поверхности в достаточно близких её точках.
должно быть непрерывной функцией на поверхности плёнки, так что выбор «положительной» стороны плёнки в одной точке локально однозначно задаёт положительную сторону поверхности в достаточно близких её точках.
Из формулы Лапласа следует, что свободная мыльная плёнка, натянутая на рамку произвольной формы и не образующая пузырей, будет иметь среднюю кривизну, равную 0.
Зависимость от температуры
С увеличением температуры величина поверхностного натяжения уменьшается и равна нулю при критической температуре. Наиболее известная эмпирическая зависимость поверхностного натяжения от температуры была предложена Лорандом Этвёшом, так называемое правило Этвёша (англ.). В настоящее время получен вывод теоретической зависимости поверхностного натяжения от температуры в области до критических температур, подтверждающей правило Этвёша (журнал «Вестник Санкт-Петербургского университета», 2012, вып. 1, с. 24-28).
Способы определения
Способы определения поверхностного натяжения делятся на статические и динамические. В статических методах поверхностное натяжение определяется у сформировавшейся поверхности, находящейся в равновесии. Динамические методы связаны с разрушением поверхностного слоя. В случае измерения поверхностного натяжения растворов (особенно полимеров или ПАВ) следует пользоваться статическими методами. В ряде случаев равновесие на поверхности может наступать в течение нескольких часов (например, в случае концентрированных растворов полимеров с высокой вязкостью). Динамические методы могут быть применены для определения равновесного поверхностного натяжения и динамического поверхностного натяжения. Например, для раствора мыла после перемешивания поверхностное натяжение 58 мДж/м², а после отстаивания — 35 мДж/м² . То есть поверхностное натяжение меняется. До установления равновесного оно будет динамическое.
Статические методы:
- Метод поднятия в капилляре
- Метод Вильгельми
- Метод лежачей капли
- Метод определения по форме висячей капли.
- Метод вращающейся капли
Динамические методы:
- Метод дю Нуи (метод отрыва кольца).
- Сталагмометрический, или метод счета капель.
- Метод максимального давления пузырька.
- Метод осциллирующей струи
- Метод стоячих волн
- Метод бегущих волн
Методы
Полностью стандартизованные методы измерений описываются в соответствующих ASTM, ГОСТ и т. д.
Метод вращающейся капли
Сущностью метода является измерение диаметра капли жидкости, вращающейся в более тяжелой жидкости. Этот способ измерения годится для измерения низких или сверхнизких значений межфазного натяжения. Он широко применяется для микроэмульсий, измерения эффективности ПАВ в нефтедобыче, а также для определения адсорбционных свойств.
Метод Дю Нуи (метод отрыва кольца)
Метод является классическим. Сущность метода вытекает из названия. Платиновое кольцо поднимают из жидкости, смачивающей его, усилие отрыва и есть сила поверхностного натяжения и может быть пересчитано в поверхностную энергию. Метод подходит для измерения ПАВ, трансформаторных масел и т. д.
Метод бегущих волн
При возмущении жидкости пластиной «лежащей» на её поверхности, по ней начинает распространяться круг волн. Если просветить кювету с жидкостью импульсным источником света с частотой равной частоте возмущения, то на экран спроецируется «стоячая» волновая картина. Измеряя длину волны на экране и геометрически перерассчитывая её (зная расстояние от источника света до поверхности жидкости и расстояние от поверхности до экрана, а также про подобие треугольников) можно получить величину поверхностного натяжения по формуле:
 , где:
, где: Поверхностное натяжение жидкостей на границе с воздухом
| Хлорид натрия 6.0M водный раствор | 20 | 82,55 |
| Хлорид натрия | 801 | 115 |
| Глицерин | 30 | 64,7 |
| Олово | 400 | 518 |
| Азотная кислота 70 % | 20 | 59,4 |
| Анилин | 20 | 42,9 |
| Ацетон | 20 | 23,7 |
| Бензол | 20 | 29,0 |
| Вода | 20 | 72,86 |
| Глицерин | 20 | 59,4 |
| Нефть | 20 | 26 |
| Ртуть | 20 | 486,5 |
| Серная кислота 85 % | 20 | 57,4 |
| Спирт этиловый | 20 | 22,8 |
| Уксусная кислота | 20 | 27,8 |
| Эфир этиловый | 20 | 16,9 |
| Раствор мыла | 20 | 40 |
Проявления
-

Мыльный пузырь.
-

-

На фотографии виден эффект, получивший название «слезы вина».
-

Капля воды на листе.
-
Навал на границе лужи и сухого асфальта.
-
Вода набегает на сухую поверхность асфальта.
Примечания
- ↑ Б. Д. Сумм «Основы коллоидной химии»
- ↑ Хайдаров Г.Г., Хайдаров А.Г., Машек А. Ч. Физическая природа поверхностного натяжения жидкости // Вестник Санкт-Петербургского университета. Серия 4 (Физика, химия). 2011. Выпуск 1. с.3-8.. Архивировано из первоисточника 25 июня 2012.
- ↑ Хайдаров Г.Г., Хайдаров А.Г., Машек А. Ч., Майоров Е.Е. Влияние температуры на поверхностное натяжения // Вестник Санкт-Петербургского университета. Серия 4 (Физика, химия). 2012. Выпуск 1. с.24-28.. Архивировано из первоисточника 27 июня 2012.
- ↑ Обратите внимание, что плёнка, вроде стенки мыльного пузыря, имеет две стороны, так что площадь поверхности жидкости в два раза больше площади плёнки.
См. также
Тензиометр
Ссылки
Библиография
- Остроумов С. А., Лазарева Е. В. Поверхностное натяжение водных растворов додецилсульфата натрия в присутствии водных растений — Вода: технология и экология. 2008 № 3 с. 57-60.
dic.academic.ru
Поверхностное натяжение воды - Територия Здоровья
Поверхностное натяжение - это один из важнейших параметров воды. Поверхностное натяжение определяет силу сцепления между молекулами жидкости, а также форму ее поверхности на границе с воздухом. Поверхностное натяжение жидкости можно определить как энергию, необходимую для разрыва единицы поверхности.
Высокое поверхностное натяжение у шарика ртути. Поэтому и держится ртуть в виде шара.
Поверхностное натяжение ацетона - 20 дин/см - вот почему он лучший растворитель чем вода.
Поверхностное натяжение хлороформа (наркоз) - 9 дин/см - скорость проникновения наркоза в клетки мозга очень велика, за три вдоха мозг отравился и отключился.
Для того, чтобы вода была биологически доступной, степень поверхностного натяжения не должна превышать определенный предел.
Поверхностное натяжение водопроводной воды составляет около 73 дин/см, а поверхностное натяжение воды, которая окружает клетки примерно 43 дин/см.
Велико поверхностное натяжение у капельки росы. Чтобы наглядно определить какое из веществ имеет меньшее поверхностное натяжение, нужно смочить этими веществами например лист бумаги. Вещество, которое активнее впитывается (смачивает, растворяет) - имеет меньшее поверхностное натяжение.
Поэтому, выбирая устройство для приготовления воды, обязательно принимайте во внимание значение поверхностного натяжения воды, которое оно дает. Чем ближе это значение к 43 дин/см, тем с меньшими энергетическими затратами может быть усвоена эта вода.
Для осознания важности поверхностного натяжения питьевой воды, обратимся к ответу на вопрос: "Почему горячая вода отмывает грязь лучше, чем холодная?". Потому что с ростом температуры воды снижается ее поверхностное натяжение. Чем ниже поверхностное натяжение воды, тем лучшим растворителем она является. Но по отношению к нашему организму мы ограничены температурой +36,6.Искусство водоподготовки состоит в том, чтобы снизить поверхностное натяжение воды до физиологической нормы без увеличения ее температуры. Гидросел Кораллового клуба - продукт, который изменяет поверхностное натяжение воды.
Гидросел снижает поверхностное натяжение воды.
viktorcoral.jimdo.com























