Анализ фенолов в воде. Определение фенола в воде. Фенол вода
это что? Свойства и состав фенола
Фенолы – это органические вещества, относящиеся к ароматическим углеводородам. Их можно обнаружить в природе, но больше всего известны человеку те, которые получены искусственным путем. Они широко сейчас используются в химической промышленности, строительстве, производстве пластмасс и даже в медицине. Из-за высоких токсичных свойств, устойчивости его соединений и способности проникать в организм человека сквозь кожу и органы дыхания часто бывает отравление фенолом. Поэтому это вещество отнесли к классу высокоопасных ядовитых соединений и жестко регламентировали его применение.
Что такое фенолы
Это химические соединения, встречающиеся в природе и производимые в искусственных условиях. Природные фенолы могут быть полезными – это антиоксидант, полифенолы, которые делают некоторые растения целительными для человека. А синтетические фенолы – это ядовитые вещества. При попадании на кожу они вызывают ожог, при проникновении в организм человека – сильное отравление. Эти сложные соединения, относящиеся к летучим ароматическим углеводородам, переходят в газообразное состояние уже при температуре чуть более 40 градусов. Но в обычных условиях это прозрачное кристаллическое вещество со специфическим запахом.
Определение фенола изучается в школе в курсе органической химии. При этом говорится о его составе, строении молекулы и вредных свойствах. Про натуральные вещества этой группы, играющие большую роль в природе, многие ничего не знают. Как же можно охарактеризовать фенол? Состав этого химического соединения очень прост: молекула бензойной группы, водород и кислород.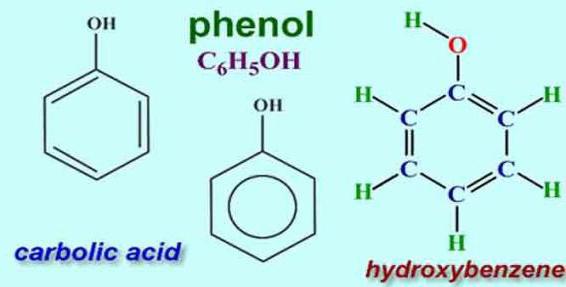
Виды фенолов
Эти вещества присутствуют во многих растениях. Они обеспечивают окраску их стеблей, аромат цветов или отпугивают вредителей. Есть также синтетические соединения, которые ядовиты. К этим веществам можно отнести:
- Природные фенольные соединения – это капсаицин, эвгенол, флавоноиды, лигнины и другие.
- Самый известный и ядовитый фенол – кислота карболовая.
- Соединения бутилфенол, хлорфенол.
- Креозот, лизол и другие.
Но в основном обычным людям известны только два названия: карболовая кислота и собственно фенол.
Свойства этих соединений
Эти химические вещества обладают не только токсичностью. Они используются человеком не просто так. Чтобы определить, какими качествами обладает фенол, состав очень важен. Соединение углерода, водорода и кислорода наделяет его особыми свойствами. Именно поэтому так широко используется человеком фенол. Свойства этого соединения такие:
- это кристаллическое вещество с сильным сладковатым запахом;
- интересна реакция фенола на воздействие воздуха – кристаллы меняют свой цвет: сначала розовеют, потом приобретают бурый оттенок;
- фенол имеет очень низкую температуру плавления;
- еще одно его качество – это кислотность;
- хорошо это вещество растворяется в спирте, масле, щелочах и других органических и неорганических растворителях,и только в воде фенол способен раствориться при температуре выше 70 градусов;
- на протяжении многих лет соединения фенола не теряют своих свойств, поэтому все изделия на их основе долго сохраняют токсичное действие на человека.

Роль фенолов в природе
Эти вещества находятся во многих растениях. Они участвуют в создании их окраски и аромата. Капсаицин придает остроту горькому перцу. Антоцианы и флавоноиды окрашивают кору деревьев, а кетол или эвгенол обеспечивают наличие аромата у цветов. В некоторых растениях содержатся полифенолы, вещества, образованные соединением нескольких молекул фенола. Они полезны для здоровья человека. К полифенолам относятся лигнины, флавоноиды и другие. Эти вещества есть в оливковом масле, фруктах, орехах, чае, шоколаде и других продуктах. Считается, что некоторые из них обладают омолаживающим эффектом и защищают организм от рака. Но есть и ядовитые соединения: танины, урушиол, карболовая кислота.
Вред фенолов для человека
Это вещество и все его производные легко проникают в организм через кожу и легкие. В крови фенол образует соединения с другими веществами и становится еще более токсичным. Чем выше его концентрация в организме, тем больший вред он может нанести. Фенол нарушает деятельность нервной и сердечно-сосудистой системы, поражает печень и почки. Он разрушает эритроциты, вызывает аллергические реакции и появление язв.
Чаще всего отравление фенолом происходит через питьевую воду, а также через воздух в помещениях, в которых использовались его производные при строительстве, производстве краски или мебели.
При вдыхании его соединений происходит ожог дыхательных путей, раздражение носоглотки и даже отек легких. Если фенол попал на кожу, получается сильный химический ожог, после которого развиваются плохо заживающие язвы. А если поражено более четверти кожных покровов человека, это приводит к его смерти. При случайном заглатывании небольших доз фенола, например, с зараженной водой, развивается язва желудка, нарушение координации движений, бесплодие, сердечная недостаточность, кровотечения и раковые опухоли. Большие дозы сразу приводят к смерти.
Где применяются фенолы
После открытия этого вещества была обнаружена его способность менять окраску на воздухе. Это качество стали использовать для производства красителей. Но потом были открыты другие его свойства. И вещество фенол стало широко использоваться в деятельности человека:
- для производства лакокрасочных изделий;
- для обработки кожи животных в легкой промышленности;
- при производстве нейлона, капрона и других синтетических тканей;
- для защиты сельскохозяйственных животных от инфекций;
- в составе пестицидов;
- при изготовлении дыма для копчения продуктов;
- при производстве пластмасс;
- в составе моющих и чистящих средств.

Применение в медицине
Когда были обнаружены бактерицидные свойства фенола, его широко стали использовать в медицине. В основном для дезинфекции помещений, инструментов и даже рук персонала. Кроме того, фенолы – это основные компоненты некоторых популярных лекарств: аспирина, пургена, препаратов для лечения туберкулеза, грибковых заболеваний и различных антисептиков, например, ксероформа.
Сейчас фенол часто применяется в косметологии для глубокого пилинга кожи. При этом используется его свойство сжигать верхний слой эпидермиса.
Использование фенола для дезинфекции
Есть и специальный препарат в виде мази и раствора для наружного применения. Он используется для дезинфекции вещей и поверхностей в помещении, инструментов и белья. Под наблюдением врача фенол применяют для лечения кондилом, пиодермий, импетиго, фолликулитов, гнойных ран и других кожных заболеваний. Раствор в сочетании с зеленым мылом применяют для дезинфекции помещений, замачивания белья. Если смешивать его с керосином или скипидаром, то он приобретает дезинсекционные свойства.

Нельзя обрабатывать фенолом обширные участки кожи, а также помещения, предназначенные для приготовления и хранения пищи.
Как можно отравиться фенолом
Смертельная дозировка этого вещества для взрослого человека может составлять от 1 г, а для ребенка – 0,05 г. Отравление фенолом может произойти по таким причинам:
- при несоблюдении техники безопасности в работе с ядовитыми веществами;
- при несчастном случае;
- при несоблюдении дозировки лекарственных средств;
- при использовании пластмассовых изделий с фенолом, например, игрушек или посуды;
- при неправильном хранении бытовой химии.
При остром отравлении признаки видны сразу и можно оказать человеку помощь. Но опасность фенола в том, что при поступлении маленьких доз этого можно не заметить. Поэтому, если человек живет в помещении, где использовались отделочные материалы, лакокрасочные изделия или мебель, выделяющие фенол, происходит хроническое отравление.
Симптомы отравления
Очень важно вовремя распознать проблему. Это поможет вовремя начать лечение и предотвратить летальный исход. Основные симптомы такие же, как при любом другом отравлении: тошнота, рвота, сонливость, головокружение. Но есть и характерные признаки, по которым можно узнать, что человек отравился именно фенолом:
- характерный запах изо рта;
- обморок;
- резкое снижение температуры тела;
- расширенные зрачки;
- бледность;
- одышка;
- холодный пот;
- снижение частоты пульса и артериального давления;
- боли в животе;
- кровянистая диарея;
- белые пятна на губах.
Нужно знать также признаки хронического отравления. При поступлении маленьких доз в организм нет сильно выраженных признаков этого. Но фенол подрывает состояние здоровья. Симптомы хронического отравления такие:
- частые мигрени, головные боли;
- тошнота;
- дерматиты и аллергические реакции;
- бессонница;
- расстройства кишечника;
- сильная утомляемость;
- раздражительность.
Первая помощь и лечение отравления
Пострадавшему необходимо оказать первую помощь и как можно скорее доставить его к врачу. Меры, которые нужно принять сразу после контакта с фенолом, зависят от места его проникновения в организм:
- При попадании вещества на кожу, промыть большим количеством воды, нельзя обрабатывать ожоги мазью или жиром.
- Если фенол попал на слизистую рта – прополоскать, ничего не глотать.
- При попадании в желудок выпить сорбент, например, уголь, «Полисорб», не рекомендуется промывать желудок во избежание ожога слизистой.
В медицинском учреждении лечение отравления сложное и длительное. Проводится вентиляция легких, дезинтосикационная терапия, вводится антидот – глюконат кальция, применяются сорбенты, антибиотики, сердечные препараты,
Правила безопасности при использовании фенолов
Санитарно-эпидемиологические нормы во всех странах установили предельно допустимый уровень концентрации фенола в воздухе помещений. Безопасной дозой считается 0,6 мг на 1 кг веса человека. Но эти нормативы не учитывают, что при регулярном поступлении даже такой концентрации фенола в организм, он постепенно накапливается и способен принести серьезный вред здоровью. Это вещество может выделяться в воздух из пластмассовых изделий, красок, мебели, строительных и отелочных материалов, косметики. Потому необходимо внимательно следить за составом покупаемой продукции и, если ощущается неприятный сладковатый запах от какой-то вещи, он нее лучше избавиться. При использовании фенола для дезинфекции необходимо строго соблюдать дозировку и правила хранения растворов.
fb.ru
Отравление фенолом - симптомы, влияние на организм, класс опасности
Фенолы – органические соединения, способные нанести человеку вред и повлиять на его здоровье. Несмотря на это, производство этого вещества в мире ежегодно возрастает.
Характеристика фенолов
Физические свойства фенола: своей формой напоминают кристаллы, которые имеют свойство окислятся на воздухе, покрываясь розовым окрасом, имеет специфический запах, схожий с запахом гуаши. Предельно допустимая концентрация (ПДК) фенола в воздухе 4 мг/ м³, в природных водоемах – 0,001.
Данное вещество прекрасно растворяется в спирте, маслах, ацетоне. В воде фенол растворяется постепенно, в отношении 1/20 если температура воды достигает +700° C. В загрязненных природных водах содержание его может достигать десятков и даже сотен микрограммов в 1 л.
Карболовая кислота – это 2-5% раствор фенола, является прекрасным антисептиком, способный уничтожить болезнетворные микробы и бактерии. Карболовую кислоту используют в производстве многих фармацевтических препаратах.
Синтетический технический фенол применяют в качестве сырья для получения капролактама, адипиновой кислоты, анилина, алкилфенола, гидрохинона. По количеству ОН-групп фенолы и спирты похожи по строению, однако фенол более сильная кислота.
Применение в медицине и других отраслях
 Область применения фенола, ввиду его опасности и токсичности – ограничена. Для снижения опасности, его используют в небольших количествах, смешивают с иными компонентами. Вещество активно используется производителями следующих отраслей:
Область применения фенола, ввиду его опасности и токсичности – ограничена. Для снижения опасности, его используют в небольших количествах, смешивают с иными компонентами. Вещество активно используется производителями следующих отраслей:
- Медицина: применяется как хороший антисептик, дезинфицирующее средство против грибковых инфекций, воспалений среднего уха. Также он задействован при изготовлении лекарственных препаратов (Аспирин), в генной инженерии;
- В косметологии: феноловый пилинг. Применяют фенол формальдегид для изготовления косметологических средств;
- Нефтеперерабатывающая промышленность: очистка остаточного масляного сырья;
- Сельское хозяйство: различные удобрения для борьбы с вредителями и сорняками. Также применяется, как антисептический препарат для дезинфекции шкур животных;
- Пищевая промышленность – для консервации продуктов;
- Химическая промышленность: изготовление чистящих и дезинфицирующих средств, эпоксидных смол, пластмасс, при изготовлении красителей.
Чем опасен фенол?
Данное вещество опасное и токсичное, его класс опасности – второй. В организм проникает через слизистые оболочки и кожу, после чего транспортируется во внутренние органы:
- Попадание одного грамма фенола в организм человека приводит к летальному исходу. Для детского организма хватит менее одного грамма. Независимо, в каком состоянии находится фенол формальдегид, для человека – это колоссальный вред, который бьет по здоровью;
- Жидкий фенол или в виде пара (газообразный) способен спровоцировать возникновение ожога или аллергических реакций, а также вызывает некроз тканей (в результате изменения белковых молекул).
- Кроме этого, они ухудшают кровообращение в организме, разрушают эритроциты, провоцируют возникновение дерматитов.
Во избежание возникновения тяжелых последствий фенол формальдегида на организм, нужно знать причины отравлений и способы борьбы с ним.
Причины отравления
Отравление происходит по следующим причинам:
- Применение фенолосодержащих лекарств, срок годности которых истек;
- Незнание состава лекарства, применение без «рецепта»;
- Отравление фенолом при контакте с игрушками (чаще всего содержится в игрушках производства КНР, хотя и другие производители грешат этим.
- Чрезмерные дозировки.
Если взрослые люди попадают под воздействие фенола по неосмотрительности, то дети страдают из-за того, что взрослые поставили лекарства в легкодоступные места, а иногда и вовсе оставили открытыми.
Симптомы отравления
Отравление фенолом подразделяют на острое и хроническое.
Острое отравление проявляется при попадании вещества на кожу, внутрь или при вдыхании паров. В домашних условиях очень трудно отравиться парами, гораздо более часто это происходит на предприятиях. Достаточно одного вдоха, чтобы наблюдать следующие симптомы:
- Постоянный кашель, вызванный раздражением легких;
- Чрезмерная возбудимость;
- Сильная боль в голове;
- Слабость и ломота в теле.
Вышеперечисленные проблемы со здоровьем могут быть причиной госпитализации.Признаки отравления фенолом при попадании на кожу:
- Поврежденный участок кожи становится белым;
- Трансформация кожи, проявление морщин и складок;
- Спустя время – кожа краснеет;
- Надуваются пузыри;
- Жжение и покалывание.
При попадании химиката внутрь, могут наблюдаться следующие симптомы:
- Неприятный запах изо рта;
- Возникновение пятен в ротовой полости;
- Боль в горле, внутренних органах;
- Плохое самочувствие, рвотные массы;
- Повышенная потливость;
- Изменение цвета мочи.
При больших дозах карболовой кислоты возможен летальный исход.
В случае постоянного, но малого воздействия вещества на организм, развивается хроническое отравление, которое сопровождается:
- Слабостью и ломотой в теле;
- Плохим сном;
- Сильной головной болью;
- Отсутствием аппетита;
- Плохим настроением.

Первая помощь при отравлении фенолом
При подозрении на отравление фенолом необходимо немедленно обратиться за медицинской помощью. Вывести вещество из организма самостоятельно невозможно, но оказать доврачебную помощь вполне реально.
Для этого нужно следовать следующим рекомендациям:
- Вывести потерпевшего на свежий воздух;
- Если концентрация вещества в желудке большая, стоит принять сорбент, запить большим количеством воды;
- При внутреннем отравлении нужно прополоскать тщательно рот водою (молоком), в течение 5 – 10 минут, после чего – сплюнуть;
- Поврежденную кожу следует промыть водою;
- Не покидайте душ до приезда скорой помощи, тщательно промывайте все пораженные участки тела.
Полноценное лечение и диагностика проводится только под наблюдением врача. Выводить яд следует с применением витамина В1, этанола (наружно), а также при помощи таких процедур, как трахеотомия и интубация.

Профилактика
Основное правило, которого необходимо придерживаться, чтобы не отравиться – это избегать контакта с веществом при работе с фенолосодержащими компонентами. Рекомендуется использовать средства защиты (перчатки, маски, костюмы и респираторы).
Не покупать лекарств, в состав которого входит фенол формальдегид, по возможности принимать аналоговые и альтернативные препараты (проще немного потратится, чем рисковать здоровьем), если таковые имеются дома – хранить в труднодоступных для детей местах.
В косметологических целях фенол формальдегид использую, как феноловый пилинг, однако он может проявить свой аллергический эффект, поэтому стоит задуматься о целесообразности такой процедуры.
vseotravleniya.ru
Химические свойства фенолов | Химия онлайн
Химические свойства фенолов определяются наличием в молекуле гидроксильной группы и бензольного кольца.
I. Реакции с участием гидроксильной группы
Фенолы являются более сильными кислотами, чем спирты и вода, т.к. за счет участия неподеленной электронной пары кислорода в сопряжении с π-электронной системой бензольного кольца полярность связи О–Н увеличивается.
Кислотные свойства
Фенолы в водных растворах диссоциируются по кислотному типу: на фенолят-ионы и ионы водорода: 1) Взаимодействие с активными металлами с образованием фенолятов (сходство со спиртами)
1) Взаимодействие с активными металлами с образованием фенолятов (сходство со спиртами)
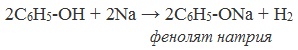
Видеоопыт «Взаимодействие фенола с металлическим натрием»
2) Взаимодействие со щелочами с образованием фенолятов (отличие от спиртов)
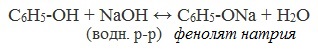
Видеоопыт «Взаимодействие фенола с раствором щелочи»
Образующиеся в результате реакций феноляты легко разлагаются при действии кислот. Даже такая слабая кислота, как угольная, вытесняет фенол из фенолятов. Следовательно, !Феноляты – соли слабой карболовой кислоты, разлагаются угольной кислотой: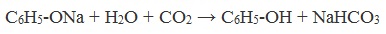
По кислотным свойствам фенол превосходит этанол в 106 раз. При этом во столько же раз уступает уксусной кислоте. В отличие от карбоновых кислот, фенол не может вытеснить угольную кислоту из её солей
C6H5-OH + NaHCO3 = реакция не идёт – прекрасно растворяясь в водных растворах щелочей, он фактически не растворяется в водном растворе гидрокарбоната натрия.
Кислотные свойства фенола усиливаются под влиянием связанных с бензольным кольцом электроноакцепторных групп (NO2- , Br- )
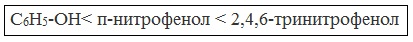
2,4,6-тринитрофенол или пикриновая кислота сильнее угольной.
3) Образование сложных и простых эфиров
Как и спирты, фенолы могут образовывать простые и сложные эфиры. Фенолы не образуют сложные эфиры в реакциях с кислотами. Сложные эфиры образуются при взаимодействии фенола с ангидридами или хлорангидридами карбоновых кислот: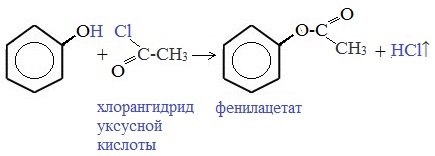
Простые эфиры образуются при взаимодействии фенолятов с алкилгалогенидами:
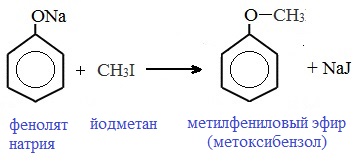
II. Реакции, с участием бензольного кольца
Взаимное влияние атомов в молекуле фенола проявляется не только в особенностях поведения гидроксигруппы, но и в большей реакционной способности бензольного ядра. Гидроксильная группа повышает электронную плотность в бензольном кольце, особенно, в орто- и пара- положениях (+М-эффект ОН-группы):
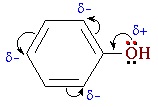
Поэтому фенол значительно активнее бензола вступает в реакции электрофильного замещения в ароматическом кольце.
Реакции замещения
1) Нитрование
Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара- нитрофенолов:
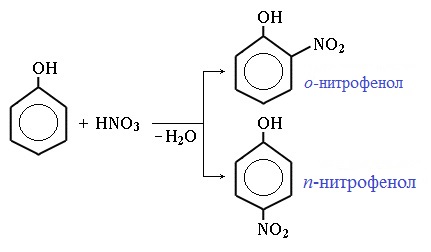
При использовании концентрированной HNO3 образуется 2,4,6-тринитрофенол (пикриновая кислота):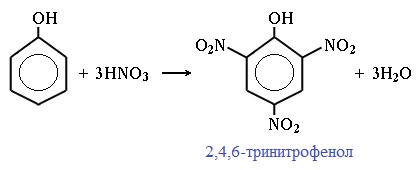
2) Галогенирование
Фенол легко при комнатной температуре взаимодействует с бромной водой с образованием белого осадка 2,4,6-трибромфенола (качественная реакция на фенол!):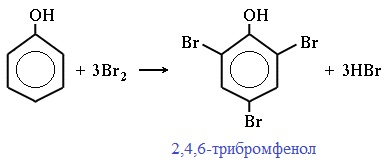
Образуется белый осадок трибромфенола.
Видеоопыт «Взаимодействие фенола с бромной водой»
3) Сульфирование
Соотношение о- и п-изомеров определяется температурой реакции: при комнатной температуре в основном образуется о-фенолсульфокислота, при t=1000С – пара-изомер: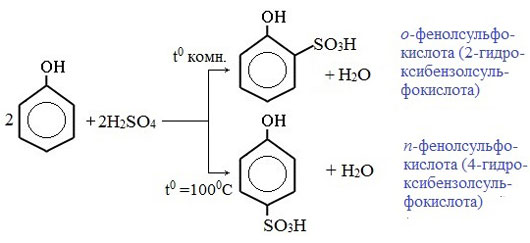 Реакции присоединения
Реакции присоединения
1) Гидрирование фенола
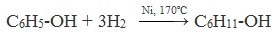
2) Конденсация с альдегидами
При нагревании фенола с формальдегидом в присутствии кислотных или основных катализаторов происходит реакция поликонденсации и образуется фенолформальдегидная смола.
Данная реакция имеет большое практическое значение и используется при получении фенолформальдегидных смол.
III. Реакция окисления
Фенолы легко окисляются даже под действием кислорода воздуха. При стоянии на воздухе фенол постепенно окрашивается в розовато-красный цвет. При энергичном окислении фенола хромовой смесью основным продуктом окисления является хинон. Двухатомные фенолы окисляются еще легче. При окислении гидрохинона также образуется хинон:
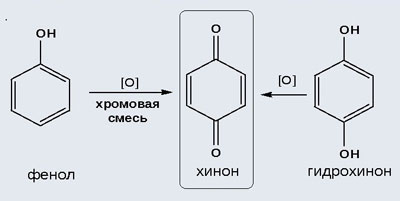
IV. Качественная реакция! - обнаружение фенола
Для обнаружения фенолов используется качественная реакция с хлоридом железа (III). Одноатомные фенолы дают устойчивое сине-фиолетовое окрашивание, что связано с образованием комплексных соединений железа.
Видеоопыт «Качественная реакция на фенол»
Образование фиолетового окрашивания при добавлении раствора FeCl3 служит качественной реакцией на фенол:
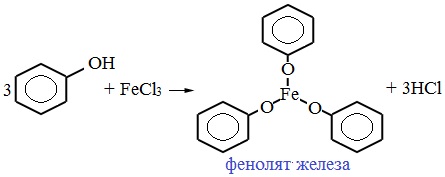
Для фенолов реакции по связям С-О не характерны, поскольку атом кислорода прочно связан с атомом углерода бензольного кольца за счет участия своей неподеленной электронной пары в системе сопряжения.
Фенолы
himija-online.ru
Анализ фенолов в воде. Определение фенола в воде
9 октября 2017 / 785 просмотров
Качество водопроводной воды в квартирах большинства украинцев оставляет желать лучшего. И дело не всегда в экологии. Даже если изначально вода и была неплохой (например, поднятой с подземного горизонта), то пройдя по изношенным трубам, она становится практически непригодной для питья. Но банальная ржавчина – это далеко не самый страшный «сюрприз» из вашего крана. Гораздо опаснее загрязнение химическими соединениями, например, такими как фенолы. Оказывается, фенол в питьевой воде – не такое уж редкое явление. Давайте разберёмся, откуда он берётся и как можно решить проблему.
Зачем нужен анализ воды на фенол?
Для начала стоит разобраться: что же такое фенолы и какую опасность они могут представлять. Выражаясь языком химии, фенолы – это органические соединения ароматического ряда, которые применяются в производстве различных феноло-альдегидных смол, полиамидов, эпоксидных смол, антиоксидантов и т.п. То есть, фенолы могут попадать в воду как следствие хозяйственной деятельности предприятий нефтеперерабатывающей, лакокрасочной, лесохимической и т.п. промышленности. Но не только. Оказывается, фенолы в воде могут появиться даже просто из-за некачественных труб и материалов, – утверждают специалисты. Трубы, прокладки, жидкие уплотнители, герметики для труб могут содержать в своём составе фенолы. Получается, что поменяв старые ржавые трубы на новые, вы можете получить фенол взамен ржавчины. Согласитесь, результаты такого «замещения» не радуют. Чтобы такая проблема не возникла, тщательно подбирайте материалы для ремонта, изучайте сертификаты качества.Фенол – очень токсичное вещество. При попадании в организм он способен вызвать тяжёлые последствия. Раствор фенола в воде оказывают разрушающее воздействие на почки и головной мозг. Значительное превышение допустимых показателей содержания фенола в воде даже может приравниваться к экологической катастрофе (как, например, произошло в 1990 году в Уфе, когда в реку попали отходы местного химического предприятия). Именно поэтому анализ фенолов в воде чрезвычайная важная составляющая исследований качества воды.

Определение фенолов в воде: как устранить проблему
Согласно государственным санитарно-гигиеническим нормам, содержание фенола в воде не должно превышать 0, 001 мг/дм3. Если этот показатель превышен, нужно устранять проблему. Оказывается, для этого даже не нужно устанавливать в квартире сложные и дорогие системы фильтрации. Даже бюджетные модели, в том числе и обычные угольные фильтры, отлично справляются с этой проблемой.
Фенолы в сточных водах
Фенолы могут негативно влиять на здоровье человека и окружающую среду, если превышено их количество в поверхностных водах. Вообще фенол – один из самых распространённых промышленных загрязнителей. Предприятия должны очищать свои стоки, для того, чтобы избежать попадания фенола в поверхностные воды. Но риск превышения допустимого уровня загрязнения всё равно присутствует. Если, к примеру, ваш приусадебный участок, находится по соседству с предприятиями химической промышленности, которые используют фенол, то определение наличия фенолов в воде будет совсем не лишним.Определение фенола в сточной воде поможет вовремя обратить внимание на проблему и принять меры.
Делаем выводы
Определение фенолов в воде входит в перечень показателей расширенного анализа воды, который делает лаборатория «УкрХимАнализ». Чтобы не переживать за качество воды, которую вы пьёте – просто сделайте анализ воды на фенол. На сайте лаборатории вы всегда сможете выбрать оптимальный пакет по количеству показателей (максимальный, базовый, расширенный). Специалисты «УкрХимАнализ» проведут качественный и точный анализ предоставленных образцов воды, а также дадут все необходимые консультации, помогут расшифровать показатели и подскажут, что делать, чтобы улучшить качество воды.
У Вас есть вопросы или Вам нужна консультация?
Заполните форму и получите бесплатную консультацию!
Читайте похожие статьи:
himanaliz.ua
Фенол — Медицинская википедия
 Игольчатые кристаллы фенола
Игольчатые кристаллы фенола Фено́л (гидроксибензол, Шаблон:Lang-old-ru) C6H5OH — простейший представитель класса фенолов. Бесцветные игольчатые кристаллы, розовеющие на воздухе из-за окисления, приводящего к образованию окрашенных веществ. Обладают специфическим запахом (таким, как запах гуаши, т. к. в состав гуаши входит фенол). Умеренно растворим в воде (6 г на 100 г воды), в растворах щелочей, в спирте, в бензоле, в ацетоне. 5 % раствор в воде — антисептик, широко применяемый в медицине.
Мировое производство фенола на 2006 год составляет 8,3 млн тонн/год. По объёму производства фенол занимает 33-е место среди всех выпускаемых химической промышленностью веществ и 17-е место среди органических веществ.
Получение
На 2006 год производство фенола в промышленном масштабе осуществляется тремя способами:
Ведутся пилотные испытания установок получения фенола прямым окислением бензола закисью азота и кислотным разложением гидропероксида втор-бутилбензола.
Фенол также можно получить восстановлением хинона.
Физические свойства
- Фенол ядовит. Это твёрдое бесцветное вещество с резким запахом. При температуре больше 70 Шаблон:Градус Цельсия растворяется в воде в любых отношениях.
Химические свойства
- Обладает слабыми кислотными свойствами (более сильными, чем у спиртов), при действии щелочей образует соли — феноляты (например, фенолят натрия — C6H5ONa):
- Вступает в реакции электрофильного замещения по ароматическому кольцу. Гидрокси-группа, являясь одной из самых сильных донорных групп, увеличивает реакционную способность кольца к этим реакциям и направляет замещение в орто- и пара-положения. Фенол с лёгкостью алкилируется, ацилируется, галогенируется, нитруется и сульфируется.
- Взаимодействие с металлическим натрием:
- Взаимодействие с бромной водой (качественная реакция на фенол):
Биологическая роль
Протеиногенная аминокислота тирозин является структурным производным фенола и может быть рассмотрена как пара-замещённый фенол или α-замещённый пара-крезол. В природе распространены и другие фенольные соединения, в том числе полифенолы. В свободном виде фенол встречается у некоторых микроорганизмов и находится в равновесии с тирозином. Равновесие поддерживает энзим тирозин-фенол-лиаза (КФ 4.1.99.2).
Биологическое значение фенола обычно рассматривается в рамках его воздействия на окружающую среду. Фенол — один из промышленных загрязнителей. Фенол довольно токсичен для животных и человека. Фенол губителен для многих микроорганизмов, поэтому промышленные сточные воды с высоким содержанием фенола плохо поддаются биологической очистке.
Применение
По данным на 2006 год мировое потребление фенола имеет следующую структуру:
- 44 % фенола расходуется на производство бисфенола А, который, в свою очередь, используется для производства поликарбона и эпоксидных смол;
- 30 % фенола расходуется на производство фенолформальдегидных смол;
- 12 % фенола гидрированием превращается в циклогексанол, используемый для получения искусственных волокон — нейлона и капрона;
- в России большое количество фенола используется в нефтепереработке, в частности для селективной очистки масел на технологических установках типа 37/1 и А-37/1. Фенол проявляет высокую селективность и эффективность при удалении из масел смолистых веществ, различных полициклических ароматических углеводородов с короткими боковыми цепями, а также соединений, содержащих серу;
- остальной фенол расходуется на другие нужды, в том числе на производство антиоксидантов (ионол), неионогенных ПАВ — полиоксиэтилированных алкилфенолов (неонолы), других фенолов (крезолов), лекарственных препаратов (аспирин), антисептиков (ксероформа) и пестицидов. Раствор 1,4 % фенола применяется в медицине (орасепт) как обезболивающее и антисептическое средство.
Фенол и его производные обусловливают консервирующие свойства коптильного дыма. Также фенол используют в качестве консерванта в вакцинах. Пример использования, в качестве антисептика — препарат «Орасепт». В косметологии как химический пилинг (токсично).
Токсические свойства
Фенол ядовит. Относится к высокоопасным веществам (Класс опасности II). При вдыхании вызывает нарушение функций нервной системы. Пыль, пары и раствор фенола раздражают слизистые оболочки глаз, дыхательных путей, кожу, вызывая химические ожоги. Доказательства канцерогенности фенола для людей отсутствуют.
Предельно допустимые концентрации (ПДК) фенола:
Попадая на кожу, фенол очень быстро всасывается даже через неповреждённые участки и уже через несколько минут начинает воздействовать на ткани головного мозга. Сначала возникает кратковременное возбуждение, а потом и паралич дыхательного центра. Даже при воздействии минимальных доз фенола наблюдается чихание, кашель, головная боль, головокружение, бледность, тошнота, упадок сил. Тяжелые случаи отравления характеризуются бессознательным состоянием, синюшностью, затруднением дыхания, нечувствительностью роговицы, скорым, едва ощутимым пульсом, холодным потом, нередко судорогами. Смертельная доза для человека при попадании внутрь 1—10 г, для детей 0,05—0,5 г.
medviki.com
Фенолы. Классификация. Физические свойства
Фенолы – это производные аренов, у которых один или несколько атомов водорода ароматического кольца замещены на ОН-группу.
Классификация.
1. Одноатомные фенолы:
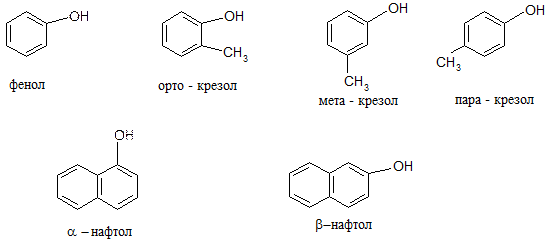
2. Многоатомные фенолы:
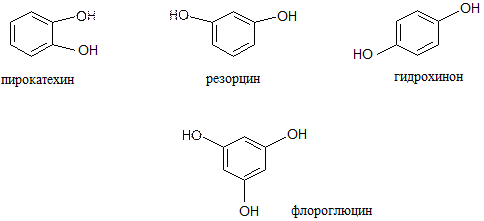
Физические свойства:
Фенол и его низшие гомологи – бесцветные низкоплавкие кристаллические вещества или жидкости с характерным запахом.
Фенол умеренно растворим в воде. Фенол способен образовывать водородные связи, что лежит в основе его антисептических свойств. Водные растворы фенола вызывают ожоги тканей. Разбавленный водный раствор фенола называется карболовой кислотой. Фенол – токсичен, токсичность гомологов фенола уменьшается, бактерицидная активность увеличивается по мере усложнения алкильного радикала.
Способы получения фенолов
1. Из каменноугольной смолы.
2. Кумольный метод
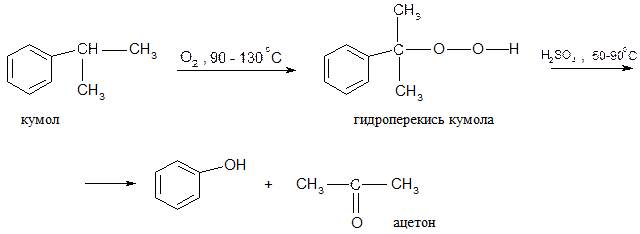
3. Сплавление солей ароматических сульфокислот с щелочью:
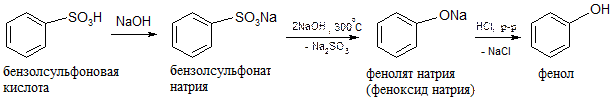
4. Разложение солей диазония:
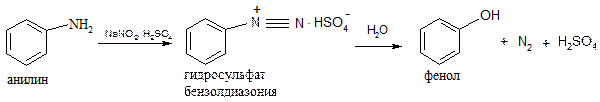
5. Гидролиз галогенпроизводных
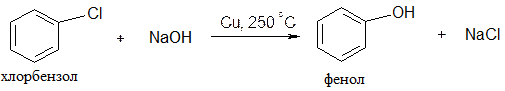
§11. Химические свойства фенолов.
1. Кислотные свойства: фенолы образуют соли:

Фенол – более слабая кислота, чем угольная Н2СО3 :
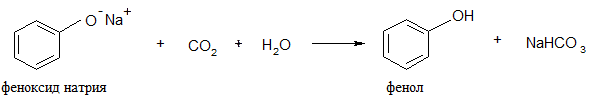
2. Реакции с участием ОН-группы.
а) алкилирование (образование простых эфиров)
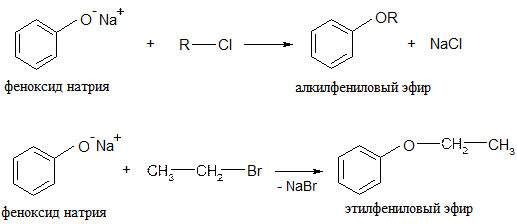
б) ацилирование (образование сложных эфиров):
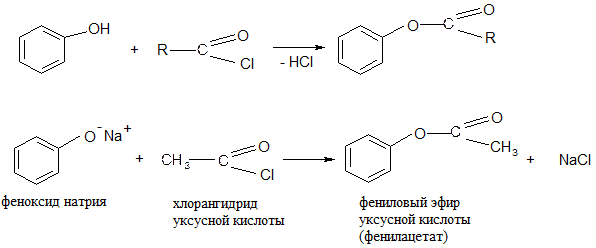
3. Реакции замещения ОН-группы:
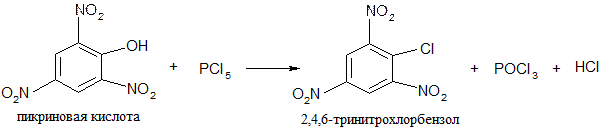
Фенол с Nh4 и R – Nh3 не взаимодействует.
4. Реакции электрофильного замещения, характерные для аренов.
Замещение протекает быстрее, чем у бензола. ОН-группа направляет новый заместитель в орто- и пара-положения.
а) галогенирование (обесцвечивание бромной воды – качественная реакция на фенол):
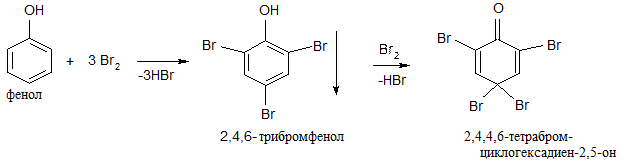
б) нитрование
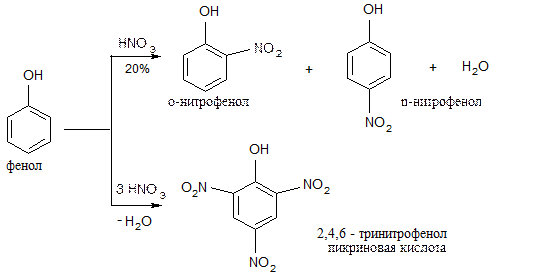
в) сульфирование:
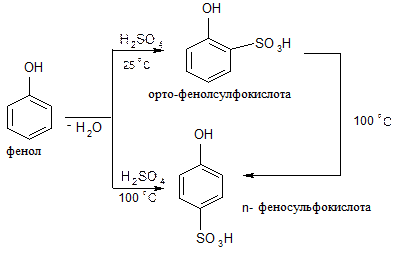
5. Реакции конденсации
а) с формальдегидом

б) с фталевым ангидридом
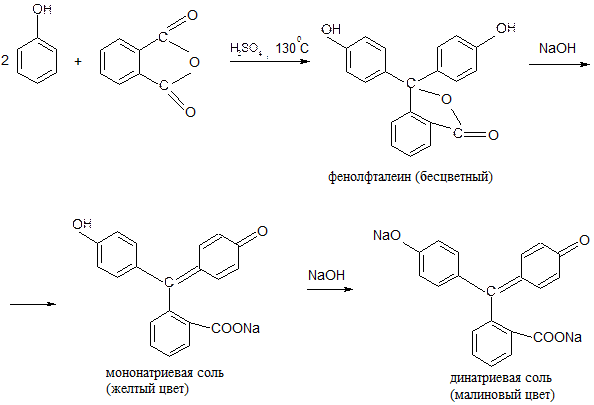
6. Окисление
а) на воздухе белые кристаллы фенола розовеют;
б) фенол с раствором FeCl3 дает красно-фиолетовое окрашивание;
крезол – голубое окрашивание;
в) окисление сильными окислителями

7. Восстановление
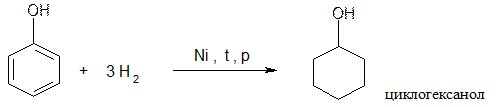
8. Карбоксилирование (реакция Кольбе – Шмитта):

Применение
1. Фенол применяется в производстве фенолформальдегидных смол, капролактама, пикриновой кислоты, красителей, инсектицидов, лекарственных средств.
2. Пирокатехин и его производные используются в производстве лекарственных средств (получен синтетический гормон – адреналин) и душистых веществ.
3. Резорцин применяют в синтезе красителей; в медицине в качестве дезинфицирующего средства.
Экспериментальная часть
Опыт 1. Влияние радикала и количества гидроксильных групп на растворимость спиртов.
В три пробирки внесите 4-5 капель этилового, изоамилового спиртов и глицерина. В каждую пробирку добавьте по 5-6 капель воды, взболтайте. Что наблюдали?
Опыт 2.Обнаружение воды в этиловом спирте и его обезвоживание.
В сухую пробирку внесите 10 капель этилового спирта, добавьте немного обезвоженного сульфата меди, тщательно перемешайте, дайте отстояться. Если спирт содержит воду, осадок сульфата меди окрасится в голубой цвет вследствии образования медного купороса СuSO4 · 5h3O. Сохраните обезвоженный спирт для дальнейшего опыта.
Опыт 3. Образование этилата натрия.
Поместите в сухую пробирку маленький кусочек натрия, добавьте 3 капли обезвоженного этилового спирта (из предыдущего опыта) и закройте отверстие пробирки пальцем. Тут же начинается выделение водорода.
По окончании реакции, не отрывая пальца от отверстия пробирки, поднесите ее к пламени горелки. При открытии пробирки водород воспламеняется с характерным звуком, образуя колечко голубоватого цвета. На дне пробирки остается беловатый осадок этилата натрия или его раствор.
При добавлении в пробирку 1 капли спиртового раствора фенолфталеина появляется красное окрашивание.
Напишите уравнения протекающих реакций.
Опыт 4. Окисление этилового спирта хромовой смесью.
Введите в пробирку 3-4 капли этилового спирта. Добавьте 1 каплю 2н раствора серной кислоты и 2 капли 0,5н раствора бихромата калия. Полученный оранжевый раствор нагрейте над пламенем горелки до начала изменения цвета. Обычно уже через несколько секунд цвет раствора становится синевато-зеленым. Одновременно ощущается характерный запах уксусного альдегида, напоминающий запах яблок. Метод можно применять для распознавания первичных и вторичных спиртов.
Напишите уравнения реакций.
Опыт 5. Получение этилацетата.
В сухую пробирку поместите немного порошка обезвоженного ацетата натрия (высота слоя около 2мм) и 3 капли этилового спирта. Добавьте 2 капли концентрированной серной кислоты и нагрейте осторожно над пламенем горелки. Через несколько секунд появляется характерный приятный освежающий запах уксусноэтилового эфира.
Уравнения реакции:
 СН3С(О)ОNа + НОSО3Н NаНSО4 + СН3С(О)ОН
СН3С(О)ОNа + НОSО3Н NаНSО4 + СН3С(О)ОН
 С2Н5ОН + НОSО3Н Н2О + С2Н5ОSО3Н
С2Н5ОН + НОSО3Н Н2О + С2Н5ОSО3Н
 СН3С(О)ОН + НОSО3Н Н2SО4 + СН3С(О)О С2Н5
СН3С(О)ОН + НОSО3Н Н2SО4 + СН3С(О)О С2Н5
Опыт 6.Реакция глицерина с гидроксидом меди (II) в щелочной среде.
Поместите в пробирку 3 капли 0,2н раствора СuSO4, 2 капли 2н раствора NаОН и перемешайте. Появляется студенистый осадок гидроксида меди (II):

При нагревании в щелочной среде до кипения полученный гидроксид
меди (II) разлагается. Это обнаруживается по выделению черного осадка оксида меди (II):
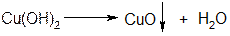
Повторите опыт, но перед кипячением гидроксида меди (II) добавьте в пробирку 1 каплю глицерина. Взболтайте. Нагрейте до кипения полученный раствор и убедитесь в том, что раствор глицерата меди при кипячении не разлагается. Здесь образуется хелатное соединение
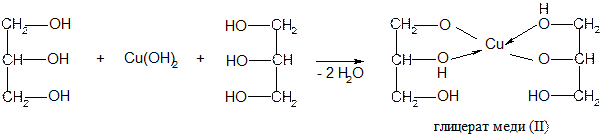
Опыт 7. Образовавние акролеина из глицерина.
Поместите в пробирку 3-4 кристалла бисульфата калия и 1 каплю глицерина. Нагрейте на пламени горелки. Признаком начавшегося разложения глицерина служит побурение жидкости в пробирке и появление тяжелых паров образующегося акролеина, обладающего очень резким запахом.
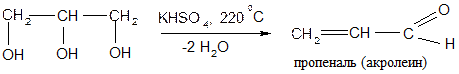
Опыт 8.Растворимость фенола в воде.
Поместите в пробирку 1 каплю жидкого фенола, добавьте 1 каплю воды и
взболтайте. Получится мутная жидкость – эмульсия фенола. При стоянии
такая эмульсия расслаивается, причем внизу будет раствор воды в феноле,
или жидкий фенол, а вверху – раствор фенола в воде, или карболовая вода.
Прибавляйте по каплям воду, каждый раз встряхивая пробирку, пока не
получится прозрачный раствор фенола в воде. Сохраните полученную
фенольную воду для последующих опытов.
Опыт 9.Цветные реакции на фенольную воду.
Поместите в пробирку 3 капли прозрачной фенольной воды и добавьте 1 каплю 0,1н раствора FeCl3 – появляется фиолетовое окрашивание.
Более чувствительной реакцией на фенол является цветная индофеноловая
проба.
Поместите в пробирку 1 каплю прозрачной карболовой воды. Добавьте к ней 3 капли 2н раствора NН4ОН и затем 3 капли насыщенного раствора бромной воды. Через несколько секунд на белом фоне бумаги можно заметить синее окрашивание, постепенно увеличивающееся за счет образования красящего вещества – индофенола.
Опыт 10.Образование трибромфенола.
Поместите в пробирку 3 капли бромной воды и добавьте 1 каплю прозрачной карболовой воды. Фенолы со свободными орто- и пара-положениями обесцвечивают бромную воду и образуют при этом продукты замещения, которые обычно выпадают в осадок.
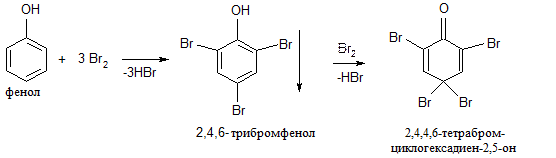
Опыт 11.Доказательство кислотного характера фенола.
К остатку фенольной воды добавьте еще 1 каплю фенола и встряхните. К вновь полученной эмульсии добавьте 1 каплю 2н раствора NаОН. Моментально образуется прозрачный раствор фенолята натрия, так как он хорошо растворяется в воде.

§10. Задачи для самостоятельного решения.
1. Напишите структурные формулы следующих соединений:
3-метил-2-пентанол; 2-метил-3-бутин-2-ол; 1-фенилпропанол-1.
2. Реакцией Гриньяра получите следующие спирты:
1) 2-метил-3-пентанол;
2) 2,3-диметил-3-пентанол;
3) 2,2-диметил-1-пропанол.
3. Получите гидратацией соответствующих этиленовых углеводородов
следующие спирты:
а) 2-метилпентанол-2; б) 3,3-диметилбутанол-2.
4. Напишите реакции окисления вторичного бутилового спирта;
2-метилбутанола-1.
5. Подвергните 2-пентанол дегидратации, затем продукт реакции окислите водным раствором перманганата калия. Полученное соединение обработайте уксусной кислотой. Напишите уравнения реакций и назовите все продукты.
6. Получите фенол из бензола и 1-бутена через стадию образования гидроперекиси втор.бутила.
7. Опишите схему следующих превращений:
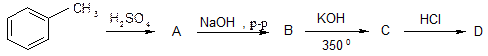
8. Расположите следующие соединения в порядке убывания кислотных свойств:
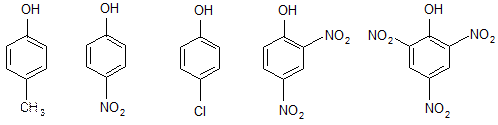
infopedia.su
Фенол - сточная вода - Большая Энциклопедия Нефти и Газа, статья, страница 1
Фенол - сточная вода
Cтраница 1
Фенолы сточных вод представлены в основном одноатомными фенолами: 60 - 65 % собственно фенола, 30 - 35 % ксиленолов и около 5 % ксиленолов. [1]
Отвод концентрированных по фенолу сточных вод, как правило, следует производить по отдельной сети, в которую не должен допускаться сброс каких-либо разбавляющих стоков. Это облегчает условия рентабельной регенерации ценных загрязнений и последующую доочистку сточных вод. Малоконцентрированные ( по фенолу) сточные воды в большинстве случаев оказывается целесообразным передавать в сеть хозяйственно-фекальной канализации, если это не нарушает нормальной работы очистных сооружений. [2]
Показаны возможности повышения качества фенолов сточных вод за счет снижения содержания железа до 0 01 % и увеличения содержания фенольного компонента. [3]
Пароциркуляционный метод применяется для очистки загрязненных фенолами сточных вод, которые превращаются в пар, проходящий через раствор щелочи. Выходными веществами являются чистый пар и нелетучий фенолят в растворе, удаляемый углекислотой. [4]
Отечественными и зарубежными учеными доказана целесообразность обработки концентрированных по фенолу сточных вод в два этапа. [5]
В настоящее время биологические способы начинают применять для очистки от фенолов сточных вод коксохимических заводов и других предприятий. [6]
В промышленном масштабе экстракционный метод применяется большей частью для предварительной очистки от фенолов сточных вод на заводах термической переработки твердого топлива. [7]
В промышленном масштабе экстракционный метод применяется в СССР для первичной очистки от фенолов сточных вод заводов термической переработки твердого топлива. В качестве экстрагента применяется бутилацетат в смеси с бутиловым спиртом. [8]
Аналогичная ситуация часто возникает при экстракции некоторых вредных примесей, например при очистке от фенолов сточных вод коксохимических заводов. [9]
В промышленном масштабе экстракционный метод применяется в СССР большей частью для предварительной очистки от фенолов сточных вод заводов термической переработки твердого топлива. Для окончательной очистки этих вод используется биохимический метод. Схема установки для экстракционной очистки, схемы отдельных ее технологических узлов и аппаратура являются типичными и могут быть использованы для очистки сточных вод химических заводов от различных растворенных в них органических загрязнений. [10]
Способ экстракции проходит в настоящее время опытные испытания с целью выявления оптимальных условий для применения при очистке от фенолов сточных вод коксохимических заводов. В качестве экстрагенге принят бензол х как наиболее дешевый продукт собственного производства коксохимзавода. Бензол хотя и имеет сравнительно невысокий коэффициент распределения, но обладает еще достаточной экстракционной способностью ( в лабораторных условиях до 99 % фенола в сточной воде), хорошо отделяется от сточной воды, легко освобождается от фенолов промывкой щелочью либо путем перегонки, химически устойчив. [11]
Вместо оценки интенсивности окраски полученного соединения при работе с диазотированным паранитроанилином применяют оттитровывание избытка диазораствора, не вступившего в реакцию с фенолами сточной воды, раствором Р - нафтола. Конец титрования определяют по ОТСУТСТВИЮ окрашивания при пробе на фарфоровой пластинке. [12]
Забор воды производят через всасывающие устройства с защитными сетками от попадания крупных кусочков кокса. Эти сетки довольно быстро ( через 5 - 6 месяцев) разрушаются под действием фенолов сточных вод, подаваемых на тушение кокса. [13]
Промышленный опыт очистки сточных вод химических заводов и нефтехимических производств не велик. Так, например, в главе об очистке от взвешенных загрязнений обобщен опыт очистки бытовых сточных вод и стоков нефтеперерабатывающих заводов; в главе об экстракционных методах очистки использован опыт очистки от фенолов сточных вод газификации и полукоксования углей и горючих сланцев. Материалы по паро-циркуляционному методу обобщают опыт очистки надсмольных вод коксохимических заводов. В главе о биологической очистке использован как промышленный опыт очистки бытовых сточных вод и фенольных вод газификации и полукоксования углей и сланцев, так и опыт очистки сточных вод различных химических производств. Однако материалы всех глав могут быть использованы при разработке и проектировании схем очистки сточных вод различных химических производств. [14]
В слабых растворах фенол при стоянии быстро разлагается, поэтому пробы должны поступать на анализ не позже 4 ч после отбора проб. В противном случае пробу консервируют, прибавляя на каждый литр сточной воды 5 мл 10 % - ного раствора едкого натрия. В щелочном растворе фенолы сточной воды связываются в фенолят натрия, и в таком виде проба может храниться в темном и прохладном месте длительный срок. [15]
Страницы: 1 2
www.ngpedia.ru



















