Окислительно-восстановительный потенциал. Окислительно восстановительные свойства воды
Окислительно восстановительный потенциал питьевой воды. ОВП
Окислительно-восстановительный потенциал
Окислительно-восстановительный потенциал (ОВП) является мерой химической активности элементов или их соединений в обратимых химических процессах, связанных с изменением заряда ионов в растворах.
ОВП, который так же иногда называют редокс-потенциалом (RedOx — англ. Reduction/Oxidation, ORP), характеризует степень активности электронов в окислительно-восстановительных реакциях, т.е. реакциях, связанных с присоединением или передачей электронов.
Значение окислительно-восстановительного потенциала для каждой окислительно-восстановительной реакции вычисляется по формуле Нернста с учетом рН-показателя (информация по измерению и расчетным данным ОВП крови и внутренних тканей содержится в книге В.И. Прилуцкого и В.М. Бахира «Электрохимически активированная вода: аномальные свойства, механизм биологического действия», Москва, 1997), выражается в милливольтах и может быть как положительным, так и отрицательным. Его положительные значения означают протекание процесса окисления и отсутствия электронов. Отрицательные значения ОВП свидетельствуют о протекании процесса восстановления и наличии электронов.
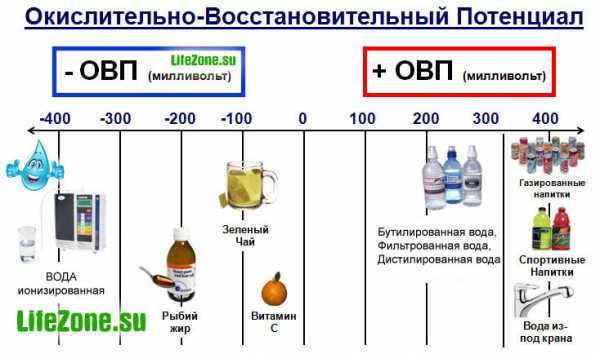
В природной воде значение ОВП обычно находится в диапазоне от — 400 до + 700 мВ, что определяется совокупностью происходящих в ней окислительных и восстановительных процессов. В условиях равновесия значение окислительно-восстановительного потенциала определенным образом характеризует водную среду, и его величина позволяет делать некоторые общие выводы о химическом составе воды.
В зависимости от значения ОВП различают несколько основных ситуаций, встречающихся в природных водах:
1. Окислительная. Характеризуется значениями ОВП превышающими значения + (100 — 150) мВ, присутствием в воде свободного кислорода, а также целого ряда элементов в высшей форме своей валентности (Fe3+, Mo6+, As5-, V5+, U6+, Sr4+, Cu2+, Pb2+). Такая ситуация наиболее часто встречается в поверхностных водах.
2. Переходная окислительно-восстановительная. Определяется величинами ОВП от 0 до + 100 мВ, неустойчивым геохимическим режимом и переменным содержанием сероводорода и кислорода. В этих условиях протекает как слабое окисление, так и слабое восстановление целого ряда металлов;
3. Восстановительная. Характеризуется отрицательными значениями ОВП. Такая ситуация типична для подземных вод, где присутствуют металлы низких степеней валентности (Fe2+, Mn2+, Mo4+, V4+, U4+), а также сероводород.
Самым распространенным природным окислителем является кислород. Примером окислительно-восстановительных реакций является коррозия металлов или потемнение поверхности фруктов, например, яблок.
Окислительно-восстановительные реакции происходят и в организме человека. Кислород, поступающий в организм, взаимодействуют с клетками нашего тела. Он действует как окислитель, а вместо ржавчины в организме образуются и накапливаются продукты окисления – свободные радикалы. Они ускоряют разрушение клеток, активизируют процессы физиологического старения и увядания всего организма.
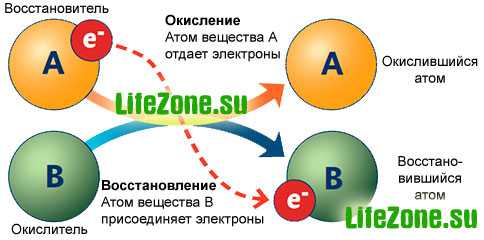
Разность электрических потенциалов между взаимодействующими веществами принято называть окислительно-восстановительным потенциалом (ОВП).
Вода с положительным значением ОВП имеет окислительные свойства. Такие показатели наиболее часто встречаются в поверхностных водах. Вода, обладающая ярко выраженными кислотными свойствами называется «мертвой» водой. Её ОВП может достигать +800+1000 мВ. Мертвая вода является сильнейшим окислителем и этим объясняются ее дезинфицирующие и бактерицидные свойства.
Вода с отрицательным значением ОВП имеет восстановительные свойства. Это типично для подземных горных источников, талой воды. Такая вода получила название «живой» воды. Живая вода (щелочная) является отличным стимулятором, тонизатором, источником энергии, придает бодрость, стимулирует регенерацию клеток, улучшает обмен веществ, нормализует кровяное давление. Живая вода быстро заживляет раны, ожоги, язвы (в т.ч. желудка и 12- перстной кишки), пролежни. Живая вода используется для лечения и профилактики остеохондроза, атеросклероза, аденомы предстательной железы, полиартрита.
Обычно ОВП организма человека колеблется в диапазоне от -90 мВ до -200 мВ, а ОВП обычной питьевой воды зачастую значительно выше нуля:
— водопроводная вода от +60 мВ до +300 мВ;— вода в пластиковых бутылках от +100 мВ до +300 мВ;— колодезная, родниковая вода от +120 мВ до +300 мВ.
В результате окислительно-восстановительных реакций, которые постоянно протекают в организме человека, высвобождается энергия, которая впоследствии используется для поддержания гомеостаза. Гомеостаз – это способность организма сохранять относительное динамическое постоянство своего внутреннего состояния путем проведения скоординированных реакций. Другими словами, энергия, полученная в ходе окислительно-восстановительных реакций, расходуется для обеспечения процессов жизнедеятельности организма человека, а также для регенерации его клеток.
Ученые провели серию экспериментов, направленную на установление величины окислительно-восстановительного потенциала человеческого организма. Для измерения окислительно-восстановительного потенциала использовался платиновый электрод, а для сравнения взяли хлорсеребряный электрон. В результате было установлено, что в нормальном состоянии ОВП человека колеблется в диапазоне от -90 до -200 милливольт.
Аналогичным методом был измерен окислительно-восстановительный потенциал питьевой воды. Эксперименты показали, что вода обычно имеет положительный ОВП, находящийся в диапазоне от +100мВ до +400 мВ. Причем не имеет значения, какая вода используется для питья или в пищу: водопроводная, купленная в магазинах в бутылках, очищенная при помощи различных фильтров, или с использованием установок обратного осмоса. Проведенные измерения ОВП человека и воды указывают на то, что активность электронов питьевой воды значительно уступает активности электронов человеческого организма.
От активности присутствующих в человеческом организме электронов зависят все процессы обеспечивающие его жизнедеятельность.
Известно, что все имеющие биологическое значение системы, которые отвечают за накопление и потребление энергии, репликацию и передачу различных наследственных признаков, а также системы организма, вырабатывающие различные ферменты, содержат определенные молекулярные структуры с разделенными зарядами, между которыми образуется напряженность электрического поля в пределах 104-106 В/см. Эти поля определяют передачу зарядов в биологических системах, что в свою очередь обуславливает осуществления выбора и автоконтроля на некоторых стадиях сложнейших биохимических превращений. Активность электронов, которую и выражает окислительно-восстановительный потенциал, оказывает большое влияние на функциональные свойства электроактивных компонентов биологических систем.
Из-за разности ОВП человеческого организма и питьевой воды, при попадании воды в ткани и клетки организма, происходит окислительная реакция, в результате которой клетки человека изнашиваются и разрушаются.
Каким образом можно уменьшить или замедлить клеточное разрушение организма человека? Это вполне достижимо при соблюдении условия, что вода, которая поступает в наш организм, будет иметь свойства, соответствующие свойствам нашей внутренней среды. То есть окислительно-восстановительный потенциал воды должен иметь значения близкие значениям ОВП человеческого организма. Чем больше разность между значениями ОВП у человека и у выпитой им воды, тем больше требуется затрат клеточной энергии для достижения соответствия воды и внутренней среды организма.
Поэтому фразу «Ты есть то, что ты ешь» с позиций современной науки можно вполне заменить фразой: «Ты есть то, что ты пьешь».
Если ОВП питьевой воды соответствует окислительно-восстановительному потенциалу внутренней среды человека, вода усваивается клетками организма без использования электрической энергии мембран клеток.
В случае, если окислительно-восстановительный потенциал потребляемой питьевой воды имеет большее отрицательное значение, нежели ОВП внутренней среды человека, то при усвоении такой воды выделяется энергия, расходуемая клетками в качестве энергетического запаса нашей антиоксидантной защиты, которая служит основным нашего щитом организма, оберегающим его от отрицательного влияния, оказываемого вредными факторами окружающей среды.
Именно из-за дисбаланса механизмов окислительно-восстановительных процессов в человеческом организме появляются многие болезни человека. Поэтому даже обычная вода может стать вредной для ослабленного человека. Проникая в клетки, такая вода отбирает у них электроны и тогда биологические структуры клеток под воздействием окислительной атаки разрушаются. Все это ведет к старению организма — физиологические системы и органы быстрее изнашиваются, накапливается хроническая усталость. Предотвратить преждевременное старение можно, если для питья регулярно использовать правильную воду, близкую по своим свойствам внутренней среде организма.
Правильная вода нормализует окислительно-восстановительный баланс. Она приводит в порядок микрофлору ЖКТ путем стимулирования роста бифидобактерий и лактобактерий и подавляет рост патогенной микрофлоры: золотистого стафилококка, сальмонеллы, возбудителя дизентерия, аспергилл, листерий, клостридий, синегнойной палочки, бактерий, виновных в развитии язвенных болезней. С помощью правильной воды быстро восстанавливается иммунная система.
Отрицательные значения ОВП правильной питьевой воды свидетельствуют о протекании процесса восстановления и наличии свободных электронов. Отрицательно заряженная вода — живая, и именно она дает нашему организму энергию и здоровье.

Показатели измерений параметров некоторых жидкостей:
Свежая талая вода: ОВП = +95, pH = 7.0Водопроводная вода: ОВП = +160 (обычно бывает хуже, до +600 ), рН= 4.0Вода, настоянная на шунгите: ОВП = +250, pH = 6.0Минеральная вода: ОВП= +250, рН= 4.6Кипяченая вода: ОВП = +218,рН=4.5Кипяченная вода, спустя 3 часа: ОВП = +465, рН= 3.7Зеленый чай: ОВП = +55, рН= 4.5Черный чай: ОВП = +83, pH = 3.5 Кофе: ОВП = +70, pH = 5.0Кока-Кола: ОВП=+320, рН= 2.7Вода Корал Майн: ОВП= -150/-200, рН= 7.5/8.3Микрогидрин, H-500: ОВП=-200/-300, рН= 7.5/8.5Айсберг / +150 / 7,0Аквалайн / +170 / 6,0Архыз / +60 / 6,5«Польза» / +165 / 5,5«Ледниковая талая вода» Приэльбрусский заповедник / +130 / 5,5Увинская жемчужина / +119 / 7,3Суздальская вода «серебряный сокол» / +144 / 6,5«Selters» Германия / +200 / 7,0«SРА» Бельгия / +138 / 5,0«Alpica» (в стекле) / +125 / 5,5«Alpica» (в пластике) / +150 / 5,5Ессентуки-Аква / +112 / 6,0«Shudag» премиум / +160 / 5,5«Родники Кавказа» Ессентуки 17 / +120 / 7,5Светлояр / +96 / 6,0«Демидовская плюс» / +60 / 5,5Акваника «Источник победы» / +80 / 6,0«Калипсик» Казахстан / +136 / 5,5«evian» вода Альпийских гор. Франция / +85Аparan / +115 / 6,8Квата / +130 / 6,0«Волжанка» / +125 / 6,0
Вот что поможет сделать живую воду с правильным ОВП
Не знаете где можно взять правильную воду? Я подскажу!
Обратите внимание:
Нажатие на кнопку «Узнать» не ведет к каким-либо финансовым тратам и обязательствам.
Вы лишь получите информацию о доступности правильной воды в Вашем регионе,
а так же получите уникальную возможность бесплатно стать членом клуба здоровых людей
и получить скидку 20% на все предложения + накопительный бонус.

Вступи в международный клуб здоровья Coral Club, получи БЕСПЛАТНО дисконтную карту, возможность участия в акциях, накопительный бонус и другие привилегии!
lifezone.su
Окислительно-восстановительный потенциал коралловой воды. - Cвойства воды. - Все о воде. - Каталог статей
ОВП воды - окислительно-восстановительный потенциал воды. Основными процессами, обеспечивающими жизнедеятельность любого организма, являются окислительно-восстановительные реакции, т.е. реакции, связанные с передачей или присоединением электронов.Во время окислительных или восстановительных реакций изменяется электрический потенциал окисляемого или восстанавливаемого вещества: одно вещество, отдавая свои электроны и заряжаясь положительно, окисляется, другое, приобретая электроны и заряжаясь отрицательно - восстанавливается. Разность электрических потенциалов между ними и есть окислительно-восстановительный потенциал (ОВП).Окислительно-восстановительный потенциал является мерой химической активности элементов или их соединений в обратимых химических процессах, связанных с изменением заряда ионов в растворах.
Значение окислительно-восстановительного потенциала для каждой окислительно-восстановительной реакции может иметь как положительное, так и отрицательное значение.
В природной воде значение ОВП колеблется от -400 до +700 мВ, что определяется всей совокупностью происходящих в ней окислительных и восстановительных процессов. В условиях равновесия значение ОВП определенным образом характеризует водную среду, и его величина позволяет делать некоторые общие выводы о химическом составе воды.
В организме человека энергия, выделяемая в ходе окислительно-восстановительных реакций, расходуется на поддержание гомеостаза (относительное динамическое постоянство состава и свойств внутренней среды и устойчивость основных физиологических функций организма) и регенерацию клеток организма, т.е. на обеспечение процессов жизнедеятельности организма.
ОВП внутренней среды организма человека, измеренный на платиновом электроде относительно хлорсеребряного электрона сравнения, в норме всегда меньше нуля, т.е. имеет отрицательные значения, которые обычно находятся в пределах от -100 до -200 милливольт. ОВП питьевой воды, измеренный таким же способом, практически всегда больше нуля, обычно находится в пределах от +100 до +400 мВ. Это справедливо практически для всех типов питьевой воды - той, которая течет из водопроводных кранов во всех городах мира, которая продается в стеклянных и пластиковых бутылках, которая получается после очистки в установках обратного осмоса и большинства разнообразных больших и малых водоочистительных систем.
Указанные различия ОВП внутренней среды организма человека и питьевой воды означают, что активность электронов во внутренней среде организма человека намного выше, чем активность электронов в питьевой воде.
Активность электронов является важнейшей характеристикой внутренней среды организма, поскольку напрямую связана с фундаментальными процессами жизнедеятельности. Практически все биологически важные системы, определяющие аккумуляцию и потребление энергии, репликацию и передачу наследственных признаков, всевозможные ферментативные системы организма, содержат молекулярные структуры с разделенными зарядами, напряженность электрического поля между которыми достигает 104 - 106 В/см. Исследования последних лет позволили установить, что именно эти поля в значительной мере определяют перенос зарядов в биологических системах и обусловливают селективность и автоконтроль отдельных стадий сложных биохимических превращений, и что ОВП, как показатель активности электронов, оказывает значительное влияние на функциональные свойства электроактивных компонентов биологических систем.
Когда обычная питьевая вода проникает в ткани человеческого (или иного) организма, она отнимает электроны от клеток и тканей, которые состоят из воды на 80-90%. В результате этого биологические структуры организма (клеточные мембраны, органоиды клеток, нуклеиновые кислоты и другие) подвергаются окислительному разрушению. Так организм изнашивается, стареет, жизненно-важные органы теряют свою функцию. Но эти негативные процессы могут быть замедлены, если в организм с питьем и пищей поступает вода, обладающая свойствами внутренней среды организма, т.е. обладающая защитными восстановительными свойствами. Это подтверждается многочисленными исследованиями в специализированных научных центрах в России и за рубежом.
ОВП организмаДля того, чтобы организм оптимальным образом использовал в обменных процессах питьевую воду с положительным значением окислительно-восстановительного потенциала, ее ОВП должен соответствовать значению ОВП внутренней среды организма. Необходимое изменение ОВП воды в организме происходит за счет затраты электрической энергии клеточных мембран, т.е. энергии самого высокого уровня, энергии, которая фактически является конечным продуктом биохимической цепи трансформации питательных веществ.
Количество энергии, затрачиваемой организмом на достижение биосовместимости воды, пропорционально ее количеству и разности ОВП воды и внутренней среды организма.
Если поступающая в организм питьевая вода имеет ОВП близкий к значению ОВП внутренней среды организма человека, то электрическая энергия клеточных мембран (жизненная энергия организма) не расходуется на коррекцию активности электронов воды и вода тотчас же усваивается, поскольку обладает биологической совместимостью по этому параметру. Если питьевая вода имеет ОВП более отрицательный, чем ОВП внутренней среды организма, то она подпитывает его этой энергией, которая используется клетками как энергетический резерв антиоксидантной защиты организма от неблагоприятного влияния внешней среды.
Важно!Коралловый кальций Корал-Майн и микрогидрин делает ОВП воды идеальным для организма!alt="ОВП>
corallinna.com
1.1 Три состояния воды
Вода – одно из самых распространенных на Земле химических соединений[4,10-11]. Она окружает нас повсеместно, даже природные явления, ежедневно наблюдаемые нами – облачность, туман, дождь, снег – всего лишь различные состояния воды жидкое, газообразное и твердое. Ведь облако – это не что иное, как скопление множества мельчайших капель воды или кристалликов льда, которые выпадают в виде осадков – дождя (жидкое состояние воды) или снега (твердое состояние воды). Если рассмотреть снежинку под микроскопом, то можно заметить, что это прекрасное природное произведение искусства создано из очень маленьких ледяных кристаллов. Газообразное состояние воды принято называть паром. В природе понятие влажности воздуха подразумевает содержание количества водяных паров в воздухе (большое содержание паров – повышенная влажность воздуха). При температуре 0°С и ниже и нормальном атмосферном давлении вода переходит в твердое состояние – лед. Лед очень плохо поддается сжиманию, а плотность льда, за счет его молекулярного строения меньше плотности воды, поэтому лед находится на поверхности воды и при температуре 0°С всегда выступает из нее на 1/5 своего объема.
1.2 Окислительно-восстановительный потенциал воды
Учеными установлено, что процесс жизнедеятельности человеческого организма – это совокупность окислительно-восстановительных реакций[9]. Под окислительно-восстановительными реакциями в химии понимают процесс отдачи электронов окисляемого вещества и присоединения их восстанавливаемым. При этом электрические потенциалы и того и другого вещества изменяются: вещество, которое окисляется, отдает свои электроны и приобретает положительный заряд; вещество, которое восстанавливается, присоединяет электроны, получая отрицательный заряд. Разность электрических потенциалов между этими двумя веществами получила название окислительно-восстановительного потенциала (сокращенно ОВП). Иными словами, окислительно-восстановительный потенциал – мера химической активности элементов или их соединений в обратимых химических процессах, которые связаны с изменением зарядов ионов в растворах. ОВП также известен под названием редокс-потенциал, так как на английском языке обозначается как Reduction/Oxidation, обозначается латинскими буквами Eh и имеет размерность милливольт (мВ).
Итак, окислительно-восстановительный потенциал показывает, насколько активно отдаются электроны одного химического вещества и присоединяются другим. Значение ОВП любого химического соединения тем больше, чем больше концентрация компонентов, отдающих свои электроны, по отношению к концентрации компонентов принимающих эти электроны. При проведении специальных измерений, было установлено, что кислород, является самым активным восстановителем и имеет высокий электрический потенциал, а водород – напротив, обладает низким электрическим потенциалом и является ярким представителем элементов с большой восстановительной способностью. Как мы уже знаем, вода – сложное химическое соединение, состоящее из атомов водорода и кислорода, а также других химических элементов, содержащихся в воде в виде примесей. Все эти примеси также обладают различными электрическими потенциалами и выступают менее активными окислителями либо восстановителями. Значение ОВП природной воды находится в пределах от -400 до +700 мВ, такой разбег показаний объясняется наличием в воде различных окислительно-восстановительных реакций. Значение показателя ОВП в некоторой степени характеризует химический состав воды. Значение окислительно-восстановительного потенциала веществ часто используется в биохимии, где оно выражается в условных единицах rH (от английского reduction Hydrogenii). Для перевода единиц rH в милливольты разработана формула Нернста:
rH=(Еh+200)/30+2pH,
где Еh – окислительно-восстановительный потенциал, мВ; рН – показатель кислотно-щелочного равновесия.
Показатели кислотно-щелочного равновесияи окислительно-восстановительного потенциала зависят друг от друга: чем выше значение rH, тем ниже показательрН, то есть при окислении показателькислотно-щелочного равновесияуменьшается, а при восстановлении, напротив, увеличивается.
В результате окислительно-восстановительных реакций, которые постоянно протекают в организме человека, высвобождается энергия, которая впоследствии используется для поддержания гомеостаза. Гомеостаз (в переводе с древнегреческого гомео означает одинаковый, подобный, а стаз – состояние) – это способность организма сохранять относительное динамическое постоянство своего внутреннего состояния путем проведения скоординированных реакций. Другими словами, энергия, полученная в ходе окислительно-восстановительных реакций, расходуется для обеспечения процессов жизнедеятельности организма человека, а также для регенерации его клеток.
Учеными была проведена серия экспериментов, направленная на установление величины окислительно-восстановительного потенциала человеческого организма. Для измерения был использован платиновый электрод, а для сравнения взяли хлорсеребряный электрон. В ходе эксперимента было выяснено, что в нормальном состоянии окислительно-восстановительный потенциал человека колеблется от -100 до -200 милливольт. Таким же способом был измерен и окислительно-восстановительный потенциал употребляемой нами питьевой воды, при это было выявлено, что вода, напротив, всегда имеет положительный ОВП в пределах значений от +100мВ до +400 мВ. При чем не имеет значения, какая вода используется для питья или в пищу: водопроводная, купленная в магазинах в бутылках, очищенная при помощи различных фильтров, или с использованием установок обратного осмоса. То есть, проведенные измерения ОВП человека и воды, позволяют сделать вывод, что активность электронов питьевой воды значительно уступает активности электронов человеческого организма. От активности присутствующих в человеческом организме электронов зависят все процессы обеспечивающие его жизнедеятельность. Известно, что все имеющие биологическое значение системы, которые отвечают за накопление и потребление энергии, репликацию и передачу различных наследственных признаков, а также системы организма, вырабатывающие различные ферменты, содержат определенные молекулярные структуры с разделенными зарядами, между которыми образуется напряженность электрического поля в пределах 104-106 В/см. Эти поля определяют передачу зарядов в биологических системах, что в свою очередь обуславливает осуществления выбора и автоконтроля на некоторых стадиях сложнейших биохимических превращений. Активность электронов, которую и выражает окислительно-восстановительный потенциал, оказывает большое влияние на функциональные свойства электроактивных компонентов биологических систем.
Из-за разности ОВП человеческого организма и питьевой воды, при попадании воды в ткани и клетки организма, происходит окислительная реакция, в результате которой клетки изнашиваются и разрушаются. Можно ли уменьшить или замедлить такое клеточное разрушение организма человека? Это возможно, при условии, что вода, которая поступает в организм, будет иметь свойства внутренней среды, а именно окислительно-восстановительный потенциал воды должен иметь значения соответствующие значениям ОВП человеческого организма. Чем больше разность ОВП человека и воды, тем больше требуется затрат клеточной энергии для достижения соответствия воды и внутренней среды организма. При условии, что ОВП питьевой воды соответствует Окислительно-восстановительный потенциал внутренней среды человека, вода усваивается клетками организма без использования электрической энергии мембран клеток. В случае, если окислительно-восстановительные потенциал воды имеет большее отрицательное значение, нежели ОВП внутренней среды человека, то при ее усвоении выделяется энергия, расходуемая клетками в качестве энергетического запаса антиоксидантной защиты, которая является основным щитом организма от отрицательного влияния, которое оказывает на него окружающая внешняя среда.
studfiles.net
Влияние среды на характер окислительно-восстановительных реакций
В зависимости от рН среды меняется характер протекания окислительно-восстановительного процесса между одними и теми же регентами. Например, взаимодействие восстановителя сульфита натрия (Na2SO3) с окислителем перманганатом калия (KMnO4) в кислотной (рН < 7), нейтральной (pH = 7) и щелочной (pH >7 ) среде приводит к образованию различных продуктов:
Na2SO3 + KMnO4N a2SO4 + MnSO4 + K2SO4 (pH <7)
Na2SO3 + KMnO4 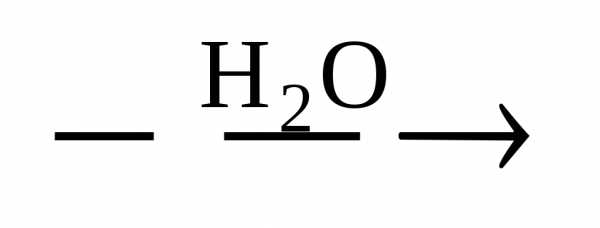 Na2SO4 + MnO2 + KOH (pH =7)
Na2SO4 + MnO2 + KOH (pH =7)
Na2SO3 + KMnO4 Na2SO4 + K2MnO4 + h3O (pH >7)
Na2SO4 + K2MnO4 + h3O (pH >7)
Получение различных продуктов объясняется различным поляризующим действием протона (Н+), полярных молекул воды и гидроксид-аниона (ОН-). Максимальное поляризующее действие оказывает протон: внедряясь в анион MnO4- ослабляет связь между марганцем и кислородом, усиливая действие восстановителя, при этом степень окисления марганца изменяется в большей степени от +7 до +2.
Поляризующее влияние диполей воды слабее, чем у протона, а гидроксид-анионы, имея большой радиус иона и малый заряд, практически не оказывают поляризующего действия.
Влияние рН среды оказывает влияние и на направление окислительно-восстановительной реакции. Так реакция:
3 J2 + 3 h3O 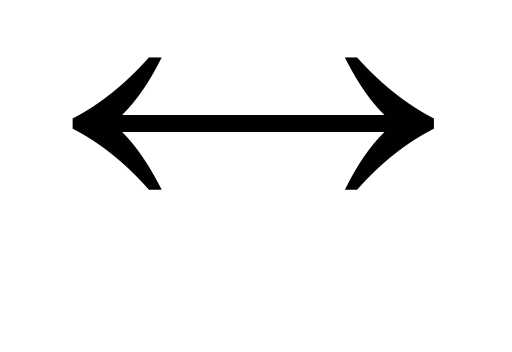 6 H+ + JO-3 + 5 J-
6 H+ + JO-3 + 5 J-
в зависимости от характера среды может протекать как в прямом, так и в обратном направлении. Прибавление к раствору кислоты (понижение рН) вызывает увеличение концентрации ионов Н+ и в соответствии с принципом Ле Шателье смещает равновесие в сторону обратной реакции. Прибавление раствора щелочи (повышение рН) смешает равновесие в направлении прямой реакции.
Направление окислительно-восстановительных реакций
Самопроизвольное протекание окислительно-восстановительной реакции определяется неравенством 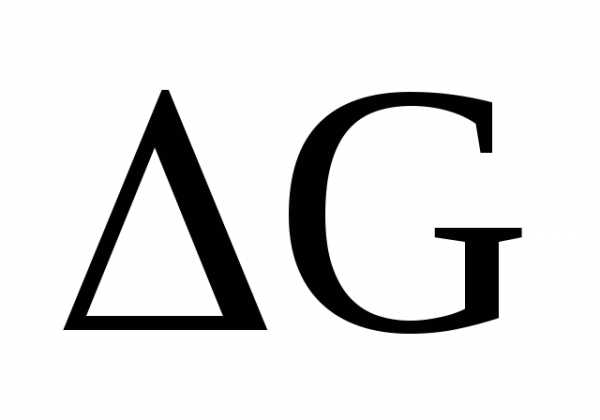 < 0 (
< 0 (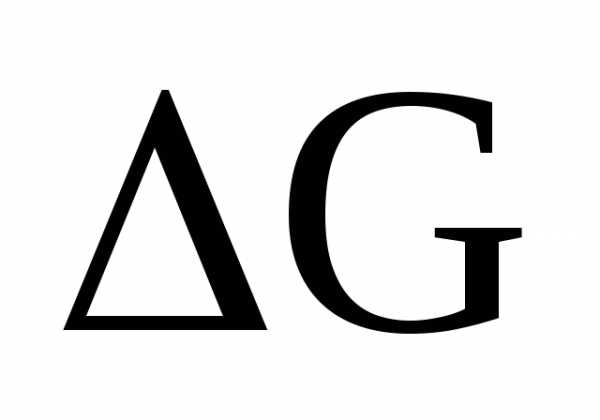 - энергия Гиббса). Если указанная энергия выше нуля (
- энергия Гиббса). Если указанная энергия выше нуля (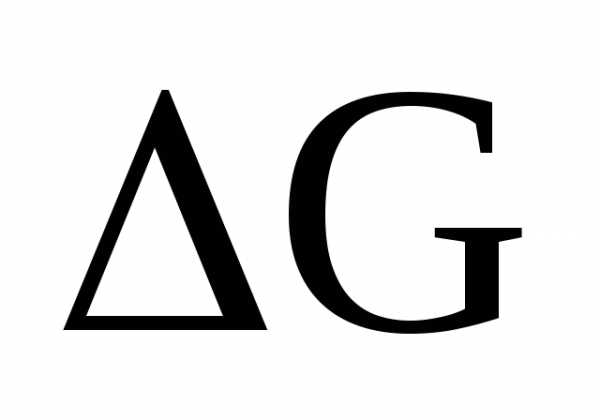 > 0), то прямая реакция в данных условиях невозможна, а возможна лишь обратная реакция. Энергию Гиббса реакции можно рассчитать, зная стандартные значения
> 0), то прямая реакция в данных условиях невозможна, а возможна лишь обратная реакция. Энергию Гиббса реакции можно рассчитать, зная стандартные значения 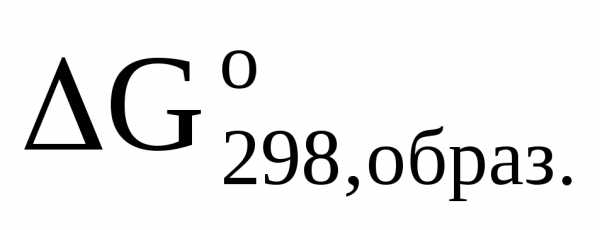 реакций образования продуктов и исходных веществ [3].
реакций образования продуктов и исходных веществ [3].
Рассмотрим для примера направление реакции взаимодействия магния с водой:
Mg(тв) + h3O(ж) 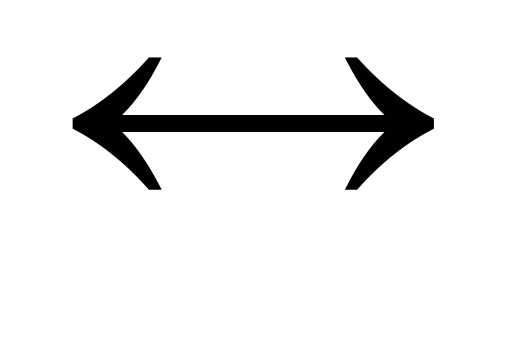 MgO(тв) + h3(г)
MgO(тв) + h3(г)
Выпишем значения  для всех веществ, участвующих в реакции и рассчитаем изменение энергии Гиббса реакции, используя уравнение:
для всех веществ, участвующих в реакции и рассчитаем изменение энергии Гиббса реакции, используя уравнение:
| Вещества | Mg(тв) | h3O(ж) | MgO(тв) | h3(г) |
|
| 0,0 | -237,2 | -569,4 | 0,0 |
Энергия Гиббса реакции при стандартных состояниях равна
–296,2 кДж/моль, т.е. в данных условиях возможно окисление магния водой
Mg + h3O(ж)  MgO + h3(г),
MgO + h3(г),
а обратная реакция окисления водорода оксидом магния невозможна.
2. Электрохимические свойства металлов.
Понятие гальванического элемента
Гальванические элементы состоят из двух электродов, имеющих различный электродный потенциал, электролита, который дает возможность перемещаться ионам от одного электрода к другому, и металлического проводника электронов в результате потока которых может быть получена электрическая энергия постоянного тока.
ЭДС гальванического элемента равна разности равновесных потенциалов положительного электрода (катода) и отрицательного электрода (анода). Если потенциал одного из электродов принять равным нулю, то относительный потенциал второго электрода будет равен ЭДС элемента. Таким образом, можно определить относительный потенциал любого электрода.
Понятие электродного потенциала
Потенциалы металлических электродов. При погружении металла в раствор, содержащий ионы этого металла, устанавливается равновесие:
Ме 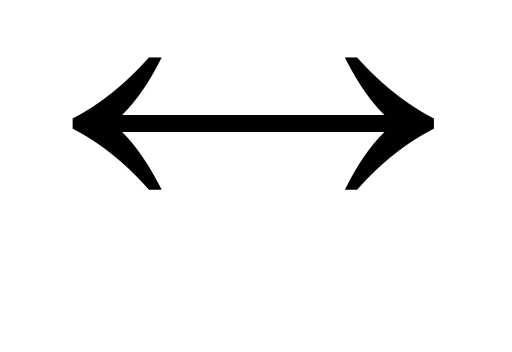 Меn+ + n
Меn+ + n
При равновесии скорость растворения металла равна скорости разряда его ионов. Потенциал, устанавливающийся на электроде при равновесии, называется равновесным потенциалом. Электродный потенциал металла определяют либо экспериментально компенсационным методом, либо вычисляют. Для его измерения составляется гальванический элемент, одним из электродов которого является измеряемый, а вторым – стандартный водородный электрод:
(катод) Pt, h3/2H+II Men+/Me (анод)
р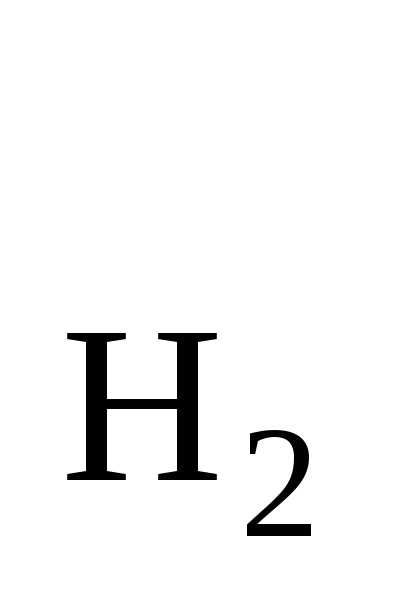 = 1 атм,aH+
= 1 атм,aH+ = 1 моль/л
= 1 моль/л
и измеряется его электродвижущая сила (ЭДС) в условиях обратимой работы элемента (при отсутствии тока в цепи) (рис. 1).
Стандартный водородный электрод. Потенциал стандартного водородного электрода принят равным 0 (Е02Н+/Н2 0,0В). Стандартный водородный электрод состоит из платиновой пластины, покрытой платиновой чернью (мелко раздробленной платиной), контактирующей с газообразным водородом под давлением 1атм и раствором серной кислоты, в котором активность ионов водорода Н+ равна единице (рис. 1).
В водородном электроде происходит реакция, аналогичная реакциям, протекающим на поверхности металлических электродов. Платина здесь играет только роль инертного проводника, а ее поверхностный слой адсорбирует (концентрирует) водород. Адсорбированный водород, взаимодействуя с молекулами воды, переходит в раствор в виде ионов, оставляя на платине электроны.
При этом платина заряжается отрицательно, а раствор – положительно, Возникает скачок потенциала между платиной и раствором. Наряду с переходом ионов в раствор идет обратный процесс восстановления ионов Н+ с образованием молекул водорода.
Равновесие на водородном электроде можно представить в виде
2Н+ + 2
 Н2
Н2
Схематически водородный электрод обозначают 2Н+/Н2, где вертикальная черта обозначает поверхность раздела фаз.
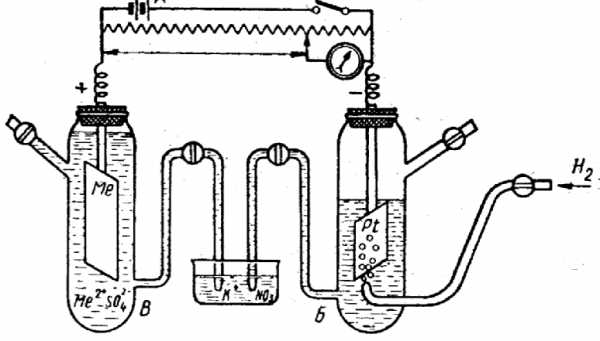
Рис. 1. Ячейка для измерения электродного потенциала металла:
а - аккумулятор; б – стандартный водородный
электрод; в–металлический электрод.
Она равна разности равновесных потенциалов катода и анода ЭДС = (│Ек- Еа│). Так как потенциал стандартного водородного электрода равен нулю (Е02Н /Н
/Н =0), то ЭДС элемента будет равна потенциалу измеряемого электрода.
=0), то ЭДС элемента будет равна потенциалу измеряемого электрода.
Для вычисления электродного потенциала применяют уравнение Нернста:

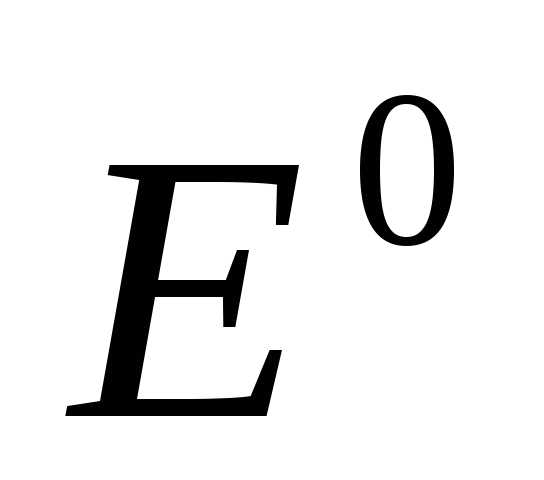 +
+ 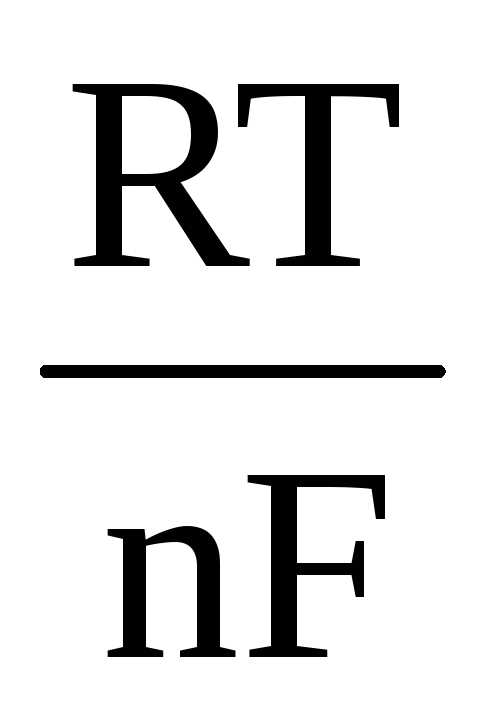 ln
ln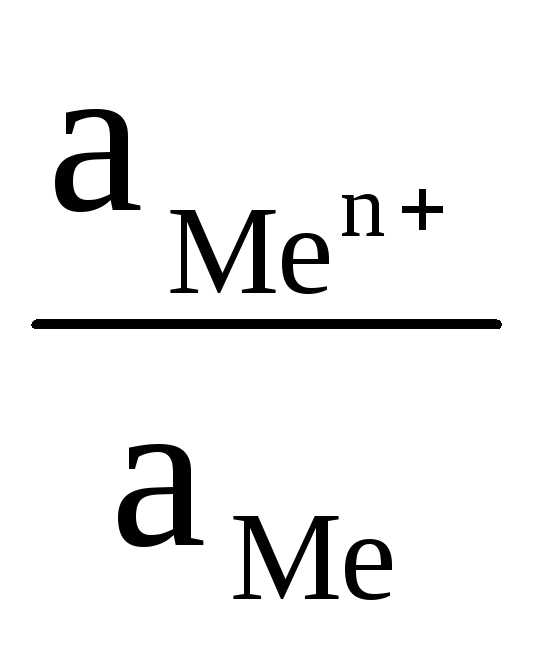 (1) ,
(1) ,
учитывая, что активность твердой фазы постоянна и равна 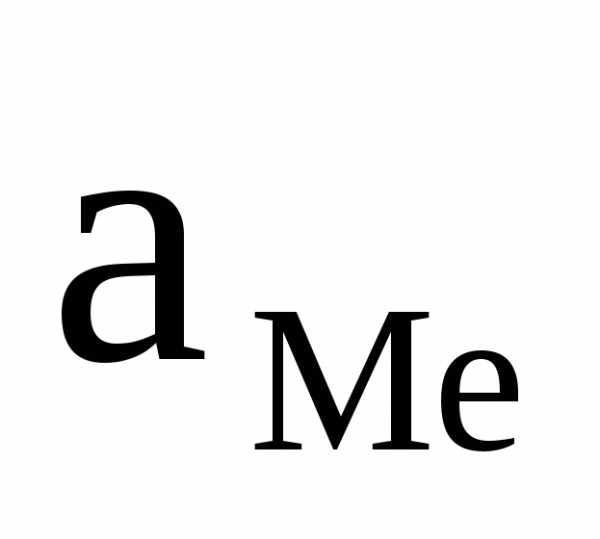 = 1 моль/л, получаем:
= 1 моль/л, получаем:

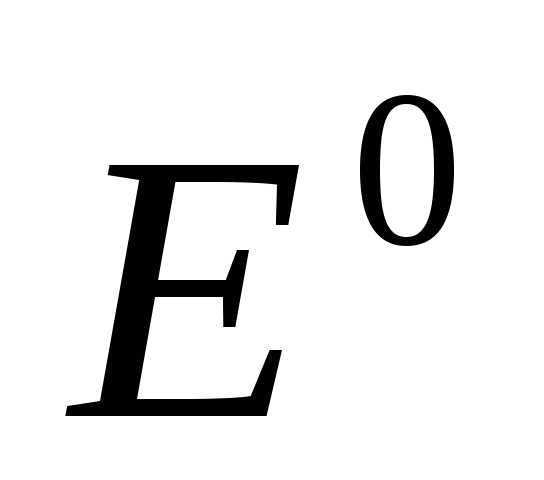 +
+ 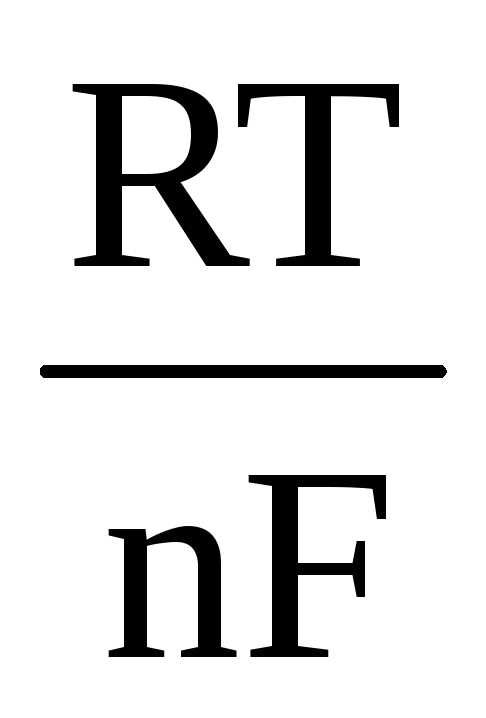 ln
ln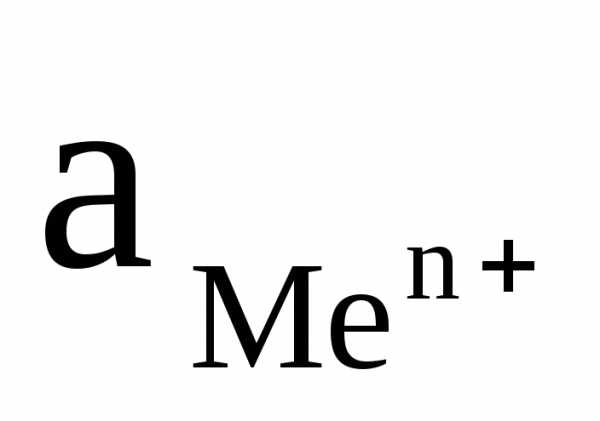 (2),
(2),
где Е0 - стандартный электродный потенциал, В;
R - универсальная газовая постоянная, равная 8,314
Вт-с/моль ∙ К;
Т - температура, К;
n - число электронов, участвующих в электродном про цессе;
F - число Фарадея, равное 96500 Кл/моль;
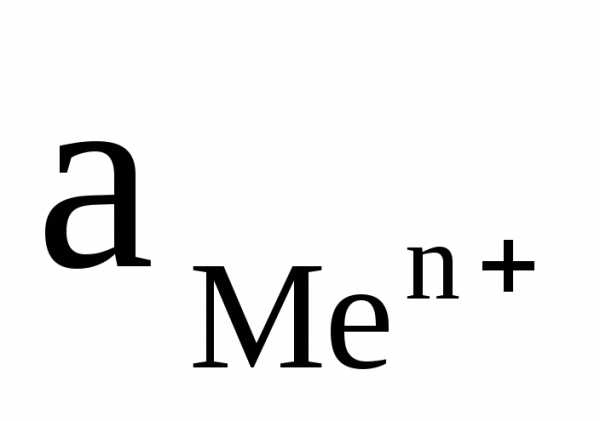 -активность ионов металла, моль/л.
-активность ионов металла, моль/л.
Переходя от натуральных логарифмов к десятичным и подставляя в уравнение Нернста Т = 298 К и соответствующие значения R и F уравнение приобретает более простой вид:

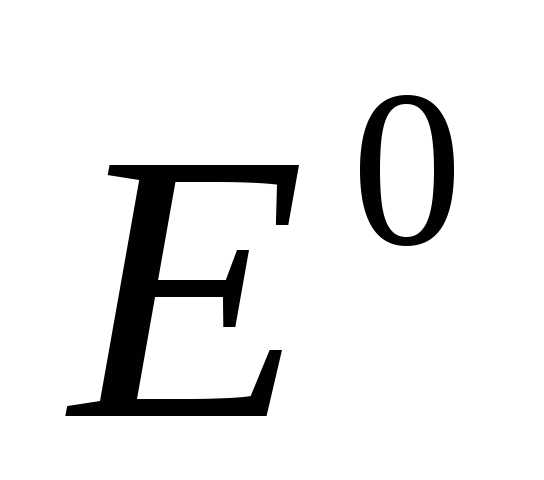 +
+ 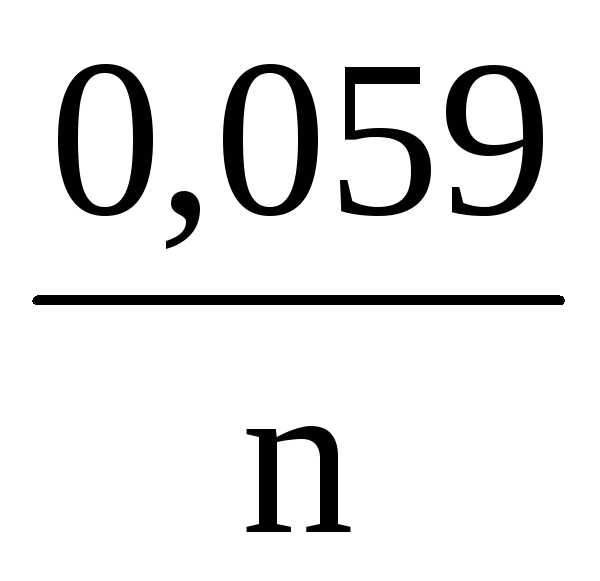
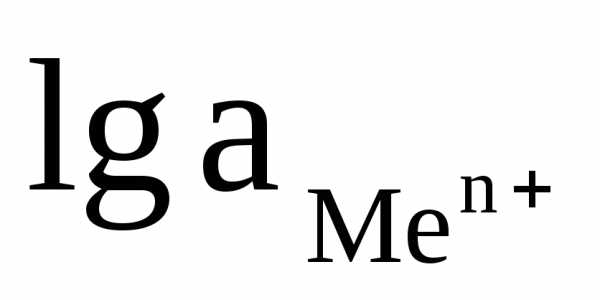 (3)
(3)
Для разбавленных растворов, в которых активности мало отличаются от концентраций (аМе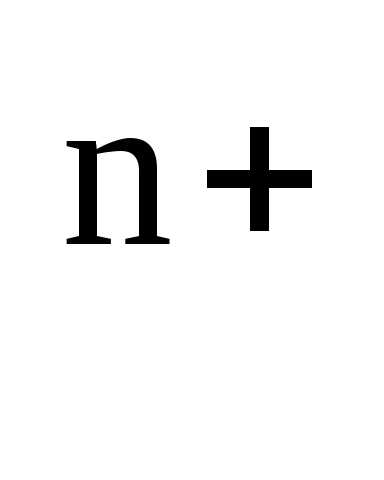
 [Men+]), в уравнении Нернста активность можно заменить концентрацией:
[Men+]), в уравнении Нернста активность можно заменить концентрацией:

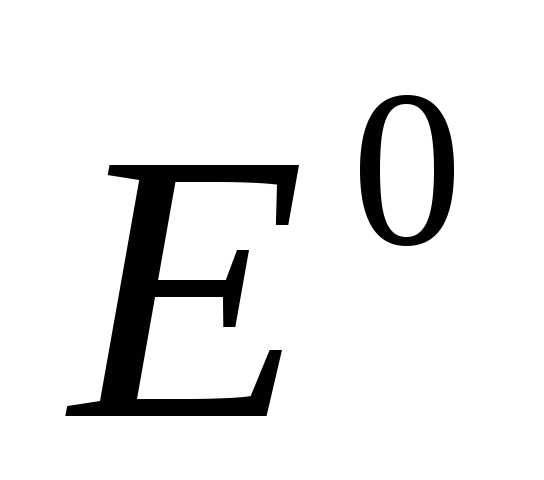 +
+ 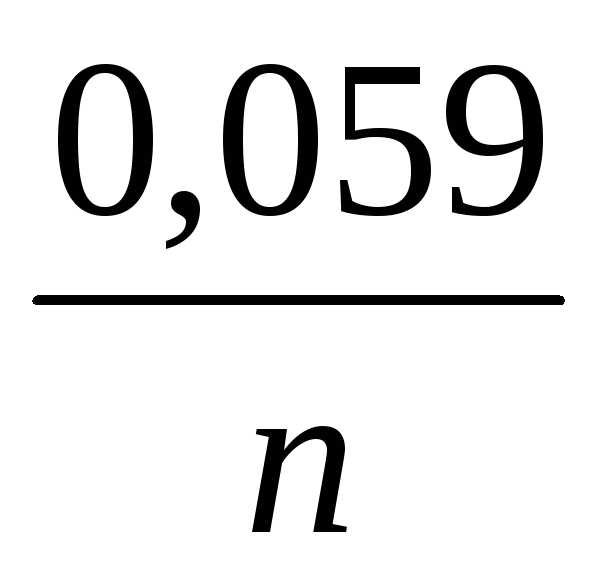
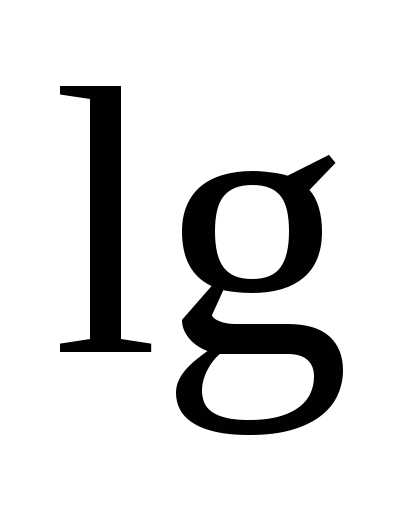 [
[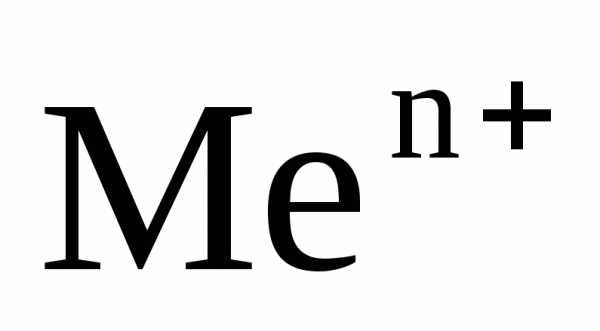 ] (4)
] (4)
Значение стандартного электродного потенциала металлического электрода 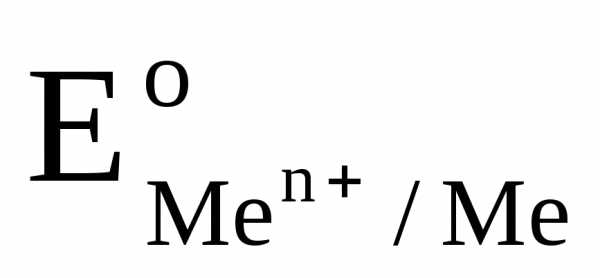 можно определить экспериментально, описанным выше, компенсационным методом при
можно определить экспериментально, описанным выше, компенсационным методом при 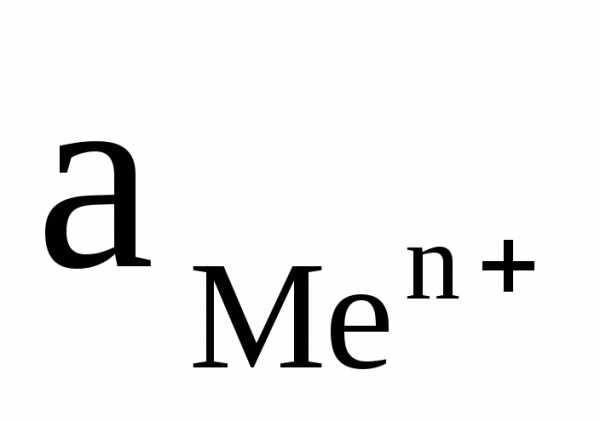 = 1 моль/л..
= 1 моль/л..
Стандартным потенциалом металлического электрода называют потенциал этого электрода в растворе собственных ионов с их активностью, равной 1 моль/л, определенный относительно стандартного водородного электрода.
Ряд стандартных электродных потенциалов (ряд напряжений металлов). Стандартные электродные потенциалы металлов являются мерой окислительно-восстановительной способности металла и его ионов. Металлы в виде простых веществ – восстановители, ионы металлов – окислители.
Знак электродного потенциала характеризует активность металла относительно водорода. Металлы имеют электродные потенциалы со знаком "минус", если их активность выше активности водорода и "плюс", если они менее активны, чем водород.
Активные металлы начала ряда, а также щелочные и щелочно-земельные вытесняют водород из воды. Например, 2K + 2h3O  2KOH + h3
2KOH + h3 .
.
Металлы, расположенные между магнием и кадмием, обычно не вытесняют водород из воды. На поверхности этих металлов образуются оксидные пленки, обладающие защитным действием.
Все металлы, стоящие в ряду стандартных электродных потенциалов до водорода, вытесняют его из растворов кислот с концентрацией (активностью) ионов водорода 1 моль/л. Например, Zn + HCl  ZnCl2 + h3
ZnCl2 + h3 .
.
Если электродный потенциал металла имеет положительный знак, то металл является окислителем по отношению к водороду и не вытесняет его из растворов кислот с концентрацией ионов водорода 1 моль/л.
Металлы способны вытеснять друг друга из растворов солей. Направление реакции определяется при этом их взаимным положением в ряду напряжений. Рассматривая конкретные случаи таких реакций, следует помнить, что активные металлы вытесняют водород не только из воды, но и из любого водного раствора. Поэтому взаимное вытеснение металлов из растворов их солей практически происходит лишь в случае металлов, расположенных в ряду после магния. Например, Zn + CuSO4  ZnSO4 +Cu.
ZnSO4 +Cu.
Л И Т Е Р А Т У Р А
Глинка Н.Л. Общая химия. М: Интеграл-Пресс, 2002, гл.9 §§ 9.1-9.3.
Коровин Н.В. Общая химия. М: Высшая школа, 2002, гл.9 § 9.1.
Болячевская К.И., Полякова Е.В. Справочные материалы по общему и элективным курсам (под редакцией проф. И.М.Паписова), М., МАДИ (ГТУ), 2004.
14
studfiles.net

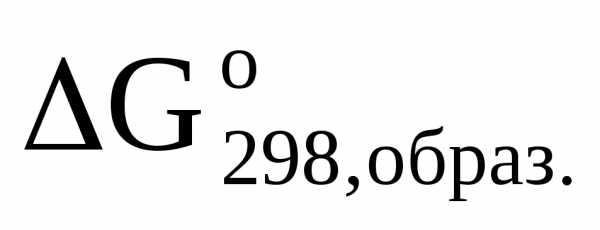 ,кДж/моль
,кДж/моль