Что представляет собой сухой остаток. Норма сухой остаток в воде
Что представляет собой сухой остаток
Сухой остаток является одним из основных критериев определения качества воды, который выявляет степень ее минерализации. Для определения типа воды используется ионно-солевой остаток.

Особенности остатка
В качестве основных ионов, благодаря которым можно определить сухой остаток, выступают: сульфаты, хлориды, карбонаты, нитраты, бикарбонаты. Существует их подразделение на органические и минеральные остатки, которые отличаются температурами кипения. Сухой остаток подразумевает наличие в воде растворенных нелетучих твердых веществ. Существует специальная методика его вычисления.

Гравиметрический расчетный метод
С его помощью осуществляется определение сухого остатка в исследуемой пробе. Для проведения подобного исследования необходимо провести фильтрование пробы, отделить ее от органических примесей.
Воду используют почти во всех отраслях современного производства. Например, в косметической промышленности ее используют в качестве питьевой воды, как сырье для создания полуфабрикатов, как вещество для мытья промышленной тары.
Именно с водой связаны органолептические показатели продукции, выпускаемые на предприятии: стабильность, запах, вкус, цвет. К примеру, внешний вид и вкус сиропов напрямую связаны с минеральными веществами, содержащимися в воде. Если сухой остаток содержит хлорид натрия, в таком случае вода приобретает некоторый соленый вкус.

Санитарные нормы
Существуют определенные нормативы, которым должна соответствовать вода. Если содержание сухого остатка им не удовлетворяет, в таком случае ее нельзя использовать. Существуют специальные физико-химические лаборатории, которые оснащены специальными измерительными приборами.
В них массовая доля сухого остатка определяется по ГОСТу «Вода питьевая» 18164-72. Используют воду в производстве лишь после того, как будет проведен полный контроль ее на соответствие всем показателям качества.
Если в ходе исследований будут выявлены несоответствия по каким-либо показателям, необходимо составить протокол о несоответствии, выполняют необходимые корректирующие мероприятия.

Методы определения сухого остатка
Существует несколько методик, позволяющих определять сухой остаток. ГОСТ допускает процедуру с добавлением соды либо с использованием соли. Рассмотрим оба варианта более подробно.
В первом случае происходит выпаривание пробы с использованием водяной бани. Сначала емкость, которую будут использовать для выпаривания, высушивают до получения постоянной массы. Далее в фарфоровую емкость наливают отфильтрованную воду. После завершения выпаривания последней пробы, чашка высушивается в термостате до постоянной массы при температуре.
Для определения сухого остатка используется специальная формула. Она связывает между собой массу пустой емкости, с сухим остатком, а также количество воды, которая взята для исследования.
Применение этого метода приводит к получению завышенных результатов. Подобная ситуация объясняется повышенной гигроскопичностью, а также протеканием гидролиза хлорида кальция и магния, сложностью передачи воды сульфатами кальция и магния.
Для устранения подобного недостатка осуществляется добавление к испытуемому образцу чистого карбоната натрия. В процессе добавления хлоридов кальция и магния происходит их переход в безводные карбонаты. Для полного удаления кристаллизационной воды, выполняют сушку полученного сухого остатка при повышенной температуре до тех пор, пока не будет получена постоянная масса в термостате.
Методика с применением раствора соды
Данный вариант предполагает предварительное фильтрование воды с применением бумажного фильтра. После высушивания пробы до получения постоянной массы, чашку нужно поставить на водяную баню. Здесь проводится выпаривание проб воды, отобранных для анализа. Как только будет внесена последняя порция воды, вносят пипеткой раствор углекислого газа. Учитывая, что вес взятой соды относится к массе сухого остатка как 2 к 1, проводят математические расчеты.
Чтобы проводить дальнейшее выпаривание, необходимо перемешивать пробу, разрушая при этом образующуюся корку. Для перемешивания применяют стеклянную палочку. Далее обмывают дистиллированной водой палочку. Потом образующийся сухой остаток с содой в чашке размещают в термостате, сушат его при температуре порядка 150 градусов по Цельсию до получения постоянной массы.
Средняя продолжительность выпаривания составляет от двух до пяти часов. Определяют разность по весу между емкостью образованного осадка и начальным весом чашки и соды. Данная разность определяет количество сухого остатка в определяемом количестве воды. Определяют сухой остаток по формуле, связывающей массу пустой емкости, добавленной соды, а также объем воды, выбранный для анализа.
Данный анализ с гигиенической точки зрения заключается в том, что можно провести технически корректировку анализируемой воды, воспользовавшись системами фильтрации, понижая при этом степень минерализации.
Заключение
Вкус считается сбалансированным, если в воде общее содержание соли составляет 600 мг на один литр. Если в ней содержится больше 1 г/л, она считается непригодной для питья, поскольку обладает горько-соленым вкусом.
Если постоянно употреблять такую воду, в организме могут возникнуть серьезные физиологические проблемы. В первую очередь происходит усиление моторной и секретной функции кишечника и желудка, при повышенной температуре организм перегревается.
fb.ru
Что такое сухой остаток в воде
Поделиться материалом в социальных сетях и мессенджерах:
О том, какого качества жидкость, можно судить, определив сухой остаток в воде, показывающий насколько она минерализована. Тип воды определяется посредством ионно-солевого остатка. Остановимся на этом более подробно.
Что показывает сухой остаток воды
Сухой остаток в воде говорит о том, что в воде имеются растворенные органические и минеральные соединения, которые закипают по достижении водой температуры более +105… +110 °С. Для выявления наличия и характера сухого остатка используются гравиметрические расчетные способы. Для установления его типа образец воды отфильтровывается либо отстаивается, пока сухая смесь не отделится в качестве взвешенных частиц.
Сухой остаток в основном выявляют, подвергнув природную воду нагреву до +103… +105 °С. Для более детального и скрупулезного изучения свойств природной и сточной воды ее высушивают, нагревая до температуры +178… +182 °С.
Особенно широко в природной воде распространены анионы НСО3, СО3 и катионы Na+, K+, Ca2+, Mg2+, H+. В зависимости от того, какие анионы или группы анионов преобладают в воде, ее можно разделить на три основных класса:
Вкусовые качества воды напрямую зависят от ее химического и минерального состава. От него зависит также частота инфекционных заболеваний в районе. На сегодняшний день вопрос о том, каким образом минерализованная вода влияет на человеческий организм, стал очень актуален, что явилось основанием для увеличения объема исследований в этой сфере. Эта тенденция связана с тем, что многие страны сталкиваются с дефицитом пресной воды.
В связи с появлением и развитием технологий, позволяющих изменять электролитный состав питьевой воды, его изучению в настоящее время уделяется значительное внимание. На данный момент недостаточно изучено, каким образом минерализованная вода влияет на организм человека, какое значение при этом имеет ее электролитный состав.
Высокоминерализованная вода не способствует утолению жажды, поскольку при попадании в организм значительного количества минералов, непосредственно количество воды в организме, в том числе в плазме крови, уменьшается. Потеря организмом воды даже в самой малой степени может увеличить давление плазмы крови, а также привести к раздражению рецепторов сосудов, что вызовет возбуждение определенных зон головного мозга – центров жажды.
Для утоления потребности в воде достаточно прекратить раздражение осморецепторов, а, следовательно, привести в норму осмотическое давление в плазме крови. С этой целью следует употреблять воду с низким уровнем содержания минералов, являющейся гипотонической по отношению к клеткам крови и межтканевой жидкости.
Какое влияние оказывает на организм сухой остаток в воде
В процессе изучения ионно-солевого состава сухого остатка воды, ученые выяснили, что различные степени остатка оказывают разное влияние на человеческий организм.
Исследования, проводимые как в отношении лабораторных животных, так и в отношении добровольцев показали, что высокоминерализованная вода способна оказать отрицательное воздействие на человека. Употребление такой воды может вызывать расстройство метаболических и биохимических процессов, кроме того, приводит к нарушениям как на морфологическом, так и на функциональном уровне.
То есть, если употреблять воду, содержание сухого остатка в которой превышает 1000 мг/л, велика вероятность нарушения гидрофильности тканей организма, задержки в организме воды, значительного сокращения мочеиспускания. В результате этих процессов повышается нагрузка на сердце и сосуды, обостряются хронические заболевания, такие как ишемическая болезнь, миокардиодистрофия, стенокардия, гипертоническая болезнь, что увеличивает риск развития инфаркта и прочих неблагоприятных последствий.
Употребляя сильно минерализованную воду, человек может испытать диспепсическое расстройство. Особенно остро ощущают смену воды люди, изменившие регион проживания. Это связано с высоким содержанием в жидкости солей магния, которые, раздражая слизистые оболочки кишечника, стимулируют перистальтические процессы.
Употребление такой воды способно изменять секрецию и моторную функцию желудка. А если пить ее в течение длительного времени и в больших количествах – может вызвать мочекаменную или желчекаменную болезни.
Однако стоит иметь в виду, что и вода с очень низким содержанием минералов (величина сухого остатка менее 100 мг/л) имеет неприятный вкус и может представлять опасность для здоровья при длительном употреблении. В такой воде содержится очень мало кальция и магния, что влечет риск возникновения сердечно-сосудистых заболеваний, а также негативно сказывается на состоянии и развитии опорно-двигательного аппарата.

Допустимое количество сухого остатка в питьевой воде
Употребляемая вода должна соответствовать определенным нормативам. В случае, если содержание сухого остатка выше или ниже, вода непригодна для использования. Измерение количества сухого остатка в воде производится при помощи специальных измерительных приборов в физико-химических лабораториях.
Для того чтобы вода была пригодна для использования, содержащийся в ней сухой остаток должен соответствовать требованиям ГОСТа «Вода питьевая» 18164-72. Применение воды в производстве возможно после проведения ее полного анализа. Если исследование покажет, что какие-либо показатели воды не отвечают требованиям, в этом случае составляется протокол несоответствия, выполняются необходимые мероприятия по коррекции показателей.
Вода, в которой содержание сухого остатка не превышает 1000 мг/л, называется пресной, в большинстве рек, пресных озер и водохранилищ содержится именно такая вода. При минерализации от 1000 до 3000 мг/л вода имеет солоноватый вкус. В случае, когда сухой остаток в воде превышает 3000 мг/л, вода будет сильносоленой на вкус, она свойственна океанам и морям.
Оптимальная степень минерализации воды составляет 300–500 мг/л. Вода, сухой остаток которой составляет 100–300 мг/л, расценивается как удовлетворительная, показатели 500–1000 мг/л считаются завышенными, но вода пригодна для употребления. Следует иметь в виду, что при использовании воды со степенью минерализации 1000 мг/л и выше можно серьезно ухудшить состояние здоровья. По этой причине питьевой считается та, сухой остаток в которой не превышает 1000 мг/л.
В то же время сухой остаток воды в водоемах, предназначенных для хозяйственно-питьевых и культурно-бытовых нужд, не должен превышать 1000–1500 мг/л.
Определение сухого остатка в сточных водах
Для оценки состава и свойств сточной воды проводят санитарно-химический анализ, включающий, помимо стандартных химических тестов, ряд параметров, определяющих физические, физико-химические и санитарно-бактериологические показатели.
Состав сточной воды достаточно сложен, проводимые исследования не позволяют определить каждое из загрязняющих веществ, в связи с этим возникла необходимость выбирать показатели, с помощью которых можно было бы охарактеризовать те или иные свойства воды, не идентифицируя отдельные вещества. Название этих данных – групповые или суммарные. Так, определив органолептические показатели (запах, цвет), нет дальнейшей необходимости определять количественные степени веществ, способных придавать воде цвет и запах.
При помощи полного санитарно-химического анализа можно определить следующие данные: температуру, окраску, наличие запаха, степень прозрачности, величину рН, количество сухого остатка, его плотность и потерю в процессе накаливания, количество взвеси, объем и массу оседающих веществ, степень перманганатной окисляемости, химическую и биохимическую потребности в кислороде (ХПК и БПК соответственно), уровень азота (общего, аммонийного, нитритного, нитратного), фосфатов, хлоридов, сульфатов, тяжелых металлов и других токсичных элементов, количество поверхностно-активных веществ, нефтепродуктов, растворенного кислорода, микробов, бактерий группы кишечной палочки (БГКП), яиц гельминтов.
Помимо указанных показателей, к обязательным тестам для определения полного санитарно-химического исследования на городских очистных станциях могут быть отнесены тесты, определяющие специфические примеси, которые поступают в канализационные сети населенных пунктов с производственных предприятий.
Анализ сухого остатка позволяет установить степень общей загрязненности сточной воды органическими и минеральными веществами, находящимися в различных агрегативных состояниях (в мг/л). Выпаривание и дальнейшее высушивание образца сточных вод при температуре +105 °С поможет установить необходимые показатели. Далее остаток прокаливается при температуре +600 °C, в результате чего можно определить его зольность. Эти показатели позволяют выявить соотношение органической и минеральной частей загрязнений в сухом остатке.
Метод определения сухого остатка в воде
Метод № 1. Без использования соды
Способ состоит в том, что образец выпаривается посредством водяной бани.
Чаша, предназначенная для выпаривания образца, высушивается до достижения постоянной массы. В фарфоровую чашу заливают фильтрованную воду объемом около 200–500 см3. После того как последняя проба воды выпарена, чаша с содержащимся в ней остатком высушивается при +110 °С в термостате постоянной массы.
Для вычисления количественного показателя сухого остатка (Х), мг/дм3 используется следующая формула:

где m – масса емкости с сухим остатком, мг;
m1 – масса пустой емкости, мг;
V – объем воды, взятой для испытания, см3.
Однако, в связи с высокой способностью поглощения водяных паров и гидролизом хлоридов магния и кальция, трудностей при передаче воды сульфатами магния и кальция, велика вероятность при проведении данного анализа получить завышенные результаты. Для исправления ситуации в испытуемый образец добавляют чистый карбонат натрия. В этом случае хлориды магния и кальция преобразуются в безводные карбонаты. С целью полного выпаривания кристаллизационной воды образовавшийся остаток подвергается высушиванию при +160… +180 °С до достижения постоянной массы в термостате.
Метод 2. Применяется раствор соды
Воду необходимо заранее отфильтровать, используя бумажные фильтры. В емкости, высушенной до постоянной массы, на водяной бане выпарить отобранные для анализа 200–500 см3 воды. После того как внесли заключительную порцию воды, при помощи пипетки добавляют 1%-ный раствор кальцинированной соды из расчета, чтобы вес соды в 2 раза превышал вес сухого остатка, предполагаемого к получению.
В случае если возникает необходимость последующего выпаривания, содержимое чаши время от времени перемешивают при помощи стеклянной палочки для разрушения образовывающейся корочки. Палочка промывается в дистиллированной воде. После этого образовавшийся сухой остаток с натрием углекислым в чаше необходимо поместить в емкость термостата и высушить при +150 °С до получения постоянной массы. Образец воды сушится в течение 2–5 часов.
Объем сухого остатка в пробе воды составляет разницу в весе между чашей с образовавшимся сухим остатком и первоначальным весом соды и емкости (в 1 см3 содового раствора содержится 10 мг Na2CO3).
Сухой остаток (Х), мг/дм3, вычисляют по формуле:

где m – масса емкости с сухим остатком, мг;
m1 – масса пустой емкости, мг;
m2 – масса добавленной соды, мг;
V – объем воды, необходимой для испытания, см3.
Практическое использование полученных показателей состоит в технической возможности корректировать используемую воду (при помощи системы фильтров), понижая степень ее минерализации.
На российском рынке присутствует немало компаний, которые занимаются разработкой систем водоочистки. Самостоятельно, без помощи профессионала, выбрать тот или иной вид фильтра воды довольно сложно. И уж тем более не стоит пытаться смонтировать систему водоочистки самостоятельно, даже если вы прочитали несколько статей в Интернете и вам кажется, что вы во всем разобрались.
Надежнее обратиться в компанию по установке фильтров, которая предоставляет полный спектр услуг – консультацию специалиста, анализ воды из скважины или колодца, подбор подходящего оборудования, доставку и подключение системы. Кроме того, важно, чтобы компания предоставляла и сервисное обслуживание фильтров.
Наша компания Biokit предлагает широкий выбор систем обратного осмоса, фильтры для воды и другое оборудование, способное вернуть воде из-под крана ее естественные характеристики.
Специалисты нашей компании готовы помочь вам:
-
подключить систему фильтрации самостоятельно;
-
разобраться с процессом выбора фильтров для воды;
-
подобрать сменные материалы;
-
устранить неполадки или решить проблемы с привлечением специалистов-монтажников;
-
найти ответы на интересующие вопросы в телефонном режиме.
Доверьте очистку воды системам от Biokit – пусть ваша семья будет здоровой!
Поделиться:
Вконтакте
Одноклассники
Google+
biokit.ru
Определение сухого остатка
Сухой остаток — масса высушенного вещества, остающегося после выпаривания 1 дм3 воды. Сухой остаток характеризует общее содержание примесей воды как растворенных, так и взвешенных, без газов и летучих веществ.
Проведение анализа. В предварительно взвешенную фарфоровую чашку диаметром около 10 см и помещенную на водяную баню постепенно приливают 500 см3 исследуемой воды и выпаривают. Водяную баню лучше наполнять дистиллированной водой во избежание попадания в чашку осадка с брызгами кипящей воды.
После выпаривания чашку с осадком высушивают в сушильном шкафу при 105 – 110 оС до постоянной массы и после охлаждения в эксикаторе взвешивают. Для вычисления сухого остатка в 1 дм3 воды найденную массу осадка умножают на 2.
Пример. Масса высушенного осадка в чашке после выпаривания 500 см3 воды равна 0,2120 г, или 212 мг. Следовательно, содержание сухого остатка равно 424 мг/ дм3 .
Определение величины окисляемости
Окисляемость – величина, характеризующая содержание в воде органических и минеральных веществ, окисляемых (при определенных условиях) одним из сильных химических окислителей. Выражается этот параметр в миллиграммах кислорода, пошедшего на окисление этих веществ, содержащихся в 1 дм3 воды.
Различают несколько видов окисляемости воды: перманганатную, бихроматную, иодатную, цериевую. Наиболее высокая степень окисления достигается бихроматным и иодатным методами. В практике водоочистки для природных малозагрязненных вод определяют перманганатную окисляемость, а в более загрязненных водах – как правило, бихроматную окисляемость (называемую также ХПК – «химическое потребление кислорода»).
Окисляемость является очень удобным комплексным параметром, позволяющим оценить общее загрязнение воды органическими веществами.
Величина окисляемости природных вод может варьироваться в широких пределах от долей миллиграммов до десятков миллиграммов О2 на литр воды. Поверхностные воды имеют более высокую окисляемость (а значит и более высокое содержание органических веществ) по сравнению с подземными. Так, горные реки и озера характеризуются окисляемостью 2…3 мг О2/дм3, реки равнинные – 5…12 мг О2 /дм3, реки с болотным питанием – десятки миллиграммов О2 /дм3. Подземные же воды имеют в среднем окисляемость на уровне от сотых до десятых долей мг О2 /дм3 (исключения составляют воды в районах нефтегазовых месторождений, торфянников, в сильно заболоченных местностях).
В водоемах и водотоках, подверженных сильному воздействию хозяйственной деятельности человека, бихроматная окисляемость (ХПК) используется в качестве меры содержания органического вещества в пробе воды.
В соответствии с требованиями к составу и свойствам воды водоемов у пунктов питьевого водопользования величина ХПК не должна превышать 15 мг О2/дм3.
При анализе питьевой воды обычно определяют перманганатную окисляемость. В основе метода перманганатной окисляемости лежат следующие реакции.
Перманганат калия (КМпО4), будучи сильным окислителем, реагирует в кислой среде с восстановителями. В анализируемую воду перманганат калия вводят в виде 0,01 моль/дм3. раствора с некоторым избытком. Для учета его количества, пошедшего на окисление примесей воды, в реакционную смесь вводят такой же объем 0,01 моль/дм3 раствора щавелевой кислоты. Не вступившую в реакцию щавелевую кислоту оттитровывают перманганатом калия и по результату титрования вычисляют окисляемость воды. Окисляемость выражают либо в миллиграммах перманганата калия, либо в миллиграммах кислорода, расходуемых на окисление примесей в 1 дм3 воды.
Проведение анализа. В коническую колбу вместимостью 250 см3 наливают 100 см3 анализируемой воды, 5 см3 серной кислоты, разбавленной водой в соотношении 1 : 3, 10см3 0,01 моль/дм3 раствора перманганата и вносят несколько стеклянных шариков или капилляров. Закрыв колбу часовым стеклом, ее содержимое за 5 мин подогревают до кипения и кипятят 10 мин. К горячему раствору добавляют 6 см3 0,01 моль/дм3 раствора щавелевой кислоты и размешивают его вращением колбы. Обесцветившийся горячий раствор титруют 0,01 моль/дм3 раствором перманганата калия до появления слабо-розового окрашивания. Температура раствора не должна падать ниже 80 оС. Израсходованное на титрование количество перманганата равно количеству его, пошедшему на окисление примесей воды. Если раствор при кипячении обесцветится или побуреет, определение повторяют с разбавленной пробой воды и одновременно ставят холостой опыт с водой, взятой для разбавления. Для холостого опыта в коническую колбу отмеривают 100 см3 дистиллированной воды и ведут определение окисляемости так же, как и в исследуемой воде. Определение окисляемости с предварительным разбавлением анализируемой воды повторяют также и тогда, когда расход перманганата на титрование составляет более 6 см3.
В конце определения окисляемости рекомендуется проверить молярную концентрацию раствора перманганата по щавелевой кислоте. Для этого в горячий раствор после титрования вносят 10 см3 0,01 моль/дм3 щавелевой кислоты и титруют перманганатом калия до появления розового окрашивания. Коэффициент нормальности перманганата вычисляют из уравнения:
K · V = 0,01 · 10,
где V - объем перманганата, пошедшего на титрование, см3.
Окисляемость воды Ок, мг кислорода на 1 дм3 воды,
Ок = 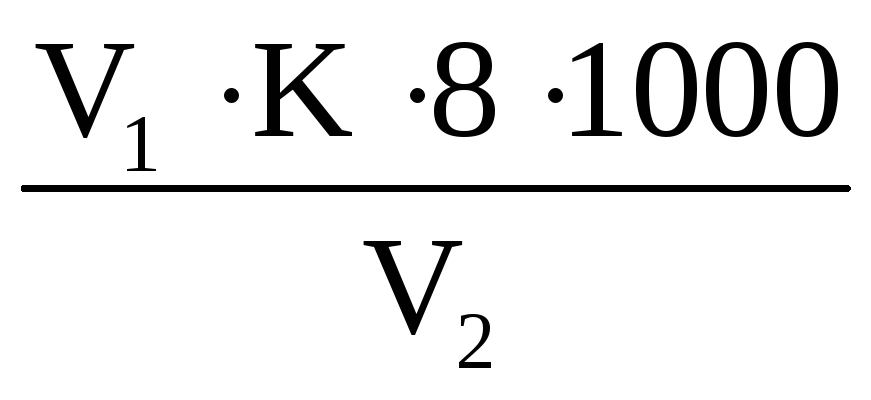 ,
,
где V1 – объем раствора перманганата, пошедшего на титрование пробы с исследуемой водой, см3; V2 – объем пробы исследуемой воды, см3; 8 – объем кислорода, эквивалентный 1 см3 нормального раствора перманганата, см3; К – коэффициент молярной концентрации перманганата.
При разбавлении пробы исследуемой воды из величины V1 вычитают объем перманганата, расходуемого на окисление пробы воды, взятой для разбавления.
О степени загрязненности воды органическими примесями по ее окисляемости можно судить только в том случае, если учесть влияние на окисляемость неорганических восстановителей. Для этого при наличии в воде железа, сероводорода, нитритов их определяют отдельно, а результат, пересчитанный на окисляемость, вычитают из величины окисляемости воды. Пересчет производят, руководствуясь тем, что 1 мг h3S соответствует 0,47 мг, 1 мг NO2 — 0,35 мг, а 1 мг Fe2+ — 0,14 мг кислорода. Влияние хлоридов на окисляемость обычно устраняют добавлением к анализируемой пробе воды 0,4 г сульфата ртути.
Пример. Вода для определения окисляемости разбавлена дистиллированной водой вдвое. На титрование пробы исследуемой воды пошло 2 см3 перманганата. На титрование холостой пробы израсходовано 0,2 см3 перманганата. Так как в пробе разбавленной воды содержится 50 см3 дистиллированной, то для окисления содержащихся в ней примесей потребуется 0,1 см3 перманганата. При проверке нормальности рабочего раствора израсходовано 10,2 см3 перманганата. Следовательно, коэффициент его молярной концентрации равен:
К =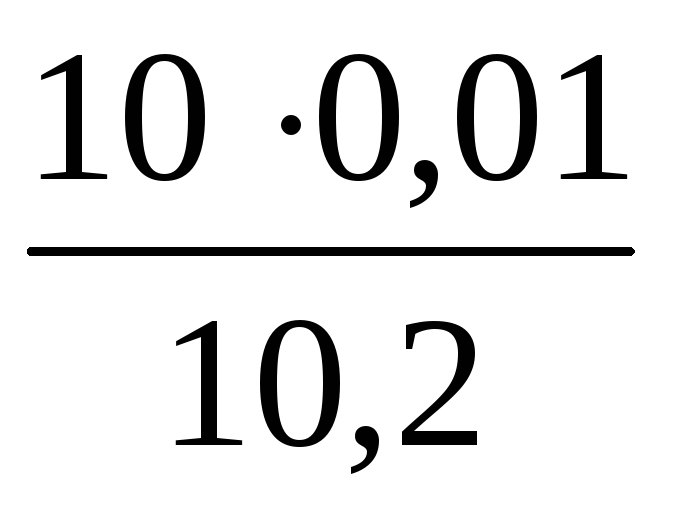 =0,0098,
=0,0098,
а окисляемость воды:
Ок = 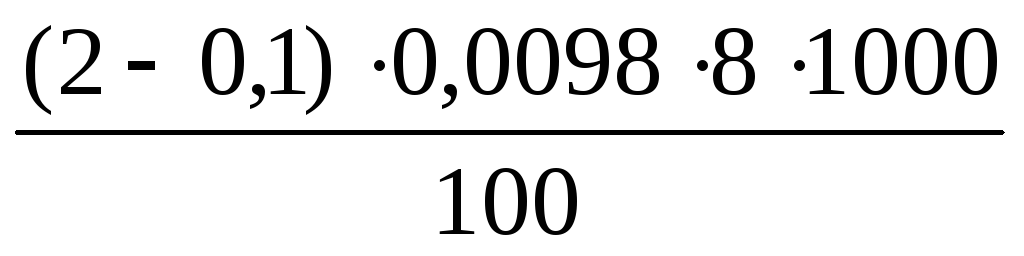 =1,49 мг О2/дм3
=1,49 мг О2/дм3
studfiles.net
ПНД Ф 14.1:2:4.261-10 ФР 1.31.2005.01523 Количественный химический анализ вод. Методика выполнения измерений массовой концентрации сухого и прокаленного остатков в пробах питьевых, природных и сточных вод гравиметрическим методом / 14 1 2 4 261 10 1 31 2005 01523
ФЕДЕРАЛЬНАЯ СЛУЖБА ПО НАДЗОРУ В СФЕРЕ ПРИРОДОПОЛЬЗОВАНИЯ
|
УТВЕРЖДАЮ |
|
Директор ФБУ «Федеральный центр |
|
анализа и оценки техногенного |
|
воздействия» |
|
__________ В.В. Новиков |
|
«13» ноября 2015 г. |
КОЛИЧЕСТВЕННЫЙ ХИМИЧЕСКИЙ АНАЛИЗ ВОД
МЕТОДИКА ИЗМЕРЕНИЙ МАССОВОЙ КОНЦЕНТРАЦИИ СУХОГО И ПРОКАЛЕННОГО ОСТАТКА В ПРОБАХ ПИТЬЕВЫХ, ПРИРОДНЫХ И СТОЧНЫХ ВОД ГРАВИМЕТРИЧЕСКИМ МЕТОДОМ
ПНД Ф 14.1:2:4.261-2010
Методика допущена для целей государственного экологического контроля
МОСКВА (издание 2015 г.)
Методика измерений аттестована Центром метрологии и сертификации «СЕРТИМЕТ» Уральского отделения РАН (Аттестат аккредитации № RA.RU.310657 от 12.05.2015), рассмотрена и одобрена федеральным бюджетным учреждением «Федеральный центр анализа и оценки техногенного воздействия» (ФБУ «ФЦАО»).
Настоящее издание методики введено в действие взамен ПНД Ф предыдущего издания и действует до выхода нового издания.
Методика зарегистрирована в Федеральном информационном фонде по обеспечению единства измерений. Информация о методике представлена на сайтах http://www.fundmetrology.ru/ в разделе «Сведения об аттестованных методиках (методах) измерений» и http://www.rossalab.ru/ в разделе «Методики анализа».
Заместитель директора ФБУ «ФЦАО» ____________ А.Б. Сучков
Разработчик:
ЗАО «РОСА», 2010
Адрес: 119297, г. Москва, ул. Родниковая, 7, стр. 35
Телефон: (495) 502-44-22, телефон/факс: (495) 439-52-13
http://www.rossalab.ru
e-mail: [email protected]
Содержание
Настоящий нормативный документ устанавливает методику измерений массовой концентрации сухого и прокаленного остатка в пробах питьевых, природных и сточных вод гравиметрическим методом. Методика распространяется на следующие объекты анализа: воды питьевые (в том числе расфасованные в емкости), воды природные пресные (поверхностные и подземные, в том числе источники водоснабжения), воды сточные (производственные, хозяйственно-бытовые, ливневые и очищенные.
Примечание - Допускается применение методики для анализа вод бассейнов и аквапарков, талых вод, технических вод и проб снежного покрова.
Диапазон измерений массовых концентраций сухого и прокаленного остатков составляет от 1,0 до 35000 мг/дм3.
Сухой остаток характеризует общее содержание в воде растворенных веществ, главным образом минеральных и частично органических веществ, имеющих температуру кипения выше 105 °С, нелетучих с водяным паром и не разлагающихся при данной температуре.
Примечание - Допускается для сточной воды наряду с термином «сухой остаток» применять термин «минерализация (плотный остаток)».
Прокаленный остаток дает представление о содержании в пробе воды минеральных веществ.
Разность между величинами сухого остатка и прокаленного остатка равна величине потерь при прокаливании, по которой можно судить о содержании органических веществ.
Блок-схема проведения анализа приведена в приложении А.
ГОСТ 12.0.004-90. Система стандартов безопасности труда. Организация обучения безопасности труда. Общие положения.
ГОСТ 12.1.004-91. Система стандартов безопасности труда. Пожарная безопасность. Общие требования.
ГОСТ 12.1.007-76. Система стандартов безопасности труда. Вредные вещества. Классификация и общие требования безопасности.
ГОСТ 12.4.009-83. Система стандартов безопасности труда. Пожарная техника для защиты объектов. Основные виды. Размещение и обслуживание.
ГОСТ 17.1.5.05-85. Охрана природы. Гидросфера. Общие требования к отбору проб поверхностных и морских вод, льда и атмосферных осадков.
ГОСТ 1770-74. Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Общие технические условия.
ГОСТ 3118-77. Реактивы. Кислота соляная. Технические условия.
ГОСТ 4147-74. Реактивы. Железо (III) хлорид 6-водный. Технические условия.
ГОСТ 4233-77. Реактивы. Натрий хлористый. Технические условия.
ГОСТ 4234-77. Реактивы. Калий хлористый. Технические условия.
ГОСТ 6709-72. Вода дистиллированная. Технические условия.
ГОСТ 12026-76. Бумага фильтровальная лабораторная. Технические условия.
ГОСТ 19908-90. Тигли, чаши, стаканы, колбы, воронки, пробирки и наконечники из прозрачного кварцевого стекла. Общие технические условия.
ГОСТ 25336-82. Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры.
ГОСТ 31861-2012. Вода. Общие требования к отбору проб.
ГОСТ 31862-2012. Вода питьевая. Отбор проб.
ГОСТ Р 12.1.019-2009. Система стандартов безопасности труда. Электробезопасность. Общие требования и номенклатура видов защиты.
ГОСТ Р 52501-2005. Вода для лабораторного анализа. Технические условия.
ГОСТ Р 53228-2008. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания.
ГОСТ Р 56237-2014. Вода питьевая. Отбор проб на станциях водоподготовки и в трубопроводных распределительных системах.
ГОСТ OIML R 76-1-2011. Государственная система обеспечения единства измерений. Весы неавтоматического действия. Часть 1. Метрологические и технические требования. Испытания.
ГОСТ Р ИСО 5725-6-2002. Точность (правильность и прецизионность) методов и результатов измерений. Часть 6. Использование значений точности на практике.
Примечание - Если ссылочный стандарт заменен (изменен), то следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
Настоящая методика обеспечивает получение результатов анализа с погрешностью, не превышающей значений, приведенных в таблице 1.
Таблица 1 - Диапазон измерений сухого и прокаленного остатка, значения показателей точности, воспроизводимости и повторяемости
|
Диапазон измерений, мг/дм3 |
Показатель повторяемости (относительное среднеквадратическое отклонение повторяемости), σr, % |
Показатель воспроизводимости (относительное среднеквадратическое отклонение воспроизводимости), σR, % |
Показатель точности (границы относительной погрешности при доверительной вероятности 0,95), ±δ, % |
|
Oт 1 до 50 включ. |
6 |
8,5 |
17 |
|
Св. 50 до 5000 включ. |
3 |
4,5 |
9 |
|
Св. 5000 до 35000 включ. |
2 |
3,5 |
7 |
Гравиметрический метод определения сухого остатка основан на выпаривании аликвотной части профильтрованной анализируемой пробы воды, высушивании полученного остатка при температуре (105 ± 2) °С и его взвешивании.
Гравиметрический метод определения прокаленного остатка основан на выпаривании аликвотной части профильтрованной анализируемой пробы воды, прокаливании полученного остатка при температуре (600 ± 20) °С и его взвешивании.
5.1.1 Весы лабораторные общего назначения специального класса точности, с наибольшим пределом взвешивания 210 г по ГОСТ OIML R 76-1 или по ГОСТ Р 53228.
5.1.2 Баня водяная лабораторная, обеспечивающая поддержание температуры до (100 ± 2) °С, любой модели.
5.1.3 Дистиллятор или установка любого типа для получения воды дистиллированной по ГОСТ 6709 или воды для лабораторного анализа 2 степени чистоты по ГОСТ Р 52501.
5.1.4 Испаритель ротационный любого типа с отгонной колбой вместимостью 1000 или 2000 см3.
5.1.5 Насос водоструйный по ГОСТ 25336.
5.1.6 Печь муфельная с рабочей камерой, футерованной керамическим муфелем, обеспечивающая температуру (600 ± 20) °С.
5.1.7 Установка для фильтрования с вакуумным насосом.
5.1.8 Холодильник бытовой любого типа, обеспечивающий хранение проб при температуре (2 - 10) °С.
5.1.9 Шкаф сушильный общелабораторного назначения, обеспечивающий температуру (105 ± 2) °С.
5.1.10 Мензурки вместимостью 50; 100 и 250 см3 по ГОСТ 1770.
5.1.11 Цилиндры мерные вместимостью 50; 100 и 250 см3, исполнения 1 по ГОСТ 1770.
5.1.12 Емкости из стекла или полимерного материала вместимостью 500 и 1000 см3 для отбора проб.
5.1.13 Воронки стеклянные по ГОСТ 25336.
5.1.14 Стаканы вместимостью 250 и 1000 см3, исполнения 1 по ГОСТ 25336.
5.1.15 Флакон из стекла или полимерного материала для хранения раствора соляной кислоты вместимостью 1000 см3.
5.1.16 Чаши кварцевые вместимостью 50 см3 по ГОСТ 19908.
5.1.17 Чашки выпарительные фарфоровые вместимостью 50 см3 по ГОСТ 9147.
5.1.18 Щипцы тигельные.
5.1.19 Эксикатор по ГОСТ 25336.
5.2.1 Вода дистиллированная по ГОСТ 6709 или для лабораторного анализа по ГОСТ Р 52501 (2-ой степени чистоты) (далее - вода дистиллированная).
5.2.2 Железо (III) хлорид 6-водный, ч. по ГОСТ 4147 (насыщенный раствор для маркировки чашек).
5.2.3 Калий хлористый, х.ч. по ГОСТ 4234 или стандарт-титр с (KCl) = 0,1 моль/дм3 (0,1 Н) по ТУ 2642-001-56278322.
5.2.4 Кислота соляная, х.ч. по ГОСТ 3118.
5.2.5 Натрий хлористый, х.ч. по ГОСТ 4233 или стандарт-титр c (NaCl) = 0,1 моль/дм3 (0,1 Н) по ТУ 2642-001-56278322.
5.2.6 Силикагель технический по ТУ 6-09-31-107 или силикагель с индикатором влажности (например, производства фирмы Merck) для заполнения эксикаторов.
5.2.7 Бумага фильтровальная по ГОСТ 12026.
5.2.8 Фильтры мембранные с диаметром пор 0,45 мкм (например, производства фирмы Milliроrе или фирмы Владипор).
5.2.9 Фильтры обеззоленные «синяя лента» по ТУ 6-09-1678.
Стандартный образец (далее - СО) массовой концентрации сухого остатка воды с относительной погрешностью аттестованного значения не более ±1 % при доверительной вероятности Р = 0,95.
Примечания -
1 Допускается использование других средств измерений утвержденных типов, обеспечивающих измерения с установленной точностью.
2 Средства измерений должны быть поверены в установленные сроки. Испытательное оборудование должно быть аттестовано в установленные сроки.
3 Допускается использование другого оборудования, материалов и реактивов с метрологическими и техническими характеристиками, не хуже, чем у вышеуказанных.
6.1 При выполнении измерений необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007.
6.2 При работе с оборудованием необходимо соблюдать правила электробезопасности по ГОСТ Р 12.1.019.
6.3 Обучение работающих безопасности труда должно быть организовано в соответствии с ГОСТ 12.0.004.
6.4 Помещение лаборатории должно соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004 и иметь средства пожаротушения по ГОСТ 12.4.009.
К выполнению измерений и обработке их результатов допускаются лица, имеющие специальное среднее или высшее образование химического профиля, владеющие техникой гравиметрического анализа и изучившие правила эксплуатации используемого оборудования.
При выполнении измерений в лаборатории соблюдают следующие условия:
|
температура воздуха |
(20 - 28) °С |
|
относительная влажность воздуха |
не более 80 % при 25 °С |
|
напряжение в сети |
(220 ± 22) В |
9.1 Отбор проб осуществляют в соответствии с ГОСТ 31861 и ГОСТ 318621. Отбор проб воды осуществляют в емкости из стекла или полимерного материала. Пробы снега отбирают в соответствии с ГОСТ 17.1.5.05 и переводят в талую воду при комнатной температуре. Объем отбираемой пробы воды составляет от 500 до 1000 см3. Например, для анализа сточной воды рекомендуется использовать 500 см3 воды, для питьевой - не менее 1000 см3.
___________
1 - В Российской Федерации с 01.01.2016 г. следует пользоваться ГОСТ Р 56237-2014.
9.2 Пробу анализируют в день отбора, не консервируют. Допускается хранение пробы не более 24 часов при охлаждении до (2 - 10) °С.
9.3 При отборе проб составляется сопроводительный документ по утвержденной форме, в котором указывается:
- цель анализа;
- место, дата и время отбора;
- шифр пробы;
- должность, фамилия сотрудника, отбирающего пробу.
10.1 Приготовление раствора соляной кислоты массовой доли 6 %
В стакане из термостойкого стекла вместимостью 1000 см3 смешивают 150 см3 соляной кислоты с 850 см3 дистиллированной воды. Смесь хранят под тягой во флаконе с притертой пробкой. Срок хранения - 6 месяцев при комнатной температуре.
10.2.1 Маркировка фарфоровых чашек
Тонкой деревянной палочкой или спичкой на фарфоровые чашки наносят идентификационные метки (номера) насыщенным раствором хлорного железа. Затем чашки ставят в муфельную печь, предварительно нагретую до (600 ± 20) °С на (5 - 10) мин. Метки приобретают коричневую окраску и не смываются водой и растворами кислот.
10.2.2 Прокаливание и взвешивание чашек
Промаркированные фарфоровые чашки промывают раствором соляной кислоты, приготовленной по 10.1, затем дистиллированной водой, подсушивают на воздухе и прокаливают при (600 ± 20) °С в течение 20 минут, охлаждают в эксикаторе до температуры окружающей среды и взвешивают. Прокаливание повторяют до достижения постоянной массы (т.е. до тех пор, пока расхождение значений между двумя последними взвешиваниями будет не более 0,0005 г). Значения массы чашки записывают в рабочем журнале (М2i).
Примечания -
1 Допускается для выполнения измерений использование кварцевых чашек, подготовленных по приведенной процедуре.
2 Если одни и те же чашки используют ежедневно, при этом их массы изменяются в допустимых пределах (±0,0005 г), разрешается проведение одного прокаливания при температуре (600 ± 20) °С в течение часа с последующим взвешиванием.
3 Если выполняется определение только сухого остатка, то фарфоровые или кварцевые чашки высушивают в сушильном шкафу при температуре (105 ± 2) °С в течение четырех часов до достижения постоянной массы.
Для определения берут от 25 до 1000 см3 анализируемой пробы воды в зависимости от предполагаемой массовой концентрации сухого или прокаленного остатка. Объем выбирают таким образом, чтобы масса привеса чашки после выпаривания и высушивания составила более 0,0010 г.
Аликвотную часть пробы воды, предварительно профильтрованную через фильтр «синяя лента» и отобранную мензуркой или цилиндром, помещают в фарфоровую чашку, подготовленную по 10.2.2, и выпаривают на водяной бане досуха. Выпаривание на водяной бане проб воды проводят в вытяжном шкафу.
При выпаривании чашку наполняют водой не более чем на 3/4 объёма, постепенно прибавляя оставшуюся воду по мере упаривания пробы.
Примечание - Если аликвотная часть пробы воды составляет (500 - 1000) см3, то допускается проводить выпаривание с применением ротационного испарителя. Воду упаривают приблизительно до 50 см3, затем количественно переносят в выпарную чашку и выпаривают на водяной бане досуха.
При анализе питьевых и природных вод допускается фильтрование пробы воды через мембранный фильтр с помощью установки для фильтрования.
После выпаривания внешнюю поверхность чашки с сухим остатком тщательно вытирают фильтровальной бумагой и помещают в сушильный шкаф, нагретый до (105 ± 2) °С, высушивают в течение трех часов, охлаждают в эксикаторе, взвешивают.
Высушивание, охлаждение в эксикаторе до температуры окружающей среды и взвешивание повторяют до достижения постоянной массы, т.е. до тех пор, пока разница между результатами двух последовательных взвешиваний будет не более 0,0005 г. Результаты взвешивания записывают в рабочем журнале (M1i).
Чашку с сухим остатком помещают в муфельную печь, предварительно нагретую до (600 ± 20) °С, и прокаливают в течение 20 минут. Охлаждают чашку в эксикаторе до температуры окружающей среды. После полного охлаждения чашку с остатком взвешивают. Прокаливание, охлаждение и взвешивание повторяют до достижения постоянной массы, т.е. до тех пор, пока разница между результатами двух последовательных взвешиваний будет не более 0,0005 г.
Если после первого прокаливания остаток в чашке имеет черный цвет, то его смачивают дистиллированной водой (приблизительно 10 см3), и далее повторяют прокаливание, охлаждение до температуры окружающей среды и взвешивание до достижения постоянной массы. Результаты взвешивания записывают в рабочем журнале (М3i).
Примечание - Допускается при определении сухого остатка проводить высушивание образца в течение 4 часов, а при определении прокаленного остатка прокаливание в течение 1 часа с последующим охлаждением в эксикаторе до температуры окружающей среды и однократным взвешиванием.
Массовую концентрацию сухого остатка Хс (мг/дм3) вычисляют по формуле

где
М1 - масса чашки с высушенным остатком, г;
М2 - масса пустой чашки, г;
V - аликвотная часть пробы воды, см3;
106 - коэффициент пересчета единиц измерения г/см3 в мг/дм3.
Массовую концентрацию прокаленного остатка Хп (мг/дм3) вычисляют по формуле:

где
М3 - масса чашки с прокаленным остатком, г;
М2 - масса пустой чашки, г;
V - аликвотная часть пробы воды, см3;
106 - коэффициент пересчета единиц измерения г/см3 в мг/дм3.
Результаты измерений, как правило, в протоколах анализов представляют в виде:
|
X ± ∆, мг/дм3 |
(P = 0,95), |
где ∆ - характеристика абсолютной погрешности, которую рассчитывают по формуле
∆ = 0,01 × δ × Х,
где δ - значение показателя точности, % (таблица 1).
Результаты измерений округляют с точностью до:
при массовой концентрации:
|
от 1 до 10 мг/дм3 |
- 0,1 мг/дм3 |
|
от 10 до 1000 мг/дм3 |
- 1 мг/дм3 |
|
от 1000 до 10000 мг/дм3 |
- 10 мг/дм3 |
|
свыше 10000 мг/дм3 |
- 100 мг/дм3 |
14.1 При получении двух результатов измерений (Х1, Х2) в условиях повторяемости (сходимости) осуществляют проверку приемлемости результатов в соответствии с требованиями ГОСТ Р ИСО 5725-6 (раздел 5).
Результат измерений считают приемлемым при выполнении условия:

Значения предела повторяемости (r) приведены в таблице 3.
При выполнении этого условия приемлемы оба результата измерений, и в качестве окончательного может быть использовано их среднее арифметическое значение. При превышении предела повторяемости могут быть использованы методы проверки приемлемости результатов измерений согласно раздела 5 ГОСТ Р ИСО 5725-6.
14.2 При получении результатов измерений в двух лабораториях (Xлаб1, Хлаб2) проводят проверку приемлемости результатов измерений в соответствии с требованиями ГОСТ Р ИСО 5725-6 (раздел 5).
Результат измерений считают приемлемым при выполнении условия:

Значения предела воспроизводимости (R) приведены в таблице 3.
При выполнении этого условия приемлемы оба результата измерений, и в качестве окончательного может быть использовано их среднее арифметическое значение. При превышении предела воспроизводимости могут быть использованы методы проверки приемлемости результатов измерений согласно раздела 5 ГОСТ Р ИСО 5725-6.
Таблица 3 - Относительные значения пределов повторяемости и воспроизводимости при доверительной вероятности 0,95
|
Диапазон измерений, мг/дм3 |
Предел повторяемости (относительное значение допускаемого расхождения для двух результатов измерений, полученных в условиях повторяемости), r, % |
Предел воспроизводимости (относительное значение допускаемого расхождения для двух результатов измерений, полученных в условиях воспроизводимости), R, % |
|
От 1 до 50 включ. |
17 |
24 |
|
Св. 50 до 5000 включ. |
8 |
13 |
|
Св. 5000 до 35000 включ. |
6 |
10 |
15.1 В случае регулярного выполнения измерений по методике рекомендуется проводить контроль стабильности результатов измерений путем контроля среднеквадратического отклонения повторяемости, среднеквадратического отклонения внутрилабораторной прецизионности и погрешности с помощью контрольных карт в соответствии с рекомендациями ГОСТ Р ИСО 5725-6 (раздел 6).
Периодичность контроля стабильности результатов измерений регламентируют во внутренних документах лаборатории.
15.2 Оперативный контроль точности результатов измерений рекомендуется проводить с каждой серией проб, если измерения по методике выполняют эпизодически, а также при возникновении необходимости подтверждения результатов измерений отдельных проб (при получении нестандартного результата измерений; результата, превышающего ПДК и т.п.).
Оперативный контроль проводят с помощью образца для контроля (ОК). Образец для контроля (ОК) готовят с использованием СО (например, СО общей минерализации воды), веществ гарантированной чистоты (например, натрий хлористый или калий хлористый или из стандарт-титров калия хлористого или натрия хлористого) и дистиллированной воды. При использовании веществ гарантированной чистоты или стандарт-титров раствор ОК готовят таким образом, чтобы массовая концентрация сухого остатка в ОК приближалась к значению массовой концентрации в реальных пробах в конкретной лаборатории.
Оперативный контроль процедуры измерений проводят путем сравнения результата отдельно взятой контрольной процедуры (KK) с нормативом контроля (K).
Результат контрольной процедуры KK рассчитывают по формуле
KK = ǀX - Cǀ,
где
X - результат контрольного измерения массовой концентрации сухого или прокаленного остатка в образце для контроля, мг/дм3;
С - аттестованное значение массовой концентрации сухого или прокаленного остатка в образце для контроля, мг/дм3.
Норматив контроля K рассчитывают по формуле
K = ∆л,
где ∆л - характеристика абсолютной погрешности аттестованного значения массовой концентрации сухого или прокаленного остатка в образце для контроля, установленная в лаборатории при реализации методики, мг/дм3.
Примечание - Допускается ∆л рассчитывать по формуле ∆л = 0,84 × ∆, где ∆ - приписанная характеристика абсолютной погрешности методики.
Качество контрольной процедуры признают удовлетворительным при выполнении условия:
KK ≤ K.
При невыполнении условия контрольную процедуру повторяют. При повторном невыполнении условия выясняют причины, приводящие к неудовлетворительным результатам, и устраняют их.
БЛОК-СХЕМА ВЫПОЛНЕНИЯ АНАЛИЗА ПО ОПРЕДЕЛЕНИЮ СУХОГО И ПРОКАЛЕННОГО ОСТАТКОВ

files.stroyinf.ru
сухой остаток
Сухой остаток по своей величине отличается от суммы ионов, во-первых, вследствие присутствия растворенных веществ, не учитываемых при анализе, во-вторых, вследствие весьма сложных изменений, происходящих с солевой частью остатка при его высушивании.[ ...]
Сухой остаток. Суммарное количество минеральных и органических примесей, содержащихся в воде в истинно растворенном и коллоидном состоянии, характеризуют величиной сухого остатка. Величина его определяется взвешиванием остатка после выпаривания некоторого объема предварительно профильтрованной воды и выражается в миллиграммах на литр.[ ...]
Сухой остаток определяют выпариванием некоторого объема вытяжки из почвы, высушиванием в термостате остатка и его взвешиванием.[ ...]
Сухой остаток дает представление об общем количестве загрязнений, находящихся в исследуемом объеме воды, за исключением тех веществ, которые улетучиваются при выпаривании и сушке. Прокаливание сухого остатка позволяет определить примерное соотношение минеральной и органической частей загрязнений.[ ...]
Сухой остаток после его прокаливания при температуре 600°С соответствует приблизительно сумме составляющих неорганических веществ, растворенных в воде.[ ...]
Сухой остаток растворяют при нагревании на водяной бане в 1 мл серной кислоты. После растворения сухого остатка вносят 1 мл раствора резорцина, перемешивают и пробирку помещают на 10 мин в глицериновую баню, предварительно нагретую до 170—180° С. Пробирке дают остыть, затем содержимое ее смывают 10—12 мл воды в мерный цилиндр, прибавляют небольшими порциями раствор РШ4ОН до слабо-щелочной реакции по лакмусовой бумаге и объем раствора доводят водой до 25 мл. Отбирают 10 мл в колориметрическую пробирку и при облучении пробы ультрафиолетовым светом сравнивают интенсивность флуоресценции со стандартной шкалой.[ ...]
Сухой остаток в воде реки даже у места сбраоа сточных вод йе превышает нормы. В пункте ‘ первого водопользования, в 5,5 км ниже места сброса сточных вод, этот показатель в разные месяцы года колеблется в пределах от 52 до 128,1 мг/л, т. е. не превышает гигиенической нормы 1000 мг/л.[ ...]
Сухой остаток подсушивают в эксикаторе или в сушильном шкафу при 80° (эта операция обязательна).[ ...]
Сухой остаток общий также минерального происхождения, потеря при прокаливании составляет 8%. Концентрация хлоридов и сульфатов относительно невелика, но концентрация солей кремневой кислоты весьма значительна (—300 мг!л) за счет применяемого в качестве флотореагента жидкого стекла. Цианиды, медь и мышьяк содержатся в незначительных количествах. Весьма существенным загрязнением являются используемые при флотации органические реагенты: нефтепродукты, терпинеол, ксантогенат (или дитиофосфат), которые повышают окисляемость воды более чем до 100 мг/л О.[ ...]
Сухой и плотный остатки. В отличие от анализа природных вод сухой остаток сточных вод определяют из натуральной (нефильтрованной) пробы, поэтому он является показателем суммарного содержания загрязнений во всех агрегатных состояниях.[ ...]
Сухим остатком называется высушенный при 105°С остаток, получающийся при выпаривании досуха профильтрованной сточной воды. Сухой остаток характеризует содержание в воде минеральных и, частично, органических примесей, температура кипения которых превышает 105 °С, а также нелетучих с водяным паром и не разлагающихся при данной температуре органических соединений.[ ...]
Сухой остаток и потеря при прокаливании. О количестве солей, содержащихся в природных водах, можно судить по величине сухого остатка и потере массы при прокаливании. Сухой остаток, образующийся при выпаривании определенного объема воды, предварительно профильтрованной через бумажный фильтр, состоит из минеральных солей и нелетучих органических соединений Органическая часть сухого остатка воды определяется потерей его при прокаливании.[ ...]
Сухой остаток в чашке высушивают до постоянного веса в сушильном шкафу при 110° С. После этого при помощи скребка (скальпель, ланцет, писчее перо) сухой остаток соскабливают со стенок чашки, растирают в той же чашке пестиком, обернутым калькой, и тщательно перемешивают. Из полученной однородной массы готовят препараты для радиометрирования.[ ...]
Сухой остаток растворяют в диметиланилине. Для этого вносят в чашку 1,0 мл диметиланилина, слегка растирают стеклянной палочкой и переводят жидкость количественно в соответствующую колориметрическую пробирку.[ ...]
Сухой остаток растворяют в 10 мл гексана и 2 мкл этого раствора вводят через самоуплотняющуюся мембрану испарителя в хроматограф. На основании данных хроматограмм строится градуировочная кривая, выражающая зависимость высоты (мм) или площади (мм2) пика от количества компонента (мкг, нг). В случае использования площади ее значение находится умножением высоты пика на его ширину, измеренную на половине высоты. Для построения градуировочной кривой используют 5 градуировочных растворов. Раствор каждой концентрации хроматографируется не менее 5-ти раз.[ ...]
Сухой остаток и потери при прокаливании. В практике водо-подготовки под сухим остатком понимают общую сумму неорганических и органических соединений в растворенном и коллоидно растворенном состоянии. Сухой остаток определяют выпариванием предварительно профильтрованной пробы с последующим высушиванием при 10 °С. Потери при прокаливании определяют содержание в сухом остатке органических веществ. Остаток после прокаливания характеризует солесодержание воды.[ ...]
Сухой остаток в воде источника хозяйственно-питьевого назначения и в питательной воде не должен превышать 1000 мг/л, так как употребление человеком воды с повышенным солесодержанием вызывает различные заболевания.[ ...]
Сухой остаток растворяют в 15 мл I М фосфорной кислоты. Полученный раствор полярографируют, предварительно удаляют из раствора кислород. Для удаления кислорода через исследуемый раствор пропускают азот, очищенный от кислорода.[ ...]
Сухой остаток - это количество растворенных солей в миллиграммах, содержащееся в 1 л воды. Т.к. масса органических веществ в сухом остатке не превышает 10-15 %, сухой остаток дает представление о степени минерализации воды.[ ...]
Различают общий сухой остаток и остаток после прокаливания. Под понятием «общий сухой остаток» подразумевают количество вещества, оставшееся после выпаривания пробы сточных вод и сушки до постоянной массы. Количество вещества, полученное после прокаливания сухого остатка, называется «остатком после прокаливания». По уменьшению массы сухого остатка после прокаливания можно судить о содержании органических веществ в сточных водах. Сукой остаток определяют ,по стандарту PN-59/Z-04519.[ ...]
Для определения сухого остатка 250—500 мл испытуемой воды, фильтрованной через беззольный фильтр («синяя лента»), выпаривают в платиновой чашке на водяной бане. При выпаривании вносят в воду 25 мл 1%-ного раствора № С03. Выпаренный .с содой сухой остаток высушивают до постоянной массы при температуре 150° С.[ ...]
Определение в ацетоне. Сухой остаток растворяют в 5,0 мл ацетона и, при взбалтывании, приливают к полученному раствору 0,50 мл 25%-ного аммиака. Вначале образуется сиреневая окраска, но через 5—10 мин. окраска переходит в розоватожелтую, которую колориметрируют через 20 мин.[ ...]
Иногда при анализе воды определяют так называемый плотный остаток, т. е. остаток, полученный при упаривании нефильтрованной воды и высушенный до постоянного веса при 105°. Напротив, сухой остаток получают путем упаривания и сушки при 105° профильтрованной воды. Следовательно, концентрация грубодисперсных примесей (взвешенных веществ) может быть определена не только непосредственно, но и по разности плотного и сухого остатка воды.[ ...]
Определение содержания толуола. Определение в спиртовом растворе. Сухой остаток после испарения эфира во всех пробирках растворяют в 5,0 мл спирта и прибавляют, при тщательном взбалтывании, 0,050 мл 5%-ного раствора едкого кали.[ ...]
После упаривания эфирного экстракта с бенз[а]пи-реном сухой остаток растворяют в 5 мл бензола.[ ...]
Общее содержание растворенных веществ в воде часто характеризуют величиной сухого остатка, а содержание растворенных минеральных солей — величиной прокаленного остатка. Однако следует иметь в виду, что сухой остаток может служить лишь приближенной характеристикой содержания растворенных веществ, так как при ¿=105° многие соединения неполностью отдают влагу- и кристаллизационную воду, а некоторые органические соединения начинают окисляться.[ ...]
В исключительных случаях по согласованию с органами санитарного надзора допустимы сухой остаток до 1500 мг/л, цветность до 35°, железо до 1 мг/л, общая жесткость до 10 мг-экв/л. При вынужденном использовании природной воды, обладающей еще большей жесткостью, ее подвергают умягчению.[ ...]
Существенное значение имеет общая сумма растворенных в воде веществ, так называемый сухой остаток (или плотный остаток) в мг/л. Для его определения выпаривают известное количество предварительно профильтрованной воды, затем остаток высушивают при температуре 105—120°С, взвешивают и пересчитывают на 1 л воды.[ ...]
Запах — неопределенный, фенольный; исчезает при разведении 1 : 10. Взвешенных веществ—200 мг/л. Сухой остаток -— ,1200 мг/л. pH—4,8; тятрирная кислотность 84 мл норм раствора щелочи. БПКлолк при разбавлении 1: 100 равна 21 мг/л, при разбавлении 1:500 — 66 мг/л при разбавлении 1:1000 — 72 мг/л.[ ...]
На линию старта (от края 1,5 см) наносят при помощи микропипетки 0,1 мл растворов пробы и шкалы стандартов, которую готовят аналогично пробам (растворяют сухой остаток в 1 мл этанола). Размер пятен не должен превышать 0,5 см. Пластинку высушивают на воздухе в течение 3-х минут и помещают в камеру для хроматографирования с системой растворителей - хлороформ : метанол : 25 %-ный раствор аммиака (90 : 10 : 1). После того как подвижный растворитель поднимается до конца пластинки, ее вынимают из камеры и оставляют на несколько минут для испарения растворителя, затем помещают в сушильный шкаф при температуре 100 °С на 10 минут, для освобождения паров аммиака, затем пластинку обрабатывают парами воды (держат 2 минуты над кипящей водяной баней) и переносят в камеру с парами хлора, где выдерживают 15 минут. Для удаления паров хлора пластинку помещают в сушильный шкаф при температуре 50 °С на 1 минуту. Далее пластинку орошают раствором о-толидина. Эфедрин гидрохлорид проявляется в виде темно-синего пятна с 1 = 0,13±0,02. Через 1 час проводят количественное измерение используя планиметр или денситометрирование.[ ...]
Подобно шахтным водам свинцово-цинковых месторождений, основными загрязнениями сточных вод полиметаллических рудников являются грубодисперсные примеси и сухой остаток общий, обусловленный содержанием сульфатов, концентрация которых »достигает 260 мг!л.[ ...]
Рудничные (шахтные и карьерные) воды характеризуются повышенной минерализацией. Например, шахтные воды Октябрьского месторождения (356,6 тыс. м3/год) имеют величину pH — 3,5, сухой остаток — 3860 мг/л. Высокое содержание различных токсикантов и в фильтрате хвостохранилищ (мг/л): Си до 0,2,2п до 0,2, РЬ до 0,09, Ре до 320, цианид натрия до 0,30 и т.д.[ ...]
При промывке дрожжевых грибков, мытье оборудования и упарке сброженного субстрата в процессе переработки щелоков на кормовые дрожжи будут образовываться сточные воды. В воде от промывки дрожжевых грибков сухой остаток равен около 40 г/л и состоит преимущественно из бетаина, вспомогательных веществ (сернокислых солей) и метаболитов торуло-вого брожения. Эти сточные воды предусматривается направлять на биологическую очистку совместно со сточными водами от промывки кальциевого цитрата и маточным рассолом, образующимися в процессе выделения лимонной кислоты.[ ...]
Более эффективной представляется технология пиролиза лакокрасочных отходов. По этой технологии шлам, содержащий краску, например автомобильную, сушат при температуре не более 200°С с целью удаления воды и органических растворителей. Сухой шлам подвергают пиролизу в инертной (N2, Аг) атмосфере при 600°С с образованием газообразных и жидких продуктов, а также сухого остатка. Газообразные и жидкие продукты улавливают и получают из них угольные материалы. Сухой остаток спекают при 900-1300°С в атмосфере N2, Аг, ЫНз до образования неорганического композиционного материала, содержащего нитрат бария и соединения титана, например его диоксида и карбида (металлы входят в состав красок) (№ги1а...).[ ...]
В фарфоровые чашки вводят 5,0; 10,0; 15,0; 20,0 и 25,0 мкг РЬ ( Ю3)2 с добавлением 0,1 мл чистого бензина и 5 мл HN03 (d = 1,4). Пробу выпаривают досуха, прокаливают в муфельной печи при 400° С; дважды обрабатывают по 2 мл НС1( 1 : 1) и выпаривают досуха на водяной бане. Сухой остаток извлекают 2 мл 2N КС! и полярографируют.[ ...]
Другой вид сточных вод — маточные рассолы, образующиеся после рекристаллизации лимонной кислоты из раствора, полученного разложением цитрата кальция серной кислотой. Количество этих сточных вод невелико, но они являются наиболее концентрированными. Сухой остаток маточных рассолов изменяется в пределах от 60 до 120 г/л. Рассолы содержат остатки патоки, побочные продукты бродильного процесса и лимонную кислоту, главным образом в виде соли.[ ...]
Показанный на рис. 30 графитовый атомизатор состоит из небольшой графитовой кюветы, установленной между двумя графитовыми электродами. Жидкую пробу объемом 1— 50 мкл помещают внутрь кюветы и систему вначале нагревают слабым электрическим током для удаления растворителя. Затем сухой остаток после прокаливания переводят в парообразное состояние при температуре около 3000 К путем увеличения силы тока для нескольких сотен ампер.[ ...]
Ход анализа. Фильтр с пробой помещают в стакан и заливают 10 мл ацетона. Через 10 мин фильтр отжимают палочкой. Экстракт переносят в небольшую фарфоровую чашку, а фильтр еще дважды промывают ацетоном порциями по 10 мл. Экстракты объединяют, нагревают на водяной бане для удаления растворителя. Сухой остаток растворяют в 1 мл ацетона, 0,1 мл пробы наносят на стартовую линию пластинки «Силуфол». Рядом с пробой наносят 0,1 мл рабочего стандартного раствора метионина («метчик»). Пластину помещают в хроматографическую камеру, в которую за 20—30 мин до начала анализа вносят на дно камеры подвижную фазу. После того как подвижная фаза поднимется на высоту 10—12 см, пластину вынимают из камеры, сушат до полного исчезновения запаха растворителя и орошают 0,2%-ным спиртовым раствором нингидрина.[ ...]
Фильтр с отобранной пробой переносят в колориметрическую пробирку, добавляют в нее 10 мл воды и оставляют на 15 минут, периодически встряхивая для лучшего растворения вещества. Степень десорбции вещества с фильтра - 97 %. Полученный раствор сливают в фарфоровую чашку и упаривают досуха на водяной бане. Сухой остаток растворяют в 0,5 мл бутанола (подкисленного НС1) и используют полученный раствор для анализа.[ ...]
Новой проблемой в целлюлозно-бумажной промышленности является очистка сточных вод производства химической древесной массы, для чего древесину, главным образом лиственных пород, подвергают горячей пропитке раствором сульфита натрия с добавлением соды, а затем размельчают на волокна. При выпаривании сточных вод после удаления волокон сухой остаток составляет 1,5 г/л и на его окисление расходуется 1,1 г/л КМп04 при остаточном содержании №2503 в 0,3 г/л. Очищать удаляемую часть сточных вод можно только биологическими методами, причем процесс очистки усложняется наличием неорганически и органически связанного сульфита. В связи с этим целесообразнее было бы производить древесную щепу, пропитанную раствором едкого натра при обычной температуре. При обработке такой щепы получается меньшее количество промывной воды, чем при обработке химической древесной массы, причем она легче поддается биологической очистке.[ ...]
Термическая очистка используется для высокоминерализованных сточных вод, а также при наличии органических токсичных веществ. Термический метод опреснения с помощью высоких температур называется дистилляцией (выпаривание), с помощью низких — кристаллизацией (вымораживание). При дистилляции сточных вод получают концентрированные растворы, из которых выделяют сухой остаток для сжигания, захоронения или последую г щего использования. При кристаллизации чистая вода образует кристаллы льда, а оставшийся рассол с растворенными в нем солями размещается в ячейках между ними. Температура замерзания рассола всегда ниже температуры замерзания чистой воды.[ ...]
Рейхтер модифицировал метод [235] и предложил следующую методику. К 2 л пробы воды приливают 10 мл 20%-ного раствора хлорида натрия, 5 мл концентрированной хлористоводородной кислоты и взбалтывают в течение 30 мин с 100 мл дважды перегнанного н-гексана. Гексановый слой отделяют, встряхивают с 50 мл 70%-ного этилового спирта и выпаривают досуха при 30 °С в вакууме, создаваемом водоструйным насосом. Остаток омыляют кипячением с обратным холодильником в течение 2 ч с 20 мл 7,5%-ного раствора КОН в 70%-ном этиловом спирте. Смесь взбалтывают с 20 мл воды и 40 мл гексана, гексановый слой отделяют, промывают 5 мл этилового спирта и выпаривают в токе азота при 50 °С досуха. Остаток извлекают 0,2 мл «-гексана и переносят на активированную при 110 °С пластинку для тонкослойной хроматографии, покрытую силикагелем. Далее анализируют 1 мкл этого раствора в газовом хроматографе с пламенно-ионизационным детектором. Набивка колонки состоит из хромосорба V-HP с 3% БЕЗО силиконовой смазки. Условия определения: температура колонки 260 °С, инжектора — 285 °С, пламенно-ионизационного детектора — 290 °С, газ-носитель — N2.[ ...]
Ход анализа. Из смешанной пробы отбирают 100 г почвы, доводят до постоянной массы по ГОСТ 51-80—75. Помещают 25 г почвы в коническую колбу вместимостью 200 мл, приливают 50 мл диэтилового эфира, энергично встряхивают 5 мин и оставляют на 20 мин. Затем эфирную вытяжку фильтруют через фильтр «синяя лента». Экстракцию ж-динитробензола из почвы повторяют 50 мл эфира. Фильтраты объединяют и выпаривают на водяной бане до сухого остатка. Сухой остаток растворяют fмaлыми порциями) 10 мл ацетона. Раствор переносят в пробирку, добавляют 0,5 мл 5%-ного раствора гидроксида натрия, взбалтывают и через 15 мин измеряют оптическую плотность окрашенного раствора при А, = 540 нм относительно контрольной пробы.[ ...]
По охлаждении раствор переливают в делительную воронку, прибавляют 10Д) мл эфира и встряхивают раствор 10 мин. Затем раствору дают расслоиться; нижний (водный) слой сливают через кран воронки; к эфирному слою прибавляют 10 мл воды и вновь встряхивают. После расслоения водный слой сливают через кран, а эфирный—через верх ворорки в фарфоровую чашку. Чашку ставят в вытяжной шкаф для испарения эфира при комнатной температуре. Сухой остаток растворяют в 10 мл этилового спирта; раствор переводят в пробирку с притертой пробкой с меткой 10 мл.[ ...]
Исследуемую жидкость переносят в делительную воронку и продукты бро-мирования извлекают трижды диэтиловым эфиром порциями по 5 мл. Объединенные эфирные вытяжки дважды быстро промывают в делительной воронке 5 мл 5%-ного двууглекислого натрия, затем 2—3 раза дистиллированной еодой (по 5 мл) до нейтральной реакции промывных вод. Эфирный экстракт переносят в коническую колбу и добавляют 3 г безводного сульфата натрия. Через 15 мин эфир отделяют от осушителя, а остаток в колбе промывают небольшими порциями эфира и присоединяют его к экстракту. Затем эфир упаривают в вакууме. Сухой остаток в колбе растворяют в 2—5 мл гексана и аликвотную часть (5 мкл) вводят в дозатор хроматографа.[ ...]
Камеру герметично закрывают. После того, как растворитель поднимется до верхнего края пластинки, ее вынимают и просматривают в УФ-свете, лампы ПРК-4. Отмечают положение флюоресцирующей зоны на уровне свидетеля и снимают окись алюминия в воронки с пористой пластинкой № 2. Элюируют 3,4-бензпирен с окиси алюминия бензолом до прекращения флюоресценции элюата ( 20—25 мл). Элюат собирают в мерный цилиндр. Полученный раствор сначала упаривают в чашках до небольшого объема (— 0,5 мл), затем остаток переносят в пробирки и продолжают упаривание досуха. Сухой остаток .растворяют в 0,2 мл гексана и емкости с раствором закрывают пробками; 5 мкл раствора вводят в хроматограф.[ ...]
Приведенные выше методы неприменимы при определении очень малых концентраций хлоридов в сточной воде. Если концентрация хлорид-ионов меньше 3—5 мг/л, для их определения значительно более чувствительным и точным оказывается колориметрический метод с применением дифенилкарбазйда, разработанный для определения хлорид-ионов в воде, питающей паровые котлы системы Рамзина. Этот метод можно применять и для анализа сильно загрязненных органическими веществами сточных вод, но только анализируемые пробы надо предварительно выпарить с добавлением соды и сухой остаток прокалить, как указано выше (см. разд. 24.1).[ ...]
Грунтовые воды типа "верховодка" содержатся в делювиальноэлювиальных четвертичных отложениях, развитых на территории месторождения повсеместно. Они представлены суглинками и гш-шями с прослоями и включениями песка и щебня коренных пород. Мощность отложений 3-15 м. Водоносными являются прослои рыхлых образований мощностью от нескольких см до 1 м. Обводненность пород слабая и носит спорадический характер. За пределами месторождения эти отложения вскрываются шахтными колодцами на глубине 4-6 м. Дебит при откачках небольшой - до 0,1 л/с. Качество воды удовлетворительное: сухой остаток 0,7 г/л, при общей жесткости 10,25 мг-экв/л, содержание хлор-иона - 53 мг/л, нитратов - 57 мг/л. Состав воды гидрокарбонатный магниев о-кальциевый (сентябрь 1994 года). Воды широко используются населением для водоснабжения.[ ...]
По накоплении некоторого количества таких отходов спесь их доводят едки» натром до сильно щелочной реакции по индикаторной бумаге, (если она почему-либо не будет иметь такой реакции ) , приливают избыток - 10 %-ного раствора сульфида или гйдросульфида натрия, оставляют в покое . Черев сутки раствор декантируют, осадок многократно пропивают декантацией же, сначала простой, затем дистиллированной водой до нейтральной реакции и, наконец, отделяют от воды на бумажном фильтре. На этом же фильтре растворяют осадок ва холоду в возможно меныем количестве азотной кислоты.[ ...]
ru-ecology.info
Вода питьевая. Метод определения содержания сухого остатка

ГОСУДАРСТВЕННЫЙ СТАНДАРТ СОЮЗА ССР
ВОДА ПИТЬЕВАЯ
МЕТОД ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ СУХОГО ОСТАТКА
ГОСТ 18164-72
ИЗДАТЕЛЬСТВО СТАНДАРТОВ
Москва
ГОСУДАРСТВЕННЫЙ СТАНДАРТ СОЮЗА ССР
|
ВОДА ПИТЬЕВАЯ Метод определения содержания сухого остатка Drinking water. Method for determination of total solids content |
ГОСТ 18164-72 |
Дата введения 01.01.74
Настоящий стандарт распространяется на питьевую воду и устанавливает весовой метод определения содержания сухого остатка.
Величина сухого остатка характеризует общее содержание растворенных в воде нелетучих минеральных и частично органических соединений.
1.1. Пробы отбирают по ГОСТ 2874 и ГОСТ 4979.
1.2. Объем пробы воды для определения сухого остатка должен быть не менее 300 см3.
Шкаф сушильный с терморегулятором.
Баня водяная.
Посуда мерная лабораторная стеклянная по ГОСТ 1770, вместимостью: колбы мерные 250 и 500 см2; пипетки без деления 25 см3, чашка фарфоровая выпарительная 500-100 см3.
Эксикаторы по ГОСТ 25336.
Натрий углекислый безводный по ГОСТ 83.
Вода дистиллированная по ГОСТ 6709.
Натрий углекислый Na2CO3, х.ч., точный раствор, готовят следующим образом: 10 г безводной соды (высушенной при 200 °С и отвешенной на аналитических весах) растворяют в дистиллированной воде и доводят объем раствора дистиллированной водой до 1 дм3.
1 см3 раствора содержит 10 мг соды.
3.1 Определение сухого остатка без добавления соды (проводится в день отбора пробы).
250-500 см3 профильтрованной воды выпаривают в предварительно высушенной до постоянной массы фарфоровой чашке. Выпаривание ведут на водяной бане с дистиллированной водой. Затем чашку с сухим остатком помещают в термостат при 110 °С и сушат до постоянной массы.
3.1.1. Обработка результатов
Сухой остаток (Х), мг/дм3, вычисляют по формуле
 ,
,
где m - масса чашки с сухим остатком, мг;
m1 - масса пустой чашки, мг;
V - объем воды, взятый для определения, см3.
Данный метод определения сухого остатка дает несколько завышенные результаты вследствие гидролиза и гигроскопичности хлоридов магния и кальция и трудной отдачи кристаллизационной воды сульфатами кальция и магния. Эти недостатки устраняются прибавлением к выпариваемой воде химически чистого карбоната натрия. При этом хлориды, сульфаты кальция и магния переходят в безводные карбонаты, а из натриевых солей лишь сульфат натрия обладает кристаллизационной водой, но она полностью удаляется высушиванием сухого остатка при 150-180 °С.
3.2. Определение сухого остатка с добавлением соды
250-500 см3 профильтрованной воды выпаривают в фарфоровой чашке, высушенной до постоянной массы при 150 °С. После того как в чашку прилита последняя порция воды, вносят пипеткой 25 см3 точного 1 %-ного раствора углекислого натрия с таким расчетом, чтобы масса прибавленной соды примерно в два раза превышала массу предполагаемого сухого остатка. Для обычных пресных вод достаточно добавить 250 мг безводной соли (25 см3 1 %-ного раствора Na2CO3). Раствор хорошо перемешивают стеклянной палочкой. Палочку обмывают дистиллированной водой, собирая воду в чашку с осадком. Выпаренный с содой сухой остаток высушивают до постоянной массы при 150 °С. Чашку с сухим остатком помещают в холодный термостат и затем поднимают температуру до 150 °С. Разность в массе между чашкой с сухим остатком и первоначальной массой чашки и соды (1 см3 раствора соды содержит 10 мг Na2CO3) дает значение сухого остатка во взятом объеме воды.
3.2.1. Обработка результатов
Сухой остаток (Х), мг/дм3, вычисляют по формуле
 ,
,
где m - масса чашки с сухим остатком, мг;
m1 - масса пустой чашки, мг;
m2 - масса добавленной соды, мг;
V - объем воды, взятый для определения, см3.
Расхождения между результатами повторных определений не должны превышать 10 мг/дм3, если сухой остаток не превышает 500 мг/дм3, при более высоких концентрациях расхождение не должно превышать 2 отн. оо/о.
ИНФОРМАЦИОННЫЕ ДАННЫЕ
1. УТВЕРЖДЕН И ВВЕДЕН В ДЕЙСТВИЕ Постановлением Государственного комитета стандартов Совета Министров СССР от 09.09.72 № 1855
2. ВВЕДЕН ВПЕРВЫЕ
3. ССЫЛОЧНЫЕ НОРМАТИВНО-ТЕХНИЧЕСКИЕ ДОКУМЕНТЫ
|
Обозначение НТД, на который дана ссылка |
Номер пункта |
|
ГОСТ 83-79 |
2 |
|
ГОСТ 1770-74 |
2 |
|
ГОСТ 2874-82 |
1.1 |
|
ГОСТ 4979-49 |
1.1 |
|
ГОСТ 6709-72 |
2 |
|
ГОСТ 25336-82 |
2 |
4. Ограничение срока действия снято Постановлением Госстандарта СССР от 25.12.91 № 2120
5. ПЕРЕИЗДАНИЕ
aquagroup.ru









