Жесткая вода на участке: что делать? Жесткая вода
Жесткая вода - что это такое и чем она опасна
Сначала приведем простой пример, с которым сталкивались почти все: что происходит после многократного использования электрочайника? На стенках появляется накипь, которую рано или поздно придется счищать. Это же относится и к любым другим водонагревательным приборам.
Чтобы отскоблить накипь, придется изрядно постараться или воспользоваться бытовой химией. Образование накипи – это прямое следствие высокой жесткости воды.
Какие проблемы может вызвать образование накипи?
Стоит отметить, что теплопроводность накипи намного меньше, чем у металла. Как следствие, придется затратить больше энергии для нагрева воды в кастрюле.
Серьезные неудобства может доставить образование накипи в радиаторах и трубах системы отопления. Между теплоносителем – водой и металлической поверхностью образуется своего рода термоизолирующая прослойка. В результате, отопительный котел можно выкрутить на максимальную температуру, но радиаторы наощупь останутся только чуть теплыми. На поддержание комфортной температуры будет уходить больше топлива. А ведь оно стоит денег.
Отопительный период в нашей стране длится более полугода, и за это время может накопиться изрядная сумма, выброшенная так сказать "в топку".
И это касается не только владельцев домов и квартир, оборудованных индивидуальными системами отопления. Ведь многие владельцы квартир с центральным отоплением сталкивались с их недостаточной эффективностью.
Жесткая вода горчит на вкус и имеет неприятный запах. Считается, что длительное употребление жесткой воды негативно сказывается на пищеварительной системе человека. Есть также гипотеза о связи показателя жесткости воды с риском сердечно-сосудистых заболеваний, но ни доказать, ни опровергнуть ее пока не смогли.
Что такое жесткость воды
Под жесткостью воды обычно понимается значительная концентрация солей кальция и, в меньшей степени, магния. Также на жесткость воды оказывают некоторое влияние соли железа и алюминия. Эти соли называют солями жесткости. При нагревании эти соединения выпадают в осадок, из которого и получается накипь. По своему химическому строению эта накипь схожа с мелом или известняком.
Необходимо отметить, что есть два вида жесткости воды - временная и постоянная. Временная, или карбонатная жесткость, обусловлена наличием в воде гидрокарбонатов и карбонатов все тех же кальция и марганца. При нагревании карбонаты выпадают в осадок, в результате чего вода после кипячения становится менее жесткой.
Постоянная жесткость вызывается присутствием солей серной соляной и азотной кислот. После кипячения они не образуют осадка, а остаются в воде.
Основную угрозу для бытовой техники, работа которой связана с нагревом воды, представляет именно постоянная карбонатная жесткость.
Как определить тип жесткости по результатам анализа воды
В большинстве случаев, в результатах анализа указывается общая жесткость, то есть суммарное количество временных и постоянных солей жесткости. Но сохраняется возможность вычислить их значения за счет такого параметра, как щелочность. Если щелочность равна или больше параметра жесткости, значит, вся жесткость относится к временной. Если меньше, значит количество солей временной жесткости равно показателю щелочности, а все остальное относится к постоянной.
Считается, что в ситуации, когда временная жесткость не более 2 мг на литр, можно обойтись без специальных мер по умягчению воды. А вот если этот параметр оказался выше, то стоит всерьез задуматься об установке умягчителя воды.
В существующих стандартах жесткость воды оценивается очень по-разному. Можно отметить, что в Европе жесткой считается вода с показателем всего в 3 – 3,6 мг-экв на литр.
| Жесткость воды в мг-экв на литр | Справочник по гидрохимии | Водоподготовка | DIN 19643 (Германия) | USEPA |
| 0-1,5 | Мягкая | Очень мягкая | Мягкая | Мягкая |
| 1,5-1,6 | Мягкая | Умеренно мягкая | ||
| 1,6-2,4 | Средней жесткости | |||
| 2,4-3,0 | Достаточно жесткая | |||
| 3,0-3,6 | Умеренной жесткости | Жесткая | ||
| 3,6-4,0 | Жесткая | |||
| 4,0-6,0 | Средней жесткости | |||
| 6,0-8,0 | Жесткая | Очень жесткая | Очень жесткая | |
| 8,0-9,0 | Жесткая | |||
| 9,0-12,0 | Очень жесткая | |||
| Более 12 | Очень жесткая |
ofiltrah.ru
Жёсткая вода - это... Что такое Жёсткая вода?
Жёсткость воды — совокупность химических и физических свойств воды, связанных с содержанием в ней растворённых солей щёлочноземельных металлов, главным образом, кальция и магния. Вода с большим содержанием таких солей называется жёсткой, с малым содержанием — мягкой. Различают временную жёсткость, образованную гидрокарбонатами и постоянную жёсткость, вызванную присутствием других солей. Временная жёсткость может быть устранена кипячением.
Жёсткая вода при умывании сушит кожу, в ней плохо образуется пена при использовании мыла. Использование жёсткой воды вызывает появление осадка (накипи) на стенках котлов, в трубах и т. п. В тоже время, использование слишком мягкой воды может приводить к коррозии труб, так как, в этом случае отсутствует кислотно-щелочная буферность, которую обеспечивает гидрокарбонатная (временная) жёсткость. Потребление жёсткой или мягкой воды обычно не является опасным для здоровья, хотя есть данные о том, что высокая жёсткость способствует образованию мочевых камней, а низкая — незначительно увеличивает риск сердечно-сосудистых заболеваний.
Жёсткость природных вод может варьироваться в довольно широких пределах и в течение года непостоянна. Увеличивается жёсткость из-за испарения воды, уменьшается в сезон дождей, а также в период таяния снега и льда.
Единицы измерения
Для численного выражения жёсткости воды указывают концентрацию в ней катионов кальция и магния.
Рекомендованная единица СИ для измерения концентрации — моль на кубический метр (моль/м3), однако, на практике для измерения жёсткости чаще используется миллимоль на литр (ммоль/л).В России для измерения жёсткости чаще используется нормальная концентрация ионов кальция и магния, выраженная в миллиграмм-эквивалентах на литр (мг-экв/л). Один мг-экв/л соответствует содержанию в литре воды 20,04 миллиграмм Ca2+ или 12,16 миллиграмм Mg2+ (атомная масса делённая на валентность).
Иногда указывают концентрацию, отнесённую к единице массы, а не объёма, особенно, если температура воды может изменяться или если вода может содержать пар, что приводит к существенным изменениям плотности.
В разных странах использовались (иногда используются до сих пор) различные внесистемные единицы — градусы жёсткости.
| Немецкий | °dH (dergees of hardness),°dGH (German (Deutsche) Hardness),°dKH (для карбонатной жёсткости) | 1 часть оксида кальция (СаО) или 0.719 частей оксида магния (MgO) на 100 000 частей воды | 0,357 | 0,179 |
| Английский | °e | 1 гран CaCO3 на 1 английский галлон воды | 0,285 | 0,142 |
| Французский | °TH | 1 часть CaCO3 на 100000 частей воды | 0,200 | 0,100 |
| Американский | 3 на 1 000 000 частей воды | 0,02 | 0,01 |
В СССР до 1952 года использовали градусы жёсткости, совпадавшие с немецкими.
По величине общей жёсткости различают воду мягкую (до 2 мг-экв/л), средней жесткости (2-10 мг-экв/л) и жёсткую (более 10 мг-экв/л). Жёсткость воды поверхностных источников существенно колеблется в течение года; она максимальна в конце зимы, минимальна — в период паводка (например, жёсткость волжской воды в марте — 4,3 мг-экв/л, в мае — 0,5 мг-экв/л[1]). В подземных водах жёсткость обычно выше (до 80-100 мг-экв/л) и меньше изменяется в течение года.
Методы устранения
Обратный осмос. Метод основан на прохождении воды через полупроницаемые мембраны (как правило, полиамидные). Вместе с солями жёсткости удаляется и большинство других солей. Эффективность очистки может достигать 99,9 %. Этот метод нашёл наибольшее применение в бытовых системах подготовки питьевой воды. В качестве недостатка данного метода следует отметить необходимость предварительной подготвки воды, подаваемой на обратноосмотическую мембрану.
Электродиализ. Основан на удалении из воды солей под действием электрического поля. Удаление ионов растворенных веществ происходит за счёт специальных мембран. Так же как и при использовании технологии обратного осмоса, происходит удаление и других солей, помимо ионов жёсткости.
Термический способ. Основан на нагреве воды, устраняет только временную (карбонатную) жёсткость. Находит применение в быту. В промышленности применяется, например, на ТЭЦ.
Реагентное умягчение. Метод основан на добавлении в воду соды или гашеной извести. При этом соли кальция и магния переходят в нерастворимые соединения и, как следствие, выпадают в осадок. Этот метод оправдан при относительно больших расходах воды, поскольку связан с решением ряда специфических проблем: фильтрации осадка, точной дозировки реагента.
Катионирование. Метод основан на использовании ионообменной гранулированной загрузки (чаще всего ионообменные смолы). Такая загрузка при контакте с водой поглощает катионы солей жёсткости (кальций и магний). Взамен, в зависимости от ионной формы, отдавая ионы натрия или водорода. Эти методы соответственно называются Na-катионирование и Н-катионирование. Как правило, жёсткость воды снижается при одноступенчатом натрий-катионировании до 0,05-0,1 мг-экв/л, при двухступенчатом — до 0,01 мг-экв/л.
Ссылки
Примечания
- ↑ Химическая энциклопедия. — М.: Советская энциклопедия, 1990. Т. 2. С. 145.
Wikimedia Foundation. 2010.
dic.academic.ru
Жесткая вода на участке: что делать?
Если ваш участок находится в населенном пункте, где забор водопроводной воды происходит из подземных вод (особенно из глубоких слоев грунта), то наверняка вы знакомы с такой проблемой, как жесткая вода. Также с повышенной жесткостью воды могут столкнуться владельцы участков с установленной на нем скважиной.

Что такое жесткая вода
Это вода с веществами горных пород, с которыми она соприкасалась долгое время (чем продолжительнее контакт, тем больше соединений в воде). Какие соединения присутствуют именно в вашей воде может подсказать состав пластов грунта и горных пород местности - обычно это соли жесткости и высокое содержание железа, магния или кальция.
Чем опасна вода с повышенным уровнем жесткости
Если один раз выпить стакан с жесткой водой, не произойдет абсолютно ничего, можете только почувствовать металлический привкус. А вот если употреблять в пищу и питье такую воду долгое время, то именно из-за нее могут образовываться камни в почках, накапливаться соли в суставах, может ухудшиться состояние кожи и волос - жесткая вода сушит их. Если говорить о неудобствах использования жесткой воды, то это вечный налет в чайнике, засор труб и шлангов, укорочение срока службы стиральной машины и других нагревательных элементов.

Как понять, что вода на участке жесткая
Во-первых, можно определить, хорошая вода или нет, воспользовавшись народными средствами. Первый способ - самый простой: капните на зеркало водой и дождитесь высыхания. Если капли оставили сильный след - вода жесткая, если след слегка различим - мягкая. Способ номер два: воспользоваться моющими средствами и посмотреть на количество пены. Дело в том, что жесткая вода значительно снижает образование пены и моющие качества средств.

Но самым точным методом был и будет измерение качеств воды в лаборатории. Существуют специальные меры жесткости, которыми и будут руководствоваться специалисты:
- мягкая вода - содержание солей не более 2 мг-экв/л;
- нормальная - содержание солей в пределах 2-4 мг-экв/л;
- жесткая - содержание солей в пределах 4-6 мг-экв/л;
- вода повышенной жесткости - содержание солей выше 6 мг-экв/л.
Стандарты питьевой воды в нашей стране таковы, что предельное значение концентрации солей жесткости установлено на уровне 7,0 мг-экв/л. Стоит отметить, что в странах Европы этот показатель не может превышать 3,0 мг-экв/л.

Методы снижения жесткости воды
Кипячение. Самый древний и простой способ умягчения воды и снижения в ней количества солей. Кипячение помогает в тех случаях, когда вода насыщена соединениями гидрокарбоната кальция (это соединение и образует осадок на чайнике при нагревании) и сульфата кальция. Не поможет кипячение, если вода насыщена магнием. Основные минусы данного метода - низкая производительность и испорченные бытовые приборы.

Мембранный способ. Принцип работы этого способа заключается в специальных молекулярных мембранах, которые задерживают прохождение посторонних примесей и солей в питьевую воду. Эффективность мембранного метода довольно высока - около 98%.
Реагентный или химический способ. Такой способ подходит для смягчения воды, которая используется только для хозяйственных нужд - из-за присутствия реагентов (известь, соединения натрия, сода и синтетические соединения, например, тринатрийфосфат) такую воду пить нельзя. Подбор реагентов ведется строго в зависимости от наличия тех или иных соединений и солей в воде.

Магнитный и электромагнитный способ. Данный способ основывается на воздействии на соли и примеси магнитным полем, проходя через которое, они теряют свойство выпадать в виде осадка. По сути, этот метод не удаляет соединения, придающие жесткость воде, он просто избавляет вас от неприятного осадка на трубах и бытовых приборах. Электромагнитный способ отличается тем, что при его применении выведенные из воды примеси сами удаляются в канализацию.

Ионообменный способ. По сути, приборы, использующие этот принцип смягчения воды, меняют ионы кальция и магния на ионы натрия, которые, в отличие от первых двух, абсолютно безопасны для здоровья и не оставляют осадка.

Стоит отметить, что в наше время создаются такие системы очистки и смягчения воды, в которых может применяться комбинация из нескольких методов, описанных выше. Чтобы узнать, какой способ подойдет для смягчения воды в вашей местности, следует обратиться в службу очистки воды города или региона. опубликовано econet.ru
econet.ru
Жесткая вода. Что делать? на Supersadovnik.ru
Вещи не отстирываются, мыло едва мылится, трубы зарастают известковыми отложениями, а на тэнах стиральной машины или водонагревателя образуется толстый слой накипи. Причина – жесткая вода, явление в наших краях весьма распространенное.
Виновники проблемы – соли магния и кальция, так называемые соли жесткости. Образованная ими накипь не только может привести к поломке бытовой техники, но и значительно увеличивает энергопотребление водонагревательного оборудования, что приводит к росту счетов за электричества. Правда, с проблемой можно бороться.
Мягкое воздействие
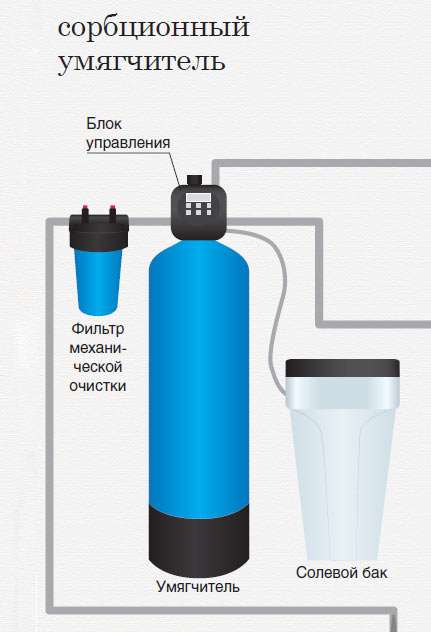
По-настоящему умягчить воду можно, только удалив из нее соли жесткости. Для этого применяют устройства умягчения с ионообменной смолой, содержащей ионы натрия. В комплектацию большинства умягчителей, представленных на рынке, включены емкость со смолой, бак для соли, а также блок управления установкой, способный менять режим работы автоматически.

Размеры и внешний вид установок могут разниться. Также различаются они и по производительности. Далеко не всегда требуется быстрое умягчение больших объемов воды. В умягченной воде можно мыться, использовать ее для приготовления пищи (предварительно очистив питьевым фильтром). Тем не менее наиболее важную роль умягчители играют в подготовке воды для водонагревательного оборудования – стиральных и посудомоечных машин, бойлеров, ЭВН и других. Поэтому часто такую установку размещают на отдельной линии, питающей именно бытовую технику. Перед устройством обязательно должны стоять фильтры механической очистки, иначе грязь может ему повредить.
Уроки химии
 Когда в емкость со смолой поступает вода, ионы кальция и магния вытесняют ионы натрия, а сами остаются в смоле. В результате соли, придающие жесткость воде, заменяются солями натрия, которые куда безобиднее, по крайней мере, не выпадают в виде накипи. После подобной обработки вода становится мягкой, порой даже слишком. Отрегулировать жесткость воды на выходе можно, подмешивая к умягченной воде обычную. Рано или поздно запасы натрия в смоле истощаются, но она способна к восстановлению своих свойств. Для регенерации смолу заливают концентрированным раствором обычной поваренной соли, и начинается обратный процесс – содержащиеся в «рассоле» ионы натрия вытесняют ранее захваченные смолой ионы кальция и магния. Использованный раствор сливается, а установка снова готова к работе. Пока идет регенерация, умягчать воду в этой же емкости невозможно. Эту проблему решают разными способами. Существуют модели, в которых автоматика следит за уровнем натрия. Если становится понятно, что запасы иссякнут "уже завтра", она проводит регенерацию досрочно (например, ночью). Более дорогостоящий вариант – установка с двумя емкостями со смолой. Пока одна находится в состоянии регенерации, вторая умягчает воду.
Когда в емкость со смолой поступает вода, ионы кальция и магния вытесняют ионы натрия, а сами остаются в смоле. В результате соли, придающие жесткость воде, заменяются солями натрия, которые куда безобиднее, по крайней мере, не выпадают в виде накипи. После подобной обработки вода становится мягкой, порой даже слишком. Отрегулировать жесткость воды на выходе можно, подмешивая к умягченной воде обычную. Рано или поздно запасы натрия в смоле истощаются, но она способна к восстановлению своих свойств. Для регенерации смолу заливают концентрированным раствором обычной поваренной соли, и начинается обратный процесс – содержащиеся в «рассоле» ионы натрия вытесняют ранее захваченные смолой ионы кальция и магния. Использованный раствор сливается, а установка снова готова к работе. Пока идет регенерация, умягчать воду в этой же емкости невозможно. Эту проблему решают разными способами. Существуют модели, в которых автоматика следит за уровнем натрия. Если становится понятно, что запасы иссякнут "уже завтра", она проводит регенерацию досрочно (например, ночью). Более дорогостоящий вариант – установка с двумя емкостями со смолой. Пока одна находится в состоянии регенерации, вторая умягчает воду.
Есть одно "но": солевые стоки, образующиеся при регенерации смолы, нужно утилизировать. Если дом подключен к централизованной системе канализации, проблем нет, а вот при сливе солевого раствора в септик нужно быть очень осторожными. По правилам - делать это нельзя. Практика показывает, что большинство именно так и поступают, утверждая, что на работе аэросептиков такое "вливание" не сказывается, просто в септики биологической очистки приходится чаще добавлять бактерии.
"Несоленые" варианты
Если по каким-то причинам в доме сложно пользоваться умягчителем на основе ионообменной смолы, можно обратиться к альтернативным способам защиты от накипи. Ведь чтобы соли не образовывали отложений на тэнах, достаточно перевести их в такие соединения, которые не выпадают в осадок. Добиться этого можно, добавляя в воду химические вещества, связывающие соли жесткости, либо воздействуя на нее магнитным полем или электромагнитным излучением.
- Установки-дозаторы, подмешивающие в воду химические реагенты, недороги сами по себе, но требуют периодического наполнения активными веществами. Выглядит дозатор как колба, засыпанная кристаллами или порошком. Такие установки лучше ставить на линию холодной воды, подающую воду для бытовой техники.
- Магнитные преобразователи тоже недороги. Их устанавливают прямо в систему водоснабжения, причем на качество питьевой воды они не влияют, потому что не используют никакой химии.
- Электромагнитные установки самые дорогие, но наиболее эффективные. Они хорошо подстраиваются под разные условия работы. Обработанная ими вода безопасна для здоровья.
Связывание солей жесткости решает проблему не полностью, а лишь частично – защищает водонагревательные приборы от известковых отложений. Вода при этом не становится мягкой. Проще говоря, накипь оседать на тэнах перестанет, а вот мыло лучше мылиться не будет.

Для бытовой техники жесткая вода опасна – это факт. А как насчет человека? Соли жесткости – это соединения кальция и магния, полезных для организма. Большую часть этих веществ мы получаем из пищи, но и вода тоже служит источником минералов. Поэтому пить жесткую воду можно. А вот в использовании такой воды для водных процедур приятного мало: на коже и волосах создается тонкая пленка, которая вызывает ощущение сухости и дискомфорта.
www.supersadovnik.ru
Чем вредна жесткая вода и как ее смягчить
Какая вода жесткая и как ее смягчить
 - А почему у вас в чайнике столько накипи (голова грязная, белье плохо выстиранное)? - А потому что у нас вода жесткая! - Именно так звучит универсальный ответ на уйму бытовых претензий. Но давайте ка разберемся, друзья, что вообще такое жесткая и мягкая вода, для каких целей какая подходит и как при необходимости смягчить (или ужесточить) льющуюся из крана/смесителя жидкость. Кстати, Всемирным днем мониторинга качества воды считается 18 сентября.
- А почему у вас в чайнике столько накипи (голова грязная, белье плохо выстиранное)? - А потому что у нас вода жесткая! - Именно так звучит универсальный ответ на уйму бытовых претензий. Но давайте ка разберемся, друзья, что вообще такое жесткая и мягкая вода, для каких целей какая подходит и как при необходимости смягчить (или ужесточить) льющуюся из крана/смесителя жидкость. Кстати, Всемирным днем мониторинга качества воды считается 18 сентября.Еще одна полезная статья о воде, опубликованная ранее: "Нужно ли заставлять себя пить воду".
Почему вода бывает жесткой
Жесткость - это химическое понятие, которым спецы обозначают содержание в аш-два-о солей кальция и магния (их вода, находящаяся в земле, вбирает в себя из известковых пород). Чем больше таких пород встретилось на пути ручейка, тем вода насыщеннее солями и, соответственно, жестче; чем меньше - тем мягче.Но это еще не все. Жесткость воды бывает временной и постоянной - в зависимости от вида солей.
Временную жесткость вызывают водорастворимые соли. При нагреве воды они распадаются и образуют тот самый осадок на чайнике или нагревательном элементе стиральной машины, который рано или поздно выводит бытовые приборы из строя.Постоянная жесткость - это "заслуга нерастворимых солей". Они не распадаются при кипячении и остаются в воде постоянно, портят нам головомойку, отчасти накапливаются на смесителях и кранах (к слову, смесители "Grohe": http://m.ua/kata/62/grohe/) и нагружают организм вредностями и болячками (например, мочекаменной болезнью).
Как определить жесткость воды
Специалисты делают это с помощью электроники (в магазинах для аквариумистов можно купить прибор кондуктометр, он же "солемер" - его показания сверяют с таблицами и высчитывают жесткость воды) или экспресс-тестов жесткости (их можно встретить в аптеках или зоомагазинах).Но есть и более простые, доступные каждому способы.
Подручные способы, позволяющие определить жесткая ли воды
- Попробовать намылить руки. В жесткой воде пены практически не получается или она будет едва заметна, как бы вы не старались. А вот в мягкой вполне удастся соорудить на руках пенного "барашка";
- Вспомнить, как часто вам приходится мыть чайник от накипи. Если его донышко и стенки обрастают заметной серой пленкой уже через 7-10 кипячений - вода у вас однозначно жесткая;
- Заварить чай. Любителям янтарного напитка давно известно, что от состава воды зависит интенсивность чая и время его приготовления. Если вода мягкая, то бодрящий напиток заварится уже через 3-4 минуты. А в жесткой чаинки будут отдавать вкус не менее 7-10 минут.
Как смягчить жесткую воду
Метод решения данного вопроса зависит от того, для чего именно вы собираетесь использовать жидкость:- Для питья - бытовые фильтры-кувшины: емкости объемом до трех литров, в которых находится сменный фильтрующий картридж. Это один из самых экономных способов смягчения воды для питья: кувшин стоит от 7-8$, картридж к нему - от 3-4$ (требуется замена раз в месяц-два). Но для посудомоечной или стиральной машины этот вариант неприемлем;
- Для безопасной работы бытовых приборов - таблетки или порошок с содержанием смягчающих солей. Таблетки (стоимостью около 1-2$ за 10 шт.) являются обязательными для владельцев посудомоечных машин. Они помогают продлить жизнь прибору, оберегая его нагревательный элемент от накипи. Но в пищу смягченная таким образом вода категорически не подходит;
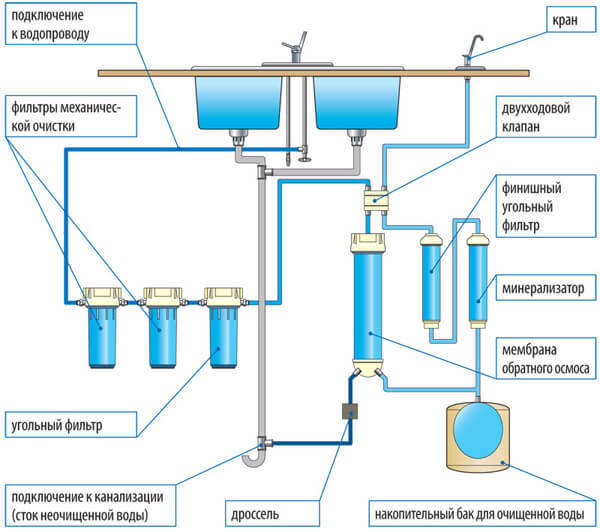
- Для питья и для безопасности техники - фильтры для воды, которые устанавливаются на системы водоснабжения в доме (так называемые фильтры с системой обратного осмоса). Цена вопроса: от 90-110$ + установка. Внутри них вода проходит через особые мембраны, где оседают соли и вредные бактерии.
А можно не смягчать воду
В принципе можно, но осторожно. Тем не менее, я бы все таки рекомендовал использовать какие-либо фильтрующие системы, пожертвовав вкусом воды ради соль бесценного здоровья и долголетия. По сути именно соли придают воде неповторимый "ключевой" вкус, а их отсутствие делает воду невкусной. Но, если все же выберите вкус, пожертвовав качеством, для этого вы должны быть уверены, что жесткость воды находится в рамках нормы - согласно ВОЗ, это 1-2 градуса жесткости. Выяснить, сколько именно градусов у вас, можно только специальными приборами (например, тем же экспресс-тестом или солемером). На этом все, друзья. Огромной всем удачи, вкусной, но очень чистой воды и крепкого здоровья :-)vkus-uspexa.ru
Жёсткость воды - это... Что такое Жёсткость воды?
Жёсткость воды — совокупность химических и физических свойств воды, связанных с содержанием в ней растворённых солей щёлочноземельных металлов, главным образом, кальция и магния (так называемых «солей жёсткости»).
Жёсткая и мягкая вода
Вода с большим содержанием таких солей называется жёсткой, с малым содержанием — мягкой.
Различают временную (карбонатную) жёсткость, обусловленную гидрокарбонатами кальция и магния (Са(НСО3)2; Mg(НСО3)2), и постоянную (некарбонатную) жёсткость, вызванную присутствием других солей, не выделяющихся при кипячении воды: в основном, сульфатов и хлоридов Са и Mg (CaSO4, CaCl2, MgSO4, MgCl2).Жёсткая вода при умывании сушит кожу, в ней плохо образуется пена при использовании мыла. Использование жёсткой воды вызывает появление осадка (накипи) на стенках котлов, в трубах и т. п. В то же время, использование слишком мягкой воды может приводить к коррозии труб, так как, в этом случае отсутствует кислотно-щелочная буферность, которую обеспечивает гидрокарбонатная (временная) жёсткость. Потребление жёсткой или мягкой воды обычно не является опасным для здоровья,есть данные о том, что высокая жёсткость способствует образованию мочевых камней, а низкая — незначительно увеличивает риск сердечно-сосудистых заболеваний. Вкус природной питьевой воды, например, воды родников, обусловлен именно присутствием солей жёсткости.
Жёсткость природных вод может варьироваться в довольно широких пределах и в течение года непостоянна. Увеличивается жёсткость из-за испарения воды, уменьшается в сезон дождей, а также в период таяния снега и льда.
Единицы измерения
Для численного выражения жёсткости воды указывают концентрацию в ней катионов кальция и магния. Рекомендованная единица СИ для измерения концентрации — моль на кубический метр (моль/м³), однако, на практике для измерения жёсткости используются градусы жёсткости и миллиграммы эквивалента на литр (мг-экв/л).
В СССР до 1952 года использовали градусы жёсткости, совпадавшие с немецкими. В России для измерения жёсткости иногда использовалась нормальная концентрация ионов кальция и магния, выраженная в миллиграммах эквивалента на литр (мг-экв/л). Один мг-экв/л соответствует содержанию в литре воды 20,04 миллиграмм Ca2+ или 12,16 миллиграмм Mg2+ (атомная масса делённая на валентность).
С 1 января 2005 года в России введен новый Национальный стандарт Российской Федерации ГОСТ Р 52029-2003 «Вода. Единица жесткости»[1]. По новому ГОСТу жесткость выражается в градусах жесткости (°Ж). 1 °Ж соответствует концентрации щелочноземельного элемента, численно равной 1/2 его моля на литр (1 °Ж = 1 мг-экв/л).
Иногда указывают концентрацию, отнесённую к единице массы, а не объёма, особенно, если температура воды может изменяться или если вода может содержать пар, что приводит к существенным изменениям плотности.
В разных странах использовались (иногда используются до сих пор) различные внесистемные единицы — градусы жёсткости.
| Немецкий | °dH (degrees of hardness),°dGH (German (Deutsche) Hardness),°dKH (для карбонатной жёсткости) | 1 часть оксида кальция (СаО) или 0.719 частей оксида магния (MgO) на 100 000 частей воды | 0,3566 | 0,1783 |
| Английский | °e | 1 гран CaCO3 на 1 английский галлон воды | 0,2848 | 0.1424 |
| Французский | °TH | 1 часть CaCO3 на 100000 частей воды | 0,1998 | 0,0999 |
| Американский | ppm | 1 часть CaCO3 на 1 000 000 частей воды | 0,0200 | 0,0100 |
По величине общей жёсткости различают воду мягкую (до 2 °Ж), средней жёсткости (2-10 °Ж) и жёсткую (более 10 °Ж).
Жёсткость воды поверхностных источников существенно колеблется в течение года; она максимальна в конце зимы, минимальна — в период паводка (например, жёсткость волжской воды в марте — 4,3 °Ж, в мае — 0,5 °Ж [2]). В подземных водах жёсткость обычно выше (до 80-100 °Ж) и меньше изменяется в течение года.
Методы устранения
Термоумягчение. Основан на кипячении воды, в результате термически нестойкие гидрокарбонаты кальция и магния разлагаются с образованием накипи:
Ca(HCO3)2 → CaCO3↓ + CO2 + h3O.Кипячение устраняет только временную (карбонатную) жёсткость. Находит применение в быту.
Реагентное умягчение. Метод основан на добавлении в воду кальцинированной соды Na2CO3 или гашёной извести Ca(OH)2. При этом соли кальция и магния переходят в нерастворимые соединения и, как следствие, выпадают в осадок. Например, добавление гашёной извести приводит к переводу солей кальция в нерастворимый карбонат:
Ca(HCO3)2 + Ca(OH)2 → 2CaCO3↓ + 2h3OЛучшим реагентом для устранения общей жесткости воды является ортофосфат натрия Na3PO4, входящий в состав большинства препаратов бытового и промышленного назначения:
3Ca(HCO3)2 + 2Na3PO4 → Ca3(PO4)2↓ + 6NaHCO3 3MgSO4 + 2Na3PO4 → Mg3(PO4)2↓ + 3Na2SO4Ортофосфаты кальция и магния очень плохо растворимы в воде, поэтому легко отделяются механическим фильтрованием. Этот метод оправдан при относительно больших расходах воды, поскольку связан с решением ряда специфических проблем: фильтрации осадка, точной дозировки реагента.
Катионирование. Метод основан на использовании ионообменной гранулированной загрузки (чаще всего ионообменные смолы). Такая загрузка при контакте с водой поглощает катионы солей жёсткости (кальций и магний, железо и марганец). Взамен, в зависимости от ионной формы, отдавая ионы натрия или водорода. Эти методы соответственно называются Na-катионирование и Н-катионирование. При правильно подобранной ионообменной загрузке жёсткость воды снижается при одноступенчатом натрий-катионировании до 0,05-0,1 °Ж, при двухступенчатом — до 0,01 °Ж. В промышленности с помощью ионообменных фильтров заменяют ионы кальция и магния на ионы натрия и калия, получая мягкую воду.
Обратный осмос. Метод основан на прохождении воды через полупроницаемые мембраны (как правило, полиамидные). Вместе с солями жёсткости удаляется и большинство других солей. Эффективность очистки может достигать 99,9 %. Этот метод нашёл наибольшее применение в бытовых системах подготовки питьевой воды. В качестве недостатка данного метода следует отметить необходимость предварительной подготовки воды, подаваемой на обратноосмотическую мембрану.
Электродиализ. Основан на удалении из воды солей под действием электрического поля. Удаление ионов растворенных веществ происходит за счёт специальных мембран. Так же как и при использовании технологии обратного осмоса, происходит удаление и других солей, помимо ионов жёсткости.
Полностью очистить воду от солей жёсткости можно дистилляцией.
См. также
- Кислые соли
- Щелочи
- Сульфаты
- Хлораты
Ссылки
Примечания
med.academic.ru
Жесткая вода - это... Что такое Жесткая вода?
Жёсткость воды — совокупность химических и физических свойств воды, связанных с содержанием в ней растворённых солей щёлочноземельных металлов, главным образом, кальция и магния. Вода с большим содержанием таких солей называется жёсткой, с малым содержанием — мягкой. Различают временную жёсткость, образованную гидрокарбонатами и постоянную жёсткость, вызванную присутствием других солей. Временная жёсткость может быть устранена кипячением.
Жёсткая вода при умывании сушит кожу, в ней плохо образуется пена при использовании мыла. Использование жёсткой воды вызывает появление осадка (накипи) на стенках котлов, в трубах и т. п. В тоже время, использование слишком мягкой воды может приводить к коррозии труб, так как, в этом случае отсутствует кислотно-щелочная буферность, которую обеспечивает гидрокарбонатная (временная) жёсткость. Потребление жёсткой или мягкой воды обычно не является опасным для здоровья, хотя есть данные о том, что высокая жёсткость способствует образованию мочевых камней, а низкая — незначительно увеличивает риск сердечно-сосудистых заболеваний.
Жёсткость природных вод может варьироваться в довольно широких пределах и в течение года непостоянна. Увеличивается жёсткость из-за испарения воды, уменьшается в сезон дождей, а также в период таяния снега и льда.
Единицы измерения
Для численного выражения жёсткости воды указывают концентрацию в ней катионов кальция и магния.
Рекомендованная единица СИ для измерения концентрации — моль на кубический метр (моль/м3), однако, на практике для измерения жёсткости чаще используется миллимоль на литр (ммоль/л).В России для измерения жёсткости чаще используется нормальная концентрация ионов кальция и магния, выраженная в миллиграмм-эквивалентах на литр (мг-экв/л). Один мг-экв/л соответствует содержанию в литре воды 20,04 миллиграмм Ca2+ или 12,16 миллиграмм Mg2+ (атомная масса делённая на валентность).
Иногда указывают концентрацию, отнесённую к единице массы, а не объёма, особенно, если температура воды может изменяться или если вода может содержать пар, что приводит к существенным изменениям плотности.
В разных странах использовались (иногда используются до сих пор) различные внесистемные единицы — градусы жёсткости.
| Немецкий | °dH (dergees of hardness),°dGH (German (Deutsche) Hardness),°dKH (для карбонатной жёсткости) | 1 часть оксида кальция (СаО) или 0.719 частей оксида магния (MgO) на 100 000 частей воды | 0,357 | 0,179 |
| Английский | °e | 1 гран CaCO3 на 1 английский галлон воды | 0,285 | 0,142 |
| Французский | °TH | 1 часть CaCO3 на 100000 частей воды | 0,200 | 0,100 |
| Американский | 3 на 1 000 000 частей воды | 0,02 | 0,01 |
В СССР до 1952 года использовали градусы жёсткости, совпадавшие с немецкими.
По величине общей жёсткости различают воду мягкую (до 2 мг-экв/л), средней жесткости (2-10 мг-экв/л) и жёсткую (более 10 мг-экв/л). Жёсткость воды поверхностных источников существенно колеблется в течение года; она максимальна в конце зимы, минимальна — в период паводка (например, жёсткость волжской воды в марте — 4,3 мг-экв/л, в мае — 0,5 мг-экв/л[1]). В подземных водах жёсткость обычно выше (до 80-100 мг-экв/л) и меньше изменяется в течение года.
Методы устранения
Обратный осмос. Метод основан на прохождении воды через полупроницаемые мембраны (как правило, полиамидные). Вместе с солями жёсткости удаляется и большинство других солей. Эффективность очистки может достигать 99,9 %. Этот метод нашёл наибольшее применение в бытовых системах подготовки питьевой воды. В качестве недостатка данного метода следует отметить необходимость предварительной подготвки воды, подаваемой на обратноосмотическую мембрану.
Электродиализ. Основан на удалении из воды солей под действием электрического поля. Удаление ионов растворенных веществ происходит за счёт специальных мембран. Так же как и при использовании технологии обратного осмоса, происходит удаление и других солей, помимо ионов жёсткости.
Термический способ. Основан на нагреве воды, устраняет только временную (карбонатную) жёсткость. Находит применение в быту. В промышленности применяется, например, на ТЭЦ.
Реагентное умягчение. Метод основан на добавлении в воду соды или гашеной извести. При этом соли кальция и магния переходят в нерастворимые соединения и, как следствие, выпадают в осадок. Этот метод оправдан при относительно больших расходах воды, поскольку связан с решением ряда специфических проблем: фильтрации осадка, точной дозировки реагента.
Катионирование. Метод основан на использовании ионообменной гранулированной загрузки (чаще всего ионообменные смолы). Такая загрузка при контакте с водой поглощает катионы солей жёсткости (кальций и магний). Взамен, в зависимости от ионной формы, отдавая ионы натрия или водорода. Эти методы соответственно называются Na-катионирование и Н-катионирование. Как правило, жёсткость воды снижается при одноступенчатом натрий-катионировании до 0,05-0,1 мг-экв/л, при двухступенчатом — до 0,01 мг-экв/л.
Ссылки
Примечания
- ↑ Химическая энциклопедия. — М.: Советская энциклопедия, 1990. Т. 2. С. 145.
Wikimedia Foundation. 2010.
dic.academic.ru




















