Справочник химика 21. Вода углерод
Общий органический углерод
Общий органический углерод (ТОС) — это та часть растворенного и нерастворенного органического вещества, которая присутствует в воде. Она не дает информации о природе органического вещества. Органический углерод может быть определен до анализа или определен в составе ТОС, а затем получен путем вычитания содержания неорганического углерода из общего содержания углерода.[ ...]
При общей очистке стоков с переменным составом неэффективно использовать специфические сорбенты, обладающие селективными свойствами. Так, если очистку общих стоков химического предприятия ведут на сугубо микропористом ГАУ, обладающем хорошей емкостью по ароматическим соединениям, то в первый период работы на АУ извлекается 70—80% органических веществ, а при изменении состава сточных вод — лишь 20— 40% загрязнений. Фирмой Са оп Согр. выполнен большой статистический анализ 222 случаев сорбционной очистки на АУ промышленных стоков 68 производств 15 отраслей. Оказалось, что в 5 случаях из 8 содержание общего органического углерода (ООУ) снижалось более чем на 90%, и лишь в двух менее чем на 85%; в 6 случаях из 7 цветность снижалась более чем на 95% и лишь в одном — менее чем на 90%. В целом, в 4/9 проб исходное содержание ООУ было выше 100, но менее 1000 мг/дм3, и в стольких же выше 1000 мг/дм3.[ ...]
Если органическое вещество окисляется, то можно определить потребление кислорода (анализ ХПК, ВПК, ОПК) или количество выделяющегося СОг (анализ общего органического углерода ООУ).[ ...]
Летучие органические вещества, такие как бензол, толуол, цикло-гексан и хлороформ могут испаряться при десорбции диоксида углерода. Общий органический углерод в этом случае должен определяться отдельно, если это невозможно, следует применять другой метод.[ ...]
Растворенные органические соединения включают синтетические химикаты, а также многие вешества растительного и животного происхождения. Количество органических примесей в воде выражается, в оснвном, при помоши двух показателей: химической и биологической потребности в кислороде. Под химической потребностью в кислороде (ХПК) понимают количество кислорода (мг/л), необходимого для окисления органических вешеств, находящихся в сточной воде, до СС , Н2О и N0- . Для определения ХПК применяется стандартная методика, по которой в качестве окислителя используется бихромат калия К2 Сг20. Количество кислорода (мг/л), необходимое для биохимического окисления (разложения) органических соединений, содержащихся в сточной воде, называется биологической потребностью в кислороде (ВПК). В зависимости от продолжительности определения различают БПК (за пять суток), а также БПКполн (полное). Однако оба эти показателя являются несовершенными для определения содержания органических веществ в воде в силу ряда причин: неспособности к биоразложению ряда органических веществ, окисления некоторых неорганических веществ, находящихся в этой же воде и т.д. Поэтому существует еще один показатель для определения органических примесей в воде - содержание общего органического углерода (00У, мг/л), которое измеряется путем окисления всех органических веществ до диоксида углерода.[ ...]
Схема анализа органических веществ подземных вод, основанная на экстракции хлороформом при различных pH нелетучих битумных компонентов, отгонке с водяным паром летучих веществ из кислой и щелочной сред и сорбции гумусовых веществ на активном угле, описана в работе [5]. Полноту выделения контролируют по общему органическому углероду. Данная схема дает наиболее полное представление о характере нелетучей части органических веществ, растворимой в хлороформе.[ ...]
Накопление озерного органического вещества происходит, как сказано выше, за счет поступления с водосборного бассейна (аллохтонное) и первичной продукции фотосинтезирующих озерных организмов — водорослей и высшей водной растительности (автохтонное). Содержание органического вещества в озерной воде обычно оценивается по концентрации в нем углерода. Общий органический углерод (TOC — total organic carbon) складывается из органического углерода взвесей (РОС — particulate organic carbon) и углерода растворенного органического вещества (DOC — dissolved organic carbon). Растворенное и взвешенное органическое вещество природных вод является основным регулятором метаболизма водных экосистем. Общий органический углерод по способности к биохимической деструкции подразделяется на лабильный (LOC — labile organic carbon), в первую очередь подвергающийся биохимическому окислению, и консервативный. Лабильная часть органического вещества формируется продуктами деструкции гидробионтов и их прижизненными выделениями (метаболитами). В больших озерах накопление лабильной фракции органического вещества происходит в основном за счет первичной продукции и метаболитов фитопланктона. Величина лабильной составляющей в пуле растворенного органического вещества характеризует интенсивность продукционно-де-струкционных процессов, а ее постоянство или резкие межгодовые колебания свидетельствуют о стабильности или дисбалансе экосистемы. Консервативная часть DOC — водное гуминовое вещество — представляет собой единый высокомолекулярный комплекс и формируется преимущественно аллохтонным органическим веществом.[ ...]
Определение концентрации органических веществ, содержащихся в сточных водах, является весьма сложной задачей, особенно когда речь идет об определении отдельных веществ. В лабораториях для этой цели используют хроматографию и другие методы анализа, которые затруднительно реализовать в автоматически действующей аппаратуре, пригодной для производственного контроля. Поэтому до сих пор как в лабораторной, так и в производственной практике широко используются обобщенные параметры для оценки содержания органических веществ: биохимическая потребность в кислороде (ВПК — в мг 02/л), химическая потребность в кислороде (ХПК — в мг Ог/л), общий органический углерод (ООУ — в мг С/л). Различают БПКэ и БПК25 — за 5 и 25 суток.[ ...]
Поскольку ХПК не характеризует все органические загрязнители, окисляемые до углекислоты и воды, проводят еще определение общего органического углерода. Для этого в пробе окисляют органические загрязнители. Выделяющийся С02 поглощают раствором щелочи. Оттитровав остаток щелочи кислотой, находят искомый показатель. Вычислив отношение ХПК к общему углероду, получают показатель загрязненности сточных вод органическими веществами.[ ...]
За последние годы для оценки суммарного количества органических веществ в сточных и природных водах стал использоваться еще один показатель — общий органический углерод (ООУ). При помощи современной аппаратуры ООУ определяется за несколько минут. Для определения требуется весьма небольшое количество воды (20—50 мкл). Само собой разумеется, что в возможной непредставительности такой малообъемной пробы воды и в необходимости ее тщательной подготовки (удаление даже самых незначительных количеств нерастворимых частиц, растворенного С02 и т. п.) кроются неточности этого метода. Указанные недостатки устраняются тщательной предварительной подготовкой пробы и статистической обработкой результатов большого числа повторных анализов.[ ...]
Качество воды. Руководство по определению общего органического углерода (ТОС).[ ...]
Имеются и отечественные работы по суммарному определение органического углерода в воздухе, в частности в отходящих газах производства синтетических жирных кислот [233]. Анализ проводили в такой последовательности: отобранную в газовую пипетку пробу вытесняли затаорной жидкостью в печь для сжигания на окиси меди, поглощали образующийся углекислый газ гидратом бария и избыток его оттитровывэли. Содержание С02 в газах предварительно определяли на ВТМ-2. По сути метод является модификацией метода определения углеводородов на ВТИ-2, в который добавлена стадия титрования. Однако он не учитывает ошибок, имеющих место при отборе газовых проб в сосуды, и, естественно, пользуясь им нельзя получить достоверные данные о количестве общего органического углерода в газах.[ ...]
| 8.3 | 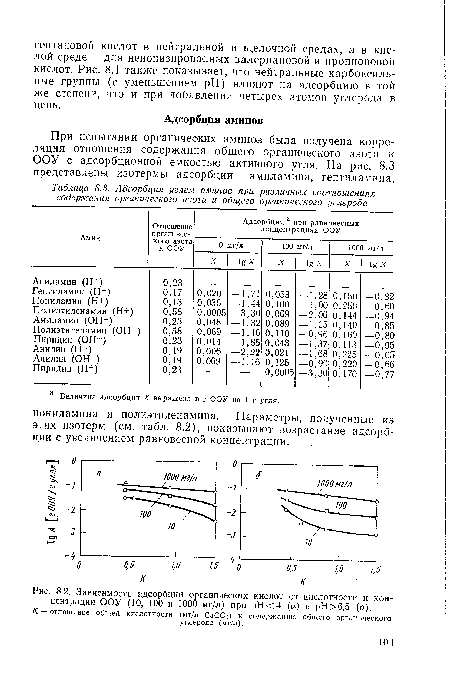 |
В лабораториях, занимающихся анализом загрязнений сточных и природных вод, общий органический углерод определяют и хроматографически. Однако эта методика не имеет преимуществ перед изложенной ни по простоте, ни по точности определений. Кроме того, она не обладает экспрессностью метода высокотемпературного сжигания.[ ...]
Наиболее эффективным методом удаления из очищенных сточных вод остаточных растворенных органических соединений, в том числе биологически неокисляемых, является сорбция активным углем. Этот метод позволяет на стадии доочистки сточных вод снизить концентрацию органических соединений на 90—99%. На. станциях биологической очистки сточных вод снижение общего органического углерода активным углем обеспечивается с 15—20 до 1—3 мг/л.[ ...]
Обратим внимание на значения символов в уравнении (4.2): С — это концентрация (в единицах ХПК, БПК, азота, общего органического углерода и т. д.), 14, или гХ18 — скорость реакции, единицы измерения этой величины определяются единицами концентрации и объема У2. Если мы пользуемся параметром гХ)3, то Х2 — это концентрация активного ила.[ ...]
Глубоким содержанием наполнен перечень обобщенных показателей при мониторинге вод, характеризующих их общую загрязненность. Ими являются химическое потребление кислорода (ХПК), биохимическое потребление кислорода (БПК), общий органический углерод, растворенный органический углерод, общий азот, адсорбирующиеся органические галогениды.[ ...]
Таким образом, из рассмотренного материала можно сделать некоторые выводы. Усовершенствованный метод определения общего органического углерода Иксфельда, по-видимому, наиболее полно учитывает особенности этого анализа.[ ...]
Поэтому необходимыми величинами при определении об щесанитарного показателя вредности, по которым нормиру егся примерно 15 % от общего количества нормируемых веществ [164], являются такие общие показатели качества вод, как биохимическое и химическое потребление кислорода и содержание общего органического углерода.[ ...]
Другими методами этой группы служат методы определения суммы нефтепродуктов после их окисления тем или иным способом. Так, например, общий органический углерод в водах определяют кондуктометрически по электропроводности конденсата после каталитического сжигания углеводородов нефти. Летучие углеводороды нефтей и нефтепродуктов после их экстракции в паровую фазу также определяют по продуктам их каталитического окисления.[ ...]
В разработанном процессе предусматривается сочетание аэробного и анаэробного окисления. Нитрификация протекает в аэробных условиях в присутствии двуокиси углерода, причём амин-ный и аммиачный азот биоокисляется до нитритов и нитратов. Денитрификация протекает в анаэробных условиях в среде био-разлагаемого продукта (обычно метанола). При этом происходит восстановление нитратов до нитритов и, в конечном счёте, до газообразного азота. Поступающие на очистку стоки имеют следующую характеристику: общий органический углерод — 3000 мг/л; ВПК — 6000 мг/л; 1Ч02, N03, 1ЧН4 в пересчёте на азот соответственно 800, 90 и 230 мг/л; органический азот в пересчёте на азот — 240 мг/л. Процесс позволяет удалять 98% ВПК и 80—90% общего азота сточных вод.[ ...]
Исследовалась агрессивность сточных вод производств хлоро-ярена, дкхлорбутадиена, 2,4-Д кислоты и окиси пропилена. Внсокошшерадизоваиные сточные воды содержали от 40 до 150 г/я № и органические примеси в количестве 1-5 г/л по общему органическому углероду СООУ). Органическими компонентами сточных вод явились хлоропрен, дихлорбутэдмен, пропилен-гликоль, проаклвкхдоргидрин, 2,4-Д кислота, гликолевая кислота и др.[ ...]
Вторым важным параметром является показатель (один или несколько), характеризующий качество сточных вод (состав и концентрацию загрязнений) . Для этой цели у нас в стране и за рубежом ведутся разработки приборов для контроля БПК, ХПК и содержания общего органического углерода. Однако пока имеются только опытные образцы таких приборов и получение серийных надежных приборов для этой цели — дело будущего. В литературе имеется сообщение, что проведенные исследования показали неприемлемость для целей управления контроля концентрации органических загрязнений в очищенной воде, поскольку изменения этого параметра происходят с большим запаздыванием и сглаживанием.[ ...]
Система классификаций продолжала развиваться по мере поступления новых сведений о водоемах разных регионов и географических широт. Лайкенс (16) привлек для Классификации пресных вод, кроме величин первичной продукции, данные по биомассе фитопланктона, содержанию хлорофилла „а” и общего органического углерода.[ ...]
К недостаткам обоих методов относится то, что одновременно окисляются различные неорганические вещества и значения ХПК нельзя целиком приравнивать БПК. Согласно грубой количественной оценке БПК составляет половину значения ХПК. Другим очень важным параметром при оценке загрязненности вод является «общий органический углерод» (ООУ). Эта величина представляет особый интерес в тех случаях, когда загрязнение связано с такими веществами, которые с трудом разлагаются микробиоло: гическим путем, как, например, лигнин, гуминовые кислоты или различные органические материалы искусственного происхождения.[ ...]
Готовые химические реактивы высокого класса чистоты получали от снабжающих торговых фирм и использовали без дальнейшей очистки. Исходные растворы адсорбатов готовили с дистиллированной водой, которую предварительно пропустили через деионизатор и фильтр с активным углем. Исходные растворы периодически анализировали с помощью анализатора общего органического углерода «Бекман-915». Адсорбционные эксперименты начинали через 4 ч после приготовления исходных растворов. В большинстве экспериментов в исходные растворы был введен 0,05 М раствор фосфатного буфера для уменьшения колебаний pH.[ ...]
Установлено, что содержащийся в сточных водах производств СК датам (диэтиловый э ир даэтиленгликоля) может быть обезврежен озоном до норм ГЩК [61]. Несмотря на го, что после озонирования ХПК вода снижается незначительно, вода легко подвергается биологической очистке (табл. 10). Исходная вода имеет следующие показатели: ХПК - 225 мг/л; БПКЦ0ЛН: ХПК - 26 ; pH - 5; общий органический углерод (00У) - 67 мг/л.[ ...]
Для выполнения этого требования рекомендуются специальные приборы для отбора проб воздуха в населенных пунктах, определяются правила контроля качества воздуха (принципы организации контроля, размещения постов, контроля и наблюдения, программу и сроки наблюдения, роль неблагоприятных »метеорологи-ческих условий, характеристики загрязнения и отбор проб), формулируются требования к методам определения загрязняющих веществ., Подземные воды классифицируют по целям водопользования (хозяйственно-питьевые и коммунально-бытовые нужды населения, лечебные, курортные и оздоровительные цели, нужды сельского хозяйства, орошение и обводнение, промышленные и т. д.). Разработаны общие требования к методам определения нефтепродуктов в природных и сточных водах, созданы и рекомендуются анализаторы общего органического углерода в природных водах (общие технические требования). ГОСТ 17.1.5.01—80 определяет общие требования к отбору проб донных отложений водных объектов для анализа на загрязненность (к программе отбора, месту, периоду, способу, устройству, консервации проб донных отложений). ГОСТ 17.1.3.06—82 определяет общие требования к охране подземных вод. ГОСТ 17.1.5.04—81 рекомендует приборы и устройства для отбора, первичной обработки и хранения проб природных вод.[ ...]
Окись алюминия способна сорбировать не только фосфаты, но и другие вещества и соединения [51]. Термическая обработка водопроводного осадка с последующим получением сферических гранул удельной поверхностью 275—360 м2/г и объемом пор 0,4 см3/г, применение его в качестве сорбента для удаления загрязнений из сточной воды показали, что он способен адсорбировать вещества, обладающие полярными молекулами: кислоты, основания, ароматические соединения с диссоциированным атомом водорода и др. Отмечены также особенности и условия практического применения фильтров с загрузкой из окиси алюминия для снижения содержания фосфатов, соединений Са, Си, N и др. Последовательная обработка воды на загрузке из окиси алюминия и активированного угля обеспечивает надежное снижение концентрации общего органического углерода на 95%.[ ...]
Результаты зависят не только от типа теста, но и от метода анализа. Биодеградация должна пройти настолько глубоко, чтобы образовались продукты, приемлемые для окружающей среды (environmentally acceptable). Изучают как первичную, так и полную деградацию ПАВ. Под первичной подразумевают потерю веществом поверхностной активности, которую определяют, измеряя специфическими методами поверхностное натяжение или устанавливая концентрацию веществ, способных соединяться с метиленовой синью (metylen blue active substances — MBAS),— для АПАВ, и веществ, способных соединяться с висмутом (Bi-active substances—BiAS),— для НПАВ. Весьма приблизительные представления о первичном разложении ПАВ дают наблюдения за потерей ими способности к ценообразованию [302]. О частичном разложении ПАВ до безвредных продуктов судят по поведению живых организмов (дафний, рыб) в исследуемой очищенной воде. Полное разложение поверхно-стно-активных соединений до неорганических веществ оценивают неспецифическими методами, определяя БПК, ХПК, общий органический углерод, выделение ССЪ. Некоторые авторы [452] предлагают судить о разрушении ПАВ по интенсивности роста бактерий-деструкторов на средах с этими веществами.[ ...]
ru-ecology.info
Углерод полное содержание в воде
Универсального консервирующего вещества не. существует. Для полного анализа воды обычно требуется отобрать пробу в несколько бутылей, в которых ее консервируют добавлением различных веществ. Для определения содержания некоторых компонентов, например сульфидов, сульфитов, агрессивной двуокиси углерода, следует брать пробы в отдельные бутыли для каждого из этих определений. [c.22] При определении общего содержания углерода и водорода прямым сжиганием необходимо принять меры для того, чтобы сжигание было полным, чтобы двуокись углерода не связывалась и не удерживалась золой, чтобы не образовалась окись углерода, чтобы вся двуокись углерода и вода поглотились абсорбентами, чтобы были удалены галогены, окислы серы и азота, а также другие соединения, помимо СОа, которые могли бы быть поглощены применяемыми поглотителями, чтобы влажность воздуха при входе и выходе из поглотительной системы была одинакова и, наконец, чтобы воздух, вводимый в систему, был свободен от углеродсодержащих веществ, двуокись углерода, водорода и воды. [c.850]Полное содержание серы находят сожжением 10—20 мг смолы в колбе с кислородом емкостью 750 мл с улавливанием полученных газообразных продуктов 15 ло воды с добавкой 3 капель пергидрола, кипячением раствора до удаления двуокиси углерода и титрованием серной кислоты щелочью по метиловому оранжевому. По найденному количеству кислоты и навеске смолы вычисляют содержание серы. Предположив, что она целиком входит в состав активных групп (1 мг-экв активных групп дает 2 мг-экв серной кислоты), находят обменную емкость по методу сожжения. [c.77]
Полный анализ воды включает большое количество различных определений и требует для проведения его длительного времени. При анализе определяют температуру, прозрачность, цвет, запах, вкус, кислотность, содержание кислорода, сероводорода, двуокиси углерода, аммония, сульфатов, нитритов, нитратов, хлоридов, органических веществ, бикарбонатов и пр. [c.238]
ИЗ которых по мере накопления автоматически перекачивается насосами в резервуар, расположенный наверху газгольдера. Такая циркуляция жидкости создает хорошее уплотнение и предохраняет стенки газгольдера от ржавчины, от налипания нафталина и других загрязнений. По мере циркуляции в уплотняющей жидкости (смоле, газгольдерном масле) накапливается вода, конденсирующаяся из газа. С целью обезвоживания смолы жидкость отводится в отдельные сборники, где смола отделяется от воды и снова подается насосами наверх, в распределительный желоб. Сборники снабжаются нагревательными приспособлениями для подогрева смолы в зимнее время. Уплотняющая жидкость должна удовлетворять следующим условиям полное отсутствие воды удельный вес y = 1Л при 20°С вязкость 2—2,5° по Энглеру при 50°С точка застывания —50°С содержание асфальтенов не более 1—2% по весу отсутствие свободного углерода, нафталина и др. [c.184]
Образование акролеина происходит одновременно с полным окислением до двуокиси углерода и воды, при этом катализаторы с высоким содержанием меди способствуют окислительной деструкции. [c.95]
В качестве углеродистых материалов для синтеза используются кокс или антрацит. Для снижения содержания в ацетилене вредных примесей к сырью предъявляются жесткие требования по чистоте. Так, известняк должен содержать не менее 97% карбоната кальция, а углеродистые материалы — не более 6—8% летучих веществ и минимальные количества серы и фосфора. Соотношение оксида кальция и углеродистого материала зависит от заданного литража . Литражом карбида кальция называется объем ацетилена в литрах, приведенный к 20°С и 0,1 МПа, полученный при полном разложении 1 кг карбида кальция водой. Теоретический литраж 100%-го СаСг равен 377,73 л. С увеличением количества углерода в шихте литраж карбида кальция повышается, но выход его падает. Обычно применяется шихта с содержанием углерода 40—50%. При этом литраж колеблется в пределах 230—300 л. При образова- [c.247]
Требования к технической воде разнообразны. Они сводятся в основном к условию примеси не должны препятствовать или вредить ее производственному использованию. Вода не должна вызывать коррозии котлов, труб, аппаратуры, механизмов, не должна содержать избытка взвешенных веществ, забивающих трубки охлаждающей системы, засорять и истирать детали прессов, насосов, труб, портить продукцию. Поэтому воду, поступающую из водоисточника, необходимо анализировать до и после ее подготовки. При полном анализе определяют содержание взвешенных веществ, сухой остаток, жесткость, остаток после прокаливания, окисляемость, щелочность, кислотность, содержание различных ионов (Са , Mg , Ре +, Ее " , С1 , С0 , 5102 ИТ. д.), содержание двуокиси углерода, сероводорода, кислорода. [c.187]
При сжигании АС окружающей среде наносится вред, гораздо меньший, чем при сжигании сераорганических соединений, поскольку при полном сгорании азотсодержащих топлив образуются вода, азот, двуокись углерода. Однако нет нефтей, содержащих только АС. Им всегда сопутствуют в больших или меньших количествах сераорганические соединения. Их содержание обычно коррелируется. Поэтому сжигать высокосернистые и высокоазотистые топлива абсолютно нецелесообразно, поскольку уничтожается ценнейшее химическое сырье. [c.3]
Проведены исследования процесса фильтрования с полным закупориванием пор и работы по изучению влияния концентрации суспензии на вид фильтрования [83. 84]. Исследовались суспензии сферических частиц полиметилметакрилата диаметром 280—360 мкм с содержанием 8—16 частиц в 1 дм смеси бензола и четыреххлористого углерода сферических частиц полистирола диаметром 310—470 мкм с содержанием 2—3500 частиц в 1 дм воды частиц активированного угля размером от О до-220 мкм в воде с содержанием 0,5 10" — 10-Ю мн-см . Горизонтальные и вертикальные фильтровальные перегородки представляли собой никелевые пластинки толщиной 0,1 мм с 400—467 круглыми отверстиями диаметром 260—280 мкм на 1 см и найлоновые ткани толщиной [c.81]
Методы борьбы с карбонильной коррозией — уменьшение содержания в синтез-газе сероводорода, диоксида углерода, воды и изготовление аппаратуры и коммуникаций, работаюш их при высокой температуре, нз легированных сталей или их футеровка. Значительно улучшает качество метанола-сырца частичная или полная замена цинк-хромового катализатора на медь-содер-жаш ий. [c.176]
Для последних критериев, а также в целях общей характеристики содержания органических примесей в воде очень важным является быстрое определение углерода органических веществ. Методики прямого определения этого показателя основаны на измерении углекислого газа, выделяющегося при полном окислении органических соединений [34]. Быстрый экспресс-анализ по Некрасову [35] осуществляется без выпаривания пробы воды с применением в качестве окислителя 1-н. раствора бихромата калия с добавкой персульфата калия (40 г/л) и азотнокислого серебра или перманганата калия (1 г/л)-, кислая реакция среды создается смесью концентрированных кислот (двух частей серной и одной части фосфорной, по объему). [c.45]
Карбонизацией и прокаливанием, объединяемых в производственных условиях в один процесс, называется высокотемпературная обработка сырого нефтяного кокса (при определенной продолжительности пребывания его в зоне реакции), направленная на из- менеиие его структуры и физико-химических свойств. Процесс сопровождается разложением и удалением некоторого количества летучих веществ и превращением части из них (высокомолекулярных углеводородов) в результате реакций уплотнения в кокс. В промышленных условиях чаще всего прокаливание проводят за счет физического тепла дымовых газов. Из-за вторичных реакций взаимодействия кокса с двуокисью углерода и парами воды при температурах выше 900—1000 °С некоторая часть углерода теряется (угар) и температура в зоне прокаливания резко снижается. Карбонизация коксов сопровождается увеличением их общей пористости и пикнометрической плотности, повышением содержания углерода и понижением содержания водорода. Степень этих изменений определяется температурой и длительностью прокаливания. Кальцинирование нефтяных коксов обеспечивает полное удаление воды и почти всех летучнх веществ из углеродистого вещества усадку твердого материала, препятствующую появлению деформаций и трещин в готовых электродных изделиях при обжиге повышение устойчивости углеродистого материала к взаимодействию с активными газами повышение электропроводности и механической прочности углеродистого материала. [c.202]
В работе Орловой [269 ] описано определение содержания воды и диоксида углерода в расплавах различных силикатов под давлением. Пробы массой 20—30 г помещали в кварцевую пробирку и сплавляли в пламени газа с кислородом. Расширенную часть пробирки охлаждали сухим льдом. При наличии в пробе железа до расплавления добавляли к ней 40—60 мг PbjOg. По окончании опыта определяли полную потерю массы пробы и каличество выделившейся воды и рассчитывали содержание Oj и НзО в анализируемом материале. В работе приведены данные анализа 65 различных силикатов, в том числе слюды, амфибола, цеолита и природных стекол. Для гранита, переплавленного при 3000 атм, соотношение Oa/H.jO составляло 1,8. [c.182]
Выделяющуюся при полиэтерификации воду в производстве А. с. удаляют двумя способами 1) способом сплавления, или блочным способом, т. е. барботирова-нием азота или двуокиси углерода через реакционную смесь со скоростью 0,04—3,0 м мин на 1 л смолы 2) азеотропным, т. е. отгонкой воды в виде азеотропной смеси с растворителем (обычно ксилолом). Этот метод заключается в том, что на стадии полиэтерификации (переэтерификацию методами алкоголиза или ацидолиза проводят без растворителя) добавляют ксилол, к-рый в виде азеотропа с водой испаряется из реактора, проходит через холодильник, конденсируется и поступает в разделительный сосуд. Отстоявшийся от воды ксилол возвращается в реактор, и цикл повторяется. На практике применяют 3% ксилола от массы реакционной смеси. Это количество определяет темп-ру кипения азеотропной смеси, а следовательно, и темп-ру синтеза до 250— 260 °С. При увеличении количества вводимого ксилола, напр, до 7%, темп-ра кипения азеотропной смеси снижается до 204—210 °С, что дает возможность осуществить достаточно полную полиэтерификацию. Содержание воды в возвратном ксилоле должно быть минимальным, а растворимость в нем фталевого ангидрида максимальной, что достигается поддержанием оптималь- [c.37]
Определение органического углерода в пробах воды быстро и надежно дает значение суммарного содержания органических примесей. Однако получение точных количественных данных о содержании этих веществ невозможно, если неизвестен их элементный состав. Нельзя также получить точных сведений о предполагаемом потреблении кислорода для их полного окисления в аэротенке или провести сравнение полученных результатов со значением БПКб, так как для этого надо еще иметь данные [c.56]
Наиболее полные сведения о стоке органических веществ в бассейнах некоторых крупных рек СССР приводят Б. А. Скопинцев и Л. П. Крылова [144]. Изучая соотношение между перманганатной окисляемостью и органическим углеродом в речной воде, они рассчитали, используя литературные данные по окисляемости, величины органического углерода. Принимая, что содержание последнего в органическом веществе в среднем составляет 50%, Б. А. Скопинцев и Л. П. Крылова вычислили величину выноса органических веществ некоторых крупных рек СССР (табл. 21). [c.72]
В 80-х годах XVIII столетия Лавуазье пытался определить относительное содержание углерода и водорода в органических соединениях. Он сжигал изучаемое соединение и взвешивал выделившиеся углекислый газ и воду. Результаты такого определения были не очень точными. В первые годы XIX в. Гей-Люссак (автор закона объемных отношений, см. гл. 5) и его коллега французский химик Луи Жак Тенар (1777—1857) усовершенствовал этот метод. Они сначала смешивали изучаемое органическое соединение с окислителем и лишь потом сжигали. Окислитель, например хлорат калия, при нагревании выделяет кислород, который хорошо смешивается с органическим веществом, в результате чего сгорание происходит быстрее и полнее. Собирая выделяющиеся при сгорании углекислый газ и воду, Гей-Люссак и Тенар могли определить соотношение углерода и водорода в исходном соединении. С помощью усовершенствованной к тому времени теории Дальтона это соотношение можно было выразить в атомных величинах. [c.74]
Проведены исследования процесса фильтрования с полным закупориванием пор и работы по изучению влияния концентрации суспензии на вид фильтрования [112, 113]. Исследовались суспензии сферических частиц полиметилме-такрилата диаметром 280—360 мкм с содержанием 8—16 частиц в 1 дм смеси бензола и четыреххлористого углерода сферических частиц полистирола диаметром 310—470 мкм с содержанием 2—Э500 частиц в 1 дм воды частиц активированного угля размером от О до 220 мкм в воде с содержанием 0,6-10- —10-10- г-см- Горизонтальные и вертикальные фильтровальные перегородки представляли собой никелевые пластинки толщиной 0,1 мм с 400— 467 круглыми отверстиями диаметром 260—280 мкм на 1 см и найлоновые ткани толщиной 0,11 мм с 1750—4000 квадратными отверстиями размером 15— 80 мкм на 1 см . Для суспензий полиметилметакрилата и полистирола использовались никелевые пластинки, а для суспензий активированного угля — найлоновые ткани. Таким образом, соблюдались условия, чтобы при фильтровании размер твердых частиц суспензии был больше размера пор фильтровальной перегородки. Благодаря этому при небольших концентрациях суспензии возможен процесс фильтрования с полным закупориванием пор, когда твердая частица увлекается струйкой жидкости к отверстию поры и закрывает это отверстие (рис. 111-2). [c.107]
Измерения скорости реакции в разреженных пламенах окиси углерода выявили прямую нропорциона.чьность степени превращения СО в СО2 (при малых степенях превращения, исключающих существенный разогрев газа) содержанию влаги в смеси [65], а также практически полное прекращение реакции при удалении влаги из зоны уже идущей реакции. Эти данные указывают па роль паров воды как гомогенного катализато1>а в механизме горения СО. Отметим, что трудность воспламенения сухих смесей СО и Ог была установлена еще в 1880 г. Диксоном (см. [194]). Кроме паров воды, ту же роль играют любые водородсодер.ч ащие примеси (КН), которзле являются поставщиками гидроксила. [c.232]
Вытекающий из реактора-метанизатора газ после охлаждения и отделения воды и разбавителя направляется в заключи-тельую ступень метанизации в неподвижном слое, где содержание водорода и окислов углерода снижается до уровня, обеспечивающего полную взаимозаменяемость с природным газом. Даже при наличии подобной заключительной стадии разработчик процесса фирма Кемикл Системс Инкорпорейшн утверждает, что этот процеос значительно экономичнее для окончательной обработки газов, получаемых из угля или остаточного топлива, чем конкурирующие процессы, такие, как системы с многократной закалкой и метанизаторы с псевдоожиженным слоем. [c.190]
Углерод и водород. В большинстве стандартов был принят метод Либиха он состоит в сжигании образца угля в токе кислорода при температуре 800—900° С, тогда как получающиеся продукты горения проходят над нагретой окисью меди, которая обеспечивает полное превращение углерода в углекислый газ и водорода в воду. Окислы серы и хлора, которые могут повлиять на результаты, удаляют соответственно путем пропускания над нагретым хроматом свинца, затем над серебряной сеткой. Содержание углерода и водорода затем вычисляют из привеса использованных поглотителей для удержания углекислого газа и воды. В Англии параллельно этому методу [18] создали метод, названный шеффильдским, котором сжигание происходит при температуре 1350° С. [c.49]
Отравление катализатора крекинга весьма специфично. Если для подавляющего большинства катализаторов сернистые соединения, окись углерода, кислород и другие вещества являются ядами, то присутствие их почти не влияет на процесс крекинга. Но зато некоторые азотсодержащие соединения резко снижают активность катализатора, вызывая обратимое отравление его. Необратимо отравляютка-тализатор соединения щелочных металлов. Длительное воздействие паров воды при высокой температуре также приводит к необратимой потере активности катализатора в основном за счет уменьшения удельной поверхности его. Все технологические схемы крекинга предусматривают тщательную очистку исходного сырья от щелочных металлов. Замечено, что степень отравления различными азотсодержащими соединениями симбатна их основным свойствам. Повышение молекулярного веса азотсодержащего соединения увеличивает отравляющую способность его. Степень отравления понижается с повышением температуры. Так, присутствие 1% хинолина снижает скорость крекинга нри 575° С на 30%, а нри 500° С уже на 80%. При этом полная потеря активности катализатора наступает при содержании хинолина, покрывающего лишь 2% всей поверхности катализатора. [c.238]
При соотношении катализатора по реакторам 1 2 6 выжиг кокса в первом реакторе завершался в течение 3 ч при температуре не выше 425 °С, во втором и третьем соответственно 48 ч (450 °С) и 84 ч (460 °С). Для полного выжига и прокалки катализатора с целью десорбции воды температуру в реакторах повышали до 510 °С, а содержание кислорода в инертном газе — до 5% (об.). Промотирование катализатора четыреххлористым углеродом (0,4% масс, на катализатор) проводили при 480°С, 0,5 МПа в потоке инертного газа, содержащем 2% (об.) кислорода. После прекращения подачи кислого промотора катализатор прокаливали при 510 °С в токе инертного газа, в котором содержание кислорода поддерживалось на уровне 5% (об.). После снижения температуры систему риформинга вакуумировали, затем продували инертным газом и переводили на режим риформинга. В ряде случаев сульфидирование катализатора рекомендуется гароводить после его регенерации. Ниже приведены показатели работы установки риформинга, включая работу на регенерированном катализаторе [119] [c.156]
Наиболее простым и надежным способом очистки сточных вод от органических веществ является биологическая очистка, в основе которой лежат процессы самоочищения воды. Суть метода заключается в том, что под действием различных микроорганизмов органические вещества подвергаются минерализации, т. е. окислению и конечному переводу в безвредные продукты этого процесса — воду, двуо кись углерода, нитратные, фосфатные и сульфатные соединения. Различные органические вещества для своего распада требуют различного количества растворенного в воде кислорода. Поэтому содержание этих веществ часто определяют количеством кислорода, которое требуется для их полного окисления, т. е. хн- [c.44]
Допустим, на воздухе полностью сгорел 1 кг бензина состава С =86 %, Н =14 %. Тогда в продуктах сгорания от углерода будет находиться углекислый газ (С + О2 СО ), водорода - вода (2Нз О2 2Н2О) и не вступивший в реакцию азот воздуха. В 1 кг бензина принятого состава содержится 0,86 кг С и 0,14 кг Н. Количество воды в продуктах сгорания определится из соотношения молекулярных масс в реакции горения при сгорании части (1 кг) водорода образуется 9 частей (9 кг) воды. Таким образом, при сгорании 1 кг бензина образуется 0,14 9 =1,26 кг воды. На превращение 1 кг воды в пар затрачивается около 2512 кДж. Если при полном сгорании 1 кг бензина выделилось 44 ООО кДж теплоты, то Сцизщ составит 44 ООО - 2512 1,26 =40 835 кДж/кг. Чем больше содержание водорода и выше влажность топлива, том больше разница между высшей и низшей теплотой сгорания. [c.8]
Сравнение биологической очистки сточных вод от поверхностноактивных веществ и таких химических или физико-химических методов как фотоокислепие, пенная сепарация, экстракция растворителями, поглон1,с[1ие сорбентами и ионитами, показало, что биологическая очистка снижает БПК, содержание органического углерода и ПАВ в сточной воде в среднем на 77%, при фотоокислепии эти показатели снижаются на 99%, при пенной сепарации — на 95—96%, при коагуляции, проводимой при pH 4—5, — на 90%. Экстракцией удаляют 50—60% ПАВ, ионным обме[гом н обратным осмосом 99% [41]. Таким образом, практически все перечисленные физико-химические методы позволяют достаточно полно извлекать ПАВ нз сточных вод. Возможность их применения определяется тем, насколько отработана и совершенна технология использования того или иного метода и каковы границы ее применимости в конкретных производственных условиях. [c.255]
Оксид углерода (IV), сероводород, оксид серы (IV) и кислород — наиболее часто присутствующие в воде, вредные коррозионноспособные газы. Поэтому воду анализируют на их содержание. Оксид углерода (IV) всегда присутствует в воде. Определение растворенного кислорода в воде — важная составная часть химического анализа воды. Недостаточное содержание его или полное отсутствие указывает на наличие загрязнений, поглощающих из воды растворенный в ней кислород. Растворимость газов в воде зависит от температуры и атмосферного давления. Определение следует делать сразу после отбора пробы воды. Источником кислорода в воде является атмосферный воздух и фитопланктон. Глубокие грунтовые воды, как правило, не содержат растворенного кислорода, они поглощают его при соприкосновении с воздухом. [c.9]
При анализе углей 1—5 г пробы (в зависимости от предполагаемого содержания галлия в исследуемом материале), насыпанной тонким слоем в фарфоровый противень, помещают в открытую муфельную печь для озоления при хорошем доступе воздуха. Доводят температуру до 400—450° С и выдерживают до полного выгорания углерода. Золу переносят в платиновую чашку, смачивают водой и обрабатывают так же, как указано при анализе бокситов и силикатов (стр. 181). Из полученного солянокислого раствора галлий экстрагируют после добавления родамина В эфирно-бензольной смесью в присутствии Ti b и сравнивают в ультрафиолетовом свете интенсивность свечения органического слоя со свечением стандартных растворов. Метод позволяет определять галлий при его содержании >10— % с ошибкой [c.186]
Применяемые каталитические системы были получены на основе солей металла переменной валентности и алюмооргани-ческих соединений. Повышенное содержание примесей приводит либо к полному отравлению или разложению катализатора, либо к его повышенному расходу. Поэтому исходное сырье должно содержать не более 10 млн оксида углерода, аммиака, ацетиленовых углеводородов, 30 млн воды, 0,2% бутадиена и 0,015% сероводорода. Как показали исследования, очистка про-пан-пропиленовых фракций на цеолитах марки ЫаХ обеспечивала необходимую чистоту исходного сырья. [c.103]
chem21.info
Углерода и водой - Справочник химика 21
После уксусной кислоты пировиноградная кислота, вероятно, самый важный промежуточный продукт в организме. Когда молекула глюкозы расщепляется с выделением энергии, в числе прочих соединений образуется и пировиноградная кислота. Дальше процесс ее превращений может идти двумя путями. Если окружающая среда содержит достаточное количество кислорода, пировиноградная кислота теряет один атом углерода и один атом кислорода, которые соединяются с кислородом внешней среды и образуют двуокись углерода. Сама же пировиноградная кислота превращается в уксусную, а та, в свою очередь, может распадаться дальше до двуокиси углерода и воды. [c.173] Под карбонилированием понимается открытая Реппе реакция присоединения окиси углерода и воды к ацетилену в присутствии карбонила никеля, ведущая к образованию акрилово кислоты [c.253]По способу, разработанному Реппе, реакция олефипов с окисью углерода и водой может легко проходить в присутствии карбонила никеля и некоторых органических кислот при нагревании в автоклаве до 170° [51]. Течение реакции можно представить следующим уравнением [c.219]
В результате превращения глюкозы в молочную кислоту мышцы получают кое-какую энергию. Но это всего лишь 7 /о той энергии, которую можно было, бы получить, если бы глюкоза расщеплялась полностью — до двуокиси углерода и воды. Правда, и эти 7% все-таки могут в течение некоторого времени поддерживать работоспособность мышцы. Во всяком случае, это максимум того, на что она может рассчитывать в отсутствие кислорода. [c.174]
Марголис и Тодес [35] установили, что катализаторы типа смеси окиси хрома и шпинеля, нанесенные на асбест, вызывают окисление таких углеводородов, как пентан и гептан, до двуокиси углерода и воды. Под влиянием таких катализаторов метилэтилкетон и бутиральдегид, содержащиеся в продуктах неполного парофазного окисления этих углеводородов, должны окисляться в органические кислоты. Поэтому можно считать, что эти соединения не образуются в качестве промежуточных продуктов в процессе поверхностного горения. [c.321]
Уксусная кислота, образовавшаяся в живой ткани из углеводородов, может быть разрушена до двуокиси углерода и воды. Но она может быть использована и как кирпичик для построения не только более крупных молекул карбоновых кислот, но и стероидов или опять-таки углеводородов. В этом отношении уксусную кислоту можно считать важнейшим промежуточным продуктом в химии живого организма. [c.157]
Если теперь тесто нагреть, молекулы угольной кислоты быстро распадаются на двуокись углерода и воду Газ, расширяясь, и образует пузырьки в тесте. Мука, в которую уже добавлены и сода, и кислота, бывает в продаже — тесто из такой муки поднимется само. [c.170]
В присутствии ванадиевого катализатора о-ксилол окисляется воздухом в ангидрид фталевой кислоты [1, 2]. Другие ксилолы превраш аются в этих условиях в бензойную кислоту, ангидрид малеиновой кислоты, окись углерода и воду, т. е. подвергаются дальнейшему окислению. [c.263]
Образование акролеина происходит одновременно с полным окислением до двуокиси углерода и воды, при этом катализаторы с высоким содержанием меди способствуют окислительной деструкции. [c.95]
Описано много случаев взрывов в аппаратах разделения воздуха, вызванных попаданием в аппараты даже незначительного количества ацетилена. Поэтому в воздухе, поступающем в цехи его разделенпя, содержание ацетилена должно быть не более 0,25 мл на 1 м воздуха. Все некондиционные ацетиленсодержащие газы должны полностью сжигаться до двуокиси углерода и воды. В производстве ацетилена (нз углеводородного сырья) такое сжигание является сложной задачей, так как газовые выбросы могут [c.199]
Эти два соединения, хлорофилл и гем, играют важнейшую роль в сложном механизме поглощения солнечной энергии и ее превращении для использования живыми организмами. Мы уже знаем, что характерным свойством комплексов переходных металлов является наличие нескольких близко расположенных -уровней, что позволяет им поглощать свет в видимой области спектра и придает окраску. Порфириновый цикл вокруг иона Mg в молекуле хлорофилла выполняет такую же роль. Хлорофилл в растениях поглощает фотоны видимого света и переходит в возбужденное электронное состояние (рис. 20-22). Эта энергия возбуждения может инициировать цепь химических реакций, приводящих в конце концов к образованию сахаров из диоксида углерода и воды [c.255]
Общепризнанным способом борьбы с загрязнением атмосферы газами окисления считается их сжигание с образованием безвредных оксидов — диоксида углерода и воды [265-270]. В связи с этим необходим надежный и простой метод расчета состава газов, который позволил бы без проведения экспери- [c.168]
По-видимому, гидроксильные радикалы, образуюш иеся в газообразном состоянии в результате диссоциации воды при безэлектродном разряде, являются более сильными окислительными реагентами, чем гидроксильные радикалы, образуюш,иеся в растворе [50]. Они вызывают разрыв олефинов со связью с образованием альдегидов и даже окисляют метан в основном до двуокиси углерода и воды. [c.371]
ВОГО ангидрида, бензиловый спирт пе был обнаружен в продуктах окисле ния, но его можно выделить при более высоких давлениях. При тех же условиях со значительным выходом были выделены бензальдегид и бензойная кислота. Известно также, что свободная карбоксильная группа довольно легко разлагается при повышенных температурах в присутствии многих металлов и окислов металлов. Следовательно, из бензойной кислоты могут образоваться бензол и двуокись углерода, а бензол может дальше окисляться до малеинового ангидрида и, наконец, до двуокиси углерода и воды. [c.12]
В конвертированном газе, кроме основных компонентов, содержатся кислород и кислородсодержаш,ие вещества, главным образом окись углерода, двуокись углерода и вода. [c.46]
Соответствующая конструкция факела, позволяющая полностью сжигать газ (до двуокиси углерода и воды) без образования сажи или дыма. [c.131]
Соединения, теплота образования которых положительна (ДЯ°>0), называются эндотермическими-, соединения, теплота образования которых отрицательна (АЯ°таким образом, является эндотермическим соединением, а двуокись углерода и вода—экзотермическими. [c.62]
Атомный кислород, окисляя формальдегид, дает окись углерода и воду [c.136]
Углеводы состоят всего из трех элементов — углерода, водорода и кислорода. В течение всей жизни в человеческом организме постоянно происходит превращение углеводов в СОз и Н2О, сопровождающееся выделением энергии. Например, глюкоза — основной поставщик энергии человеческого организма - имеет формулу С Н,20 . Сначала, когда это вещество было только открыто, его формулу записывали так С (Н20) , т. е. в виде комбинации углерода и воды. Отсюда и происхождение названия углевод . Хотя теперь мы знаем, что на самом деле никаких молекул воды в углеводах нет, название сохранилось. [c.244]
Уменьшение выбросов вплоть до соответствия их принятым стандартам требовало дополнительных мер. Хорошие результаты были достигнуты благодаря каталитическим конвертерам. Конвертер — реакционная камера на пути выхлопов. Выхлопные газы и внешний воздух проходят над катализаторами, которые помогают превратить оксид азота в молекулярный азот, а углеводороды в диоксид углерода и воду. Соотношение топлива и воздуха в карбюраторе таково, что выбрасывается достаточно много моноксида углерода и водорода. Эти газы проходят через первую половину конвертера, где восстанавливаются оксиды азота, например, [c.422]
Во второй части конвертера моноксид углерода и углеводороды окисляются до диоксида углерода и воды. [c.422]
Этот процесс следует отличать от типично некаталитического металлопарового процесса получения водорода, в рамках которого осуществляется полное окисление углеводородного сырья окислом металла до двуокиси углерода и воды. В рассматриваемом процессе только часть углеводородного сырья участвует в этой реакции. Другая его часть конвертируется с образовавшимися (по указанной реакции) двуокисью углерода и водяным паром. Катализатором конверсии, видимо, являются поверхностно восстановленные до металла частицы окисла металла (см. табл. 18). [c.38]
В предыдущем разделе мы установили, что в составе бензина преобладают два элемента — углерод и водород. В связи с этим, при полном сгорании бензина будут образовываться, главным образом, двуокись углерода и вода. Основываясь на элементарных реакциях сгорания [c.31]
Когда газ пропан СзН сжигают в кислороде, в результате реакции образуются диоксид углерода и вода. Эта реакция может быть описана химическим уравнением [c.70]
Этот пример показывает, почему химикам интересно знать, самопроизвольна ли каждая реакция, т.е. иметь представление о ее естественной тенденции к осуществлению. Если изучаемая химическая реакция является самопроизвольной, но медленной, можно попытаться ускорить ее протекание. Чаще всего для этого достаточно повысить температуру или подобрать катализатор. Действие катализаторов будет подробнее обсуждаться в гл. 22. Но вкратце уже сейчас можно определить катализатор как вещество, которое помогает самопроизвольной реакции протекать быстрее, обеспечивая ей более легкий путь. При достаточно высокой температуре бензин быстро горит в воздухе. Роль искры зажигания в автомобильном двигателе заключается в создании исходной высокой температуры. Выделяющееся в результате реакции тепло поддерживает высокую температуру, необходимую для дальнейшего протекания реакции. Но если подобрать подходящий катализатор, бензин будет соединяться с кислородом и при комнатной температуре, потому что в естественных условиях реакция между этими веществами является самопроизвольной, хотя и медленной. Однако никакой катализатор никогда не заставит соединяться диоксид углерода и воду с образованием бензина и кислорода при комнатной температуре и умеренных давлениях, и только невежественный химик потратит время на поиски такого катализатора. Короче говоря, понимание различия между самопроизвольными и несамопроизвольными реакциями помогает химику увидеть границы возможного. Если реакция возможна, но пока еще не найден путь ее осуществления, целесообразно заниматься поисками таких путей. Если же процесс принципиально невозможен, не следует тратить на него время. [c.169]
Различия между стереоизомерами могут показаться незначительными, но они очень важны. Стереоизомерия свойственна большинству соединений, входящих в состав живых тканей, и организм легко отличает один стереоизо-м,ер от другого. Например, в составе крови есть глюкоза, но нет никаких других гексоз, хотя их существует шестнадцать. У взрослого человека в крови содержится в среднем шесть граммов глюкозы. Это энергетическое сырье человеческого организма кровь разносит его по всем клеткам, и каждая клетка использует на свои нужды столько глюкозы, сколько ей необходимо. В клетках глюкоза превращается в двуокись углерода и воду, а энергия, выделяющаяся при этом, потребляется клеткой. [c.137]
Присоединение окиси углерода и воды к олефинам в присутствии катализаторов, особенно концентрированной серной кислоты, с образованием карбоновых кислот разветвленного строения идет с исключительно хорошими выходами при определенных условиях даже в отсутствие давления. Целесообразно работать при температуре от О до 50° н при давлении окиса углерода 50—100 ат в присутствии 96—97%-нои серной кислоты. В этих условиях из нропена получают изомасляную кислоту, а из изобутена — триметилуксусную кислоту [52]. Реакция идет в строгом соответствиш с правилом Марковникова [c.220]
Конечными продуктами этой реакции являются двуокись углерода и вода. Для получения формальдегида реакцию нужно проводить до промежуточной стадии, ограничивая время контактиро-, вания реагентов с катализатором и снижая температуру послереакционной смеси. С этой целью смесь пропускают через систему холодильников, а затем в нее вводится такое количество воды, чтобы получить раствор, содержащий 30% НСНО и -3% СН3ОН. Выход достигает 82% от теоретически возможного. [c.377]
Термическое окисление становится заметным при 400° С, однако при температуре ниже 575° С процесс протекает медленно. В течение индукционного периода происходит экспонентное возрастание концентрации формальдегида до стационарной величины. Вслед за индукционным периодом происходит быстрая реакция, основными продуктами которой являются окись углерода и вода. Путем добавления к газовой смеси формальдегида можно частично или полностыо сократить продолжительность индукционного периода если же добавить формальдегид в таком количестве, чтобы концентрация его превысила стационарную, скорость быстрой реакции также соответственно увеличится и формальдегид будет разрушаться до тех пор, пока снова не установится нормальная стационарная концентрация его. Важная роль формальдегида в процессе окисления подчеркивается также следующим наблюдением если реакционную смесь метана и кислорода подвергнуть при 485° С сильному облучению ультрафиолетовым светом с длинами волн в интервале от 2400 [c.321]
Окисление до любого из возможных промежуточных соединений является сильно экзотермической реакцией, поэтому не вполне ясно, почему окисление должно остановиться на какой-либо определенной стадии или почему полное окисление до двуокиси углерода и воды не протекает в качестве единственной реакции, как при несколько более высоких температурах. Баргойн и другие [1] изучали медленное некаталитическое окисление о-ксилола воздухом при несколько менее высоких температурах и при давлении 4,6 апг. Из их данных видно (табл. 2), что избирательность реакции чрезвычайно мала. Не опубликовано ни одного исследования по механизму или кинетике реакции окисления о-ксилола в условиях, применяемых для производства фталевого ангидрида. Такое исследование представляло бы очень большие трудности вследствие гетерогенности реакции, чрезвычайно малого времени реакции и высокой температуры. Однако, изучая основные и побочные продукты этой и подобных ей реакций, можно получить некоторое представление о ходе реакции. [c.11]
Анаэробная ферментация (или гликолиз), цикл лимонной кислоты и дыхательная цепь присущи всему живому на Земле вьипе уровня бактерий. Некоторые аэробные, т.е. поглощающие кислород, бактерии тоже используют этот процесс для полного окисления глюкозы или аналогичного метаболита-в диоксид углерода и воду. Другие анаэробные, т.е. непотребляющие кислород, бактерии осуществляют только ферментацию поглощение глюкозы или других богатых энергией молекул, их разрыв на меньшие молекулы, такие, как пропионовая кислота, уксусная кислота или этанол, и использование сравнительно небольших количеств высвобождаемой сво- [c.333]
Углеводородные газы контактируют контактом в псевдоожиженном слое. Часть контакта выводят из реакционной зоны в окислительную и затем возвращают обратно. Взвесь образующейся окиси никеля окисляет часть углеводородов в двуокись углерода и воду, и восстанавливается до металла. Углеводороды конвертируют с обра.зовавшимися двуокисью углерода и водяным паром [c.110]
Для одновременной очистки газа от сероводорода, двуокиси углерода и воды применяют смесь этаиоламина с этиленгликолем. Такая комбинированная очистка приводит к обезвоживанию сырья и снижению расхода водяного пара, используемого для регенерации растворителей. На рис. 72 приведена технологическая схема очистки природного газа смесью этаноламина с этиленгликолем. [c.161]
Процесс включает обессери-вание сырья, каталитическую конверсию углеводородов с водяным паром, метанизацию, очистку газа от двуокиси углерода и воды [c.142]
Если не принять меры к удалению из отходящих газов моноокиси углерода и водорода (обычно это проделывают с помощью окиси меди), так же как и двуокиси углерода и воды, растворение кислорода после продолжительного окисления уменьшается настолько сильно, что это может вызвать ошибку при определении момента автозамедления. Посторонними газами, образующимися при окислении, являются метан, этан, этилен и пропилен. [c.82]
Концентр)1рован 1ЫЙ раствор хлорида натрия насыщают ам-маком, а з тем пропускают в него иод давлением диоксид угле-)да, нолу заемый обжигом известняка. При взаимодействии ам-иака, диоксида углерода и воды образуется гидрокарбонат и мои и я [c.441]
Кроме того, газообразный кислород смешивается с водой в результате аэрации, которая происходит, если вода падает с плотин, перетекает через валуны и другие препятствия, образуя в результате водо-воздушную пену . Газообразный кислород попадает в природные водоемы в результате фотосинтеза - процесса, при котором зеленые растения у океанский планктон синтезируют углеводы из диоксида углерода и воды пря н.шичии солнечного света. В дневные часы водные зеленые растения постоянно синтезируют сахара. При этом также получается газообразный кислород, который выделяется из водных растений в окружающую воду. Суммарное химическое уравнение, описывающее образование глюкозы ((Ь5Н1205) и кислорода при фотосинтезе, может быть представлено следующим образом [c.58]
Если бы химия не была количественной наукой, то такое описание реакции, включающее указание реагентов и продуктов, было бы вполне достаточным. Однако мы хотим извлечь из химического уравнения больше сведений. Интересно знать, сколько молекул кислорода расходуется в расчете на 1 молекулу пропана и сколько молекул диоксида углерода и воды получается в результате. Уравнение (2-1) не дает ответа на эти вопросы, так как оно не является полным. Когда мы введем в него численные коэффициенты (записав их перед соответствуюшими формулами), которые укажут, сколько молекул каждого сорта принимает участие в реакции, то в левой и правой, частях уравнения должно будет оказаться одинаковое число атомов каждого сорта, поскольку в ходе химической реакции не возникает новых атомов и не происходит уничтожения имевшихся. Так мы получим полное уравнение реакции. [c.70]
Теплота сгорания 1 моля жидкого ацетальдегида, СН3СНО, с образованием диоксида углерода и жидкой воды равна - 1164 кДж. а) Составьте полное уравнение этой реакции, б) Какое количество теплоты вьщеляется при сгорании 1 моля ацетальдегида Какое количество теплоты вьщеляется в расчете на моль образующейся воды В расчете на моль использованного кислорода в) Какое количество теплоты вьщеляется при сгорании 1 г ацетальдегида г) Воспользуйтесь полученными данными, а также данными для диоксида углерода и воды из приложения 3, чтобы вычислить стандартную теплоту образования ацетальдегида. Сравните полученный результат с приведенным в приложении 3. [c.39]
Сахар глюкоза, образующийся в листьях зеленых растений, относится к числу углеводов. Название углеводы связано с прошлыми неверными представлениями о структуре этих соединений. Формулу глюкозы, СбН120 , можно записать в виде (С-Н20)б. Вещества, формулы которых могут быть представлены равными количествами углерода и воды, в свое время получили название углеводов . [c.308]
Средний размер капель. В примере 4 рассчитан средний размер капель при перемешивании тетрахлорида углерода и воды в аналогичном аппарате с мешалкой (Ф = 0,05). Данных по межфазиому натяжению между водой и тетрахлоридом углерода в присутствии брома в литературе нет. Если принять межфазное натяжение равным межфазному натяжению между чистыми водой и тетр а хлоридом углерода (0,046 Н/м), то расчет среднего размера капель по уравнению (111.21) при всех значениях удерживающей способности дает примерно одинаковое значение d = 0,268 мм- [c.57]
Сбрасываемые нефтеперерабатывающими предприятиями органические вещества под действием микроорганизмов окисляются до диоксида углерода и воды. Проявляется способность самоочищения водоема. При этом расходуется кислород, содержащийся в воде водоема и поступающий туда из атмосферы. Количество кислорода в мг О2 на 1 л (мг/л), которое поглощают в процессе окисления органические вещества за определенный промежуток времени, называется биологической потребностью в кислороде—ВПК. Различают БПК5 (пятидневный) БПК20 (двадцатидневный), БПКполн (полный, когда вещество окисляется полностью). Сточные воды НПЗ до очистки имеют БПКполн 250—450 мг/л, в то время как по санитарным нормам этот показатель в воде водоема должен составлять 3—6 мг/л в зависимости от его категории. При сбросе неочищенных сточных вод концентрация имеющегося в водоеме кислорода может резко снизиться (либо он израсходуется полностью), что вызывает гибель планктона, бентоса, рыб и других организмов, потребляющих растворенный в воде кислород. [c.314]
chem21.info
Водой углерода и фосфора - Справочник химика 21
Минеральными удобрениями называют соли, содержащие элементы, необходимые для питания растений и вносимые в почву для получения высоких и устойчивых урожаев. В состав растений входят около 60 химических элементов. Для образования ткани растения, его роста и развития требуются в первую очередь углерод, кислород и водород, образующие основную часть растительной массы, далее азот, фосфор, калий, магний, сера, кальций и железо. Источниками веществ, необходимых для питания растений, служат воздух и почва. Из воздуха растения извлекают основную массу углерода в виде диоксида углерода, усваиваемого путем фотосинтеза, а из почвы — воду и минеральные вещества. Некоторое количество диоксида углерода воспринимается корневой системой растений из почвы. Среди минеральных веществ особенно важны для жизнедеятельности растений азот, фосфор и калий. Эти элементы способствуют обмену веществ в растительных клетках, росту растений и особенно плодов, повышают содержание ценных веществ (крахмала в картофеле, сахара в све-кле, фруктах и ягодах, белка в зерне), повышают морозостойкость и засухоустойчивость растений, а также их стойкость к заболеваниям. При интенсивном земледелии почва истощается, т. е. в ней резко снижается содержание усваиваемых растениями минеральных веществ, в первую очередь растворимых в воде и почвенных кислотах соединений азота, фосфора и калия. Истощение почвы снижает урожайность и качество сельскохозяйственных культур. Уменьшение содержания питательных веществ в почве необходимо постоянно компенсировать внесением удобрений. Ввиду огромных масштабов потребления минеральные удобрения— наиболее крупнотоннажный вид химической продукции, годовое количество которой составляет десятки миллионов тонн. [c.143] Отходяш,ие газы содержат 80—85% оксида углерода, 8— 10% азота, 2—3% воды, а также -водород, фосфин, диоксид углерода, фосфор. Теплота сгорания газов около 11 МДж/м Наиболее приемлемым решением проблемы использования тепла отходящих газов является их применение в качестве топлива для технологических аппаратов или для выработки пара. Одно из условий использования тепла отходящих газов — создание специального теплообменного оборудования, устойчивого в агрессивной среде. [c.226]В ряде работ микроанализ газов сводится к измерению их объемов в капиллярных трубках и к последующему поглощению отдельных компонентов газовой смеси различными абсорбентами. На этом принципе в Институте химической физики АН СССР [53] был разработан прибор для микроанализа газов, дающий возможность измерять количества газа порядка 0,5 мл с ошибкой, не превышающей 1 %. Для устранения растворения газов в воде, были применены сухие поглотители, которые в виде крупинок помещали в платиновую петлю, впаянную в стеклянную палочку. В отдельных случаях применяли жидкие поглотители, которыми пропитывали кусочки пористого стекла. Пары воды поглощались фосфорным ангидридом, двуокись углерода — слегка влажным КОН. Этилен поглощался нанесенной специальным методом на кусочки пористого стекла серной кислотой, содержащей 25% ЗОз по окончании поглощения, которое длится 5 мин., в смесь газов вводили кусочек КОН для удаления паров 80з. Поглощение ацетилена производили пастой, приготовленной из однохлористой меди и гидрата окиси калия полное поглощение ацетилена этой пастой происходит в течение 2—3 минут. Кислород определялся желтым фосфором, который плавился в специальной ложечке, погруженной в нагретую до 50° воду после этого в ложечку вводили платиновую петлю. Обливая ложечку холодной водой, получали фосфор в виде застывшего на петле шарика. Окись углерода окислялась, а затем поглощалась активной окисью серебра, осажденной из раствора А КОз крепким раствором КОН. Осадок тщательно промывали и фильтровали. Слегка влажную окись серебра хранили в склянке с притертой пробкой, а перед анализом препарат прессовали и укрепляли на платиновой проволочке с помощью капли концентрированного раствора жидкого стекла. Горючие компоненты газовой смеси сжигали в микронипетке, схематически изображенной на рис. 73. Основная часть микропипетки для сожжения 1 закрыта сверху капиллярным краном 2, а снизу — обыкновенным краном 3, на стеклянную оливку [c.189]
Напишите уравнения реакций каждого из перечисленных веществ с водой оксид фосфора (V) гидрид лития оксид азота (IV) оксид углерода (IV) оксид серы (IV). Что можете сказать [c.232]
Напишите уравнения реакций каждого из перечисленных веществ с водой оксид фосфора (V), гидрид лития, оксид азота (IV), оксид углерода (IV), оксид серы (IV). Что можете сказать о каждом из образующихся соединений [c.256]
Основная масса тела бактерий состоит из воды (до 85%). Сухое вещество бактерий содержит главным образом белок (до 80%), а также углеводы, жиры (количество последних варьирует в широких пределах), минеральные элементы или зольные вещества — калий, кальций, фосфор, серу, магний, натрий, хлор, железо и т. д. Питание бактерий осуществляется проникновением питательных веществ через всю поверхность бактериальной клетки. Вода и растворимые в ней вещества усваиваются клеткой непосредственно, поступая в нее под действием осмотических сил, а растворимые в жирах предварительно подвергаются воздействию.бактериальных ферментов, которые являются высоко дифференцированными катализаторами [99]. Для нормального роста и размножения бактерий им необходимы в основном вода, углерод, азот, фосфор, калий, железо, магний и другие минеральные вещества, а также витамины В1, Вг, В3, /г-аминобензойная кислота и другие органические соединения. [c.46]
В настоящее время существует значительное количество конструкций автоматических химических газоанализаторов, действие которых основано на принципе поглощения. Регистрирующий аппарат для определения кислорода отличается от газоанализатора на двуокись углерода только устройством реакционного сосуда, наполненного находящимися под водой палочками фосфора. Газоанализатор на кислород удовлетворительно работает в помещениях с температурой выше +15°, так как окисление фосфора идет с достаточной скоростью только при этих температурах. Автоматические химические газоанализаторы применяются также для реакций, идущих при более высоких температурах. В газоанализаторах на азот вместо реакционного сосуда устанавливают реакционную печь, нагреваемую электрическим током. К печи автоматически подводится исследуемая газовая смесь и воздух. После сжигания водорода и окиси углерода над окисью меди, наполняющей электрическую печь, последующей конденсации водяного пара и поглощения двуокиси углерода раствором КОН, оставшийся азот регистрируется с учетом количества азота, поступившего с воздухом для сжигания. [c.320]
Существенный теоретический и большой практический интерес представляет изучение элементарных потоков экосферы в большом геологическом круговороте, ряд которых довольно хорошо изучен в количественном отношении, например глобальные круговороты воды, углерода, азота, серы, фосфора, ряда других элементов, потоки энергии и ряда сырьевых материалов [157]. [c.32]
Отходящие газы фосфорных печей содержат 80—85% окиси углерода, 8—10% азота, 2—3% воды, а также водород, фосфин, двуокись углерода, фосфор. Теплота сгорания газов — около И МДж/м , причем на 1 т фосфора образуется около 3000 м отходящих газов. [c.193]
Органические загрязнения бывают растительного и животного происхождения. К растительным относятся остатки растений, плодоовощей и злаков, бумага, масла (растительные) и пр. Основным химическим элементом этого рода загрязнений является углерод. К загрязнениям животного происхождения относятся физиологические выделения людей и животных, остатки мускульных и жировых тканей животных, клеевые вещества и пр. Они характеризуются довольно значительным содержанием азота. Кроме того, в сточных водах содержится фосфор, сера и водород- [c.168]
Способность придавать лакмусу красный цвет — одно из характерных свойств кислот. Изменение цвета лакмуса в наших опытах объясняется тем, что вещества, получающиеся при горении углерода, фосфора и серы дают с водой кислоты. [c.95]
Таким образом, эвтрофикацию водоемов можно предупредить удалением из воды хотя бы одного питательного вещества. Практически это сводится к удалению из сточных вод соединений фосфора, так как углерод в виде бикарбонатов, а азот в результате ассимиляции из воздуха некоторыми видами водной растительности почти всегда присутствуют в природных водах. К тому же из-за высокой растворимости большинства минеральных азотсодержащих солей изыскание эффективных и экономичных методов их удаления вызывает большие затруднения. Тем не менее, в последнее время выявилась необходимость строгого нормирования содержания аммонийных солей и нитратов в воде водоемов. Действующими в нашей стране Правилами охраны поверхностных вод от загрязнения сточными водами (1975) по токсикологическому признаку в воде водоемов рыбохозяйственного значения лимитируется содержание аммонийных соединений, а в воде водоемов хозяйственнопитьевого и культурно-бытового пользования — содержание нитратов. Предельно допустимая концентрация аммонийных соединений принята 0,5 мг/л, а для нитратов (в пересчете на азот) — 10 мг/л. [c.109]
Как все чистые металлы, платина имеет большой температурный коэффициент электросопротивления, и поэтому пользоваться платиновыми печами следует, включая их последовательно с реостатом, так как сопротивление холодной печи в четыре раза меньше нагретой до 1000°. При включении через холодную печь пойдет очень сильный ток и вызовет быстрое нагревание, опасное как для керамических частей печи, так и для самого нагревателя, который может перегореть. Платина при нагревании в окислительной атмосфере вполне устойчива. В восстановительной атмосфере она очень чувствительна к углероду, фосфору, сере и к металлам, а в присутствии воды на нее действуют также и галоиды. При температурах выше 1300° платина становится заметно летучей и сравнительно быстро перегорает. [c.141]
Фосфорит - - кварц+углерод (графит). .......... Фосфорит -[- кварц+углерод (графит) Ч-вода (пар). . . Фосфорит+кварц+углерод (графит) 4-водород. ... Фосфорит 4- кварц водород 98-99 24-32 10—15 Нет 1-2 2-4 0,2-0,8 Нет Нет 41-59 82-86 96—99 Нет 7-15 0,1-0,4 Нет 90—95 24-30 50-55 10—12 [c.74]
Так, если фосфорит, поступающий в печь, был предварительно прокален при 1000—1050° С, то содержание в печном газе двуокиси углерода (продукта разложения карбонатов) составляет 0,5—0,7%, но, если фосфорит был высушен при 200—250° С, то содержание двуокиси углерода достигает 5%-От влажности шихты зависит содержание водорода, так как он образуется в процессе термической диссоциации и восстановления паров воды. В результате взаимодействия водорода с серой образуется сероводород, с углеродом и азотом — синильная кислота. Взаимодействие паров воды с фосфором приводит к образованию фосфина. При высоких температурах в печи четырехфтористый кремний образуется в результате взаимодействия, содержащихся в шихте, фторидов щелочноземельных металлов с двуокисью кремния. Восстановленные щелочные металлы при низких температурах окисляются до соответствующих окислов, которые уносятся печным газом вместе с первичной пылью шихты и, по мере снижения температуры печного газа, конденсируются, образуя основу частиц вторичной пыли. [c.6]
Для создания большого многообразия сложных органических веществ растения потребляют значительное количество питательных элементов кислород и водород они получают в виде воды, углерод ассимилируют из воздуха, а азот, фосфор, серу, калий, кальций, магний, бор, цинк, молибден, медь и другие поглощают из почвы. Всего растениями потребляется свыше 50 химических элементов. [c.194]
При использовании воды источника и водопровода для производственных целей будут иметь значение другие показатели. Так, для развития биологических обрастаний теплообменных аппаратов, градирен и трубопроводов имеет значение наличие в воде биогенных элементов — азота, углерода, фосфора и железа, а также органических веществ, которые при наличии в воде кислорода Я при благоприятной температуре (15—40° С) обеспечивают питание и жизненные условия для развития микроорганизмов. [c.444]
Выпуск неочищенных сточных вод никотиновых заводов в естественные водоемы, особенно маломощные, нарушит процессы естественного самоочищения воды и создаст в водоеме анаэробные условия. Интенсивная окраска и резкий специфический запах сточных вод ухудшат физические свойства воды. Наличие большого количества питательных соединений в стоке (азота, углерода, фосфора) может вызвать пышное развитие микроорганизмов по течению реки, что создаст угрозу использования речной воды для технических целей. [c.92]
Образующийся СО и парообразный фосфор удаляются из реакционной печи и поступают в холодильни с водой, где фосфор оседает в виде белого фосфора. Оксид углерода (И) удаляется, а расплавленную масс Са510з (шлак) периодически выпускают из печи. Это-, шлак может быть использован для изготовления шлако блочных кирпичей, технического стекла. Так как нр производстве фосфора все продукты удаляются из элек трической печи, то процесс является непрерывным Шихта в печь поступает непрерывно из бункера с по мощью шнековой подачи. [c.260]
Из простых тел только немногие металлы соединяются с водородом (напр., палладий, натрий), и дают вещества, очень легко разлагаемые . некоторые же металлы, особенно платина и железо, способны его поглощать (см. далее, окклюзия). Из металлоидов галоиды (фтор, хлор, бром и иод) легче всего образуют свои единственные водородистые соединения из них хлористый й особенно фтористый водород прочны, а бромистый и особенно иодистый водород легко разлагаемы другие же металлоиды, напр., сера, углерод, фосфор, дают водородистые соединения различного состава и свойств, но обыкновенно менее прочные, чем вода, и получаемые рааио-образдыми способами, чаще всего замещением металлов водородом. [c.419]
Алюминий во МН01Г0М напоминает бор, но металлические свойства его выражены гораздо ярче. В частности, соединение окисла алюминия с водой уже обнаруживает свойства основания не в виде исключения, как у бора, а почти как праиило. Как близкие родственники похожи кремний — на углерод, фосфор — на азот, с е р а — на кислород, хлор —на фтор. Снова подобралась группа, в которой исчерпаны все главные химические свойства — от активнейшего металла до типичного неметалла. И очередной в последовательности атомов калий, открывающий следующую, третью группу элементов, — опять активнейший металл, член семейства лития и натрия, идущий за ним к а л ь ц и й— родич бериллия и магния и т. п. [c.168]
В этой реакции, родственной реакции Виттига, вместо илидов фосфора используются фосфонатные карбанионы [489]. Эта реакция обладает следующими преимуществами во-первых, фосфонатный карбанион более нуклеофилен и реагирует в мягких условиях с самыми разнообразными альдегидами и кетона-ми во-вторых, растворимость фосфонатов в воде облегчает выделение продуктов реакции из реакционной смеси при обработке в-третьих, фосфонаты, которые получают по реакции Арбузова, дешевле и более доступны. Обычные фосфонаты, с успехом используемые в реакции Хорнера, включают заместитель К , резонансно стабилизирующий карбанион. Если Кз = Н или алкил, то олефины образуются с низким выходом. С точки зрения стереохимии образованию гранс-олефинов благоприятствуют небольшие заместители у а-углерода фосфоната. Стерические затруднения как в фосфонате, так и в карбонильном реактанте способствуют промежуточному образованию бетаина, что приводит к чис-олефинам [490, 491]. [c.257]
На рис. 6.10 приведены принципиальные схемы биофильтра и аэротенка. В процессе очистки сточных вод микроорганизмы активного ила и биопленки, контактируя с органическими веществами, разрушают их при помощи большого количества ферментов, состав которых еще недостаточно изучен. Для создания протоплазмы клетке нужны биогенные элементы — углерод, водород, кислород, азот, фосфор, калий, железо, сера, магний и различные микроэлементы. Многие из этих элементов бактериальная клетка может почерпнуть из загрязнений сточных вод. Недостающие элементы — чаще всего азот, фосфор, калий — приходится добавлять в очищаемую жидкость. [c.349]
При обычной температуре свободный азот химически малоактивный элемент. Лишь с литием он реагирует при низких температурах, образуя нитрид. С другими элементами азот не реагирует даже при высокой температуре. Исключение составляют три неметалла — бор, углерод, фосфор — и металлы — кальций, барий, магний, алюминий, марганец, титан, церий и уран. Три последних металла при высоких температурах весьма бурно реагируют с азотом, как бы сгорая в атмосфере азота с образованием нитридов. При растворении в воде все нитриды, за исключением нитрида титана, разлагаются, образуя окислы или гидроокислы металлов и аммиак. Казалось весьма заманчивым использовать это свойство нитридов металлов для получения аммиака, но, к сожалению, обратное восстановление металлов из их окислов является слишком сложным, энергоем- [c.10]
В исследованиях, проведенных Э. В. Брицке, Н. Е. Пестовьш и Н. Н. Постниковым [22], процесс окисления фосфора парами воды изучался на установке, показанной на рис. 121. Азот или двуокись углерода, подаваемые из баллона, проходили регулятор давления 1 и измеритель скорости 4 и поступали в прибор 7 для последовательного насыщения газа парами воды и фосфора. Реакционная газовая смесь далее вводилась в электрическую трубчатую печь 15, заполненную катализатором. По выходе из печи газы проходили через электрофильтр 19 для улавливания тумана фосфорной кислоты. [c.249]
Белый фосфор не только огнеопасен, но и ядовит. Для безопасности поглотительный и уравнительный сосуды помещают в металлический ящик с водой. Вместо фосфора часто пользуются щелочным раствором пирогаллола, который приготовляют из пирогаллола и едкого кали. В 180 см воды растворяют 76 г КОН и в 100 см воды при нагревании растворяют 44 г пирогаллола. Затем оба раствора смешивают и. хранят в закрытом сосуде из темного стекла. Раствор годен в течение нескольких месяцев. При иопользовании пирогаллола применяют такой же прибор, как и показанный на рис. 216. В поглотительный сосуд заливают раствор пирогаллола и помещают стеклянные трубки, которые, смачиваясь раствором, увеличивают поверхность его контакта с газом. На трубку 4 надевают мешочек из резиновой пленки, чтобы предотвратить контакт раствора с воздухом. (Кислород из газа, находящегося в сосуде 1, поглощается раствором сразу после сборки прибора.) В процессе поглощения кислорода раствором пирогаллола выделяется некоторое количество окиси углерода, которая присоединяется к анализируемой пробе газа. При малых концентрациях кислорода (до 10— 15%) это явление не дает значительной ошибки, но при больших содержаниях кислорода в смеси результат анализа может исказиться. Поэтому на пирогаллоловом приборе анализируют только технический азот или сырой аргон. Раствор заменяют после 100—120 анализов. [c.354]
Э. В. Брицке с сотрудниками были изучены реакции между фосфором и окисью углерода, фосфором и углекислотой, между фосфорным ангидридом и окисью углерода, фосфорным ангидридом и водородом, между фосфористым водородом, водой и углекислотой. Можно сказать, что Э. В. изучил ббльшую часть реакций взаимодействия фосфоритов с различными реагентами, проторил новые пути, которые будут еще многие годы служить прогрессу технологии важнейшего элемента жизни . Значительная часть этих его исследований освещена в монографии. Термическое получение фосфорной кислоты и высокопроцентных фосфатов , написанной Э. В. Брицке и И. Е. Пестовым (1929). После Великой Отечественной войны Э. В. совместно с А. А. Ионасс провел ценные в теоретическом и практическом отношениях работы по химии и технологии плавленых магнезиальных фосфатов. [c.10]
Кремнезем отнимает от фосфата оксид кальция, а образующийся оксид фосфора (V) восстанавливается углеродом. Фосфор получают в герметически закрытой электрической печи, где высокая температура развивается за счет образования электрической дуги между угольными электродами, погруженными в шихту, и за счет сопротивления шихты. Это производство относится к числу электротермических, в которых переменный электрический ток применяется для нагревания в результате превращения электрической энергии в тепловую. Углерод вводят в виде кокса или антрацита. Большим преимуществом этого способа является возможность использования даже низкопроцентных фосфоритов после обжига их для разложения примесей. Печь загружают периодически, так же выпускают из нее силикат. Расход электроэнергии составляет 13—15 тыс. квт-ч на 1 т фосфора. Мощность печи до 72 тыс. кет. Отходящий газ, содержащий пары белого фосфора, очищают в электрофильтре от пыли, охлаждают и пары фосфора конденсируют под горячей (60 °С) водой. Жидкий фосфор (темп. пл. 44 °С) сжигают в камере при соединении образующегося оксида фосфора (V) с водой можно получить фосфорную кислоту любой концентрации (обычно не менее 85%) или даже (при количестве воды менее 3 моль на 1 моль Р2О5) так называемую полифосфорную (суперфосфорную) кислоту она представляет собой смесь кислот с преобладанием пиро- и триполифосфорной в пересчете на Н3РО4 имеет концентрацию до 115%. Это, а также высокая чистота термической кислоты являются достоинствами этого способа производства. Мощность до 80 тыс. т 100-процентной кислоты в год. Фосфорную кислоту используют главным образом для получения концентрированных фосфорных удобрений, а также других ее солей. [c.87]
Прежде всего необходимо определить, относится ли данное вещество к органическим, т. е. содержит ли оно в своем составе углерод. Для этой цели испытуемое вещество сжигают на воздухе. Если оно горит, то с большой вероятностью можно предположить присутствие углерода но гореть могут и другие вещества (например, содержащие фосфор или серу). Если горение сопровождается копотью, присутствие углерода ясно если копоти нет, газообразные продукты горения пропускают через известковую или баритовую воду углерод, если он есть, при горении превращается в угольный ангидрид, СО , который в. известковой или баритовой воде производит муть (осадок СаСОд или ВаСОд). Вместо простого сожигания на воздутсе можно накаливать испытуемое вещество, смешанное с чистой окисью меди, в трубке из тугоплавкого стекла. На счет кислорода окиси меди углерод окисляется в СО , который открывается реакцией с известковой или баритовой водой. [c.6]
Большие успехи достигнуты в области определения углерода, фосфора и серы — наиболее важных элементов в технологии производства стали. Определение этих элементов проводят, используя вакуумные спектрометры, причем нробу возбу>1 дают искровым разрядом в атмосфере аргона. Основные линии этих э. 1ементов расположены в области 2000 А, которую поглощают кис.т1ород воздуха и пары воды. Применение вакуумных спектрометров или спектрометров с аргоновой продувкой -- единственное решение проблемы определения углерода, фосфора и серы. [c.177]
Поступающее на нефтетехнологические установки нефтяное сырье значительно различается по физико-химическим константам углеводородному составу, плотности, вязкости, содержанию растворимых в нефтях минеральных солей, газа, серы, парафина, механических примесей и др. Кроме углерода и водорода, которые обычно составляют 95—97 вес. % (в том числе С —84—85 вес. %, И—12—14 вес. %), в нефти находится не менее 3—4 вес. % побочных элементов и соединений — кислорода, фосфора, серы, газа, воды и др. [c.23]
chem21.info
Четыреххлористый углерод с водой - Справочник химика 21
II 298,15° К окиси углерода, двуокиси углерода, водорода, кис лорода, азота, четыреххлористого углерода, воды, сероводорода аммиака, двуокиси серы. Результаты сопоставить с приложением 1 [c.85]Газовый конденсат Четыреххлористый углерод Вода 3.5—16,5 1.5-8,5 до 100 Удаление АСПО А. с. 1180375 [c.123]
Это было показано нами совместно с С. И. Кольцовым (1963 г.) на модельных системах поликремниевая кислота — четыреххлори-стый углерод и поликремниевая кислота — четыреххлористый углерод— вода. [c.245]
Отделив щелочной слой, промывают четыреххлористый углерод водой (при встряхивании) и повторяют обработку половинным количеством водноспиртового раствора едкого кали. [c.70]Изучению состояния воды, находящейся в растворах, посвящено много работ. При этом наибольщее внимание уделено изучению состояния воды, растворенной в полярных растворителях, нежели в растворителях неполярных. Равновесные концентрации воды, растворенной в неполярных растворителях, на несколько порядков ниже, чем в полярных, что, естественно, существенно затрудняет постановку эксперимента. Больше других изучены ИК-спектры растворенной в четыреххлористом углероде воды [40, 132, 158—160]. На участке спектра 4000—3000 сл , соответствующего валентным колебаниям ОН-групп молекул воды, наблюдаются две четко выраженные и интенсивные полосы поглощения с максимумами 3614 н 3705 см К Указанные полосы принадлежат симметричным и асимметричным колебаниям молекул воды, растворенной в ССЦ. [c.47]
В полярных системах, очевидно, образуются сильные водородные связи между водой и молекулами растворителя. Это можно проиллюстрировать на примере системы, содержащей диоксан. В разбавленных растворах во многих неполярных растворителях, например в четыреххлористом углероде, вода может находиться в свободном состоянии, если не образуются межмолекулярные водородные связи. Гидроксильные группы, не участвующие в образовании водородных связей, обычно дают в спектре узкие полосы, а связанные группы — интенсивные широкие полосы поглоще- [c.380]
На рис. 8-6 показана зависимость химического сдвига сигнала протонов воды от содержания воды в системе вода—ацетон. В этом случае при увеличении содержания воды наблюдается последовательный сдвиг сигнала в сильное поле. Заметное влияние окружения (эффект среды) на химический сдвиг протонов воды иллюстрируют примеры, приведенные в табл. 8-2. При почти одинаковом содержании воды в рассматриваемых системах наблюдается существенное различие химических сдвигов относительно сигналов метильных протонов. В четыреххлористом углероде вода находится преимущественно в форме мономера. При 0,14% (мол.) воды величина наблюдаемого химического сдвига относительно метильных протонов ТМС составляет 1,0 м. д., что соответствует только 0,016% НзО, определенной с помощью реактива Фишера. При 800-кратном усилении сигнал ЯМР воды регистрируется вполне надежно даже при столь низком содержании воды. [c.461]
Окисление четыреххлористого углерода водой в хлороформ температура 15—20° Мелкодиспергированное железо как катализаторы могут применяться металлические свинец, медь, магний, сурьма или теллур, или их соединения могут применяться также смеси с солями аммония, например бромистым аммонием, уксуснокислым аммонием или щавелевокислым аммонием 788 [c.213]
К рассмотренному методу принципиально очень близок метод определения коэффициентов активности по распределению вещества между двумя жидкими фазами. Разница состоит только в том, что вместо распределения вещества между газообразной и жидкой фазами теперь происходит распределение вещества между жидкими не смешивающимися фазами. Чаще всего исследуют распределение между неводной и водной фазами. Распределение становится возможным тогда, когда жидкости не смешиваются между собой. Поскольку, однако, принципиально нет несмешивающихся жидкостей и взаимная растворимость часто изменяется — увеличивается под влиянием распределяемого вещества, то этот способ не очень точен. Но в ряде случаев, например в сисгемах четыреххлористый углерод — вода или бензол — вода, взаимная растворимость невелика. [c.89]
Четыреххлористый углерод Вода 6 [c.459]
С целью проверки применимости изложенного метода" к описанию экстракционных систем нами изучены при 25° С фазовые равновесия в следуюш их простейших системах тина вода — экстрагент — разбавитель вода — ТБФ — дибутилфосфат (ДБФ) вода — ТБФ — бензол вода — ДБФ — бензол вода — ТБФ — н.гептан вода — ТБФ — четыреххлористый углерод вода — ТБФ — дибутиловый эфир вода — ТБФ — хлороформ. Системы такого рода особенно удобны для наших целей, так как вследствие малой растворимости экстрагента и разбавителя в воде одной из равновесных фаз постоянно является практически чистая вода, что позволяет определять коэффициенты активности воды в органической фазе вдоль линии расслаивания непосредственно из данных по растворимости воды. Изучены также следуюш,ие тройные системы типа вода — экстрагент — экстрагируемое веш,ество вода — ТБФ — иодистый калий [9] вода — ТБФ — иодистый натрий вода — ТБФ — азотнокислое серебро. Можно полагать, что в этих системах процессы стехиометрического гидрато- и соль-ватообразования не имеют места. Изопиестическим методом изучены при 25° С двойные системы вода — ТБФ и вода — ДБФ [Ю]. Обе системы могут быть описаны трехчленными уравнениями Маргулеса. [c.80]
Спирты С1— i Хлороформ ИЛИ четыреххлористый углерод Вода У Целит [c.519]
Четыреххлористый углерод — вода [c.325]
Вода — этиловый спирт — четыреххлористый углерод. Вода — н- или изо-пропиловый спирт — четыреххлористый углерод, Солютропы. [c.211]
Коэффициент распределения дитизона в системе четыреххлористый углерод — вода (pH —1) найден равным 1,1 10 [50 ], иными словами, в кислых растворах дитизон почти полностью находится в фазе органического растворителя. [c.20]
Он устойчив только при пониженной температуре, образует светло-желтые кристаллы с температурой плавления от —2 до —3°. Расплав вскоре спонтанно разлагается с выделением желтого дыма и с образованием кирпично-красного аморфного твердого вещества. Несколько устойчивее он в растворе. В спирте и эфире родан растворяется чрезвычайно легко, хорошо растворим он также в сероуглероде и четыреххлористом углероде. Вода тотчас разлагает (S N)2. В органических растворителях также протекает разложение — медленное при низких температурах, моментальное при комнатной температуре. При этом выделяется желтое аморфное вещество, которое получал еще Либих, пытаясь приготовить свободный родан путем окисления цианидов хлором в водных растворах. В химическом отношении свободный родан очень напоминает иод. Он также соединяется с металлами и даже обладает почти такой же окислительной способностью, как иод. Родан способен вытеснять свободный иод из иодидов.и сам может быть вытеснен избытком иода. Следовательно, существует отчетливое равновесие [c.505]
Растворимость Легко растворим в этилацетате, ацетоне растворим в метиленхлориде, этиловом спирте плохо растворим в бензоле практически нерастворим в бензине, четыреххлористом углероде, воде Плохо растворим в бензине, бе золе, четыреххлористом углерод метиленхлориде, этиловом спирт ацетоне практически нераствор в бензине, этилацетате и воде [c.428]
В работе [173], проводившейся импульсным методом в ПСЭ двух размеров (0 = 0,056 и 0,3 м) на системах четыреххлористый углерод — вода и трихлорэтилен — вода были получены зависимости Ес и д от интенсивности пульсаций I, аналогичные указанным выше, причем точка максимума на кривой Ец=1[х) соответствовала точке минимума на кривой зависимости задержки от интенсивности пульсаций х=1 1). [c.324]
Более подробное исследование массопередачи при различных гидродинамических режимах работы ПСЭ было осуществлено Циолковским и Новинска [183]. Опыты проводились в лабораторном аппарате (Дк = 0,059 м, Яр = 0,445 м, о = 3 мм, /гт = 50 мм, ф = =23,6%) на системах дихлорэтан — вода четыреххлористый углерод— вода трихлорэтилен — вода диметилбензол — вода. Распределяемым компонентом во всех случаях являлась уксусная кислота. Авторами предложены идентичные по структуре уравнения для ВЕП в дисперсной и сплошной фазах [c.325]
Эти явления отмечаются не только на каплях, но и на плоской поверхности раздела фаз. На фото 6.18 показана [51] одновременная массопередача фенола и пропиоиовой кислоты в системе четыреххлористый углерод — вода в горизонтальном прямоточном смесителе. Концентрация и направление массопередачи выбраны таким образом, чтобы избежать образования концентрационных вихрей, часто затемняющих картину, а иногда вызывающих истинную межфазную конвекцию. Именно это происходило при переносе про-пионовой кислоты из четырехх.т1ористого углерода в воду и фенола в обратном направлении. [c.238]
Бесцветная легко подвижная, остро пахнущая, чрезвычайно едкая жидкость, сильно дымящая на воздухе. Пл. 2,852 г/см при 15 °С. Т. пл. —40, т. кип. 172,9 С. Растворима в диэтиловом эфире, ацетоне, хлороформе, бензоле, сероуглероде и четыреххлористом углероде. Водой реактив разлагается (с сильным выделением тепла), образуя HjPOa и НВг, с этиловым спиртом выделяет бромистый этил. [c.375]Кларк и Тэйлор, проверявшие синтез, рекомендуют для получения абсолютно безводного аллилового спирта с.л(едующий способ продукт, полученный высаливанием поташом, перегоняют по способу, указанному выше, и, получив спирт, содержащий около 30% воды, смешивают его с четвертой частью (по объему) четыреххлористого углерода (примечание 6). Затем смесь медленно перегоняют из круглодонной колбы с дефлегматором высотой не менее 80 См. Первую низкокипящую фракцию, состоящую из четыреххлористого углерода, воды и аллилового спирта, сушат поташом и выливают обратно в колбу (примечание 7). Этот процесс повторяют несколько раз до тех пор, пока в первой фракции почти не будет воды. Затем смесь перегоняют полностью, собирая следующие фракции до 80°, 80—90°, 90—95,5°, 95,5—97° последняя представляет собой спирт, который по титрованию бромом содержит 100% чистого вещества остальные фракции сушат отдельно и снова фракционируют таким образом получают еще некоторое количество продукта, кипящего при 95,5—97°. [c.26]
В обобщающел исследовании гидродинамики и массопередачи в пульсационных колоннах Каган и др. [76] определяли величину продольной дисперсии сплошной фазы в системах керосин — вода и четыреххлористый углерод — вода. Проведены две серии экспериментов с введением индикатора в виде дельта-импульса. Измерены общие коэффициенты продольного перемешивания Еа. Для определения коэффициентов Ев применяли стационарный метод введения индикатора. Получены значительные расхождения между этими велнчиналш, но не было сделано попыток объяснить его. [c.144]
Диметилсудь-фоксид, четыреххлористый углерод, вода, бензол [c.774]
Добавки бензола, четыреххлористого углерода, воды, соли Ге(1И), Си(1), Си(И) оказывают значительное влияние на гомолитическое присоединение треххлористого фосфора к непредельным соединениям, что показано на примере циклогексена табл. 23) [18]. Добавки бензола, СС14 и воды повышают выход хлорциклогексил-дихлор фосфин а. Добавки соли Ге(П1) снижают выход на 70—80%, а соли Си(1) и Си(П) полностью ингибируют процесс присоединения. Такое влияние добавок подтверждает радикально-цепной механизм [c.46]
Эйзенберг и Кауцман [44 ] проанализировали обширную литературу о структуре и свойствах воды и предложили теорию, удовлетворяющую большинству надежных экспериментальных данных. Вероятно, наиболее полное рассмотрение свойств и структуры воды было проведено Дорси [38]. В обзоре Христиана и сотр. [29] рассмотрены сложные молекулярные структуры воды в газовой фазе и в разбавленных растворах в полярных и неполярных органических растворителях и приведены константы равновесия образования ряда комплексов амин — вода в неполярных растворителях. В противоположность выводам Дорси [38] о почти полной идеальности паров воды, данные Р — V —Т при высоких температурах [79] и ИК-спектры [93] свидетельствуют о значительных отклонениях от идеальности и о существовании агрегатов при температурах выше 100 °С. Шибата и Бар-телл [139] исследовали структуру водяных паров методом дифракции электронов с использованием секторного микрофотометра. Имеются указания на то, что в углеводородах и в четыреххлористом углероде вода находится в форме мономера [29]. (См. также гл. 7.) В слабополярных органических растворителях присутствует, однако, некоторое количество полимерной воды. Константы образования димеров и тримеров воды в органических жидкостях, а также константы равновесия гидратообразования для кетонов, простых эфиров, амидов, диметилсульфоксида и комплексов амины — вода приведены в работе [29]. Магнуссон [96] [c.9]
Гизоамилацетат, толуол, дихлорэтан, четыреххлористый углерод - вода керосин-диэтиленгликоль [c.112]
Кафаров исследовал экстракцию бензойной и уксусной кислот из четыреххлористого углерода водой в очень малых инжекторах (длина около 75 мм, внутренний диаметр отверстия сопла примерно 2,5 жж). Достигалась эффективность ступепи от = 0,8 до =1,0 при расходах жидкостей приблизительно от 0,06 до 0,1 м 1ч. Расход энергии был относительно невысок, величина P/Q изменялась в пределах 1400—40 000 дж1м . Эти инжекторы были применены для промышленной экстракции антибиотиков [c.488]
Раствор для поглощения хлора (растворяют в 1 л воды 270 г хлорида натрия и 25 г роданида калия или 100 г тиосульфата натрия) раствор гидрокснда натрия (200 г в 1 л) четыреххлористый углерод вода дистиллированная [c.516]
Значения К для систем четыреххлористый углерод — вода и хлороформ — вода неоднократно определялись также в присутствии различных электролитов. Для систем бензол — вода и изоамиловый спирт — вода значение К равно соответственно 2,9 10 и 0,1 10 ° [52 ] . Соотношение [П20г]орг./[Н02Чводн. (7) служит мерой экстракции дитизона данным органическим растворителем из водного щелочного раствора при определенном pH. На рис. 5 приведены кривые распределения дитизона в двух наиболее часто применяющихся в анализе двухфазных системах растворителей. Переход дитизона [c.21]
В щелочном растворе преимущественно образуется красно-коричневый комплекс АигОгз, не растворимый в воде и трудно растворимый в четыреххлористом углероде [35 ]. Из растворов минеральных кислот с помощью раствора дитизона в четыреххлористом углероде выделяется экстракт красновато-желтого цвета с серо-коричневатыми хлопьями, сконцентрированными на границе четыреххлористый углерод — вода. С помощью дитизона в хлороформе получают прозрачный красновато-желтый экстракт. На основании израсходованного количества дитизона установлено, что эти экстракты представляют собой смесь, состоящую из Аи(Н02)з -Ь + АпгОгз. В экстракте четыреххлористого углерода содержится преимущественно комплекс Аи(НВг)з, в хлороформном экстракте — преимущественно комплекс АпгОгз. Состав экстракта меняется в зависимости от взятой концентрации исходного компонента и значения pH. В определенных значениях pH и определенных пределах концентраций органические экстракты в данном органическом растворителе имеют довольно идентичный состав, что позволяет использовать для многих целей [c.189]
П. получают радикальной полимеризацией соответствующих винилимидазолов в ирисутствии динитрила азодиизомасляной к-ты, гидроперекиси кумола или персульфата калия в среде бензола, трет-бутило-вого спирта или воды. К-Винил-2-метилимидазол иоли-MepjKiyoT H иод действием одиовремеппо четыреххлористого углерода, воды и целлюлозы. [c.203]
Уотсон с сотр. [63—65] провели в насадочном экстракторе ( >к==50 мм, Я = 610 мм, насадка — фарфоровые кольца Ращига, н = 9,5 мм) исследования предельных нагрузок на системах жидкость — жидкость (вода — ртуть ртуть — раствор глицерина диб-ромметан — вода четыреххлористый углерод — вода), отличающихся значительно большим диапазоном изменения физических свойств (Лр, х), чем обычно применяющиеся йодно-органические системы. Обработкой результатов собственных опытов и данных других исследователей (всего для 56-ти систем жидкость — жидкость) показано, что предельные фиктивные скорости фаз (Ус)з и (Од)з связаны зависимостью [c.279]
chem21.info





















