Секреты водно-солевого баланса или зачем нужны электролиты при похудении? Вода электролит
примеры. Состав и свойства электролитов. Сильные и слабые электролиты
Электролиты как химические вещества известны с древних времён. Однако большинство областей своего применения они завоевали относительно недавно. Мы обсудим самые приоритетные для промышленности области использования этих веществ и разберёмся, что же последние собой представляют и чем отличаются друг от друга. Но начнём с экскурса в историю.

История
Самые старые известные электролиты - это соли и кислоты, открытые ещё в Древнем мире. Однако представления о строении и свойствах электролитов развивались со временем. Теории этих процессов эволюционировали, начиная с 1880 годов, когда был сделан ряд открытий, связанный с теориями свойств электролитов. Наблюдались несколько качественных скачков в теориях, описывающих механизмы взаимодействия электролитов с водой (ведь только в растворе они приобретают те свойства, благодаря которым их используют в промышленности).
Сейчас мы подробно разберём несколько теорий, оказавших наибольшее влияние на развитие представлений об электролитах и их свойствах. И начнём с самой распространённой и простой теории, которую каждый из нас проходил в школе.
Теория электролитической диссоциации Аррениуса
в 1887 году шведский химик Сванте Аррениус и русско-немецкий химик Вильгельм Оствальд создали теорию электролитической диссоциации. Однако тут тоже не всё так просто. Сам Аррениус был сторонником так называемой физической теории растворов, которая не учитывала взаимодействие составляющих вещества с водой и утверждала, что в растворе существуют свободные заряженные частицы (ионы). Кстати, именно с таких позиций сегодня рассматривают электролитическую диссоциацию в школе.
Поговорим всё-таки о том, что даёт эта теория и как она объясняет нам механизм взаимодействия веществ с водой. Как и у любой другой, у неё есть несколько постулатов, которые она использует:
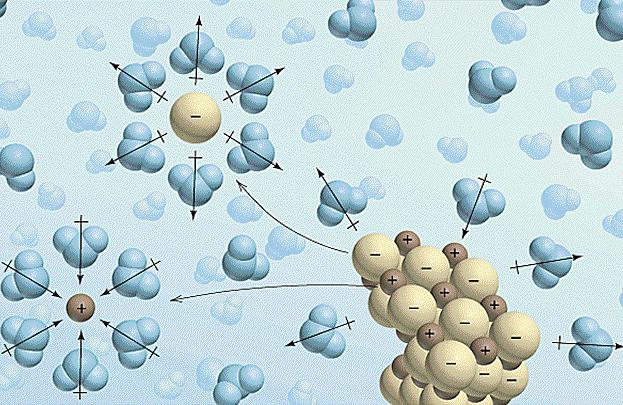
1. При взаимодействии с водой вещество распадается на ионы (положительный - катион и отрицательный - анион). Эти частицы подвергаются гидратации: они притягивают молекулы воды, которые, кстати, заряжены с одной стороны положительно, а с другой - отрицательно (образуют диполь), в результате формируются в аквакомплексы (сольваты).
2. Процесс диссоциации обратим - то есть если вещество распалось на ионы, то под действием каких-либо факторов оно вновь может превратиться в исходное.
3. Если подключить к раствору электроды и пустить ток, то катионы начнут движение к отрицательному электроду - катоду, а анионы к положительно заряженному - аноду. Именно поэтому вещества, хорошо растворимые в воде, проводят электрический ток лучше, чем сама вода. По той же причине их назвали электролитами.
4. Степень диссоциации электролита характеризует процент вещества, подвергшегося растворению. Этот показатель зависит от свойств растворителя и самого растворённого вещества, от концентрации последнего и от внешней температуры.
Вот, по сути, и все основные постулаты этой несложной теории. Ими мы будем пользоваться в этой статье для описания того, что же происходит в растворе электролита. Примеры этих соединений разберём чуть позже, а сейчас рассмотрим другую теорию.

Теория кислот и оснований Льюиса
По теории электролитической диссоциации, кислота - это вещество, в растворе которого присутствует катион водорода, а основание - соединение, распадающееся в растворе на гидроксид-анион. Существует другая теория, названная именем известного химика Гилберта Льюиса. Она позволяет несколько расширить понятие кислоты и основания. По теории Льюиса, кислоты - это ионы или молекулы вещества, которые имеют свободные электронные орбитали и способны принять электрон от другой молекулы. Несложно догадаться, что основаниями будут являться такие частицы, которые способны отдать один или несколько своих электронов в "пользование" кислоте. Очень интересно здесь то, что кислотой или основанием может быть не только электролит, но и любое вещество, даже нерастворимое в воде.

Протолитическая теория Брендстеда-Лоури
В 1923 году, независимо друг от друга, двое учёных - Й. Бренстед и Т. Лоури -предложили теорию, которая сейчас активно применяется учёными для описания химических процессов. Суть этой теории в том, что смысл диссоциации сводится к передаче протона от кислоты основанию. Таким образом, последнее понимается здесь как акцептор протонов. Тогда кислота является их донором. Теория также хорошо объясняет существование веществ, проявляющих свойства и кислоты и основания. Такие соединения называются амфотерными. В теории Бренстеда-Лоури для них также применяется термин амфолиты, тогда как кислота или основания принято называть протолитами.
Мы подошли к следующей части статьи. Здесь мы расскажем, чем отличаются друг от друга сильные и слабые электролиты и обсудим влияние внешних факторов на их свойства. А затем уже приступим к описанию их практического применения.
Сильные и слабые электролиты
Каждое вещество взаимодействует с водой индивидуально. Какие-то растворяются в ней хорошо (например, поваренная соль), а какие-то совсем не растворяются (например, мел). Таким образом, все вещества делятся на сильные и слабые электролиты. Последние представляют собой вещества, плохо взаимодействующие с водой и оседающие на дне раствора. Это означает, что они имеют очень низкую степень диссоциации и высокую энергию связей, которая не позволяет при нормальных условиях распадаться молекуле на составляющие её ионы. Диссоциация слабых электролитов происходит либо очень медленно, либо при повышении температуры и концентрации этого вещества в растворе.
Поговорим о сильных электролитах. К ним можно отнести все растворимые соли, а также сильные кислоты и щёлочи. Они легко распадаются на ионы и очень трудно собрать их в осадки. Ток в электролитах, кстати, проводится именно благодаря ионам, содержащимся в растворе. Поэтому лучше всех проводят ток сильные электролиты. Примеры последних: сильные кислоты, щёлочи, растворимые соли.
Факторы, влияющие на поведение электролитов
Теперь разберёмся, как влияет изменение внешней обстановки на свойства веществ. Концентрация напрямую влияет на степень диссоциации электролита. Более того, это соотношение можно выразить математически. Закон, описывающий эту связь, называется законом разбавления Оствальда и записывается так: a = (K / c)1/2. Здесь a - это степень диссоциации (берётся в долях), К - константа диссоциации, разная для каждого вещества, а с - концентрация электролита в растворе. По этой формуле можно узнать много нового о веществе и его поведении в растворе.
Но мы отклонились от темы. Кроме концентрации, на степень диссоциации также влияет температура электролита. Для большинства веществ её увеличение повышает растворимость и химическую активность. Именно этим можно объяснить протекание некоторых реакций только при повышенной температуре. При нормальных условиях они идут либо очень медленно, либо в обе стороны (такой процесс называется обратимым).
Мы разобрали факторы, определяющие поведение такой системы, как раствор электролита. Сейчас перейдём к практическому применению этих, без сомнения, очень важных химических веществ.
Промышленное использование
Конечно, все слышали слово "электролит" применительно к аккумуляторам. В автомобиле используют свинцово-кислотные аккумуляторы, роль электролита в котором выполняет 40-процентная серная кислота. Чтобы понять, зачем там вообще нужно это вещество, стоит разобраться в особенностях работы аккумуляторов.
Так в чём принцип работы любого аккумулятора? В них происходит обратимая реакция превращения одного вещества в другое, в результате которой высвобождаются электроны. При заряде аккумулятора происходит взаимодействие веществ, которого не получается при нормальных условиях. Это можно представить как накопление электроэнергии в веществе в результате химической реакции. При разряде же начинается обратное превращение, приводящее систему к начальному состоянию. Эти два процесса вместе составляют один цикл заряда-разряда.
Рассмотрим вышеизложенный процесс на конкретном примере - свинцово-кислотном аккумуляторе. Как нетрудно догадаться, этот источник тока состоит из элемента, содержащего свинец (а также диокисд свинца PbO2) и кислоты. Любой аккумулятор состоит из электродов и пространства между ними, заполненного как раз электролитом. В качестве последнего, как мы уже выяснили, в нашем примере используется серная кислота концентрацией 40 процентов. Катод такого аккумулятора делают из диоксида свинца, а анод состоит из чистого свинца. Всё это потому, что на этих двух электродах протекают разные обратимые реакции с участием ионов, на которые продиссоциировала кислота:
- PbO2 + SO42-+ 4H+ + 2e- = PbSO4 + 2h3O (реакция, происходящая на отрицательном электроде - катоде).
- Pb + SO42- - 2e- = PbSO4 (Реакция, протекающая на положительном электроде - аноде).
Если читать реакции слева направо - получаем процессы, происходящие при разряде аккумулятора, а если справа налево - при заряде. В каждом химическом источнике тока эти реакции разные, но механизм их протекания в общем описывается одинаково: происходят два процесса, в одном из которых электроны "поглощаются", а в другом, наоборот, "выходят". Самое главное то, что число поглощённых электронов равно числу вышедших.
Собственно, кроме аккумуляторов, существует масса применений этих веществ. Вообще, электролиты, примеры которых мы привели, - это лишь крупинка того многообразия веществ, которые объединены под этим термином. Они окружают нас везде, повсюду. Вот, например, тело человека. Думаете, там нет этих веществ? Очень ошибаетесь. Они находятся везде в нас, а самое большое количество составляют электролиты крови. К ним относятся, например, ионы железа, которые входят в состав гемоглобина и помогают транспортировать кислород к тканям нашего организма. Электролиты крови также играют ключевую роль в регуляции водно-солевого баланса и работе сердца. Эту функцию выполняют ионы калия и натрия (существует даже процесс, происходящий в клетках, который назвается калий-натриевым насосом).
Любые вещества, которые вы в силах растворить хоть немного, - электролиты. И нет такой отрасли промышленности и нашей с вами жизни, где бы они ни применялись. Это не только аккумуляторы в автомобилях и батарейки. Это любое химическое и пищевое производство, военные заводы, швейные фабрики и так далее.
Состав электролита, кстати, бывает разным. Так, можно выделить кислотный и щелочной электролит. Они принципиально отличаются своими свойствами: как мы уже говорили, кислоты являются донорами протонов, а щёлочи - акцепторами. Но со времением состав электролита меняется вследствие потери части вещества концентрация либо уменьшается, либо увеличивается (всё зависит от того, что теряется, вода или электролит).
Мы каждый день сталкиваемся с ними, однако мало кто точно знает определение такого термина, как электролиты. Примеры конкретных веществ мы разобрали, поэтому перейдём к немного более сложным понятиям.

Физические свойства электролитов
Теперь о физике. Самое важное, что нужно понимать при изучении этой темы - как передаётся ток в электролитах. Определяющую роль в этом играют ионы. Эти заряженные частицы могут переносить заряд из одной части раствора в другую. Так, анионы стремятся всегда к положительному электроду, а катионы - к отрицательному. Таким образом, действуя на раствор электрическим током, мы разделяем заряды по разным сторонам системы.
Очень интересна такая физическая характеристика, как плотность. От неё зависят многие свойства обсуждаемых нами соединений. И зачастую всплывает вопрос: "Как поднять плотность электролита?" На самом деле ответ прост: необходимо понизить содержание воды в растворе. Так как плотность электролита большей частью определяется плотностью серной кислоты, то она большей частью зависит от концентрации последней. Существует два способа осуществить задуманное. Первый достаточно простой: прокипятить электролит, содержащийся в аккумуляторе. Для этого нужно зарядить его так, чтобы температура внутри поднялась чуть выше ста градусов по цельсию. Если этот способ не помогает, не переживайте, существует ещё один: просто-напросто заменить старый электролит новым. Для этого нужно слить старый раствор, прочистить внутренности от остатков серной кислоты дистиллированной водой, а затем залить новую порцию. Как правило, качественные растворы электролита сразу имеют нужную величину концентрации. После замены можете надолго забыть о том, как поднять плотность электролита.
Состав электролита во многом определяет его свойства. Такие характеристики, как электропроводность и плотность, например, сильно зависят от природы растворённого вещества и его концентрации. Существует отдельный вопрос о том, сколько электролита в аккумуляторе может быть. На самом деле его объём напрямую связан с заявленной мощностью изделия. Чем больше серной кислоты внутри аккумулятора, тем он мощнее, т. е. тем большее напряжение способен выдавать.

Где это пригодится?
Если вы автолюбитель или просто увлекаетесь автомобилями, то вы и сами всё понимаете. Наверняка вы даже знаете, как определить, сколько электролита в аккумуляторе находится сейчас. А если вы далеки от автомобилей, то знание свойств этих веществ, их применения и того, как они взаимодействуют друг с другом будет совсем не лишним. Зная это, вы не растеряетесь, если вас попросят сказать, какой электролит в аккумуляторе. Хотя даже если вы не автолюбитель, но у вас есть машина, то знание устройства аккумулятора будет совсем не лишним и поможет вам в ремонте. Будет гораздо легче и дешевле сделать всё самому, нежели ехать в автоцентр.
А чтобы лучше изучить эту тему, мы рекомендуем почитать учебник химии для школы и вузов. Если вы хорошо знаете эту науку и прочитали достаточно учебников, лучшим вариантом будут "Химические источники тока" Варыпаева. Там изложены подробно вся теория работы аккумуляторов, различных батарей и водородных элементов.
Заключение
Мы подошли к концу. Подведём итоги. Выше мы разобрали всё, что касается такого понятия, как электролиты: примеры, теория строения и свойств, функции и применение. Ещё раз стоит сказать, что эти соединения составляют часть нашей жизни, без которой не могли бы существовать наши тела и все сферы промышленности. Вы помните про электролиты крови? Благодаря им мы живём. А что насчёт наших машин? С помощью этих знаний мы сможем исправить любую проблему, связанную с аккумулятором, так как теперь понимаем, как поднять плотность электролита в нём.
Всё рассказать невозможно, да мы и не ставили такой цели. Ведь это далеко не всё, что можно рассказать об этих удивительных веществах.
fb.ru
Электролиты: понятие и свойства
Электролиты — растворы, содержащие большую концентрацию ионов, обеспечивающих прохождение электрического тока. Как правило, это водные растворы солей, кислот и щелочей.
Это интересно
В организме человека и животных электролиты играют важную роль: к примеру, электролиты крови с ионами железа транспортируют кислород в ткани; электролиты с ионами калия и натрия регулируют водно-солевой баланс организма, работу кишечника и сердца.
Свойства
Чистая вода, безводные соли, кислоты, щелочи ток не проводят. В растворах же вещества распадаются на ионы и проводят ток. Именно поэтому электролиты называют проводниками второго порядка (в отличие от металлов). Электролитами могут быть также расплавы и некоторые кристаллы, в частности диоксид циркония и иодид серебра.
Главное свойство электролитов — способность к электролитической диссоциации, то есть к распаду молекул при взаимодействии с молекулами воды (или других растворителей) на заряженные ионы.
По типу ионов, образующихся в растворе, различают электролит щелочной (электропроводимость обусловлена ионами металлов и ОН-), солевой и кислотный (с ионами Н+ и остатками основания кислоты).
Для количественной характеристики способности электролита к диссоциации введен параметр «степень диссоциации». Эта величина отражает процент молекул, подвергшихся распаду. Она зависит от: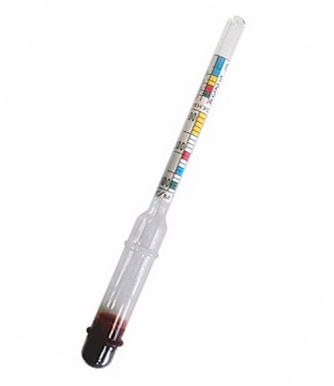 • самого вещества;• растворителя;• концентрации вещества;• температуры.
• самого вещества;• растворителя;• концентрации вещества;• температуры.
Электролиты делят на сильные и слабые. Чем лучше реагент растворяется (распадается на ионы), тем сильнее электролит, тем лучше он проводит ток. К сильным электролитам относятся щелочи, сильные кислоты и растворимые соли.
Для электролитов, использующихся в аккумуляторах, очень важен такой параметр, как плотность. От нее зависят условия эксплуатации аккумулятора, его емкость и срок службы. Определяют плотность с помощью ареометров.
Меры предосторожности при работе с электролитами
Самые популярные электролиты, это раствор концентрированной серной кислоты и щелочи — чаще всего гидроксиды калия, натрия, лития. Все они вызывают химические ожоги кожи и слизистых, очень опасные ожоги глаз. Именно поэтому все работы с такими электролитами нужно производить в отдельном, хорошо вентилируемом помещении, используя средства защиты: одежду, маски, очки, резиновые перчатки.• Рядом с помещением, где проводятся работы с электролитами, должна храниться аптечка с набором нейтрализующих средств и кран с водой. • Кислотные ожоги нейтрализуются раствором соды (1 ч.л. на 1 ст. воды).• Ожоги щелочью нейтрализуют раствором борной кислоты (1 ч.л. на 1 ст. воды).• Для промывания глаз нейтрализующие растворы должны быть в два раза слабее.• Поврежденные участки кожи сначала промывают нейтрализатором, а потом мылом и водой. • Если электролит пролили, его собирают опилками, потом промывают нейтрализатором и вытирают насухо.
При работе с электролитом следует выполнять  все требования техники безопасности. Например, кислоту наливают в воду (а не наоборот!) не вручную, а с помощью приспособлений. Куски твердой щелочи в воду опускают не руками, а щипцами или ложками. Нельзя работать в одном помещении с аккумуляторами на разнотипных электролитах, и хранить их вместе тоже запрещается.
все требования техники безопасности. Например, кислоту наливают в воду (а не наоборот!) не вручную, а с помощью приспособлений. Куски твердой щелочи в воду опускают не руками, а щипцами или ложками. Нельзя работать в одном помещении с аккумуляторами на разнотипных электролитах, и хранить их вместе тоже запрещается.
Некоторые работы требуют «кипения» электролита. При этом выделяется водород — горючий и взрывоопасный газ. В таких помещениях должна использоваться взрывобезопасная электропроводка и электроприборы, запрещается курение и любые работы с открытым огнем.
Хранят электролиты в пластиковых емкостях. Для работы подходит стеклянная, керамическая, фарфоровая посуда и инструменты.
В следующей статье расскажем подробнее о видах и применении электролита.
pcgroup.ru
Вода как слабый электролит. Понятие о рН растворов. Индикаторы.
Количество просмотров публикации Вода как слабый электролит. Понятие о рН растворов. Индикаторы. - 518
Тщательно очищенная от посторонних примесей вода обладает определённой, хотя и незначительной, электрической проводимостью, заметно возрастающей с повышением температуры. Наличие электрической проводимости должна быть объяснено только тем, что молекулы воды, частично распадаются на ионы, ᴛ.ᴇ. h3O является слабым электролитом. Процесс диссоциации воды должна быть записан
h3O + h3O ↔ h4O+ + OH¯. Этот процесс принято называть самоионизацией. Реакцию воды часто записывают в более простом виде:h3O ↔ H+ + OH¯. Константа диссоциации воды должна быть вычислена по уравнению
Кд = (aH aOH)/ah3O (1). Учитывая, что при комнатной температуре на ионы распадается лишь одна из примерно 108 молекул воды, активности ионов в уравнении бывают заменены их концентрациями , а концентрацию нераспавшихся молекул воды можно считать равной общей концентрации молекул воды. Концентрацию молекул можно рассчитать, разделив массу 1 л воды на массу её моля: 1000/18 = 55,5 моль/л. Считая эту величину постоянной, можно уравнение (1) записать в виде: [H+] [OH¯] = Кд 55,5 = Кв, где Кв – ионное произведение воды. При расчётах связанных с водными растворами электролитов, используют не концентрации, активности ионов: aH·aOH = Кв.
Водородным показателем, или pH, принято называть взятый с обратным знаком десятичный логарифм активности ионов водорода в растворе: pH = - lg aH. Водородный показатель определяет характер реакции раствора. При pH<7 реакция раствора кислая, при pH>7 – щелочная, при pH=7 – реакция нейтральная. Водородный показатель имеет важное значение для понимания большинства процессов, протекающих в жидкой фазе, так как ионы H+ и OH¯ непосредственно участвуют во многих из этих процессов. Вместе с тем, эти ионы являются гомогенными катализаторами многих реакций. Величина pH может служить критерием силы кислоты или основания. Водородный показатель играет важную роль в жизнедеятельности организма, так в норме pH сыворотки крови равен 7,40 ± 0,05, слёз – 7,4 ± 0,1. отклонение pH от нормальных значений приводит к расстройству деятельности организма. Существенно влияние на урожайность оказывает pH почвы, на экологию водоёма – pH воды.
Индикаторы (позднелат. indicator - указатель), химические вещества, изменяющие окраску, люминесценцию или образующие осадок при изменении концентрации какого-либо компонента в растворе. Указывают на определенное состояние системы или на момент достижения этого состояния.
Различают индикаторы обратимые и необратимые. Изменение окраски первых при изменении состояния системы должна быть повторено многократно. Необратимые индикаторы подвергаются необратимым химическим превращениям, к примеру, азосоединения при окислении ионами BrO3- разрушаются. Индикаторы. которые вводят в исследуемый раствор, называют внутренними, в отличие от внешних, реакцию с которыми проводят вне анализируемой смеси. В последнем случае одну или несколько капель анализируемого раствора помещают на бумажку, пропитанную индикатором, или смешивают их на белой фарфоровой пластинке с каплей индикатора.
Индикаторы применяют чаще всего для установления конца какой-либо химической реакции, главным образом конечной точки титрования (к. т. т.). В соответствии с титриметрическими методами различают кислотно-основные, адсорбционные, окислительно-восстановительные и комплексонометрические индикаторы.
Кислотно-основные индикаторы представляют из себярастворимые органические соединения, которые меняют свой цвет или люминесценцию исходя из концентрации ионов Н+ (рН среды).
Адсорбционные индикаторы - вещества, способные адсорбироваться на поверхности осадка и менять при этом окраску или интенсивность люминесценции. Эти индикаторы, как правило, обратимы и используются в осадительном титровании
Окислительно-восстановительные индикаторы - вещества, способные изменять окраску исходя из окислительно-восстановительного потенциала раствора.
Комплексонометрические индикаторы - вещества, образующие с ионами металлов (М) окрашенные комплексы, по цвету отличающиеся от самих индикаторов.
Иногда в качестве комплексонометрических индикаторов применяют комплексонат какого-либо иона (к примеру, [CuY]2-, где Y - анион этилендиаминтетрауксусной кислоты) в смеси с металлохромным индикаторы, к примеру ПАН. При введении определяемого иона М2+ происходит реакция: М2+ + [CuY]2- + ПАН D [MY]2- + [СuПАН]+. При титровании каким-либо комплексоном в к. т. т. окраска раствора меняется от фиолетовой к желто-оранжевой, ᴛ.ᴇ. очень контрастно. При комплексонометрическом определении Сu используют в качестве индикатора ее комплекс с ПАН, адсорбированный на поверхности осажденного AgI. В этом случае можно определять Ag и Сu при совместном присутствии: в кислой среде раствором KI оттитровывают сначала ионы Ag, а затем комплексоном - ионы Сu.
Применяются также так называемые неокрашенные комплексонометрические индикаторы, избирательно взаимодействующие с ионами определяемого металла с образованием слабо окрашенных (el 103) комплексов, к примеру,сульфосалициловая кислота при титровании Fe (III). Флуоресцентные комплексонометрические индикаторы(или металлофлуоресцентные индикаторы) взаимодействуют с катионами металлов с образованием интенсивно флуоресцирующих хелатов.
21. Типы химических реакций, их характеристика
referatwork.ru
Что такое электролит? | Автоблог
Вопрос от читателя:
«Здравствуйте. У меня стала плохо заводиться машина. После поездки на станцию мне сказали: — нужно долить электролит в аккумулятор и проехать 100 км, для зарядки аккумулятора. Но не объяснили что такое электролит и зачем он нужен в аккумуляторе? Если не сложно расскажите, как вы можете, для таких как я!  Заранее спасибо вам, Александра»
Заранее спасибо вам, Александра»
Ваш вопрос понятен, как обычно ничего сложного, читайте дальше …


Большая часть аккумуляторных батарей свинцово-кислотные, конечно сейчас начинают появляться гелевые аккумуляторы для автомобилей (они мощнее, долговечнее и с ними меньше возни), однако они очень дорогие. Поэтому практически все производители, сейчас устанавливают на свои автомобили именно свинцово-кислотные, как ни крути они дешевле в разы. Есть обслуживаемые и необслуживаемые аккумуляторы. Если с необслуживаемыми вы практически не будете возиться, то вот с обслуживаемыми вариантами всегда нужно быть внимательными! Касается это жидкости внутри аккумулятора (она всегда должна быть в норме) именно эта жидкость и называется – электролит.
Автомобильный аккумуляторный электролит – токопроводящая жидкость, состоит из серной кислоты и воды. Второе название «кислотный электролит». Для автомобильных аккумуляторов готовят из серной кислоты плотностью 1,4.
Принцип работы
Электролиты (которые выражены в расплавах и растворах), распадаются на ионы, или как можно сказать по научному – «диссоциируют», и поэтому проводят электрический ток. К электролитам в различных сферах можно отнести кислоты, соли и т.д. составы, те у которых имеются сильные полярные и ионные связи. Чем выше ионная связь, тем легче проводится ток и идет процесс «диссоциации».
Немного сложно, но на примере все просто. Даже обычная вода (не дистиллированная) является своеобразным электролитом (правда плохим, но все же), также все живые клетки также имеют составы электролитов, у людей это кровь, которая обеспечивает электропроводность для нервных импульсов, которые позволяют нам с вами двигаться и ощущать.
В автомобильном аккумуляторе без этой жидкости не было бы тока. Обычные свинцовые решетки на это не способны. Именно электролит создает нужный токопроводящий раствор.
Приготовление
Как я писал выше — делают из раствора воды и серной кислоты. Причем вода берется дистиллированная. Емкость для смешивания должна быть либо керамическая, либо фаянсовая или эбонитовая. Стекло брать опасно, потому как при смешивании двух растворов выделяется высокая температура и стекло может треснуть. Однако остывший состав хранить в стекле уже можно.
Чтобы получить состав плотностью 1,4 нужно взять серную кислоту плотностью 1,83 и вливать ее в воду. Из расчета 0.65 литра серной кислоты на 1 литр дистиллированной воды. Обязательно нужно помнить что заливать нужно серную кислоту в воду, потому как если сделать все наоборот – залить воду в кислоту, можно получить «бурлящую» жидкость которая разбрызгается в разные стороны.
Понятно, что вы не будете сами готовить электролит, его можно купить практически во всех автомобильных магазинах. И при надобности добавить в аккумулятор.
Хочу дать вам совет. Не всегда нужно покупать электролит (состав серной кислоты и воды), иногда достаточно добавить в аккумулятор дистиллированную воду.
Все дело в том, что при элетрохимической реакции (электролизе) теряется именно вода, то есть ее уровень в смеси становится ниже, а уровень кислоты остается на прежнем месте. Поэтому добавляем только воду, и 80% случаев будет все хорошо. Однако есть остальные 20 % случаев когда нужно менять – добавлять сам электролит, например из-за низкого показателя плотности.
Вот и все на сегодня, надеюсь я вам помог.
avto-blogger.ru
Секреты водно-солевого баланса или зачем нужны электролиты при похудении?
 Довольно часто на программах похудения мы сталкиваемся с такой ситуацией – несмотря на обильное питье и активные тренировки, организм остается обезвоженным. Процент жидкости в организме остается низким и не позволяет сдвинуться жирам. Причина кроется в нарушении водно-солевого баланса, так как степень перемещения и направление движения воды зависит от концентрации электролитов.
Довольно часто на программах похудения мы сталкиваемся с такой ситуацией – несмотря на обильное питье и активные тренировки, организм остается обезвоженным. Процент жидкости в организме остается низким и не позволяет сдвинуться жирам. Причина кроется в нарушении водно-солевого баланса, так как степень перемещения и направление движения воды зависит от концентрации электролитов.
Водно-солевой баланс – это совокупность процессов всасывания, распределения и выделения воды в организме, которые тесно связаны с концентрацией солей в жидкостях организма. Для организма крайне важно поддерживать постоянные концентрации ионного состава и кислотно-щелочного равновесия внутренней среды.
Постоянство ионного состава жидкостей организма поддерживается с одной стороны количеством воды с другой стороны количеством растворенных в ней ионов основных электролитов.
Электролиты — это вещества, которые в жидкостях организма образуют заряженные частицы и обеспечивают регуляцию баланса жидкости во внутренней среде организма.
Электролиты отвечают:
- за скорость метаболизма,
- за движением жидкости от капилляров к клеткам и обратно,
- за появление электрического потенциала на мембранах клетки, без которого не возможно ОБРАЗОВАНИЕ ЭНЕРГИИ!
- определяют рН жидкостей тела, а именно защелачивают, что способствует оптимальному здоровью!
- препятствуют разрушению костной ткани (т.к. организм теряет кальций на нейтрализацию кислой среды, а с достаточным уровнем электролитов этого НЕ ПРОИСХОДИТ),
- за процессы свертывания крови,
- поддержания иммунитета.
Электролиты также непосредственно влияют на аппетит, уровень сахара в крови, функции гормонов надпочечников и щитовидной желез, а также использование жира в качестве источника энергии.
 К основным электролитам относятся натрий, калий, магний, кальций и хлор.
К основным электролитам относятся натрий, калий, магний, кальций и хлор.
Натрий – основной катион внеклеточной жидкости (96%). Движение натрия внутрь клетки и обратно инициирует генерацию электрических импульсов, которые играют существенную роль в жизненных функциях организма. Электрические нервные импульсы обеспечивают работу всей нервной системы, поддерживают память, влияют на состояние мышечной, сердечно-сосудистой систем. Ионы натрия и хлора играют важную роль в секреции соляной кислоты в желудке. Его задача сохранять водный баланс.
Задержка жидкости, т.е. отёки и УВЕЛИЧЕНИЕ ВЕСА появляются когда натрия очень много! Когда баланс натрия в норме, лишняя жидкость легко выводится из организма, выводя с собой токсины, а вес, если он был избыточен, снижается!
Калий - основной катион внутриклеточной жидкости, 98% калия находится внутри клетки. Главная задача калия – формирование вместе с натрием разницы потенциалов на мембранах клеток, генерация нервного импульса и передача его на нервные и мышечные клетки.
Калий:
- поддерживает осмотическое давление в клетках, тканях и жидкостях,
- обеспечивает кислотно-щелочное равновесие,
- нормализует сердечный ритм,
- выводит лишнюю воду,
- способствует снабжению мозга кислородом,
- поддерживает энергетический уровень организма,
- повышает выносливость.
Калий помогает при похудении — он работает в процессах по увеличению мышечной массы и стимулирует мышцы к активной работе, что в свою очередь увеличивает общее потребление калорий организмом для своих нужд — УСКОРЯЕТСЯ МЕТАБОЛИЗМ!
Во время тренировок калий выводится из организма вместе с потом, поэтому потребление калиевых продуктов крайне важно!
Магний:
- входит в состав структуры 300 ферментов, основных участников метаболизма в организме
- оказывает антистрессовое действие на нервную систему,
- отвечает за процессы торможения нервной системы, регуляцию сердечного ритма,
- препятствует возникновению спазмов и судорог,
- необходим для формирования костей, превращения глюкозы в клеточную энергию.
Хлор:
- участвует в обмене веществ, в секреции желудочного сока,
- вместе с калием и натрием регулирует водно-электролитный баланс,
- нормализует осмотическое давление,
- активирует целый ряд ферментов
- поддерживает кислотно-щелочное равновесие.
Когда водно-электролитный баланс в норме, лишняя жидкость легко выводится из организма, способствует выведению токсинов и снижению веса.
Основные электролиты организм получает из еды. При нарушении электролитного баланса организм может страдать или от обезвоживания или от отёков. Обезвоживание может быть результатом потери электролитов с потом во время активных тренировок, при обильном питье деминерализованной воды, которая будет выводить электролиты с мочой, а также при приеме мочегонных препаратов. При потере электролитов вода не может активно перемещаться из внутриклеточного пространства в кровь. В это время наступает усталость, ощущение полной потери сил.
Именно с такими ситуациями сталкиваются люди, которые находятся на программах похудения. Особенно в зимнее время, когда сокращается потребляемых овощей (основной источник электролитов). К тому же в рационе питания во время похудения крайне мало или вовсе нет картофеля и бананов, а это основной источник калия.
Известно, что при интенсивных тренировках (более 45 минут) спортсменам рекомендуется употреблять не чистую воду, а специальные спортивные напитки. Они обогащены основными электролитами и углеводами с высоким гликемическим индексом. Такие напитки компенсируют потерю электролитов и предотвращают обезвоживание и задержку воды в клетках.
Однако, на программах похудения такие напитки могут стать дополнительным источником углеводов с высоким гликемическим индексом.
Альтернативой служит продукт «Электролайтс» компании Витамакс
 Электролайтс содержит хлориды натрия, калия и магния, обогащен сульфатом цинка и лимонной кислотой.
Электролайтс содержит хлориды натрия, калия и магния, обогащен сульфатом цинка и лимонной кислотой.
Цинк – очень важный микроэлемент, который поддерживает иммунную систему, мыслительные функции и входит в состав порядка 200 энзимов.
Лимонная кислота – важнейший элемент энергетического цикла клетки, так называемого цикла Кребса, в результате которого клетка получает энергию. Этот цикл часто называют циклом лимонной кислоты.
Электролайтс не содержит калорий, сахара и других углеводов, искусственных ингредиентов и красителей, имеет приятный лимонный вкус и хорошо растворяется в воде.
Электролайтс необходим:
- Во время пробежек, тренировок и длительных прогулок;
- Для поддержания нормального водного баланса и гидратации клеток после физических упражнений;
- Для восстановления электролитного баланса;
- Для повышения выносливости и работоспособности.
Электролайтс обеспечивает оптимальное количество каждого электролита для максимальной гидратации и эффективной жизнедеятельности организма. Поможет мозгу и нервной системе генерировать и передавать важные сигналы. Повысит энергетику организма.
Пить Электролайтс значит быстро возвращать жидкость и электролиты, которые теряются при нагрузках, помогать восстановлению мышц, предотвращать обезвоживание, а также повышать выносливость в ходе физических нагрузок.
Способ применения: одна чайная ложка на стакан воды 1 – 2 раза в день. ОБЯЗАТЕЛЬНО в тренировочный день!
Ваш велнес-консультант Сирануш Назинян
www.wellneschool.com
Электролиты
Проводниками электрического тока являются не только металлы и полупроводники. Электрический ток проводят растворы многих веществ в воде. Чистая вода не проводит электрический ток, то есть, в ней нет свободных носителей электрических зарядов. Не проводят электрический ток и кристаллы поваренной соли (хлорида натрия). Но если растворить соль в воде, раствор будет хорошим проводником электрического тока. Растворы солей, кислот и оснований, которые способны проводить электрический ток называются электролитами.
 Прохождение электрического тока через электролиты обязательно сопровождается выделением вещества в твёрдом или газообразном состоянии на поверхности электродов. Выделение вещества на электродах показывает, что в электролитах электрические заряды переносят заряженные атомы вещества – ионы.
Прохождение электрического тока через электролиты обязательно сопровождается выделением вещества в твёрдом или газообразном состоянии на поверхности электродов. Выделение вещества на электродах показывает, что в электролитах электрические заряды переносят заряженные атомы вещества – ионы.
По степени диссоциации (способности распадаться на ионы) электролиты можно разделить на сильные и слабые. Степень диссоциации сильных электролитов в растворах равна единице: они полностью диссоциируют, не зависимо от концентрации раствора (щёлочи, соли, некоторые кислоты). Степень диссоциации слабых электролитов в растворах меньше единицы: они диссоциируют не полностью. И с ростом концентрации раствора степень диссоциации уменьшается (вода, ряд кислот и оснований).
Четкой границы между этими двумя группами нет: одно и то же вещество может в одном растворителе проявлять свойства сильного электролита, а в другом – слабого.
Закон электролиза. Электрохимический эквивалент вещества
Электролизом называют физико-химический процесс, протекающий на электродах, погруженных в электролит, под действием электрического тока: на электродах выделяются составные части растворённых веществ или других веществ, которые являются результатом вторичных реакций.
В проводящих жидкостях упорядоченное движение ионов происходит в электрическом поле, созданном электродами – проводниками, которые соединены с полюсами источника электрической энергии. При электролизе положительный электрод называется анодом, а отрицательный – катодом. Отрицательные ионы – анионы – движутся к аноду, положительные ионы – катионы – к катоду. На аноде отрицательные ионы отдают лишние электроны (окислительная реакция). На катоде положительные ионы получают недостающие электроны (восстановительная реакция).
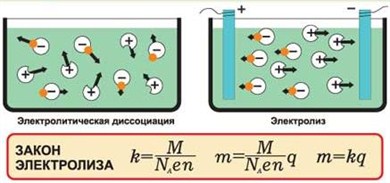
М. Фарадей на основе экспериментов с различными электролитами установил, что при электролизе масса m выделившегося вещества пропорциональна прошедшему через электролит заряду ∆q или силе тока I и времени ∆t прохождения тока:
m = k∆q = kI∆t
Данное уравнение называется законом электролиза, коэффициент k, зависящий от выделяющегося вещества, называется электрохимическим эквивалентом вещества.
Проводимость жидких электролитов объясняется тем, что при растворении в воде нейтральные молекулы солей, кислот и оснований распадаются на отрицательные и положительные ионы. В электрическом поле ионы приходят в движение и создают электрический ток.
Существуют не только жидкие, но и твёрдые электролиты. Примером твёрдого электролита может служить стекло. В составе стекла имеются положительные и отрицательные ионы. В твёрдом состоянии стекло не проводит электрический ток, так как ионы не могут двигаться в твёрдом теле. При нагревании стекла ионы получают возможность перемещаться под действием электрического поля и стекло становится проводником.
Явление электролиза применяется на практике для получения многих металлов из раствора солей. С помощью электролиза для защиты от окисления или для украшения производится покрытие различных предметов и деталей машин тонкими слоями таких металлов, как хром, никель, серебро, золото.
Остались вопросы? Не знаете, что такое электролиты?Чтобы получить помощь репетитора – зарегистрируйтесь.Первый урок – бесплатно!
Зарегистрироваться
© blog.tutoronline.ru, при полном или частичном копировании материала ссылка на первоисточник обязательна.
blog.tutoronline.ru
Что доливать в аккумулятор: воду или электролит?

Электролит представляет собой жидкость состоящую из серной кислоты и дистиллированной воды. В некоторых ситуациях уровень электролита в аккумуляторе падает и требуется его нормализовать. В зависимости от причин снижения уровня в батарею доливают либо электролит, либо дистиллированную воду. Как же узнать, что именно залить в АКБ?
В аккумулятор доливают электролит, если падение его уровня вызвано повреждением корпуса, либо вытеканием при наклоне. В аккумулятор доливают дистиллированную воду в тех случаях, когда произошло ее выкипание (испарение), т.к. выкипает именно вода, а не серная кислота.
Как доливать дистиллированную воду
Для доливки воды требуется именно дистиллированная вода. Сырая вода из под крана, либо кипяченная не подходит, т.к. содержит в себе примеси, которые негативно сказываются на протекании химических процессов и даже способны ухудшить состояние батареи, т.к. примеси оседают на элементах батареи. Кипячение не удаляет из воды жесткие примеси, соли и металлы, кипячением можно только убить бактерии и микробов в воде.
Марка дистиллированной воды, которую будете заливать, значения не имеет. У батареи выкручиваются пробки и аккуратно доливается вода до уровня, который нанесен на моноблоке. Если моноблок не прозрачный, то доливают столько воды, чтобы скрыть электроды полностью, а запас воды сверху составлял не менее 1 см.
После процедуры доливки воды, батарею рекомендуется зарядить на зарядном устройстве. Полностью заряженная батарея будет иметь плотность 1,26-1,28. Если плотность значительно отличается, то что-то пошло не так и вам лучше обратиться к специалистам.
Как доливать воду в необслуживаемый аккумулятор без доступа к банкам
На практике без доступа в банки делают необслуживаемые аккумуляторы по кальциевой технологии, т.е. которые не требуют доливки жидкости на протяжении всего срока службы. Но случается, что при перезаряде выкипание все же происходит. Если доступа в аккумулятор нет, а долить жидкость нужно, то придется помучатся. Рекомендуется высверлить в крышке АКБ небольшие отверстия 2-4 мм. и в них шприцом аккуратно долить дистиллированную воду.
Что будет, если вместо воды долить электролит
Если в батарею требуется долить дистиллированную воду, а вы дольете электролит, то после зарядки батареи его плотность превысит 1,30 и содержание серной кислоты станет запредельным. Это приведет к ускоренной сульфатации пластин батареи и выходу его из строя. Аккумуляторы с повышенной плотностью существуют и используются на крайнем севере, чтобы в батареи не образовывался лед, но при этом сам аккумулятор в таком состоянии способен отработать не более 1 года.
Как доливать электролит в аккумулятор
Перед тем, как электролит в аккумулятор заливать, его требуется сначала приготовить. В батарею можно доливать только электролит плотностью 1,26-1,29. Корректирующий электролит плотностью 1,40 можно доливать лишь в том случае, когда залили дистиллированной воды больше, чем этого требовалось и плотность даже после зарядки не поднялась для рекомендованного значения. В продаже можно найти готовый электролит, который можно сразу доливать в банки батареи. Корректирующий электролит придется разбавлять дистиллированной водой. Здесь нужно быть предельно внимательный и соблюдать строгие правила техники безопасности. Есть один серьезный нюанс – электролит (серная кислота) тяжелее воды, поэтому воду доливают в электролит, а не наоборот. В противном случае процесс разбавления будет сопровождаться брызгами, которые могут попасть на оголенные участки кожи.
Замена электролита в аккумуляторе
Замена электролита в аккумуляторе – процедура не только бесполезная, но и наоборот вредная. Срок службы аккумулятора подходит к концу в основном из-за оплывания активной массы – она с пластин осыпается на дно аккумулятора в виде шлама. От этого электролит темнеет, а аккумулятор теряет емкость. Темные электролит - это следствие оплывания активной массы, а не причина выхода его из строя. Смена электролита не вернет аккумулятору емкость, но при этом способна убить батарею.
Дело в том, что шлам скапливается на дне моноблока, а при опрокидывании его для сливания электролита шлам перемещается на внутреннюю часть крышки батареи и в следствии попадает на оголенные элементы электродов, которые сверху не защищены сепараторами-изоляторами. В итоге происходит замыкание в одной или нескольких банках аккумулятора.
Электролит представляет собой жидкость состоящую из серной кислоты и дистиллированной воды. В некоторых ситуациях уровень электролита в аккумуляторе падает и требуется его нормализовать.
Емкость автомобильного аккумулятора – это способность батареи хранить определенное количество энергии. За емкость аккумулятора отвечает количество активной массы на электродах аккумуляторной батареи. Емкость аккумулятора определяется количество активной м
Напряжение аккумулятора – это физическая величина электрической цепи, которая определяется потенциалов между положительным выводом и отрицательным. Напряжение в теории физики тесно связано с ЭДС и многие автомобилисты путают их, поэтому для начала нужно
Сегодня современный автомобиль - это не просто кусок металла с колесами. Современные автомобили буквально напичканы электроникой, о которой еще 10 лет назад могли только мечтать инженеры.
akb-sales.ru





















