Что такое диэлектрики и где они используются. Вода диэлектрик
Диэлектрики в науке и в быту
Диэлектрики - это вещества, которые не проводят электрический ток, до определенной поры. При определенных условиях проводимость в них зарождается. Этими условиями выступают механические, тепловые - в общем, энергетические виды воздействий. Кроме диэлектриков, вещества также классифицируются на проводники и полупроводники.
Теоретическую разницу между этими тремя видами материалов можно представить, и я это сделаю, на рисунке ниже:
Рисунок красивый, знакомый со школьной скамьи, но что-то практическое из него не особо вытянешь. Однако, в этом графическом шедевре четко определена разница между проводником, полупроводником и диэлектриком.
И отличие это в величине энергетического барьера между валентной зоной и зоной проводимости.
В проводниках электроны находятся в валентной зоне, но не все, так как валентная зона - это самая внешняя граница. Точно, это как с мигрантами. Зона проводимости пуста, но рада гостям, так как у неё полно для них свободных рабочих мест в виде свободных энергетических зон. При воздействии внешнего электрического поля, крайние электроны приобретают энергию и перемещаются в свободные уровни зоны проводимости. Это движение мы еще называем электрическим током.
В диэлектриках и проводниках всё аналогично, за исключением того, что имеется “забор” - запрещенная зона. Эта зона расположена между валентной и зоной проводимости. Чем больше эта зона, тем больше энергии требуется для преодоления электронами этого расстояния. У диэлектриков величина зоны больше, чем у полупроводников. Этому есть даже условие: если дЭ>3Эв (электронвольт) - то это диэлектрик, в обратном случае дЭ
В данной статье речь далее пойдет только о диэлектриках. И раз уж мы чуть углубились в науку, то поговорим далее о свойствах и величинах, которые характеризуют эти электротехнические материалы в общем.
Классификация диэлектриков довольна обширная. Тут встречаются жидкие, твердые и газообразные вещества. Далее они делятся по определенным признакам. Ниже приведена условная классификация диэлектриков с примерами в форме списка.
- - полярные
- - неполярные (воздух, элегаз)
- - полярные (вода, аммиак)
- - жидкие кристаллы
- - неполярные (бензол, трансформаторное масло)
- - центросимментричные
- - аморфные
- - смолы, битумы (эпоксидная смола)
- - стекла
- - неупорядоченные полимеры
- - поликристаллы
- - нерегулярные кристаллы
- - керамика
- - упорядоченные полимеры
- - ситаллы
- - монокристаллы
- - молекулярные
- - ковалентные
- - ионные
- - параэлектрики смещения
- - параэлектрики „порядок-беспорядок”
- - дипольные
- - нецентросимментричные
- - монокристаллы
- - пироэлектрики
- - сегнетоэлектрики смещения
- - сегнетоэлектрики „порядок-беспорядок”
- - линейные пироэлектрики
- - пьезоэлектрики
- - с водородными связями
- - ковалентные
- - ионные
- - текстуры
- - электронных дефектов
- - ионных дефектов
- - полярных молекул
- - макродиполей
- - сегнетоэлектрических доменов
- - кристаллов в матрице
Если брать жидкие и газообразные диэлектрики, то основная классификация лежит в вопросе полярности. Разница в симметричности молекул. В полярных молекулы несимметричны, в неполярных - симметричны. Несимметричные молекулы называются диполями. В полярных жидкостях проводимость настолько велика, что их невозможно использовать в качестве изоляционных веществ. Поэтому для этих целей используют неполярные, тоже трансформаторное масло. А наличие полярных примесей даже в сотых долях значительно снижает планку пробоя и негативно сказывается на изоляционных свойствах неполярных диэлектриков.
кристаллы представляют собой нечто среднее между жидкостью и кристаллом, как следует из названия.
Еще популярным вопросом о свойствах и применении жидких диэлектриков будет следующий: вода - диэлектрик или проводник? В чистой дистиллированной воде отсутствуют примеси, которые могли бы вызвать протекание тока. Чистую воду можно создать в лабораторных, промышленных условиях. Эти условия сложны и трудновыполнимы для обычного человека. Есть простой способ проверить проводит ли дистиллированная вода ток.

Создать электрическую цепь (источник тока - провод - вода - провод - лампочка - другой провод - источник тока), в которой одним из участков для протекания тока будет сосуд с дистиллированной водой. При включении схемы в работу, лампочка не загорится - следовательно ток не проходит. Ну а если загорится, значит вода с примесями.
Поэтому любая вода, которую мы встречаем: из крана, в озере, в ванной - будет проводником за счет примесей, которые создают возможность для протекания тока. Не купайтесь в грозу, не работайте влажными руками с электричеством. Хотя чистая дистиллированная вода - полярный диэлектрик.
Для твердых диэлектриков классификация в основном лежит в вопросе активности и пассивности что ли. Если свойства постоянны, то диэлектрик используют в качестве изоляционного материала, то есть он пассивен. Если свойства меняются, в зависимости от внешних воздействий (тепло, давление), то этот диэлектрик применяют для других целей. Бумага является диэлектриком, если вода пропитана водой - то ток проводится и она проводник, если бумага пропитана трансформаторным маслом - то это диэлектрик.
Фольгой называют тонкую металлическую пластину, металл - как известно является проводником. В продаже имеется например ПВХ-фольга, тут слово фольга для наглядности, а слово ПВХ - для понимания смысла - ведь ПВХ это диэлектрик. Хотя в википедии - фольгой называется тонкий лист металла.
Аморфные жидкости - это и смола, и стекло, и битум, и воск. При повышении температуры этот диэлектрик тает, это замороженные вещества - это дикие определения, которые характеризуют лишь одну грань правды.
Поликристаллы - это, как бы сросшиеся кристаллы, объединенные в один кристалл. Например, соль.
Монокристалл - это цельный кристалл, в отличие от вышеупомянутого поликристалла имеющий непрерывную кристаллическую решетку.
Пьезоэлектрики - диэлектрики, у которых при механическом воздействии (растяжении-сжатии), возникает процесс ионизации. Применяется в зажигалках, детонаторах, УЗИ-обследовании.
Пироэлектрики - при изменении температуры в этих диэлектриках происходит самопроизвольная поляризация. Также она происходит при механическом воздействии, то есть пироэлектрики являются еще и пьезоэлектриками, но не наоборот. Примерами служат янтарь и турмалин.
Физические свойства диэлектриков
Чтобы оценить качество и степень пригодности диэлектрика, необходимо как-то описать его параметры. Если следить за этими параметрами, то можно вовремя предотвратить аварию, заменив элемент на новый с допустимыми параметрами. Этими параметрами выступают: поляризация, электропроводность, электрическая прочность и диэлектрические потери. Для каждого из этих параметров существует своя формула и постоянная величина, в сравнении с которой производится заключение о степени пригодности материала.
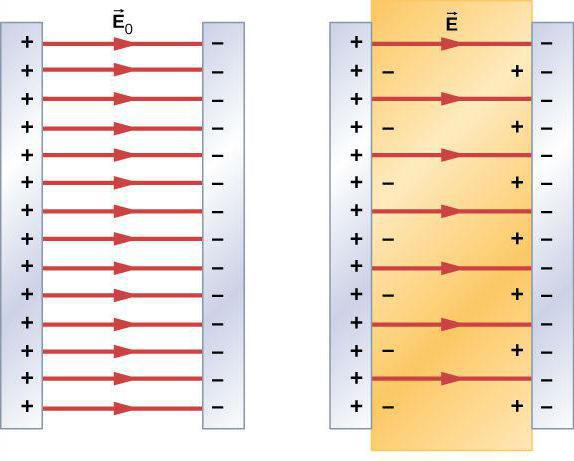
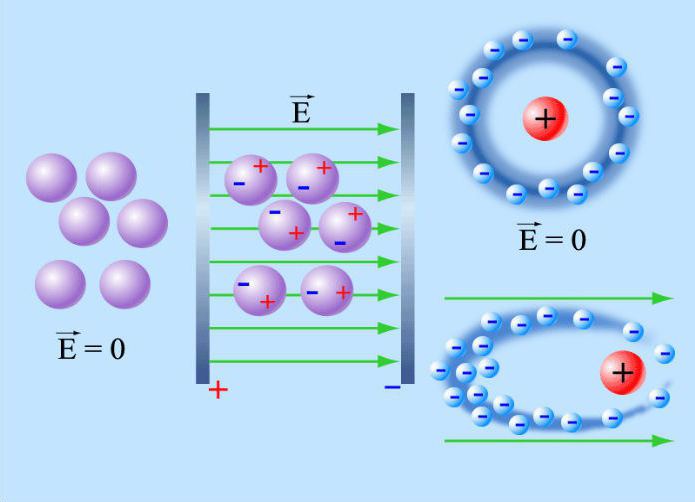
Главными электрическими свойствами диэлектриков являются поляризация (смещение зарядов) и электропроводность (способность проводить электрический ток) Смещение связанных зарядов диэлектрика или их ориентация в электрическом поле называется поляризацией. Это свойство диэлектрических материалов характеризуется относительной диэлектрической проницаемостью ε. При поляризации на поверхности диэлектрика образуются связанные электрические заряды.
В зависимости от типа диэлектрика поляризация может быть: электронной, ионной, дипольно-релаксационной, спонтанной. Более подробно про их свойства на инфографике ниже.

Под электропроводностью понимают способность диэлектрика проводить электрический ток. Ток, протекающий в диэлектрике называется током утечки. Ток утечки состоит из двух составляющих - тока абсорбционного и тока сквозного. Сквозные токи обусловлены наличием свободных зарядов в диэлектрике, абсорбционный ток - поляризационными процессами до момента установления равновесия в системе.
Величина электропроводности зависит от температуры, влажности и количества свободных носителей заряда.
При увеличении температуры электропроводность диэлектриков увеличивается, а сопротивление падает.
Зависимость от влажности вновь возвращает нас к классификации диэлектриков. Ведь, неполярные диэлектрики не смачиваются водой и на изменение влажности им нет дела. А у полярных диэлектриков при увеличении влажности повышается содержание ионов, и электропроводность увеличивается.
Проводимость диэлектрика состоит из поверхностной и объемной проводимостей. Известно понятие удельной объемной проводимости, обозначается буквой сигма σ. А обратная величина называется удельное объемной сопротивление и обозначается буквой ро ρ.
Резкое увеличение проводимости в диэлектрике при возрастании напряжения может привести к электрическому пробою. И аналогично, если сопротивление изоляции падает, значит изоляция не справляется со своей задачей и необходимо применять меры. Сопротивление изоляции состоит из поверхностного и объемного сопротивлений.
Под диэлектрическими потерями в диэлектриках понимают потери тока внутри диэлектрика, которые рассеиваются в виде тепла. Для определения этой величины вводят параметр тангенс дельта tgδ. δ - угол, дополняющий до 90 градусов, угол между током и напряжением в цепи с емкостью.
Диэлектрические потери бывают: резонансные, ионизационные, на электропроводность, релаксационные. Теперь подробнее поговорим про каждый тип.

Электрическая прочность это отношение пробивного напряжения к расстоянию между электродами (или толщина диэлектрика). Эта величина определяется минимальной величиной напряженности электрического поля, при которой произойдет пробой.
Пробой может быть электрическим (ударная ионизация, фотоионизация), тепловым (большие диэлектрические потери, следовательно много тепла, и обугливание с оплавлением может произойти) и электрохимическим (в результате образования подвижных ионов).
И в конце таблица диэлектриков, как же без нее.
В таблице выше приведены данные по электрической прочности, удельному объемному сопротивлению и относительной диэлектрической проницаемостью для различных веществ. Также тангенс угла диэлектрических потерь не обошли стороной.
pomegerim.ru
Диэлектрик - что такое? Свойства диэлектриков
Диэлектрик - это материал или вещество, которое практически не пропускает электрический ток. Такая проводимость получается вследствие небольшого количества электронов и ионов. Данные частицы образуются в не проводящем электрический ток материале только при достижении высоких температурных свойств. О том, что такое диэлектрик и пойдёт речь в этой статье.
Описание
Каждый электронный или радиотехнический проводник, полупроводник или заряженный диэлектрик пропускает через себя электрический ток, но особенность диэлектрика в том, что в нем даже при высоком напряжении свыше 550 В будет протекать ток малой величины. Электрический ток в диэлектрике - это движение заряженных частиц в определённом направлении (может быть положительным и отрицательным).

Виды токов
В основе электропроводимости диэлектриков лежат:
- Токи абсорбционные – ток, который протекает в диэлектрике при постоянном токе до тех пор, пока не достигнет состояния равновесия, изменяя направление при включении и подаче на него напряжения и при отключении. При переменном токе напряжённость в диэлектрике будет присутствовать в нём всё время, пока находится в действии электрического поля.
- Электронная электропроводность – перемещение электронов под действием поля.
- Ионная электропроводность – представляет собой движение ионов. Находится в растворах электролитов – соли, кислоты, щёлочь, а так же во многих диэлектриках.
- Молионная электропроводность – движение заряженных частиц, называемых молионами. Находится в коллоидных системах, эмульсиях и суспензиях. Явление движения молионов в электрическом поле называется электрофорезом.
Электроизоляционные материалы классифицируют по агрегатному состоянию и химической природе. Первые делятся на твёрдые, жидкостные, газообразные и затвердевающие. По химической природе делятся на органику, неорганику и элементоорганические материалы.
Электропроводимость диэлектриков по агрегатному состоянию:
- Электропроводимость газов. У газообразных веществ достаточно малая проводимость тока. Он может возникать при наличии свободных заряженных частиц, что появляется из-за воздействия внешних и внутренних, электронных и ионных факторов: излучение рентгена и радиоактивного вида, соударение молекул и заряженных частиц, тепловые факторы.
- Электропроводимость жидкого диэлектрика. Факторы зависимости: структура молекулы, температура, примеси, присутствие крупных зарядов электронов и ионов. Электропроводимость жидких диэлектриков во многом зависит от наличия влаги и примесей. Проводимость электричества полярных веществ создаётся ещё при помощи жидкости с диссоциированными ионами. При сравнении полярных и неполярных жидкостей, явное преимущество в проводимости имеют первые. Если очистить жидкость от примесей, то это поспособствует уменьшению её проводимых свойств. При росте проводимости жидкого вещества и его температуры возникает уменьшение её вязкости, приводящее к увеличению подвижности ионов.
- Твёрдые диэлектрики. Их электропроводимость обуславливается как перемещение заряженных частиц диэлектрика и примесей. В сильных полях электрического тока выявляется электропроводимость.
Физические свойства диэлектриков
При удельном сопротивлении материала равном меньше 10-5 Ом*м их можно отнести к проводникам. Если больше 108 Ом*м — к диэлектрикам. Возможны случаи, когда удельное сопротивление будет в разы больше сопротивления проводника. В интервале 10-5-108 Ом*м находится полупроводник. Металлический материал — отличный проводник электрического тока.

Из всей таблицы Менделеева только 25 элементов относятся к неметаллам, причём 12 из них, возможно, будут со свойствами полупроводника. Но, разумеется, кроме веществ таблицы, существует ещё множество сплавов, композиций или химических соединений со свойством проводника, полупроводника или диэлектрика. Исходя из этого, трудно провести определённую грань значений различных веществ с их сопротивлениями. Для примера, при пониженном температурном факторе полупроводник станет вести себя подобно диэлектрику.
Применение
Использование не проводящих электрический ток материалов очень обширно, ведь это один из популярно используемых классов электротехнических компонентов. Стало достаточно ясно, что их можно применять благодаря свойствам в активном и пассивном виде.

В пассивном виде свойства диэлектриков используют для применения в электроизоляционном материале.
В активном виде они используются в сегнетоэлектрике, а также в материалах для излучателей лазерной техники.
Основные диэлектрики
К часто встречающимся видам относятся:
- Стекло.
- Резина.
- Нефть.
- Асфальт.
- Фарфор.
- Кварц.
- Воздух.
- Алмаз.
- Чистая вода.
- Пластмасса.
Что такое диэлектрик жидкий?
Поляризация данного вида происходит в поле электрического тока. Жидкостные токонепроводящие вещества используются в технике для заливки или пропитки материалов. Есть 3 класса жидких диэлектриков:
Нефтяные масла – являются слабовязкими и в основном неполярными. Их часто используют в высоковольтных аппаратурах: масло трансформаторное, высоковольтные воды. Масло трансформаторное - это неполярный диэлектрик. Кабельное масло нашло применение в пропитке изоляционно-бумажных проводов с напряжением на них до 40 кВ, а также покрытий на основе металла с током больше 120 кВ. Масло трансформаторное по сравнению с конденсаторным имеет более чистую структуру. Данный вид диэлектрика получил широкое распространение в производстве, несмотря на большую себестоимость по сравнению с аналоговыми веществами и материалами.
Что такое диэлектрик синтетический? В настоящее время практически везде он запрещён из-за высокой токсичности, так как производится на основе хлорированного углерода. А жидкий диэлектрик, в основе которого кремний органический, является безопасным и экологически чистым. Данный вид не вызывает металлической ржавчины и имеет свойства малой гигроскопичности. Существует разжиженный диэлектрик, содержащий фторорганическое соединение, которое особо популярно из-за своей негорючести, термических свойств и окислительной стабильности.
И последний вид, это растительные масла. Они являются слабо полярными диэлектриками, к ним относятся льняное, касторовое, тунговое, конопляное. Касторовое масло является сильно нагреваемым и применяется в бумажных конденсаторах. Остальные масла - испаряемые. Выпаривание в них обуславливается не естественным испарением, а химической реакцией под названием полимеризация. Активно применяется в эмалях и красках.
Заключение
В статье было подробно рассмотрено, что такое диэлектрик. Были упомянуты различные виды и их свойства. Конечно, чтобы понять всю тонкость их характеристик, придётся более углубленно изучить раздел физики о них.
fb.ru
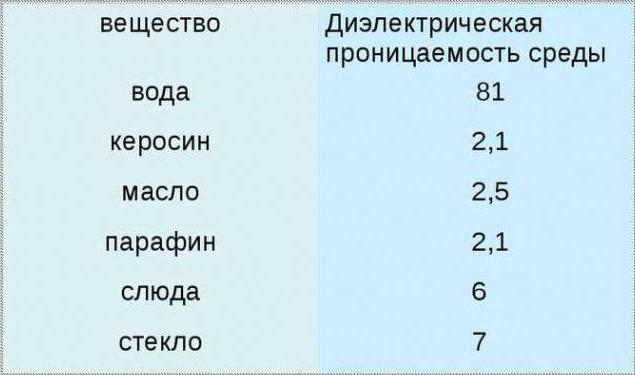
Вода диэлектрическая проницаемость - Справочник химика 21
Ионы в растворах образуются различными путями. Наиболее полно изучено образование ионов за счет электрической диссоциации. Согласно этой теории, молекулы электролита, как правило, полярного соединения, попадая в раствор, взаимодействуют с молекулами растворителя, в результате чего их внутренние связи ослабляются и молекула распадается на ионы — катионы и анионы. Это явление полного или частичного распада молекул на ионы носит название электролитической диссоциации. Большое влияние на степень диссоциации одного и того же электролита в различных растворах оказывает диэлектрическая проницаемость растворителя. В соответствии с законом Кулона, электростатические силы взаимодействия между ионами при одинаковом расстоянии между ними обратно пропорциональны диэлектрической проницаемости среды (для разбавленных растворов). Чем больше г среды, тем меньше сила взаимодействия между ионами, составляющими молекулу, и тем в большей степени ионы изолированы друг от друга и, следовательно, тем выше степень диссоциации электролита при заданных условиях. Например, вода, диэлектрическая проницаемость которой очень велика (е 80), по сравнению с другими веществами является наилуч- [c.5] Что касается ионизирующей способности растворителя, то два фактора заслуживают особого упоминания. Прежде всего ионизирующая способность возрастает при увеличении диэлектрической проницаемости, так как при этом становится более эффективным разделение ионов — силы, действующие между заряженными частицами находятся в обратной зависимости от диэлектрической проницаемости среды (стр. 155). По этой причине вода, диэлектрическая проницаемость которой равна 80, должна быть гораздо более эффективна, чем углеводород с диэлектрической проницаемостью 2. Сходным и возможно более важным фактором является способность растворителя сольватировать разделенные ионы. Катионы наиболее эффективно сольватируются соединениями элементов первого периода периодической системы, имеющими неподеленные пары электронов. Примерами могут служить аммиак, вода, спирты, карбоновые кислоты, сернистый ангидрид и диметилсульфоксид (СН 3)280. Анионы сольватируются наиболее эффективно растворителями, в которых атомы водорода соединены с сильно электроотрицательными элементами Y, так что связь Н — Y значительно поляризована. В случае таких растворителей водородные связи между растворителем и уходящей группой способствуют ионизации примерно таким же образом, каким ион серебра катализирует ионизацию алкилгалогенидов (стр. 272). [c.274]Связь между диэлектрической проницаемостью D растворителя и его способностью образовывать растворы, проводящие электрический ток, отмечалась давно. Вода, диэлектрическая проницаемость которой D — S при 18° С, а также H N (D = 107 при 25° С) и НСООН (1> = 57,0 при 25° С) принадлежат к растворителям, вызывающим сильную диссоциацию. Низшие спируксусная кислота, пиридин имеют диэлектрические проницаемости в пределах 20—35 и также способны образовывать электролиты, хотя и в меньшей степени, чем вода. [c.392]
Диспергированные в нефти глобулы воды, диэлектрическая проницаемость которой в 40 раз больше, чем нефти (около 80), стремятся расположиться вдоль силовых линий поля, образуя цепочки из капель воды. При этом несколько изменяется направление электрических силовых линий, вследствие чего электрическое поле становится неоднородным. [c.47]
По мере увеличения количества спирта в воде диэлектрическая проницаемость смеси понижается. Практически между диэлектрической проницаемостью смеси и содержанием спирта имеет место почти линейная зависимость, и шкала диэлектрической проницаемости пропорциональна шкале состава смеси спирта с водой. [c.278]
Относительные значения диэлектрической проницаемости также показывают, что степень ассоциации в жидкой перекиси водорода меньше, чем в воде. Несмотря на то, что перекись обладает большим дипольным моментом, чем вода, диэлектрическая проницаемость воды больше, чем перекиси водорода. Поскольку диэлектрическая проницаемость является функцией как числа диполей в единице объема, так и величины их, то трудно заранее рассчитать итоговое влияние одновременного изменения момента мономера, степени агрегации и специфической ориентации агрегатов. Гросс и Тейлор 11151 считают возможным, что больший момент перекиси водорода компенсируется снижением степени ассоциации, и приводят лежащие в основе такого вывода теоретические рассуждения [116], касающиеся взаимозависимости между водородными связями и диэлектрической проницаемостью перекиси водорода. [c.291]
Были сделаны попытки вычислить растворимость ионного соединения в различных растворителях, но они были малоуспешны. При выполнении таких расчетов следует иметь в виду, что в процессе растворения ионного соединения главную роль играет диэлектрическая проницаемость растворителя. В этом можно убедиться, рассмотрев растворение кристалла (рис. 10-3). Если удалять ион с поверхности кристалла на бесконечное расстояние в вакууме, то получится кривая потенциальной энергии, изображенная на рис. 10-4,а. Если же поместить кристалл в диэлектрик, то кривая потенциальной энергии при удалении иона в бесконечность будет иметь вид, изображенный на рис. 10,4,6. Отделение иона от кристалла в диэлектрике потребует значительно меньше энергии. Очевидно, чем больше диэлектрическая проницаемость растворителя, тем меньше работы надо затратить для разделения ионов. Гораздо легче разделить два иона в воде, диэлектрическая проницаемость которой равна 78,5 при 25°С, чем в этаноле с диэлектрической проницаемостью 24,2 при той же температуре. Это проявляется в уменьшении растворимости соли. [c.360]
Наиболее отрицательно на электроизоляционные свойства веществ влияет вода (диэлектрическая проницаемость е=82, мол. вес 18), что будет рассмотрено отдельно. [c.64]
Для эмульсии масло в воде диэлектрическая проницаемость меняется так [c.210]
При растворении КС1 в воде, диэлектрическая проницаемость которой D = 80, энергия разрыва ионной связи, подсчитанная по формуле (IV.33), становится равной 6,8-10 эрг, а эта величина — того же порядка, что и кинетическая энергия молекул воды при комнатной температуре. [c.122]
Причину понижения силы электролитов в амфотерных растворителях по сравнению с водой можно назвать уверенно более низкая, чем в воде, диэлектрическая проницаемость. Тяга к протону, т. е. степень основности, у большинства амфотерных растворителей выражена более отчетливо, чем у воды. Так, энергия сродства к протону у воды равна 707, а у метанола 753 кДж/моль . Но поскольку ДП метанола почти в 2,5 раза меньше, чем у воды, кислоты в нем существенно ослаблены по сравнению с водой. [c.62]
Исходя из общих принципов проявления вяжущих свойств [81], можно предположить, что насыщенный раствор кристаллогидрата может играть роль связки. При смачивании порошкообразного материала таким раствором часть растворителя (воды) будет адсорбирована на поверхности частичек, что приведет к пересыщению и далее к кристаллизации раствора. Способствовать кристаллизации будет пониженная растворяющая способность адсорбированной воды (диэлектрическая проницаемость пленочной воды 2—5). Учитывая высокие исходные значения Т/Ж (10/1), можно ожидать, что кристаллизация гидрата приведет к заметному упрочнению образцов. Однако, как показывает эксперимент, прочность таких образцов невысока и часто имеет тот же порядок, что и прочность образцов, отформованных на воде. Вместе с тем имеют место случаи, когда прочность образцов, отформованных на насыщенных растворах кристаллогидратов, в 2—3 раза больше прочности образцов, отформованных на воде. [c.109]
Сольволиза. Где такая рацемизация будет происходить более эффективно — в воде (диэлектрическая проницаемость 80) или уксусной кислоте (диэлектрическая проницаемость [c.294]
Применяя закон Кулона к случаю взаимодействия ионов, можно понять и объяснить то, что хорошими растворителями для кристаллов, построенных из ионов, являются только растворители с высокой диэлектрической проницаемостью. Среди них в первую очередь должна быть названа вода, диэлектрическая проницаемость которой намного выше, чем у большинства известных жидкостей. [c.112]
Сравнимость между собой величин реакционных способностей в воде (диэлектрическая проницаемость 1)=80) и этаноле (0=26) и сильное повышение реакционной способности в ацетоне ф = 20) и диметилформамиде (0 = 40) показывают, что в случае гидроксилсодержащих растворителей десольватация связана с отрывом молекул растворителя, сольватирующих особым образом [13] (причем энергии водородных связей в воде и этаноле сходны по величине), как предполагалось в первоначальных расчетах Поляни и сотрудников. Диэлектрическое влияние мало, поскольку оно учитывается в уравнении Борна в виде члена [1—(1//))]. По мере уменьшения диэлектрической проницаемости гораздо большее влияние на скорость реакции будет оказывать ассоциация ионов, чем диэлектрическая стабилизация переходного состояния [27]. [c.127]
Итак, химия растворов веществ в аммиаке весьма сходна с химией водных растворов. Главные отличия — повышенная основность аммиака и его более низкая, чем у воды, диэлектрическая проницаемость. Последняя не только снижает растворимость ионных кристаллов, но и способствует образованию ионных пар и ионных кластеров. Поэтому многие соединения, растворенные в аммиаке, оказываются в значительной степени ассоциированными. [c.225]
Ионизирующая способность растворителя, в котором растворен данный электролит. Она определяется его диэлектрической проницаемостью, т. е. величиной, показывающей, во сколько раз притяжение между двумя противоположно заряженными ионами в растворителе меньше, чем в пустоте. Чем больше диэлектрическая проницаемость растворителя, тем сильнее в нем диссоциирует электролит. Хорошим ионизирующим растворителем является вода, диэлектрическая, проницаемость которой при обыкновенной температуре очень высокая, равная 81. [c.12]
Выше были приведены результаты расчетов, сделанных в предположении, что взаимодействует только пара туннельных протонов. Если концентрация туннельных протонов увеличивается, то взаимодействует уже не только пара протонов, а все туннельные протоны. В этом случае, однако, среду вокруг протонов уже нельзя рассматривать как чистую воду. Диэлектрическая проницаемость резко возрастает, когда избыточные протоны удаляются от анионов [232], т. е. при увеличении числа избыточных туннельных протонов. Теперь между парами туннельных протонов находятся другие туннельные протоны, а не только вода. Диэлектрическая проницаемость такой среды значительно больше и в соответствии с выражениями (26), (27), (34) и (38) разд. V. 13. Б(1) взаимодействие между протонами существенно меньше. По всей вероятности, именно этим и обусловлен эффект насыщения интенсивности непрерывного поглощения и, следовательно, он связан с переходом от взаимодействия пары протонов к взаимодействию всех туннельных протонов. [c.298]
Чистая НаОа— сиропообразная жидкость бледно-голубого цвета, кипящая при 152,Г и замерзающая при —0,89°. По многим физическим свойствам она напоминает воду. Диэлектрическая проницаемость чистой жидкости при 25° равна 93, а ее 65%-ного раствора в воде 120.Таким образом, как чистая жидкость, так и ее водные растворы потенциально представляют собой превосходные ионизирующие растворители, однако их применение ограничено вследствие легкости разложения в присутствии даже следов многих ионов тяжелых металлов [c.212]
В процессе экспозиции в воде диэлектрическая проницаемость и тангенс угла диэлектрических потерь мате- [c.250]
Водостойкость (привес в воде), % Диэлектрическая проницаемость при 800 гц [c.456]
Учитывая общие соображения, трудно предполагать, что ионные соединения будут экстрагироваться органическими растворителями из водных растворов (из-за большой потери электростатической энергии сольватации, которая имела бы место). Это можно понять, пользуясь уравнением Борна [29], для расчета свободной энергии переноса голого иона с радиусом г и зарядом из воды (диэлектрическая проницаемость бц,) в органический растворитель (диэлектрическая проницаемость ) [c.18]
Будет ли отличаться электролитическая диссоциация Na l в спирте (диэлектрическая проницаемость спирта е = 24) по сравнению с диссоциацией в воде (диэлектрическая проницаемость воды е = 80) [c.75]
На процессах гидратации, конденсации и других существенно сказываются микросвойства воды — диэлектрическая проницаемость, структурные особенности. Реакционная способность воды является совокупным проявлением свойств жидкости и индивидуальных свойств молекул. [c.83]
П ар а о К С и д и ф е и и л ам и н (ВТИН1) предназначен для стабилизации турбинных и трансформаторных масел. Рекомендуемая концентрация 0,01 °/о- С повышением концентрации присадки может происходить увеличение образования шлама в масле. Присадка трудно растворима в воде, но может извлекаться из масла паровых турбин под влиянием воды, содержащей водорастворимые кислоты. При этом вода принимает синий оттенок. Отрицательного влияния на -материалы масляной системы присадка -не оказывает как в присутствии, так и в -отсутствии воды. Диэлектрическая проницаемость присадки 2, 8, б равен 6,6 при 20 С. [c.149]
Руше И Гуд [134] не обнаружили разрывов в ряду значений диэлектрической проницаемости воды в интервале температур от — 1 до 21 °С (измерения выполняли через каждый градус). Квист и Маршалл [127] приводят значения диэлектрической проницаемости воды в интервале температур 0—800 °С. Браун и Айвз [24 ] сообщают, что диэлектрическая проницаемость (е) смеси вода — трет-бутшоп имеет минимальное значение (11,79) при мольной доле спирта 0,87 (е спирта и воды при 25 °С равна 12,52 и 78,54 соответственно), что, вероятно, обусловлено особой формой ассоциации молекул спирта с молекулами воды. Диэлектрические проницаемости различных чистых жидкостей были измерены с помощью модифицированного резонансного метода, применимого для исследования жидкостей, имеющих большое сопротивление. Браун и Айвз также описали метод расчета парциальных давлений на основе состава паровой фазы и давления пара одного из чистых компонентов. [c.25]
Вблизи поверхности электрода из-за адсорбции молекул воды диэлектрическая проницаемость раствора уменьшается (рис. 1, а). В своей модели плотной части ДС Грэм предложил это изменение апроксимировать ступенчатой кривой [25] (рис. 1, б). Однако в этом случае в плоскости z = h разрыва ди- [c.88]
Диэлектрические свойства жидкой фазы — нефти, пресной-воды, электролитов в зависимости от температуры и частоты поляризующего поля изучены рядом авторов [6, 7, 29, 54] Нефть относится к неполярным веществам, поскольку ее диэлектрическая проницаемость колеблется в пределах 2—2,7. Од- нако присутствующие в нефти полярные и неполярные компоненты способствуют приближению ее к слабополярным диэлектрикам. До частоты электрического поля не свыше 50 МГц диэлектрическая проницаемость нефти не зависит от частоты. Исследования Ю. Л. Брылкина и Л. И Дубмана показали, что мезозойские нефти месторождений Западной Сибири имеют диэлектрическую проницаемость 2,2 она остается практически постоянной при изменении температуры от 24 до 100°С и не зависит от частоты внешнего поляризующего поля в пределах 5-10 4-5-10 Гц При повышении температуры от нуля до 100° С диэлектрическая проницаемость воды уменьшается до 40%. С увеличением концентрации солей в воде диэлектрическая проницаемость растворов растет незначительно. [c.109]
Совершенно ясно, что величина как следует из формулы (1,10), тем больше, чем больше величина диэлектрической проницаемости. У воды диэлектрическая проницаемость примерно равна 80,0 и величина 1 — jблизкa к еди-( 1 [c.47]
Для проверки уравнения (4.109) можно рассмотреть, насколько хорощо экспериментальные данные по скорости электронного обмена между Нр(У) и Ыр(У1) описываются этим уравнением. В качестве В следует брать диэлектрическую проницаемость компоненты смещанного растворителя с наибольшей диэлектрической приницаемостью (в данном случае такой компонентой является вода). Диэлектрическая проницаемость воды при температуре 0°, при которой проводили рассматриваемые опыты, равна 88,3. Фактическая диэлектрическая проницаемость в выделенном объеме в форме капсулы, занятом реакционным комплексом, по-видимому, будет несколько меньше, чем 88,3, вследствие диэлектрического насыщения включенного растворителя. Но поскольку истинное значение В не известно, будет использовано значение 88,3. Можно считать, что это относительно неплохое приближение. Величины г и 2 примем равными 5,0 и 1,0 соответственно. Величина г —заряд на центральном атоме комплексного иона Мр(У) г —заряд иона гидроксония — переменная величина, которая зависит от [c.125]
Эмп. ф-ла С12Н27РО4 м. м. 266,32 сокращение ТБФ Свойства жидкость, т. к. 177—178 °С, сл. раств. в воде диэлектрическая проницаемость е = 8,0 Применения в анализе экстр. — актиноиды, Со, 1г, Мп, Мо, Pd, Pt, Rh, Тс, Th, и, W фл. — U ТСХ — Rh, U спектр. — Mo [c.713]
Первое уравнение Онзагера сравнивали с экспериментальными данными. Весьма важно исследовать зависимость константы ионной ассоциаций от диэлектрической проницаемости растворителя. Для этой цели особенно пригодны смеси воды и 1,4-диоксана (С4Н8О2), поскольку, несмотря на свою низкую диэлектрическую проницаемость (е = 2,21 при 25 °С), диоксан смешивается с водой. Диэлектрическую проницаемость смеси диоксан — вода можно варьировать в интервале 78,5—2,2. Однако при добавлении диоксана к воде изменяется не только диэлектрическая проницаемость среды, но и, что весьма существенно,— структура жидкости. Соответственно изменение проводимости водных растворов электролита вследствие присутствия диоксана обусловлено не только изменением диэлектрической проницаемости, но также и всех взаимодействий, определяющих подвижность ионов и зависящих от структуры жидкости. Тем не менее было показано, что в смесях диоксан — вода влияние на проводимость изменений диэлектрической проницаемости значительно. [c.365]
Упражнение 11-32. Объясните, каким образом оптически активный а-метилаллилхлорид может в условиях реакции SnI рацемизоваться быстрее, чем образовывать продукты сольволиза. Где такая рацемизация будет происходить более эффективно — в воде (диэлектрическая проницаемость 80) или уксусной кислоте (диэлектрическая проницаемость [c.294]
Согласно обычным воззрениям, например в теории Дебая — Гюккеля, диэлектрическая проницаемость воды за границами слоя первичной сольватации принимается равной макроскопической диэлектрической постоянной воды. При этом игнорируется влияние на свойства воды значительного давления (доходящего до десятков тысяч атмосфер [12]), возникающего вблизи иона за счет его электростатического поля. Между тем с увеличением давления и с уменьшением удельного объема воды ее диэлектрическая проницаемость заметно увеличивается [13]. Так, например, при повышении давления от 1 до 3000 ат диэлектрическая проницаемость воды (при 20° С) возрастает от 80,8 до 91,9. Можно предположить, исходя из формулы Оуэна и Бринклея [14], что с ростом давления до 10 ООО ат диэлектрическая постоянная увеличивается до —105. Можно ожидать также, что в окрестностях иона имеет место не простое уплотнение воды, но и какой-то фазовый переход, подобный переходу воды в лед VI под повышенным давлением при обычной температуре. Такой фазовый переход также будет связан с увеличением диэлектрической проницаемости, как это видно на примере замерзания воды, диэлектрическая проницаемость которой увеличивается при этом от 87,7 до 91,5. [c.128]
В данной главе будут рассмотрены кислотно-основные взаимодействия в воде, диэлектрическая проницаемость которой равна 80, и, следовательно, в этом растворителе в равновесии будут находиться только недиссоциированные молекулы и свободные ионы и те, и другие, естественно, будут сольватированы растворителем AH-fHjO = А"-ЬНзО [c.96]
chem21.info
Вода диэлектрическая постоянная - Справочник химика 21
Образованию зарядов сильно благоприятствуют растворители с большой диэлектрической постоянной (лучшие изоляторы). Поэтому константа ионизации аминов в этаноле [уравнение (40), ВОН СгНзОН] примерно в 10 раз меньше, чем в воде (SOH = Н2О). Аналогично константа ионизации карбоновых кислот в этаноле [уравнение (41), SOH = С2Н5ОН] примерно в 10 раз меньше, чем в воде (SOH —HjO). Азотная кислота, которая в поде является сильной, практически полностью ионизированной кислотой, обладает в этаноле константой ионизации Ка = 2,5 10 , примерно тождественной константе ионизации муравьиной кислоты в воде. (Диэлектрическая постоянная этанола = 26, а воды t = 80 при 20°.) [c.216] Градиент избыточного давления внутри влажного материала возникает еще при одном способе сущки — подводе тепла с помощью токов высокой частоты. Данный способ основан на том, что все влажные материалы являются в некоторой степени диэлектриками (для воды диэлектрическая постоянная равна 80) и при по- [c.252]Предельные коэффициенты наклона для коэффициентов активности смесей диоксан—вода. Диэлектрические постоянные [c.505]
Как и следовало ожидать, вода и окись дейтерия сходны по кислотно-основному поведению. Обратимый к ионам дейтерия, газовый дейтериевый электрод легко получается на платиновой поверхности, погруженной в тяжелую воду. Диэлектрические постоянные окиси дейтерия и воды весьма близки (77,9 для окиси дейтерия и 78,4 для воды при 25 °С), тогда как плотность тяжелой воды (1,1 г/мл при 25°С) на 10% выше плотности обычной воды. [c.345]
К этому нужно еще добавить, что в органической фазе с меньшей, чем у воды, диэлектрической постоянной многие ионы, например [c.3]
Предел прочности на разрыв, кг/сж . Коэффициент преломления света,. Водостойкость (привес в воде), %. . . Диэлектрическая постоянная при 800 гц [c.313]
Как видно из табл. 3, значения диэлектрической постоянной для различных растворителей значительно отличаются по величине. Они близки к единице для молекул гексана, бензола и других симметричных неполярных молекул и возрастают в десятки раз для таких полярных жидкостей, как спирты и вода. Именно эти последние полярные растворители больше всего подходят для растворения веществ с ионной структурой. Особенно важную роль в этом отношении играет вода, диэлектрическая постоянная которой равна 81. [c.20]
Как изменяется при переходе от воды (диэлектрическая постоянная е = 80) к метиловому спирту (е = 31,5) константа следующего равновесия [c.51]
При растворении КС1 в воде, диэлектрическая постоянная которой D Ai 80, энергия разрыва ионной связи, подсчитанная по формуле (IV,39), становится равной 6,8- 10 эрг, а эта величина будет того же порядка, что и кинетическая энергия молекул воды при комнатной температуре. / [c.91]
На рис. 9 ) означает диэлектрическую постоянную раствора, — диэлектрическую постоянную чистой воды, — диэлектрическую постоянную раствора при частоте, которая слишком велика для молекул белка, не успевающих в этом случае следовать за колебаниями заряда. Заметим, что меньше, чем D. Молекулы растворенного вещества при такой частоте инертны и занимают определенный объем, так что в единице объема раствора содержится меньше воды, чем в чис- [c.90]
ТОЙ воде. —диэлектрическая постоянная раствора при такой высокой частоте, при которой уже ни молекулы растворителя, ни молекулы растворенного вещества не успевают реагировать на колебания знака заряда. При этой частоте действуют только атомный и электрон-нмй факторы поляризации. [c.91]
В зависимости от природы полимера, температуры, давления изменяется не только общее количество связанной воды при набухании, но связанная вода в полимерах обладает и особыми физическими свойствами, отличными от свойств обычной воды. Так, ее плотность достигает 2 г/см , т. е. почти в два раза больше чем у обычной воды, диэлектрическая постоянная вместо 81 имеет значение около 2,2, что обусловливает ее пониженную способность растворять электролиты и полярные неэлектролиты изменяются упругость пара и температура замерзания. [c.358]
С увеличением частот измерения до величин, соответствующих скорости реориентации молекул воды, диэлектрическая постоянная отклоняется от своего статического значения пропорциональ-ноу удельной электропроводности. Электропроводность (Ом -м- ), измеренная при частотах выше зоны дисперсии, составляет около [c.42]
Итак, и у льда, и у жидкой воды диэлектрическая постоянная весьма велика, что объясняется, как помним, наличием большого электрического момента молекулы воды. Пусть величина этого момента, рассчитанная применительно к единице объема, будет ж пусть молекулы воды расположены по тетраэдрической схеме рис. 526, а. Тогда диэлектрическая постоянная [c.831]
Определенную роль играет также диэлектрическая проницаемость растворителя е. При низкой проницаемости ионы, образующиеся согласно (4.16) и (4.18), могут ассоциироваться. Тогда в растворе в значительных количествах присутствуют совокупности противоэаряжснных иопов. Такие совокупности называют ионными ассоциатами ионными парами). Они возникают только вследствие электростатического притяжения и этим отличаются от молекул. За счет образования ионных ассоциатов, например, можно в основном объяснить уменьшение силы уксусной кислоты в этаноле (е = 24,2 рКа=Ю,3) по сравнению с силой этого протолита в воде (ё = 78,5 рКд =4,8). В случае воды диэлектрическая постоянная настолько велика, что с образованием ионных ассоциатов в водных растворах можно не считаться. [c.49]
Образование комплексных ионов при уменьшении диэлектрической постоянной растворителя можно наблюдать, если концентрированный водный раствор хлористого кобальта o lg, имеющий розовый цвет, обусловленный наличием в растворе катионов Со +, нагреть, то из-за нарушения ориентации диполей молекул воды диэлектрическая постоянная ее уменьшается, что способствует образованию комплексных ионов [СоСЦ] [c.274]
Скорость салюрастворения железного электрода в принципе может быть снижена также путем повышения перенапряжения выделения на нем водорода. Но этот путь встречает еще большие затруднения, объясняющиеся тем, что в данном случае выделение водорода происходит с участием молекул воды, заполняющих жидкостную обкладку двойного электрического слоя. Следовательно, для уменьшения скорости выделения водорода нeoбxoдн ю вытеснить воду из двойного слоя. Практически решение этой задачи в настоящее время невозможно ввиду отсутствия веществ, которые, обладая более высокой, чем вода, диэлектрической постоянной, были бы способны адсорбироваться на железном электроде. [c.91]
Воотен и Хаммет [40] сделали интересное наблюдение, что заместители, увеличивающие силы кислот (Ка), увеличивают также и их относительную силу (Кг) при замене воды бутанолом в качестве растворителя. Точно так же заместители, уменьшающие Ка, уменьшают и Кг- Это показано в последнем столбце табл. 6. Сопоставление ограничивается мета- и лара-замещенными бензойными кислотами, и, насколько можно верить существующим ныне данным, это столь же верно и для других растворителей, имеющих меньшую, чем у воды, диэлектрическую постоянную. [c.373]
Из всех перечисленных видов воды особый интерес представляет связанная вода в набухших высокополимерах. То или иное количество ее в полимере зависит не только от внешних факторов (температуры, давления), но и от природы полимера, т. е. от гидрофильности полимера, и, в общем, количество это довольно велико. Так, например, для желатины содержанйе связанной воды в два раза, а для агара даже в четыре раза превышает вес сухого вещества. Исследования показали, что связанная вода в полимерах обладает совершенно особыми физическими свойствами, отличными от свойств обычной воды. Так, ее плотность й достигает 2 г/см , т. е. почти в два. раза больше, чем у обычной воды диэлектрическая постоянная, наоборот, весьма мала, всего лишь около 2,2 вместо 81, что обусловливает ее пониженную способность растворять электролиты и полярные неэлектролиты [c.188]
Задача данной работы состоит в воспроизведении опыта А. И. Каблукова. Можно также Вместо . разных спиртов,. эфира и бензола готовить водно-опиртовые среды, начиная от чистой воды (диэлектрическая постоянная 81) до чистого этилового спирта (диэлектрическая постоянная 25). [c.92]
Так, в воде,диэлектрическая постоянная которой высокая (6 78,5) [77], кислота растворяется плохо, а растворииость ее в н-гептане и бензоле, значения диэлектрических постояннкх которых близки ( = 1,9 и 2,3), резко различна. [c.15]
chem21.info
Диэлектрическая постоянная вода - Большая Энциклопедия Нефти и Газа, статья, страница 2
Диэлектрическая постоянная вода
Cтраница 2
Диэлектрическая постоянная жидкого аммиака при 25 в четыре с лишним раза меньше диэлектрической постоянной воды. [16]
Эти два объяснения электролитической диссоциации, основывающиеся одно - на высоком значении диэлектрической постоянной воды, а другой - на дипольном характере ее молекул, не представляют, однако, взаим ноддоолняющих гипотез. Высокая диэлектрическая постоянная воды является прямым следствием резкой полярности ее молекул. Поэтому, в сущности говоря, обе гипотезы представляют в действительности одну и ту же гипотезу, но изложенную в первом случае на языке макроскопических явлений ( высокая диэлектрическая постоянная), а во втором - как бы в переводе на язык молекулярной физики. [17]
Важность учета наличия Н - связей может быть продемонстрирована на результатах теоретических расчетов диэлектрической постоянной воды при разных температурах. Соответствующие данные приведены в табл. 4, а на рис. 3 показано изменение диэлектрической постоянной воды с температурой. Как видно из рисунка, некоторые расчеты не только дают правильную величину диэлектрической постоянной, но и правильно описывают ее изменение с температурой [854, 877], другие - приводят к неверным значениям одной или обеих из этих характеристик. [18]
В настоящее время мы но знаем, насколько точно уравнение ( 6) выражает зависимость диэлектрической постоянной воды от давления при температурах, отличных от 20, однако поскольку оно является единственным уравнением, которым мы располагаем, и, кроме того, оно было тщательно проверено с применением других жидкостей, мы воспользовались этим уравнением для определения S ( V), & ( К) и ( К) fljm ьсех температур, которые встречаются в таблице. В § 4 будут рассмотрены экспериментальные доказательства того, что значения коэффициента наклона S ( V), невидимому, определены правильно с точностью до диух значащих цифр при комнатной температуре. [19]
В настоящее время мы не знаем, насколько точно уравнение ( 6) выражает зависимость диэлектрической постоянной воды от давления при температурах, отличных от 20, однако поскольку оно является единственным уравнением, которым мы располагаем, и, кроме того, оно было тщательно проверено с применением других жидкостей, мы воспользовались этим уравнением для определения S ( v, SK и § ( Е) Для всех температур, которые встречаются в таблице. В § 4 будут рассмотрены экспериментальные доказательства того, что значения коэффициента наклона S ( v, невидимому, определены правильно с точностью до двух значащих цифр при комнатной температуре. Слабая зависимость & ( к) от температуры и изменение знака S ( E) при низких температурах также подтверждаются опытными данными [12, 13], однако изученные в этих исследованиях концентрации слишком высоки, чтобы можно было проверить правильность численных значений этих теоретических коэффициентов наклона. [21]
Поскольку диэлектрическая постоянная D в обоих уравнениях стоит в знаменателе, то очевидно, что высокое значение диэлектрической постоянной воды ( 78 6 при 25 С) заметно понижает и энергию, и силу. Так, например, энергия, необходимая для разделения ионов в воде, значительно меньше энергии разделения ионов практически во всех органических растворителях, поскольку последние имеют низкие значения диэлектрической постоянной. Диэлектрическая постоянная - иногда ее называют удельной наведенной емкостью-является одной из характеристик самого вещества, зависящей от температуры и от той длины волны, при которой проводятся измерения. Как только ионы разделятся, молекулы воды под действием сил ион-дипольного притяжения тотчас же ориентируются вокруг заряженных частиц. В результате образующиеся ионы приобретают изолирующую оболочку, состоящую из молекул растворителя, которая препятствует их непосредственному контакту с ионами, несущими заряд противоположного знака. [22]
Первую производную в этом уравнении он, как и Кричевский [143], вычислил по данным Киропулоса [145] об изменении диэлектрической постоянной воды с давлением. Для оценки величины второй производной Хаманн воспользовался данными Бриджмена по сжимаемости NaCl, предположив, что изменение среднего ионного радиуса Na и СГ составляет одну треть этой величины. [23]
Согласно обычным воззрениям, например в теории Дебая - Гюккеля, диэлектрическая проницаемость воды за границами слоя первичной сольватации принимается равной макроскопической диэлектрической постоянной воды. При этом игнорируется влияние на свойства воды значительного давления ( доходящего до десятков тысяч атмосфер [12]), возникающего вблизи иона за счет его электростатического поля. Можно ожидать также, что в окрестностях иона имеет место не простое уплотнение воды, но и какой-то фазовый переход, подобный переходу воды в лед VI под повышенным давлением при обычной температуре. [24]
Некоторые расчеты диэлектрической постоянной воды были основаны на теории Кирквуда для полярных диэлектриков. [25]
Вместе с тем внутреннее трение частиц воды невелико, так что при вращении диполей воды значительных потерь не возникает. Большая величина диэлектрической постоянной воды практически сохраняется и в случае переменных полей достаточно высоких частот. Отсюда следует, что покрытие проводников цепи пленкой влаги во время дождя практически не увеличивает потерь при передаче энергии. Возрастание же параметра утечки G в этом случае объясняется исключительно ухудшением изоляции в точках крепления проводов цепи к опорам. [26]
Исследования показывают, что первым членом уравнения ( 1 - 5) для сильных электролитов ( в отличие от слабых) можно пренебречь. Второй член учитывает зависимость электропроводности от диэлектрической постоянной воды и вязкости среды и существенно влияет на А. [27]
При температуре ниже - 83 фтористый водород превращается в твердое вещество. Диэлектрическая постоянная жидкого фтористого водорода при 0 выше диэлектрической постоянной воды. При нагревании концентрированного водного раствора перегоняется сначала газ НгРг, а затем 38 2 % - ная жлота, обладающая постоянной точкой кипения. До 40 кислота би молекулярна, выше же 80 она мономолекулярна. [28]
Второе существенное отличие растворов кислот и оснований в жидком аммиаке от растворов в воде вызвано различием диэлектрических постоянных этих растворителей. Диэлектрическая постоянная жидкого аммиака в несколько раз меньше диэлектрической постоянной воды. [29]
При температуре ниже - 83 фтористый водород превращается в твердое вещество. Диэлектрическая постоянная жидкого фтористого водорода при 0 выше диэлектрической постоянной воды. При нагревании концентрированного водного раствора перегоняется сначала газ НгРг, а затем 38 2 % - ная жлота, обладающая постоянной точкой кипения. До 40 кислота би молекулярна, выше же 80 она мономолекулярна. [30]
Страницы: 1 2 3 4
www.ngpedia.ru



















