Чистые вещества: примеры. Получение чистых веществ. Вода чистое вещество
Чистые вещества — урок. Химия, 8–9 класс.
В античные времена древнегреческими учёными было сформулировано предположение, которое позже полностью подтвердилось — о том, что вещества состоят из мельчайших невидимых глазу частиц.
Например, вода состоит из одинаковых частиц, называемых молекулами воды. Сахар состоит из одинаковых частиц, называемых молекулами сахара. Вода и сахар — это чистые вещества.
Чистыми веществами называются вещества, которые состоят из частиц одинакового вида.
Если же сахар смешать с водой, происходит диффузия — молекулы сахара проникают между молекулами воды. Образуется раствор, в состав которого входят как молекулы воды, так и молекулы сахара.Раствор — это смесь веществ.
Смесями называют вещества, в состав которых входят частицы разного вида.
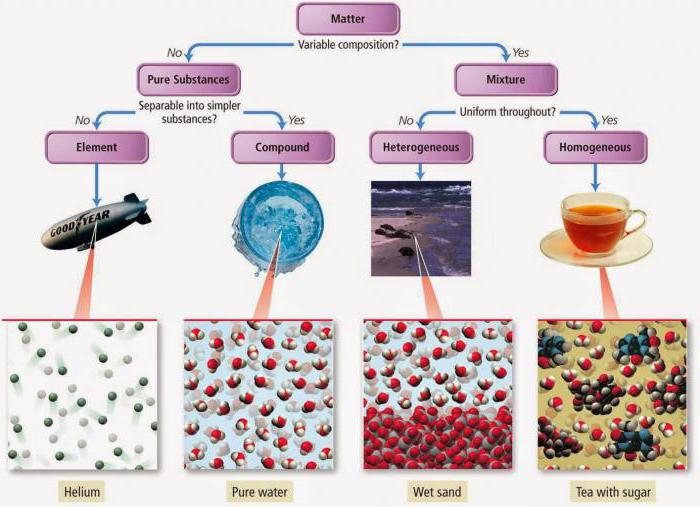
Все вещества являются либо чистыми, либо смесями.

Чистые вещества состоят из частиц одного вида, а смеси — из частиц разного вида.
Кроме веществ, состоящих из молекул, существуют вещества, имеющие немолекулярное строение.
Например, металлы и инертные газы состоят не из молекул, а из более мелких частиц — атомов.
Таким образом, медь состоит только из атомов меди, а цинк состоит только из атомов цинка. Медь и цинк — чистые вещества. Если к меди добавить цинк и сильно нагреть, получится сплав, который называют латунью.
Латунь — это смесь, в состав которой входят как атомы меди, так и атомы цинка.
Существуют вещества немолекулярного строения, состоящие из частиц другого вида, называемых ионами. В состав ионных соединений входят не электрически нейтральные атомы или молекулы, а частицы, несущие на себе положительный или отрицательный заряд.
Примером таких веществ может служить хлорид натрия, то есть обычная поваренная соль, кристаллы которой состоят из положительно заряженных ионов натрия и отрицательно заряженных ионов хлора. Поваренная соль является чистым веществом. Если же её растворить в воде, образуется раствор, который является смесью двух веществ — воды и поваренной соли.
Сравнение чистых веществ и смесей
| Чистые вещества | |
| Состав | Чистое вещество состоит из частиц одного вида. Например, вода состоит только из молекул воды.
Чистое вещество имеет постоянный состав. Например, любая молекула воды состоит из двух атомов химического элемента водорода и одного атома химического элемента кислорода. | Смесь состоит из частиц разного вида. Например, раствор сахара в воде содержит как молекулы воды, так и молекулы сахара.
Смесь не имеет постоянного состава: содержание отдельных составных частей одной и той же смеси может быть разным. Условно говоря, в стакане воды можно растворить и одну чайную ложку сахара, и две. |
| Свойства | Чистое вещество имеет постоянные свойства. | В смеси каждое вещество в основном сохраняет свои свойства. Например, железо так же, как обычно, притягивается магнитом, поваренная соль остаётся солёной.
Физические свойства смеси отчасти меняются с изменением её количественного состава. |
Обрати внимание!
Следует иметь в виду, что идеально чистых веществ не существует, поскольку ни одно из веществ невозможно полностью очистить от содержащихся в нём примесей.
Какое же вещество в таком случае на практике считается чистым?Практически чистым (чистым) называют вещество, в котором содержание примесей столь ничтожно, что эти примеси существенным образом не влияют на его свойства.
Например, вода считается практически чистой, если образец жидкости не имеет цвета, вкуса и запаха, замерзает при температуре \(0\) °С, кипит при температуре \(+100\) °С, при температуре \(+4\) °С имеет плотность \(1000\) кг/м³ и практически не проводит электрический ток.
Чистые вещества: кислород, дистиллированная вода, рафинированный сахар
В некоторых отраслях науки и техники используют особо чистые вещества.


В банках золото хранится в слитках, массовая доля благородного металла в которых составляет \(99,9\) %; в технике для изготовления электронных приборов и микросхем используется кремний, чистота которого составляет \(99,999\) %.
В природе, в технике и в повседневной жизни большей частью приходится иметь дело со смесями. Так, смесью является воздух, природная вода, почва, биологические жидкости, пища и многое другое.
Смеси бывают двух видов: однородные (гомогенные) и неоднородные (гетерогенные).

www.yaklass.ru
Чистое вещество и смеси. Химия
В 8-м классе школьники изучают в курсе химии чистые вещества и смеси. Наша статья поможет им разобраться в этой теме. Мы расскажем, какие вещества называют чистыми, а какие – смесями. А вы когда-нибудь задумывались над вопросом: «Существует ли абсолютно чистое вещество?» Возможно, ответ вас удивит.

Для чего эту тему изучают в школе?
Прежде чем рассматривать определение «чистого вещества», необходимо разобраться с вопросом: «С каким веществом мы на самом деле имеем дело – с чистым или смесью?»
Во все времена чистота вещества волновала не только научных сотрудников, ученых, но и простых людей. Что мы обычно вкладываем в это понятие? Каждый из нас хочет пить воду без примесей тяжелых металлов. Мы хотим дышать свежим воздухом, который не загрязнен выхлопными газами автомобилей. Но можно ли назвать незагрязненные воду и воздух чистыми веществами? С точки зрения науки – нет.
Что такое смесь?
Итак, смесь – это вещество, которое содержит молекулы нескольких видов. Теперь подумайте о составе воды, кторая течет из крана – да-да, в ней много примесей. В свою очередь вещества, которые составляют смесь, называются компонентами. Рассмотрим пример. Воздух, которым мы дышим, – это смесь разных газов. Компоненты, входящие в его состав – кислород, азот, углекислый газ и так далее. В случае, если масса одного компонента в десятки раз меньше массы другого, то такое вещество называют примесью. Часто в природе встречается воздух, который загрязнен примесями сероводорода. Этот газ имеет запах тухлых яиц и является ядовитым для человека. Когда отдыхающие на берегу реки разводят костер, то он загрязняет воздух углекислым газом, который тоже опасен в большом количестве.
У особо догадливых ребят, возможно, уже возник вопрос: «Что чаще встречается – чистые вещества или смеси?» Отвечаем на ваш вопрос: «В основном все, что нас окружает – это смеси».
Таким удивительным образом устроена природа.

Несколько слов о видах чистых веществ
В начале статьи мы обещали рассказать о том, существуют ли вещества абсолютно без примесей. Как вы думаете, бывают ли такие? О водопроводной воде мы уже говорили. Номожет ли содержать в себе примеси родниковая вода? Ответ на этот вопрос прост: абсолютно чистые вещества в природе не встречаются. Однако в научных кругах принято говорить об относительной чистоте вещества. Звучит это так: «Вещество чистое, но с оговоркой». Так, например, оно может быть чистым технически. Чернила черные и фиолетовые содержат примеси. Если их нельзя обнаружить при помощи химической реакции, то такое вещество называют химически чистым. Такой бывает дистиллированная вода.
О чистоте
Итак, пришло время поговорить о чистом веществе. Это такое вещество, которое в своем составе имеет частицы только одного вида. Оказывается, оно имеет особенные свойства. У него есть еще одно название: индивидуальное вещество. Давайте попробуем охарактеризовать свойства чистой воды:
- индивидуальное вещество: дистиллированная вода;
- температура кипения – 100°C;
- температура плавления – 0°C;
- такая вода не имеет вкуса, запаха и цвета.

Как разделять вещества?
Этот вопрос тоже уместен. Очень часто в быту и на производстве (в большей мере) человек разделяет вещества. Так, например, в молоке образуются сливки, которые можно собрать с поверхности, если применить метод отстаивания. Во время переработки нефти человек производит бензин, ракетное топливо, керосин, машинное масло и так далее. На всех этапах переработки человек применяет самые разные способы разделения смесей, которые зависят от агрегатного состояния вещества. Рассмотрим каждый из них.
Фильтрация
Данный метод применяют в том случае, когда есть жидкое вещество, в котором содержатся нерастворимые твердые частицы. Например, вода и речной песок. Такую смесь человек пропускает через фильтр. Таким образом, песок задерживается в фильтре, а чистая вода спокойно через него проходит. Мы редко придаем этому значение, но каждый день на кухне многие горожане пропускают воду из-под крана через очистительные фильтры. Так что в определенной степени вы можете считать себя учеными!

Отстаивание
Об этом методе мы сказали несколько слов чуть выше. Однако рассмотрим его подробнее. К такому методу химики прибегают в случае, когда необходимо разделить суспензии или эмульсии. Например, если в чистую воду проникло растительное масло, то полученную смесь необходимо встряхнуть, затем дать ей настояться некоторое время. После этого человек будет наблюдать явление, когда масло в виде пленки покроет воду.
В лабораториях химики применяют еще один метод, который называется делительная воронка. При использовании этого способа очищения плотная жидкость проникает в емкость, а то, что легче – остается.
Метод отстаивания имеет серьезный недостаток – это низкая скорость протекания процесса. В этом случае необходимо длительное время для формирования осадка. На промышленных предприятиях такой способ все равно используют. Инженеры проектируют специальные конструкции, которые имеют название «отстойники».
Магнит
Каждый из нас хотя бы раз в жизни играл с магнитом. Его удивительное свойство притягивать металлы казалось магическим. Находчивые люди догадались применить магнит для того, чтобы разделять смеси. Например, разделение деревянных и железных опилок возможно при помощи магнита. Но стоит учесть, что не все металлы он может притягивать, ему подвластны только те смеси, в которых содержатся ферромагнетики. К ним можно отнести никель, тербий, кобальт, эрбий и так далее.

Дистилляция
Этот термин имеет латинские корни, в переводе означает «стекание каплями». Такой метод представляет собой разделение смесей, основанное на разницах температуры кипения веществ. Именно этот способ поможет разделить воду и спирт. Последнее вещество испаряется при +78°C. Когда его пары касаются холодных стенок и поверхностей, пары конденсируются, превращаясь в жидкое вещество.
В тяжелой промышленности данным методом добывают продукты нефти, чистые металлы, а также разнообразные душистые вещества.
Можно ли разделить газы?
Мы с вами говорили про чистые вещества и смеси в жидком и твердом состоянии. А как быть, если необходимо провести разделение газовых смесей? Светлые головы химической промышленности сегодня практикуют несколько физических способов разделения газообразных смесей:
- конденсация;
- сорбирование;
- мембранное разделение;
- дефлегмация.

Итак, в нашей статье мы с вами рассмотрели понятие чистых веществ и смесей. Мы выяснили, что чаще встречается в природе. Теперь вы знаете различные способы разделения смесей – и некоторые из них можете продемонсттрировать самостоятельно, например магнит. Надеемся, что наша статья была для вас полезной. Изучайте науку сегодня, чтобы завтра она помогла вам решить любую проблему – как у себя дома, так и на производстве!
fb.ru
Чистые вещества: примеры. Получение чистых веществ
Вся наша жизнь в буквальном смысле построена на работе различных химических веществ. Мы дышим воздухом, который содержит в себе множество различных газов. На выходе получается углекислый газ, который затем перерабатывается растениями. Мы пьем воду или молоко, которое представляет собой смесь воды с другими компонентами (жиром, минеральными солями, белком и так далее).
Банальное яблоко – это целый комплекс сложных химических веществ, которые взаимодействуют друг с другом и нашим организмом. Как только что-то попадает в наш желудок, вещества, входящие в продукт, поглощенный нами, начинают взаимодействие с желудочным соком. Абсолютно каждый объект: человек, овощ, животное – это набор частиц и веществ. Последние делятся на два разных типа: чистые вещества и смеси. В данном материале разберемся, какие вещества чистые, а какие из них относятся к категории смесей. Рассмотрим способы разделения смесей. А также взглянем на типичные примеры чистых веществ.

Чистые вещества
Итак, в химии чистые вещества – это те вещества, что всегда состоят только из одного-единственного вида частиц. И это первое важное свойство. Чистым веществом является вода, например, которая состоит исключительно из молекул воды (то есть своих собственных). Также чистое вещество всегда имеет постоянный состав. Таким образом, каждая молекула воды состоит из двух атомов водорода и из одного атома кислорода.
Свойства чистых веществ, в отличие от смесей имеют постоянный характер и изменяются при появлении примесей. Только дистиллированная вода имеет температуру кипения, а морская кипит при более высокой температуре. При этом стоит учитывать, что любое чистое вещество не является абсолютно чистым, так как даже чистый алюминий имеет примесь в составе, хоть она и имеет долю в 0.001 %. Возникает вопрос, как выяснить массу чистого вещества? Формула для вычисления выглядит следующим образом – m (масса) чистого вещества = W (концентрация) чистого вещества * смесь / 100 %.
Также существует такой тип чистых веществ, как особо чистые вещества (ультрачистые, высокочистые). Такие вещества используются в производстве полупроводников в различных измерительных и вычислительных устройствах, атомной энергетике и во многих других профессиональных областях.

Примеры чистых веществ
Мы уже выяснили, что чистым веществом является то, что содержит в себе элементы одного вида. Хорошим примером чистого вещества может послужить снег. По сути это та же вода, но в отличие от той воды, с которой мы сталкиваемся ежедневно, эта вода гораздо чище и не содержит примесей. Алмаз тоже является чистым веществом, поскольку он содержит в себе только углерод без примесей. Это же относится и к горному хрусталю. На ежедневной основе мы сталкиваемся с еще одним примером чистого вещества – рафинированным сахаром, который содержит в себе одну лишь сахарозу.
Смеси
Мы уже рассмотрели чистые вещества и примеры чистых веществ, теперь перейдем к другой категории веществ – смесям. Смесь – это когда несколько веществ смешиваются друг с другом. Мы сталкиваемся со смесями на постоянной основе даже в быту. Тот же чай или мыльный раствор представляют собой смеси, которые мы применяем ежедневно. Смеси могут быть созданы человеком, а могут быть природными. Они находятся в твердом, жидком и газообразном состоянии. Как уже было сказано выше, тот же чай является смесью воды, сахара и чая. Это пример смеси, созданной человеком. Молоко является природной смесью, так как оно появляется без участия человека в процессе выработки и содержит в себе множество разных компонентов.

Смеси созданные человеком почти всегда долговечны, а природные под воздействием тепла начинают распадаться на отдельные частицы (молоко, к примеру, прокисает через несколько дней). Смеси также делятся на гетерогенные и гомогенные. Гетерогенные смеси являются неоднородными, а их компоненты видны невооруженным взглядом и под микроскопом. Такие смеси именуют взвесями, которые в свою очередь делят на суспензии (вещество в твердом состоянии и вещество в жидком состоянии) и эмульсии (два вещества в жидком состоянии). Гомогенные смеси однородные, а их отдельные компоненты невозможно рассмотреть. Их также именуют растворами (могут быть веществами в газообразном, жидком или твердом состоянии).
Характеристики смеси и чистых веществ
Для удобства восприятия информация представлена в виде таблицы.
Сравнительный признак | Чистые вещества | Смеси |
Состав веществ | Сохраняют постоянный состав | Имеют непостоянный состав |
Виды веществ | Содержат одно вещество | Включают в себя различные вещества |
Физические свойства | Сохраняют постоянные физические свойства | Имеют непостоянные физические свойства |
Изменение энергии вещества | Изменяется при образовании энергии | Не изменяется |
Способы получения чистых веществ
В природе многие вещества существуют в виде смесей. Они применяются в фармакологии, промышленном производстве.
Для получения чистых веществ применяются различные методы разделения. Гетерогенные смеси делят с помощью отстаивания и фильтрования. Гомогенные смеси делят с помощью выпаривания и дистилляции. Рассмотрим каждый способ отдельно.
Отстаивание
Этот метод используется для разделения суспензий, таких как смесь речного песка с водой. Главным принципом, на котором основывается процесс отстаивания, является разница в плотностях тех веществ, которые будут разделены. Например, одно тяжелое вещество и вода. Какие чистые вещества тяжелее воды? Это песок, например, который в силу своей массы начнет оседать на дно. Таким же образом разделяют различные эмульсии. Например, от воды можно отделить растительное масло или нефть. Эти вещества в процессе разделения образуют небольшую пленку на поверхности воды. В лабораторных условиях этот же процесс проводят с использованием делительной воронки. Этот способ разделения смесей работает и в природе (без участия человека). Например, осаждение сажи из дыма и отстаивание сливок в молоке.
Фильтрование
Этот метод подходит для получения чистых веществ из гетерогенных смесей, например, из смеси воды с поваренной солью. Итак, каким образом работает фильтрация в процессе разделения частиц смеси? Суть заключается в том, что у веществ различные уровни растворимости и размеры частиц.
Фильтр конструируется таким образом, чтобы через него могли пройти только частицы с той же растворимостью или тем же размером, что он может пропустить. Более крупные и другие неподходящие частицы не смогут пройти через фильтр и будут отсеяны. Роль фильтров могут играть не только специализированные устройства и растворы в пределах лаборатории, но и знакомые всем вещи, такие как вата, уголь, обожженная глина, спрессованное стекло и другие пористые объекты. Фильтры используются в реальной жизни гораздо чаще, чем может показаться.
По такому принципу работает всем нам знакомый пылесос, который отделяет крупные частицы мусора и ловко всасывает мелкие, неспособные повредить механизм. Когда вы болеете, то надеваете марлевую повязку, которая может отсеять бактерии. Рабочие, чья профессия связана с распространением опасных газов и пыли, носят респираторные маски, защищающие их от отравления.
Воздействие магнита и воды
Таким способом можно разделить смесь порошка железа и серы. Принцип разделения основан на воздействии магнита на железо. Частицы железа притягиваются к магниту, в то время как сера останется на месте. Этот же метод можно использовать для отделения других металлических деталей из общей массы разных материалов.
Если порошок серы, смешанный с порошком железа высыпать в воду, то несмачиваемые частицы серы всплывут на поверхность воды, в то время как тяжелое железо сразу же ляжет на дно.
Выпаривание и кристаллизация
Этот способ работает с гомогенными смесями, такими как раствор соли в воде. Это работает в естественных природных процессах и лабораторных условиях. Например, некоторые озера при нагревание испаряют воду, а на ее месте остается поваренная соль. С точки зрения химии, этот процесс основывается на том, что разница между температурой кипения двух веществ, не позволяет им испариться единовременно. Уничтоженная вода обратится в пар, а оставшаяся соль останется в своем обычном состоянии.
Если вещество, которое нужно извлечь (сахар, например) плавится при нагревании, то воду не испаряют полностью. Смесь сначала прогревают, а затем получившуюся модифицированную смесь настаивают, чтобы частицы сахара осели на дне. Иногда стоит более сложная задача - отделение вещества с более высокой температурой кипения. Например, отделение воды от соли. В таком случае, испаренное вещество необходимо собрать, охладить и сконденсировать. Этот метод разделения гомогенных смесей называют дистилляцией (или просто перегонкой). Существуют специальные устройства, которые дистиллируют воду. Такая вода (дистиллированная) активно используется в фармакологии или в автомобильных системах охлаждения. Естественно, этим же методом люди перегоняют спирт.

Хроматография
Последний метод отделения – хроматография. Он основан на том, что некоторые вещества имеют свойство поглощать другие компоненты веществ. Это работает следующим образом. Если вы возьмете кусочек бумаги или ткани, на которой что-то написано чернилами и погрузите ее часть в воду, то заметите следующее: вода начнет впитываться бумагой или тканью и будет ползти вверх, а вот красящее вещество будет немного отставать. Используя данную методику ученый М. С. Цвет смог отделить хлорофилл (вещество, дающее зеленый окрас растениям) от зеленых частей растения.
fb.ru
Чем отличаются чистые вещества и смеси? Особо чистые вещества :: SYL.ru
Все существующие предметы, жидкости и газы представляют собой чистые вещества и смеси. Не зная, что они такое, очень легко их спутать. Как же отличить одно от другого? Давайте разбираться.
От элементов к веществу
В настоящий момент в мире известно 118 химических элементов. Они обладают своими названиями и химическими символами, которые обозначаются латинскими буквами. Каждый из них представляет один вид атомов, которые обладают определенным количеством электронов, расположенных в строгом порядке.
Элементы – это своеобразные строительные материалы. Их можно сравнить с кирпичами: соприкасаясь, они формируют стены, а то и целое здание. Так, соединяясь друг с другом, атомы одного элемента могут «построить» простое вещество (кислород O2, водород h3, азот N2 и т.д.). Сложное, в свою очередь, образуется от слияния разных элементов (вода h3O, аммиак Nh4 и т.д.).
И в том, и в другом случае они являются чистыми веществами. Почему? Потому что соединение происходит при помощи химических реакций. При этом может выделяться или поглощаться энергия.

Что такое смесь?
Смесь тоже состоит из двух или более различных компонентов. Но её составляющими частями являются не отдельные элементы, а вещества (могут быть и сложными, и простыми). Смеси бывают гетерогенные и гомогенные.
Первые понять гораздо проще. В них компоненты смешиваются чисто механически и спокойно отделяются друг от друга фильтрацией, магнитом, отстаиванием и другими методами. Гетерогенные смеси неоднородны, а их компоненты целиком сохраняют индивидуальные свойства.

Примером такого образования может служить добавление речного песка в воду. Они не смогут смешаться и образовать новое вещество, и легко отделяются, если использовать сито.
Гомогенные смеси образуют однородное на первый взгляд вещество. Они представляют собой газы, твердые или жидкие растворы. Их компоненты тоже сохраняют первичные свойства, но не могут быть отделены механическим способом. Для их разделения используют более изощренные методы: перегонку, кристаллизацию, сорбцию (поглощение), экстракцию (растворение одного компонента) т. д.
Типичная гомогенная смесь - это воздух. Он состоит из различных газов, крупинок пыли, капель воды. Морская вода тоже не является чистым веществом. Кроме собственно воды, в ней содержатся соли металлов (натрия, хлора, калия и других).
Отличия смеси от веществ
Порой смеси и чистые вещества очень просто перепутать. Например, латунь обладает металлическими свойствами и внешне напоминает какой-нибудь металл. Однако она является сплавом, который состоит из меди, цинка и других компонентов (часто это бывает олово, никель, свинец, железо).
В чем же разница? Главным отличием является то, что вещество – это полностью однородное образование. Разделить его составные части можно, только используя химические реакции. Свойства чистого вещества отличаются от свойств его компонентов по-отдельности, оно является новой структурой и приобретает иные качества.
Кроме того, вещество обладает постоянным составом. Существует даже специальный реестр с перечнем всех известных структур. Смесь, наоборот, не обладает четким составом. В той же латуни может быть меньше никеля, и больше другого металла, но это все равно латунь. В чай, например, можно добавить больше или меньше сахара, но чаем он от этого быть не перестанет. Если же из молекулы чистой воды h3O убрать кислород (O), то это будет не вода, а молекула водорода – бесцветного газа.

Особо чистое вещество
В природе чаще встречаются смеси, чем вещества. Так, в земной коре залегает множество минералов, металлических руд и газов, но чистыми их назвать сложно. Большинство из них содержат примеси.
Для промышленного производства они, как правило, не подходят. Поэтому их очищают и отделяют друг от друга всевозможными способами. Вещества, которые содержат настолько небольшой процент примесей, что они не могут повлиять на его свойства, называют ультрачистыми или особо чистыми. Их получают при помощи очень тщательной очистки. Так, для создания полупроводников нужно максимально однородное вещество, поэтому от примесей избавляют не только материал для него, но и воздух в помещении, где его производят.
www.syl.ru
Урок №3. Чистые вещества и смеси. Способы разделения смесей
I. Новый материал
При подготовке урока использованы материалы автора: Н.К.Черемисиной,
учителя химии средней школы № 43
(г. Калининград), Источник
Мы живем среди химических веществ. Мы вдыхает воздух, а это смесь газов (азота, кислорода и других), выдыхаем углекислый газ. Умываемся водой - это еще одно вещество, самое распространенное на Земле. Пьём молоко - смесь воды с мельчайшими капельками молочного жира, и не только: здесь еще есть молочный белок казеин, минеральные соли, витамины и даже сахар, но не тот, с которым пьют чай, а особый, молочный - лактоза. Едим яблоки, которые состоят из целого набора химических веществ - здесь и сахар, и яблочная кислота, и витамины... Когда прожеванные кусочки яблока попадают в желудок, на них начинают действовать пищеварительные соки человека, которые помогают усваивать все вкусные и полезные вещества не только яблока, но и любой другой пищи. Мы не только живем среди химических веществ, но и сами из них состоим. Каждый человек - его кожа, мышцы, кровь, зубы, кости, волосы построены из химических веществ, как дом из кирпичей. Азот, кислород, сахар, витамины – вещества природного, естественного происхождения. Стекло, резина, сталь – это тоже вещества, точнее, материалы (смеси веществ). И стекло, и резина - искусственного происхождения, в природе их не было. Совершенно чистые вещества в природе не встречаются или встречаются очень редко.
Чем же отличаются чистые вещества от смесей веществ?
Индивидуальное чистое вещество обладает определённым набором характеристических свойств (постоянными физическими свойствами). Только чистая дистиллированная вода имеет tпл = 0 °С, tкип= 100 °С, не имеет вкуса. Морская вода замерзает при более низкой, а закипает при более высокой температуре, вкус у нее горько-соленый. Вода Черного моря замерзает при более низкой, а закипает при более высокой температуре, чем вода Балтийского моря. Почему? Дело в том, что в морской воде содержатся другие вещества, например растворенные соли, т.е. она представляет собой смесь различных веществ, состав которой меняется в широких пределах, свойства же смеси не являются постоянными. Определение понятия «смесь» было дано в XVII в. английским ученым Робертом Бойлем: «Смесь – целостная система, состоящая из разнородных компонентов».
Сравнительная характеристика смеси и чистого вещества
| Признаки сравнения | Чистое вещество | Смесь |
| Состав | Постоянный | Непостоянный |
| Вещества | Одно и то же | Различные |
| Физические свойства | Постоянные | Непостоянные |
| Изменение энергии при образовании | Происходит | Не происходит |
| Разделение | С помощью химических реакций | Физическими методами |
Смеси отличаются друг от друга по внешнему виду.
Классификация смесей показана в таблице:

Приведём примеры суспензий (речной песок + вода), эмульсий (растительное масло + вода) и растворов (воздух в колбе, поваренная соль + вода, разменная монета: алюминий + медь или никель + медь).
В суспензиях видны частицы твердого вещества, в эмульсиях – капельки жидкости, такие смеси называются неоднородными (гетерогенными), а в растворах компоненты не различимы, они являются однородными (гомогенными) смесями.
Способы разделения смесей
В природе вещества существуют в виде смесей. Для лабораторных исследований, промышленных производств, для нужд фармакологии и медицины нужны чистые вещества.
Для очистки веществ применяются различные способы разделения смесей

Эти способы основаны на различиях в физических свойствах компонентов смеси.
Рассмотрим способы разделения гетерогенных и гомогенных смесей.
| Пример смеси | Способ разделения |
| Суспензия – смесь речного песка с водой | Отстаивание Разделение отстаиванием основано на различных плотностях веществ. Более тяжелый песок оседает на дно. Так же можно разделить и эмульсию: отделить нефть или растительное масло от воды. В лаборатории это можно сделать с помощью делительной воронки. Нефть или растительное масло образует верхний, более легкий слой. В результате отстаивания выпадает роса из тумана, осаждается сажа из дыма, отстаиваются сливки в молоке. Разделение смеси воды и растительного масла отстаиванием |
| Смесь песка и поваренной соли в воде | Фильтрование На чем основано разделение гетерогенных смесей с помощью фильтрования?На различной растворимости веществ в воде и на различных размерах частиц. Через поры фильтра проходят лишь соизмеримые с ними частицы веществ, в то время как более крупные частицы задерживаются на фильтре. Так можно разделить гетерогенную смесь поваренной соли и речного песка. В качестве фильтров можно использовать различные пористые вещества: вату, уголь, обожженную глину, прессованное стекло и другие. Способ фильтрования – это основа работы бытовой техники, например пылесосов. Его используют хирурги – марлевые повязки; буровики и рабочие элеваторов – респираторные маски. С помощью чайного ситечка для фильтрования чаинок Остапу Бендеру – герою произведения Ильфа и Петрова – удалось забрать один из стульев у Эллочки Людоедки («Двенадцать стульев»). Разделение смеси крахмала и воды фильтрованием |
| Смесь порошка железа и серы | Действие магнитом или водой Порошок железа притягивался магнитом, а порошок серы – нет. Несмачивающийся порошок серы всплывал на поверхность воды, а тяжелый смачивающийся порошок железа оседал на дно. Разделение смеси серы и железа с помощью магнита и воды |
| Раствор соли в воде – гомогенная смесь | Выпаривание или кристаллизация Вода испаряется, а в фарфоровой чашке остаются кристаллы соли. При выпаривании воды из озер Эльтон и Баскунчак получают поваренную соль. Этот способ разделения основан на различии в температурах кипения растворителя и растворенного вещества.Если вещество, например сахар, разлагается при нагревании, то воду испаряют неполностью – упаривают раствор, а затем из насыщенного раствора осаждают кристаллы сахара.Иногда требуется очистить от примесей растворители с меньшей температурой кипения, например воду от соли. В этом случае пары вещества необходимо собрать и затем сконденсировать при охлаждении. Такой способ разделения гомогенной смеси называется дистилляцией, или перегонкой. В специальных приборах – дистилляторах получают дистиллированную воду, которую используют для нужд фармакологии, лабораторий, систем охлаждения автомобилей. В домашних условиях можно сконструировать такой дистиллятор: Если же разделять смесь спирта и воды, то первым будет отгоняться (собираться в пробирке-приемнике) спирт с tкип = 78 °С, а в пробирке останется вода. Перегонка используется для получения бензина, керосина, газойля из нефти. Разделение однородных смесей |
Особым методом разделения компонентов, основанным на различной поглощаемости их определенным веществом, является хроматография.
Дома вы можете проделать следующий опыт. Подвесьте полоску из фильтровальной бумаги над сосудом с красными чернилами, погружая в них лишь конец полоски. Раствор впитывается бумагой и поднимается по ней. Но граница подъема краски отстает от границы подъема воды. Так происходит разделение двух веществ: воды и красящего вещества в чернилах.
С помощью хроматографии русский ботаник М. С. Цвет впервые выделил хлорофилл из зеленых частей растений. В промышленности и лабораториях вместо фильтровальной бумаги для хроматографии используют крахмал, уголь, известняк, оксид алюминия. А всегда ли требуются вещества с одинаковой степенью очистки?
Для различных целей необходимы вещества с различной степенью очистки. Воду для приготовления пищи достаточно отстоять для удаления примесей и хлора, используемого для ее обеззараживания. Воду для питья нужно предварительно прокипятить. А в химических лабораториях для приготовления растворов и проведения опытов, в медицине необходима дистиллированная вода, максимально очищенная от растворенных в ней веществ. Особо чистые вещества, содержание примесей в которых не превышает одной миллионной процента, применяются в электронике, в полупроводниковой, ядерной технике и других точных отраслях промышленности.
Прочитайте стихотворение Л. Мартынова «Дистиллированная вода»:
ВодаБлаговолилаЛиться!ОнаБлисталаСтоль чиста,Что ни напиться,Ни умыться.И это было неспроста.Ей не хваталоИвы, талаИ горечи цветущих лоз,Ей водорослей не хваталоИ рыбы, жирной от стрекоз.Ей не хватало быть волнистой,Ей не хватало течь везде.Ей жизни не хваталоЧистой –Дистиллированной воде!
Применение дистиллированной воды
II. Задания для закрепления
1) Поработайте с тренажёрами №1-4 (необходимо загрузить тренажёр, он откроется в браузере Internet Explorer)
Тренажёр №1. Чистые вещества и смеси
Тренажёр №2. Смеси
Тренажёр №3. Смеси в природе
Тренажёр №4. Смеси в сельском хозяйстве
2) Решите задачу:
Дана смесь сахара, речного песка и железных опилок. Предложите способ разделения этой смеси.3) Творческое задание:
Подготовьте электронную презентацию на тему "Чистые вещества и смеси, которые нас окружают"
sites.google.com
Чистые вещества и смеси | Дистанционные уроки
19-Мар-2014 | Нет комментариев | Лолита Окольнова

Начнем с определений
Чистое вещество состоит из молекул одного вида.
Чистые вещества могут быть элементного состава (т.е. состоять из элементов одного вида) — простые вещества:
- твердые вещества: железо, сера
- газы: h3, O2, N2 и т.д.
Чистые вещества — соединения — сложные вещества — состоят из молекул одного вида.
В природе не существует абсолютно чистых веществ. Например, особо чистый алюминий содержит 0,001% примесей.
Даже когда мы считаем воду чистой, то должны понимать, что там есть примеси. Даже дистиллированная вода не может считаться абсолютно чистым веществом — это тоже смесь, только примесей в ней намного меньше, чем в обычной воде.
Фильтрованная вода — тоже не чистое вещество, а смесь растворимых компонентов и воды, водопроводная — тем более!
Смеси — содержит молекулы нескольких видов.
Вещества, составляющие смесь, могут быть простыми и сложными.
Запомните: если вам дана задачи и в условии этой задачи дана смесь веществ, то вещества из этой смеси не реагируют друг с другом!
Однородные смеси (гомогенные)
«Гомо» — означает «одинаковый». Т.е. вещества в гомогенной смеси находятся в одинаковых агрегатных состояниях ( в одинаковых фазах):
- растворы;
- сплавы;
- газовые смеси

Воздух — пример однородной газовой смеси (если учитывать именно газовый состав, частички пыли и т.п. мы здесь не учитываем), молярная масса воздуха принята равной 29 г\моль.
Все растворы — однородные смеси растворимого вещества и растворителя.
Неоднородные смеси (гетерогенные)
Неоднородная смесь — это смесь, где вещества находятся в разных фазах.
- Суспензия: тв. фаза+ жидка фаза; существует только в «смешанном» виде. Если такую смесь оставить на время. то под действием силы тяжести твердые частички осядут. Примеры: зубная паста, гуашь, эмалевые краски и т.д.
- Эмульсия — смесь двух жидкостей разной плотности. Со временем четко разделяются на две фазы. Примеры: жидкость для снятия макияжа, масло в воде, молоко и т.д.
- Аэрозоль — смесь газа и жидкости. Самый известный пример — туман или лак для волос.
С определениями чистых веществ и смесей мы определились, теперь давайте разберем способы разделения смесей.
- Химический способ разделения смеси: в реакцию вводится вещество, реагирующее с одним компонентом и не взаимодействующее с другим. В идеале образующееся новое вещество может образовывать другую фазу, чтобы его можно было легко удалить (осадок или газ).
Физические способы:

Еще одно важное отличие чистых веществ от смесей — температуры плавления и кипения:
| Чистые вещества | Смеси |
| имеют четкие температуры плавления и кипения | плавятся и кипят в интервале температур |
- в ЕГЭ это вопрос А26
- в ГИА (ОГЭ) — А13
Еще на эту тему:
Обсуждение: "Чистые вещества и смеси"
(Правила комментирования)distant-lessons.ru
Учебник химии - Чистые вещества и смеси
Чистые вещества и смеси
В природе вещества встречаются преимущественно в виде смесей (схема 2)
Однородным называют такие смеси, в которых даже с помощью микроскопа нельзя обнаружить частицы веществ, входящих в смесь.
Например, растворы сахара или поваренной соли в воде.
Неоднородным называют такие смеси, в которых невооруженным глазом или при помощи микроскопа можно заметить частицы веществ, составляющих смесь.
Для химических лабораторий и промышленности часто требуются чистые вещества. Чистыми называют вещества, которые обладают постоянными физическими свойствами, например, дистиллированная вода. (Практически абсолютно чистые воды не получены.)
Существует различные способы разделения смесей. Ознакомимся более подробно с этими способами ( схема 3).
Выделение веществ из неоднородной смеси
1. Отстаивание
а) Выделение веществ из неоднородной смеси, образованной нерастворимым в воде веществами с различной плотностью. Например, железные опилки от древесных можно отделить, взбалтывая эту смесь с водой, а затем отстаивая. Железные опилки опускается на дно сосуда, а древесные всплывают, и их вместе с водой можно слить.
б) Некоторые вещества осаждаются в воде с различной скоростью. Если взболтать с водой глину с примесью песка, то песок оседает значительно быстрее. Этот способ используется в керамическом производстве для отделения песка от глины (производство красных кирпичей, глиняной посуды и др.).
в) Разделение смеси малорастворимых друг в друге жидкостей с различной плотностью. смеси бензина с водой, нефти с водой, растительного масла с водой быстро расслаиваются, поэтому их можно разделить с помощью делительной воронки или колонки. Иногда жидкости с различной плотностью отделяют центрифугированием, например славки от молока.
2. Фильтрование
Выделение веществ из неоднородной смеси, образованной растворимыми и нерастворимыми в воде веществами. Для выделения поваренной соли смесь ее с песком взбалтывают в воде. Поваренная соль растворяется, а песок оседает.
Чтобы ускорить отделение нерастворимых частиц из раствора, смесь фильтруют. Песок остается на фильтровальной бумаге, а прозрачный раствор поваренной соли проходит через фильтр.
3. Действие магнитом
Выделение из неоднородной смеси веществ, способных к намагничиванию. Если имеется, например, смесь порошков железа и серы, то их можно разделить при помощи магнита.
Выделение веществ из однородной смеси
4. Выпаривание. Кристаллизация
Чтобы растворное вещество, например поваренную соль, выделить из раствора, последний выпаривают. Вода испаряется, а фарфоровой чашке остается поваренная соль. Иногда применяют упаривание, т. е. частичное испарение воды. В результате образуется более концентрированный раствор, при охлаждении которого растворенное вещество выделяется в виде кристаллов. Этот способ очистки веществ называется кристаллизацией.
5. Дистилляция
Этот способ разделения смесей основан на различии в температурах кипения растворимых друг в друге компонентов.
Дистилляция ( перегонка) прием разделения однородных смесей путем испарения летучих жидкостей с последующей конденсацией их паров. Например, получение дистиллированной воды. Для этого воду с растворенными в ней веществами кипятят в одном сосуде. Образующиеся водяные пары конденсируются в другом сосуде в виде дистиллированной воды.
6. Хроматография
Этот способ основан на том, что отдельные вещества с различной скоростью поглощаются ( связываются ) поверхностью другого вещества.
С сущностью этого способа можно познакомиться на следующем опыте.
Если посуду из фильтрованной бумаги подвесить над сосудом с красными чернилами и погрузит в них лишь конец полоски, то можно заметить, что раствор будет впитываться бумагой и подниматься по ней. Однако граница подъема краски будет отставать от границы подъема воды. Таким образом происходит разделение двух веществ: воды и красящего вещества, придающего раствору красный цвет. В химических лабораториях и на производстве вместо фильтрованной бумаги применяют уголь, известняк и др. Этот метод разделения и очистки веществ весьма перспективной и широко применяется в различных отраслях народного хозяйства.
Хроматографию осуществляют с помощью специальных приборов - хроматографов, основные части которого - хроматографическая колонка и детектор. Сигнал детектора регистрируется самописцем.
sochi-nochi.narod.ru












