Содержание
Ученые выяснили, как отличить по вкусу тяжелую воду от обычной
https://ria.ru/20210407/voda-1727199552.html
Ученые выяснили, как отличить по вкусу тяжелую воду от обычной
Ученые выяснили, как отличить по вкусу тяжелую воду от обычной — РИА Новости, 21.04.2021
Ученые выяснили, как отличить по вкусу тяжелую воду от обычной
Ученые из Чехии, Израиля и Германии в результате лабораторных экспериментов и молекулярного моделирования выяснили, что у человека есть рецепторы, которые… РИА Новости, 21.04.2021
2021-04-07T15:06
2021-04-07T15:06
2021-04-21T10:28
наука
вода
химия
биология
/html/head/meta[@name=’og:title’]/@content
/html/head/meta[@name=’og:description’]/@content
https://cdnn21.img.ria.ru/images/07e5/04/07/1727178918_0:123:1440:933_1920x0_80_0_0_3ae94a30605e0b3c9355aa51c841028f.jpg
МОСКВА, 7 апр — РИА Новости. Ученые из Чехии, Израиля и Германии в результате лабораторных экспериментов и молекулярного моделирования выяснили, что у человека есть рецепторы, которые активируются под воздействием тяжелой воды. Это ставит окончательную точку в научной дискуссии о том, можно ли по вкусу отличить тяжелую воду от обычной. Статья опубликована в журнале Communications Biology.Тяжелая вода имеет ту же химическую формулу, что и обычная, но вместо двух атомов легкого изотопа водорода, протия, она содержит два атома его тяжелого изотопа — дейтерия. Основные химические свойства D2O и h3O, такие как рН, температуры плавления и кипения, очень близки. Различаются два вещества лишь по плотности — у тяжелой воды она примерно на 10 процентов больше. Это различие обусловлено исключительно ядерными квантовыми эффектами, а именно — изменениями нулевых колебаний, которые приводят к немного более сильной водородной связи в D2O по сравнению с h3O. Однако еще в 1930-х годах, сразу после открытия тяжелой воды американских химиком Гарольдом Юри, появились неофициальные данные о том, что тяжелую воду легко отличить от обычной — она сладкая на вкус.Несмотря на то, что сам Юри, получивший за свое открытие Нобелевскую премию по химии, авторитетно заявлял, что тяжелая вода не обладает каким-то особым вкусом, дискуссия о том, можно ли на вкус отличить D2O от h3O, продолжается до сих пор.
Это ставит окончательную точку в научной дискуссии о том, можно ли по вкусу отличить тяжелую воду от обычной. Статья опубликована в журнале Communications Biology.Тяжелая вода имеет ту же химическую формулу, что и обычная, но вместо двух атомов легкого изотопа водорода, протия, она содержит два атома его тяжелого изотопа — дейтерия. Основные химические свойства D2O и h3O, такие как рН, температуры плавления и кипения, очень близки. Различаются два вещества лишь по плотности — у тяжелой воды она примерно на 10 процентов больше. Это различие обусловлено исключительно ядерными квантовыми эффектами, а именно — изменениями нулевых колебаний, которые приводят к немного более сильной водородной связи в D2O по сравнению с h3O. Однако еще в 1930-х годах, сразу после открытия тяжелой воды американских химиком Гарольдом Юри, появились неофициальные данные о том, что тяжелую воду легко отличить от обычной — она сладкая на вкус.Несмотря на то, что сам Юри, получивший за свое открытие Нобелевскую премию по химии, авторитетно заявлял, что тяжелая вода не обладает каким-то особым вкусом, дискуссия о том, можно ли на вкус отличить D2O от h3O, продолжается до сих пор. Исследователи из Института органической химии и биохимии Чешской академии наук под руководством Павла Юнгвирта (Pavel Jungwirth) вместе с коллегами из Еврейского университета в Иерусалиме и Технического университета Мюнхена провели эксперименты на клеточных культурах и мышах, а также тесты на людях, а результаты обработали с привлечением моделей молекулярной динамики.Авторы выяснили, что у человека действительно есть рецепторы сладкого вкуса — TAS1R2 / TAS1R3, которые активируются тяжелой водой. У мышей таких рецепторов нет, поэтому сладкий вкус D2O люди чувствуют, а грызуны нет.Для проверки своей гипотезы ученые использовали в тестах на людях ингибитор сладости лактизол, действующий через рецепторы TAS1R2 / TAS1R3. При введении лактизола люди переставали чувствовать сладкий вкус тяжелой воды.»Несмотря на то, что два изотопа номинально химически идентичны, мы убедительно показали, что люди могут отличать по вкусу, основанному на химическом восприятии, h3O от D2O — последний имеет отчетливый сладкий вкус, — приводятся в пресс-релизе чешского Института органической химии и биохимии слова Павла Юнгвирта.
Исследователи из Института органической химии и биохимии Чешской академии наук под руководством Павла Юнгвирта (Pavel Jungwirth) вместе с коллегами из Еврейского университета в Иерусалиме и Технического университета Мюнхена провели эксперименты на клеточных культурах и мышах, а также тесты на людях, а результаты обработали с привлечением моделей молекулярной динамики.Авторы выяснили, что у человека действительно есть рецепторы сладкого вкуса — TAS1R2 / TAS1R3, которые активируются тяжелой водой. У мышей таких рецепторов нет, поэтому сладкий вкус D2O люди чувствуют, а грызуны нет.Для проверки своей гипотезы ученые использовали в тестах на людях ингибитор сладости лактизол, действующий через рецепторы TAS1R2 / TAS1R3. При введении лактизола люди переставали чувствовать сладкий вкус тяжелой воды.»Несмотря на то, что два изотопа номинально химически идентичны, мы убедительно показали, что люди могут отличать по вкусу, основанному на химическом восприятии, h3O от D2O — последний имеет отчетливый сладкий вкус, — приводятся в пресс-релизе чешского Института органической химии и биохимии слова Павла Юнгвирта. — Таким образом, наше исследование разрешает старый спор относительно особого вкуса тяжелой воды, демонстрируя, что небольшой ядерный квантовый эффект может оказывать заметное влияние на такую базовую биологическую функцию, как распознавание вкуса».Авторы планируют продолжить изучение воздействия тяжелой воды на рецепторы человека — не только те, которые находятся на языке, но и на коже. Тяжелая вода используется в медицинских процедурах, и эта информация, по мнению ученых, может оказаться полезной для врачей и пациентов.
— Таким образом, наше исследование разрешает старый спор относительно особого вкуса тяжелой воды, демонстрируя, что небольшой ядерный квантовый эффект может оказывать заметное влияние на такую базовую биологическую функцию, как распознавание вкуса».Авторы планируют продолжить изучение воздействия тяжелой воды на рецепторы человека — не только те, которые находятся на языке, но и на коже. Тяжелая вода используется в медицинских процедурах, и эта информация, по мнению ученых, может оказаться полезной для врачей и пациентов.
https://ria.ru/20210407/elektrootritsatelnost-1727163698.html
https://ria.ru/20201119/voda-1585416112.html
РИА Новости
1
5
4.7
96
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
2021
РИА Новости
1
5
4.7
96
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og. xn--p1ai/awards/
xn--p1ai/awards/
Новости
ru-RU
https://ria.ru/docs/about/copyright.html
https://xn--c1acbl2abdlkab1og.xn--p1ai/
РИА Новости
1
5
4.7
96
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
1920
1080
true
1920
1440
true
https://cdnn21.img.ria.ru/images/07e5/04/07/1727178918_32:0:1440:1056_1920x0_80_0_0_2916c689342797955eb0646a84bd0c0a.jpg
1920
1920
true
РИА Новости
1
5
4.7
96
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
РИА Новости
1
5
4.7
96
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
вода, химия, биология
Наука, Вода, Химия, биология
МОСКВА, 7 апр — РИА Новости. Ученые из Чехии, Израиля и Германии в результате лабораторных экспериментов и молекулярного моделирования выяснили, что у человека есть рецепторы, которые активируются под воздействием тяжелой воды. Это ставит окончательную точку в научной дискуссии о том, можно ли по вкусу отличить тяжелую воду от обычной. Статья опубликована в журнале Communications Biology.
Ученые из Чехии, Израиля и Германии в результате лабораторных экспериментов и молекулярного моделирования выяснили, что у человека есть рецепторы, которые активируются под воздействием тяжелой воды. Это ставит окончательную точку в научной дискуссии о том, можно ли по вкусу отличить тяжелую воду от обычной. Статья опубликована в журнале Communications Biology.
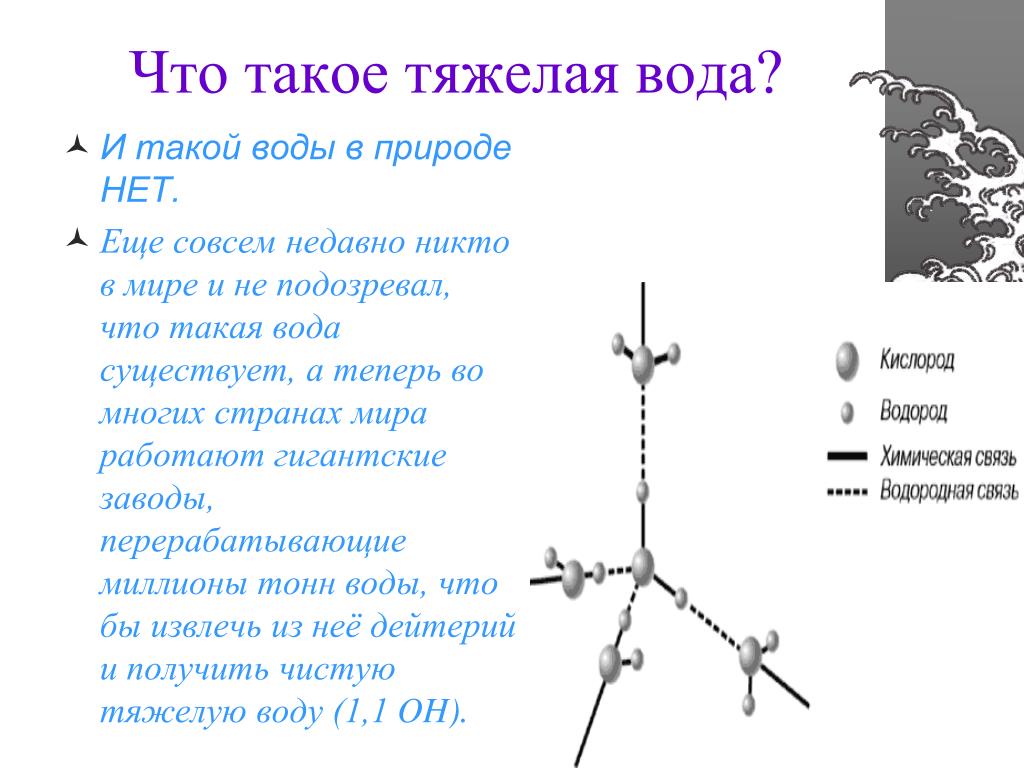
Тяжелая вода имеет ту же химическую формулу, что и обычная, но вместо двух атомов легкого изотопа водорода, протия, она содержит два атома его тяжелого изотопа — дейтерия. Основные химические свойства D2O и H2O, такие как рН, температуры плавления и кипения, очень близки.
Различаются два вещества лишь по плотности — у тяжелой воды она примерно на 10 процентов больше. Это различие обусловлено исключительно ядерными квантовыми эффектами, а именно — изменениями нулевых колебаний, которые приводят к немного более сильной водородной связи в D2O по сравнению с H2O.
Однако еще в 1930-х годах, сразу после открытия тяжелой воды американских химиком Гарольдом Юри, появились неофициальные данные о том, что тяжелую воду легко отличить от обычной — она сладкая на вкус.
Несмотря на то, что сам Юри, получивший за свое открытие Нобелевскую премию по химии, авторитетно заявлял, что тяжелая вода не обладает каким-то особым вкусом, дискуссия о том, можно ли на вкус отличить D2O от H2O, продолжается до сих пор.
7 апреля 2021, 12:44Наука
Российские химики нашли несоответствие в формуле нобелевского лауреата
Исследователи из Института органической химии и биохимии Чешской академии наук под руководством Павла Юнгвирта (Pavel Jungwirth) вместе с коллегами из Еврейского университета в Иерусалиме и Технического университета Мюнхена провели эксперименты на клеточных культурах и мышах, а также тесты на людях, а результаты обработали с привлечением моделей молекулярной динамики.
Авторы выяснили, что у человека действительно есть рецепторы сладкого вкуса — TAS1R2 / TAS1R3, которые активируются тяжелой водой. У мышей таких рецепторов нет, поэтому сладкий вкус D2O люди чувствуют, а грызуны нет.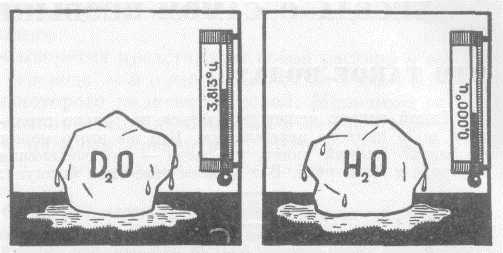
Для проверки своей гипотезы ученые использовали в тестах на людях ингибитор сладости лактизол, действующий через рецепторы TAS1R2 / TAS1R3. При введении лактизола люди переставали чувствовать сладкий вкус тяжелой воды.
«Несмотря на то, что два изотопа номинально химически идентичны, мы убедительно показали, что люди могут отличать по вкусу, основанному на химическом восприятии, H2O от D2O — последний имеет отчетливый сладкий вкус, — приводятся в пресс-релизе чешского Института органической химии и биохимии слова Павла Юнгвирта. — Таким образом, наше исследование разрешает старый спор относительно особого вкуса тяжелой воды, демонстрируя, что небольшой ядерный квантовый эффект может оказывать заметное влияние на такую базовую биологическую функцию, как распознавание вкуса».
Авторы планируют продолжить изучение воздействия тяжелой воды на рецепторы человека — не только те, которые находятся на языке, но и на коже. Тяжелая вода используется в медицинских процедурах, и эта информация, по мнению ученых, может оказаться полезной для врачей и пациентов.
19 ноября 2020, 22:00Наука
Ученые доказали, что вода может иметь несколько жидких состояний
Що таке важка вода | Блог Ecosoft
Короткий зміст
Склад і властивості важкої води
Радіоактивність важкої води
Отримання важкої води
Застосування
Вплив на людину
Важка чи тверда?
Що таке легка вода?
Чи можна очистити воду від дейтерію вдома?
Ми звикли, що формула води H2O означає, що вона містить два атоми водню та один атом кисню. У типовому стані атом водню має заряд 1, тобто в його ядрі знаходиться один протон, його називають протієм. Але існують і особливі атоми, які містять два (дейтерій) або три (тритій) протона в ядрі. Вони називаються ізотопами. Їхні хімічні властивості настільки близькі до атомів звичайного водню, що вони з легкістю утворюють такі ж молекули.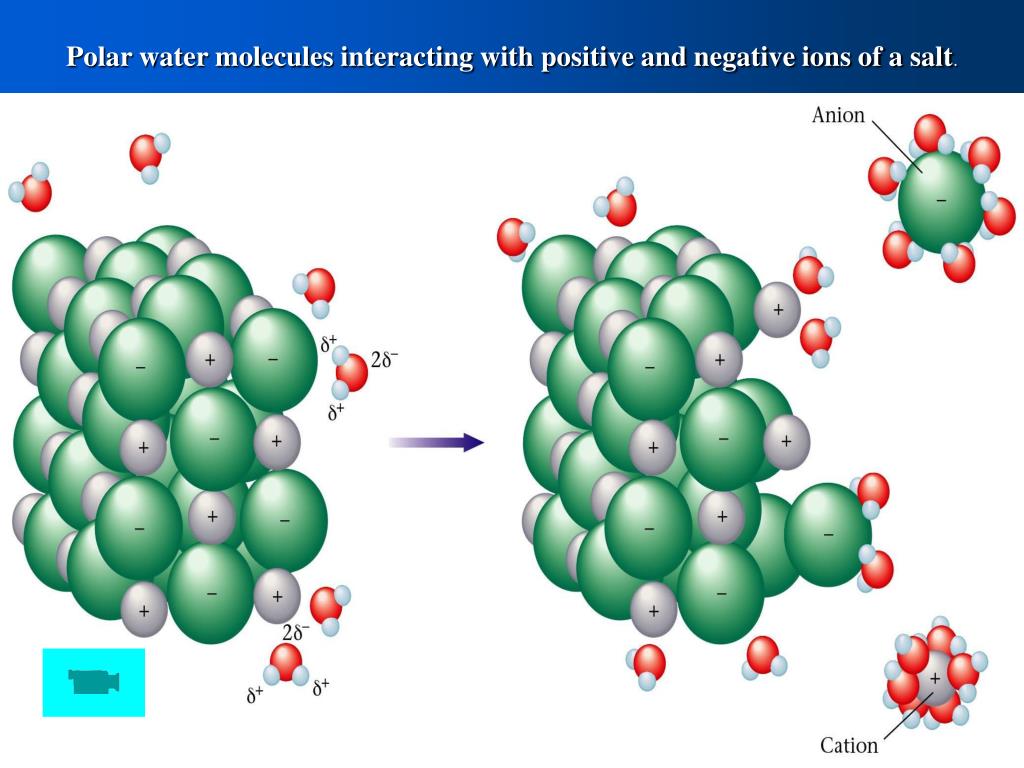
Відповідно, можуть існувати кілька модифікацій звичної нам води.
Склад і властивості важкої води
Найбільш поширеною є протіева або звичайна вода (H2O). Вона становить близько 99,985% загальної маси води на планеті. Решта 0,015% можуть складатися з молекул, які містять різні ізотопи водню згадані вище, а також кисню.
Найпоширенішою модифікацією є напівважка вода (HDO), яка містить один атом звичайного водню (протію) і один атом дейтерію, вона становить основну масу важкої води в цілому. Але фактично завдяки реакціям ізотопного обміну, вона являє собою суміш H2O, HDO, D2O в приблизному співвідношенні 2: 1: 1.
Надважку воду в складі містить тритій. Загалом до неї належить 9 модифікацій, тобто існує 9 формул важкої води, які містять в різних співвідношеннях протій, дейтерій, тритій і ізотопні модифікації кисню — 16O, 17O, 18O та ін. Вміст надважкої води критично малий — до декількох молекул в літрі.
Будова атомів в молекулах призводить до зміни фізичних властивостей води. Нижче ви можете порівняти показники для різних вод.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Варто розуміти, що важка вода в природі існувала завжди, та її кількість не збільшилася і не зменшилася. Цікаво, що в гірських джерелах її менше, ніж в інших поверхневих водоймах.
Цікаво, що в гірських джерелах її менше, ніж в інших поверхневих водоймах.
Радіоактивність важкої води
Варто відзначити, що дейтерій і кисень O16, O17, O18 не є радіоактивними ізотопами, як, відповідно, і їх сполуки.
Щодо тритію, період його напіврозпаду дорівнює 12 рокам. Він дійсно має високу радіотоксичність, як і ряд атомів кисню. При цьому важливо розуміти що вміст тритію в воді менший, ніж 1:1018 мільйонів атомів водню. Його просто неможливо виявити в природних водах.
Причиною його надходження в навколишнє середовище є безперервні ядерні реакції, що відбуваються в атмосфері. Звідси можна прийти до висновку, що він також існує в воді мільйони років і не може впливати на здоров’я людини.
Найбільше тритію в дощі та снігу, найменше в океанічній воді. А в глибинних льодах Антарктиди його просто немає, оскільки він повністю розпадається.
Отримання важкої води
До 1946 року важка вода утворювалась лише завдяки електролізу, пізніше з’явилися технології ректифікації рідкого водню, а також ізотопного обміну в різних системах (водень/аміак, водень/вода, сірководень/вода).
У сучасному виробництві використовують метод, в якому вихідною (початковою) водою є стоки електролітичних цехів отримання водню. Вона містить до 0,2% важкої води. Після застосовується технологія ізотопного обміну в системах сірководень/вода, де відбувається концентрування до 5 — 10%. І на кінцевому етапі проводиться ступінчастий електроліз лужного розчину з отриманням ступеню чистоти дейтерієвої води 99,75 — 99,995%.
Вартість дейтерієвої води відрізняється в залежності від її чистоти. Для прикладу, грам води з вмістом атомів дейтерію від 70% загального числа водню коштує приблизно 0,8 $, а грам води містить вже понад 99,6% коштує 2,5 $.
Якщо розглянути отримання важкої води вдома з точки зору технології виробництва, яка описана вище, ви здогадаєтеся, що це неможливо. Існує теорія, що її можна отримати частковим заморожуванням води, за рахунок різниці температур замерзання води. Теоретично даний метод може допомогти вам підвищити вміст дейтерію на 10-20%, але доцільність цих маніпуляцій залишається під великим питанням. Така вода не має практичного застосування.
Така вода не має практичного застосування.
Використання
Існує кілька сфер застосування важкої води.
- Енергетика. Існують ядерні реактори, в яких важка вода застосовується в якості теплоносія. Її використання дозволяє використовувати природний уран більш низького ступеня збагачення.
- У лабораторіях. Як індикатор і розчинник в фізико-хімічному аналізі, в дослідженнях біологічних об’єктів, а також живих організмів, в тому числі людини.
- В медицині. Крім лабораторних досліджень людини, важка вода може застосовуватися для лікування грибків і бактерій, гіпертензії та ін.
Вплив на людину
Вище ми акцентували на головному факторі — чи шкідлива важка вода? Оскільки її вміст стабільний в атмосфері вже протягом багатьох тисячоліть, то її невисокі кількості у питній воді точно не є небезпечними для людства.
Що стосується експериментів із застосуванням концентрованої дейтерієвої води, то її не дарма називають мертвою водою.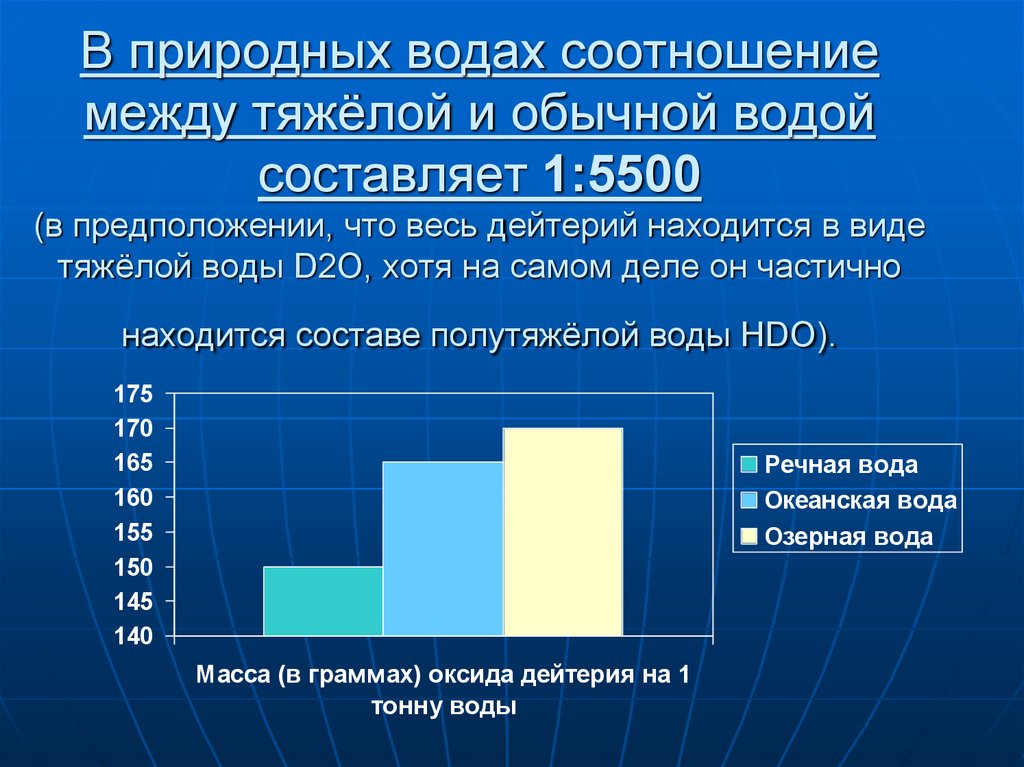
Через відмінності фізичних властивостей, зокрема, густини, вона складніше проходить через клітинні мембрани, тому фактично пригнічує життєдіяльність. А через більш міцні водневі зв’язки хімічні реакції уповільнені.
Найпростіші можуть адаптуватися до 70-% води, а водорості здатні жити й розмножуватися навіть у 99% дейтерієвій воді.
Що стосується ссавців, тут заміщення 25% відсотків води призводить до неможливості давати потомство. Також великий обсяг важкої води мав ефективність при лікуванні ракових пухлин, але при цьому приводив до смерті тварини.
Людина може спокійно випити кілька склянок важкої води без будь-якого впливу на стан внутрішніх органів і самопочуття. Сьогодні така вода використовується для лікування певних випадків гіпертонії, що доводить відсутність побічних ефектів навіть при регулярному застосуванні її невеликих кількостей.
Варто також відзначити, що в організмі людини міститься певна кількість важкої води — рівна тій, що знаходиться в п’яти грамах звичайної води.
Важка чи жорстка вода?
Коли ми вивчали публікації про важку воду в інтернеті, дізналися, що деякі люди плутають її з «твердою» чи «жорсткою».
Тверда вода — це вода, яка містить певну кількість солей твердості, переважно карбонатів кальцію і магнію. Тверда — вода це про вапняний наліт і накип.
Що таке легка вода
Легкою є вода, яка містить меншу концентрацію дейтерієвої води. Хтось намагається виготовити її вдома, а хтось купує. Як ми писали вище, важка вода є природним компонентом поверхневих і питних вод, які вживали наші предки. Яких-небудь підтверджених клінічних досліджень про терапевтичний ефект такої води не існує.
Чи можна очистити воду від дейтерію вдома?
Ніякі фільтри для води, зокрема системи зворотного осмосу не здатні затримувати дейтерієву воду, оскільки між частинками дейтерію і протію немає істотних відмінностей.
Ми вже писали в нашому блозі про очищення води заморожуванням. Теоретично цей метод здатний видалити певну кількість важкої води, але раціональність цих маніпуляцій залишається під питанням.
Теоретично цей метод здатний видалити певну кількість важкої води, але раціональність цих маніпуляцій залишається під питанням.
У цьому тексті ми спробували пояснити, що являє собою важка вода, де її шукати, і як з нею жити. Також сподіваємося, що вдалось розвіяти популярні псевдонаукові міфи та занепокоєння наших клієнтів та читачів.
Якщо у вас залишилися питання, пишіть в коментарях. З радістю дамо відповідь.
Оксид дейтерия — Американское химическое общество
- Вы здесь:
СКУД
Молекула недели
Молекула недели Архив
Архив — Д
- Оксид дейтерия
Молекула недели Архив
15 октября 2018 г.
Предыдущий
Далее
Я старший брат воды.
Какая я молекула?
Оксид дейтерия (D 2 O), также известный как «тяжелая вода», представляет собой форму воды, которая содержит два атома 2 H или D, изотоп. Термин «тяжелая вода» также используется для обозначения воды, в которой 2 атомов Н замещают лишь некоторые из 1 атомов Н. В этом случае быстрый обмен между двумя изотопами образует в два раза больше «полутяжелых» молекул HDO, чем D 2 O
Гарольд Юри, лауреат Нобелевской премии по химии 1934 года, был пионером в области химии дейтерия. В 1931 году он и его коллеги из Колумбийского университета (Нью-Йорк) тщательно перегнали 5 л жидкого азота, чтобы получить 1 мл молекулярного дейтерия. Вскоре после этого они выпустили D 2 О из обычной воды с помощью пролонгированного электролиза.
В течение десятилетий D 2 O был чрезвычайно полезен во многих химических применениях. Разница между скоростью реакции в растворителе D 2 O и H 2 O часто дает представление о механизме реакции. Это особенно важно, если вода является одним из реагентов.
Разница между скоростью реакции в растворителе D 2 O и H 2 O часто дает представление о механизме реакции. Это особенно важно, если вода является одним из реагентов.
В некоторых ядерных реакторах D 2 O используется для замедления нейтронов, чтобы они реагировали с делящимися 235 U вместо неделящегося 238 U, что устраняет необходимость в обогащении урана. D 2 O превосходит H 2 O для этого использования из-за его ≈6 раз большего сечения захвата тепловых нейтронов.
| Классификация СГС*: не опасное вещество или смесь |
*Глобально согласованная система классификации и маркировки химических веществ. Пояснения к пиктограммам.
Краткие сведения о оксиде дейтерия
Рег. CAS. № № | 7789-20-0 |
| Эмпирическая формула | Д 2 О |
| Молярная масса | 20,03 г/моль |
| Внешний вид | Бесцветная жидкость |
| Температура плавления | 3,8 °С |
| Точка кипения | 101,4 °С |
| Растворимость в воде | Смешивается |
Узнайте больше об этой молекуле из CAS, самого авторитетного и всеобъемлющего источника химической информации.
Молекула недели нуждается в ваших предложениях!
Если вашей любимой молекулы нет в нашем архиве, отправьте электронное письмо по адресу [email protected]. Молекула может быть примечательна своим текущим или историческим значением или по какой-либо причудливой причине. Благодарю вас!
Оставайтесь на шаг впереди химии
Узнайте, как ACS может помочь вам оставаться впереди в мире химии.
Узнайте больше
Определение и смысл тяжелой воды
- Верхние определения
- Викторина
- Примеры
- British
- Scientific
- Culatural
Это показано на уровне класса на основе уровня слов.
Сохрани это слово!
Показывает уровень оценки в зависимости от сложности слова.
сущ.
вода, в которой атомы водорода заменены дейтерием, используемая главным образом в качестве теплоносителя в ядерных реакторах.
ВИКТОРИНА
Сыграем ли мы в «ДОЛЖЕН» ПРОТИВ. «ДОЛЖЕН» ВЫЗОВ?
Должны ли вы пройти этот тест на «должен» или «должен»? Это должно оказаться быстрым вызовом!
Вопрос 1 из 6
Какая форма обычно используется с другими глаголами для выражения намерения?
Также называется оксидом дейтерия.
Происхождение тяжелой воды
Впервые зафиксировано в 1930–35 гг. хебдомад
Dictionary.com Полный текст
Основано на словаре Random House Unabridged Dictionary, © Random House, Inc. 2022
Как использовать тяжелую воду в предложении
Молекулы воды, состоящие из более тяжелого дейтерия вместо обычного водорода, достаточно прямо известны как тяжелая вода.
На Марсе гораздо больше воды, чем считалось ранее, но есть одна загвоздка|Джеффри Клюгер|16 марта 2021|Time
Фтор впервые попал в американское водоснабжение в результате довольно неизящной технократической схемы.
Противники фтора — антипрививочники|Майкл Шульсон|27 июля 2016|DAILY BEAST
Когда в начале 1900-х годов города начали добавлять хлор в систему водоснабжения, это вызвало общественный резонанс.
Anti-Fluoriders Are the OG Anti-Vaxxers|Michael Schulson|27 июля 2016|DAILY BEAST
До противников вакцинации были противники фторирования: добавлена группа, распространяющая страх перед средством против кариеса к питьевой воде.

Антифториды — антипрививочники OG|Майкл Шульсон|27 июля 2016 г.|DAILY BEAST
Фтор, добавленный в питьевую воду, может помочь людям, которые в противном случае не имеют доступа к стоматологической помощи.
Противники фтора — антипрививочники|Майкл Шульсон|27 июля 2016|DAILY BEAST
В тайне, перед референдумом, совет все равно фторировал воду.
Сторонники фтора — антипрививочники из прошлого|Майкл Шульсон|27 июля 2016 г.|DAILY BEAST
Городское вино открывает воду, которая не нуждается в извинениях, и придает изюминку худшему винтажу.
Pearls of Thought|Maturin M. Ballou
Две женщины не собирались купаться; они только что спустились на пляж, чтобы прогуляться и побыть наедине с водой.
Пробуждение и Избранные рассказы|Кейт Шопен
Миссис Вудбери пишет маслом и акварелью; последние представляют собой жанровые сцены, и среди них несколько голландских сюжетов.

Женщины в изобразительном искусстве, седьмой век до н.э. в двадцатый век нашей эры | Клара Эрскин Клемент
Полицейские выглядели скучными и тяжелыми, как будто никогда больше никто не будет преступником, и как будто они узнали это.
Белла Донна|Роберт Хиченс
Дрон: самая большая трубка волынки, дающая глухой тяжелый звук.
Gulliver’s Travels|Jonathan Swift
Определения тяжелой воды из Британского словаря
тяжелая вода
сущ.0019
Английский словарь Коллинза — полное и полное цифровое издание 2012 г.
© William Collins Sons & Co. Ltd., 1979, 1986 © HarperCollins
Publishers 1998, 2000, 2003, 2005, 2006, 2007, 2009, 2012
Научные определения тяжелой воды
тяжелая вода
Вода, в которой дейтерий, тяжелый изотоп водорода, заменяет водород. Тяжелая вода имеет такие же физические и химические свойства, как и обычная вода, но тяжелая вода на 10 процентов тяжелее и имеет более высокие температуры замерзания и кипения. Также называется оксидом дейтерия. Химическая формула: D2O. ♦ Полутяжелая вода похожа на тяжелую воду, но только один из двух атомов водорода в каждой молекуле заменен дейтерием. Химическая формула: ДГО.
Также называется оксидом дейтерия. Химическая формула: D2O. ♦ Полутяжелая вода похожа на тяжелую воду, но только один из двух атомов водорода в каждой молекуле заменен дейтерием. Химическая формула: ДГО.
Пристальный взгляд
Ядро большинства атомов водорода состоит из одного протона, но у одного изотопа водорода, называемого дейтерием или тяжелым водородом, ядро также содержит нейтрон и поэтому весит почти в два раза больше, чем стандартный водород. Вещество, называемое тяжелой водой, химически идентично обычной воде (h3O), за исключением того, что атомы водорода в молекуле представляют собой изотопы дейтерия (D2O). Тяжелая вода составляет небольшой процент (0,02%) естественной воды на Земле. Это отличный замедлитель ядерных реакций, замедляющий быстрые нейтроны, образующиеся в реакции ядерного деления, увеличивая вероятность того, что нейтроны успешно столкнутся с тяжелыми ядрами, вызывая дальнейшее деление. Хотя тяжелая вода химически почти идентична обычной воде, она примерно на десять процентов тяжелее и препятствует митозу клеток, если ее употреблять вместо обычной воды.