Исключение SiO2, который с водой не. Sio2 вода
SiO2 - это... Что такое SiO2?
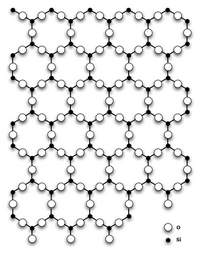
Кварц

Кварцевое стекло
Диокси́д кре́мния (оксид кремния (IV), кремнезём, SiO2) — бесцветные кристаллы, tпл 1713—1728 °C, обладают высокой твёрдостью и прочностью.
Свойства
Диоксид кремния имеет несколько полиморфных модификаций.
Самая распространенная из них на поверхности земли — α-кварц — кристаллизуется в тригональной сингонии
При нормальных условиях диоксид кремния чаще всего находится в полиморфной модификации α-кварца, которая при температуре выше 573 °C обратимо переходит в β-кварц.
При дальнейшем повышении температуры кварц переходит в тридимит и кристобалит. Эти полиморфные модификации устойчивы при высоких температурах и низких давлениях. При высоких температуре и давлении диоксид кремния сначала превращается в коэсит, а затем в стишовит (который впервые был обнаружен на месте эпицентра ядерного взрыва). Согласно некоторым исследованиям стишовит слагает значительную часть мантии, так что вопрос о том какая разновидность SiO2 наиболее распространена на Земле, пока не имеет однозначного ответа.Также имеет аморфную модификацию — кварцевое стекло.
Химические свойства
Диоксид кремния SiO2 — кислотный оксид, не реагирующий с водой.
Химически стоек к действию кислот, но реагирует с плавиковой кислотой:
SiO2 + 6HF → h3[SiF6] + 2h3O,
и газообразным фтороводородом HF:
SiO2 + 4HF → SiF4↑ + 2h3O.
Эти две реакции широко используют для травления стекла.
При сплавлении SiO2 с щелочами и основными оксидами, а также с карбонатами активных металлов образуются силикаты — соли не имеющих постоянного состава очень слабых, нерастворимых в воде кремниевых кислот общей формулы xh3O·ySiO2 (довольно часто в литературе упоминаются не кремниевые кислоты, а кремниевая кислота, хотя фактически речь при этом идет об одном и том же).
Например, может быть получен ортосиликат натрия:
SiO2 + 4NaOH → (2Na2O)·SiO2 + 2h3O,
метасиликат кальция:
SiO2 + СаО → СаО·SiO2,
или смешанный силикат кальция и натрия:
Na2CO3 + CaCO3 + 6SiO2 → Na2O·CaO·6SiO2 + 2CO2↑.
Из силиката Na2O·CaO·6SiO2 изготовляют оконное стекло.
Следует отметить, что большинство силикатов не имеет постоянного состава. Из всех силикатов растворимы в воде только силикаты натрия и калия. Растворы этих силикатов в воде называют растворимым стеклом. Из-за гидролиза эти растворы характеризуются сильно щелочной средой. Для гидролизованных силикатов характерно образование не истинных, а коллоидных растворов. При подкислении растворов силикатов натрия или калия выпадает студенистый белый осадок гидратированных кремниевых кислот.
Главным структурным элементом как твердого диоксида кремния, так и всех силикатов выступает группа [SiO4/2], в которой атом кремния Si окружен тетраэдром из четырех атомов кислорода О. При этом каждый атом кислорода соединен с двумя атомами кремния. Фрагменты [SiO4/2] могут быть связаны между собой по-разному. Среди силикатов по характеру связи в них фрагментов [SiO4/2] выделяют островные, цепочечные, ленточные, слоистые, каркасные и другие.
Получение
Синтетический диоксид кремния получают нагреванием кремния до температуры 400—500°C в атмосфере кислорода, при этом кремний окисляется до диоксида SiO2.
В лабораторный условиях синтетический диоксид кремния может быть получен действием кислот на силикатные соли. Например:
Na2SiO3 + 2Ch4COOH → 2Ch4COONa+h3SiO3,кремниевая кислота сразу разлагается на воду и SiO2, выпадающий в осадок.
Натуральный диоксид кремния в виде песка используется там, где не требуется высокая чистота материала.
Применение
Диоксид кремния применяют в производстве стекла, керамики, абразивов, бетонных изделий, для получения кремния, как наполнитель в производстве резин, при производстве кремнезёмистых огнеупоров, в хроматографии и др. Кристаллы кварца обладают пьезоэлектрическими свойствами и поэтому используются в радиотехнике, ультразвуковых установках, в зажигалках.
Диоксид кремния — главный компонент почти всех земных горных пород, в частности, кизельгура. Из кремнезёма и силикатов состоит 87% массы литосферы.
Аморфный непористый диоксид кремния применяется в пищевой промышленности в качестве вспомогательного вещества E551, препятствующего слёживанию и комкованию, парафармацевтике (зубные пасты), в фармацевтической промышленности в качестве вспомогательного вещества (внесён в большинство Фармакопей), а также пищевой добавки или лекарственного препарата в качестве энтеросорбента.
Искусственно полученные плёнки диоксида кремния используются в качестве изолятора при производстве микросхем и других электронных компонентов.
Также используется для производства волоконно-оптических кабелей. Используется чистый плавленый диоксид кремния с добавкой в него некоторых специальных ингредиентов.
Пористые кремнезёмы
Пористые кремнезёмы получают различными методами.
Силохром получают путём агрегирования аэросила, который, в свою очередь, получают сжиганием силана (Sih5). Силохром характеризуется высокой чистотой, низкой механической прочностью. Характерный размер удельной поверхности 60—120 м²/г. Применяется в качестве сорбента в хроматографии, наполнителя резин, катализе.
Силикагель получают путём высушивания геля кремневой кислоты. В сравнении с силохромом обладает меньшей чистотой, однако может обладать чрезвычайно развитой поверхностью: до 320 м²/г.
Кремниевый аэрогель приблизительно на 99,8 % состоит из воздуха может иметь плотность до 1,9 кг/м³ (всего в 1,5 раза больше плотности воздуха).
Wikimedia Foundation. 2010.
dic.academic.ru
Исключение SiO2, который с водой не — КиберПедия
Реагирует
2. Взаимодействие с кислотой или основанием:
-Основные оксиды-- при реакции с кислотой образуется соль и вода:
MgO + h3SO4 t= MgSO4 + h3O
CuO + 2HCl t= CuCl2 + h3O
-Кислотные оксиды-- при реакции с основанием образуется соль и вода:
CO2 + Ba(OH)2 =BaCO3 + h3O
SO2 + 2NaOH = Na2SO3 + h3O
Амфотерные оксиды взаимодействуют с кислотами как основные:
ZnO + h3SO4 = ZnSO4 + h3O
с основаниями как кислотные:
ZnO + 2NaOH + h3O = Na2[Zn(OH)4])
3. Взаимодействие основных и кислотных оксидов между собой приводит к солям.
Na2O + CO2 = Na2CO3
4. Восстановление до простых веществ:
3CuO + 2Nh4 = 3Cu + N2 + 3h3O
P2O5 + 5C = 2P + 5CO
4.Опишите классификацию и номенклатуру основания, приведите примеры
Основания классифицируются по растворимости и по кислотности
- растворимые в воде (щелочи)
М – IА и IIА, кроме Be и Mg
NaOH, Ca(OH)2 ;
- нерастворимые в воде
Ni(OH)2, Cr(OH)3
-oднокислотные: NaOH, KOH - двухкислотные: Ca(OH)2
-трёхкислотные: Fe(OH)3
НОМЕНКЛАТУРА ОСНОВАНИЙ
ГИДРОКСИД + Э(русское название, род. падеж) + (валентность Э)
NaOH – гидроксид натрия
Cr(OH)3 – гидроксид хрома (III)
Ba(OH)2 – гидроксид бария
Опишите способы получения оснований
1. Реакции активных металлов ( щелочных и щелочноземельных металлов) с водой:
2Na + 2h3O = 2NaOH + h3
Ca + 2h3O = Ca(OH)2 + h3
2. Взаимодействие оксидов активных металлов с водой:
BaO + h3O = Ba(OH)2
3. Электролиз водных растворов солей:
2NaCl + 2h3O = 2NaOH + h3 + Cl2
Опишите химические свойства оснований
ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ
Щелочи
1. Действие на индикаторы.
лакмус– синий
метилоранж - жёлтый
Нерастворимые основания
----
фенолфталеин - малиновый
2. Взаимодействие с кислотными оксидами.
2KOH + CO2 = K2CO3 + h3O ----
KOH + CO2 = KHCO3
3. Взаимодействие с кислотами (реакция нейтрализации)
NaOH + HNO3 = NaNO3 + h3 Cu(OH)2 + 2HCl = CuCl2 + 2h3O
4. Обменная реакция с солями
Ba(OH)2 + K2SO4 = 2KOH + BaSO4↓ ----
3KOH+Fe(NO3)3 = Fe(OH)3 ↓ + 3KNO3
5. Термический распад.
--- Cu(OH)2 t°= Cu2O + h3O
7.Опишите классификацию и номенклатуру кислот, приведите примеры
НОМЕНКАТУРА КИСЛОТ
1.БЕСКИСЛОРОДНЫЕ КИСЛОТЫ(Н+1 n Э -n )
Э + [o] + водородная кислота
HCl –хлороводородная кислота
HF –фтороводороная кислота
h3S –сероводородная кислота
h3Se –селеноводородная
2.КИСЛОРОДСОДЕРЖАЩИЕ КИСЛОТЫ(Н +1 Э +n О -2 )
а) Степень окисления Э = № группы
Э + [ная] кислота
[овая]
б) Степень окисления Э < № группы
Э + [истая] кислота
h3S+6O4 -cерная кислота
h3S+4O3 –сернистая кислота
h4As+5O4 –мышьяковая кислота
h4As+3O3 –мышьяковистая кислота
Опишите способы получения кислот
Получение кислот
1. Взаимодействие кислотного оксида с водой (для кислородсодержащих кислот):
SO3 + h3O = h3SO4
P2O5 + 3h3O =2h4PO4
2. Взаимодействие водорода с неметаллом и последующим растворением полученного продукта в воде (для бескислородных кислот):
h3 + Cl2 = 2HCl
h3 + S = h3S
3. Реакциями обмена соли с кислотой
Ba(NO3)2 + h3SO4 = BaSO4↓ + 2HNO3
в том числе, вытеснение слабых, летучих или малорастворимых кислот из солей более сильными кислотами:
Na2SiO3 + 2HCl = h3SiO3↓ + 2NaCl
2NaCl(тв.) + h3SO4(конц.) t°= Na2SO4 + 2HCl
Опишите химические свойства кислот

10.Опишите классификацию и номенклатуру солей, приведите примеры
КЛАССИФИКАЦИЯ
1. Средние (нормальные) – продукт полного замещения атомов водорода в кислоте на металл
а) соли кислородсодержащих кислот
Н2SO4 → Na2SO4 – сульфат натрия
Н2SO3 → Na2SO3 – сульфит натрия
б) соли бескислородных кислот
HCl → KCl - хлорид калия


4. Двойные соли состоят из ионов двух разных металлов и кислотного остатка.
KNaCO3 – калий натрий карбонат
5. Смешанные соли – содержат один ион металла и анионы двух кислот.
AlCl(SO4) – алюминий хлорид сульфат.
6. Комплексные соли состоят из сложных (комплексных) ионов
[Ag(Nh4)2] Cl
cyberpedia.su
Кремний IV оксид
Кремний IV оксид ТУ 6-09-3379-79
SiO2
Диоксид кремния (кремнезём, SiO2; лат. silica) — оксид кремния (IV). Бесцветные кристаллы с температурой плавления+1713…+1728 °C, обладающие высокой твёрдостью и прочностью.
Диоксид кремния — главный компонент почти всех земных горных пород, в частности, кизельгура. Из кремнезёма и силикатов состоит 87 % массы литосферы. В крови и плазме человека концентрация кремнезёма составляет 0,001 % по массе.
|
оксид кремния(IV) |
|
кремнезём |
|
O₂Si |
|
1 600°C |
|
2 950°C °C |
|
0±1 мм рт. ст. |
Свойства
- Относится к группе кислотных оксидов.
- При нагревании взаимодействует с основными оксидами и щелочами.
- Реагирует с плавиковой кислотой.
- SiO2 относится к группе стеклообразующих оксидов, то есть склонен к образованию переохлажденного расплава — стекла.
- Один из лучших диэлектриков (электрический ток не проводит, если не имеет примесей и не нагревается).
Полиморфизм
Диоксид кремния имеет несколько полиморфных модификаций.
Самая распространённая из них на поверхности земли — α-кварц — кристаллизуется в тригональной сингонии. При нормальных условиях диоксид кремния чаще всего находится в полиморфной модификации α-кварца, которая при температуре выше +573 °C обратимо переходит в β-кварц. При дальнейшем повышении температуры кварц переходит в тридимит и кристобалит. Эти полиморфные модификации устойчивы при высоких температурах и низких давлениях.
В природе также встречаются формы — опал, халцедон, кварцин, лютецит, аутигенный кварц, которые относятся к группе кремнезёма. Опал (SiO2*nh3O) в шлифе бесцветен, изотропен, имеет отрицательный рельеф, отлагается в морских водоемах, входит в состав многих кремнистых пород. Халцедон, кварцин, лютецит — SiO2 — представляют собой скрытокристаллические разновидности кварца. Образуют волокнистые агрегаты, розетки, сферолиты, бесцветные, голубоватые, желтоватые. Отличаются между собой некоторыми свойствами — у халцедона и кварцина — прямое погасание, у лютецита — косое, у халцедона — отрицательное удлинение.
При высоких температуре и давлении диоксид кремния сначала превращается в коэсит (который в 1953 году был синтезирован американским химиком Лорингом Коэсом), а затем в стишовит (который в 1961 году был синтезирован С. М. Стишовым, а в 1962 году был обнаружен в метеоритном кратере)[источник не указан 2294 дня]. Согласно некоторым исследованиям, стишовит слагает значительную часть мантии, так что вопрос о том, какая разновидность SiO2 наиболее распространена на Земле, пока не имеет однозначного ответа.
Также имеет аморфную модификацию — кварцевое стекло.
Химические свойства
Диоксид кремния SiO2 — кислотный оксид, не реагирующий с водой.
Химически стоек к действию кислот, но реагирует с газообразным фтороводородом:

и плавиковой кислотой:
![{\mathsf {SiO_{2}+6HF\rightarrow H_{2}[SiF_{6}]+2H_{2}O}}](/800/600/https/wikimedia.org/api/rest_v1/media/math/render/svg/13b99cb061378a488154c85d2b6585eaba673596)
Эти две реакции широко используют для травления стекла.
При сплавлении SiO2 с щелочами и основными оксидами, а также с карбонатами активных металлов образуются силикаты — соли не имеющих постоянного состава очень слабых, нерастворимых в воде кремниевых кислот общей формулы xh3O·ySiO2 (довольно часто в литературе упоминаются не кремниевые кислоты, а кремниевая кислота, хотя фактически речь при этом идет об одном и том же веществе).
Например, может быть получен ортосиликат натрия:

метасиликат кальция:

или смешанный силикат кальция и натрия:

Из силиката Na2CaSi6O14 (Na2O·CaO·6SiO2) изготовляют оконное стекло.
Большинство силикатов не имеет постоянного состава. Из всех силикатов растворимы в воде только силикаты натрия и калия. Растворы этих силикатов в воде называют жидким стеклом. Из-за гидролиза эти растворы характеризуются сильно щелочной средой. Для гидролизованных силикатов характерно образование не истинных, а коллоидных растворов. При подкислении растворов силикатов натрия или калия выпадает студенистый белый осадок гидратированных кремниевых кислот.
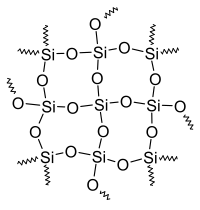
Главным структурным элементом как твердого диоксида кремния, так и всех силикатов, выступает группа [SiO4/2], в которой атом кремния Si окружен тетраэдром из четырёх атомов кислорода О. При этом каждый атом кислорода соединен с двумя атомами кремния. Фрагменты [SiO4/2] могут быть связаны между собой по-разному. Среди силикатов по характеру связи в них фрагментов [SiO4/2] выделяют островные, цепочечные, ленточные, слоистые, каркасные и другие.
Получение
Синтетический диоксид кремния получают нагреванием кремния до температуры +400…+500 °C в атмосфере кислорода, при этом кремний окисляется до диоксида SiO2. А также термическим оксидированием при больших температурах.
В лабораторных условиях синтетический диоксид кремния может быть получен действием кислот, даже слабой уксусной, на растворимые силикаты. Например:

кремниевая кислота сразу распадается на воду и SiO2, выпадающий в осадок.
Натуральный диоксид кремния в виде песка используется там, где не требуется высокая чистота материала.
Применение
Диоксид кремния применяют в производстве стекла, керамики, абразивов, бетонных изделий, для получения кремния, как наполнитель в производстве резин, при производстве кремнезёмистых огнеупоров, в хроматографии и др. Кристаллы кварца обладают пьезоэлектрическими свойствами и поэтому используются в радиотехнике, ультразвуковых установках, в зажигалках.Аморфный непористый диоксид кремния применяется в пищевой промышленности в качестве вспомогательного вещества E551, препятствующего слёживанию и комкованию, парафармацевтике (зубные пасты), в фармацевтической промышленности в качестве вспомогательного вещества (внесён в большинство Фармакопей), а также пищевой добавки или лекарственного препарата в качестве энтеросорбента.
Искусственно полученные плёнки диоксида кремния используются в качестве изолятора при производстве микросхем и других электронных компонентов.
Также используется для производства волоконно-оптических кабелей. Используется чистый плавленый диоксид кремния с добавкой в него некоторых специальных ингредиентов.
Кремнезёмная нить также используется в нагревательных элементах электронных сигарет, так как хорошо впитывает жидкость и не разрушается под нагревом спирали.
Крупные прозрачные кристаллы кварца используются в качестве полудрагоценных камней; бесцветные кристаллы называют горным хрусталём, фиолетовые — аметистами, жёлтые — цитрином.
В микроэлектронике диоксид кремния является одним из основных материалов. Его применяют в качестве изолирующего слоя, а также в качестве защитного покрытия. Получают в виде тонких плёнок термическим окислением кремния, химическим осаждением из газовой фазы, магнетронным распылением.
Пористые кремнезёмы
Пористые кремнезёмы получают различными методами.
Силохром получают путём агрегирования аэросила, который, в свою очередь, получают сжиганием силана (Sih5). Силохром характеризуется высокой чистотой, низкой механической прочностью. Характерный размер удельной поверхности 60—120 м²/г. Применяется в качестве сорбента в хроматографии, наполнителя резин, катализе.
Силикагель получают путём высушивания геля кремниевой кислоты. В сравнении с силохромом обладает меньшей чистотой, однако может обладать чрезвычайно развитой поверхностью: обычно от 300 м²/г до 700 м²/г .
Кремниевый аэрогель приблизительно на 99,8 % состоит из воздуха и может иметь плотность до 1,9 кг/м³ (всего в 1,5 раза больше плотности воздуха).
himmax.ru
свойства, получение и применение :: SYL.ru
Введение
В вашей квартире ремонт, и необходимо купить керамическую плитку. В магазине, долго перебирая различные варианты форм и расцветок, вы нашли подходящую и, направляясь к кассе, мельком взглянули на ту часть упаковки с плиткой, где написан ее состав. Почти все ингредиенты знакомы, но один из них вызвал у вас удивление - оксид кремния. Естественно, вы захотите узнать о нем побольше. Сегодня я постараюсь удовлетворить ваш интерес.
 Определение
Определение
Кремний имеет переменную валентность, и из-за этого в химии известно два его соединения с кислородом. Сегодня мы рассмотрим высший оксид кремния, в котором последний имеет валентность IV.
Название
В разных источниках его могут обозвать диоксидом кремния, кремнезёмом или оксидом силиция.
Свойства
Он является кислотным оксидом, которому присущи твердость и прочность. Если нагреть его и любую щелочь/основный оксид, то они будут взаимодействовать друг с другом. Это соединение кремния - стеклообразующее, т. е. из него может получиться переохлажденный расплав - стекло.  Также (в чистом виде) он не пропускает электрический ток (является диэлектриком). У оксида кремния атомная кристаллическая решетка. Он является стойким к воздействию кислот, однако исключение составляют плавиковая и газообразный фтороводород. Продукты реакции с последним - фторид кремния и вода. Если же второй реагент - раствор фтороводорода, то ее продуктами будут гексафторкремниевая кислота и та же вода. Если оксид кремния (IV) сплавить с щелочью/основным оксидом/карбонатом любого активного металла, продуктом реакции станет соль кремниевых кислот - силикат, из них растворимы только силикаты калия и натрия. Продукты взаимодействия любого из последних с водой носят название жидкого стекла. У них сильно щелочная среда, причина этому - гидролиз. Гидролизованные силикаты образуют не истинные, а коллоидные растворы. Если растворы силикатов калия или натрия немного окислить, произойдет выпадение студенистого белого осадка, который составляют гидратированные кремниевые кислоты.
Также (в чистом виде) он не пропускает электрический ток (является диэлектриком). У оксида кремния атомная кристаллическая решетка. Он является стойким к воздействию кислот, однако исключение составляют плавиковая и газообразный фтороводород. Продукты реакции с последним - фторид кремния и вода. Если же второй реагент - раствор фтороводорода, то ее продуктами будут гексафторкремниевая кислота и та же вода. Если оксид кремния (IV) сплавить с щелочью/основным оксидом/карбонатом любого активного металла, продуктом реакции станет соль кремниевых кислот - силикат, из них растворимы только силикаты калия и натрия. Продукты взаимодействия любого из последних с водой носят название жидкого стекла. У них сильно щелочная среда, причина этому - гидролиз. Гидролизованные силикаты образуют не истинные, а коллоидные растворы. Если растворы силикатов калия или натрия немного окислить, произойдет выпадение студенистого белого осадка, который составляют гидратированные кремниевые кислоты.
Получение
В промышленности оксид кремния получают, нагревая кремний в кислородной среде. Он окисляется и образует искомый продукт. Также его добывают при помощи термического оксидирования. В лаборатории оксид кремния получают при действии любых кислот на растворимый силикат, для этого подходит даже слабая уксусная. К примеру, если соединить ее и силикат натрия, продуктом реакции станет ацетат натрия и кремниевая кислота. Тут же произойдет разложение последней, и продуктами ее распада станут вода и искомый оксид.
 Применение
Применение
С помощью оксида кремния производят стекло, керамику, абразивы, бетонные изделия, а также получают сам кремний. Еще он выполняет роль наполнителя в отрасли производства резины. Кристаллы аморфной модификации оксида кремния - кварцевого стекла - имеют пьезоэлектрические свойства, и этим пользуются создатели радиотехники, ультразвуковых установок и зажигалок. Силикаты и кремнезёмы - почти 90% массы литосферы. Также оксид кремния известен как пищевая добавка E551. Это его аморфная непористая разновидность. Она предотвращает слеживание и комкование пищи, в фармацевтике используется как вспомогательное вещество и лекарственный препарат-энтеросорбент. Пленки данного оксида служат изолятором, когда производят микросхемы и другие электронные компоненты. Также с их помощью создают волоконно-оптические кабели. А нагревательные элементы электронной сигареты были бы невозможны без кремнезёмной нити.
Заключение
Вот как широко используется данный оксид. И чтобы увидеть его, не нужно бежать в магазин и любопытства ради рассматривать цемент и бетон. Природный оксид кремния находится у нас под ногами - это обыкновенный песок. Оказывается, и он может быть полезным.
www.syl.ru
Оксид кремния (IV) - это... Что такое Оксид кремния (IV)?

Кварц

Кварцевое стекло
Диокси́д кре́мния (оксид кремния (IV), кремнезём, SiO2) — бесцветные кристаллы, tпл 1713—1728 °C, обладают высокой твёрдостью и прочностью.
Свойства
Диоксид кремния имеет несколько полиморфных модификаций.
Самая распространенная из них на поверхности земли — α-кварц — кристаллизуется в тригональной сингонии
При нормальных условиях диоксид кремния чаще всего находится в полиморфной модификации α-кварца, которая при температуре выше 573 °C обратимо переходит в β-кварц.
При дальнейшем повышении температуры кварц переходит в тридимит и кристобалит. Эти полиморфные модификации устойчивы при высоких температурах и низких давлениях. При высоких температуре и давлении диоксид кремния сначала превращается в коэсит, а затем в стишовит (который впервые был обнаружен на месте эпицентра ядерного взрыва). Согласно некоторым исследованиям стишовит слагает значительную часть мантии, так что вопрос о том какая разновидность SiO2 наиболее распространена на Земле, пока не имеет однозначного ответа.Также имеет аморфную модификацию — кварцевое стекло.
Химические свойства
Диоксид кремния SiO2 — кислотный оксид, не реагирующий с водой.
Химически стоек к действию кислот, но реагирует с плавиковой кислотой:
SiO2 + 6HF → h3[SiF6] + 2h3O,
и газообразным фтороводородом HF:
SiO2 + 4HF → SiF4↑ + 2h3O.
Эти две реакции широко используют для травления стекла.
При сплавлении SiO2 с щелочами и основными оксидами, а также с карбонатами активных металлов образуются силикаты — соли не имеющих постоянного состава очень слабых, нерастворимых в воде кремниевых кислот общей формулы xh3O·ySiO2 (довольно часто в литературе упоминаются не кремниевые кислоты, а кремниевая кислота, хотя фактически речь при этом идет об одном и том же).
Например, может быть получен ортосиликат натрия:
SiO2 + 4NaOH → (2Na2O)·SiO2 + 2h3O,
метасиликат кальция:
SiO2 + СаО → СаО·SiO2,
или смешанный силикат кальция и натрия:
Na2CO3 + CaCO3 + 6SiO2 → Na2O·CaO·6SiO2 + 2CO2↑.
Из силиката Na2O·CaO·6SiO2 изготовляют оконное стекло.
Следует отметить, что большинство силикатов не имеет постоянного состава. Из всех силикатов растворимы в воде только силикаты натрия и калия. Растворы этих силикатов в воде называют растворимым стеклом. Из-за гидролиза эти растворы характеризуются сильно щелочной средой. Для гидролизованных силикатов характерно образование не истинных, а коллоидных растворов. При подкислении растворов силикатов натрия или калия выпадает студенистый белый осадок гидратированных кремниевых кислот.
Главным структурным элементом как твердого диоксида кремния, так и всех силикатов выступает группа [SiO4/2], в которой атом кремния Si окружен тетраэдром из четырех атомов кислорода О. При этом каждый атом кислорода соединен с двумя атомами кремния. Фрагменты [SiO4/2] могут быть связаны между собой по-разному. Среди силикатов по характеру связи в них фрагментов [SiO4/2] выделяют островные, цепочечные, ленточные, слоистые, каркасные и другие.
Получение
Синтетический диоксид кремния получают нагреванием кремния до температуры 400—500°C в атмосфере кислорода, при этом кремний окисляется до диоксида SiO2.
В лабораторный условиях синтетический диоксид кремния может быть получен действием кислот на силикатные соли. Например:
Na2SiO3 + 2Ch4COOH → 2Ch4COONa+h3SiO3,кремниевая кислота сразу разлагается на воду и SiO2, выпадающий в осадок.
Натуральный диоксид кремния в виде песка используется там, где не требуется высокая чистота материала.
Применение
Диоксид кремния применяют в производстве стекла, керамики, абразивов, бетонных изделий, для получения кремния, как наполнитель в производстве резин, при производстве кремнезёмистых огнеупоров, в хроматографии и др. Кристаллы кварца обладают пьезоэлектрическими свойствами и поэтому используются в радиотехнике, ультразвуковых установках, в зажигалках.
Диоксид кремния — главный компонент почти всех земных горных пород, в частности, кизельгура. Из кремнезёма и силикатов состоит 87% массы литосферы.
Аморфный непористый диоксид кремния применяется в пищевой промышленности в качестве вспомогательного вещества E551, препятствующего слёживанию и комкованию, парафармацевтике (зубные пасты), в фармацевтической промышленности в качестве вспомогательного вещества (внесён в большинство Фармакопей), а также пищевой добавки или лекарственного препарата в качестве энтеросорбента.
Искусственно полученные плёнки диоксида кремния используются в качестве изолятора при производстве микросхем и других электронных компонентов.
Также используется для производства волоконно-оптических кабелей. Используется чистый плавленый диоксид кремния с добавкой в него некоторых специальных ингредиентов.
Пористые кремнезёмы
Пористые кремнезёмы получают различными методами.
Силохром получают путём агрегирования аэросила, который, в свою очередь, получают сжиганием силана (Sih5). Силохром характеризуется высокой чистотой, низкой механической прочностью. Характерный размер удельной поверхности 60—120 м²/г. Применяется в качестве сорбента в хроматографии, наполнителя резин, катализе.
Силикагель получают путём высушивания геля кремневой кислоты. В сравнении с силохромом обладает меньшей чистотой, однако может обладать чрезвычайно развитой поверхностью: до 320 м²/г.
Кремниевый аэрогель приблизительно на 99,8 % состоит из воздуха может иметь плотность до 1,9 кг/м³ (всего в 1,5 раза больше плотности воздуха).
Wikimedia Foundation. 2010.
dic.academic.ru



















