Буферные растворы Буферные растворы. Буферизация воды
Буферные растворы Буферные растворы
Одним из основных свойств живых организмов является поддержание кислотно-основного гомеостаза на определенном уровне. Протолитический гомеостаз – постоянство рН биологических жидкостей, тканей и органов. Это находит выражение в достаточно постоянных значениях рН биологических сред (крови, слюны, желудочного сока и т.д.) и способности организма восстанавливать нормальные значения рН при воздействии протолитов. Система, поддерживающая протолитический гомеостаз, включает в себя не только физиологические механизмы (легочную и почечную компенсацию), но и физико-химические: буферное действие, ионный обмен и диффузию.
Буферными растворами называются растворы, сохраняющие неизменными значения рН при разбавлении или добавлении небольшого количества сильной кислоты или основания. Протолитические буферные растворы представляют смеси электролитов, содержащие одноимённые ионы.
Различают в основном протолитические буферные растворы двух типов:
Кислотные т.е. состоящие из слабой кислоты и избытка сопряженного с ней основания (соли, образованной сильным основанием и анионом этой кислоты). Например: СН3СООН и СН3СООNa - ацетатный буфер
СН3СООН + Н2О ↔ Н3О+ + СН3СОО- избыток сопряженного
кислота
основания
СН3СООNa → Na+ + Ch4COO-
Основные, т.е. состоящие из слабого основания и избытка сопряженной с ним кислоты (т.е. соли, образованной сильной кислотой и катионом этого основания). Например: Nh5OH и Nh5Cl – аммиачный буфер.
Nh4 + h3O ↔ OH- + Nh5+ избыток
Основание
сопряженной
Nh5Cl → Cl- + Nh5+ кислоты
Уравнение буферной системы рассчитывается по формуле Гендерсона-Гассельбаха:
рН = рК + ℓg 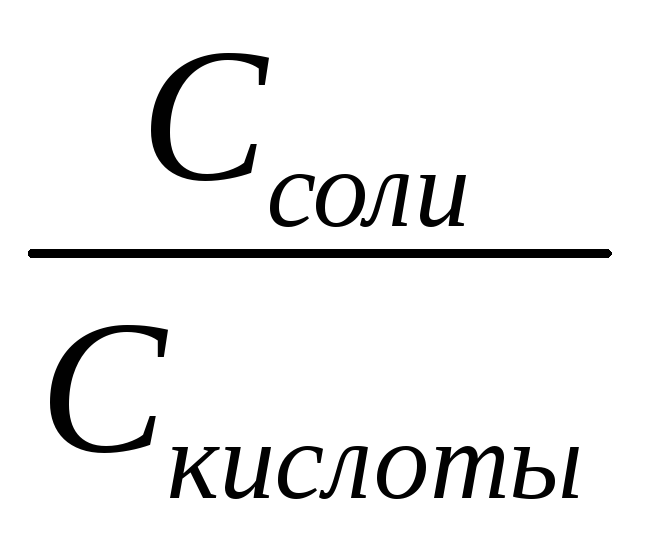 , pOH = pK + ℓg
, pOH = pK + ℓg ,
,
где рК = -ℓg КД.
С – молярная или эквивалентная концентрация электролита (C = V N)
Механизм действия буферных растворов
Рассмотрим его на примере ацетатного буфера: СН3СООН + СН3СООNa
Высокая концентрация ацетат-ионов обусловлена полной диссоциацией сильного электролита – ацетата натрия, а уксусная кислота в присутствии одноименного аниона существует в растворе практически в неионизированном виде.
При добавлении небольшого количества хлороводородной кислоты, ионы Н+ связываются с имеющимся в растворе сопряженным основанием СН3СОО- в слабый электролит СН3СООН.
Ch4COO‾ +H + ↔ Ch4COOH (1)
Из уравнения (1) видно, что сильная кислота НС1 заменяется эквивалентным количеством слабой кислоты СН3СООН. Количество СН3СООН увеличивается и по закону разбавления В. Оствальда степень диссоциации уменьшается. В результате этого концентрация ионов Н+ в буфере увеличивается, но очень незначительно. рН сохраняется постоянным.
При добавлении кислоты к буферу рН определяется по формуле:
рН = рК + ℓg 
При добавлении к буферу небольшого количества щелочи протекает реакция её с СН3СООН. Молекулы уксусной кислоты будут реагировать с гидроксид-ионами с образованием Н2О и СН3СОО ‾:
Ch4COOН + OH ‾ ↔ Ch4COO‾ + h3O (2)
В результате этого щелочь заменяется эквивалентным количеством слабоосновной соли Ch4COONa. Количество СН3СООН убывает и по закону разбавления В. Оствальда степень диссоциации увеличивается за счет потенциальной кислотности оставшихся недиссоциированных молекул СН3СООН. Следовательно, концентрация ионов Н+ практически не изменяется. рН остаётся постоянным.
При добавлении щелочи рН определяется по формуле:
рН = рК + ℓg 
При разбавлении буфера рН также не меняется, т.к. константа диссоциации и соотношение компонентов при этом остаются неизменными.
Таким образом, рН буфера зависит от: константы диссоциации и соотношения концентрации компонентов. Чем эти величины больше, тем больше рН буфера. рН буфера будет наибольшим при соотношении компонентов равным единице.
Для количественной характеристики буфера вводится понятие буферной ёмкости.
studfiles.net
Буферизация кокосового субстрата - Почва и субстраты - Публикации - Статьи
Кокосовый субстрат обладает большой популярностью среди садоводов. Высокая влагоемкость и гидрофобность (прим.: легко отдает влагу растениям), высокая воздухопроницаемость, в кокосе могут жить микроорганизмы, это полностью органический и экологически безопасный продукт с весьма долгим сроком эксплуатации, до 5 лет. Буквально идеальный субстрат.
Единственный факт, омрачающий его уникальные свойства, в том, что кокос поглощает кальций и магний и имеет повышенную концентрацию калия и натрия. Более подробно со свойствами кокосового субстрата можно ознакомиться тут.
В данной статье мы разберемся почему кокос так себя ведёт, так ли уж это плохо с точки зрения садоводства и что можно сделать, что бы кокос не был таким «жадным» до питательных веществ.

Кратко о химии ионного обмена
Минеральные удобрения являются растворами солей. Но растения могут их поглотить только в ионной форме. Попадая в воду, кристаллическая структура солей удобрений растворяется, и остаются только положительные и отрицательные ионы. Теперь растение готово их «съесть».
В нормальных условиях концентрация ионов внутри корней выше, чем в питательном растворе, поэтому вода проталкивается через клеточную мембрану посредством осмотического давления. И поскольку в химии все идет по направлению к точке максимального равновесия, вода будет перемещаться со стороны более низкой концентрации ионов в сторону более высокой. И пока вода проталкивается в растение, ионы буквально захватываются им. Часть ионов является микро и макроэлементами, которые были поглощены растением, а другая часть – H+ и OH-, образовавшихся в результате диссоциации воды. Так как каждый ион в растворе имеет свой собственный заряд, растение не может просто их забрать, иначе равновесие будет нарушено. Поэтому оно заменяет их равнозначным количеством H+ и OH-. Например, калий (К+) заменяется на Н+; кальций (Са++), магний (Mg++) – на 2 молекулы Н+; нитраты (NO3-) – на молекулу OH- и т.д.
Таким образом, равновесие электрического заряда остается прежним, а корни выпускают H+ или OH-, что, кстати, и приводит к изменениям уровня pH раствора.

Так почему же кокос удерживает кальций и магний?
Кокосовый субстрат характеризуется высоким содержанием коллоидов – некристаллизующееся вещество, растворы которого не проходят через клеточные мембраны. Наличие коллоидов обуславливает высокую емкость катионного обмена (ЕКО). Коллоид можно представить как большую сферу с отрицательно заряженной поверхностью. За счет этого коллоиды способны связывать огромное количество катионов (прим.: положительно заряженных ионов). Сильнее поглощаются двухвалентные катионы (Са++, Mg++), слабее одновалентные (К+, Na+, Nh5). Именно поэтому бытует мнение, что «кокос поглощает кальций и магний» и садоводы полагают, что для выращивания в кокосе необходим дополнительный кальций и магний. Хотя на деле растениям нужно такое же количество питательных веществ, что и при выращивании в других субстратах. Все дело в ЕКО.
ЕКО означает способность субстрата обмениваться положительно заряженными ионами как с раствором удобрений, так и с корнями. Коллоиды будут удерживать катионы до тех пор, пока ЕКО не будет заполнен полностью, т.е. коллоиды достигнут равновесия с раствором удобрений. Поэтому данное свойство кокоса не является ни хорошим и не плохим. Просто следует с ним считаться.
По сути, обладая высоким ЕКО, кокос является буфером для удобрений. Полив кокосового субстрата чистой водой приведет к высвобождению катионов. А полив раствором с высоким PPM к тому, что коллоиды будут вынуждены связывать большее количество катионов. Так что главное правильно заполнять ЕКО.

Подготовка кокоса к использованию
Изначально ЕКО кокоса содержит калий (K) и натрий (Na), и практически не содержит кальций (Ca) или магний (Mg). Эти четыре катиона – важнейшие в буферизации кокоса. Цель буферизации – значительно снизить в ЕКО долю K и Na и увеличить долю Ca и Mg.
Первая рекомендация – покупайте кокосовый субстрат у проверенного производителя. Ознакомьтесь с описанием, качественный продукт уже буферизирован в процессе производства, и его подготовка займет меньше времени и усилий.
Самым оптимальным способом является вариант буферизации кокосового субстрата раствором удобрений, которые вы планируете применять в дальнейшем процессе выращивания. То есть при размачивании кокоса будет использоваться не вода, а раствор удобрений.
Если такое применение удобрений для вас слишком расточительно, то можно использовать эконом вариант. В этом случае для замачивания кокоса вам понадобится кальциевая селитра и сульфат магния.
Если используемый кокос сомнительного качества, то перед буферизацией его надо обязательно промыть осмотической водой и отжать, и буферизировать исключительно раствором удобрений.
Уровень электропроводимости полученного буферного раствора (не зависимо от того, что вы используете удобрения или порошки кальциевой селитры и сульфата магния) должен быть около 1ЕС или 500-700 ppm. Время замачивания кокоса в растворе – 10-15 минут, этого достаточно для осуществления катионного обмена, дальнейшее замачивание не даст больших результатов, так как скорость обмена упадет.
Температура окружающей среды при буферизации должна быть не ниже 17-18°С, температура раствора около 20°С. При более низкой температуре замещение катионов будет происходить медленнее.

Подводя итог, скажем, что процесс буферизации кокосового субстрата выглядит примерно так:
1) Подготавливаем воду для буферного раствора. Используйте только чистую воду, не речную, не талый снег, ничего подобного. Если вода из-под крана, то дайте ей обязательно отстояться пару дней и слейте. Воду со дна емкости, в которой она отстаивалась не использовать! Если есть фильтр, отфильтруйте воду.
2) Вскрываем упаковку кокосового субстрата.
3) Рассчитываем объем буферного раствора, который необходим для получения нужного количества субстрата. То есть, например, если на упаковке написано «Необходимо 4 литра воды, чтобы получить 11 литров высококачественного кокосового субстрата», то это тот объем буферного раствора, который вы должны приготовить (а желательно даже чуть больше).
4) Помещаем кокос в емкость, в которой он будет замачиваться. Учитываем, что кокос при размачивании сильно увеличивается в объеме, и также в эту емкость должен поместиться весь объем буферного раствора. Если кокос не очень качественный не забываем предварительно промыть его осмосом.
5) Замешиваем буферный раствор.
5.1. Выровняйте уровень рН воды, которую будете использовать для приготовления раствора.
5.2. Если вы готовите буферный раствор с применением удобрений, то добавьте в воду необходимое количество удобрений, следуя пропорциям для вегетативной фазы указанным производителем.
5.3. Если используете вариант с селитрой кальция и сульфатом магния, то сначала в одной емкости разведите кальциевую селитру из расчета 25 г на 15 л воды, затем в другой емкости – сульфат магния, также 25 г на 15 л воды. И только потом смешайте оба раствора. В сухом виде порошки не смешивать!
6) Замерьте уровень электропроводимости полученного буферного раствора. Он должен равняться 1ЕС или 500-700 ppm. Если он значительно ниже, повысьте концентрацию удобрений.
7) Залейте сухой (или уже промытый осмосом) кокосовый субстрат полученным буферным раствором и оставьте вымачиваться на 10-15 минут.
8) Дайте излишкам раствора стечь, можно немного отжать субстрат.
9) Кокос буферизирован и готов к дальнейшему применению.
Другие статьи про кокосовый субстрат:
Кокосовый субстрат в качестве почвы
Статья из блога DzagiGrow

dzagi.site
Что такое буферизация: подробная информация
Буферизация – это способ организации обмена, а именно ввода и вывода данных в вычислительных устройствах и компьютерах. Буфер используется как место для временного хранения данных. Во время ввода данных одни устройства производят запись данных в буфер, в то время как другие производят чтение данных из буфера. При выводе все с точностью до наоборот.
Где мы встречаемся с буферизацией?
 Фактически все процессы в ПК связаны с этим процессом. Неинформированному человеку нелегко понять, что такое буферизация. Однако наблюдать ее очень просто: та же загрузка фильма онлайн - происходит буферизация данных, фильм загружается в КЭШ и воспроизводится, хотя его на компьютере и нет.
Фактически все процессы в ПК связаны с этим процессом. Неинформированному человеку нелегко понять, что такое буферизация. Однако наблюдать ее очень просто: та же загрузка фильма онлайн - происходит буферизация данных, фильм загружается в КЭШ и воспроизводится, хотя его на компьютере и нет.
Операция эта позволяет процессам выполнять ввод и вывод данных независимо друг от друга. Благодаря такой своей полезности, буферизация используется в многофункциональных ОС.
Несколько ее видов применяются в компьютерной графике для ввода, вывода и обработки изображения. Их реализация происходит аппаратно или программно.
Примером буферизации в аппаратном обеспечении служит оперативная память модема, которая используется для временного хранения получаемых и отсылаемых файлов.Примером буферизации в программном обеспечении являются многозадачные ОС, в них при вводе данных на печать происходит временная закачка файлов в очереди печати.
Продвинутым пользователям ПК необходимо знать, что такое буферизация.В сфере информационных технологий всегда существует поверхностная информация и углубленная. Разобравшись, что такое буферизация, можно пойти дальше и рассмотреть детальней сами ее виды.
Известно, что существует двойная и тройная буферизация. О них пойдет речь в следующем подзаголовке.
Тройная буферизация - что это такое?
 В компьютерной графике данный вид обсуждаемого процесса представляет собой разновидность двойной буферизации. Разница лишь в методе вывода изображений. Тройная позволяет избежать или уменьшить число артефактов. Также различия между двойной и тройной буферизацией наблюдаются и в скорости вывода изображения.
В компьютерной графике данный вид обсуждаемого процесса представляет собой разновидность двойной буферизации. Разница лишь в методе вывода изображений. Тройная позволяет избежать или уменьшить число артефактов. Также различия между двойной и тройной буферизацией наблюдаются и в скорости вывода изображения.
Методом тройной буферизации также является синхронизация с частотой обновления экрана. Третий буфер здесь используется как метод предоставления свободного пространства для запросов на изменение в общем объёме выводимой графики. Он действует как своего рода хранилище. Метод тройной буферизации требует больше ресурсов, но обеспечивает согласованную частоту кадров.
Три буфера - это не предельное количество. Однако необходимости в 4 и более местах для временного хранения закачиваемых файлов нет, активно работать всегда будут только 3 из них. Поэтому оптимальный вариант – тройная буферизация.
Рассмотрим, что такое буферизация в играх?
 Для передачи изображения игр также используется буферизация. В играх используется как двойная, так и тройная. Двойная буферизация предназначена для более слабых ПК и ОС, в то время как тройная - для более мощных.
Для передачи изображения игр также используется буферизация. В играх используется как двойная, так и тройная. Двойная буферизация предназначена для более слабых ПК и ОС, в то время как тройная - для более мощных.
Если использовать тройную буферизацию на слабой ОС, игра может глючить. Иными словами, от того, какого вида процесс используется на вашем компьютере, зависит производительность. Игры тоже бывают разные, с разными требованиями к ПК и ОС.
Подбирать вид буферизации достаточно сложно, так как производители игр создают свое детище, используя разнообразные методы. Поэтому на игровых форумах можно часто слышать о том, как определенная игра плохо работает с тройной буферизацией, и наоборот.
В идеале, производители должны указывать системные требования конкретной игры, её совместимость с различными ОС, поддержка буферизации и т. д.
В случае если производитель не дал конкретной информации по поводу совместимости, её можно проверить самому. В любом случае тратится только время, компьютеру это никакого вреда не принесет. Несовместимость можно будет заметить практически сразу, так как она отражается в торможении графической визуализации и плохой синхронизации изображения со звуком.
О буферизации вывода
Буферизация вывода – достаточно полезная вещь. Данная функция заключается в складывании в стопку всего вывода скрипта, добавлении туда заголовков cookie и другого получившегося в результате работы конкретного скрипта. После завершения обработки информации все данные отправляются к клиенту в обратной последовательности, то есть сначала заголовки, потом страница и затем результат работы скрипта.
Возможности, которые открываются благодаря буферизации вывода

- Посылка cookie из абсолютно любого места в скрипте.
- Начало сессии в любое время.
- Сжатие данных перед отправкой клиенту.
Следует помнить, что сжатие потребует дополнительных ресурсов процессора. Но скорость передачи увеличится на 40% (в зависимости от количества картинок и текста). Известно, что картинки сжимаются намного хуже текста. Буферизация вывода по умолчанию не включена.
Существует 2 метода включить буферизацию вывода:
- Подходит для тех, кто владеет самим сервером или у кого есть доступ к файлу php.ini. Все, что требуется, найти в этом файле директиву output_buffering и присвоить ей значение On.
- Второй способ заключается в использовании ob_start() в скрипте, вывод которого необходимо буферизовать.
Вот мы и разобрались с тем, что такое буферизация.
fb.ru
Что нужно знать о химии воды, или Что такое pH, gH и kH - Вода и всё, что с ней связано - Обслуживание аквариума - Ваш Аквариум
Вода в природе редко бывает чистой и дистиллированной, она содержит растворенные соли, питательные вещества и т. д., концентрация которых зависит от местных условий. Рыбы и растения развивались в течение миллионов лет в конкретных условиях и могут попросту не выжить в воде, которая существенно отличается по химическому составу от водоема их привычного местообитания.
Начинающие аквариумисты предпочитают содержать рыбок, которые могут жить в обычной водопроводной воде. Опытные и аквариумисты могут изменять характеристики воды в соответствии с потребностями рыб, хотя сделать это почти всегда труднее, чем кажется на первый взгляд. В любом случае, вы должны знать достаточно о химическом составе воды, чтобы вода в аквариуме соответствовала потребностям рыб, которых вы держите.
Вода имеет четыре измеряемых свойства, которые обычно используются, чтобы характеризовать ее химический состав. Это:
- Мера кислотности воды (рН).
- Карбонатная жесткость (буферная емкость, kH)
- Общая жесткость (gH)
- Минеральный состав воды.
рН – Мера кислотности воды
рН является мерой соотношения свободных ионов водорода (H +) и свободных ионов гидроксида (OH) в воде. Измеряется по шкале от 0 до 14. pН=7 считается нейтральной, рН ниже 7 – кислой и рН выше 7 – основной или щелочной.
Для начинающих химиков уравнение выглядит следующим образом:
Подобно шкале Рихтера для измерения силы землетрясений, шкала рН является логарифмической. Другими словами, вода с рН=6,0 в 10 раз более кислая, чем вода с рН=7,0 и рН=5,0 в 100 раз более кислая, чем рН=7.0.
Для аквариумистов важны два аспекта рН. Во-первых, быстрое изменение рН вызывает стресс для рыб, и его следует избегать. Изменение рН на более чем 0,3 пункта в день может вызвать у рыб стресс. Таким образом, рН вашего аквариума нужно поддерживать постоянным и стабильным в течение длительного времени. Во-вторых, рыбы приспособились жить в воде определенного (иногда узкого) значения рН. Значит, вы должны быть уверены, что рН в вашем аквариуме отвечает условиях содержания тех рыб, которых вы держите.
Когда pH падает из-за увеличения концентрации кислот (например повышение концентрации нитритов [NO2] и нитратов [NO3]), карбонаты и бикарбонаты реагируют с кислотами и «нейтрализуют» их. При этом щелочность воды (kH) понижается. Если в воде все больше и больше кислоты (нитратов), то щелочность все ниже и ниже, и в конце концов больше не сможет буферизировать (сохранять) pH. Когда щелочность сильно упала, то есть исчерпался буфер kH, pH резко падает.
Так как кислота, которой является нитрат, – конечный продукт азотного цикла, это объясняет, почему в аквариуме со временем уровень нитратов повышается, а уровень pH понижается.
Оптимальным уровнем pH в аквариуме с растениями считается 6,8–7,2.
В мягкой воде с низким pH=6,0 примерно 80% двуокиси углерода будет находится в форме CO2 или в виде угольной кислоты [h3CO3], и только 20% в виде гидрокарбоната. При pH=7.0 преобладает бикарбонат HCO3-. Соответственно, чем ниже pH, тем больше CO2 находится в легко доступной для растений форме.
При повышении pH с нормальных 7,0 до 8,0 менее токсичный аммоний [Nh5+] переходит в форму высокотоксичного аммиака [Nh4] – его доля увеличивается с 0,5% до 5% – в 6 раз !
Большинство рыб может приспособиться к рН, немного отличающемся от оптимального диапазона. Если рН вашей воды находится в пределах от 6,5 до 7,5, вы сможете содержать большинство видов рыб без каких-либо проблем. Если рН в пределах этого диапазона, то нет необходимости его корректировать.
Таблица кислотности воды (рН)
| Сильнокислая | 1–3 |
| Кислая | 3–5 |
| Слабокислая | 5–6 |
| Очень слабокислая | 6–7 |
| Нейтральная | 7 |
| Очень слабощелочная | 7–8 |
| Слабощелочная | 8–9 |
| Щелочная | 9–10 |
| Сильнощелочная | 10–14 |
kH – буферная емкость (карбонатная жесткость, щелочность)
Карбонатная жесткость, выраженная в градусах жесткости (kH). измеряет количество карбонатов и бикарбонатов в воде. На самом деле kH измеряет не жесткость, а щелочность воды (буферная емкость – способность нейтрализовать кислоты).
Буферная емкость относится к способности воды сохранять стабильный рН при добавлении кислоты или щелочи. рН и буферная емкость тесто связаны друг с другом. Если вода имеет достаточный потенциал буферизации, буферная емкость может поглотить и нейтрализовать кислоты без существенного изменения рН. Концептуально буфер действует наподобие большой губки. «Мощность» губки, тем не менее, ограничена – как только буферная емкость расходуется, рН при добавлении кислоты изменяется более быстрыми темпами.
Буферизация имеет как положительные, так и отрицательные стороны. С одной стороны, без буферизации рН в аквариуме будет падать с течением времени – это плохо. С достаточной буферизацией рН остается стабильным – это хорошо. С другой стороны, жесткая водопроводная вода почти всегда имеет большую буферную емкость. Если рН воды слишком высок для рыб, буферная емкость затрудняет снижение рН до более подходящего значения.
В пресноводных аквариумах буферная емкость воды связана с содержанием карбонатов и гидрокарбонатов. Таким образом, термины «карбонатная жесткость» (kH), «щелочность» и «буферная емкость» используются как синонимы. Хотя технически это не одно и то же, на практике они эквивалентны. Примечание: термин «щелочность»' не следует путать с термином «щелочной». Щелочность относится к буферизации, а «щелочная» относится к воде с высоким значением рН (например, > 7).
Какая буферная емкость необходима вашему аквариуму? Чем больше значение kH, тем вода более устойчива к изменениям рН. Уровень kH должен быть достаточно высоким, чтобы предотвратить резкие колебания рН в аквариуме с течением времени. Если kH ниже 4,5 dН, вы должны обратить особое внимание на рН в аквариуме. Это особенно важно, если вы не часто меняете воду в аквариуме. В круговороте азота существует тенденцию к уменьшению значения рН со временем. Изменение рН зависит от количества и скорости производства нитратов, а также kH. Если рН падает более чем 0,5 пункта в течение месяца, вы должны подумать об увеличении kH или производить частичную замену воды чаще.
Примечание: не рекомендуется использовать в аквариуме дистиллированную воду. По определению, дистиллированная вода практически не имеет буферной емкости. Это означает, что добавление даже немного кислоты значительно изменит рН.
gH – общая жесткость
Общая жесткость (GH) – это общее количество ионов магния (Mg +) и кальция (Ca +) в воде. «Жесткая» вода часто поступает из водоносных горизонтов, проходящих в известняке. Известняк содержит карбонат кальция, который при растворении в воде увеличивает значение как gH (от кальция), так и kH (от карбоната). Увеличение значения kH также обычно увеличивает рН.
Жесткость воды измеряется в следующих единицах. Термин dН обозначает «градус жесткости», а ppm означает « часть на миллион», что примерно эквивалентно мг/л в воде. 1 градус dН равен 17,8 ppm CaCO 3. Большинство тестов показывают жесткость в градусах CaCO3; и это означает, что жесткость эквивалентна количеству CaCO3 в воде, но это не значит, что фактически такое количество CaCO3 содержится в воде..
Таблица общей жесткости воды
| 0–4 dH | 0–70 ppm | очень мягкая вода |
| 4–8 dH | 70–140 ppm | мягкая вода |
| 8–12 dH | 140–210 ppm | вода средней жесткости |
| 12–18 dH | 210–320 ppm | довольно жесткая вода |
| 18–30 dH | 320–530 ppm | очень жесткая вода |
Соленость
Соленость воды – общее количество растворенных в ней веществ. Соленость рассчитывать как сумма компонентов kH и gH, а также других веществ, в частности, натрий. Значение солености воды важно для морских аквариумов. В пресноводных аквариумах достаточно знать значения рН, kH и gH.
Некоторые пресноводные рыбы легко переносят (или даже чувствуют себя лучше) небольшое количество соли в воде. Кроме того, паразиты (например, ихтиофтириус) не переносят соль вообще. Таким образом, добавление соли в концентрации до 1 столовой ложки на 5 литров может реально помочь предотвратить и вылечить рыб от ихтиофтириуса и других паразитарных инфекций.
С другой стороны, некоторые виды рыб не переносят соль. Все бесчешуйчатые рыбы, а также некоторые сомы, например, рода Corydoras, гораздо более чувствительны к соли, чем большинство пресноводных рыб. Добавляйте соль, только если вы уверены, что это не нанесет вред обитателям аквариума.
Питательные вещества и микроэлементы
Водопроводная вода содержит питательные вещества и микроэлементы в очень низких концентрациях. Наличие (или отсутствие) микроэлементов может быть важно в некоторых ситуациях.
Наиболее распространенные микроэлементы:
- нитраты;
- фосфаты, которые связаны с ростом водорослей. Если у вас постоянные проблемы с водорослями, причиной может быть высокое содержание фосфатов. Оптимальный уровень фосфатов в аквариуме – 0,2 мг/л и ниже. Для контроля роста водорослей рекомендуются частая подмена воды.
- железо, в котором нуждаются растения. Водопроводная вода во многих районах может не содержать железа.
Углекислый газ (CO2)
Углекислый газ не также является неотъемлемой частью химического состава воды. CO2 присутствует в воде в гораздо большем количестве, чем кислород и азот вместе взятые (70:2:1). Часто аквариумисты используют установки CO2, чтобы увеличить темпы роста растений. Но углекислый газ напрямую связан с уровнем kН и рН. Когда углекислый газ растворяется в воде, в аквариуме увеличивается количество кислоты и снижается значение рН. Количество присутствующих в воде карбонатов (kH) будет определять, насколько падает уровень рН.
Соотношение значений рН, kН и CO2

aqua-wonder.my1.ru
Буферная емкость | Любителям аквариума

Буферная емкость и Буферное опрокидывание.
Буферностью называют способность раствора (а аквариумная вода — это слабый раствор) сохранять величину водородного показателя при добавлении щелочи или кислоты. Буферность аквариумной воды не измеряют, ее лишь характеризуют словами “слабая” или “сильная”. Бывают растворы со слабой буферностью, когда каждая добавленная капля кислоты или щелочи изменяет рН, бывают сильно буферные растворы, способные поддерживать постоянную величину рН, несмотря на существенные добавки химических веществ. Конечно, в определенных условиях даже вода с сильной буферностью начинает изменять рН, однако важно ориентироваться в особенностях этого свойства и правильно использовать его там, где это необходимо.
Любые изменения в уровне рН должны производиться плавно и постепенно! Скудно буферизованная вода будет более подвержена резким колебаниям уровня pH, нежели хорошо буферизованная. Буфером может считаться грунт, имеющий в своем составе много известняка — для поддержания высокой жесткости воды. Аквариумный гравий часто состоит из кальцийсодержащего материала, который повышает жесткость воды и рН. Также буфером может являться кусок дерева, коряга, которая подкисляет воду и понижает pH. Заметим, что буферизация и щелочность тесно связаны, т.к. фактически, щелочность является буфером, замедляющим изменение pH в воде. Как правило, жёсткая вода обычно имеет щелочной состав (pH более 7) и является хорошим буфером. В то же время мягкая вода (pH ниже 7) – несколько кислее и в качестве буфера не годится.
Карбонатная жесткость — это концентрация в воде анионов гидрокарбоната и карбоната. KH и pH взаимосвязаны между собой, и потому будет логичным рассмотреть их совместно. Связь же этих параметров очень проста. Чем выше содержание гидрокарбоната в воде, то есть значение KH, тем выше, а самое главное, стабильнее, значение pH, так, например, гидрокарбонат кальция является прекрасным буфером воды. Обратите внимание на слово “стабильнее”. В данном контексте оно означает, что вода с высокой, более 12 градусов карбонатной жесткостью, имеет щелочную реакцию. Вода средней жесткости (6-12 градусов) скорее всего, будет близка к нейтральной реакции (pH ~7.0), а вот вода с карбонатной жесткостью менее 6 градусов KH, по большому счету может быть какой угодно, но, скорее всего, будет кислой.
Буферное опрокидывание — резкое изменение значения рН, наиболее вероятно в щелочной среде или в среде, близкой к щелочной, когда значение рН приближается к 7. При этом вследствие щелочной реакции безвредный аммоний переходит в аммиак, и рыбы, особенно молодые, быстро погибают. Такое явление обычно наблюдается в аквариумах, перегруженных рыбами, при добавлении свежей воды. В таких аквариумах на изменения рН влияют процессы окисления, вызываемые как белковыми соединениями, в избытке имеющимися в перегруженных аквариумах, так и накапливающимися продуктами обмена, видимыми и невидимыми (растворимыми). Добавку воды в такие аквариумы следует производить небольшими порциями, причем показатель pH добавляемой воды должен быть ниже 7. В слишком жесткой и щелочной (рН выше 9) воде, тоже все плохо.
Во-первых, при повышении щелочности воды все большее количество ионизированного аммония переходит в чистый аммиак, растворенный в воде. Аммиак во много раз токсичнее аммония, поэтому при незначительных, казалось бы, увеличениях концентрации аммония неожиданно может произойти тяжелое отравление всего аквариума. Не допускать этого просто — нужно чаще подменивать воду. Либо пользуйтесь специальными кондиционерами воды. Во-вторых, по мере повышения щелочности среды у рыб ухудшается усваивание кислорода. В щелочной среде рыба может задохнуться при вполне, вроде бы, достаточном его содержании в воде. Ну и, конечно, сама по себе (особенно при резком повышении рН) щелочная вода вызывает ожоги и повреждения внешних органов рыб.

В пресноводных аквариумах, уровень буферизации зависит от уровня карбонатов и бикарбонатов в воде. Таким образом, термины карбонатная жесткость воды и Буферная емкость воды используется попеременно. Хотя теоретически это не одно и тоже, но они эквивалентны практически в плане содержания рыб. Буферная емкость относится к способности воды сохранить уровень pH устойчивым при добавлении, как кислоты, так и щелочи в воду. Если вода имеет достаточный уровень буферизации, то буферная емкость воды может поглощать и нейтрализовать добавленную кислоту, без значительного изменения уровня pH. Образно говоря буфер действует, подобно большой губке. Так при добавлении кислоты, губка поглощает кислоту и не дает измениться уровню pH. Емкость губки не безгранична, и как только буферная емкость исчерпывается, pH начинает сильно изменяться при дальнейшем добавлении кислоты.
Буферная емкость имеет, и положительные и отрицательные качества. Положительная сторона, когда при функционировании цикла азота появляется нитрат, он подкисляет воду. Без буферизации, показатель pH аквариума понизился бы через некоторое время, (это плохо). С достаточной буферизацией, уровень pH остается устойчивым (это хорошо). С другой стороны, вода (особенно жесткая), имеет высокий уровень буферизации. И если показатель pH воды слишком высок, для Вашей рыбы, то буферная емкость воды, препятствует снижению уровня pH при попытке это сделать. Если не учитывать буферную емкость воды, то попытки изменить показатель pH в аквариуме обречены на неудачу.
Какой уровень буферизации необходим для аквариума? В большинстве случаев тестовые наборы, предназначенные для измерения буферизации, фактически измеряют KH воды. Чем выше KH, тем более стойкой будет вода к изменению pH. KH воды в аквариуме должна быть достаточно высока, чтобы предотвратить большие колебания pH, в течение некоторого времени. Если KH воды — ниже 4,5° dH, Вы должны постоянно контролировать уровень pH в аквариуме, для того что бы быть уверенным, что он не изменяется в опасных пределах. Это особенно важно, если Вы не производите регулярных подмен воды. В частности цикл азота, создает тенденцию для уменьшения уровня pH в течение некоторого времени.
Насколько точно понизится уровень pH, зависит от количества произведенных нитратов, также как и от жесткости воды. Если pH снижается больше чем на 0,2 пункта в месяц, необходимо позаботиться о повышении жесткости воды, либо более часто производить ее подмену. К тому же следует учесть важную особенность воды – ее способность к самовосстановлению. В особенности это касается жесткой воды. Так, например, разбавив на 50% водопроводную воду с рН = 7,5 дистиллированной водой и опустив тем самым рН до 6,5 или еще ниже, можете быть уверены, что через несколько часов рН станет близко к первоначальному 7,5. KH воды непосредственно не влияет на рыб, и обычно нет никакой необходимости точно выдерживать фиксированный уровень жесткости для специфических рыб.
В аквариуме с озерными цихлидами необходимо обеспечить достаточную буферизацию воды солями кальция и магния, так как нечаянный перекорм рыбок может запросто привести к самым печальным последствиям. Речные африканские виды легко выдерживают подкисление воды ниже уровня 7,0, но все же лучше себя чувствуют в щелочной воде. Нужно поддерживать идеальную чистоту и стабильный хим. состав воды.
 Влияние показателя рН на жизнь рыбок и растений.
Влияние показателя рН на жизнь рыбок и растений.
Равновесие рН – КН – Со2. Определение показателя активной реакции воды. 


aquafisher.org.ua