Свойства и применение анилина. Анилин вода
Химические свойства анилина | Химия онлайн
Для анилина характерны реакции как по аминогруппе, так и по бензольному кольцу. Особенности этих реакций обусловлены взаимным влиянием атомов.
С одной стороны, бензольное кольцо ослабляет основные свойства аминогруппы по сравнению алифатическими аминами и даже с аммиаком.
С другой стороны, под влиянием аминогруппы бензольное кольцо становится более активным в реакциях замещения, чем бензол.
I. Основные свойства
Уменьшение электронной плотности на атоме азота приводит к снижению способности отщеплять протоны от слабых кислот.
Анилин более слабое основание, чем предельные амины и аммиак.
Поэтому анилин взаимодействует лишь с сильными кислотами (HCl, h3SO4) и, в отличие от алифатических аминов и аммиака, не образует с водой гидроксида, а его водный раствор не окрашивает лакмус в синий цвет.
Анилин с водой не реагирует и не изменяет окраску индикатора!!! 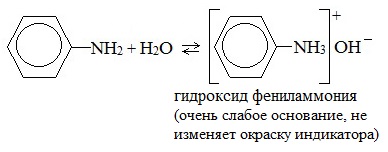
Видеоопыт «Изучение среды раствора анилина»
Соли анилина, в отличие от анилина, хорошо растворимы в воде.
II. Особые свойства анилина
Реакции с участием аминогруппы
1. Взаимодействие с кислотами (образование солей)
Анилин реагирует с сильными кислотами, образуя соли фениламмония, которые растворимы в воде, но не растворимы в неполярных органических растворителях: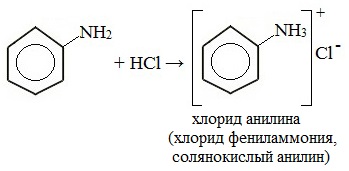
Видеоопыт «Взаимодействие анилина с соляной кислотой»
Анилин, который практически не растворяется в воде, можно растворить в соляной кислоте и отделить нерастворимые примеси.
Солянокислый анилин хорошо растворим в воде. если к такому раствору добавить достаточное количество щелочи, то анилин снова выделится в свободном виде:
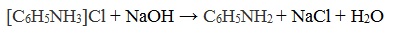
Реакции с участием бензольного ядра
Аминогруппа как заместитель I рода облегчает реакции замещения в бензольном ядре, при этом заместители становятся в орто- и пара-положения к аминогруппе.
При бромировании анилин легко образует 2, 4, 6 — тризамещенные продукты реакции. По той же причине анилин легко окисляется.
1. Галогенирование
Анилин энергично реагирует с бромной водой с образованием белого осадка 2,4,6-триброманилина. Эта реакция может использоваться для качественного и количественного определения анилина:
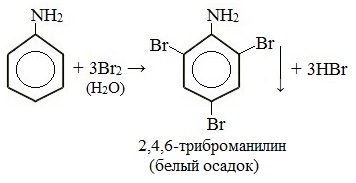
Качественная реакция на анилин!
Видеоопыт «Бромирование анилина»
2. Сульфирование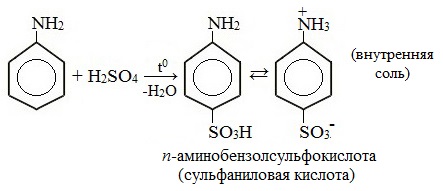
Сульфаниловая кислота является важным промежуточным продуктом в синтезе лекарственных веществ (сульфаниламидных препаратов).
III. Окисление анилина
Анилин легко окисляется различными окислителями с образованием ряда соединений, поэтому он темнеет при хранении.
При действии хлорной извести Ca (Cl) OCl на водный раствор анилина появляется интенсивное фиолетовое окрашивание.
Качественная реакция на анилин!
Видеоопыт «Окисление анилина раствором хлорной извести – качественная реакция»
При взаимодействии анилина с хромовой известью (смесь концентрированной серной кислоты и дихромата калия К2Cr2O7) образуется черный осадок, называемый черным анилином (краситель «анилиновый черный»).
Черный анилин применяется как прочный краситель (для окраски тканей и меха в черный цвет). Обычно ткань сначала пропитывают раствором окислителя. Образующийся черный анилин откладывается в порах волокна. Он не растворим в воде и устойчив к мылу и свету.
Видеоопыт «Окисление анилина раствором дихроматом калия – получение красителей»
IV. Диазотирование анилина
Практическое значение имеет реакция взаимодействия анилина с азотистой кислотой при пониженной температуре (около 0°С). В результате этой реакции (реакции диазотирования) образуются соли диазония, которые используются в синтезе азокрасителей и ряда других соединений.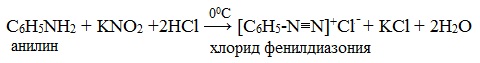
При более высокой температуре реакция идет с выделением азота и анилин превращается в фенол:
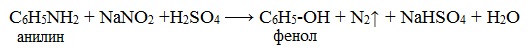
Подобно анилину реагируют с азотистой кислотой и другие первичные ароматические амины.
Анилин
himija-online.ru
Ароматические амины Опыт14. Растворимость анилина и его солей в воде. Основные свойства анилина
Реактивы и оборудование:анилин, концентрированная соляная кислота, 10%-ный раствор серной кислоты, раствор гидроксида натрия, синяя и красная лакмусовая бумага; пробирки.
К 5—6 каплям анилина приливают 2—3 мл воды. После тщательного перемешивания получают мутную жидкость — эмульсию анилина в воде. Анилин плохо растворяется в воде, поэтому иногда его называют анилиновым маслом. В полученную эмульсию опускают красную, а затем синюю лакмусовые бумажки. Изменение цвета индикаторов не наблюдается.
Кислотно-основные свойства анилина выражены слабо. Однако основные свойства анилина четко проявляются в его способности образовывать соли с минеральными кислотами.
Эмульсию анилина разливают в две пробирки. К одной части по каплям при встряхивании добавляют концентрированную соляную кислоту. Постепенно происходит просветление мутной жидкости вследствие образования легко растворимой в воде соли — хлорида фениламмония:
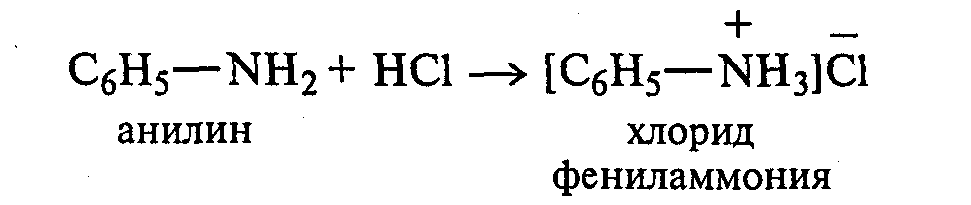
В пробирку с полученной солью приливают раствор гидроксида натрия. Наблюдают помутнение жидкости вследствие выделения анилина:
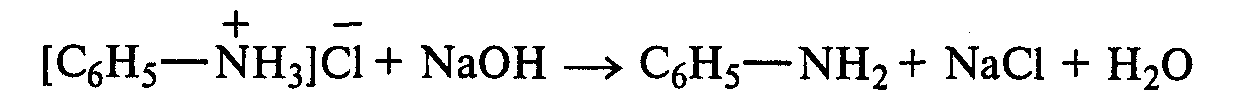
Во вторую пробирку с эмульсией анилина прибавляют по каплям 10%-ный раствор серной кислоты. После ее встряхивания и охлаждения наблюдают выпадение белого осадка трудно растворимого в воде гидросульфата фениламмония:
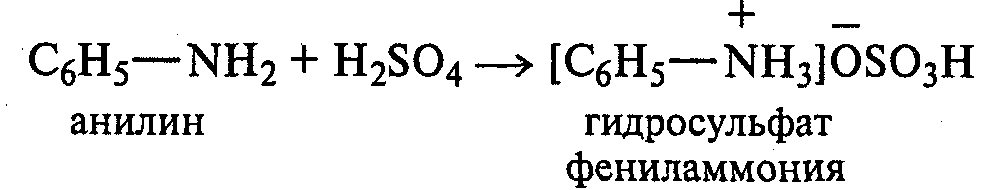
При добавлении раствора гидроксида натрия осадок растворяется, и жидкость мутнеет.
Опыт 15. Взаимодействие анилина с бромной водой
Реактивы и оборудование:анилин, насыщенная бромная вода; пробирки.
В пробирку наливают 2—3 мл воды, добавляют 1—2 капли анилина и тщательно перемешивают. К полученной эмульсии по каплям при перемешивании прибавляют бромную воду. Выпадает белый осадок триброманилина:
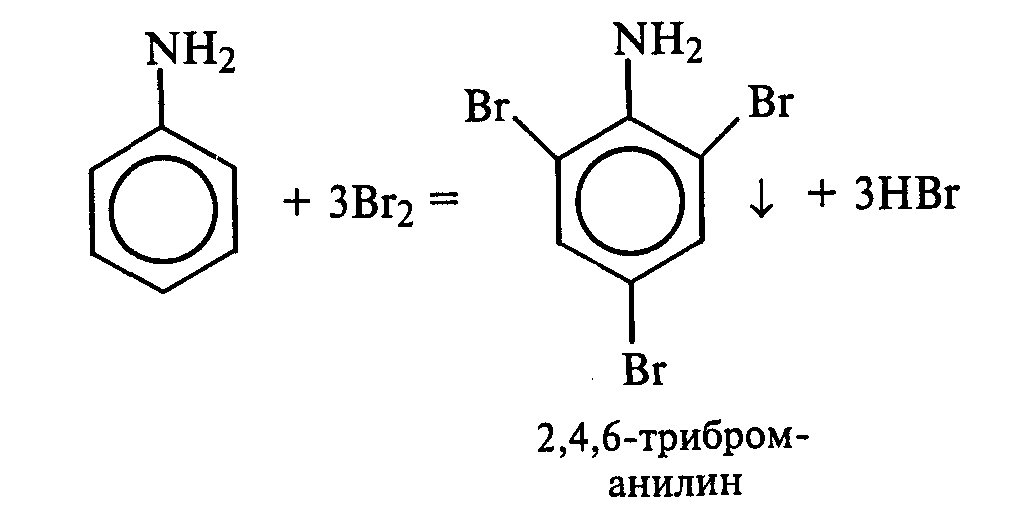
Аминогруппа — это электронодонорная группа, она увеличивает электронную плотность в бензольном кольце, поэтому реакции электрофильного замещения идут очень легко и без катализатора.
Рассмотрите механизм монобромирования анилина и объясните влияние аминогруппы с точки зрения статического и динамического факторов.
Опыт 16. Ацилирование анилина
Реактивы и оборудование:анилин, уксусный ангидрид; пробирки.
В пробирку наливают 0,5 мл анилина и 1,5 мл воды и энергично перемешивают. К полученной смеси добавляют 0,5 мл уксусного ангидрида. Пробирку закрывают пробкой и сильно встряхивают ют. Разогревшуюся пробирку охлаждают водой. Выпадает белый осадок ацетанилида:
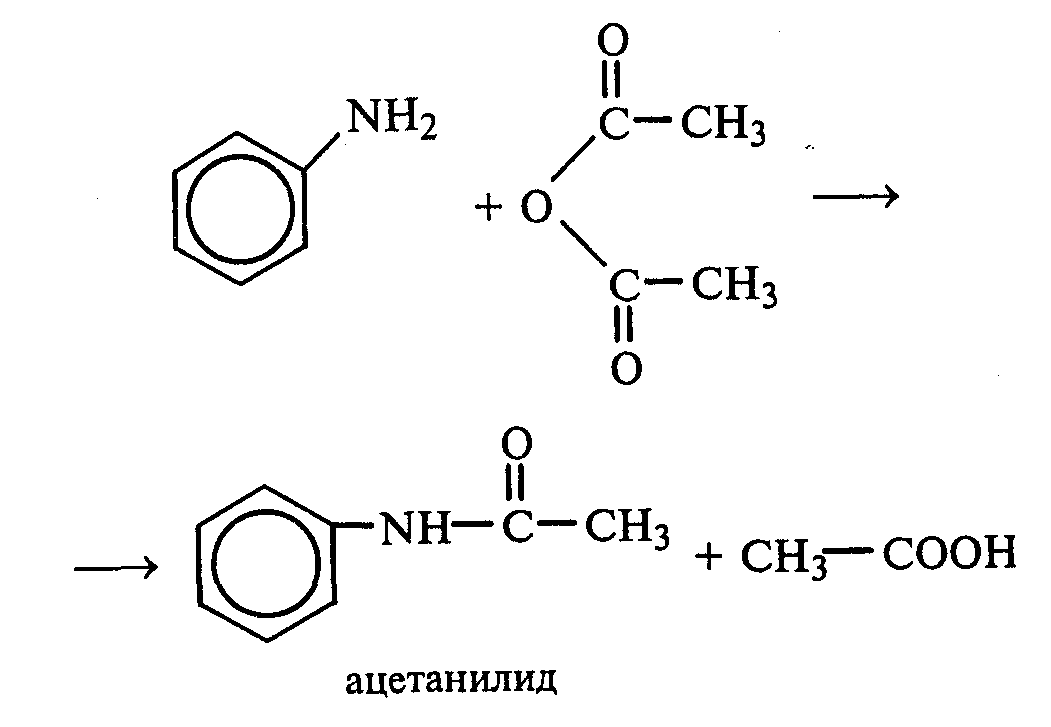
В медицине ацетанилид известен под названием антифебрин. Он применялся как средство от лихорадки и в настоящее время снят с производства ввиду его токсичности.
Напишите механизм реакции ацилирования анилина.
Опыт 17. Окисление анилина
Реактивы и оборудование:анилин, хромовая смесь; пробирки.
В пробирку наливают 1 мл воды и 2—3 капли анилина, тщательно перемешивают и добавляют 1—2 мл хромовой смеси (раствор дихромата калия в разбавленной серной кислоте).
Окраска раствора меняется от оранжевой до зеленой, а затем наблюдается почернение реакционной смеси.
Конечным продуктом окисления анилина является краситель сложного строения — «черный анилин», который используют для окрашивания тканей и получения красящего слоя копировальной бумаги.
studfiles.net
Анилин и водой - Справочник химика 21
Данные о взаимной растворимости анилина и воды представлены в табл. 9. [c.295]Найти максимальное давление пара при ( = 100 над смесью анилина и воды, если при t = 100 растворимость воды в анилине равна 10,3 вес.%. анилина в воде 7,18 вес. 7о, а давление паров чистого анилина и воды равно соответственно 45,7 и 760 мм. Для расчета воспользоваться результатом решения примера I. [c.204]
Взаимная растворимость анилина и воды [c.295]
На рис. 169 представлена диаграмма зависимости парциального давления паров анилина и воды от состава смеси этих веществ при ЮО ". [c.295]
В интервале концентраций анилина от 0,0148 до 0,628 мол. доли анилин и вода ведут себя как две несмешивающиеся жидкости, парциальное давление паров которых не меняется с изменением состава (участки fD н ВВ). [c.295]
Таким образом, смешение анилина и воды в любых соотношениях, отвечающих интервалу между концентрациями насыщенных растворов анилина в воде н воды в анилине (нода ВС), приводит к образованию двух равновесных жидких фаз с определенным и постоянным для данной температуры составом каждой из них. Такие растворы называют сопряженными. Парообразная фаза над обоими жидкими слоями общая. [c.99]Давления паров анилина и воды при различных температурах такие [c.191]
В табл, 11 приведен химический состав двух слоев, образовавшихся при смешивании анилина с водой при различных температурах, Из таблицы видно, что при повышении температуры в водном слое будет расти концентрация анилина, а в анилиновом слое —концентрация воды. При температуре 441 К составы обоих растворов становятся равными, граница раздела между слоями исчезает, и уже выше 441 К анилин и вода смешиваются друг с другом в любых соотношениях. [c.89]
Изменение температуры может либо увеличить, либо уменьшить растворимость веществ. Это зависит от знака теплового эффекта растворения. Вследствие эндотермичности теплоты растворения анилина в воде и воды в анилине повышение температуры приводит к сближению точек, отвечающих концентрациям насыщенных растворов, и, наконец, к полному их слиянию (точка К). Выше температуры, соответствующей точке К, называемой верхней критической температурой (Ткр°) смешения (растворения), анилин и вода неограниченно взаимно растворяются (система гомогенна). [c.37]
Ограниченная растворимость двух жидкостей. В зависимости от своей природы жидкости в разных соотношениях смешиваются друг с другом — от практической нерастворимости в любых условиях до неограниченной взаимной растворимости. Рассмотрим сДучай ограниченной взаимной растворимости на примере двойной системы анилин—вода. Если при постоянной температуре путем длительного и энергичного встряхивания перемешать произвольные, но достаточно большие количества анилина и воды, получится неустойчивая эмульсия. С течением времени она расслаивается на два сопряженных раствора верхний — насыщенный раствор анилина в воде и нижний — насыщенный раствор воды в анилине. При постоянной температуре оба раствора имеют строго определенный равновесный состав, который (в известных пределах концентраций) не изменяется при добавлении новых порций анилина и воды, изменяются лишь относительные количества растворов. [c.197]
Данным методом анализировали четыре типичных соединения с активными атомами водорода я-бутанол, бензойную кислоту, анилин и воду. Каждое из соединений анализировали с одной отдельной порцией реагента, причем удельные радиоактивности этих порций были различны. Графики зависимости радиоактивности от количества активного водорода были прямолинейными для всех четырех соединений. То, что продолжения этих графиков пересекали отрицательную часть оси ординат, объяснили потерями водорода за счет неколичественного переноса растворов, улетучиванием анализируемого соединения до реакции или, возможно, неполным извлечением газа из ячейки в процессе измерения радиоактивности в течение 10 мин. Целью этого начального исследования было показать линейность упомянутых выше калибровочных графиков и возможность аналитического применения метода. В связи с этим не проводилось анализов соединений различных классов с ириме-нением одной и той же порции радиореагента. Стехиометрия реакции с данным реагентом подробно изучена в работе [17]. [c.252]
При смешении двух жидкостей могут наблюдаться всевозможные градации взаимной растворимости от практически полной нерастворимости друг в друге (например, ртуть и вода) до смешения в любых соотношениях с образованием однородного раствора (например, этиловый спирт и вода). Промежуточное положение занимает смесь ограниченной взаимной растворимости. Смесь жидкостей А и В (например, анилина и воды) разделяется после взбалтывания на два слоя насыщенный раствор А в В и насыщенный раствор В в А, Однако и в этом случае могут существовать области температуры и состава, где А и В образуют однородную смесь [c.196]
На основании данных по взаимной растворимости анилина и воды можно считать, что средняя линия в этом случае является вертикалью. [c.190]
На рис. 8.14 приведена кривая ДНП — температура для смеси анилина и воды, перегоняющейся при 98 °С и 1 атм. Нагревание анилина при атмосферном давлении сопровождается частичным разложением его до достижения температуры кипения, равной 190 °С. [c.181]
I iii, ир H-ii, r.i Отношение масс анилина и воды в дистилляте равно I u(I ( . 0,212, что соответствует массовому содержанию анилина 17,5 %. [c.182]
В частности, вода на границе с анилином обладает очень малым поверхностным натяжением сг=4,8 эрг/см, так как вода и анилин — полярные жидкости (1Ан,о= 1,84 О [ас.н,м =1,48 О), обладающие значительной взаимной растворимостью. Таким образом, контактируют не анилин и вода, а их растворы. При некоторой температуре (167°С) концентрации растворов совпадут и граница раздела вообще исчезнет (табл. 36). При контакте воды с деканом С Нгг, дипольный момент которого равен нулю, поверхностное натяжение достаточно велико (0,05124 Дж/м ). [c.221]
В круглодонную колбу прибора 1 помещают 13 мл анилина (осторожно] анилин ядовит), 16,7 г бензойной кислоты и нагревают смесь при 180—190 °С до тех пор, пока не перестанут отгоняться анилин и вода. Затем доводят температуру до 225°С и поддерживают ее на этом уровне до прекращения перегонки. Удаляют масляную баню, дают колбе немного охладиться, добавляют еще 5 мл анилина и повторяют нагревание, как описано выше. [c.165]
После прекращения отгонки анилина и воды содержимое колбы выливают в фарфоровую чашку. Остывший и затвердевший продукт растирают в ступке, переносят в стакан, где размешивают со 125 мл 1 н. раствора соляной кислоты. С осадка сливают жидкость и снова повторяют эту операцию, чтобы удалить из осадка не вступивший в реакцию анилин. Затем таким же образом промывают продукт водой, два раза 1 н. раствором едкого натра для удаления непрореагировавшей бензойной кислоты и, наконец, еще несколько раз водой. [c.165]
Основное количество полученного анилина отгоняется из редуктора с водяным паром, часть которого образуется вследствие выделения теплоты реакции, а часть подается в редуктор через барботер. Расход пара стабилизируется регулятором 17. Пары анилина и воды направляются в конденсатор 19. Шламовая жидкость, в которой осталось более 40% анилина, непрерывно удаляется из редуктора через верхний боковой штуцер и перетекает в отгонный аппарат 1 (рис. 33). [c.105]
В аппарате 9 конденсируются пары анилина и воды. Для полного улавливания анилина газы проходят через теплообменник 10 с развитой охлаждающей поверхностью и сепаратор 11. Избыток водорода возвращается в цикл, конденсат стекает в отстойник 12, из которого анилиновая вода поступает на экстракцию нитробензолом, а анилин — на вакуум-перегонку. Выход анилина — 98% от теоретического. [c.123]
BOM давлении в системе координат, где на оси абсцисс отложены температуры кипения воды, а на оси ординат — температуры кипения вещества А с водой. Для рассматриваемой системы все нанесенные точки будут лежать на одной прямой. На рис. 30 линии вода — анилин и вода — хлорбензол показывают температуры, при которых давление воды равно сумме парциальных давлений воды [c.61]
С анилин и вода смешиваются в любглх соотношениях. [c.74]
Подни.мающиеся из редуктора пары воды способствуют агломерации стружки на выходе из питателя. Во избежание этого част1, анилиновой воды подается по той же трубе, по которой заг[>ужается чугунная стружка. Основное количество полученного анилина отгоняется нз редуктора вместе с водяным паром, часть которого образуется вследствие выделения тепла реакции, а часть подводится через барботер 9. Расход пара стабилизируется регулятором 10. Пары анилина и воды направляются в конденсатор 13, шламовая жидкость непрерывно удаляется из редуктора через верхний боковой штуцер. [c.283]
На рис. 164 приведена принципиальная схема установки для измерения содержания нитробензола в анилине. Смесь паров анилина и воды, отфильтрованная от шлама на фильтре 1, поступает в конденсатор 2 и затем в разделитель фаз 3. Неконденси-рующиеся газы удаляются в атмосферу, конденсат через холодильник 4 [юступает в сепаратор 5, где анилин отделяется от воды. Уровешз анилина в сепараторе автоматически регулируется прибором 6. Анилиновь[й слой поступает через подогреватель 7 в кювету фотоколориметра 13, которая вмонтирована в прибор, со- стоящи из фотоэлементов 5, линз 11, светофильтров 10, регулирующей диафрагмы 9 и осветителя 12. Фотоколориметрический прибор сигнализирует о повьппении содержания невосстановленного [c.283]
Рнс. 169. Диаграмма зависимости между йарцыальным давлением паров анилина и воды [c.296]
Рассмотрим несколько примеров, начав с уже упомянутой системы анилин — вода. Вследствие эндотермичности последней теплоты растворения повышение температуры приводит к сближению точек, отпечающих концентрациям насыщенных растворов (рис. VIII. 1), точки В м С, Е м F, М и N), и, наконец, к odepkmue Н2О, / (масс. полному слиянию двух точек в одну точку К при 167 °С. Выше этой температуры, называемой верхней критической температурой растворения, анилин и вода неограниченно взаимно растворяются, т. е. образуют одну жидкую фазу. [c.101]
От типичных лиофобных эмульсий следует отличать так называемые критические—лиофильные эмульсии. Критические эмульсии — это системы, образующиеся обычно из двух ограниченно смешивающихся жидкостей (например, анилина и воды, йзоами-лового nnpTa и воды) при температурах, весьма близких к критической температуре смешения, когда поверхностное натяжение на границе фаз становится весьма малым (порядка 0,01 эрг/см ) и теплового движения молекул уже достаточно для диспергирования одной жидкости в другой. В результате такого самопроизвольного диспергирования образуется тончайшая эмульсия, в которой коалесценция отдельных капелек уравновешивается стремлением обеих жидкостей равномерно распределиться в объеме (см. гл. VIII, разд. 1). [c.368]
ТЛервые систематические исследования взаимной растворимости жидкостей были осуществлены В. Ф. Алексеевым. Рассмотрим смесь анилина с водой. Нальем в пробирку некоторое количество анилина и воды и будем встряхивать пробирку до тех пор, пока в системе не установится равновесие, т. е. пока при постоянной температуре и давлении при повторных встряхиваниях состав образовавшихся двух жидких слоев не станет постоянным. Химический анализ показывает, что верхний слой состоит в основном из воды и содержит в небольшом количестве анилин, наоборот, нижний слой состоит из анилина и содержит незначительное количество воды. Сколько бы мы ни прибавляли в пробирку анилина или воды, состав жидких слоев при данных условиях будет оставаться неизменным. [c.140]
При ограниченной растворимости каждая из жидкостей переходит в другую до определенного предела, в результате образуется двухслойная система. Верхний и нижний слои обладают неодинаковым составом и представляют собой иасыщенные при данной температуре растворы одной жидкости в другой. Между иими имеется отчетливая граница раздела. Например, при смешении анилина и воды образуется два слоя нижний — анили- [c.228]
ЭНКИ анилина и воды. Затем температуру повышают до 225 С Ш поддерживают на этом уровне до окончания перегонки. Колбу хлаждают, убрав масляную баню, добавляют еще 2,2 г (2,1 мл) ршилина и повторяют нагревайие, как описано выше (при 180.,. 190, а затем при 225°С), после чего содержимое колбы еще горя- чим выливают в фарфоровую чашку. [c.173]
В круглодонной колбе емкостью 300 мл, соединенной с холодильником Лнбиха и погруженной в масляную баню, нагревают смесь 50 г (0,54 моля) анилина и 67 г (0,55 моля) бензойной кислоты до 180—190°. Эту температуру поддерживают до тех пор, пока не перестанут отгоняться анилин и вода. Затем температуру поднимают до 225° и поддерживают на этом уровне до прекращения перегонки. Колбе дают несколько охладиться (удалив масляную баню) и добавляют еще 22 г (0,23 моля) анилина. Нагревают повторно так, как описано выше (при 185 и 225°), к затем горячее содержимое колбы выливают в фарфоровую чашку. Остывший затвердевший продукт растирают в ступке, переносят в стакан емкостью 1 л и размешивают с 500 мл 1 н. соляной кислоты. После декантации эту операцию повторяют вновь (примечание 1). Затем падобным же образов продукт промывают несколько раз водой, два раза 1 1, раствором ед гс натра (примечание 2) и, наконец, еще несколько раз водой. Осадок отс сывают на воронке Бюхнера и сушат на бумаге, сперва на воздухе, том в сушильном шкафу при 100°. Получают 65 г сырого бензанйлАа (примечание 3). Его можно очистить кристаллизацией из этилового спирта с добавкой активированного угля. Кристаллический бензанилИд почти бесцветен, т. пл. 160—161°. [c.392]
Представляя зависимость Ад от Р в догарифмичесрсом масштабе (рис. 52) и определяя из угла наклона показатель степени при значении Я, для хлорбензола, анилина и воды найдем величину, близкую к 2/7. На первый взгляд это говорит о справедливости уравнения (88) для хлорбензола и анилина. Однако уравнение (88) обычно не соответствовало условиям проведения опытов, при которых, как правило, выполнялось соотношение Пт > АРа-Измерения в случае тонких слоев между капельками эмульсий дали совершенно иные результаты [205]. Так, не обнаружена зависимость критической толщины пленки от величины поверхности соприкосновения. По-видимому, причина состоит в том, что подобные пленки нельзя рассматривать как плоскопараллельные. В периферийной зоне пленок всегда имеется утоньшение, а в центре — утолщение (см. рис. 37) . Эта неоднородность увеличивается с возрастанием радиуса. При измерении толщины интерференционным методом путем фотометрирования всей пленки влияние радиуса изучается лишь формально. Напротив, если измеряют толщину малых сегментов пленки и направляют фотоумножитель в место с наименьшей толщиной, то значение Лс оказывается независимым от радиуса. [c.96]
chem21.info
Система вода анилин - Справочник химика 21
Примером может служить та же система вода —анилин (рис. 112). [c.331]Ограниченная взаимная растворимость двух жидкостей наблюдается в системах со значительным отклонением от идеальности. Такая растворимость зависит от температуры, однако влияние температуры на разные системы различно. В одних системах взаимная растворимость жидкостей увеличивается с ростом температуры, и при этом составы двух равновесных жидких фаз сближаются. При некоторой температуре, называемой критической температурой растворения, составы обеих равновесных жидких фаз становятся одинаковыми и достигается полная гомогенность системы. Системы, состоящие из двух ограниченно смешивающихся жидкостей, взаимная растворимость которых возрастает с повышением температуры, называются системами с верхней критической температурой растворения. К таким системам относятся системы вода — анилин, вода — фенол, вода — нитробензол. [c.386]
Зависимость взаимной растворимости жидкостей от температуры при постоянном давлении представляют на диаграммах состояния в координатах температура — состав. На рис. 127 приведена диаграмма состояния для системы вода — анилин, в которой взаимная растворимость двух жидкостей увеличивается с ростом температуры. На этой диаграмме кривая аКЬ, называемая кривой расслоения, делит диаграмму на две области гомогенную, лежащую выше кривой расслоения (незаштрихованная область), и гетерогенную, находящуюся под кривой расслоения (заштрихованная область). Фигуративные точки в гомогенной области, например точка (1, изображают состояние однофазной дивариантной системы (С = 2 — 1 + 1 =2). Любая фигуративная точка, лежащая внутри гетерогенной области, например точка О, изображает состояние двухфазной равновесной системы, обладающей при постоянном давлении одной степенью свободы (С = 2 — 2 -г 1 =1). [c.386] Таким образом, критическая точка растворения для системы вода — анилин 441 К- [c.89]Пример. Использовать полученные соотношения для расчета координат изотермических кривых кипения и конденсации р — х, у системы вода — анилин, находящейся при /=100°, если весовые составы равновесных жидких слоев по анилину равны л д=0,0718 и д д = 0,897, молекулярные веса воды и анилина Мд=18 и М = 93 и упругости их насыщенных паров при 100 соответственно равны Р1 = 760 мм и Р, = 45,7 мм рт. ст. [c.119]
Когда экстремум температуры оказывается минимумом (см. рис. 130), ее называют нижней критической температурой, примером может служить система вода — анилин. [c.425]
Изменение внешних условий вызывает изменение и состава равновесных слоев. Повышение температуры обычно ведет к увеличению взаимной растворимости жидкостей. Примером может служить та же система вода — анилин (рис. 112). В. Ф. Алексеевым было найдено (1876 г.), что в таких системах повышение температуры может привести к достижению полной взаимной растворимости, причем температура, выше которой имеет место неограниченная взаимная смешиваемость обоих компонентов, получила название критической температуры растворения (точнее, верхней критической температуры растворения). В системе вода — анилин она равна 168°С. [c.325]
Ограниченную растворимость в двух компонентной системе можно наблюдать на примере системы вода—анилин. [c.109]
Результаты наблюдений проиллюстрированы также (см. рис. 115) на треугольной призматической модели, вычерченной для тройной системы вода — анилин — бензол с постоянной концентрацией метанола. [c.91]Зависимость степени извлечения от высоты колонны при лимитирующем сопротивлении сплошной фазы для системы вода — анилин — ксилол (Диаметр капель = 0,15 см) [87]. [c.96]
Экстракция единичными каплями в системе вода — анилин — ксилол (диаметр капель 0,15 см) при различной высоте рабочей зоны колонны [c.109]
Взаимная растворимость жидкостей существенно изменяется с изменением внешних условий. Повышение температуры во многих случаях увеличивает взаимную растворимость обоих компонентов. Температура, выше которой жидкости растворяются друг в друге в любых отношениях, была названа В. Ф. Алексеевым верхней критической температурой растворения. В системе вода — анилин она равна 168°С. [c.81]
Ограниченную растворимость в двухкомпонентной системе можно наблюдать на примере системы вода — анилин. [c.99]Ограниченная растворимость жидкостей наблюдается, например, в системе вода-анилин (рис. 2.22). Кривая на рис. 2.22 разделяет области существования гомогенных и гетерогенных систем. Заштрихованная площадь - это область существования гетерогенной системы, т. е. расслаивания жидкой системы. Так, 50%-ная смесь анилин - вода при 160 "С рассла- [c.254]
Для всех трех пар компонентов (А —В, В — С и А —С) наблюдается ограниченная взаимная растворимость (например, в системе вода —анилин-—гексан). Добавление к двухфазной системе третьего компонента резко увеличивает взаимную растворимость двух компонентов и приводит к образованию однофазной системы (рис. 91, е). Добавление к двухфазной системе третьего компонента существенно не увеличивает взаимной растворимости и может привести к образованию тре.хфазной системы (рис. 91, ж). [c.208]
Различают верхнюю и нижнюю К. т. р. В первом случае расслаивание происходит при темн-рах ниже критич. темп-ры, по втором случае — выше критич. теми-ры. Системы с нижней К. т. р. встречаются значительно реже, чем систсмы с верхней К. т. р. При-м( ро51 систем с верхней К. т. р. может служить рассмотренная вын1е система вода — анилин, а с нижней К. т. р. — ( истема пода — диэтиламин. Известны и Tai iie систе.мы, которые обладают верхней и нижней [c.432]Концевой эффект на входе диспергированной фазы в случае капельного истечения жидкости объясняется некоторыми авторами дополнительным насыщением капли за время ее образования и отрыва, а также некоторым увеличением скорости массопередачи в начальный момент движения капли из-за более высокой степени ее турбулизации. Однако, как было показано в работе [101], концевой эффект на входе диспергированной фазы наблюдается лищь при экстракции в системах, где лимитирующим является сопротивление диспергированной фазы. В случае же, когда лимитирующим является сопротивление сплошной фазы, концевой эффект на входе диспергированной фазы не наблюдается. В табл. 4-6 приведены данные, полученные при экстракции в системе вода — анилин — ксилол ири различной высоте рабочей зоны колонны. [c.109]
Диаграмма состояния системы вода — анилин изображена на рис. 20. Кривая взаимной растворимости компонентов на диаграмме называется кривой расслоения или бинодальной кривой. Поле на диаграмме за границей кривой расслоения отвечает существованию гомогенного жидкого раствора переменного состава. Поле, ограниченное кривой расслоения, представляет собой гетерогенную область существования в равновесии двух жидких слоев. Точки на кривой, взятые для определенной температуры, характеризуют состав равновесных слоев. Прямая, соединяющая такие точки сопряженных (равновесных) слоев, например линия А — Л", называется нодой или копнодой. Точка К на рисунке соответствует критической температуре растворения. [c.81]
Изменение внешних условий вызывает изменение и состава равновесных слоев. Повышение температуры обычно ведет к увеличению взаимной растворимости жидкостей. Примером может служить та же система вода—анилин (рис. 100). В. Ф. Алексеевым было найдено (1876 г.), что в таких системах повышение температуры может привести к достижению полной взаимной растворимости, причом температура, выше которой имеет место кеогра- [c.311]
chem21.info
Анилиновая вода - Справочник химика 21
Качественная реакция на анилин — появление фиолетового окрашивания при действии хлорной извести. В пробирке взбалтывают 2—3 капли анилина с 10 мл воды, полученную анилиновую воду переносят в стакан, добавляют 10 мл воды и 2—3 мл профильтрованного водного раствора хлорной извести — появляется фиолетовое окрашивание. Следует иметь в виду, что эту реакцию дают только водные растворы свободного анилина, но не его солей. [c.114] Жидкий нитробензол, водный раствор электролита (например, хлористого аммония) и анилиновая вода из напорных емкостей / [c.282]Анилиновая вода. Для проведения опытов по экстракции анилина его перемешивают с водой в объемном соотношении 1 20 и оставляют, не разделяя слои. Для исследования химических свойств анилина достаточно его растворить в воде в объемном соотношении 1 100. [c.189]
Эти же авторы разработали колориметрический метод определения никотина, используя известную реакцию на пиридиновый ЦИК.Я с бромцианом и анилиновой водой. Сущность метода заключается в присоединении бромциана к пиридиновому кольцу с образованием соединения [c.139]
Для восстановления нитробензола применяют реакционные аппараты (редукторы) емкостью 10—20 м с мощной тихоходной мешалкой. Аппараты выполнены из стальных или чугунных царг, защищенных изнутри от коррозии и истирания кислотоупорной футеровкой. Редукторы некоторых конструкций имеют паровую рубашку для обогрева. Загрузка в редуктор чугунной стружки и нитробензола проводится в несколько приемов. Вначале загружают воду (или возвратную анилиновую воду), часть чугунной стружки и электролит и нагревают массу до кипения. Затем начинают добавлять первую порцию нитробензола. [c.103]
Непрерывный способ. При непрерывном восстановлении нитробензола применяют редуктор той же конструкции, что и при периодическом. Для ускорения реакции восстановления в процесс вводят самый активный электролит — хлорид аммония и чугунную стружку, обладающую повышенной активностью, равномерно измельченную и очищенную от примесей. Нитробензол, раствор хлорида аммония и анилиновая вода из напорных емкостей 1, 2. 3 [c.103]
Основным приемом, обеспечивающим полное превращение нитробензола в анилин в условиях непрерывного процесса, является автоматическое регулирование подачи в редуктор нитробензола, раствора хлорида аммония и анилиновой воды. При постоянной [c.104]
Отгонный аппарат по конструкции такой же, как и редуктор. Анилин и водяной пар конденсируются в аппарате 2, охлаждаемом водой. Конденсат попадает в отстойник шлама 4, холодильник 5 и сепаратор 6, в котором водный анилин отделяется от анилиновой воды. Анилин подвергают обычной вакуум-перегонке в кубе 22, снабженном конденсатором 21 и вакуум-сборниками 16 и 17. При атмосферном давлении или небольшом разрежении сначала перегоняется вода с анилином (до температуры в парах 125°С), а затем при разрежении (остаточное давление 11,3— 19,95 кПа) и ПО—140°С — чистый анилин. В кубе остается небольшое количество смолы. Анилиновая вода перегоняется в насадочной колонне непрерывного действия 20 без укрепляющей [c.105]
В аппарате 9 конденсируются пары анилина и воды. Для полного улавливания анилина газы проходят через теплообменник 10 с развитой охлаждающей поверхностью и сепаратор 11. Избыток водорода возвращается в цикл, конденсат стекает в отстойник 12, из которого анилиновая вода поступает на экстракцию нитробензолом, а анилин — на вакуум-перегонку. Выход анилина — 98% от теоретического. [c.123]
Насколько сложны реакции дифосгена, ведущие к образованию соединений, представляющих собой как бы продукт действия двух молекул фосгена, можно судить nd взаимодействию дифосгена с анилином (вернее анилиновой водой) прн недостатке последнего [c.132]
Анилиновая вода. Насыщенный водный раствор анилина, перегнанного при 184°С. [c.266]
К подготовленному одним из указанных способов раствору, перенесенному в делительную воронку емкостью 50 мл, приливают 1 мл свежеприготовленного раствора бромциана в н-амиловом спирте, смесь взбалтывают, приливают 1 мл анилиновой воды, снова интенсивно взбалтывают в течение 2—3 мин и дают постоять 15—20 мин. Затем приливают 3 мл н-амилового спирта, сильно взбалтывают, дают слоям разделиться, сливают нижний водный слой, переносят слой амилового спирта в кювету для колориметрирования (расстояние между стенками 0,5 см) и определяют оптическую плотность, поместив во вторую кювету раствор, полученный в холостом опыте с 20 мл воды, в которую были прибавлены все указанные реактивы. Измерение проводят при длине волны проходящего света 450 ммк. Молярный коэффициент светопоглощения 5500. [c.267]
Анилиновый слой содержит 4,1—6,5% НгО (рис. 47), водный слой — 3,5—4,3% анилина (рис. 48). Сырой анилин перегоняется в вакууме. Из анилиновой воды анилин извлекается разными методами повторным испарением и возвращением в редуктор в виде острого пара ( анилиновый паровой котел ), ректи- [c.180]
Вакуум-отгонка анилина из реакционной массы. По окончании восстановления нитробензола в редукторе с паровой рубашкой реакционная масса нейтрализуется и передается в чугунный вакуум-перегонный куб. При вакуум-перегонке вначале отгоняется анилиновая вода, а затем товарный анилин. После отгонки 50% анилина масса становится вязкой, и для ее перемешивания требуется двигатель большой мощности. По окончании вакуум-перегонки из куба выгружает- [c.181]
Стоимость выделения анилина по первому методу (перегонка с паром всего анилина из реакционной массы, испарение анилиновой воды и возвращение ее в редуктор вместо острого пара), % 100 То же, при применении редуктора с паровой [c.182]
То же, при экстракции нитробен.толом анилина из анилиновой воды в обычном редукторе, % 64,5 То же, при применении редуктора с паровой рубашкой, %................49 [c.182]
Из редуктора суспензия железного шлама, в котором осталось более 40% анилина, перетекает в отгонный аппарат / (рис. 54). Отгонный аппарат по конструкции такой же, как и редуктор. Анилин и водяной пар конденсируются в аппарате 2, охлаждаемом водой. Конденсат попадает в отстойник шлама 4, в холодильник 5 и в сепаратор 6, в котором водный анилин отделяется от анилиновой воды. [c.187]
Анилиновая вода перегоняется в насадочной колонне непрерывного действия 15 без укрепляющей части. Куб колонны 16 обогревается острым паром. Разбавленная анилиновая вода из куба 16, охлажденная в холодильнике 17, возвращается в редуктор, а смесь анилина с водой — в сепаратор 6. Если баланс анилиновой воды почему-либо нарушился, то перед сбросом в канализацию анилин экстрагируют нитробензолом из избытка воды. [c.187]
Вследствие неодинаково активного окисления разных партий чугунной стружки необходим непрерывный контроль интенсивности образования железного шлама. Такой контроль ведется путем измерения магнитной проницаемости реакционной массы при помощи прибора с датчиком /4. Магнитная проницаемость реакционной массы зависит от содержания в ней недоокисленной стружки и концентрации шлама, поэтому датчик /4 связан с регулятором и подачи анилиновой воды. [c.283]
Подни.мающиеся из редуктора пары воды способствуют агломерации стружки на выходе из питателя. Во избежание этого част1, анилиновой воды подается по той же трубе, по которой заг[>ужается чугунная стружка. Основное количество полученного анилина отгоняется нз редуктора вместе с водяным паром, часть которого образуется вследствие выделения тепла реакции, а часть подводится через барботер 9. Расход пара стабилизируется регулятором 10. Пары анилина и воды направляются в конденсатор 13, шламовая жидкость непрерывно удаляется из редуктора через верхний боковой штуцер. [c.283]
В 4 мерные колбы (2 со стандартным раствором и 2 с испытуемым раствором) прибавляется по 2 мл анилиновой воды и по 2 мл бромроданистого реактива. [c.142]
Технические примечания. В производс пенном масштабе аннлин перегоняется с водяным паром, уже насыщенным анилином для этого паровой котел питают водой, полученной при этой перегонке. На заводе Вейлер-Тор Меера просто экстрагируют анилиновую воду нитробензолом, причем основание извлекается кз жидкости полностью, смссь нитробензола с анилином затем восстанавливается, как указано выше. Благодаря эгому становится ненужным применение парового котла с анклиноной водой, которое всегда спязано с некоторыми неудобствами. [c.72]
I, 2, 3—напорные бакн 4, 5, 6—регулирующие ротаметры 7—смеситель 8—насос 5—редуктор 10, /4—двигатели II—регулятор числа оборотов двигателя 12 — питатель для чугунной стружки ГЗ—вычислительное устройство /5—датчик прибора для определения магнитной проницаемости реакционаой массы 16—регулятор расхода анилиновой воды 17—регулятор расхода пара /8- ярибор для определения нитробензола в парах анилина /5—конденсатор 20, 2/— исполнительный механизм, переключающий краны. [c.104]
Далее, если вещество жидкое, то определяют его температуру кипения, если же твердое, то температуру плавления (см. ниже) при этом следует помнить, что некоторые твердые О. В. (напр., иприт, дифенилцианарсин, бромбензилцианид) могут, будучи в загрязненном состоянии, являться при обычной температуре жидкостями. После определения характерных температур, можно выделить из списка лишь немногие О. В., подходящие к данным опыта. Затем производятся простейшие пробы на присутстиие характерных элементов — мышьяка, серы, азота и галоида. После этих проб неизвестное О. В. может быть определено по таблицам с почти полной уверенностью. Для контроля следует испытать характерные свойства того О. В., которое определено — его растворимость, гидролиз, действие щелочей и характерных реактивов. Например, если предыдущие пробы указывают на дифосген, то следует применять, как реактив, анилиновую воду если иприт, — то реактив Гринь-яра и т. п. [c.199]
Как показывает второе уравнение, образующаяся при этом взаимодействии хлористоводородная кислота связывается избытком анилина с образованием легко растворимого в воде хлоргидрата анилина. Таким образом образовавшийся осадок дифенилмочевины после фильтрования дол5кен быть отмыт как от водного раствора анилина, так и от образовавшегося хлоргидрата анилина. Однако дифенилмочевина является веществом, слегка растворимым в воде, поэтому при промывке осадка водой и при проведении реакции с чистой анилиновой водой возможны потерн дифенилмочевины. Этим и обусловливается необходимость употребления при реакции с фосгеном анилиновой воды, насыщенной на холоду дифенилмочевиной. Последнее достигается пропусканием в анилиновую воду небольшого количества фосгена до появления опалесцен- [c.124]
В ряду Лукашевича на последнем месте стоит NaOH, активность которого в 120 раз меньше активности Nh5 I. Ионы ОН вообше замедляют реакцию восстановления нитробензола в анилин. При рН>12 реакция практически прекращается. Повышение pH и уменьшение скорости реакции восстановления нитробензола может быть вызвано введением солей щелочных металлов, понижением температуры и другими причинами. В одном из цехов по производству анилина в реактор возвращалась анилиновая вода, полученная после отгонки анилина из железного шлама, содержавшего хлористый аммоний. В анилиновой воде присутствовал аммиак, pH среды в реакторе повысился, и скорость реакции снизилась почти в 2 раза. После прекращения введения в реактор аммиака производительность аппарата повысилась до проектных норм. Сильное замедление реакции восстановлени я нитробензола наблюдается также в присутствии ионов SOI. [c.177]
Фильтрование реакционной массы. Из редуктора реакционная масса перекачивается на фильтрпрессы. Отфильтрованный шлам промывается водой, а фильтрат расслаивается на два слоя (сырой анилин и анилиновая вода, к которой присоединяется вода от промывки шлама). По утверждению П. Грогинса, потери анилина при этом методе составляют всего 1%, что соответствует остаточному содержанию его в шламе не более 0,05%. Данный метод не применяется в производстве анилина из-за плохой фильтруемости железного шлама. В про- [c.181]
Для непрерывного восстановления нитробензола применяют редуктор той же конструкции, что и при периодическом методе производства (рис. 51). Для ускорения реакции восстановления в редуктор 9 вводят самый активный электролит — хлористый аммоний, чугунную стружку (измельченную и очищенную от крупных и мелких частиц и примесей, обладающую повышенной активностью) и анилиновую воду как вместе с чугунной стружкой, так и с другими компонентами. Нитробензол, анилиновая вода и раствор НН4С1 смешиваются в смесителе 7 и нагнетаются под слой чугунной стружки через сопла под давлением , создаваемым насосом 8. Для интенсификации отгонки анилина в редуктор подают также небольшое количе ство пара. [c.183]
Ректификация анилиновой воды основана на следующих за шномерностях [c.187]
chem21.info
Анилин - это... Что такое Анилин?
Анили́н (фениламин) — органическое соединение с формулой C6H5Nh3, простейший ароматический амин.
Представляет собой бесцветную маслянистую жидкость с характерным запахом, немного тяжелее воды и плохо в ней растворим, хорошо растворяется в органических растворителях. На воздухе быстро окисляется и приобретает красно-бурую окраску. Ядовит. Название «анилин» происходит от названия одного из растений, содержащих индиго — Indigofera anil (современное международное название растения — Indigofera suffruticosa).История
Впервые анилин был получен в 1826 году при перегонке индиго с известью немецким химиком Отто Унфердорбеном (нем. Otto Unverdorben), который дал ему название «кристаллин».
В 1834 Ф. Pyнгe обнаружил анилин в каменно-угольной смоле и назвал «кианолом».
В 1841 Ю. Ф. Фришце получил анилин нагреванием индиго с раствором KOH и назвал его «анилином».
В 1842 анилин был получен Н. Н. Зининым восстановлением нитробензола действием (Nh5)2S и назван им «бензидамом».
В 1843 А. В. Гофман установил идентичность всех перечисленных соединений.
Промышленное производство фиолетового красителя мовеина на основе анилина началось в 1856 году.
Получение
В промышленности анилин получают в две стадии. На первой стадии бензол нитруется смесью концентрированной азотной и серной кислот при температуре 50 - 60°C в результате образуется нитробензол. На втором этапе нитробензол гидрируют при температуре 200-300°C в присутствии катализаторов

Впервые восстановление нитробензола было произведено с помощью железа:

Другим способом получение анилина является восстановление нитросоединений — Реакция Зинина:

Химические свойства
Для анилина характерны реакции как по аминогруппе, так и по ароматическому кольцу. Особенности этих реакций обусловлены взаимным влиянием атомов. С одной стороны, бензольное кольцо ослабляет основные свойства аминогруппы по сравнению с алифатическими аминами и даже с аммиаком. С другой стороны, под влиянием аминогруппы бензольное кольцо становится более активным в реакциях замещения, чем бензол. Например, анилин энергично реагирует с бромной водой с образованием 2,4,6-триброманилина (белый осадок).
Окисление
В отличие от аминов алифатического ряда, ароматические амины легко окисляются. Примером может служить реакция хромовой смеси с анилином, в результате образуется краситель «черный анилин».
Реакции электрофильного замещения
Аминогруппа являясь заместителем первого рода оказывает сильное активирующее влияние на бензольное ядро, что при нитровании может произойти окисление молекулы анилина, для предотвращения окисления аминогруппу перед нитрованием «защищают» ацилированием
Реакции на азот
Другие реакции
Гидрирование анилина в присутствии никелевого катализатора дает циклогексиламин.
Производство и применение
Изначально анилин получали восстановлением нитробензола молекулярным водородом; практический выход анилина не превышал 15 %. При взаимодействии концентрированной соляной кислоты с железом выделялся атомарный водород, более химически активный по сравнению с молекулярным. Реакция Зинина является более эффективным методом получения анилина. В реакционную массу вливали нитробензол, который восстанавливается до анилина.
По состоянию на 2002 год, в мире основная часть производимого анилина используется для производства метилдиизоцианатов, используемых затем для производства полиуретанов. Анилин также используется при производстве искусственных каучуков, гербицидов и красителей (фиолетового красителя мовеина).[1]
В России он в основном применяется в качестве полупродукта в производстве красителей, взрывчатых веществ и лекарственных средств (сульфаниламидные препараты), но в связи с ожидаемым ростом производства полиуретанов возможно значительное изменение картины в среднесрочной перспективе.
Токсичные свойства
Анилин оказывает негативное воздействие на центральную нервную систему. Вызывает кислородное голодание организма за счёт образования в крови метгемоглобина, гемолиза и дегенеративных изменений эритроцитов.
В организм анилин проникает при дыхании, в виде паров, а также через кожу и слизистые оболочки. Всасывание через кожу усиливается при нагреве воздуха или приёме алкоголя.
При лёгком отравлении анилином наблюдаются слабость, головокружение, головная боль, синюшность губ, ушных раковин и ногтей. При отравлениях средней тяжести также наблюдаются тошнота, рвота, иногда, шатающаяся походка, учащение пульса. Тяжёлые случаи отравления крайне редки.
При хроническом отравлении анилином (анилизм) возникают токсический гепатит, а также нервно-психические нарушения, расстройство сна, снижение памяти и т. д.
При отравлении анилином необходимо прежде всего удаление пострадавшего из очага отравления, обмывание тёплой (но не горячей!) водой. Так же вдыхание кислорода с карбогеном. Также применяют введение антидотов (метиленовая синь), сердечно-сосудистые средства. Пострадавшему надо обеспечить покой.
Предельно допустимая концентрация анилина в воздухе рабочей зоны 3 мг/м3. В водоёмах (при их промышленном загрязнении) 0,1 мг/л (100 мг/м3).[2]
См. также
Примечания
Литература
Артеменко А.И. - Органическая химия - 1987.
Ссылки
dic.academic.ru
Свойства и применение анилина
Анилин - органическое вещество. Впервые его получили в 1826 году. Другие названия – фениламин, аминобензол. Наименование «анилин» произошло от названия растения «индигофера анил», в котором содержится индиго. Раньше фениламин создавался с участием этого вещества. Рассмотрим свойства и применение анилина.
Вещество относится к простейшим ароматическим аминам. Его формула C6H5Nh3.
Физические свойства анилина
Ядовитое вещество, пары которого токсичны. Представляет собой маслянистую жидкость, не имеющую цвета. Запах слабый, характерный именно для этого вещества. При его возгорании пламя яркое, коптящее.
Частично растворим в воде (при температуре кипения растворимость 6,4 %). Минерализованная вода понижает его растворимость, за исключением содержания бромидов лития и цезия, а также йодида цезия. Последний, наоборот, повышает растворимость анилина.
При хранении вещество темнеет, особенно быстро это происходит при воздействии воздуха и света. При этом он делается более вязким. Иначе данный процесс называют «аутооксидацией». Окисление может быть замедленно при помощи добавления антиоксидантов – щавелевой кислоты, гидро- и тиосульфата натрия.
Ниже приведены характеристики анилина при нормальном атмосферном давлении:
- температура кипения - 184,4 °С;
- температура плавления/замерзания – минус 5,89 °С;
- плотность при температуре 20 °С - 1,02 г/см куб.;
- температура самовоспламенения на воздухе - 562 °C;
- температура вспышки на воздухе – 79 °C.
Основные области применения анилина
В России вещество в основном применяют для синтеза красителей и лекарственных средств, в текстильной и фармацевтической промышленности. С помощью анилина получают препараты группы сульфамидов, обладающие антибактериальным действием, а также синтезируют заменители сахара.
Существуют и другие области применения аниолина. В химии его используют для получения гидрохинона – вещества, использующегося в косметике, в основном в составе отбеливающих кожу средств. Также вещество применяется в создании взрывчатых веществ, клеев, герметиков.
При помощи анилина замедляется коррозия металлов: его фосфаты добавляют к растворам сильных электролитов, в результате чего ингибируется коррозия углеродистой стали.
Применяют анилин и для повышения антидетонационности топлива (автомобильного, ракетного, авиационного). Октановое число бензина при однопроцентном содержании анилина повышается на 3 единицы и более. Но в чистом виде вещество стараются не использовать, так как при длительном хранении понижается качество бензина с анилином, а также токсичность его газов. Чаще используются производные вещества. В ряде западных государств существуют ограничения на применение анилина в составе топлива.
В мире большая часть получаемого анилина используется в производстве полиуретанов, а также синтетических каучуков, красок, средств от сорняков.
Анилиновые красители
Самой главной сферой применения анилина было и остается производство красителей. Они изготовляются при помощи окисления анилина и его солей.
Первоначально анилиновые краски выпускались только в форме порошка. В СССР им находили применение в быту, реставрируя и переделывая вещи посредством их окраски. Но покрашенные вещи быстро блёкли при попадании солнечного света, краска вымывалась в процессе стирки. В настоящее время анилиновые красители производятся и в форме растворов, причем некоторые производители выпускают концентрированные растворы, которые в отличие от порошков не требуют особой подготовки ткани. Но, несмотря на ощутимый прогресс и улучшение красителей, ткани, покрашенные ими, по-прежнему быстро выгорают на солнце.
Токсичность анилина
Анилин - токсичное вещество. Может угнетать нервную систему, при попадании в кровь вызывает кислородное голодание тканей. Попасть в организм может в виде паров, а также проникнуть через кожу и слизистые оболочки.
Сейчас отравления анилином бывают редко. Опасность это вещество представляет в основном для тех, кто работает с ним. Во избежание попадания токсина в организм нужно соблюдать установленные меры безопасности. При окрашивании дома вещей анилиновыми красителями, в особенности порошковыми, нужно беречь их от детей, проветривать помещение, в котором производится окраска, не глотать вещество, при попадании на части тела немедленно смывать его водой и производить окрашивание в перчатках. Если анилин был случайно проглочен, нужно незамедлительно обращаться к врачу.
fb.ru


















