Жесткость воды – единицы измерения и способы умягчения. Жесткость воды питьевой
Норма жесткости питьевой воды - как определить и формула расчета
Повышение внимания к норме жёсткости питьевой воды связано с повсеместным распространением стиральных и посудомоечных машин, поскольку определение расчётной загрузки моющих средств и частота очистки машин зависит от фактической степени жёсткости. Однако единицы измерения этого показателя в разных странах отличаются, а, кроме того, отличаются и составляющие для каждой из специфических единиц измерения.
Что такое жёсткая вода и что на неё влияет?
Степень жёсткости воды определяется как совокупность свойств, зависящих от содержания магния, кальция и других растворённых солей. Общий показатель складывается из постоянной и временной составляющей:
- Временная (карбонатная) устраняется кипячением благодаря способности ряда солей выпадать в осадок с образованием накипи. Характеризуется наличием бикарбонатов магния и кальция – при рН>8.3.
- Постоянная (некарбонатная) сохраняется при кипячении. Характеризуется наличием солей магния и кальция хлоридных, сульфатных и нитратных анионов.

На величину жёсткости влияют следующие факторы:
- интенсивность растворения гидропотоками горных пород (известняков, доломитов),
- использование подземных или поверхностных вод (поверхностные при прочих равных более «мягкие»),
- сезонные колебания для поверхностных ресурсов (показатель максимальной «мягкости» отмечается в периоды паводков и половодий с активным поступлением дождевых и талых «пополнений» в источники водоснабжения, а минимальная «мягкость» приходится на зимний период).
Единицы измерения, формулы и расчёты
В России единица измерения содержания солей по данному параметру называется «градус жёсткости» (°Ж), который с помощью распространённых онлайн-калькуляторов пересчитывается в единицы измерения, принятые в других странах (см. таблицу).
| Страна | Единицы измерения | Россия | Германия | Великобритания | Франция | США |
| Россия | 0Ж | 1 | 2.8 | 3.51 | 5 | 50.4 |
| Германия | 0DH | 0.357 | 1 | 1.25 | 1.78 | 17.84 |
| Великобритания | 0Clark | 0.285 | 0.8 | 1 | 1.43 | 14.3 |
| Франция | 0F | 0.20 | 0.56 | 0.70 | 1 | 10 |
| США | ppm | 0.02 | 0.056 | 0.070 | 0.10 | 1 |
Так 1°Ж = 2,8°DH = 3,51°Clark = 5°F = 50,04ppm.
Каждая величина соответствует следующим показателям для воды:
- 1°Ж = 20,04 мг Ca2+ или 12,15 Mg2+ в 1 дм3
- 1°DH = 10 мг CaO в 1 дм3
- 1°Clark = 10 мг CaCO3 в 0,7 дм3
- 1°F = 10 мг CaCO3 в 1 дм3
- 1 ppm = 1 мг CaCO3 в 1 дм3
1°Ж = 1 мг-экв/л (чаще используют в практике) = 1/2 моль/м3 = 20,04 миллиграмма ионов Ca2+ (или 12,16 миллиграмма ионов Mg2+)
Формула расчёта жёсткости воды при карбонатном типе:
- Ca2+ + 2HCO3- (при нагревании)= CaCO3↓ + h3O + CO2↑
- Mg2+ + 2HCO3- (при нагревании)= MgCO3↓ + h3O + CO2↑
Общая °Ж определяется как сумма временной и постоянной: Hобщ = Нкарб + Ннекарб
Нормативные требования
- Российские нормативы – СанПиН-ы 2.1.4.1074-01; ГН 2.1.5.1315-03 – определяют норму жёсткости питьевой воды в пределах 7°Ж с установлением нормативного значения для магния – в пределах 50 мг/л и не регламентируя его для кальция.
- Для бутилированного продукта, по СанПиН-ам 2.1.4.1116-02: °Ж находится в интервале 1,5-7 с показателями 25-130 мг/л/кальций, 5-65 мг/л/магний.
- Рекомендации ВОЗ для питьевой воды °Ж не регламентируют, определяя при этом норму 20-80 мг/л/кальций, 10-30 мг/л/магний, что ниже российских нормативных значений, однако фактические значения при водообеспечении, например, для Москвы, укладываются в рекомендации ВОЗ.
По данным московского водоканала, для Москвы (по сравнению с остальными крупными городами мира), характерны следующие показатели (см. таблицу):
| Жесткость, Ж | Кальций, мг/л | Магний, мг/л | |
| Москва | 2,0 - 5,5 | 46 | 11 |
| Париж | 5,0 - 6,0 | 90 | 6 |
| Берлин | 5,0 - 8,8 | 121 | 12 |
| Нью-Йорк | 0,3 - 0,4 | 6 | 1 |
| Сидней | 0,2 - 1,3 | 15 | 4 |
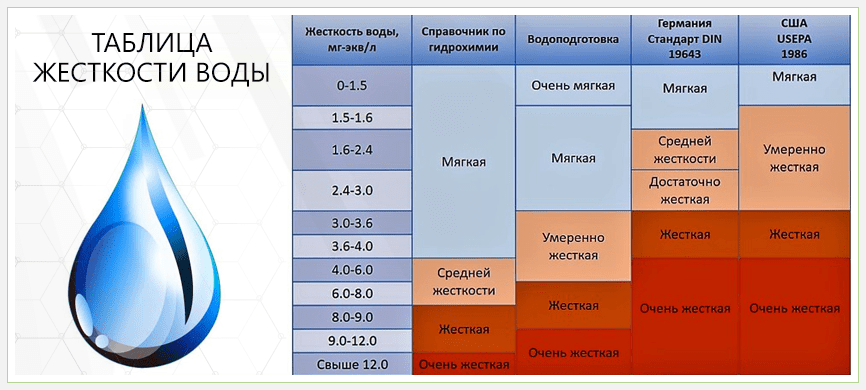
Если определять степень мягкости по 3 категориям, то деление соответствует следующим величинам:
- до 2°Ж – мягкая,
- в интервале 2-10°Ж – средне-жёсткая,
- свыше 10°Ж – жёсткая.
В некоторых случаях эта шкала детализируется, нередко со смещением, однако для конкретных ситуаций лучше применять не описательные, а точные значения градусов. Так жёсткость воды в аквариуме в норме составляет 3-15°Ж с разделением предпочитаемых интервалов для каждого вида рыб, моллюсков, водорослей. Например, раковина улиток остаётся в лучшем состоянии в жёсткой воде, а для живородящих рыб предпочтителен диапазон в 6-10°Ж. При этом следует учитывать, что содержание кальция в водной среде будет постепенно снижаться за счёт усвоения его обитателями аквариума.
В домашних условиях, помимо кипячения, применяют следующие способы смягчения:
- Реагентный – основан на добавлении кальцинированной соды или гашеной извести с выпадением в осадок нерастворимых соединений солей магния и кальция. Одним из самых эффективных реагентов считается ортофосфат натрия, способный снизить градус до 0,05°Ж.
- Мембранный – благодаря нанофильтрации и обратному осмосу полупронецаемой мембраны задерживаются ионы.
- Магнитный – благодаря магнитогидродинамическому резонансу карбонат кальция не кристаллизуется, а модифицируется в арагонит, который не откладывается на теплообменных поверхностях.
При этом различного типа аэраторные насадки на кран и экономители с поворотным механизмом (http://water-save.com/) благодаря постоянному механическому сдвигу шарниров в незначительной мере могут повлиять на образование накипи, однако ни остановить её образование, ни снизить значение °Ж не способны.
Читайте далее
Оставьте комментарий и вступите в дискуссию
hitropop.com
Жесткость воды - норма и ее влияние на качество жизни
Жесткостью воды называют химическое качество, определяющее объем присутствующих в жидкости примесей соляного кальция и магния. Данный показатель - одно из ключевых качеств воды, которое всегда проверяется в процессе анализа жидкости на предмет пригодности для употребления и бытового применения. Знать о норме показателей и о том, как определить жесткость воды, крайне важно. Знание данного качества жидкости позволит сохранить здоровье и продлить работоспособность техники, так или иначе использующей в своей работе воду.Микробиологические исследования и химические научные опыты определили, что жесткостью воды единицы измерения является содержание в ней большей части солей кальция (Са2+) и несколько меньшего количества магния (Mg2+). На самом деле ситуация обстоит так, что оба эти элементы участвуют в формировании показатель определения жесткости воды и не могут существовать отдельно. В процессе химических реакций с анионами, соли кальция и магний формируют специальные кристаллы жесткости, которые оседают на дно и в дальнейшем используются в качестве биологического материала при проверке воды и ее химического состава.
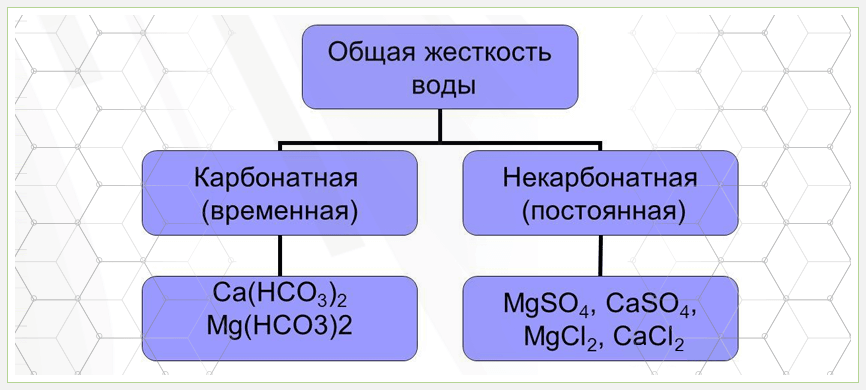
Таблица наличия в воде катионов металлов и анионов и тест на жесткость воды позволяют узнать детальней о процессе формирования кристаллов жесткости и характере их развития. Влияние на временную жесткость воды и каждого из металлов является различным и зависит от типа жидкости и источника ее происхождения. К примеру такие металлы, как стронций, железо и марганец могут оказывать на состав и степень жесткости воды менее выраженное воздействие и практически не котироваться при анализе и проведении химической экспертизы. Алюминий оказывает влияние на общую жесткость воды, только если кислотность воды достигает нужного уровня, что встречается исключительно в природных водоемах. Из этого следует, что наличие и патогенное воздействие на воду выше указанных металлов при проверке воды бытового использования практически не учитывается из-за крайне низких показателей. Крайне малое влияние на показатель жесткости воды и способы ее устранения также может оказывать барий.
Какие можно выделить типы жесткости воды?
Проверка воды на показатель жесткости проводится в несколько этапов, с учетом типа водоема, в котором был произведен забор, условий содержания жидкости и цели произведенной экспертизы. Как определить жесткость воды в домашних условиях? Чаще всего жесткость при проверке делят на следующие группы:- Жесткость воды общего типа. В процессе определения вида жесткости воды этого показателя выводится единица наибольшей концентрации солей кальция и магния. Данный показатель рассчитывается путем выведения данных о постоянной жесткости воды и непостоянной, временной жесткости некарбонатного типа. Для того чтобы смягчить воду при завышенных показателях общей жесткости используют ионизирующие фильтрующие установки для воды и таблицу жесткости воды.
- Жесткость карбонатного типа. Проверка позволяет выявить наличие в составе воды карбонатных и гидрокарбонатных элементов солей кальция и магния. Такой вид жесткости нередко может называться временным, поскольку устранить завышенные показатели поможет кипячение и вываривание лишних солей. Нагревание воды способствует тому, что гидрокарбонаты и карбонаты кальция и магния раскладываются и становятся осадочным веществом на дне посудины. Такой тип не постоянной жесткости воды превращается в бытовой налет, который нередко можно наблюдать на посуде, в которой часто кипятится вода. Как устранить жесткость воды? Очистить жесткость такой воды можно также путем использования ионизирующих фильтров или механизмов для устранения лишних солей.
- Жесткость воды некарбонатного типа. Данный тип проверки позволяет выявить в воде присутствие кислот солей кальция и магния сильного воздействия. В число таких кислот входят серная, азотная и соляная кислоты. Данный вид не карбонатной жесткости воды нельзя устранить простым кипячением воды и вывариванием патогенных элементов. Постоянную жесткость нередко очищают ионизирующими фильтрами или растворяющими соль веществами.
В чем измеряется жесткость воды? Стоит отметить, что мировая таблица единиц измерений имеет несколько разных обозначений для типов и разновидностей жесткости. Каждая из этих единиц взаимосвязана с остальными. На территории постсоветского пространства до их пор используют единицу моль для обозначения показателя определения общей жесткости воды. В европейских государствах могут нередко использовать такие обозначения как do, dH, fo. В США используется обозначение ppm CaCO3.
Позвоните сейчас и получите бесплатную консультацию специалиста
Почему вода становится жесткой?
Изначально стоит отметить, что вся жидкость мирового океана имеет определенные показатели жесткости, то есть в ее химическом составе неизменными веществами являются соли кальция и магний, а также несколько других щелочных металлов и земельных веществ. От чего зависит жесткость воды? Такой состав жидкости обуславливается тем, что минеральные воды изначально проистекают на поверхность из залежей многовековых пластов известняка и разных типов доломита. Соли кальция и магний попадают в воду путем химической связи диоксида углерода с группой минералов. Процесс выветривания и химической деформации горных пород приводит к образованию кристаллов жесткости в воде. Их источники - природные залежи известняков, гипса и доломитов. Ионизирующие вещества многовековых залежей, через которые протекает вода, могут появляться из-за еще не изученных биологических реакций и процессов в глубине плит на месте, из которого проистекает жидкость. Добавлять в состав побочные минералы и кристаллы способны и другие химические примеси, сточные воды, элементы и организмы окружающей среды.
Что показывает таблица жесткости воды?
Большинство минерализованной воды, которая попадает в открытые водоемы и становится источником жидкости для бытового и промышленного существования, имеет жесткость, превышающую показатели 75-85%. Как проверить жесткость воды в домашних условиях? Такой высокий показатель свидетельствует о том, что вода содержит повышенное количество солей кальция и магния из-за наличия ионизирующих горных пород. С учетом источника минеральной воды, в ряде случаев уровень жесткости не превышать 60%. Важно отметить, что от показателя минерализации напрямую зависит наличие ионов кальция. Жесткость воды, норма для питьевой воды такова: в открытых водоемах с пресной водой уровень содержания кальция не поднимается выше, чем 1 г из расчета на литр воды; соленые водоемы могут содержать примерно 10-15 г солей кальция на литр.
Стоит сказать, что показатель жесткости и концентрация солей кальция в воде напрямую определяется типом воды и местом ее расположения. Так, поверхностные воды нередко могут иметь наиболее низкие показатели жесткости, тогда как подземные водоемы или озера могут быть максимально жесткими и насыщенными солями. Концентрация солей в воде находится также в прямой зависимости от времен года и сезонных осадков. В конце зимы наличие кристаллов жесткости может увеличиваться, однако в период таяния снега и выпадения мягкой воды в виде снега и дождя кристаллы солей разбавляются и показатели жесткости заметно снижаются. Максимально жесткой вода считается в океанах и морях, где концентрация солей является максимально высокой.
Как может влиять показатель жесткости на качество жидкости?
Жесткость воды и ее показатели являются позволительными и удовлетворительными, в зависимости от цели использования жидкости. Если вода предназначается для использования в бытовых целях, показатели ее жесткости не должны превышать 2-6 мг на литр. Такая концентрация солей кальция считается максимально допустимой для бытового использования и не вредит человеческому здоровью. Прибор для измерения жесткости воды показывает, что промышленные цели использования воды могут повышать показатель жесткости до 10 мг на литр, однако не более этих рамок. Важно отметить, что вода с высоким показателем жесткости является, как правило, слишком горькой и имеет характерный запах, а также может оказывать патогенное воздействие на пищеварительную систему и желудочно-кишечный тракт, что делает ее непригодной для использования в пищевых или бытовых целях.
Важно сказать, что Всемирная организация здравоохранения проводит множество исследований и до сих пор не может найти единого ответа на вопрос о том, насколько велика патогенность влияния жесткой воды на человеческий организм и полезно ли постоянное использование в пищу только мягкой и фильтрованной воды без примесей солей и кальция. Предварительные исследования говорят о том, что некоторые типы вод с повышенным показателем жесткости могут провоцировать сердечно-сосудистые заболевания, проблемы с суставами и каменные болезни.
Специалисты компании ЭкоТестЭкспресс производят качественную аналитику жесткости воды в зависимости от требуемых целей и особенностей проверки. Связаться с нами, оставить заявку можно в онлайн-форме ниже.
ecotestexpress.ru
Норма жесткости питьевой воды. Какая нормальная жесткость воды
30 октября 2017 / 2023 просмотров
Один из важных показателей качества воды – это её жёсткость. Жёсткость воды определяется наличием в ней солей кальция и магния. Это так называемые «соли жёсткости». Для нормального функционирования организма необходимо, чтобы их концентрация была в норме. Если же этот показатель превышен, то вода считается жёсткой. Насколько употребление такой воды опасно для здоровья человека? Давайте разберёмся.
Норма жёсткости питьевой воды: что мы пьём
Согласно государственным санитарным нормам, максимально допустимая жёсткость воды – не больше 7 ммоль/дм3. Более жёсткой является вода из подземных источников, особенно, если данная местность богата солями кальция и магния. Жёсткость воды из поверхностных источников относительно невысокая.
Жёсткая вода содержит переизбыток солей кальция и магния. По словам специалистов лаборатории «УкрХимАнализ», по такому показателю как жёсткость бракуется около половины всех исследуемых образцов. Впрочем, заподозрить, что показатель жёсткости воды превышен, можно и без специального анализа. Быстро появляется накипь на чайнике? Чай и кофе кажутся невкусными? Плохо пенятся моющие средства? Барахлит сантехника? Причиной всех этих проблем может быть именно повышенная жёсткость воды. При этом налёт на чайнике вы видите сразу, а вот проблемы с бытовой техникой (например, стиральной и посудомоечной машиной) станут заметны лишь со временем, когда уже будет необходим серьёзный ремонт. Ведь накипь образуется на внутренних поверхностях (деталях барабана, нагревательных элементах и т.п.).
Но проблемы с бытовыми приборами – это ещё пол-беды. Гораздо хуже, что превышение нормы жёсткости воды для питья может привести к серьёзным последствиям для здоровья.
Постоянно употребляя жёсткую воду, вы можете заметить, что существенно ухудшилось состояние кожи и волос. Кожа становится сухой, а волосы ломкими, тусклыми, может появиться перхоть. И это только внешние проявления. Соли откладываются в организме, что приводит к болезням суставов, а также появлению камней в почках и жёлчном пузыре.
Какая норма жёсткости воды: оптимальный показатель
Слишком жёсткая вода, как и чересчур мягкая неполезна для здоровья – утверждают специалисты. Нормальная жёсткость воды – около 3 – 4 ммоль/дм3. По результатам мониторинга, проведённого в 2014 году в разных городах Украины, повышенной жёсткостью характеризуется вода во Львове и Харькове. Дело в том, что источниками водоснабжения здесь являются подземные водоносные горизонты, а также водохранилище, подпитываемые подземными водами. В таких областных центрах как Днипро, Черкассы, Одесса, Николаев, а также Киев – нормальная жёсткость воды, соответствующая среднему показателю. Причина в том, что водоснабжение здесь идёт из поверхностных источников.
Жёсткость воды может измеряется в разных единицах, в разных странах приняты свои стандарты. Например, в Украине жёсткость может измеряться как в ммоль/дм3, так и в мг-экв/л. Так, 1 ммоль/дм3 – это 2 мг-экв/л. Также в Интернете или специальной литературе легко найти таблицу жёсткости воды, позволяющую перевести отечественные показатели жёсткости воды в единицы, принятые за рубежом (в Германии, Франции, США и т.п.).
Жёсткость воды: заботимся о здоровье
Итак, мы разобрались, какая жёсткость воды является оптимальной для организма. Как же узнать, соответствует ли вода в вашем кране этим нормам? Необходимо сделать анализ воды на жёсткость. Лаборатория «УкрХимАнализ» предлагает различные пакеты «Базовый» (20 показателей), «Расширенный» (30 показателей), «Максимальный» (50 показателей). Если результаты анализа показали, что вода слишком жёсткая или находится на пределе нормы, то возможный вариант решения проблемы – установка фильтра-умягчителя воды. Если же, кроме повышенной жёсткости, есть и другие несоответствия, то специалисты лаборатории помогут в выборе подходящего прибора, чтобы исправить ситуацию.
У Вас есть вопросы или Вам нужна консультация?
Заполните форму и получите бесплатную консультацию!
Читайте похожие статьи:
himanaliz.ua
Жёсткость воды - единицы измерения, методы устранения и последствия для здоровья
 Обычная вода состоит не только из атомов водорода и кислорода, в ней так же присутствует большое количество различных примесей. Именно наличие примесей определяет жесткость воды, а единицы измерения (°Ж – градус жёсткости) показывает, насколько этот показатель превышает допустимые нормы.
Обычная вода состоит не только из атомов водорода и кислорода, в ней так же присутствует большое количество различных примесей. Именно наличие примесей определяет жесткость воды, а единицы измерения (°Ж – градус жёсткости) показывает, насколько этот показатель превышает допустимые нормы.
Жёсткость воды требуется определять не только инженерам, которые занимаются прокладкой коммуникаций, но и обычной людям в быту. Если мы используем электрический чайник или стиральную машину с функцией нагрева воды, то все это может выйти из строя, если данный показатель будет слишком высок. Даже хорошо растворить мыло в такой воде у вас вряд ли получится.
О том, как определить уровень жесткости водопроводной воды, а также о методах борьбы с большим содержанием примесей будет подробно рассказано в данной статье.
Краткое содержание статьи
Жёсткая и мягкая вода – в чём разница
На количество соли в воде влияет наличия растворённых в ней элементов кальция и магния. Значительно повысить этот показатель может также наличие гидрата железа, содержание которого в артезианских водах бывает избыточным.
В том случае, когда таких примесей содержится незначительное количество, её называют “мягкой”. Этот показатель обычно разделяется на 3 категории:
- Мягкая.
- Средняя.
- Жёсткая.
 Мягкая – это дождевая или полученная в результате перегонки жидкость. В такой воде практически отсутствуют минеральные примеси.
Мягкая – это дождевая или полученная в результате перегонки жидкость. В такой воде практически отсутствуют минеральные примеси.
В большинстве случаев она может получиться и в результате длительного кипячения или добавления специальных химических реагентов.
Средняя – встречается наиболее часто в водопроводных системах, а также в родниковой и артезианской воде.
Жёсткая – к данной категории относится морская, океанская, а также вода вытекающая из пластов породы богатой минеральными отложениями. В ней может быть растворено большое количество солей. Если брать в процентном соотношении, то соленость может достигать до 33% от общего объема.
Рассмотрим разновидности жёсткости
Этот показатель принято разделять на следующие категории.
- Постоянная – является неизменным показателем, который зависит от содержания сульфатов и хлоридов.
- Временная – обусловлена содержанием бикарбонатов кальция и магния. Название этот вид жёсткости получил за способность практически полностью нейтрализоваться в результате кипячения.
- Жёсткость общая – получается в результате сложения показателей постоянной и временной.
Для того чтобы точно определить этот показатель, необходимо знать какими единицами измерения это можно сделать.
Единицы измерения жёсткости
Для правильного подсчёта уровня жёсткости необходимо определить концентрацию катионов кальция и магния. В настоящее время этот показатель определяется в следующих единицах измерения:
- Моль/м3 (моль на кубический метр) – применялся в России до 2014 г.
- °Ж (градус жёсткости) – данная единица измерения используется в России с 2014 г.
- dH (немецкий градус) – единица измерения используется в странах Европы.
- fo (французский градус) – также применяется в европейский странах.
- ppm CaCO3 (американский градус) – единица измерения используется в североамериканских штатах.
Следует отметить, что в нашей стране выражение общей жёсткости моль/м3 стало использоваться только с 1952 года. До этого времени расчёты осуществлялись в градусах, которые были равны современному немецкому градусу.
С 2014 года в России действует международный стандарт подсчёта жёсткости, который выражается в градусах (°Ж). Один градус равен 1/2 миллимоля на литр жидкости, поэтому подсчитать уровень концентрации вещества в жидкости не составит большого труда.
Причины появления жёсткости воды
 При круговороте воды в природе жидкость превращается в пар и поднимается в верхние слои атмосферы. После конденсации она выпадает в виде осадков и не содержит примесей влияющих на жёсткость, но проходя через слой земной коры, жидкость растворяет различные породы, в которых содержатся калий и магний. Насыщаясь этими элементами вода увеличивает свою жёсткость. В море она всегда жёсткая по причине большой концентрации хлорида натрия.
При круговороте воды в природе жидкость превращается в пар и поднимается в верхние слои атмосферы. После конденсации она выпадает в виде осадков и не содержит примесей влияющих на жёсткость, но проходя через слой земной коры, жидкость растворяет различные породы, в которых содержатся калий и магний. Насыщаясь этими элементами вода увеличивает свою жёсткость. В море она всегда жёсткая по причине большой концентрации хлорида натрия.
При необходимости снизить концентрацию ионов калия и магния, можно применить различные методы уменьшения количества солевых примесей.
Методы устранения жёсткости
Для борьбы с чрезмерным содержанием солей применяются следующие методы:
- Кипячение – полностью устраняет временную жёсткость. Данный процесс сопровождается обильным выпадением осадка на дне и стенках резервуара, где происходит кипячение.

- Химическим путём – уменьшить количество солей можно с помощью гашённой извести. Если к извести будет добавлена сода, то можно избавиться и от постоянной жёсткости
- Заморозка – данный метод позволяет легко справиться с постоянной жёсткостью. Чтобы смягчить воду достаточно заморозить её до такого состояния, когда будет не более 10% воды, а 90% льда. Затем незамерзшая жидкость сливается, а вода в твёрдом состоянии растапливается и используется по назначению.
- Перегонка – все соли являются нелетучими веществами, поэтому достаточно воду сначала превратить в пар с помощью нагрева, а затем конденсировать.
- Электромагнитный способ – для смягчения жидкости используется электромагнитное поле. Данный способ уменьшения солей в воде применяется наиболее часто в котельных установках.
- Катионный обмен – высокоэффективный способ очистки воды от избыточного количество солей. Очищение происходит при пропускании воды через слой катионита.

Любой из предложенных способов умягчения воды позволяет справиться с высоким уровнем этого показателя, но для очистки от солей питьевой воды химический способ обычно не применяется.
Как влияет жёсткость на качество воды
Жёсткость питьевой воды влияет, прежде всего, на её вкусовые качества. Порог вкуса ионов кальция находящихся в питьевой воде составляет 2-6 мг-экв/л. Порог вкуса для ионов магния значительно ниже, поэтому самой приятной на вкус питьевой водой считается та, в которой этот показатель равен от 1,6 до 3 мг-экв/л.
В некоторых случаях вода с жёсткостью до 10 мг-экв/л может использоваться в качестве питьевой, но длительное её употребление может негативно влиять на здоровье человека. Слишком жёсткая вода нежелательна для применения в устройствах нагрева жидкости. Электрические чайники, бойлеры, стиральные и посудомоечные машины обязательно имеют в своей конструкции ТЭН, который в кратчайшие сроки “обрастает” отложениями, и процесс нагрева жидкости осуществляется менее эффективно.
Длительная эксплуатация электро нагревателя со значительным слоем накипи приводит к перегреву элемента и выходу его из строя. К счастью, для очистки от накипи достаточно растворить 2 пакетика лимонной кислоты в 1 литре воды и хорошо прокипятить чайник или любой другой водонагреватель. После чего следует тщательно промыть прибор и использовать его далее по назначению.
Смотреть видео
Негативно влияет высокое содержание солей воды и на процесс стирки. Растворение моющего вещества в воде богатой ионами калия и магния приводит к чрезмерному образованию пены. Пена способствует образованию налёта на элементах стиральной машины, который также может негативно влиять на работоспособность некоторых узлов этого бытового прибора.
Последствия для здоровья человека
При длительном употреблении жёсткой воды в организме человека наблюдаются серьёзные отклонения от нормы, которые прежде всего проявляются в работе следующих органов:
- Желудочно-кишечный тракт (ЖКТ) – при соединении солей входящих в состав жёсткой воды с животными жирами образуются соли жирных кислот, которые обволакивая стенки желудка и кишечника, препятствуя нормальной ферментации и значительно затормаживают перистальтику. В результате в организме накапливаются вредные вещества и шлаки, развивается дисбактериоз.
- Работа суставов – некоторые виды солей попадая в организм человека образуют неорганические вещества, которые со временем вытесняют синовиальную жидкость из суставов. В результате такого замещения происходит обрастание суставов кристаллами, которые вызывают сильную боль при движении. Длительное употребление жёсткой воды может привести к заболеванию артритом и полиартритом.
- Сердечно-сосудистая система – при значительном увеличении показателя жесткости питьевой воды, работа сердца ухудшается, вплоть до проявления выраженной аритмии.
- Состояние кожных покровов – жёсткая вода приводит к преждевременному старению кожи. Негативное воздействие наблюдается как при приёме жидкости внутрь, так и при мытье посуды. При контакте средства для мытья посуды с жёсткой водой образуется плёнка, которая при оседании на кожу долгое время оказывает негативное влияние на верхние слои эпидермиса.
- Образование камней в почках – данное утверждение является мифом, который развенчан благодаря работе учёных. Процесс камнеобразования не зависит от качества питьевой воды. Камни в почках образуются в основном из-за нехватки кальция в организме. В результате дефицита этого элемента происходит вымывание его из костей с оседанием в мочевыводящей системе.
Смотреть видео
Всех перечисленных недугов и болезненных состояний можно избежать, если использовать многоступенчатую фильтрацию воды. Применение таких устройств не будет стоить слишком дорого, а вот лечение различных патологий может обойтись в значительные суммы денег.
Методы определения жёсткости воды
Чтобы избежать негативного влияния на здоровье жёсткой воды, а также продлить срок эксплуатации нагревающим приборам, необходимо определить примерное количество солей калия и магния растворённых в жидкости. Сделать это на вкус довольно проблематично, ведь изменения могут быть выявлены таким способом только в случае превышения определённого значения.
Чтобы определить в домашних условиях большое содержание солей калия, магния и натрия можно воспользоваться следующими методами:
- Попытаться растворить мыло в воде, если пена не образуется, то вода очень жёсткая и употреблять её не следует.
- Если в чайнике и других приборах образуется большое количество накипи в течение небольшого промежутка времени, то вода, однозначно, превышает безопасные показатели этого значения.
- С помощью индикаторных полосок можно более точно определить количество солей в жидкости, но такой метод потребует небольших финансовых расходов. Для проведения опыта достаточно опустить индикаторную полоску в воду на несколько секунд, а через минуту сравнить её цвет с имеющейся в инструкции таблицей.
Смотреть видео
Заключение
Очень важно знать какой жёсткости вода используется для питья, а так же в котлах отопления и в других водонагревательных приборах. Необходимость применения точных единиц измерения для проведения вычислений в домашних условиях не всегда обязательно.
В химической промышленности и на других высокотехничных производствах, наоборот потребуется знать количество растворённых в воде солей до миллиграмма, поэтому можно использовать любые единицы измерения этого показателя, предложенные в данной статье, чтобы определить и, при необходимости, снизить количество солей в воде.
Смотреть видео
 Загрузка...
Загрузка... trubanet.ru
Способы умягчения жесткой воды
Знать степень жесткости используемой воды обязательно. От показателя жесткости питьевой воды зависит множество аспектов нашей жизни: сколько использовать стирального порошка, нужны ли меры по умягчению жесткой воды, сколько проживут аквариумные рыбки в воде, нужно ли введение полифосфатов в обратном осмосе и т.д.
Существует множество способов определения жесткости:
- по количеству образованной пены моющего средства;
- по району;
- по количеству накипи на нагревательных элементах;
- по вкусовым свойствам воды;
- с помощью реагентов и специальных приборов
Что такое жесткость?
В воде присутствуют основные катионы: кальций, магний, марганец, железо, стронций. Последние три катиона мало влияют на жесткость воды. Существуют еще трехвалентный катион алюминия и железа, которые при определенном рН образуют известняковый налет.
Жесткость может быть разного вида:
- общая жесткость – общее содержание ионов магния и кальция;
- карбонатная жесткость – содержание гидрокарбонатов и карбонатов при рН большем 8,3. Их легко удалить через кипячение: во время нагревания распадаются на угольную кислоту и осадка;
- некарбонатная жесткость – соли кальция и магния сильных кислот; нельзя удалить с помощью кипячения.
Существует несколько единиц жесткости воды: моль/м3, мг-экв/л, dH, d⁰, f⁰, ppm CaCO3.

Жесткая вода
Почему вода имеет жесткость? Ионы щелочноземельных металлов есть во всех минерализованных водах. Они берутся из залежей доломитов, гипса и известняка. Источники воды могут иметь жесткость в различных диапазонах. Существует несколько систем жесткости. За границей к ней подходят более «жестко». К примеру у нас вода считается мягкой при жесткости 0-4 мг-экв/л, а в США – 0-1,5 мг-экв/л; очень жесткая вода в России – свыше 12 мг-эк/л, а в США – свыше 6 мг-экв/л.
Жесткость маломинерализованных вод на 80% обусловлена ионами кальция. С ростом минерализации доля ионов кальция резко снижается, а ионов магния – увеличивается.
Чаще всего поверхностные воды обладают меньшей жесткостью, чем подземные. Так же жесткость зависит от сезона: во время таяния снегов она снижается.
Жесткость питьевой воды изменяет ее вкус. Порог чувствительности для иона кальция – от 2 до 6 мг-экв/л, зависит от анионов. Вода становиться горьковатой и плохо влияет на процесс пищеварения. ВОЗ не дает каких-либо рекомендаций по жесткости воды, так как нет точных доказательств ее влияния на организм человека.
Ограничение жесткости необходимо для нагревательных приборов. Например, в котлах – до 0,1 мг-экв/л. Мягкая вода имеет низкую щелочность и вызывает коррозию водопроводных коммуникаций. Коммунальные службы используют специальную обработку, что бы найти компромисс между налетом и коррозией.
Умягчение жесткой воды

Существует три группы способов умягчения воды:
- физический;
- химический;
- экстрасенсорный.
Реагентные способы умягчения воды
Ионный обмен
Химические способы основаны на ионном обмене. Фильтрующей массой является ионообменная смола. Она представляет собой длинные молекулы, которые собрали в шарики желтого цвета. Из шариков выступают маленькие отростки с ионами натрия.
Во время фильтрации вода пропитывает всю смолу, а ее соли становятся на место натрия. Сам натрий уноситься водой. Из-за разницы зарядов ионов вымывается в 2 раза больше солей, чем оседает. С течением времени соли все заменяются и смола перестает работать. Период работы у каждой смолы свой.
Ионообменная смола может быть в картриджах или насыпаться в длинный болон — колонна. Картриджи имеют небольшой размер и используются только для снижения жесткости питьевой воды. Идеально подходит для умягчения воды в домашних условиях. Ионообменная колонна используется для умягчение воды в квартире или небольшом производстве. Кроме большой стоимости колонна должна периодически загружаться восстановленной фильтрующей массой.
Если в смоле картриджа не осталось ионов натрия, то его просто заменяют на новый, а старый – выбрасывают. При использовании ионообменной колоны смолу восстанавливают в специальном баке с рассолом. Для этого растворяют таблетированию соль. Солевой раствор регенерирует способность смолы к обмену ионами.
Обратной стороной является дополнительная способность воды удалять железо. Оно забивает смолу и приводит ее в полную непригодность. Следует вовремя делать анализ воды!
Использование других химических реагентов
Существует ряд менее популярных, но эффективных способов умягчения воды:
- кальцинированная сода или известь;
- полифосфаты;
- антискаланты – соединения против образования накипи.
Умягчение известью и содой

Умягчение воды содой
Метод умягчения воды с использованием извести называется известкованием. Используют гашенную известь. Содержание карбонатов снижается.
Смесь соды и извести наиболее эффективно. Для наглядности умягчения воды в домашних условиях можно добавить кальцинированную соду в воду для стирки. На ведро берут 1-2 чайные ложки. Хорошо размешивают и ожидают выпадения осадка. Подобным методом пользовались женщины в Древней Греции, используя печную золу.
Вода после извести и соды не пригодна для пищевых целей!
Умягчение полифосфатами
Полифосфаты способны связывать соли жесткости. Они представляют собой крупные белые кристаллы. Вода проходит через фильтр и растворяет полифосфаты, связывая соли.
Недостатком является опасность полифосфатов для живых организмов, в том числе и человека. Они являются удобрением: после попадания в водоем наблюдается активный рост водорослей.
Полифосфаты так же непригодны для умягчения питьевой воды!
Физический метод умягчения воды

Фильтр для умягчение воды
Физические способы борются с последствиями высокой жесткости – накипью. Это безреагентная очистка воды. При ее использовании не происходит снижение концентрации соли, а просто предотвращается вред для труб и нагревательных элементов. Вода становиться мягкой или для большего понимания – умягченной.
Выделяют следующие физические способы:
- использование магнитного поля;
- с помощью электрического поля;
- ультразвуковая обработка;
- термический способ;
- использование малоточечных токовых импульсов.
Магнитное поле
Безреагентное умягчение воды с помощью магнитного поля имеет множество нюансов. Эффективность достигается только при соблюдении определенных правил:
- определенная скорость потока воды;
- подобранная напряженность поля;
- определенный ионный и молекулярный состав воды;
- температура входящей и выходящей воды;
- время обработки;
- атмосферное давление;
- давление воды и т.д.
Изменение какого-либо параметра требует полной перенастройки всей системы. Реакция должна быть незамедлительной. Несмотря на сложность контроля параметров, магнитное умягчение воды используют в котельных.
Но для умягчения воды в домашних условиях с помощью магнитного поля почти невозможно. При появлении желания приобрести магнитик на трубопровод, подумайте, как вы подберете и будите обеспечивать необходимые параметры.
Использование ультразвука
Ультразвук приводит к кавитации – образованию газовых пузырьков. Повышается вероятность встречи ионов магния и кальция. Появляются центры кристаллизации не на поверхности труб, а в толще воды.
При умягчении горячей воды ультразвуком кристаллы не достигают размера, необходимого для осаждения – накипь не образуется на теплообменных поверхностях.
Дополнительно возникают высокочастотные колебания, которые препятствуют образования налета: отталкивают кристаллы от поверхности.
Изгибные колебания пагубны для образованного слоя накипи. Она начинает откалываться кусочками, которые могут засорить каналы. Перед использованием ультразвука необходимо очистить поверхности от накипи.
Электромагнитные импульсы
Безреагентные умягчители воды на основе электромагнитных импульсов меняют способ кристаллизации солей. Создаются динамические электрические импульсы с разными характеристиками. Они идут по проводу-обмотке на трубе. Кристаллы обретают форму длинных полочек, которым трудно закрепиться на поверхности теплообмена.
В процессе обработки выделяется углекислота, которая борется с уже имеющимся известковым налетом и образует защитную пленку на металлических поверхностях.
Термоумягчение
Кто-то слышит про этот метод первый раз. Но на самом деле им пользуется каждый с детства. Это привычное для нас кипячение воды.
Все замечали, что после кипячения воды образуется осадок из солей жесткости. Кофе или чай делают из более мягкой воды, чем водопроводная.
А сколько нужно кипятить? Все просто: с ростом температуры и ее воздействием соли жесткости менее растворимые и больше выпадают в осадок. В процессе нагревания выделяется углекислый газ. Чем быстрее он улетучивается, тем больше образуется известняковый налет. Плотно закрытая крышка препятствует выведению углекислого газа, а в открытой емкости быстро испаряется жидкость.
При использовании термоумягчения следует оставлять крышку в емкости слегка открытой. Так же следует обеспечить максимальную площадь осаждения солей для ускорения умягчения питьевой воды.
При жесткости до 4 мг-экв/л термическое умягчение не нужно: соли будут оседать медленнее, чем испаряется вода. В оставшейся воде будет повышенная концентрация многих примесей.

vse-o-vode.ru
Независимый Испытательный Центр – Анализ воды в Москве и Московской Области Жесткость воды
Жесткость воды является важным показателем качества воды. Vodalab.ru рассказывает о жесткости воды, ее видах и способах умягчения воды.
ЖЕСТКОСТЬ ВОДЫ
Жесткая вода чаще всего ассоциируется с накипью на дне чайника или ощущением мыла на руках после мытья рук, некоторые испытывают ощущение «жестких волос». По этому критерию люди обычно оценивают качество воды. В этой статье мы рассмотрим жесткость со стороны физики и химии, изучим ее свойства, разновидности, влияние на здоровье человека и способы ее устранения жесткости воды.

Вода, содержащая большое количество солей кальция
Эффект жесткой воды
Жесткость воды — это концентрация растворённых в ней солей магния (Mg) и кальция (Ca): гидрокарбонатов, хлоридов и сульфатов. Проще говоря, жесткой называется вода, содержащая в себе большое количество солей. Почему воду назвали «жесткой»? Женщины в старину стирали вещи на берегу рек и озер, в воде которых содержат кальций, отчего ткань становилась жесткой на ощупь.
Жесткость воды делится на 3 вида:
- Карбонатная, т.е. временная. Она ликвидируется с помощью обычного кипячения воды и обусловлена гидрокарбонатами кальция и магния Са(НСО3)2; Mg(НСО3)2.
- Некарбонатная, т.е. постоянная. Возникает из-за присутствия других солей, например CaSO4, Ca(Cl)2, MgSO4, Mg(Cl)2. При кипячении воды не устраняется.
- Общая. Представляет собой суммарную концентрацию ионов кальция и магния. Представляет собой сумму карбонатной и некарбонатной жесткости.
Единицы измерения жесткости:
Не существует единой единицы измерения жесткости. В России, в соответствии с Госстандартом, в качестве единицы жесткости воды установлен моль на кубический метр (моль/м3). В Германии — 2.8DH°; во Франции — 5F°; в Америке — 50.05 ppm CaCO3.
Классификация воды по жесткости:
| Характеристика | Жесткость, мг-экв/л |
| очень мягкая вода | до 1,5 мг-экв/л |
| мягкая вода | от 1,5 до 4 мг-экв/л |
| вода средней жесткости | от 4 до 8 мг-экв/л |
| жесткая вода | от 8 до 12 мг-экв/л |
| очень жесткая вода | более 12 мг-экв/л |
Согласно требованиям СанПиН 2.1.4.1074-01 жесткость питьевой воды должна быть не выше 7 мг-экв/л.
Влияние на здоровье человека:
Как же влияет жесткая вода на наш организм? Медики связывают появление мочекаменной болезни именно с этой особенностью воды. Но на данный момент официального подтверждения этой гипотезе нет. Но мы знаем, что слишком жесткая вода неблагоприятно влияет на органолептические свойства воды, придавая ей горьковатый вкус. Также жесткая вода сушит нашу кожу и волосы. Однако, полностью переходить на мягкую воду не рекомендуется. Наш организм нуждается в солях кальция и магния для укрепления сердечно-сосудистой системы. А вот комнатные растения лучше поливать мягкой или талой водой.
Способы борьбы с жесткой водой:
Для смягчения жесткости воды специалисты рекомендуют приобрести умягчители, которые являются самыми эффективными в борьбе с солями жидкости. Также существует несколько способов смягчения воды в домашних условиях, самым простым и привычным из которых является кипячение воды.
Для борьбы с постоянной жёсткостью воды используют такой метод, как вымораживание льда. Необходимо просто постепенно замораживать воду. Когда примерно 90% жидкости превратится в лед, нужно разморозить его обратно, а соли останутся в оставшейся незамороженной жидкости.
При выборе степени жесткости воды лучше придерживаться середины. Самым оптимальным является использование воды средней жесткости для приготовления пищи и мягкой воды для гигиенических процедур. А чтобы ваша бытовая техника не страдала от повышенной жесткости, лучше приобрести умягчитель.
Заказать анализ воды на жесткость вы можете на нашем сайте vodalab.ru. Каждый из представленных на сайте анализов содержит исследование воды на жесткость.

О других загрязнителях воды, таких как железо, мутность и марганец, вы также можете узнать подробнее в нашем блоге.
vodalab.ru
выбираем фильтр для жесткой воды
Накипь на чайнике, тэне бытового водонагревателя, стиральной и посудомоечной машины – не что иное, как результат использования жесткой воды. Представляете, что происходит в организме человека, который употребляет такую воду! Когда чайник за несколько недель использования покрывается накипью, люди, задумываются о том, как смягчить жесткую воду и отправляются в магазин за фильтром. Какие нюансы нужно учесть?

Жесткая вода имеет целый ряд недостатков, которые исчезают в процессе смягчения
Жесткостью называется сумма ионов кальция и магния, растворенных в воде. Термин «жесткая вода» первоначально применяли к воде, в которой трудно было отстирать вещи. Откуда соли кальция и магния попадают в воду? Основной источник – залежи гипса, известняков и доломитов, которые размываются природными водами. Ионов кальция больше всего в маломинерализированных водах. Чем больше степень минерализации воды, тем меньше в ней содержится ионов кальция. Что касается ионов магния, то в минерализованных водах их количество может достигать нескольких граммов на литр, а в соленых водах – до нескольких десятков г/л.
На первый взгляд кажется, что жесткая вода вред здоровью не несет, а только доставляет массу бытовых неудобств:
- в нагреваемой посуде и на нагревательных элементах бытовой техники со временем появляется толстый слой накипи;
- на стеклянной посуде остаются белые круги;
- эффективность мыла и моющих средств снижается – они недостаточно хорошо пенятся;
- сокращается срок службы одежды, она быстро теряет цвет после стирок в жесткой воде.
Кроме того, что щелочноземельные металлы кальций и магний при нагревании оседают на чайнике или тэнах бытовой техники, остаются на сантехнике и смесителях в виде белого налета, они ещё и стягивают кожу при умывании, а волосы делают жесткими, непослушными, сухими. Попадая внутрь организма, соли оседают в сосудах и почках, образуют камни. Именно поэтому необходима очистка жесткой воды и её умягчение. Проблему можно решить, используя фильтр для жесткой воды.

Аквафор Кристалл Трио для жесткой воды — фильтр, превосходно смягчающий воду
Но интересная ситуация сложилась. С одной стороны, с экранов телевизоров на нас льется поток рекламной информации о вреде, который наносит жесткая вода нашему здоровью и бытовой технике. С другой стороны, медики авторитетно утверждают, что недостаток кальция в организме может стать причиной различных заболеваний опорно-двигательной системы, а недостаток магния может стать причиной инфаркта миокарда. Не значит ли это, что питьевая вода должна содержать эти соли жесткости в достаточном количестве?
Согласно нормам потребления воды, в среднем человек расходует в день от 300 до 400 л воды, при этом основная часть уходит на хозяйственные нужды. Всего 5-10 литров в день необходимо человеку для питья и приготовления пищи, а пьет он примерно два литра в день. Казалось бы, не проще ли смягчать только воду для душа и стиральных и посудомоечных машин, а пить жесткую? Ведь в жесткой воде кальций, а он нужен организму. Восполнять недостаток кальция в организме советуют молочными продуктами (кстати, жесткость молока составляет 60 мг-экв/л, поскольку в 100 г молока содержится 120 мг кальция). Стакан молока заменяет 3-4 литра воды.

Фильтр под мойку «Аквафор-Дуэт» для жесткой воды компактен и удобен в эсплуатации
ВОЗ (Всемирная организация здравоохранения) не дает никаких рекомендаций относительно жесткости питьевой воды. Несмотря на то, что рядом исследований выявлена связь между жесткостью воды и сердечно-сосудистыми заболеваниями, данных не достаточно для того, чтобы делать выводы о причинном характере этой зависимости. Таким образом, вред жесткой воды не доказан, равно как и её польза, но на вкус все же приятнее мягкая вода.
Самый простой способ борьбы с солями магния и кальция – кипячение воды. Но, как известно, во время кипячения из воды уходят и полезные вещества. Есть и ещё один «бабушкин» метод умягчения. Это добавление в воду кальцинированной соды (карбонат натрия). Достаточно двух чайных ложек на ведро воды. Соду следует размешать в воде и дождаться выпадения осадка. В Древней Греции умягчали воду аналогичным образом. В неё добавляли золу из печей. Сегодня разработаны другие технологии очистки воды от магния и кальция. Рассмотрим основные из них.
Как смягчить жесткую воду специальными солями ↑

Самый простой способ смягчения жесткой воды — использование умягчающего фильтра-насадки, который помещается на кран
Существуют специальные смягчающие соли, их использование является обязательным для большинства посудомоечных машин. Именно соль, которая выпускается в виде специальных таблеток, не дает посудомоечной машине быстро выйти из строя. Некоторые даже оснащены специальным индикатором, который подсказывает хозяйке, когда нужно добавить в машину соль.
Магнитный фильтр для смягчения воды ↑
Такие фильтры смягчают воду без использования химии. На жесткую воду воздействуют магнитным полем, которое создает пара магнитов. Так удаляются различные примеси, а вместе с ними и ионы магния и кальция. Магниты располагаются снаружи трубы водопровода. Производители уверяют, что способ эффективный, но утверждение это весьма сомнительно. Но есть место, где магниты точно дают результат. Речь идет о трубах в котельной. Замечено, что воздействие магнитного поля делает отложения на трубах более рыхлыми, они легко удаляются.
В продаже можно встретить и магнитные душевые насадки для смягчения жесткой воды. Они накручиваются непосредственно перед душевой лейкой. Если верить рекламе, они насыщают организм витамином С, удаляют остаточный хлор, смягчают воду и ароматизируют её. При более тщательном изучении упаковки можно обнаружить и такие свойства, как сокращение расхода воды в два раза (за счет меньшего разбрызгивания), увеличение скорости и давления. Цена такого изделия сравнительно невысока. В продаже есть и насадки для душа с турмалином, которые также уменьшают вред жесткой воды для волос и тела.
Кувшин с фильтром для жесткой воды ↑

Кассета для душа сделает принятие ванны более комфортным и полезным
Это емкость, в которой закреплен фильтрующий элемент, который выполнен в виде сменного картриджа. Это один из самых простых и дешевых фильтров с эффектом смягчения, которые используются для питьевой воды. Применяются картриджи, основой которых является активированный уголь.
Очистка воды ионообменными умягчителями ↑
Как известно, жесткая вода зачастую становится причиной выхода из строя дорогой техники – посудомоечных и стиральных машин. Для смягчения воды применяют специальные устройства, которые работают по принципу ионного обмена. Состоит оно из двух резервуаров. В одном находится специальная ионообменная смола, в другом – солевой раствор. Поступая из водопровода, вода сначала проходит через резервуар со смолой, насыщаясь её ионами. Ионы смолы вступают в реакцию с солями магния и кальция и удаляют их. После вода отправляется в следующий резервуар, где вступает в реакцию с солевым раствором. Тут недостающие ионы кальция и магния замещаются ионами натрия. Так жесткая вода смягчается методом ионного обмена.
Как умягчить воду, используя обратный осмос ↑
Система обратного осмоса считается самым надежным фильтром и с эффектом смягчения воды. В основе способа – природное явление осмоса. Суть метода в том, что вода, проходя через полупроницаемую мембрану из более концентрированного раствора в менее концентрированный, очищается от примесей. Их задерживает мембрана, поскольку вода переходит из более концентрированного раствора в менее концентрированный, при этом на неё воздействуют давлением, которое превышает разницу осмотического давления для обоих растворов. Смягчение жесткой воды – это удаление солей магния и кальция, что, собственно, и происходит. Но у системы очистки воды методом обратного осмоса есть существенный недостаток: вода при прохождении через полупроницаемую мембрану теряет как вредные, так и полезные примеси.

Система обратного осмоса эффективно смягчит и очистит воду

Питьевую воду перед употреблением также рекомендуется смягчать
Мягкая вода стоит немалых денег. За границей, например, умягчают далеко не всю воду. Там, кстати, и потребляют её значительно меньше. Для сравнения: в Германии один человек тратит в сутки около 130 л. Воды, в Германии – 190 л, в России – 400. За границей смягчают далеко не всю воду, которая необходима для бытовых нужд. Разводку коммуникаций проектируют так, чтобы минимизировать затраты по фильтрации и умягчению. Так, умягченная вода подается в контур горячего водоснабжения, что увеличивает срок службы котла. А жесткость холодной воды поддерживается на уровне 3-4 мг-экв/л (миллиграмм-эквивалент). Смешивая горячую и холодную воду, потребитель получает воду с жесткостью 1-2 мг-экв/л. Холодную воду, которая поступает в сливные бачки унитазов и воду, идущую на полив газонов, тоже не умягчают.
Согласно ГОСТ 2874-82 «Вода питьевая», показатель жесткости воды не должен превышать 7 мг-экв/л. Но в том же ГОСТе есть примечание о том, что такая жесткость допустима для воды, которая подается по водопроводам без специальной обработки. Ведь при жесткости свыше 7 мг-экв/л, срок службы труб уменьшается, поскольку они быстрее зарастают известковыми отложениями. А если жесткость воды будет слишком низкой, вода приобретет коррозийные свойства: она станет мягкой, но железистой. Но сейчас активно используются пластиковые трубы, не подверженные коррозии, поэтому мы можем использовать мягкую воду.
loading...
loading...
kitchenguide.su









