Способ извлечения из сточных вод фосфатов и органически связанного фосфора. Удаление из питьевой воды фосфатов
Фосфаты удаление из сточных вод
Биологически очищенную воду можно сбрасывать в море или реки, где природные биологические процессы завершают очистку. Вместе с тем эту воду можно подвергнуть третичной обработке, продукт которой может быть использован в системах промышленного и даже питьевого водоснабжения. Третичная обработка сточных вод включает процессы сорбции на активированных углях, селективной коагуляции, аэрации, осаждения фосфатов, удаления соединений азота, бактериальной фильтрации, электрохимической обработки и стерилизации. [c.194] При удалении фосфатов из сточных вод на канализационных сооружениях возникают серьезные трудности. Применение реагентных методов целесообразно лишь при очистке не более чем на 90%, так как более глубокое удаление фосфатов связано с резким [c.64]Ионообменные методы применяют для глубокой очистки сточных вод от ионов тяжелых и цветных металлов, для корректировки минерального состава (умягчения, снижения общего солесодержания. удаления фосфатов) очищенных сточных вод, повторно используемых в замкнутых и обычных системах теплообменного оборотного водоснабжения. Ионообменные смолы могут применяться и в локальных системах очистки сточных вод от ряда органических веществ — ароматических и алифатических аминов, фенолов и органических кислот, в том числе анионных ПАВ. [c.1078]
Приведенный выше обзор лишь частично отражает реальный объем исследований, проводимых за рубежом в этом направлении. Можно констатировать, что использование водопроводного осадка с предварительной его термообработкой для получения высококачественного сорбента — бесспорно перспективный метод удаления не только фосфатов из сточных вод, но и других загрязнений, характеризующихся такими показателями, как БПК, ХПК и др. Применение водопроводного осадка позволит отказаться от сорбентов природного происхождения. В этом направлении ведет исследования отечественная наука и практика. [c.41]
В процессе удаления соединений фосфора концентрация его в сточных водах при сбросе их в водоем устанавливается из условия недопустимости эвтрофикации. При концентрации фосфора в воде водоема менее 0,001 мг/л эвтрофикация не наблюдается. Величина допустимой концентрации фосфора в сточных водах зависит от разбавления сточных вод в водоеме, фоновой концентрации в нем фосфора, наличия прочих источников фосфатов в сточной воде и обычно принимается равной 0,01—0,1 мг/л. [c.214]
Железо —не один элемент, который влияет на содержание фосфора в водной среде такие элементы, как алюминий (А1 +) и кальций (Са2+), оказывают подобное воздействие, однако в меньшей степени. Все три элемента тем не менее успешно используются на очистных сооружениях для удаления фосфатов из сточных и эвтрофных вод [c.150]
Химическое осветление сточных вод. Как указывалось ранее, метод химического осветления сточных вод основан на том, что нри добавлении к ним неорганических и(или) органических коагулянтов (флоккулянтов) при соответствующем pH среды происходит интенсивное хлопьеобразование, сопровождаемое удалением из сточных вод фосфора в виде нерастворимых солей — фосфатов и тяжелых металлов — в виде нерастворимых гидроокисей. Присутствующие во взвешенном и коллоидном состояниях загрязнения адсорбируются на образующихся хлопьях и также удаляются-. Эффективность химического осветления зависит от многих факторов, в частности от соотношения концентраций коагулянта, флоккулянта и загрязнений, от интенсивности и времени перемешивания обрабатываемых сточных вод при контакте их с химикалиями, от pH среды и температуры, от содержания солей, величины и знака заряда частиц и др. Обычно химическую обработку сточных вод проводят в реакторах-смесителях, в которых (в условиях интенсивного перемешивания) химикалии контактируют со сточными водами при оптимальной величине pH, которую устанавливают в ходе предварительных лабораторных и (или) пилотных испытаний. [c.136]
Один из методов удаления фосфат-иона PO4 при третичной обработке сточных вод заключается в их обработке СаО. Составьте соответствующие химические уравнения и, пользуясь нужным значением ПР, объясните, каким [c.169]
Процессы, протекающие в сооружениях, не ограничиваются вышеописанными. В камерах установок также происходят нитрификация, денитрификация, в некоторых установках предусматривается удаление фосфатов, лимитируемых к сбросу в водоем, возможность обеззараживания сточных вод. [c.181]
При доочистке сточных вод наряду с удалением механических примесей и снижением химической потребности в кислороде (ХПК) уменьшаются концентрации фосфатов, азота, синтетических детергентов и многих других примесей. Оптимальные значения [c.330]
Анионные флокулянты, включая полиакриламид, были эффективны только с минеральными коагулянтами. Минеральные коагулянты с ПАА оказались наиболее эффективными при очистке сточных вод от органических загрязнений, характеризуемых ХПК и ВПК, а также фосфатов ПЭИ—при удалении ПАВ, нефтепродуктов, солей тяжелых металлов и красителей. Действие ПЭИ объясняется взаимодействием аминогрупп, флокулянта с кислотными группами ПАВ и нефтепродуктов и способностью ПЭИ к образованию комплексных. соединений с солями тяжелых металлов. [c.191]
ОЧИСТКИ, однако большую часть воды, забираемой из различных источников, необходимо обрабатывать для улучшения ее качества до требуемого уровня. Основная функция очистки воды для городского водоснабжения заключается в удалении нежелательных примесей, содержащихся в стоках бытового и промышленного происхождения. Загрязнениями являются человеческие испражнения, отходы обработки пищи и всевозможные разновидности органических и неорганических веществ, находящихся в производственных стоках. Сточные воды очищают для улучшения их качества перед сбросом в поверхностные водные источники. Традиционная технология обработки, включающая биологическую очистку, соответствует самой низкой допустимой степени очистки сточных вод. Для обеспечения возможности непрямого повторного использования этой воды необходимо существенное разбавление стоков в естественных водоемах. В некоторых случаях, когда невозможно обеспечить достаточное разбавление, могут быть применены усовершенствованные способы очистки сточных вод (доочистка) для удаления остаточных органических примесей, фосфатов, азотных соединений и других загрязнений. Регенерация воды представляет собой комбинацию обычных и усовершенствованных способов очистки, применяемых для восстановления качества сточной воды до первоначального состояния, когда становится возможным ее повторное использование. Применение такой воды для общественного водоснабжения не допускается, однако она может использоваться для сельскохозяйственных и промышленных нужд. [c.114]
Там, где отвод сточных вод невозможен, например, на Великих озерах, для удаления питательных веществ из сточных вод могут быть применены более совершенные способы очистки. Обычная технология, включающая биологическую очистку бытовых сточных вод, обеспечивает удаление примерно 30% фосфора и 40—50% азота. Степень очистки может быть и меньшей в зависимости от концентрации питательных веществ в неочищенной сточной воде и от способов обработки осадков сточных вод. В настоящее время особое внимание уделяется удалению фосфора, так как он считается лимитирующим питательным веществом, и уже разработаны методы химического осаждения фосфатов [c.131]
При добавлении достаточного количества извести осаждающее умягчение продолжается с образованием гидроокиси магния. Для удаления основной фосфорной фракции требуется pH в диапазоне 9,5—11,5. При дозах извести в форме СаО, равных 150—300 мг/л, выводится 80—90°/о фосфатов из обычных бытовых сточных вод. Требуемое количество извести зависит главным образом от щелочности, концентрации фосфора и требуемой степени удаления последнего. [c.370]
Коагуляция исходной сточной воды приводит к осаждению фосфатов вместе с органическими веществами, которые осаждаются в процессе первичного отстаивания. Если используются отработанный травильный раствор и известь, то оба коагулянта обычно добавляют именно на этой стадии очистки, и степень удаления фосфора составляет 70—80°/о- Для удаления 80% фосфора в процессе первичного отстаивания вводят избыточное количество извести, что не оказывает отрицательного влияния на процесс вторичной биологической очистки, если pH жидкости не превышает 9,5. Выделяемый микроорганизмами углекислый газ прн биоло- [c.370]
На традиционных сооружениях для биологической очистки сточных вод удаляется большая часть органических веществ и в значительной степени тяжелые металлы, хотя от последних проще всего освобождаться иа промышленных предприятиях. В настоящее время разработаны усовершенствованные способы химической обработки сточных вод, предназначенные для удаления фосфатов, а та>кже ряд способов химической и биологической обработки для удаления азота однако эти процессы лишь в очень незначительной степени снижают концентрацию растворенных примесей. В связи с тем, что в бытовых сточных водах содержится при- [c.389]
Некоторые обсуждаемые вопросы рассмотрены на примере удаления фосфатов при дополнительной очистке биологически или химически очищенных сточных вод. [c.8]
УДАЛЕНИЕ ФОСФАТОВ НРИ ОЧИСТКЕ БЫТОВЫХ СТОЧНЫХ ВОД [c.15]
Соли алюминия широко применяются как при очистке питьевой воды, так и при физико-химической очистке сточных вод для удаления суспендированных твердых примесей и осаждения фосфата. Разработка рациональной модели процесса осаждения фосфата с использованием солей алюминия затруднена, так как химическое взаимодействие между алюминием и фосфатом изучено недостаточно, особенно процесс растворения конденсированной фазы в метастабильных растворах. Кроме того, для достижения большой эффективности процессов обработки сточной воды необходимо тш,ательно изучить систему фосфата алюминия, в частности способность алюминия коагулировать суспендированные твердые примеси и осаждать фосфат. [c.48]
При использовании А12(804)з оптимальные значения pH для удаления фосфатов из сточных вод лежат в интервале 6,0—7,1 при использовании Ре2(304)з —в интервале 4,7—7,4. Помимо корректировки значений pH среды и добавления ВМФ, для новыше- [c.225]
В практике очистки сточных вод от поверхностно-активных веществ экстракционные процессы пока еще не получили широкого распространения. Однако в последние годы в этом направленпн уже выполнено несколько исследований, публикации о которых носят, в основном, патентный характер. Описан экстракционный метод удаления из сточных вод анионоактивных моющих средств и фосфатов. В сточные воды дозируется серная кислота для снижения pH до 4,0—5,0. Затем в воду добавляется какой-либо алифатический амин, нерастворимый в воде, в виде раствора в органической жидкости, не смешивающейся с водой. В качестве амина можно применять, например, триоктиламин или диолеиламин в качестве органического растворителя — керосин, растительные масла и т. д. Смесь воды и раствора амина в органической жидкости подается в верхнюю часть цилиндрического бака, разделенного двумя перегородками, не доходящими либо до дна, либо до верха, на три секции. Сточная вода, проходя через бак, обтекает [c.133]
Удаление отработанного катализатора. Использованный катализатор выводят из системы в виде водного раствора. Обычно отработанный катализатор лучше всего применять для обработки сточной воды. Часто его продают или используют как заменитель квасцов или купороса при осветлении воды. Можно его использовать, как это делается в городском хозяйстве США, для обработки полей орошения с целью извлечения фосфатов. В Японии отработанный хлористый алюминий пр ращают в полиалюминий-хлорид и используют для обработки воды. Существуют и другие пути его использования. [c.276]
Эта технологическая схема (рис. 1Х-5) включает следующие этапы обработки воды адсорбционную доочистку биологически очищенных сточных вод в аппаратах с псевдоожиженным слоем активного угля, обеспечивающую уменьшение ХПК воды дО 8—Ш г/м удаление из очищенной воды пыли активного угля и других взвешенных веществ отстаиванием и фильтрованием Н+-катиопирование адсорбционно очищенной воды для удаления из нее катионов жесткости, уменьшения содержания ионов щелочных металлов и аммония отдувку диоксида углерода из Н+-катионированной воды в дегазационных колоннах 0Н -анионирование воды для извлечения анионов сульфатов, фосфатов, уменьшения содержания хлоридов и нейтрализации кислотности Н+-катионированной воды. [c.248]
Практически на всех заводах удаление вредных примесей из стоков производится биологической очисткой. Перед биологической очисткой стоки отстаиваются, нейтрализуются, смешиваются с фекальными стоками, при необходимости в них добавляются фосфаты, калийные и азотные удобрения для обеспечения жизнедеятельности необходимых бактерий. На биологической очистке сточных вод происходит аэробна минерализация органических и части неорганических соединений в присутствии кислорода с помощью аэробных микроорганизмов (бактерий). В результате жизнедеятельносги бактерий органические вещества распадаются на СО2 и Н2О, нитраты и нитриты. В результате поглощения органики происходит рост количества бактерий, образуется биомасса. [c.165]
Долгое время бытовало такое мнение, что биологическое удаление фосфора осуществляется только бактериями A inetoba ter. Однако в настоящее время уже хорошо известно, что способностью аккумулировать фосфор обладают очень многие гетеротрофные микроорганизмы, содержащиеся в сточной воде и в иле очистных сооружений. Все эти микроорганизмы называют био-Р-бактериями или фосфат-аккумулирующими организмами (ФАО) [41]. Механизм аккумуляции фосфора не всегда активирован в бактериях, поэтому определение концентраций, например, био-Р-бактерий в сточной воде может быть затруднено. В очистных сооружениях с биологическим удалением фосфора активны несколько групп гетеротрофных микроорганизмов, конкурирующих за субстрат, особенно за низкомолекулярные жирные кислоты, которые и необходимы для реализации фосфор-аккумулирующего механизма. Многие из конкурирующих бактерий не являются ФАО. Именно результат этой конкуренции и определяет успех био-Р-процесса. [c.137]
Усиление контроля над загрязнением окружающей среды повышает требования не только к снижению БПК, но предусматривает также более полное, чем в настоящее время, удаление иа сточных од красящих веществ, вызывающих рефракцию света органических ешеств, таких, как лигнин, а также фосфатов, нитратов и других олей. Удаление этих компонентов биоокислением очень трудно, а шогда и невозможно. Поэтому необходима дополнительная обработка стоков. С помощью метода обратного осмоса можно в одной сту-аени выделить и сконцентрировать все эти различные компоненты, и поэтому его можно считать перспективным новым методом обработки сточных вод. [c.248]
С помощью мембранных систем можно выделять фосфор — вещество, необходимое для. развития водорослей. В работе /6/ сообщается об использовании биомембранной системы, в которой при pH = 7-8 задерживалось 22% фосфатов, содержащихся в поступак>-щей на обработку сточной Ьоде, Когда значение pH полностью смешанного материала в реакторе было повышено до 8,5-9,0, удаление фосфата из воды, т.е. удерживание его мембранами, достигло 90%. По-видимому, в этом случае мембрана способна удерживать в некоторой форме фосфат кальция, который обычно невозможно удалить из воды при ее нормальных значениях pH (7,0-8,0). Этот результат может внести сомнения относительно обычных данных по растворимости. Эта соль или комплексная форма фосфата кальция удерживалась очень пористой мембраной, в то время как все одновалентные вещества и некоторые небольшие органические молекулы через нее проходили. [c.292]
Более полное удаление из сточной жидкости трудноокисля-ющихся примесей (фосфатов, синтетических ПАВ и др.) и микроэлементов. [c.329]
В соответствии с программой перспективного внедрения новых технологических решений в области очистки сточных вод Унрав-лежие по охране окружающей среды США предполагает широкое внедрение коагуляции для удаления фосфатов [61]. Уже теперь коагуляция как способ очистки воды от фосфатов используется примерно на 300 пунктах обработки сточных вод [62]. В перспективном плане развития канализации реагентным методам очистки отведена доминирующая роль [63. [c.330]
На схеме функционирования типового очистного сооружения (рис. 12.3) показаны испытания, необходимые для оценки эксплуатационных свойств сооружения. Для соблюдения стандартов на качество очищенных сточных вод нужен ежедневный контроль средних концентраций по БПК и взвешенным веществам, значения pH и количества фекальных колиформ. В некоторых случаях правилами предусмотрено проведение анализов на остаточный хлор, присутствие тяжелых металлов, фосфатов и содержание аммонийного азота. Степень удаления органических ве- [c.363]
Практика сброса сточных вод в реки основывалась на предположении, что разбавление и самоочищение движущейся воды достаточно эффективны для обеспечения безопасности здоровья людей и сохранения удовлетворительных условий для размножения рыб. Очистные сооружения возводили с целью удаления подверженных биораспаду органических веществ для поддержания определенного минимального уровня растворенного кислорода в природных водоемах. Позднее было введено хлорирование очищенных сточных вод во избежание заражения природных водных источников патогенными микроорганизмами. По мере того как возможность использования самоочищающих свойств водных источников постепенно исчерпывалась, а потребление воды увеличивалось, возникла необходимость в расширении косвенного повторного использования воды, а это потребовало повышения качества с истки сточных вод. В некоторых случаях оказалось необходимым в дополнение к традиционной биологической очистке ввести доочистку сточных вод, например, с целью удаления фосфатов, стимулирующих рост водорослей. Питательные соли, пена, окрашенные вещества и другие устойчивые загрязнения могут быть удалены только специальными методами очистки. [c.366]
Фосфаты и неорганический азот выводятся из раствора при фотосинтезе водорослей. Однако доказано, что выращивание и сбор водорослей для удаления из сточных вод питательных веществ представляют собой сложную в экономическом отношении задачу. Трудности, возникающие в связи с поддержанием требуемых отношения углерода к азоту и фосфору, значения pH и темперятуры, интенсивность солнечного освещения, невозможность отвода больших земельных участков для обеспечения требуемой длительности пребывания и высокая стоимость механизмов для сбора водорослей — все это служит препятствием к практическому использованию фотосинтеза для удаления питательных веществ. [c.368]
Первая стадия намеченной программы была осуществлена в 1965 г. Она заключалась в хранении избыточного количества очищенных сточных вод в гравийном карьере, откуда вода подавалась для поливки площадок для игры в гольф. Это было сделано вместо перекачки избыточного количества сточных вод для сброса их в океан на расстояние около 32 км. В 1967—1970 гг. распределительная система была расширена, что позволило использовать регенерированную воду для поливки парков и зеленых насаждений. Были возведены сооружения для третичной очистки с целью повышения эффективности функционирования системы грунтовой фильтрации. Третичная очистка включает в себя удаление нитратов с помощью биологической нитрнфикации-денитрифика-ции, уменьшение содержания фосфатов посредством химической флокуляции и отстаивания с использованием сульфата алюминия и извести и окончательное фильтрование через фильтры с двухслойной загрузкой. Прошедшая все стадии очистки вода хлорируется и отводится в пруды, предназначенные для купания и отдыха. Созданы и проходят испытания опытные установки, состоящие из угольных фильтров, ионообменников и блоков электродиализа. Они предназначены для удаления устойчивых органических соединений и снижения общего содержания растворенных прпмесей до уровня, более низкого, чем предусмотренный стандартами [c.380]
Схема восстановления сточной воды (рис. 14.3) включает процессы традиционной обработки и доочистки. После первичного отстаивания и вторичной очистки с использованием биофильтров сточная вода поступает в расположенные последовательно три стабилизационных пруда с общим временем пребывания около 18 сут. Рост водорослей в этих прудах снижает концентрации неорганического азота и фосфатов. В стабилизационных прудах уменьшается также содержание других загрязнений. Вода, выходящая из стабилизационных прудов, подвергается рекарбонизации, в результате чего pH снижается с 9,0 до 7,5, и в нее вводится сульфат алюминия в концентрации 150 мг/л для флотационного отделения водорослей. Плавающие на новерхности водоросли собираются скребками, а затем вода подвергается фракционированию путем нено-образования. Сжатый воздух, вводимый в нижнюю часть резервуара, перемешивает воду и приводит к образованию пены. Последняя собирается с поверхности и разбивается струями воды для облегчения ее удаления. Затем вода подвергается хлорированию до точки перегиба с целью окисления и выведения большой части оставшегося неорганического азота и получения необходимой концентрации свободного остаточного хлора. Небольшая доза извести (около 30 мг/л) добавляется вместе с хлором для улучшения осаждаемости взвешенных частиц. Осветленная вода фильтруется через скорые песчаные фильтры, а затем обрабатывается в колоннах с загрузкой из гранулированного активного угля. у дсорбция с помощью активного угля способствует извлечению остаточных растворенных веществ, что приводит к улучшению органолептических характеристик воды, таких, как вкус, цветность и запах. Периодически проводится обратная промывка колонн, а уголь по мере необходимости заменяется. Отработанный уголь складируется и хранится для последующей регенерации. [c.381]
Существующая в настоящее время станция восстановления воды (рис, 14.4) с расчетной производительностью 28 ООО м /сут состоит из сооружений традиционной биологической очистки и оборудования для третичной физико-химической очистки. Первичная и вторичная очистка проводится с использованием активного ила, причем избыточный активный ил обезвоживается и сжигается. Стоки освобождаются от фосфора и азота посредством обработки известью и воздушной отдувки аммиака. Для максимального осаждения фосфатов необходима дозировка извести 400 мг/л (в пересчете на СаО), Сточная вода с получаемым высоким значением pH перекачивается через противоточные градирни для удаления азота. Затем перед фильтрованием через напорные фильтры со смешанной загрузкой проводится рекарбонизация воды для снижения pH до 7,5. Адсорберы из активного угля поглощают устойчивые растворимые органические вещества, не удаленные при коагуляции известью, а на последней стадии очистки производится окончательное хлорирование. Известковый осадок рекальцинируется для повторного использования в технологическом процессе. [c.384]
Для коагуляции примесей в сточной воде и удаления фосфатов в ряде городов широко применяется известь для образования карбоната и фосфата кальция. Целесообразность обработки сточной воды известью может определиться степенью кинетического ингибирования процесса образования карбоната кальция примесями сточной воды. Успешное использование такой обработки сточной воды в реальных условиях требует детального знания химических принципов, лежаших в основе процессов образования и взаимодействия карбоната кальция в системах очистки сточных вод [12—19]. Обработка сточных вод известью часто усложняется из-за неполного осаждения фосфата и плохого отстаивания воды. На практике для удовлетворительного удаления фосфата и хорошего отстаивания обработку воды проводят при высоких значениях pH (10—11) и при боль-Ш.ИХ дозировках извести. [c.27]
При обсуждении метода удаления фосфата обработкой известью Меррим и Джорден отмечают, что фосфат удаляется лучше, если процесс образования карбоната кальция ингибирован. К сожалению, эти авторы использовали неточные значения растворимости карбоната кальция, который образуется в результате добавления извести к сточным водам. Тем не менее они сделали вывод, что для характеристики реакций осаждения, вызванных добавками извести, могут быть использованы равновесные модели или модели неизменного состояния. Как будет показано ниже, использование таких моделей для расчета процесса образования карбоната кальция в сточных водах может привести к большим ошибкам. Так, обычные концентрации определенных примесей, например фосфата, могут снизить константу скорости образования карбоната кальция па несколько порядков и быть причиной успешной или неудачной обработки сточной воды известью. [c.28]
chem21.info
Способ очистки сточных вод от фосфатов
Изобретение относится к реагентным способам обработки бытовых и промышленных сточных вод, а именно к очистке стоков от фосфатов, и может быть использовано на станциях очистки и водоподготовки, в частности на биологических очистных сооружениях. Обработку фосфорсодержащих сточных вод ведут полученным в промышленных условиях алюмохлоридным раствором - отходом (сточными водами) производства этилбензола, который характеризуется следующими показателями, г/дм3: хлорид алюминия 1,5-8,2; свободная соляная кислота 1,1-48,0; рН 0,9-2,9. Алюмохлоридный раствор перед употреблением обрабатывают раствором щелочи, доводя величину рН до 3,8-4,3, а затем его добавляют в воду в количестве 1,0-3,2 дм3/м3 ( в пересчете на А1+3 - 1,6-5,0 мг/дм3 ). Обработку стоков и осаждение ведут при рН 6,5-7,4. Использование такого алюмохлоридного раствора для осаждения фосфатов позволяет получить осветленную воду хорошего качества, утилизировать отход производства, а также упростить и повысить стабильность процесса осаждения и последующего процесса биологической очистки.
Изобретение относится к реагентной обработке бытовых и промышленных сточных вод, а именно к очистке стоков от фосфатов, и может быть использовано на станциях очистки и водоподготовки, в частности на биологических очистных сооружениях (БОС).
Фосфор относится к числу биогенных элементов, имеющих особое значение в биологическом цикле как в водных объектах, так и в активном иле станций биологической очистки. При недостатке соединений фосфора в воде тормозится рост и развитие водной флоры и фауны, однако их избыток также приводит к негативным последствиям, вызывая развитие процессов эфтрофикации и ухудшение качества воды. Поэтому в технологии биологической очистки бытовых и производственных сточных вод на БОС существует настоятельная потребность снижения концентрации фосфатов в очищенных стоках до нормативов, предусмотренных санитарными нормами.
Соединения фосфора в природных и сточных водах представлены в виде ортофосфатов, полифосфатов и органических фосфорсодержащих соединений, причем преобладающей формой являются ортофосфаты.
Ортофосфорная кислота (средней силы), будучи трехосновной, способна образовывать три вида солей, например:
Кислые соли:
- NaН2РO4 первичный фосфорнокислый натрий;
- Na2HPO4 вторичный фосфорнокислый натрий;
Средняя соль:
- Nа3РO4 третичный фосфорнокислый натрий.
Все первичные фосфаты хорошо растворимы в воде, из вторичных и третичных растворимы лишь очень немногие, в частности соли натрия (Б.Н.Некрасов. Основы общей химии,. Т.1, изд. 3-е испр. и доп., М.: Химия, 1973, с.440).
В водах соединения фосфора как минеральные, так и органические могут присутствовать в растворенном, коллоидном и взвешенном состоянии. Переход из одной формы в другую осуществляется сравнительно легко.
Обработку сточных вод осуществляют на очистных сооружениях как с использованием, так и без применения химических реагентов. Обработка воды коагулянтами позволяет перевести минеральные примеси в нерастворимую форму. К таким реагентам относятся соли кальция, железа и алюминия.
Способ очистки сточных вод, характеризующийся улучшенными характеристиками отделения твердых частиц, сниженной биологической потребностью в кислороде (БХПК) в очищенных сточных водах и повышенным удалением азота и фосфата, описан в пат. RU 2148033, 7 С 02 F 3/30. Из пат. RU 2145942, 7 С 02 F 1/52, 1/54, опубл. 27.02.2000, №6, известно, что очистку сточных вод ведут с использованием извести и гидролизующейся соли железа или алюминия при оптимальных значениях рН. Способ очистки сточных вод, включающий смешивание стоков с сернокислым алюминием (12-20 мг/л) при заданной величине рН (6,5-7,6), изложен в пат. RU 2145575, 7 С 02 F 1/52, опубл. 20.02.2000, №5.
Для очистки многотоннажных промышленных стоков с использованием химических реагентов является характерным большой расход дефицитных и дорогостоящих коагулянтов, производство которых сопряжено не только со значительными материальными затратами, но и с экологическими проблемами. На станциях очистки при этом возникает настоятельная потребность в сооружении реагентных хозяйств и их оснащении специальным технологическим оборудованием, что обуславливает высокую себестоимость очистки за счет больших материальных и энергетических затрат.
Наиболее близок по техническому решению к предлагаемому изобретению способ, изложенный в пат. RU 2151172, 7 С 12 F 3/10, опубл. 20.06.2000. №17. Сущность данного технического решения заключается в удалении взвешенных, коллоидных и растворенных органических и минеральных примесей методом коагуляции на стадии осаждения гидроксидом алюминия.
Общим признаком с предлагаемым изобретением является использование для агломерации частиц на стадии осаждения гидролизующейся соли алюминия. Данному способу присущи вышеперечисленные недостатки.
Наиболее близким к заявляемому способу очистки воды от фосфатов (прототипом) является способ извлечения из сточных вод (СВ) фосфатов, описанный в (В.А.Проскуряков, Л.И.Шмидт. Очистка сточных вод в химической промышленности. Изд. Химия, Ленинградское отделение, 1977, с.138). Сущность данного технического решения заключается в осаждении фосфатов сульфатом алюминия в щелочной среде. Эффективность очистки составляет 90-95%.
Кроме перечисленных выше недостатков, в данном случае имеет место вторичное загрязнение осветленной воды солями и ионами, т.к. характерной особенностью технических реагентов являются высокое содержание в них балласта и небольшое количество основного вещества (активное начало).
Задачей предлагаемого изобретения является:
- расширение ассортимента высокоэффективных, доступных и недорогих реагентов для извлечения фосфатов из сточных вод с сохранением высокой степени очистки воды;
- предотвращение вторичного загрязнения очищаемых стоков солями и ионами, содержащимися в используемых растворах реагентов;
- уменьшение себестоимости очистки за счет сокращения материальных и энергетических затрат;
- упрощение и повышение стабильности проведения технологического процесса;
- квалифицированное использование отхода производства.
Исключение указанных недостатков в способе очистки сточных вод от фосфатов, включающем обработку воды гидролизующейся солью алюминия, и достижение технического результата возможно за счет того, что в качестве гидролизующейся соли алюминия используют алюмохлоридный раствор - отход производства этилбензола, который характеризуется следующими показателями, г/дм3: хлорид алюминия 1,5-8,2, свободная соляная кислота 1,1-48,0, величина рН 0,9-2,9, причем перед употреблением его обрабатывают раствором щелочи, доводя величину рН до 3,8-4,3, реагент вводят в воду в количестве 1,0-3,2 дм3/м3 (в пересчете на А1+3 1,6-5,0 мг/дм3), а величина рН очищаемой воды изменяется в пределах 6,5-7,4.
Сопоставительный анализ прототипа и предлагаемого изобретения показывает, что общим признаком является использование в качестве осадителя фосфатов гидролизующейся соли алюминия.
Отличие заявляемого способа от прототипа заключается в том, что в качестве алюминийсодержащего реагента для осаждения фосфатов используют отход производства этилбензола - алюмохлоридный раствор, который перед добавлением в очищаемую воду обрабатывают щелочью до рН 3,8-4,3, доза реагента составляет 1,0-3,2 дм3/м3 (в пересчете на Аl+3 1,6-5,0 мг/дм3), а величина рН очищаемой воды изменяется в пределах 6,5-7,4.
Отличительной особенностью данного реагента является то, что он получен в промышленных условиях в результате производства этилбензола с использованием в качестве катализатора безводного хлорида алюминия и представляет собой сточные воды. Перед сбросом в общезаводские канализационные сооружения эти стоки обрабатывают щелочью для соблюдения санитарных норм по величине рН. Практика показала, что имеют место большие затраты материальных средств на защелачивание отхода и его дальнейшее обезвреживание.
Предложено подщелачивать алюмохлоридный раствор до рН 3,8-4,3, что позволяет получать раствор гидроксохлоридов алюминия общей формулы Al(OH)nClm, где n=1-5, m=6-n. Расход щелочи при этом значительно сокращается.
Предлагаемый способ испытан в лабораторных условиях. Обработанный щелочью раствор алюмохлорида добавляют в смесь хозбытовых и химзагрязненных фосфорсодержащих стоков, поступающих на первичные отстойники биологических очистных сооружений (БОС) в количестве 1,0-3,2 дм3/м3 (в пересчете на Аl+3 1,6-5,0 мг/дм3).
Для сравнения фосфорсодержащую воду обрабатывают раствором сульфата алюминия, количество добавленного реагента в пересчете на А1+3 составляет 2,0 мг/дм3 (24,7 мг/дм3 по Al2(SO4)3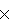 18 Н2О).
18 Н2О).
Опыты моделируют процесс отстаивания сточных вод в отстойниках БОС и их проводят следующим образом. Сточную воду перемешивают и разливают в мерные цилиндры, затем добавляют расчетную аликвоту того или иного реагента. Все пробы тщательно и однообразно перемешивают в течение 1-3 мин и отстаивают в течение 2-х часов при 18-22 С. В процессе отстаивания контролируют кинетику осаждения образующегося осадка, а по истечении 2-х часов осветленную воду декантируют от последнего и анализируют.
С. В процессе отстаивания контролируют кинетику осаждения образующегося осадка, а по истечении 2-х часов осветленную воду декантируют от последнего и анализируют.
Экспериментальные данные показывают, что при добавлении в очищаемую воду названных выше реагентов наблюдается интенсивное хлопьеобразование, агломерация мелких частиц и осаждение образующихся продуктов гидролиза с адсорбированными на их поверхности загрязняющими веществами (фосфаты в т.ч.).
Эффективность выделения фосфатов из обработанной алюмохлоридом (2,0 мг/дм3 по Аl+3) воды составляет не менее 90 мас.%. При использовании алюмохлорида в количестве 2,0 мг/дм3 (по А1+3) величина рН изменяется в пределах санитарных норм и составляет 6,9-7,4. Увеличение в сточных водах концентрации этого реагента до 5 мг/дм3 (по Аl+3) не требует корректировки их величины рН, которая колеблется в пределах 6,5-7,2. Положительным моментом при использовании в качестве реагента алюмохлоридного раствора является более стабильное проведение процесса очистки воды. Достигнутая степень очистки стоков от фосфатов при использовании отхода производства представляется вполне допустимой, т.к. их остаточная концентрация в осветленной воде является необходимой и достаточной для нормального проведения в дальнейшем процесса биологической очистки названных выше стоков. Успешное проведение биохимической очистки сточных вод, а также эффективная денитрификация и дефосфатизация обусловлены тем, что в обработанной предложенным реагентом воде отношение концентрации БПК к концентрации соединений азота и фосфора соответствует требованиям санитарных норм.
Глубина очистки воды от фосфатов сульфатом алюминия (2,0 мг/дм3 по Аl+3) составляет не менее 97 мас.%. Однако при использовании сульфата алюминия существенным недостатком является двухкратное увеличение в осветленной воде концентрации сульфат-ионов и общего солесодержания, снижение величины рН осветленной воды до 4,4-6,4, возможность передозировки названного реагента и дестабилизации процесса очистки воды. Добавление сульфата алюминия в осветляемую воду в количестве более 2,0 мг/дм3 (по Аl+3) без корректировки величины рН также не представляется возможным, т.к. рН воды снижается до 4,3-5,7. Последнее, кроме того, не является оптимальным для осаждения фосфатов.
Предлагаемый способ очистки сточных вод от фосфатов позволяет:
- расширить ассортимент реагентов для извлечения фосфатов и получить при этом высокий эффект очистки;
- исключить необходимость проведения сложной, трудоемкой и дорогостоящей обработки (например, центрифугирования и нагревания) отхода производства перед его использованием;
- сократить материальные затраты на обработку отхода производства и очищаемой воды;
- исключить недостатки, характерные для традиционно используемых в процессах обработки воды реагентов, а именно: уменьшить влияние используемых реагентов на параметры санитарных норм очищаемой воды; исключить необходимость дополнительной обработки (корректировки величины рН) очищаемой воды как на стадии осаждения фосфатов, так и на стадии биологической очистки; уменьшить вторичное загрязнение очищаемой воды ингредиентами, содержащимися в используемых реагентах;
- упростить и повысить стабильность процесса осаждения фосфатов и проводимого затем процесса биологической очистки этой воды;
- Утилизировать отход производства, ценный компонент которого находит применение на том же предприятии.
Формула изобретения
Способ очистки сточных вод от фосфатов, включающий обработку воды гидролизующейся солью алюминия, отличающийся тем, что в качестве алюминийсодержащего реагента используют алюмохлоридный раствор - отход производства этилбензола, который характеризуется следующими показателями, г/дм3: хлорид алюминия 1,5-8,2; свободная соляная кислота 1,1-48,0; величина рН 0,9-2,9, причем перед употреблением его обрабатывают раствором щелочи, доводя величину рН до 3,8-4,3, а затем добавляют в воду в количестве 1,0-3,2 дм3/м3 (в пересчете на А1+3 - 1,6-5,0 мг/дм3), величина рН очищаемой воды при этом изменяется в пределах 6,5-7,4.
www.findpatent.ru
Фосфаты в рифовом аквариуме
Автор: Ренди Холмс-Фарли.
Атом фосфора – один из основных компонентов любой живой материи. Фосфор присутствует в любом живом существе и в воде любого рифового аквариума. К сожалению, зачастую он присутствует в рифовом аквариуме в избытке, и этот избыток фосфора создает как минимум две проблемы для рифоводов. Во-первых, фосфат зачастую ключевой фактор для роста водорослей, т.е. повышенное содержание фосфата способствует избыточному росту нежелательных водорослей. Во-вторых, фосфат может напрямую ингибировать кальцификацию у кораллов и коралины. Поскольку для большинства рифоводов оба процесса не являются желательными, контроль количества фосфатов в аквариуме является очень актуальным вопросом. К счастью, есть несколько эффективных мер удержания концентрации фосфата в допустимых пределах. В данной статье мы рассмотрим методы контроля концентрации фосфатов, а также допустимые для аквариума значения концентрации фосфата.
Фосфор в морской воде представлен двумя основными формами: неорганический фосфат (особенно ортофосфат) и органические фосфат-соединения. Ортофосфат легко усваивается водорослями и активно ингибирует кальцификацию. Органические соединения фосфора могут быть доступны или недоступны таким организмам как водоросли. Аквариумисты могут определить концентрации неорганических ортофосфорных соединений с помощью стандартных тестовых наборов, а вот определить органический фосфор в воде – задача более трудоемкая. Более того, если в аквариуме есть проблемы с ростом низших водорослей, это указывает, что вероятно водоросли потребляют ортофосфат, как только тот поступает в воду и тем самым маскируют проблему. Соответственно, многие аквариумисты могут не выявить фосфат и при этом иметь проблемы с низшими водорослями.
В настоящей статье мы рассмотрим некоторые аспекты присутствия фосфора в рифовых аквариумах, в том числе те формы, в которых фосфор присутствует в воде, источники их происхождения, способы выявления и, что особенно важно, способы удаления их из воды.
Самая простая форма фосфора в морской воде – неорганический ортофосфат. Он состоит из центрального атома фосфора, окруженного четырьмя атома кислорода в форме четырехгранника (Рисунок 1 и 2). Три атома кислорода могут либо присоединять атом водорода, либо нести отрицательный заряд (Рисунок 2). Тот или иной вариант зависит от величины рН морской воды. При показателе рН 8.1 в морской воде содержится Н2РО4-, 79% НРО42- и 20% РО43-. При более высоких значениях рН равновесие смещается в пользу РО43-, а НРО42- становится меньше. По ряду причин, в особенности благодаря образованию ионных пар и последующей стабилизации РО43- за счет кальция и магнезии, в морской воде гораздо больше РО43- , чем в пресной воде при аналогичном показателе рН. Это явление оказывает существенное влияние на такие вещи, как связывание фосфата с карбонатом кальция камней и песка, поскольку различные формы имеют различную степень взаимодействия.
В мировом океане концентрация ортофосфата существенно варьирует в зависимости от региона, а также в зависимости от времени суток и глубины. Поверхностные воды значительно беднее на ортофосфаты в сравнение с глубоководными участками, это обусловлено биологической активностью организмов, потребляющих фосфор. Типичный показатель концентрации фосфата в поверхностных водах по меркам рифовой аквариумистики довольно низкий, около 0,005 ррм.
При концентрациях ниже 0,03 ррм скорость роста многих видов фитопланктона зависит от концентрации фосфата (при условии, что другие факторы, такие как азот или железо, не сдерживают скорость роста). При более высоких концентрациях скорость роста многих организмов не зависит от концентрации фосфата. Таким образом, для ограничения роста нежелательных водорослей за счет снижения уровня фосфата, необходимо поддерживать концентрацию последнего на низких значениях.
Фосфор часто присутствует в других формах: полифосфаты, в которых кольца и цепочки ионов фосфора связаны по принципу Р-О-Р. Эти формы неорганического фосфора в природных условиях практически не представлены в морской воде, они входят в состав многих жидкостей, которые добавляются в рифовые аквариумы. Есть множество соединений такого плана, но большинство из них при попадании в аквариум распадутся до ортофосфатов. В промышленности полифосфаты используются для связывания металлов, например, в некоторых стиральных порошках: в данном случае, они образуют растворимые комплексы с кальцием и магнием, смягчая воду и усиливая очищающее действие. Количество фосфата, попадающего в природные водоемы с теми же моющими средствами достаточно для того, чтобы вызвать бурную вспышку водорослей, поэтому использование фосфатов в моющих средствах в настоящее время запрещено во многих регионах.
В морской воде органический фосфор представлен гораздо большим разнообразием форм, нежели неорганический фосфор. Множество биохимических комплексов содержат фосфор, в каждой клетке есть фосфор в самых разнообразных комплексах. Молекулы ДНК, АТФ, фосфолипидов (лецитин), многие протеины содержат фосфорные группы. В этих молекулах основные фосфатные структуры ковалентно присоединяются к остальной части молекулы посредством одного или более эфирных соединений с атомом углерода.
Такие связи стабильны на протяжение некоторого периода времени в воде, но рано или поздно распадаются с высвобождением ортофосфата из органической части молекулы. Данный процесс в условиях рифового аквариума можно ускорить с помощью ферментов. Большую часть этих органических фосфорных соединений удастся удалить из аквариума с помощью скиммера. Экспорт органических фосфатов – пожалуй, основной способ снижения уровня неорганического фосфата в аквариуме, если речь идет о скиммере. Эффективность скиммера в удалении неорганических ортофосфорных ионов незначительна, а вот удаление органического фосфата до того, как он превратится в неорганический ортофосфат - задача для скиммера вполне выполнимая.
Еще одна важная деталь касательно органических фосфатов – они плохо удаляются адсорбентами, способными выводить неорганический фосфат. Соответственно, адсорбенты могут активно связывать неорганический ортофосфат, но малоэффективны в борьбе с органическими фосфат-соединениями.
И наконец, большинство тестов не определяют органический фосфат. Те тесты, которые чувствительны к органическому фосфату (например, Hach PO-24), предварительно расщепляют фосфатную группу и органическую часть соединения, тем самым переводя фосфатную группу в неорганический ортофосфат. Такие тесты весьма трудоемки и недешевы, а потому не подходят многим аквариумистам. Я, например, никогда ими не пользовался.
Органика в морской воде часто измеряется по присутствующему в ней азотному компоненту, а именно растворенный органический азот (dissolved organic nitrogen, DON) и дисперсный органический азот (particulate organic nitrogen, PON). То же самое касается и фосфора, растворенный органический фосфат (DOP) и дисперсный органический фосфат (POP). Таблица 1 показывает относительные концентрации углерода, азота и фосфора в стандартном органическом компоненте морской воды: содержание азота, как правило, в 10 раз меньше содержания углерода, а содержания фосфора в сотни раз меньше, чем содержание углерода.
Органический фосфат, как и ортофосфат, настолько широко представлен в биосистемах, что любой натуральный продукт питания содержит значительное количество фосфора. Органический материал может не только быть использован как прямой источник углерода, азота и фосфора, органика может быть расщеплена и выведена в виде неорганики: ортофосфатов, аммиака, нитрита и нитрата. Ниже приведена схема метаболического расщепления типичного органического материала у фитопланктона:
Или прощеОрганика+ кислород = углекислый газ+вода+ион водорода+фосфат+нитрат
Сухие корма в виде хлопьев обычно содержат около 1% фосфора (эквивалент 3% фосфата) по весу (и многие другие корма, согласно информации на этикетке, содержат такое же количество фосфора). Соответственно, если 5 грамм хлопьев попадает в 100-галлонный (примерно 400-литровый) аквариум, то весьма вероятно, что лишь за одно кормление содержание ортофосфата поднимется на 0,4 ррм. Сам факт может стать серьезной проблемой для аквариумистов: что делать с таким количеством фосфора? Если бы пища полностью преобразовывалась в тканевую массу, то избытка фосфора не было бы. Однако, значительная часть пищи, потребляемая гетеротрофными организмами, преобразуется в энергию, при этом остаются побочные продукты в виде углекислого газа, фосфата и различных азотистых соединений (аммиак, нитрит, нитрат и пр.), как показано выше в схеме. Рыба, будь то растущая или взрослая особь, выделяет большое количество фосфора, потребляемого с пищей, в виде фосфата в продуктах жизнедеятельности. Разумеется, избыточное кормление приведет к избыточной экскреции фосфатов, а умеренное кормление уменьшит количество продуктов жизнедеятельности.
К сожалению, многие виды морепродуктов, встречающие в продаже в магазинах, содержат дополнительные источники фосфата, преднамеренно добавленные к морепродуктам в качестве консервантов. Сюда относятся замороженные и консервированные морепродукты, а также некоторые свежие морепродукты. В некоторых случаях промывание таких продуктов перед их употреблением уменьшает количество фосфатов, вносимых в аквариум с пищей.
Наконец, сама проточная вода может стать серьезным источником фосфата. Водопроводная вода, например, в Штате Массачусетс отличается приемлемо низким содержанием фосфата, по крайней мере, таковыми были мои последние результаты исследований. Однако, в других регионах уровень фосфата в воде слишком высок, что делает ее непригодной для рифового аквариума. В 2005 году по официальным данным в водопроводной воде города Нью-Йорк содержание фосфата было на уровне 3 ррм. Я бы советовал всем, кто использует водопроводную воду в аквариуме и сталкивается с проблемой нежелательных водорослей, провести детальное тестирование воды на уровень содержания в ней фосфата.
Обратная сторона проблемы – аквариумы без рыб. Поскольку фосфор – обязательный элемент для построения тканей, некоторое количество фосфора должно содержаться в воде в доступной для кораллов и беспозвоночных форме. Это простая задача, если в аквариуме есть рыбы, но в аквариумах, где рыб нет, рифоводам необходимо добавлять альтернативных источник фосфора. Решение простое: либо добавлять корм для рыб даже при отсутствии рыб, либо вносить удобрения для растений (причем, если удобрение не содержит азот, то его внесение тоже может потребоваться).
Ингибирование кальцификации фосфатами
Важной проблемой, возникающей при повышенном уровне концентрации фосфата в рифовом аквариуме, является ингибирование (угнетение) процессов кальцификации фосфатами и фосфат-содержащими органическими соединениями. Как известно, фосфат ингибирует осаждение карбоната кальция в морской воде. Присутствие фосфатов в воде также замедляет скелетообразование у кораллов, например у Poccilopora damicornis. Вероятно, это связано с присутствием фосфата в экстрацитоплазменной кальцифицирующей жидкости (ЭКЖ; extracytoplasmic calcifying fluid, ECF), где непосредственно у кораллов проходят процессы скелетообразования, и также с присутствием фосфата на поверхности растущего кристалла. Каким именно образом фосфат попадает в ЭКЖ до конца неясно.
Ингибирование кальцификации наступает при таких концентрациях фосфата, которые довольно часто регистрируются в рифовых аквариумах, и зачастую начинаются еще при значениях, которые не определяются любительскими тестами. Например, по данным одной исследовательской группы, длительное повышение уровня содержания фосфата (0,19 ррм в течение трех часов ежедневно) на естественном участке Большого Барьерного Рифа ингибировало общее скелетообразование у кораллов на 43%. Еще одна группа исследователей получила аналогичные результаты у нескольких видов акропор при идентичных концентрациях фосфата.
Органический фосфат и фосфонатные ингибиторы кальцификации, исходя из результатов исследований, работают по сходному принципу. Этидронат (бифосфонат, применяемый при лечении остеопороза) ингибировал кальцификацию у Stylophora pistillata на 36% при концентрации 2 ррм, и полностью приостанавливал (99% ) при концентрации 100 ррм (см. схему 3), при этом процессы фотосинтеза не подвергались изменениям как при указанных концентрациях, так и при более высоких показателях уровня ингибитора (следовательно, данный ингибитор не функционирует как общий токсин).
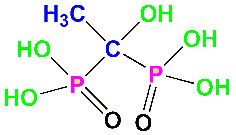
Схема 3. Химическая структура этидроната, представленная
в полной протонированной форме.
Способы удаления фосфата
Теперь, зная, откуда берется фосфат, и какое влияние он оказывает, рассмотрим, куда расходуется этот элемент и как максимально увеличить процессы его расходования. Разумеется, часть фосфора уходит на построение тканей растущих организмов, в том числе бактерий, водорослей, кораллов и рыб. Некоторые из этих организмов постоянно присутствуют в аквариумах, другие периодически удаляются путем прореживания водорослей, в результате работы скиммера и вследствие обрезки кораллов. Далее рассмотрим по отдельности каждый из этих способов.
Выведение фосфатов методом кальций-преципитации
Одним из механизмов снижения концентрации фосфата в рифовом аквариуме может быть метод преципитации (осаждения) фосфата кальция Ca3(PO4)2. Вода во многих рифовых аквариумах перенасыщена этим веществом, его концентрация превышает равновесную концентрацию, которая по фосфату составляет все лишь 0.002 ppm (то есть теоретически при концентрации фосфата выше 0.002 ppm фосфат должен выпадать в осадок в виде фосфата кальция). Так же как и с карбонатом кальция CaCO3, осаждение фосфата кальция Ca3(PO4)2 в морской воде ограничено скорее кинетическими факторами, чем равновесной концентрацией, так что невозможно сказать, сколько именно фосфата кальция выпадает в осадок в аквариумных условиях (если только, конечно, кто-либо не определит это экспериментально).
Реакция преципитации особенно вероятна в тех случаях, когда в аквариум вносятся добавки для поднятия уровня кальция и рН (например, кальквассера). Высокий рН преобразует значительное количество НРО42- в РО43- . А вместе с высоким уровнем кальция (также при добавлении кальквассера), высокий уровень РО43- может привести к перенасыщению Са3(РО4)2 до нестабильных значений, результатом чего станет эффект преципитации. Если выпавшие в осадок кристаллы фосфата кальция формируются в толще воды (например, если они образуются локально в месте, где кальквассер взаимодействует с водой), то кристаллы могут покрыться органикой и будут выведены скиммером.
Многие рифоводы считают, что использование кальквассера снижает уровень фосфатов. Возможно, это верно, однако важно также понимать сам механизм такого процесса. Крейг Бингман провел ряд экспериментов на данную тему и опубликовал результаты в старом журнале Aquarium Frontiers. И, несмотря на то, что многие аквариумисты не вникают в детали механизма преципитации, знание того, что происходит, поможет нам оценить эффективность данного метода и определить наилучший способ его применения.
Один из механизмов – преципитация фосфата кальция как описано выше. Еще один механизм снижения фосфатов с помощью добавок с высоким рН – соединение фосфата с карбонатом кальция. Абсорбция фосфата из морской воды в арагонит зависит от величины рН, максимально абсорбция протекает при рН около 8,4 и менее интенсивно при показаниях ниже или выше 8,4. Хабиб Секха (владелец Салиферта) указывал, что добавки кальквассера могут приводить к преципитации значительного количества карбоната кальция в аквариуме. Это абсолютно верная идея. В конце концов, дело не в том, что есть множество аквариумов, где четкий кальциевый баланс поддерживается за счет того, что вся испарившаяся вода восполняется насыщенным раствором кальквассера. Причем многие аквариумисты отмечают, что кальций и карбонатная жесткость остаются стабильными на протяжении длительного времени в результате применения именно такого способа. Такой результат имеет место, если избыток кальция и карбоната, обычно вносимый в аквариум с раствором кальквассера, в дальнейшем выводится за счет оседания карбоната кальция (на помпах, грелках, песке, камнях и т.д.). Тогда именно эта преципитация карбоната кальция и может снижать уровень фосфата: фосфат присоединяется к растущим поверхностям преципитата и становится его составной частью.
Если кристаллы карбоната кальция статичны (не растут), то описанный процесс обратимый, а арагонит может действовать как резервуар фосфата. Этот резервуар может ингибировать полное выведение фосфата из аквариума с высокими его концентрациями, и может дать возможность низшим водорослям прекрасно себя в таких условиях чувствовать, несмотря на то, что все дополнительные источники фосфата будут исключены. В таких крайних случаях может потребоваться удаление самого субстрата.
Если запасы карбоната кальция растут, то фосфат оказывается заключенным внутри растущего кристалла, а последний становится абсорбентом фосфата, по крайней мере до тех пор, пока СаСО3 каким-то образом не начнет растворяться. Кроме того, если такие кристаллы находятся в толще воды (например, если они формируются в точках соприкосновения кальквассера и морской воды), они далее могут быть покрыты органикой и выведены скиммером.
Если фосфаты связываются с поверхностью карбоната кальция в значительных количествах, описанный механизм можно запустить с помощью других добавок с высоким показателем рН (например, с помощью двухкомпонентной добавки по моему рецепту №1 для моей самодельной системы). К сожалению, добиться преципитации фосфата на поверхности карбоната кальция не удастся при низких значениях рН (например, в системах, использующих кальцивые реакторы или системы, в которых показатель рН низкий в силу избыточного атмосферного углекислого газа), потому что низкий рН ингибирует преципитацию избыточного кальция и карбоната, а также ингибирует связывание фосфата с карбонатом кальция.
Потребление фосфата живыми организмами
Каким образом живые организмы получают фосфат, практически во всех случаях остается малопонятным. Даже механизмы всасывания фосфата в организме человека по сей день до конца не изучены. Одна из областей моей научной деятельности включает использование медицинских препаратов для модификации абсорбции фосфата у людей. Пациенты с заболеваниями почек часто страдают от повышенного содержания фосфата в крови, поскольку не могут эффективно выводить из организма фосфаты, попавшие в организм с продуктами питания. Одним из результатов моей работы стало широкое применение препарата, снижающего усвоение фосфата (Renagel ®). Тем не менее, даже после многих лет работы, несмотря на потраченные миллионы долларов и время многих ученых в моей команде, я буду первым, кто признает, что механизмы поступления фосфора из пищи в кровь человека на молекулярном уровне до конца неясны. Неудивительно, что механизм абсорбции фосфата рифовыми обитателями тоже весьма мало изучен.
Потребление фосфата микроводорослями
Принято считать, что снижение уровня фосфатов ограничивает рост водорослей в аквариуме. В целом это почти полностью верное мнение, хотя некоторые виды микроводорослей гораздо лучше себя чувствуют при более низких значениях фосфата. Некоторые виды микроводорослей также могут существенно регулировать собственные объемы потребления неорганического фосфата в зависимости от уровня концентрации последнего. Многие организмы также могут с помощью ферментов расщеплять органический фосфат до неорганического ортофосфата, а уже впоследствии его потреблять. Вывод: мы слабо представляем себе, какие именно организмы в аквариуме потребляют какие именно формы и какие именно количества фосфора. Более того, аквариумная вода, как правило, отличается от природной морской воды с точки зрения сбалансированности остальных питательных элементов (азот, железо и пр.), поэтому нельзя делать выводы о состоянии аквариума лишь на основании оценки уровня фосфатов.
И все же, многие аквариумисты добиваются хороших результатов в контролировании низших водорослей лишь за счет снижения уровня фосфатов с помощью методов, рассмотренных далее в настоящей статье. Даже при низких концентрациях фосфатах (например, 0,02 ррм и менее) можно контролировать излишний рост водорослей, если организовать выведение фосфата другими способами до того, как они станут доступны водорослям. Как ранее отмечалось, при концентрации неорганического фосфата менее 0,03 ррм темпы роста многих видов фитопланктона зависит именно от количества доступного фосфата (при условии, что другие факторы, например азот или железо, не оказывают сдерживающего рост влияния). При концентрациях более 0,03 ррм уровень фосфата на темпы роста этих организмов влияния уже не оказывает. Следовательно, чтобы контролировать рост водорослей за счет уровня фосфатов, последний должен оставаться в пределах очень низких значений.
Наличие в системе достаточного количества микроводорослей может удерживать уровень фосфата ниже 0,02 ррм. То же относится к макроводорослям – достаточное количество макроводорослей может удерживать уровень фосфатов ниже 0,02 ррм – поэтому многие рифоводы используют макроводоросли для удаления фосфатов. Соответственно, сама по себе концентрация фосфатов не есть четким критерием в вопросе, поможет ли снижение уровня фосфатов в решении проблем с нежелательными водорослями. На самом деле, в большинстве случаев такой подход оказывается эффективным, хотя не всегда оказывается простой задачей выведение адекватных количеств фосфата, особенно если их уровень очень высок (скажем, выше 0,2 ррм).
Выведение фосфата макроводорослями
Выращивание макроводорослей может быть очень эффективным способом снижения уровня фосфатов (как и других питательных веществ) в рифовом аквариуме. В моей системе есть большой освещенные рефуджиум для выращивания каулерпы и хетоморфы (Caulerpa racemosa и Chaetomorpha sp.) – эти два вида водорослей однозначно самые активные потребители фосфата. Аквариумы с большим количеством процветающих макроводорослей не сталкивается с проблемами избыточного роста микроводорослей или избыточного содержания фосфатов, которые могли бы ингибировать скелетообразование у кораллов. Неясно, является ли снижение уровня фосфатов причиной уменьшения количества микроводорослей; недостаток других питательных элементов тоже может быть причиной. Хотя для аквариумистов, сталкивающихся с проблемой излишнего роста низших водорослей, четкие причины не имеют значения. Если быстро растущие макроводоросли в результате потребляют достаточное количество фосфора, в результате чего в воде остается очень малое количество ортофосфата, и в то же время не дают развиваться микроводорослям, то большинство аквариумистов будут довольны.
Для тех же, кому интересны конкретные факты, сколько фосфора потребляется макроводорослями, будет интересно ознакомиться с бесплатной статьей в pdf-формате из журнала Marine Biology. В статье приводится информация о содержании фосфора и азота у 9 различных видов макроводорослей, в том числе и тех видов, что часто встерчаются в морских аквариумах. Например, в сухом веществе виноградной каулерпы (С. Racemosa), собранной на Гавайях, содержится 0,08% фосфора и 5,6% азота. Значит, с каждыми 10 граммами выращенной в аквариуме каулерпы (ее сухого вещества) из воды будет выведено 24 мг фосфата. Это количество равно снижению концентрации фосфата с 0,02 ррм до 0,01 ррм в 67-галлонном (250-литровом) аквариуме. Все другие виды водорослей, использованные в исследовании, показали аналогичные результаты (с небольшими отличиями). Интересно, что согласно того же источника, с каждыми 10 граммами сухого вещества водорослей выводится 2,5 грамма нитрата, или 10 ррм на те же 67 галлонов (250 литров).
Выведение фосфата бактериями
Рост популяции бактерий – следующий способ выведения фосфатов. Рост популяции бактерий можно стимулировать с помощью внесения источников углерода в воду, к примеру, сахара, уксусной кислоты (уксус) и этанола (этиловый спирт, водка). Есть ряд коммерческих систем, таких как зеовит, построенных вероятно на методе внесения источника углерода, хотя в таких системах редко известно, на работе каких именно компонентов основан принцип работы. Бактерии потребляют дополнительно вносимые источники углерода, преобразуя их в энергию. В процессе роста и размножения, бактерии в обязательном порядке потребляют азот и фосфор из толщи воды, идущие на построение разнообразных биомолекул (ДНК, РНК, фосфолипиды и пр.). Впоследствии бактерии обычно выводятся из системы с помощью скиммера.
У этого способа есть один недостаток по сравнению, например, с культивированием макроводорослей: в процессе жизнедеятельности бактерии потребляют еще и кислород. Еще один момент – видовой состав популяции бактерий постоянно меняется. Эта изменчивость иногда может иметь весьма негативные последствия.
Экспорт фосфата скиммером
Органическое вещество, выводимое скиммером из аквариумной системы, обобщенно содержит углерод, водород, азот, фосфор и серу, а также ряд других элементов. Так что скимминг и удаление органики имеют весьма полезную функцию: они удаляют из воды вышеуказанные молекулы до того, как те будут преобразованы в фосфат, нитрат, сульфат и т.п. Ряд живых организмов, от рыб до бактерий, потребляют органику как источник энергии и выделяют избыточный азот, серу и фосфор, которые не задействованы в процессах роста. Во многих случаях в аквариуме эти выделенные элементы превращаются в фосфат (нитрат, сульфат и т.д.): это либо собственно продукты жизнедеятельности (как в случае с фосфатом и нитратом), либо промежуточные продукты (аммоний, мочевина и прочие азотистые соединения), которые далее в результате деятельности бактерий в конечном итоге превращаются в нитрат.
Неорганический ортофосфат сам по себе не адсорбируется на границе воды с воздухом, поэтому он не будет напрямую выводиться скиммером. Более того, такие сильнозаряженные ионы как ионы фосфата наоборот отталкиваются поверхностью воды и воздуха, что препятствует их гидратации.
Экспорт фосфата адсорбентами
В морской аквариумистике применяется множество различных коммерческих адсорбентов фосфата. Многие из этих адсорбентов являются неорганическими твердыми субстанциями, которые присоединяют фосфат к своим поверхностям. Одним из типичных адсорбентов является оксид алюминия (например, Seachem PhosGuard, Kent Phosphate Sponge). Еще один типичный адсорбент – метагидроксид железа (например, ROWAphos, PhosBan, Phosphate Killer от Салиферт). Эти вещества связывают, прежде всего, неорганический ортофосфат, а также некоторое количество органического материала.
Многие рифоводы ( в том числе и я) успешно применяют перечисленные продукты, однако у последних есть ряд побочных свойств, которые следует учитывать. Далее в статье мы более детально рассмотрим эти побочные свойства, но в целом можно сказать, что фосфатные адсорбенты имеют свойство частично растворяться в аквариумной воде, высвобождая свои компоненты (а именно алюминий и железо), а также примеси, которые могут в них содержаться. Эти примеси также могут обратимо связывать фосфат, но могут и высвобождать фосфат в воду при определенных условиях.
Активированный уголь в принципе не связывает больших количеств неорганического ортофофсфата, но при этом связывает значительное количество фосфат-содержащей органики (например, фосфолипидов). Тем не менее, если снижение уровня фосфатов является основной задачей, то есть более эффективные методы, нежели использование активированного угля.
Некоторые органические полимеры (например, мой препарат Renagel) разработаны с целью связывания фосфатов в различных формах. При том, что ряд подобных полимеров продаются в аптеках и предназначены для связывания фосфата, такие вещества не слишком эффективны в борьбе с неорганическим ортофосфатом в условиях морского аквариума. Эти вещества конкурируют в морской воде с избыточными количествами хлоридов (Cl-) и сульфатов SO42-). Органические полимеры могут эффективно связывать органику, аналогично активированному углю.
В настоящее время я занимаюсь сравнением относительной эффективности различных фосфатных адсорбентов, и надеюсь в скором времени опубликовать результаты своих исследований. К несчастью, такие сравнительные исследования занимают много времени, поскольку может пройти много дней, прежде чем конкретный реагент достигнет равновесного состояния (то есть, прекратит связывать или высвобождать фосфат) в насыщенной фосфатом морской воде, и понадобится не одна серия тестов различной концентрации фосфата (на основании которых ученые сравнивают эффективность различных адсорбентов).
Оксид алюминия
Оксид алюминия – основной компонент ряда выпускаемых фосфатных адсорбентов, например, Seachem PhosGuard. Это твердое вещество белого цвета, хотя не все адсорбенты белого цвета являются оксидами алюминия. Фосфат присоединяется исключительно к поверхностно расположенным ионам алюминия. Считается, что фосфат связывается с поверхностными ионами алюминия за счет прямого ионного взаимодействия между одним или двумя негативно заряженными ионами кислорода в молекуле фосфата и ионами алюминия (Al 3+), расположенными на поверхности вещества-адсорбента. Спустя достаточное количество времени, адсорбент удаляется из воды, а вместе с ним выводится и связанный фосфат. Этот механизм применялся и в других областях, в том числе и в медицине (ныне такой метод не рекомендуется, поскольку алюминий имеет токсичные свойства).
Недостаток данного метода в том, что оксид алюминия частично растворим в морской воде. Я показал экспериментально, что алюминий может высвобождаться из PhosGuard, и что добавление схожих концентраций алюминия в морскую воду может вызывать раздражение у кораллов, последние втягивают полипы и сжимаются. Это объясняет те побочные эффекты, которые отмечались рядом рифоводов еще до проведения тестов. Промывание адсорбента перед его использованием поможет снизить риск того, что мелкие частицы, содержащие алюминий, попадут в аквариум, но не исключит вероятности высвобождения ионов алюминия с поверхности адсорбента.
При всем сказанном, многие аквариумисты успешно применяют адсорбенты на основе оксида алюминия и при этом не сталкиваются с негативными последствиями. Я сам ранее применял такие адсорбенты без видимого ущерба для аквариума, однако я использовал весьма небольшие количества. Промывание перед использованием и использование малых количеств адсорбента снизит риск побочных эффектов.
Гранулированный оксид/метагидроскид железа
В последние годы в рифовой аквариумистике стали пользоваться адсорбенты на основе железа. Такие материалы используются для очистки питьевой воды (например, от мышьяка) или очистки сливных вод (для удаления ряда примесей, в том числе и фосфатов). Адсорбенты на основе железа продаются под различными названиями и торговыми марками (PhosBan, Phosphate Killer, ROWAPhos и пр). Цвет этих адсорбентов варьирует от красновато-коричневого до почти черного. В одной из предыдущих статей я подробно описал принцип их действия, а также возможные побочные эффекты их применения.
Несмотря на то, что выпускаемые сегодня адсорбенты на основе железа имеют довольно крупный размер частиц (на этикетке Салиферта указан размер 0,2 – 2 мм), у этих частиц на самом деле довольно большая внутренняя поверхность взаимодействия (сходно с активированным углем). Соответственно, внешний размер частиц адсорбента не является абсолютным критерием оценки доступной площади поверхности (в отличие от непористых твердых веществ, например, столовой соли). Я не встречал данных о размерах доступных площадей поверхности у доступных аквариумистам гранулированных оксидов железа, ГОЖ (granular ferric oxide, GFO). Компания Warner Marine выпустила ГОЖ (PHOSaR), размер частиц у которого намного больше, чем у большинства аналогов других брендов, что позволяет использовать данный адсорбент в стандартных мешочках для адсорбентов без риска, что мелкие частицы попадут в аквариум. Я сам этим адсорбентом не пользовался.
Фосфат, присоединенный к поверхности ГОЖ, может высвобождаться обратно в воду, то есть связывание носит временный, а не постоянный характер. Этот факт описан в литературе и может быть показан экспериментально. Детальному описанию я посвящу одну из своих последующих статей, вкратце же продемонстрирую следующий момент: допустим, определенное количество фосфата адсорбировалось на поверхности ГОЖ, а в воду добавлено количество фосфата, которое определяется тестами (например, 0,01 ррм) и находится в равновесном состоянии с количеством твердого вещества. Затем ГОЖ перемещается в морскую воду, в которой уровень фосфата не определяется. Обнаруженный в итоге фосфат в такой морской воде подтверждает, что ГОЖ высвобождает связанный фосфат при снижении концентрации фосфата в морской воде.
Одним из возможных побочных эффектов применения гранулированного оксида железа является вероятность попадания растворимого железа в морскую воду. Это железо, скорее всего, будет способствовать росту макроводорослей и я рекомендую добавки растворимого железа для стимуляции роста макроводорослей. В то же время, нехватка железа может быть сдерживающим фактором в развитии нежелательных водорослей (что наблюдается в некоторых областях мирового океана), поэтому добавление железа может способствовать еще и избыточному росту нежелательных микроводорослей. В большинстве же случаев аквариумисты отмечают спад в развитии водорослей при использовании ГОЖ, поскольку снижение уровня фосфатов гораздо существеннее влияет на уменьшение количества водорослей, нежели высвобождение железа – на их развитие.
Еще одним побочным эффектом использования ГОЖ в некоторых случаях может стать избыточная преципитация карбоната кальция вокруг ГОЖ или непосредственно на его поверхности. Оказывается, растворимое железо может вызывать преципитацию карбоната кальция. Такое явление может превратить целый мешок ГОЖ в единый комок и способствовать засорению помп, хотя в целом, если и будет иметь место, то, скорее всего, локально в области расположение ГОЖ. Степень проявления эффекта преципитации будет зависеть от того, насколько насыщена морская вода карбонатом кальция, а также от уровня концентрации магнезии и органики (оба эти компонента обычно снижают степень вероятности осаждения карбоната кальция).
Наконец, важно промывать гранулированный оксид железа в пресной или соленой воде перед использованием его в аквариуме, поскольку мелкие частицы могут высвобождаться, окрашивая и засоряя воду, а также создавая другие проблемы. Не существует каких-либо особых требований к промыванию ГОЖ. Аквариумистам, использующим ГОЖ в реакторах или канистровых фильтрах, достаточно несколько минут прополоскать порцию адсорбента пресной или морской водой. Мешок с адсорбентом достаточно промыть в нескольких порциях морской или осмосной воды. Важно не сдавливать адсорбент внутри мешка при полоскании, это может привести к разламыванию гранул и высвобождению мелких частиц.
В заключение: буду ли я применять гранулированный оксид железа для экспорта фосфатов? Ответ утвердительный, и я часто закладываю ГОЖ в канистровый фильтр, где также содержится активированный уголь.
Выводы: методы снижения концентрации фосфата
Мой совет аквариумистам – стремиться удерживать фосфаты на уровне 0,02 ррм или менее. Ниже приведен перечень возможных мер и способов выведения избыточных концентраций фосфата и поддержания его количества на желаемом уровне. Данный перечень составлен в порядке убывания согласно моим собственным предпочтениям:
1. Макроводоросли являются моими бесспорными фаворитами. Они не только эффективно справляются с задачей снижения уровня фосфата, но также способствуют выведению ряда других веществ (например, азотистых соединений). Это достаточно недорогой способ, который, помимо вышеозначенного, создает отличные условия для размножения мелких живых организмов, важных представителей морской фауны и бесценных элементов пищевой цепочки. Кроме того, за ними очень интересно наблюдать. В эту группу я бы еще включил другие организмы, которые рифоводам приходится периодически прореживать, будь то кораллы (например, ксения) или иные фотосинтетики.
2. Скиммер – еще одно весьма эффективное средство снижения уровня фосфата. Он не только выводит органические формы фосфата, снижая тем самым риск его расщепления до неорганических форм, но также выводит другие вещества и улучшает газообмен. Важность газообмена недооценивается многими аквариумистами, хотя это первостепенный фактор в вопросах поддержания рН.
3. Кальквассер, а также возможно другие добавки с высоким значением рН, также хороший выбор. Он недорог и выполняет еще две важных задачи: поддержание уровня кальция и кН. Достаточно удерживать рН в аквариуме на высоких значениях (8,4), чтобы предотвратить высвобождение фосфата, связанного с камнями и песком, обратно в воду. Если рН падает до значений в области 7,0-7,9, особенно, если он падает до значений при которых начинает растворяться арагонит, в воду будет высвобождаться фосфат. В системах с подобной картиной (такие, где используется кальциевый реактор), нужно поднимать показания рН.
4. Адсорбенты, выпускаемые различными фирмами, достаточно эффективны. Они могут быть достаточно дорогостоящими и имеют побочные эффекты, но при этом могут значительно снизить концентрацию фосфатов, а это часто является первостепенной задачей.
5. Стимуляция роста популяции бактерий. Эффективный способ борьбы с фосфатом и другими веществами (азотистые соединения). Недорогой способ, имеющий ряд дополнительных преимуществ (дополнительный источник пищи для многих жителей морского аквариума). Недостаток этого способа в том, что становится сложно поддерживать большую популяцию бактерий и одновременно минимальное количество питательных веществ. Также проблемой может стать недостаток кислорода.
Общие выводы
Проблемы, связанные с накоплением фосфатов и последующим ростом водорослей , могут быть одними из наиболее сложно решаемых в рифовом аквариуме, особенно если живые камни и песок подверглись действию высоких концентраций фосфата и в результате превратились в его резервуары. К счастью, есть ряд превентивных мер, в том числе и уменьшение концентрации фосфата, от которых состояние аквариума улучшится, даже если аквариум не страдает от избыточного роста водорослей. К таким мерам в первую очередь относится выращивание макроводорослей и использование скиммера. Каждый аквариумист, создающий новую систему, должен иметь четкое представление о том, как фосфат будет удаляться из аквариума. Если пренебречь этим вопросом, скорее всего, накопление фосфата в итоге приведет к росту микроводорослей, с чем многим рифоводам придется постоянно бороться.
Желаю вам успехов!Первоисточник: http://reefkeeping.com
Если вы увидели этот материал на другом сайте - значит, он был украден.
reefcentral.ru
Способ извлечения из сточных вод фосфатов и органически связанного фосфора
Использование: удаление фосфатов и органически связанного фосфора из сточных вод. Сущность изобретения: сточные воды обрабатывают Al-содержащим коагулятом и флокулянтом. Коагулянт представляет собой стабилизированный щелочью раствора глинозема, который получают щелочным растворением боксита и/или путем щелочного травления алюминия. Молярное отношение оксидов Na2O : Al2O3 в растворе составляет 1,5-5,0. Раствор содержит 100-300 г/л Al2O3 и 100-400 г/л Na2O3 . Раствор глинозема вводят в сточные воды в количестве 10-200 мг/л. 1 с. и 8 з.п. ф-лы, 4 табл.
Изобретение относится к технологии очистки сточных вод и может быть использовано для извлечения фосфора из бытовых и промышленных сточных вод.
Известные способы извлечения растворенных фосфатов основаны на осаждении путем добавления солей железа и алюминия. При этом используют кислые соли, предпочтительно хлориды железа, сульфаты железа, сульфат хлорида железа, хлорид алюминия или сульфат алюминия, и комбинированные продукты этих соединений. Применение солей железа и алюминия при осаждении фосфатов приводит к тому, что наступает дополнительное засаливание хлоридами и сульфатами, и кроме того, происходит дополнительное снижение значения рН до кислого интервала. При удалении фосфатов хлоридом железа по уравнению FeCl3 + PO43- FePO4 + 3Cl- на 1 мг фосфора в 1 л приходится 3,4 мг хлорида в 1 л. На практике это значение составляет приблизительно на 50% больше, так как соли хлорида железа содержат избыточное количество хлорида (соляная кислота). Приблизительно так же высоко загрязнены сточные воды сульфатами, если вместо названных хлоридов используют сульфаты железа или сульфаты алюминия: Fe2(SO4)3 + 2PO43- 2FePO4 + 3SO4-2 На 1 мг Р приходится 4,6 мг SO42- на литр сточных вод. В случае стадии биологической очистки применяют так называемые способы оживления, при которых сточные воды наполняют активным шламом с аэробными бактериями. Механически предварительно осветленные сточные воды смешивают с активным шламом и через смесь пропускают в течение 1-4 ч воздух при постоянном перемешивании. Степень очистки составляет 85-90 или 60-80% Известно выделение фосфатов в виде фосфата кальция или апатита из сточных вод, при этом чаще всего сочетают механическо-биологическую очистку сточных вод при добавлении едкого натра или гидроокиси кальция при рН выше 9. Проблематичным в этих способах является образование трудно осаждающихся или отделяющихся мельчайших частиц и заряжение водной фазы ионами Са, которые могут привести к камнеобразованию и отложению нежелательных примесей. Наиболее близким по технической сущности является способ очистки сточных вод от фосфатов с использованием алюмината натрия и анионного флокулянта гомополимера или сополимера акриловой кислоты. Недостатком способа является недостаточная эффективность очистки. Задачей изобретения является создание способа извлечения фосфатов из сточных вод, который наряду с эффективным извлечением фосфатов позволяет избежать засаливания сточных вод. Для осуществления способа используют для очистки щелочно стабилизированный раствор глинозема. При этом следует подразумевать такой раствор, в котором отношение Na2O:Al2O3 составляет 1-1,5. Сточными водами могут быть любые воды, которые загрязнены фосфатом. Основная область применения изобретения это очистка сточных вод в установках осветления. Особенно пригоден способ в стадии очистки механическо-биологического осветления с последующим дополнительным осветлением, так как щелочной раствор алюмината натрия приводит также к слабому подщелачиванию сточных вод, что вредит оптимальной кондиции для эффективной активности бактерий. Добавление щелочно-стабилизированного раствора глинозема приводит в соответствии со следующей реакцией к осаждению нерастворимого фосфата алюминия: PO43- + Na(Al(OH)4) AlPO4 + NaOH + 3OH-. Особое значение изобретения состоит в том, что для осаждения фосфата используют щелочно растворимую соль алюминия, предпочтительно в виде алюмината натрия из растворенного в щелочи глинозема. Чистый алюминат натрия, который получается в результате растворения гидрата алюминия в едком натре, имеет тот недостаток, что при понижении температуры очень быстро выкристаллизовывается и может служить слабым коагулянтом в установках осветления особенно зимой. Технический раствор алюмината натрия имеет, как правило, отношение Al2O3: Na2O (весовое) 1:(0,6-0,8), т.е. около 25% Al2O3 приходится на приблизительно 20% Na2O. В предложенном способе используют предпочтительно щелочно растворенный глинозем, в котором существует обратное соотношение, т.е. явный избыток Na2O или натриевой щелочи. Предпочтительно он содержит около 12% Al2O3 и около 18% Na2O. В результате этого при применении в биологических установках осветления повышается значение рН, что является большим преимуществом. Благоприятным отношением Al2O3 и Na2O является приблизительно 1:1,2, т. е. около 170 г/л Al2O3 приблизительно соответствуют 200 г/л Na2O. Способ в соответствии с изобретением с особым эффектом применяют в случае осветлительных установок. Одновременно удаляются из воды вещества, замутняющие воду. Кроме того, способ приводит к уменьшению органических остаточных загрязнений, что выражено в снижении содержания CSB. В результате явно улучшается качество воды. Кроме того, неожиданно оказалось, что растворенные в щелочи органические вещества, облегчают введение полимерных биологически активных веществ. Полимерное биологически активное вещество состоит предпочтительно из гомополимеризата акриловой кислоты и сополимера акриламида и акрилата натрия. При этом количество акрилата натрия, считая на сополимер, составляет 10-80 мол. предпочтительно 20-40 мол. Действие полимеризата состоит в том, что при применении смеси алюмината и полимеризата при дозировке 50-500 мг/л и предпочтительно 50-200 мг/л, в зависимости от содержания фосфата в сточных водах, образуется фосфат алюминия и/или гидроксид алюминия, который в присутствии дополнительного полимеризата значительно быстрее осаждается. Положительное действие полимеризата при осаждении гидрооксида алюминия и фосфата совершенно явно проявляется при сравнении с осаждением, которое проводят с или без добавки сополимера. Описываемый способ имеет, кроме того, преимущество, которое заключается в том, что при применении щелочного глинозема и образовании фосфата алюминия имеет место незначительное дополнительное засаливание системы, так как введение хлоридов и сульфатов исключено. Кроме того, имеет место небольшое восстановление значения рН. Другим положительным побочным эффектом является приблизительно на 20% меньшее образование продуктов осаждения фосфата по сравнению с солями железа или также гидроксидом кальция. Стехиометрия вышеназванного уравнения реакции такова: при удалении 1 мг р/л получается при использовании FeCl3 4,86 мг/л шлама FePO4, при использовании щелочного раствора глинозема только лишь 3,93 мг/л шлама фосфата алюминия. Кроме того, изобретение имеет явные экономические и экологические преимущества. Используемый в соответствии с изобретением коагулянта ("алтон") содержит приблизительно 7 мас. Al и имеет концентрацию Na2O приблизительно 200 г/л. Добавка поликарбоновой кислоты составляет около 0,5 мас. муравьиной кислоты и в качестве коагулянта содержатся около 0,2 мас. сополимера акриламида и акриловой кислоты сополимера (приблизительно 70:30). Соотношение Na2O:Al2O3 составляет 1,7. П р и м е р 1. Проводят различные тесты с "алтоном" со сточными водами осветлительной установки по сравнению с хлоридами железа (раствор FeCl3, 40% -ный). Соответственно смешивают 1 л сточных вод после предварительного осветления с различными концентрациями осадителями. Через 1 ч сточную воду отфильтровывают и анализируют фильтрат (табл.1). Изменения значения рН. В результате использования "алтона" значение рН слегка поднимается, в результате добавления кислого раствора хлорида железа значение рН снижается. То же относится к м-значению, которое является мерой кислотности и буферной способности воды. В результате добавления "алтона" общая жесткость снижается. Это значит, что в результате повышения значения рН образуется дополнительно фосфат кальция или карбонат кальция. При использовании хлорида железа жесткость изменяется незначительно. С увеличением добавляемого количества осадителя содержание фосфата может уменьшаться. "Алтон" уже при малых дозировках дает хорошую эффективность, в то время как хлорид железа лишь при больших дозировках становится эффективным. Считая на Al или Fe, оказалось, что при одинаковых мольных количествах алюминий значительно эффективнее алюмината. Сравнительный пример. В стадии работы биологической установки осветления сточную воду аэрируют. В результате окисления микроорганизмами получается угольная кислота и органические кислоты, которые соответственно снижают значение рН, или препятствуют повышению рН. Сточная вода находится благодаря растворенной угольной кислоте в природном равновесии известь/угольная кислота. В результате аэрации воды (например, в охладительной башне) угольная кислота удаляется, так что нарушается равновесие известь/угольная кислота и карбонат кальция или фосфат кальция могут осаждаться. При обработке воды охлаждением это является известным парадоксом. Один литр сточной воды аэрируют. Изменение значения рН регистрируют с помощью самописца через измерительный электрод. Через определенные промежутки времени отбирают пробы, фильтруют и анализируют. В результате аэрирования сточной воды (без активного шлама) повышается щелочность или рН воды, так что растворенные гидрокаpбонаты или гидрофосфаты осаждают в виде солей кальция и наступает уменьшение концентрации фосфатов. П р и м е р 2. Чтобы изменить влияние осадителя при обработке активным шламом, принимая во внимание равновесие известь/ угольная кислота, проводят дополнительную серию опытов. При этом сточную воду с установки осветления, а также смесь с возвратным шламом из обработки активным шламом (1:1) аэрируют с или без кондиционирования осадителя 4 ч. В результате активности бактерий, воспроизводящих кислоту, значение рН в возвратном шламе находится в слегка кислом интервале (рН 6,8). Смешивание со сточными водами дает значение рН 7,2 и изменяется в результате аэрации лишь до 7,5, в то время как значение рН с чистой водой в результате аэрации увеличивается до 7,7-8,4. В результате добавления "алтона" значение рН слегка увеличивается, а добавление кислого раствора хлорида железа снижает значение рН. То же самое относится к значению -м, которое в результате аэрации при добавлении FeCl3 понижается до 1,1. В результате введения "алтона" и в результате аэрации значение общей жесткости снижается, что указывает на то, что в результате сдвига равновесия сточных вод образуется фосфат кальция или карбонат кальция. Даже только в результате аэрации содержание фосфата уже снижается. В результате добавления щелочного "алтона" происходит более полное удаление фосфата, чем в результате добавления кислого хлорида железа. Степень дозирования коагулянта поддерживают сознательно низкой, чтобы лучше наблюдать реакции в соотношении равновесия известь/угольная кислота. В результате аэрации и активности шлама равновесие известь/угольная кислота сточных вод изменяется по известным закономерностям. Это сказывается на значении рН, кислотоемкости (м-значении), содержании кальция и на удалении фосфата. Теоретически достаточно 1 градуса жесткости по немецким стандартам /= 10 мг СаО/л/, чтобы осадить 3,7 мг Р/л в виде фосфата кальция, если значение рН соответственно высокое. Применение щелочного раствора глинозема "алтон" имеет многообразное действие, особенно при общем осаждении: ионы алюминия осаждают фосфаты, буферная кислотная нагруженность воды увеличивается, ионы кальция используются одновременно для осаждения фосфата, не происходит дополнительного засаливания хлоридами. П р и м е р 3. На установке осветления (подача сточных вод около 2400 м3/день/ используют для удаления фосфата "алтон". Продукт дозировано подают шнековым насосом в концентрированном виде на входе в бассейн с активным шламом. Дозированное количество постепенно снижают от 12 кг "алтона" в 1 ч (около 120 ппм) до 6 кг в 1 ч (около 60 ппм). Уже через день проявляется позитивное действие на всю работу установки для осветления. Возможно снизить не только содержание фосфора приблизительно 5 до 0,5 ппм, но одновременно улучшить снижение CSB в биологии, а также качество сточных вод в последующем осветлении. Содержание CSB смогли снизить более чем с 110 ппм до приблизительно 80 ппм при выходе из установки осветления. Результаты приведены в табл.3. П р и м е р 4. Влияние "алтона" на осаждаемые вещества в мг/л (на примере коммунальной установки для осветления) выражено очень сильно. П р и м е р 5. В установке для осветления с рН сточных вод 5,5-6,0 применяют алюминат натрия с отношением Na2O:Al2O3, равным 4,0:1. Дозировка составляет 100 мг/л. При этом биологическое значение рН составляет 7,0-7,5. Это дает возможность проводить биологическую нитрификацию с одновременным осаждением фосфата в виде гидрофосфата алюминия. Содержание фосфата снижается от 5,2 (на входе) до 0,8 мг/л на выходе. П р и м е р 6. На осветлительной установке в условиях примера 5 повторяют описанный в нем способ с использованием щелочно стабилизированного раствора Al2O3 с молярным соотношением Na2O:Al2O3, равным 5,0:1. Дозировка 100 мг/л сточных вод. Содержание фосфата снижается с 5,2 (на входе) до 0,6 мг/л (на выходе). П р и м е р 7. В условиях примера 5 осуществляют очистку с использованием щелочно стабилизированного раствора глинозема с молярным соотношением Na2O: Al2O3, равным 1,5:1. Дозировка 150 мг/л сточных вод. Снижение содержания фосфатов 5,2-1,3 мг/л. Как показывают приведенные выше примеры, использование заявленного алюминийсодержащего реагента позволяет достичь высоких степеней очистки сточных вод от фосфатов как при высоких молярных соотношениях Na2O:Al2O3, так и при низких. Помимо этого в качестве положительного побочного эффекта дополнительной нитрификацией была достигнута стабилизация кислой среды при биологической очистке.Формула изобретения
1. СПОСОБ ИЗВЛЕЧЕНИЯ ИЗ СТОЧНЫХ ВОД ФОСФАТОВ И ОРГАНИЧЕСКИ СВЯЗАННОГО ФОСФОРА путем введения алюминийсодержащего реагента и флокулянта, отличающийся тем, что, с целью повышения эффективности очистки, в качестве алюминийсодержащего реагента используют стабилизированный щелочью раствор глинозема с молярным отношением оксидов Na2O / AI2O3 1,5 - 5,0, который получают щелочным растворением боксита или путем щелочного травления алюминия. 2. Способ по п.1, отличающийся тем, что в качестве стабилизированного щелочью раствора глинозема используют смесь раствора, полученного щелочным растворением боксита, и раствора, полученного путем щелочного травления алюминия. 3. Способ по пп.1 и 2, отличающийся тем, что стабилизированный щелочью раствор глинозема содержит 100-300 г/л AI2O3, предпочтительно 150-200 г/л. 4. Способ по пп. 1-3, отличающийся тем, что стабилизированный щелочью раствор глинозема содержит 100-400 г/л Na2O, предпочтительно 200-250 г/л. 5. Способ по пп.1-4 отличающийся тем, что стабилизированный щелочью раствор глинозема вводят в количестве 10-200 мг/л сточных вод, предпочтительно 50-100 мг/л. 6. Способ по пп.1-5, отличающийся тем, что стабилизированный щелочью раствор глинозема содержит поликарбоновую кислоту в количестве 0,1-1,0мас. предпочтительно 0,5 мас. 7. Способ по пп.1-6, отличающийся тем, что стабилизированный щелочью раствор глинозема содержит сополимер акриламида и акриловой кислоты в количестве 0,1-1,0 мас. предпочтительно 0,2-0,5 мас. 8. Способ по п.7, отличающийся тем, что сополимер содержит 10-80 мол. акриловой кислоты, предпочтительно 20-40 мол. 9. Способ по пп.1-8, отличающийся тем, что очистку от фосфатов и органически связанного фосфора совмещают с биологической очисткой, причем предпочтительно при аэрации.РИСУНКИ
Рисунок 1, Рисунок 2, Рисунок 3www.findpatent.ru
Очистка воды от азота и фосфора так же необходима, как и механическая очистка
Очистка воды от азота должна выполняться в обязательном порядке, поскольку его соединения, находящиеся в воде, очень токсичны. И для эффективного удаления азота из воды используются специальные ионообменные смолы или цеолиты. Очень часто для более качественной очистки используются установки обратного осмоса воды.
Сегодня разработаны специализированные биотехнологии для полной водоочистки и удаления из городских бытовых сточных вод соединений фосфора и азота, помимо органических веществ. Делается это для того, чтобы привести показатели воды к требованиям, допускающим сброс ее в природные водоемы.
При использовании традиционных установок биологической очистки (аэротенков), добиться максимальной степени удаления азота не удается, максимальная степень очистки не превышает тридцати процентов, что недопустимо по требованиям стандартов. И для качественной глубокой очистки от соединений фосфора и азота используются биотехнологии дефосфотации и нитриденитрификации.
В устройствах нитриденитрификации соединения аммонийного азота преобразуются в нитратные, после чего в молекулярный азот, выдуваемый в атмосферу. В процессе денитрификации (биологического восстановления нитратов и преобразования их в молекулярный азот) биологическое окисление органических соединений происходит не под воздействием кислорода, а осуществляется нитратами, вследствие чего появляется хорошая возможность сократить расход воздуха на аэрацию и материальные затраты.
Нужно отметить, что очистка воды от азота с помощью методов озонирования воды, хлорирования, ультрафиолетового облучения, электролиза и ионного обмена малоэффективна, и более того, для выполнения такой очистки требуется дорогостоящее оборудование и химические реагенты. Также она достаточно сложна в эксплуатации. Куда более эффективным является использование биологических способов (аэротенков).
Для удаления соединений азота используются взвешенные культуры ила, активного ила с прикрепленными микроорганизмами или же комбинацией из этих способов. При выполнении данных методов происходят процессы денитрификации и нитрификации — то есть, превращения аммиака в азотную кислоту (путем окисления), что сопровождается нитрификацией (ассимиляцией углекислоты) нитрита и преобразования его в газообразный азот.
Бактерии-верификаторы, находящиеся в активном иле, объединяются с гетеротрофной микрофлорой. И данная микрофлора начинает усиленно поглощать кислород, окисляя органические вещества, что создает весьма неблагоприятные условия для нитрифицирующих микроорганизмов. А окисление аммониевого азота в воде происходит после того, когда органические вещества почти все используются, функционирование гетеротрофной микрофлоры выходит на стабильный режим, а в аэрируемой смеси находится кислород в растворенном виде.
Самая эффективная очистка воды от азота — с использованием метода сорбации. Данная глубокая очистка позволяет удалить из воды почти 99 процентов фосфора и азота. Также сегодня были разработаны несколько мероприятий, с помощью которых можно эффективно бороться с загрязнениями непосредственно в водоемах — например, специально увеличивать содержание в воде кислорода посредством использования аэрационных установок. Данные установки сегодня применяются во многих развитых странах Европы, немало их и в нашей стране. Для того, чтобы снизить рост в водоемах водорослей, применяют всевозможные гербициды.
Однако довольно часто бывает такое, что стоимость осуществления глубокой очистки воды от азота намного меньше, чем стоимость гербицидов, которые нужно использовать для уменьшения количества водорослей. Поэтому актуальной является проблема снижения в воде концентрации нитратов, которые также представляют для людей опасность. По стандартам Всемирной Организации Здравоохранения допустимое количество нитратов в воде 45 мг/литр, а если пересчитать на азот, то всего 10 мг/литр. Данная величина является стандартом и для питьевой воды, и для той, что находится в водоемах. характер и количество соединений азота влияют на общее состояние водоемов, следовательно, их включили в число основных показателей при оценке качества воды.
Смотрите также:
www.bwt.ru
Удаление - фосфат - Большая Энциклопедия Нефти и Газа, статья, страница 3
Удаление - фосфат
Cтраница 3
Наиболее простым способом является значительное повышение величины рН добавлением извести для образования гидроксида аммония и удаление аммиака отдувкой воздухом в контактной башне. Хотя этот процесс может быть совмещен с удалением фосфатов, он используется редко, так как для больших расходов сточных вод требуются огромные сооружения с большим числом вентиляторов. Кроме того, возникает ряд проблем в зимнее время, а также существует постоянная угроза отложения карбоната кальция в башне. [31]
Понизить содержание фосфата можно также, возвращая химический осадок, образующийся на стадии постосаждения, в реактор, где происходит биологическая очистка, иными словами, объединяя постосаждение и одновременное осаждение. При этом используется сорбционная емкость химического осадка для удаления фосфатов на биологической стадии, где концентрация фосфатов несколько выше, чем в реакторе постосаждения. [32]
При определении многих катионов весовым, комплексометри-ческим или атомноабсорбционным методом мешают фосфаты. Хинсон [30] определял кальций в растениях атомноабсорбционным методом после удаления фосфатов с помощью ионного обмена. [33]
Предлагается прокаливать водопроводный осадок, состоящий в основном из А1 ( ОН) з при температуре 500 - 1000 С, и переводить в таблетированное состояние с добавлением связующего агента с последующим перемешиванием. Полученные таким образом таблетки можно использовать не только как сорбент для удаления фосфатов, но и как катализатор. Возможно также использование в качестве катализатора для увеличения степени очистки сточных вод смеси окислов, содержащих 50 - 52 % окиси алюминия. [34]
На традиционных сооружениях для биологической очистки сточных вод удаляется большая часть органических веществ и в значительной степени тяжелые металлы, хотя от последних проще всего освобождаться на промышленных предприятиях. В настоящее время разработаны усовершенствованные способы химической обработки сточных вод, предназначенные для удаления фосфатов, а та кже ряд способов химической и биологической обработки для удаления азота; однако эти процессы лишь в очень незначительной степени снижают концентрацию растворенных примесей. [36]
При наличии фосфат-ионов иногда применяют обратное титрование. В некоторых работах, однако, предложено применять комплексометрическое титрование в сочетании с ионообменным разделением для удаления фосфата и других мешающих анионов. Во многих случаях такое сочетание, безусловно, весьма полезно. [37]
Отмечается также [50], что окись алюминия не может полностью заменить активированный уголь из-за недостаточной эффективности очистки ею сточной воды. Однако большая величина удельной адсорбции и простота регенерации окиси алюминия делают целесообразным использование ее на доочищен-ных сточных водах с целью удаления фосфатов. [38]
На этой стадии могут быть проведены также испытания на молибден и мышьяк. Для этого раствор подкисляют серной кислотой, насыщенной сероводородом под давлением, фильтруют и особенно тщательно промывают ( водой, свеженасыщенной сероводородом) для удаления фосфата и следов алюминия. Фильтр разрывают на две части; одну испытывают азотной кислотой на синюю окраску молибдена, как описано на стр. После обработки дымящей азотной кислотой выпаривают большую часть кислоты, разбавляют, фильтруют и добавляют аммиак и магнезиальную смесь. Поскольку весь фосфор был вымыт, белый кристаллический осадок, появляющийся при стоянии, вызывается только мышьяком из сульфидного осадка. Большое количество мышьяка придает сульфидному осадку желтый оттенок. [39]
С в течение нескольких часов. По окончании инкубации оставшуюся РНК осаждают из 7О % - ного спирта ( над - осадочная жидкость при этом содержит отщепившееся основание), вновь растворяют в водном буфере и обрабатывают фосфатазой для удаления концевого фосфата. [40]
Монацит, ксенотим и другие урансодержащие фосфаты можно также разлагать сплавлением с. Поскольку большие количества фосфатов мешают при последующих операциях, водную вытяжку сплава кипятят с несколькими миллилитрами спирта для разложения перекисей; нерастворимый остаток отфильтровывают, лучше с применением отсасывания, хорошо промывают горячим 2 % - ным раствором нитрата натрия для удаления фосфата натрия и затем растворяют в азотной кислоте. Кислоту, которой обмывались стенки тигля, присоединяют к основному раствору на этой стадии анализа. Полученный азотнокислый раствор выпаривают до небольшого объема. [41]
Небольшие частицы ( диаметром меньше 2 мкм) имеют отрицательный заряд, препятствующий их агломерации. Коагулянты, содержащие положительно заряженные ионы А13, Fe3, притягивают такие частицы, образуя агрегаты и способствуя осаждению. Для удаления фосфатов также используют химическую обработку. [42]
Водопроводные осадки, образующиеся при коагулировании сернокислым алюминием высокоцветных маломутных вогх ( Ц60, 10 %; М4 мг / л, 10 %), могут быть использованы в качестве реагентов для удаления из сточных вод соединений фосфора. Для достижения 90 % - ного эффекта удаления ( при начальной концентрации фосфатов РО4 -, равной 6 5 мг / л) доза водопроводного осадка должна быть не менее 100 мг / л по сухой массе на один литр сточной воды. Во всех остальных случаях эффект удаления фосфатов из сточных вод определяется экспериментально. [43]
Особенно типичной проблемой являются помехи, вызываемые фосфат-ионами. Так как фосфат-ионы, подобно мономерному кремнезему, образуют желтую фосформолибденовую кислоту при взаимодействии с молибденовой кислотой, то необходимо их устранять. Они включают: - а) осаждение и удаление фосфата в виде соли кальция; б) регулирование значения рН для того, чтобы желтый цвет давал только мономерный кремнезем; в) разрушение желтого фосфатного комплекса действием лимонной, щавелевой или винной кислот; г) селективное превращение кремнемолибденовой кислоты в молибденовую синь. [44]
В настоящей главе приводятся результаты изучения метода химической коагуляции для удаления водорослей с целью улучшения качества сточных вод после биологического пруда. Изучено воздействие различных коагулянтов и определена степень эффективности снижения БПК, ХПК, содержания общих фосфатов, азота, co / i-бактерий и водорослей. Для исследования предложена математическая модель, связывающая степень удаления фосфатов с дозой коагулянта. [45]
Страницы: 1 2 3 4
www.ngpedia.ru
Технология Phoslock в борьбе с цветением водоемов
26 ноября 2012На протяжении уже более десятилетия, эффективность продукта по очистке воды под названием Phoslock® в осаждении и удалении фосфора была доказана во всем мире с помощью многочисленных исследований и опытных испытаний для водохранилищ питьевой воды и пресноводных озер. С 2008 года в Онтарио были проведены испытательные работы (оценка которых осуществлялась независимым агентством) для демонстрации эффективности Phoslock® в решении вопросов избытка фосфора и проблем роста сине-зеленых водорослей для регулирующих поверхностных сток прудов, водохранилищ, озер и сельскохозяйственных дренажных систем.
Недавно в комплексе с удалением избыточной растительности впервые этот препарат был применен как основное средство очистки для сооружения по регулированию поверхностного стока в масштабе города. С точки зрения перспектив эксплуатации, использование Phoslock® было определено как наиболее экономически эффективное по сравнению с другими доступными технологиями очистки воды или подходами в удалении осадка.
В состав Phoslock® входит редкоземельный элемент лантан и бентонитовая глина. Лантан формирует постоянную электростатическую связь с бентонитом и не выщелачивается из него. Получающийся в результате продукт крепко связывается с фосфатами, формируя зернистый материал, который осаждается на дне.

Схема действия препарата Phoslock® (ссылка на источник)
После распределения Phoslock® в водоеме в виде гранул или взвеси, препарат удаляет до 99% растворенных в воде фосфатов за первые четыре часа. В результате реакции формируется очень стабильный нерастворимых минерал известный под названием рабдофан (LaPO4.nh3O). Когда Phoslock® оседает на разделе сред вода - донные осадки, он формирует тонкий проницаемый слой. Этот слой способен абсорбировать фосфор из осадков.
При связывании с Phoslock® фосфаты перестают быть доступным для водорослей, что позволяет снизить их рост. Одна тонна Phoslock® способна удалить 34 кг фосфатов, или 11 кг фосфора.
Удаление фосфора из воды увеличивает соотношение азота к фосфору, что приводит к изменению набора видов водорослей и значительного снижения сине-зеленых водорослей в водоемах.
Препарат нечувствительный к окислительно-восстановительным условиям и рН в широких диапазонах (от 4 до 11) и поэтому удаление фосфатов происходит в постоянном режиме. Phoslock® одинаково применим для удаления фосфатов и в пресной, и в морской воде. Когда Phoslock® применяется для водоемов с высоким уровнем содержания питательных веществ, снижение концентраций растворенных фосфатов снижает и его трофический статус. Со временем, сильно эвтрофицированный водоем может перейти в состояние с низким содержанием питательных веществ.
Применение Phoslock® для озер и водохранилищ продемонстрировало снижение концентрации фосфатов в воде до очень низких уровней, достаточных значительно ограничить развитие сине-зеленых водорослей. Продукт наиболее эффективен, если его применять в период поздней осени, обеспечивая то, что концентрации фосфатов в следующий сезон будут достаточно низкими, чтобы сдержать рост водорослей. Phoslock® не является гербицидом. Основной принцип действия Phoslock® - это быстрое удаление практически всех фосфатов из водной толщи, за счет чего происходит угнетение первичных продуцентов.
В водоемах, где есть внешние источники поступления фосфатов, Phoslock® будет работать до тех пор, пока будет оставаться ненасыщенный лантан. Если же поступление фосфатов в водоем будет продолжаться, то период времени, в течение которого будет сохраняться результат действия Phoslock®, будет ниже. И через несколько лет, может потребоваться повторное применение препарата.
Ссылка на источник:
http://www.waterworld.com/articles/2012/11/stormwater-management-in-canada-improved-with-new-phoslock-technology.html
www.awatereng.ru









