Содержание
реакция среды, формула и примеры
Что такое водородный показатель pH и зачем он нужен
Водные растворы веществ могут быть кислыми, нейтральными или щелочными. Кислотность среды зависит от концентрации положительно заряженных ионов водорода (H+) и отрицательно заряженных гидроксид-ионов (OH−) относительно друг друга.
Если в растворе [H+] > [OH−], то его называют кислотным,
если [OH−] > [H+] — щелочным,
если [H+] = [OH−] — нейтральным.
В нейтральном растворе концентрация Н+ и ОН− ничтожно мала, поскольку эти ионы активно взаимодействуют друг с другом с образованием малодиссоциирующего соединения Н2О. Поэтому в нейтральном растворе присутствуют только те ионы водорода и гидроксид-ионы, которые образовались в результате обратимой диссоциации:
Н2О ⇆ Н+ + ОН–.
Константа диссоциации имеет незначительную величину и равна:
.
Концентрация воды практически не изменяется в растворе, поэтому мы можем упростить выражение константы диссоциации воды:
Kw = [H+][OH−] = 10−14.
Получившееся выражение называют ионным произведением воды. Эта величина постоянна при заданной температуре (для T = 22–25 °С Kw = 10−14) для воды и ее растворов.
Концентрация ионов H+ и OH− при комнатной температуре всегда одинакова и равняется:
[H+] = [OH−] = 10−7 моль/л.
Для характеристики кислотности среды более удобно использовать водородный показатель pH (читается «пэ аш»), который равен десятичному логарифму величины [H+] с отрицательным знаком.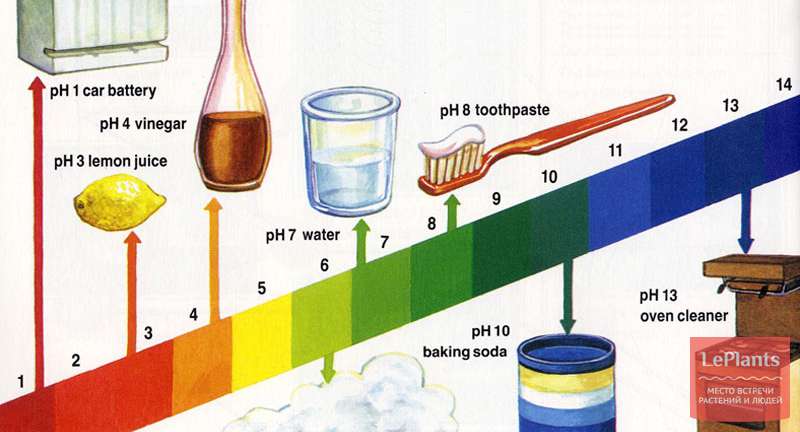 Формула расчета pH:
Формула расчета pH:
pH = −lg[H+].
Название величины указывает на то, что кислотность или щелочность среды можно выразить через концентрацию только ионов водорода.
Практикующий детский психолог Екатерина Мурашова
Бесплатный курс для современных мам и пап от Екатерины Мурашовой. Запишитесь и участвуйте в розыгрыше 8 уроков
Расчет водородного показателя для растворов разной кислотности
Попробуем посчитать pH для чистой воды и нейтральных водных растворов:
pH= −lg[H+] = −lg10−7 = −(−7) = 7.
Для нейтральных водных растворов и чистой воды pH = 7.
Рассчитаем значения водородного показателя для раствора сильной одноосновной кислоты (например, HCl) концентрации 1 моль/л. Концентрация ионов водорода Н+ равняется также 1 моль/л. Подставим значения в ионное произведение воды, которое сохранит свое значение 10−14 и в этом растворе:
Кw = [H+][ОН−] = [1 моль/л] × [ОН−] = 10−14.
В таком случае [Н+] = 100 (так как 100 = 1 моль/л).
Тогда рН = −lg100 = 0.
Для растворов сильных кислот pH = 0.
Рассчитаем значения водородного показателя для раствора сильного основания (например, KOH) концентрации 1 моль/л. Ионное произведение воды принимает вид:
Кw = [Н+][1 моль/л] = 10−14.
Кw = [Н+][100 моль/л] = 10−14.
Тогда .
Следовательно, рН = −lg10−14 = 14.
Для растворов сильных оснований pH = 14.
Таким образом, значения pH могут варьироваться в интервале от 0 до 14. Чем меньше рН, тем выше кислотность среды. И наоборот: чем больше рН, тем выше щелочность среды.
Сильнокислотные свойства раствора характерны для pH = 0–3, а сильнощелочные — для pH = 12–14.
Значения pH в зависимости от характера среды:
в нейтральных водных растворах pH = 7;
в кислотных — pH < 7;
в щелочных — pH > 7.
Водородный показатель в быту и производстве
В быту нейтральной средой принято считать диапазон pH = 5–8,5. Растворы такой кислотности (или щелочности) безопасны для кожи и слизистых человека. Ниже приведены pH некоторых веществ, которые мы встречаем в повседневной жизни:
Водородный показатель имеет важное значение во многих отраслях:
в косметологии многие продукты проходят проверку на оптимальное значение pH для безопасности кожи;
в сельском хозяйстве кислотность среды определяют для выращивания сельскохозяйственных культур;
в экологии изменение кислотности дождевых вод, рек, озер свидетельствует об ухудшении экологических условий и т.
 д.
д.
Запоминать теорию проще, если она подкреплена примерами из реальной жизни. Ученики онлайн-курсов по химии в Skysmart на каждом уроке узнают что-то новое об окружающем мире и учатся применять знания на практике.
Бесплатные занятия по английскому с носителем
Занимайтесь по 15 минут в день. Осваивайте английскую грамматику и лексику. Сделайте язык частью жизни.
Методы определения водородного показателя раствора
Характер среды (кислый, нейтральный или щелочной) определяют с помощью индикатора.
Индикаторы — вещества, которые изменяют окраску раствора при различных значениях pH.
Чтобы определить характер среды, в исследуемый раствор достаточно добавить несколько капель водно-спиртового раствора индикатора — и окраска последнего изменится.
На практике наиболее распространены несколько индикаторов: метилоранж, лакмус и фенолфталеин. Окраска этих индикаторов в кислой, нейтральной и щелочной среде представлена в таблице:
Окраска этих индикаторов в кислой, нейтральной и щелочной среде представлена в таблице:
Определение pH среды с помощью индикатора — быстрый и наглядный метод, но для определения более точного значения pH используют универсальный индикатор.
Универсальный индикатор представляет собой смесь высушенных веществ, нанесенных на бумагу. С его помощью можно определить характер среды в широком диапазоне pH — от 1 до 14.
Для измерения водородного показателя pH на бумажную полоску наносят исследуемый раствор, а затем сравнивают цвет индикатора с эталонной шкалой.
Помимо определения характера среды, с помощью индикатора можно отследить изменение концентрации компонента в растворе. Например, реакция нейтрализации (реакция между кислотой и щелочью) протекает без каких-либо признаков (выпадения осадка или выделения газа). Но если к раствору кислоты добавить индикатор лакмус, раствор окрасится в красный, а после добавления к нему щелочи — в фиолетовый. Изменение окраски индикатора подтвердит протекание реакции нейтрализации.
Изменение окраски индикатора подтвердит протекание реакции нейтрализации.
Использование специального прибора pH-метра позволяет измерять значения pH в более широком интервале и с большей точностью (до 0,01 единицы pH) по сравнению с индикаторами.
Работа pH-метра основана на измерении электродвижущей силы (ЭДС), которая создается электродами после погружения в раствор.
Вопросы для самопроверки
Какие значения pH характерны для кислой, нейтральной и щелочной среды?
В каких областях науки и производства необходимо измерять значения pH раствора вещества? Приведите несколько примеров.
Что такое индикатор? Как определить с его помощью характер среды?
В чем преимущества универсального индикатора?
Как называется прибор для более точного определения водородного показателя среды? Приведите его преимущества.

Анализ воды на водородный показатель (ph) — описание, цена
Артикул
ПСВ
В наличии
Популярность
Производитель:
- Аналитический центр качества воды
msk
filter
Водоочистка для дома
Специалисты отвечают
Ремонт умягчителя воды
Механизмы фильтрации воды
Получить консультацию
Заполните имя, телефон, почту и наши менеджеры свяжутся
с Вами в рабочее время для уточнения деталей заказа
Имя
Телефон
Пожалуйста, введите корректный номер
Комментарий
Заявка успешно отправлена
Заявка успешно отправлена
Отзыв про
Мы ценим Ваше время и звоним только по делу!
Как Вас зовут?
Ваш email
Телефон для связи
Пожалуйста, введите корректный номер
Отзыв
Уточните район / населенный пункт
Протестировать
Заполните имя, телефон, почту и наши менеджеры свяжутся
с Вами в рабочее время для уточнения деталей заказа
Имя
Телефон
Пожалуйста, введите корректный номер
Комментарий
Заявка успешно отправлена
Что нужно знать о рН воды
В самой чистой форме вода имеет рН 7, что находится точно в центре шкалы рН. Частицы в воде могут изменить pH воды, и большая часть используемой воды имеет pH где-то между 6,5 и 8,5.
Частицы в воде могут изменить pH воды, и большая часть используемой воды имеет pH где-то между 6,5 и 8,5.
Есть несколько важных вещей, которые нужно знать о шкале рН и о том, как она связана с водой. Например, возможно, что употребление щелочных напитков может принести некоторую пользу для здоровья.
Продолжайте читать, чтобы узнать больше о рН воды.
Поделиться на PinterestРН воды может варьироваться в зависимости от частиц в жидкости.
В химии pH — это измерение концентрации ионов водорода в растворе на водной основе. Более низкий pH означает, что в жидкости больше ионов водорода, тогда как более высокий pH указывает на меньшее количество ионов водорода в жидкости.
Простыми словами, pH — это шкала от 1 до 14, которая измеряет кислотность или щелочность жидкости. В середине шкалы находится чистая дистиллированная вода с нейтральным рН 7. Все, что имеет рН ниже 7, является кислотой, а все, что имеет рН выше 7, является щелочью или основанием.
Если использовать повседневные примеры, уксус очень кислый, с pH около 2. И наоборот, отбеливатель сильно щелочной, с pH около 13,5.
И наоборот, отбеливатель сильно щелочной, с pH около 13,5.
Важно отметить, что эта шкала применима только к жидкостям на водной основе.
pH играет важную роль в свойствах жидкости, содержащей воду.
Например, рН воды может сделать некоторые содержащиеся в ней элементы, такие как минералы и металлы, более или менее доступными для организма. Тяжелые металлы в воде с более низким pH, как правило, более токсичны, поскольку они более доступны для организма. Высокий рН сделал бы тяжелые металлы менее доступными и, следовательно, менее токсичными.
Значение pH также может быть признаком других загрязняющих веществ или бактериальной жизни в жидкости. Как правило, очень высокий или очень низкий pH может сделать воду непригодной для определенных целей.
Например, жесткой водой называют воду, содержащую много минералов. Эти минералы делают воду очень щелочной. Когда вода проходит через трубы и машины, использующие воду, такие как посудомоечные машины или душевые, эти минералы прилипают как к трубам, так и друг к другу, что приводит к накоплению минералов.
Накопление минералов может вызвать различные проблемы с водой в доме, например сделать моющие средства и мыло менее эффективными. Это также может привести к снижению давления воды или даже к ее засорению.
С другой стороны, вода с низким pH может вызывать коррозию металлических труб и извлечение ионов металлов в воду, что делает ее вредной для питья или использования в домашних условиях.
Большую часть времени вода, которую поставщики намереваются использовать или пить, будет ближе к нейтральной точке 7, хотя она все же может немного отличаться. Агентство по охране окружающей среды (EPA) рекомендует поддерживать pH питьевой воды на уровне от 6,5 до 8,5, и многие штаты США предпочитают обеспечивать соблюдение этих уровней.
Питьевая вода и другие напитки на водной основе с различными уровнями pH могут влиять на несколько различных факторов здоровья.
Щелочная вода и другие щелочные продукты приобрели популярность в последние годы, став новой тенденцией в области здравоохранения.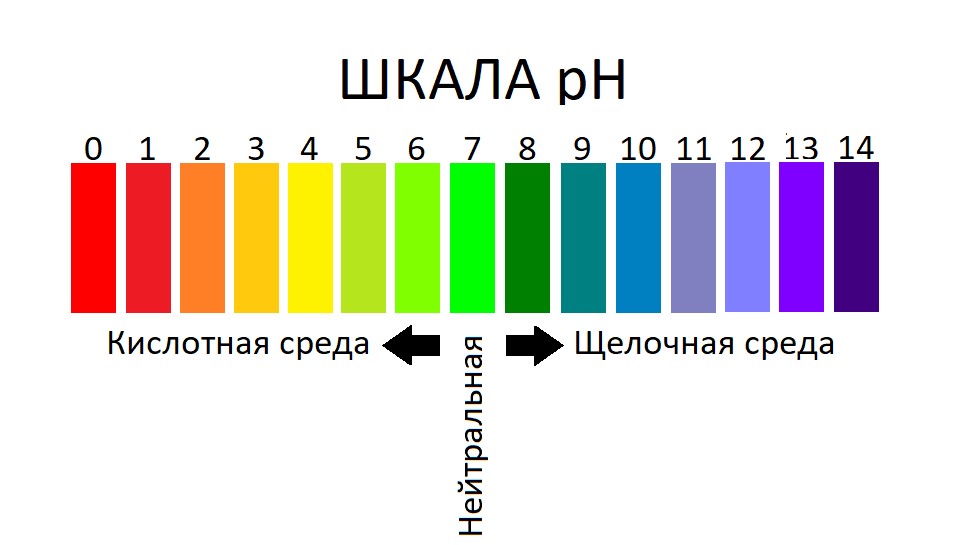 По мнению сторонников щелочных напитков, кислая среда в организме вызывает ряд хронических заболеваний, которые, по их утверждению, не могут сохраняться в щелочной среде.
По мнению сторонников щелочных напитков, кислая среда в организме вызывает ряд хронических заболеваний, которые, по их утверждению, не могут сохраняться в щелочной среде.
Идея, стоящая за этим, заключается в том, что употребление щелочной воды помогает самому организму стать более щелочным, что лечит ряд болезней, включая рак.
Тем не менее, существует мало доказательств, подтверждающих эти утверждения. Хотя употребление щелочной воды может временно повлиять на pH рта или мочи, нет научных доказательств того, что она изменит общий pH тела.
Организм строго регулирует уровень pH. Изменения внутреннего рН организма, например рН крови, могут означать серьезные проблемы в органах и тканях. Итак, если бы можно было изменить рН тела с помощью еды и питья, это было бы опасно.
Тем не менее, щелочная вода может быть полезна для некоторых людей. В общем, щелочная вода имеет тенденцию быть более щелочной, потому что в ней есть минералы и электролиты. В связи с этим употребление этой воды после тренировки или во время болезни может помочь сохранить баланс минералов и электролитов и предотвратить обезвоживание.
Кроме того, результаты небольшого исследования показывают, что людям с кислотным рефлюксом может быть полезно пить щелочную воду с pH 8,8. Исследователи обнаружили, что щелочная вода, по-видимому, навсегда инактивирует фермент, который играет роль в изжоге, что может уменьшить симптомы.
Исследователи также обнаружили, что питьевая вода с pH 8,5–10 может быть полезной для людей с синдромом раздраженного кишечника (СРК), основным симптомом которого является диарея. Люди, которые пили воду с pH 8,5–10, по самооценке через 8 недель имели более высокие показатели качества жизни, чем те, кто этого не делал.
Однако это небольшие исследования, и для подтверждения этих первоначальных результатов необходимы дополнительные исследования на людях.
Узнайте больше о потенциальной пользе щелочной воды для здоровья здесь.
Лаборатории обычно используют электронный рН-метр для точного измерения рН. Однако можно получить приблизительную оценку рН с помощью лакмусовой бумаги. Лакмусовая бумага широко доступна в Интернете и в некоторых магазинах, таких как магазины здоровой пищи и зоомагазины.
Лакмусовая бумага широко доступна в Интернете и в некоторых магазинах, таких как магазины здоровой пищи и зоомагазины.
Лакмусовая бумага представляет собой чувствительную полоску бумаги, которая меняет цвет при контакте с жидкостями на водной основе. Изменение цвета может дать приблизительную оценку рН жидкости. Тем не менее, человек должен иметь в виду, что это приблизительные оценки и что фактический pH жидкости может отличаться от того, что показывает лакмусовая бумажка.
pH жидкости будет меняться в зависимости от ингредиентов внутри. В результате возможны колебания даже в двух очень похожих продуктах, например, в двух типах воды.
Вот некоторые общие диапазоны pH для различных напитков:
pH воды для питья или использования в домашних условиях очень важен. Слишком щелочная или слишком кислая вода может повредить трубы и приборы, и пить ее, как правило, вредно для здоровья.
Вода в естественных условиях колеблется между 6,5 и 8,5 по шкале pH, и это нормально. Вода, которая находится слишком далеко за пределами этой шкалы, может быть небезопасной для питья.
Вода, которая находится слишком далеко за пределами этой шкалы, может быть небезопасной для питья.
Некоторым людям полезно пить щелочную воду с pH выше 8,5. К таким людям относятся люди с проблемами пищеварения, такими как СРК. Тем не менее, более масштабные и качественные исследования должны подтвердить эти утверждения, прежде чем эксперты смогут сделать какие-либо общие заявления о возможных преимуществах щелочной воды.
Что нужно знать о рН воды
В самой чистой форме вода имеет рН 7, что находится точно в центре шкалы рН. Частицы в воде могут изменить pH воды, и большая часть используемой воды имеет pH где-то между 6,5 и 8,5.
Есть несколько важных вещей, которые нужно знать о шкале рН и о том, как она связана с водой. Например, возможно, что употребление щелочных напитков может принести некоторую пользу для здоровья.
Продолжайте читать, чтобы узнать больше о рН воды.
Поделиться на PinterestРН воды может варьироваться в зависимости от частиц в жидкости.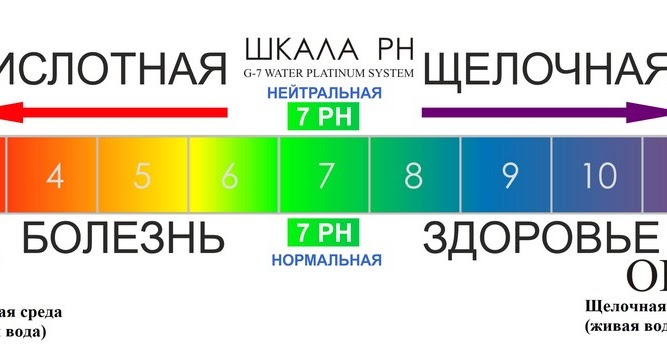
В химии pH — это измерение концентрации ионов водорода в растворе на водной основе. Более низкий pH означает, что в жидкости больше ионов водорода, тогда как более высокий pH указывает на меньшее количество ионов водорода в жидкости.
Говоря простыми словами, рН представляет собой шкалу от 1 до 14, которая измеряет кислотность или щелочность жидкости. В середине шкалы находится чистая дистиллированная вода с нейтральным рН 7. Все, что имеет рН ниже 7, является кислотой, а все, что имеет рН выше 7, является щелочью или основанием.
Если использовать повседневные примеры, уксус очень кислый, с pH около 2. И наоборот, отбеливатель сильно щелочной, с pH около 13,5.
Важно отметить, что эта шкала применима только к жидкостям на водной основе.
pH играет важную роль в свойствах жидкости, содержащей воду.
Например, рН воды может сделать некоторые содержащиеся в ней элементы, такие как минералы и металлы, более или менее доступными для организма. Тяжелые металлы в воде с более низким pH, как правило, более токсичны, поскольку они более доступны для организма. Высокий рН сделал бы тяжелые металлы менее доступными и, следовательно, менее токсичными.
Высокий рН сделал бы тяжелые металлы менее доступными и, следовательно, менее токсичными.
Значение pH также может быть признаком наличия в жидкости других загрязняющих веществ или бактерий. Как правило, очень высокий или очень низкий pH может сделать воду непригодной для определенных целей.
Например, жесткой водой называют воду, содержащую много минералов. Эти минералы делают воду очень щелочной. Когда вода проходит через трубы и машины, использующие воду, такие как посудомоечные машины или душевые, эти минералы прилипают как к трубам, так и друг к другу, что приводит к накоплению минералов.
Накопление минералов может вызвать различные проблемы с водой в доме, например сделать моющие средства и мыло менее эффективными. Это также может привести к снижению давления воды или даже к ее засорению.
С другой стороны, вода с низким pH может вызывать коррозию металлических труб и извлечение ионов металлов в воду, что делает ее вредной для питья или использования в домашних условиях.
Большую часть времени вода, которую поставщики намереваются использовать или пить, будет ближе к нейтральной точке 7, хотя она все же может немного отличаться. Агентство по охране окружающей среды (EPA) рекомендует поддерживать pH питьевой воды на уровне от 6,5 до 8,5, и многие штаты США предпочитают обеспечивать соблюдение этих уровней.
Питьевая вода и другие напитки на водной основе с различными уровнями pH могут влиять на несколько различных факторов здоровья.
Щелочная вода и другие щелочные продукты приобрели популярность в последние годы, став новой тенденцией в области здравоохранения. По мнению сторонников щелочных напитков, кислая среда в организме вызывает ряд хронических заболеваний, которые, по их утверждению, не могут сохраняться в щелочной среде.
Идея, стоящая за этим, заключается в том, что употребление щелочной воды помогает самому организму стать более щелочным, что лечит ряд болезней, включая рак.
Тем не менее, существует мало доказательств, подтверждающих эти утверждения.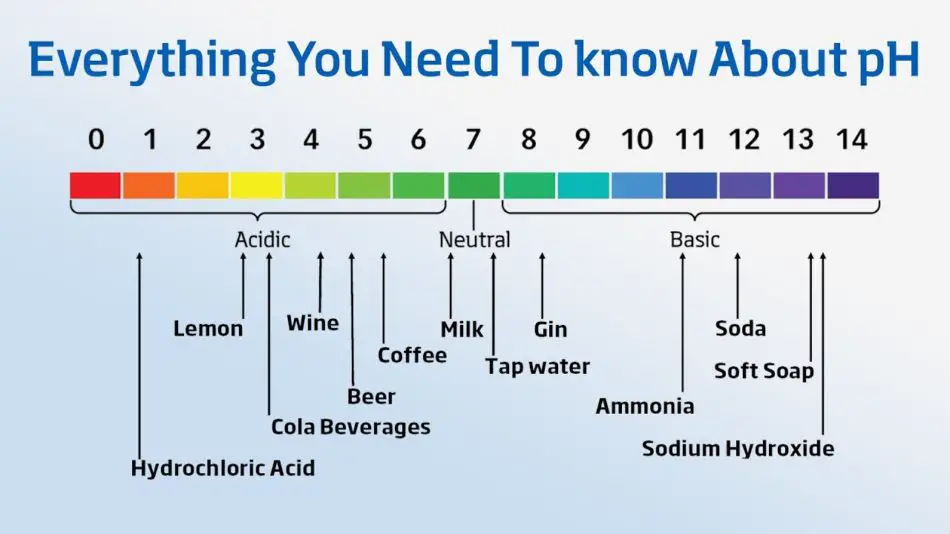 Хотя употребление щелочной воды может временно повлиять на pH рта или мочи, нет научных доказательств того, что она изменит общий pH тела.
Хотя употребление щелочной воды может временно повлиять на pH рта или мочи, нет научных доказательств того, что она изменит общий pH тела.
Организм строго регулирует уровень pH. Изменения внутреннего рН организма, например рН крови, могут означать серьезные проблемы в органах и тканях. Итак, если бы можно было изменить рН тела с помощью еды и питья, это было бы опасно.
Тем не менее, щелочная вода может быть полезна для некоторых людей. В общем, щелочная вода имеет тенденцию быть более щелочной, потому что в ней есть минералы и электролиты. В связи с этим употребление этой воды после тренировки или во время болезни может помочь сохранить баланс минералов и электролитов и предотвратить обезвоживание.
Кроме того, результаты небольшого исследования показывают, что людям с кислотным рефлюксом может быть полезно пить щелочную воду с pH 8,8. Исследователи обнаружили, что щелочная вода, по-видимому, навсегда инактивирует фермент, который играет роль в изжоге, что может уменьшить симптомы.
Исследователи также обнаружили, что питьевая вода с pH 8,5–10 может быть полезной для людей с синдромом раздраженного кишечника (СРК), основным симптомом которого является диарея. Люди, которые пили воду с pH 8,5–10, по самооценке через 8 недель имели более высокие показатели качества жизни, чем те, кто этого не делал.
Однако это небольшие исследования, и для подтверждения этих первоначальных результатов необходимы дополнительные исследования на людях.
Узнайте больше о потенциальной пользе щелочной воды для здоровья здесь.
Лаборатории обычно используют электронный рН-метр для точного измерения рН. Однако можно получить приблизительную оценку рН с помощью лакмусовой бумаги. Лакмусовая бумага широко доступна в Интернете и в некоторых магазинах, таких как магазины здоровой пищи и зоомагазины.
Лакмусовая бумага представляет собой чувствительную полоску бумаги, которая меняет цвет при контакте с жидкостями на водной основе. Изменение цвета может дать приблизительную оценку рН жидкости.

 д.
д.