Содержание
Почему вода необходима для жизни? EcoWater
Вода составляет 60-75% веса человеческого тела. Потеря всего 4% воды в организме приводит к обезвоживанию, а потеря 15% может быть смертельной. Поэтому, хотя человек может прожить месяц без еды, но без воды он обычно не может прожить больше 3 дней. Эта критическая зависимость от воды является ключевым регулятором всех форм жизни. Ясно, что вода необходима для выживания, но почему она так важна?
Вода с молекулярной точки зрения
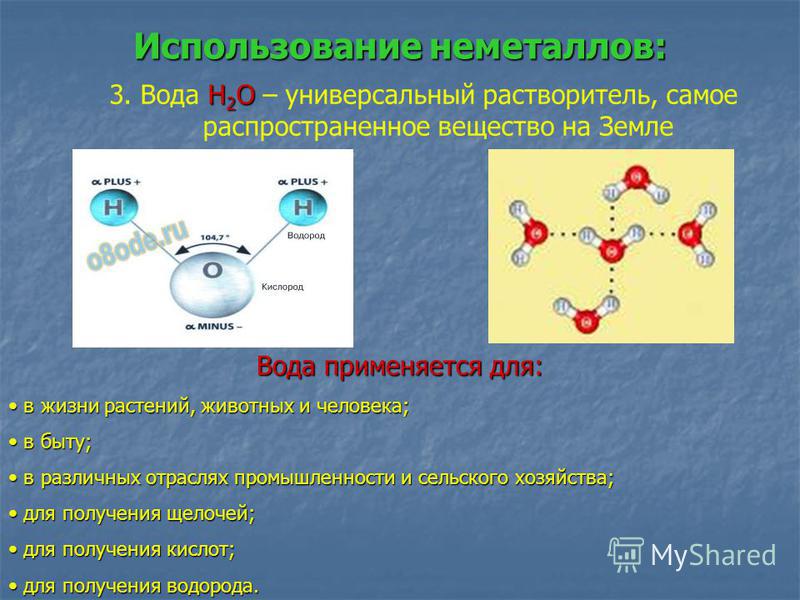
Многие функции воды в поддержании жизни обусловлены ее молекулярной структурой и несколькими особыми свойствами. Вода — это простая молекула, состоящая из двух небольших положительно заряженных атомов водорода и одного большого отрицательно заряженного атома кислорода. Когда атомы водорода связываются с кислородом, образуется асимметричная молекула с положительным зарядом на одной стороне и отрицательным — на другой (рис. 1). Эта разница в зарядах называется полярностью, и она определяет способ взаимодействия воды с другими молекулами.
Рисунок 1: Химический состав воды. Молекулы воды состоят из двух атомов водорода и одного кислорода. Эти атомы различаются по размеру и заряду, что приводит к асимметрии в молекулярной структуре и к прочным связям между водой и другими полярными молекулами, включая саму воду.
Вода — универсальный растворитель
Как полярная молекула вода лучше всего взаимодействует с другими полярными молекулами, такими как она сама. Это происходит из-за явления, при котором противоположные заряды притягиваются друг к другу: поскольку каждая отдельная молекула воды имеет как отрицательную, так и положительную части, каждая сторона притягивается к молекулам с противоположным зарядом. Притяжение позволяет воде образовывать относительно прочные связи с другими полярными молекулами вокруг нее, включая другие молекулы воды. Затем положительный атом водорода одной из молекул воды объединится с отрицательным атомом кислорода соседней молекулы, собственные атомы водорода которой притягиваются к следующему атому кислороду, и так далее (рис. 1). Важно отметить, что эта связь приводит к тому, что молекулы воды объединяться. Такое свойство воды известно как когезия. Когезия воды помогает растениям «вытягивать» воду из корней. Когезия также способствует высокой температуре кипения воды, что помогает животным регулировать температуру тела.
1). Важно отметить, что эта связь приводит к тому, что молекулы воды объединяться. Такое свойство воды известно как когезия. Когезия воды помогает растениям «вытягивать» воду из корней. Когезия также способствует высокой температуре кипения воды, что помогает животным регулировать температуру тела.
Кроме того, поскольку большинство биологических молекул имеют некоторую асимметрию напряжения, они также полярны, и молекулы воды могут образовывать связи и окружать как их положительные, так и отрицательные части. Окружая полярные молекулы другого вещества, вода попадает в каждый уголок и щель между молекулами, эффективно разрушая и растворяя их. Вот что происходит, когда мы добавляем кристаллы сахара в воду: и вода, и сахар полярны, так что отдельные молекулы воды окружают каждую молекулу сахара, расщепляя сахар и растворяя его. Как и в случае с поляризацией, некоторые молекулы состоят из ионов или противоположно заряженных частиц. Вода также разрушает эти ионные частицы, взаимодействуя как с положительно, так и с отрицательно заряженными частями. Вот что происходит, когда мы добавляем соль в воду, потому что соль состоит из ионов натрия и хлора.
Вот что происходит, когда мы добавляем соль в воду, потому что соль состоит из ионов натрия и хлора.
Благодаря сильной способности воды растворять различные молекулы, она стала известна как «универсальный растворитель», и именно эта способность делает воду такой бесценной силой поддержания жизни. На биологическом уровне вода как растворитель помогает клеткам переносить и использовать кислород и питательные вещества. Растворы на водной основе, такие как кровь, помогают перемещать вещества в нужные места. Таким образом, роль воды как растворителя облегчает транспортировку веществ, таких как кислород, для дыхания, и имеет большое влияние на способность лекарств достигать своих целей в организме.
Вода поддерживает клеточную структуру
Вода также играет важную структурную роль в биологии. Вода заполняет клетки, помогая сохранять их форму и структуру (рис. 2). Вода во многих клетках (включая те, что составляют человеческое тело) создает давление, противодействующее внешним силам, как воздух в воздушном шаре. Даже некоторым растениям, способным поддерживать свою клеточную структуру какое-то время без воды, для выживания все равно потом нужна вода. Вода способствует тому, что все внутри клеток сохраняет свою правильную форму на молекулярном уровне. Поскольку форма имеет решающее значение для биохимических процессов, это тоже является одной из самых важных ролей воды.
Даже некоторым растениям, способным поддерживать свою клеточную структуру какое-то время без воды, для выживания все равно потом нужна вода. Вода способствует тому, что все внутри клеток сохраняет свою правильную форму на молекулярном уровне. Поскольку форма имеет решающее значение для биохимических процессов, это тоже является одной из самых важных ролей воды.
Рисунок 2: Вода влияет на форму клетки. Вода создает в клетке давление, которое помогает ей сохранять форму. В гидратированной клетке (слева) вода выталкивается наружу, и ячейка остается круглой. В обезвоженной клетке вытесняется меньше воды, поэтому клетка становится морщинистой.
Помимо влияния на общую форму клеток, вода также влияет на некоторые основные компоненты каждой клетки: ДНК и белки. Белки производятся в виде длинной цепочки строительных блоков, называемых аминокислотами, и для правильного функционирования они должны иметь определенную форму. Вода направляет сборку аминокислотных цепей, поскольку разные типы аминокислот ищут и избегают взаимодействия с водой. Белки обеспечивают структуру, улавливают сигналы и катализируют химические реакции в клетке. В конечном итоге белки управляют сокращением мышц, коммуникацией, перевариванием питательных веществ и многими другими жизненно важными функциями. Без правильной формы белки не смогли бы выполнять эти функции, и клетка (не говоря уже обо всем теле человека) не смогла бы выжить. Точно так же ДНК должна иметь определенную форму, чтобы ее инструкции были правильно расшифрованы. Белки, которые читают или копируют ДНК, могут связываться с ДНК только определенной формы.
Белки обеспечивают структуру, улавливают сигналы и катализируют химические реакции в клетке. В конечном итоге белки управляют сокращением мышц, коммуникацией, перевариванием питательных веществ и многими другими жизненно важными функциями. Без правильной формы белки не смогли бы выполнять эти функции, и клетка (не говоря уже обо всем теле человека) не смогла бы выжить. Точно так же ДНК должна иметь определенную форму, чтобы ее инструкции были правильно расшифрованы. Белки, которые читают или копируют ДНК, могут связываться с ДНК только определенной формы.
Химические реакции воды
Вода принимает непосредственное участие во многих химических реакциях, предназначенных для создания и разрушения важных компонентов клетки. Фотосинтез, процесс, который происходит в растениях, который производит сахар для всех форм жизни, требует воды. Вода также участвует в создании более крупных молекул в клетках. Молекулы, такие как ДНК и белки, состоят из повторяющихся единиц более мелких молекул. Соединение этих маленьких молекул происходит в результате реакции с образованием воды. И наоборот, вода необходима для того, чтобы обратить вспять реакцию, которая разрушает эти молекулы, позволяя клеткам получать питательные вещества или повторно использовать части больших молекул.
Соединение этих маленьких молекул происходит в результате реакции с образованием воды. И наоборот, вода необходима для того, чтобы обратить вспять реакцию, которая разрушает эти молекулы, позволяя клеткам получать питательные вещества или повторно использовать части больших молекул.
Кроме того вода защищает клетки от вредного воздействия кислот и щелочей. Сильно кислые или щелочные вещества, такие как отбеливатель или соляная кислота, являются едкими даже для самых прочных материалов. Это связано с тем, что кислоты и основания выделяют избыток водорода или забирают избыток водорода из окружающих материалов. Потеря или приобретение положительно заряженного водорода нарушает структуру молекул. Для правильного функционирования протеинам требуется определенная структура, поэтому важно защищать их от кислот и щелочей. Вода делает это, действуя как кислота и основание (рис. 3). Хотя химические связи в молекуле воды очень стабильны, молекула воды может отдать водород и стать ОН-, таким образом действуя как основание, или принять другой водород и превратиться в h4O +, таким образом действуя как кислота. Эта адаптивная способность позволяет воде противодействовать резким изменениям pH, вызванным кислотными или щелочными веществами в организме, в процессе, называемом буферизацией. В конечном итоге это защищает белки и другие молекулы в клетке.
Эта адаптивная способность позволяет воде противодействовать резким изменениям pH, вызванным кислотными или щелочными веществами в организме, в процессе, называемом буферизацией. В конечном итоге это защищает белки и другие молекулы в клетке.
Рисунок 3: Вода действует как буфер, высвобождая или поглощая атомы водорода.
Вода необходима для любой жизни. Её универсальность и адаптируемость помогает проводить важные химические реакции. Никакая другая молекула не может сравниться с водой, с ее уникальными жизнеобеспечивающими свойствами. Интересно, что исследователи все еще выявляют новые свойства воды, такие как дополнительные преимущества ее асимметричной структуры. Ученым еще предстоит определить физиологические эффекты этих свойств. Удивительно, насколько простая молекула универсально важна для организмов с разными потребностями.
Оригинальная статья: https://sitn.hms.harvard.edu/uncategorized/2019/biological-roles-of-water-why-is-water-necessary-for-life/
Назад ко всем новостям
Вода – универсальный растворитель — МК Челябинск
Свежий МК
1317
Поделиться
Воздух и вода – два основополагающих фактора, влияющих на продолжительность жизни и наличие многих заболеваний.
Большинство из нас относится к воде наплевательски, пьет что попало, совершенно не думая, что наносит своему организму непоправимый вред.
О влиянии воды на здоровье человека мы спросили у педиатра-гастроэнтеролога, заведующего гастроэнтерологическим отделением Областной детской клинической больницы Вадима ЗЕМЛЯКОВА.
— Вода — основной элемент состава человеческого организма. В организме человека вода выполняет множество функций: помогает усваивать питательные вещества, преобразовывает пищу в энергию, способствует регулированию температуры тела, смазывает суставы, выводит шлаки из организма, – рассказал Вадим Леонидович. — Научные исследования крови подтвердили, что причина многих болезней — в обезвоживании организма, которое ведет к закислению крови. Употребление воды можно сравнить с влажной уборкой организма, очищением его от токсинов и шлаков. В течение суток человек теряет до двух литров воды, значит, ему нужно выпить столько же. Для того чтобы организм и его органы были здоровыми, пейте 1,5- 2 литра воды ежедневно.
Вода — универсальный растворитель, в ней растворяются все соли и микроэлементы, все лишние вещества, поступающие к нам с пищей и напитками. При сокращении количества потребления воды в организме происходит концентрация всех этих веществ. Это приводит к образованию солевых отложений в почках, к запорам. Ну а последствия запоров все мы знаем — это интоксикация и еще пучок заболеваний.
Ну а последствия запоров все мы знаем — это интоксикация и еще пучок заболеваний.
Одна из современных нехороших тенденций – дети предпочитают чистой воде соки, а взрослые литрами пьют минералку, считая, что это замена обычной питьевой воде. Это заблуждение. Заметьте, ни чай, ни соки, ни минералка к воде не имеют никакого отношения. Снижая за счет этих напитков потребление обычной воды, мы обезвоживаем слизистую оболочку наших внутренних органов. Отсюда и чувство жажды, заболевания кожи, дерматиты, ощущение сухости во рту, боль в глазных яблоках.
Желательно употреблять бутилированную очищенную воду или природную. Но не пейте воду из колодца, если она не прошла анализ. Не стоит рисковать. В подземных водах, как правило, повышенное содержание кальция, что приводит к камнеобразованию в почках, поджелудочной железе или селезенке. Люди об этом и не подозревают.
Особое внимание обратите на качество питьевой воды сейчас, когда во время таяния снега водопроводная вода подвергается усиленному хлорированию.
СПРАВКА «МК
Все живые организмы более чем наполовину состоят из воды. Например, рыбы и животные – на 75%, медузы – на 99%, яблоки – на 85%, огурцы – на 95%, а вот организм пожилого человека на 50% состоит из воды, а организм новорожденного – на 86%.
По данным Всемирной организации здравоохранения, около 85% заболеваний передается водой. В жизни человека вода является незаменимым природным богатством, гораздо больше, чем нефть, газ, уголь, железо.
Подписаться
Авторы:
Екатерина ВОРОНИНА
21 окт
Креативные индустрии Сибири могут получить новый импульс развития благодаря культурным событиям
20 окт
Решить кадровую проблему поможет цифровизация
17 окт
Новые медиа: кто и как формирует современное инфополе
Что еще почитать
«Мелкий бес» из Камерного театра вошел в лонг-лист «Золотой маски»
54
Челябинск
Кукольники из Челябинска покорили Дальний Восток
57
Челябинск
Стремоусов: российские войска могут покинуть правый берег Херсона
328447
Артем Кошеленко
Беспилотник ВСУ атаковал гранатами окопы российских военных в Белгородской области
37696
Артем Кошеленко
В смертельной болезни Бориса Моисеева обнаружили украинский след
Фото
16661
Денис Сорокин
Что почитать:Ещё материалы
В регионах
Зерновая сделка приостанавливается из-за теракта в Севастополе
42165
Крым
Фото: Pixabay.
 com
com«У девочки началась истерика»: что творилось в момент обстрела автобуса в Пскове
Фото
22690
Псков
Светлана Пикалёва
В Ярославле элитный комплекс остался без воды и отопления
13479
Ярославль
Минобоpоны РФ: Севастополь атаковали 9 летательных и 7 морских дронов
12976
Крым
фото: crimea.
 mk.ru
mk.ruГлава Ярославской области рассказал ярославцам, что делать с полученными повестками
7999
Ярославль
В работе Свердловского областного суда усматривается волокита и «творческое» толкование законов
4282
Екатеринбург
Максим Бойков
В регионах:Ещё материалы
Вода, универсальный растворитель | Геологическая служба США
Школа водных наук
9 июня 2018 г.
Свойства воды Фотогалерея
Узнайте о свойствах воды с помощью изображений
Дом школы водных наук
Обзор
Мы должны принять заявление «Вода является универсальным растворителем» с недоверием (каламбур). Конечно, она не может растворить все, но она растворяет больше веществ, чем любая другая жидкость, так что этот термин вполне подходит. Растворяющие свойства воды влияют на всю жизнь на Земле, поэтому вода важна для всех нас.
• Школа наук о воде ДОМАШНЯЯ СТРАНИЦА • Темы о свойствах воды •
Источники/Использование: Некоторое содержимое может иметь ограничения. Посетите СМИ, чтобы узнать подробности.
Знаете ли вы, что можно растворить M из M&M? Все, что вам нужно сделать, это положить несколько M&Ms в воду стороной M вверх и наблюдать, что происходит!
Фото: coffeecupsandcrayons. com
com
Воду называют «универсальным растворителем», потому что она способна растворять больше веществ, чем любая другая жидкость. Это важно для всего живого на земле. Это означает, что куда бы ни попадала вода, будь то по воздуху, земле или через наши тела, она уносит с собой ценные химические вещества, минералы и питательные вещества.
Химический состав и физические свойства воды делают ее таким превосходным растворителем. Молекулы воды имеют полярное расположение атомов кислорода и водорода — одна сторона (водород) имеет положительный электрический заряд, а другая сторона (кислород) — отрицательный. Это позволяет молекуле воды притягиваться ко многим другим типам молекул . Вода может настолько сильно притягиваться к другому соединению, например к соли (NaCl), что может нарушить силы притяжения, удерживающие вместе натрий и хлорид в солевом соединении, и, таким образом, растворить его.
Наши почки и вода — отличная пара
Наши почки и растворяющие свойства воды — отличная пара, поддерживающая нашу жизнь и здоровье. Почки отвечают за фильтрацию веществ, которые попадают в наш организм из продуктов и напитков, которые мы потребляем. Но почки должны избавляться от этих веществ после их накопления. Вот где вода помогает; Будучи таким прекрасным растворителем, вода, промывая почки, растворяет эти вещества и выводит их из нашего тела.
Почки отвечают за фильтрацию веществ, которые попадают в наш организм из продуктов и напитков, которые мы потребляем. Но почки должны избавляться от этих веществ после их накопления. Вот где вода помогает; Будучи таким прекрасным растворителем, вода, промывая почки, растворяет эти вещества и выводит их из нашего тела.
Источники/Использование: Некоторое содержимое может иметь ограничения. Посетите СМИ, чтобы узнать подробности.
На этой диаграмме показаны положительные и отрицательные части молекулы воды. На нем также показано, как заряд, например, иона (например, Na или Cl) может взаимодействовать с молекулой воды.
Авторы и права: Мариана Руис Вильярреал, Фонд CK-12
Почему соль растворяется в воде
На молекулярном уровне соль растворяется в воде благодаря электрическим зарядам и тому факту, что и вода, и солевые соединения полярны, причем положительные и отрицательные заряды на противоположных сторонах молекулы. Связи в соединениях солей называются ионными, потому что обе они имеют электрический заряд: ион хлорида заряжен отрицательно, а ион натрия — положительно. Точно так же молекула воды имеет ионную природу, но связь называется ковалентной, при этом два атома водорода располагаются со своим положительным зарядом по одну сторону от атома кислорода, который имеет отрицательный заряд. Когда соль смешивается с водой, соль растворяется, потому что ковалентные связи воды сильнее, чем ионные связи в молекулах соли.
Связи в соединениях солей называются ионными, потому что обе они имеют электрический заряд: ион хлорида заряжен отрицательно, а ион натрия — положительно. Точно так же молекула воды имеет ионную природу, но связь называется ковалентной, при этом два атома водорода располагаются со своим положительным зарядом по одну сторону от атома кислорода, который имеет отрицательный заряд. Когда соль смешивается с водой, соль растворяется, потому что ковалентные связи воды сильнее, чем ионные связи в молекулах соли.
Положительно заряженная сторона молекул воды притягивается к отрицательно заряженным ионам хлора, а отрицательно заряженная сторона молекул воды притягивается к положительно заряженным ионам натрия. По сути, происходит перетягивание каната, когда молекулы воды побеждают в матче. Молекулы воды раздвигают ионы натрия и хлорида, разрывая ионную связь, удерживающую их вместе. После того, как солевые соединения разделены, атомы натрия и хлорида окружены молекулами воды, как показано на этой диаграмме. Как только это произойдет, соль растворится, в результате чего получится однородный раствор.
Как только это произойдет, соль растворится, в результате чего получится однородный раствор.
- Обзор
Мы должны принять заявление «Вода является универсальным растворителем» с долей скептицизма (каламбур). Конечно, она не может растворить все, но она растворяет больше веществ, чем любая другая жидкость, так что этот термин вполне подходит. Растворяющие свойства воды влияют на всю жизнь на Земле, поэтому вода важна для всех нас.
• Школа наук о воде ДОМАШНЯЯ СТРАНИЦА • Темы о свойствах воды •
Источники/Использование: Некоторое содержимое может иметь ограничения. Посетите СМИ, чтобы узнать подробности.
Знаете ли вы, что можно растворить M из M&M? Все, что вам нужно сделать, это положить несколько M&Ms в воду стороной M вверх и наблюдать, что происходит!
Фото: coffeecupsandcrayons.comВоду называют «универсальным растворителем», потому что она способна растворять больше веществ, чем любая другая жидкость.
 Это важно для всего живого на земле. Это означает, что куда бы ни попадала вода, будь то по воздуху, земле или через наши тела, она уносит с собой ценные химические вещества, минералы и питательные вещества.
Это важно для всего живого на земле. Это означает, что куда бы ни попадала вода, будь то по воздуху, земле или через наши тела, она уносит с собой ценные химические вещества, минералы и питательные вещества.Химический состав и физические свойства воды делают ее таким превосходным растворителем. Молекулы воды имеют полярное расположение атомов кислорода и водорода — одна сторона (водород) имеет положительный электрический заряд, а другая сторона (кислород) — отрицательный. Это позволяет молекуле воды притягиваться ко многим другим типам молекул . Вода может настолько сильно притягиваться к другому соединению, например к соли (NaCl), что может нарушить силы притяжения, удерживающие вместе натрий и хлорид в солевом соединении, и, таким образом, растворить его.
Наши почки и вода — отличная пара
Наши почки и растворяющие свойства воды — отличная пара, поддерживающая нашу жизнь и здоровье. Почки отвечают за фильтрацию веществ, которые попадают в наш организм из продуктов и напитков, которые мы потребляем.
 Но почки должны избавляться от этих веществ после их накопления. Вот где вода помогает; Будучи таким прекрасным растворителем, вода, промывая почки, растворяет эти вещества и выводит их из нашего тела.
Но почки должны избавляться от этих веществ после их накопления. Вот где вода помогает; Будучи таким прекрасным растворителем, вода, промывая почки, растворяет эти вещества и выводит их из нашего тела.Источники/Использование: Некоторое содержимое может иметь ограничения. Посетите СМИ, чтобы узнать подробности.
На этой диаграмме показаны положительные и отрицательные части молекулы воды. На нем также показано, как заряд, например, иона (например, Na или Cl) может взаимодействовать с молекулой воды.
Авторы и права: Мариана Руис Вильярреал, Фонд CK-12
Почему соль растворяется в воде
На молекулярном уровне соль растворяется в воде благодаря электрическим зарядам и тому факту, что и вода, и солевые соединения полярны, причем положительные и отрицательные заряды на противоположных сторонах молекулы. Связи в соединениях солей называются ионными, потому что обе они имеют электрический заряд: ион хлорида заряжен отрицательно, а ион натрия — положительно.
 Точно так же молекула воды имеет ионную природу, но связь называется ковалентной, при этом два атома водорода располагаются со своим положительным зарядом по одну сторону от атома кислорода, который имеет отрицательный заряд. Когда соль смешивается с водой, соль растворяется, потому что ковалентные связи воды сильнее, чем ионные связи в молекулах соли.
Точно так же молекула воды имеет ионную природу, но связь называется ковалентной, при этом два атома водорода располагаются со своим положительным зарядом по одну сторону от атома кислорода, который имеет отрицательный заряд. Когда соль смешивается с водой, соль растворяется, потому что ковалентные связи воды сильнее, чем ионные связи в молекулах соли.Положительно заряженная сторона молекул воды притягивается к отрицательно заряженным ионам хлора, а отрицательно заряженная сторона молекул воды притягивается к положительно заряженным ионам натрия. По сути, происходит перетягивание каната, когда молекулы воды побеждают в матче. Молекулы воды раздвигают ионы натрия и хлорида, разрывая ионную связь, удерживающую их вместе. После того, как солевые соединения разделены, атомы натрия и хлорида окружены молекулами воды, как показано на этой диаграмме. Как только это произойдет, соль растворится, в результате чего получится однородный раствор.
Вода Вопросы и ответы: Почему вода является «универсальным растворителем»?
Школа водных наук
20 июня 2019 г.
Вопросы и ответы по науке о воде
Дополнительные вопросы и ответы по науке о воде см. здесь
Фотогалереи наук о воде
Узнайте все о воде с помощью картинок
Дом школы водных наук
Обзор
Узнайте, почему химический состав и физические свойства воды делают ее таким превосходным растворителем.
• Школа наук о воде HOME • Вопросы и ответы по наукам о воде •
Почему вода является «универсальным растворителем»?
Источники/использование: общественное достояние.
Вода способна растворять множество различных веществ, поэтому она является таким хорошим растворителем. А воду называют «универсальным растворителем», потому что она растворяет больше веществ, чем любая другая жидкость. Это важно для всего живого на земле. Это означает, что куда бы вода ни шла, через землю или через наши тела, она берет с собой ценные химические вещества, минералы и питательные вещества.
Химический состав и физические свойства воды делают ее таким превосходным растворителем. Молекулы воды имеют полярное расположение атомов кислорода и водорода — одна сторона (водород) имеет положительный электрический заряд, а другая сторона (кислород) — отрицательный. Это позволяет молекуле воды притягиваться ко многим другим типам молекул. Вода может так сильно притягиваться к другой молекуле, например к соли (NaCl), что она может разрушить силы притяжения, удерживающие вместе натрий и хлорид в молекуле соли, и, таким образом, растворить ее.
- Обзор
Узнайте, почему химический состав и физические свойства воды делают ее таким превосходным растворителем.
• Школа наук о воде HOME • Вопросы и ответы по наукам о воде •
Почему вода является «универсальным растворителем»?
Источники/использование: общественное достояние.
Вода способна растворять множество различных веществ, поэтому она является таким хорошим растворителем.


 com
com mk.ru
mk.ru Это важно для всего живого на земле. Это означает, что куда бы ни попадала вода, будь то по воздуху, земле или через наши тела, она уносит с собой ценные химические вещества, минералы и питательные вещества.
Это важно для всего живого на земле. Это означает, что куда бы ни попадала вода, будь то по воздуху, земле или через наши тела, она уносит с собой ценные химические вещества, минералы и питательные вещества. Но почки должны избавляться от этих веществ после их накопления. Вот где вода помогает; Будучи таким прекрасным растворителем, вода, промывая почки, растворяет эти вещества и выводит их из нашего тела.
Но почки должны избавляться от этих веществ после их накопления. Вот где вода помогает; Будучи таким прекрасным растворителем, вода, промывая почки, растворяет эти вещества и выводит их из нашего тела. Точно так же молекула воды имеет ионную природу, но связь называется ковалентной, при этом два атома водорода располагаются со своим положительным зарядом по одну сторону от атома кислорода, который имеет отрицательный заряд. Когда соль смешивается с водой, соль растворяется, потому что ковалентные связи воды сильнее, чем ионные связи в молекулах соли.
Точно так же молекула воды имеет ионную природу, но связь называется ковалентной, при этом два атома водорода располагаются со своим положительным зарядом по одну сторону от атома кислорода, который имеет отрицательный заряд. Когда соль смешивается с водой, соль растворяется, потому что ковалентные связи воды сильнее, чем ионные связи в молекулах соли.