Валентность. Определение валентности. Валентность воды
Урок 6. Валентность – HIMI4KA
В уроке 6 «Валентность» из курса «Химия для чайников» дадим определение валентности, научимся ее определять; рассмотрим элементы с постоянной и переменной валентностью, кроме того научимся составлять химические формулы по валентности. Напоминаю, что в прошлом уроке «Химическая формула» мы дали определение химическим формулам и их индексам, а также выяснили различия химических формул веществ молекулярного и немолекулярного строения.

Вы уже знаете, что в химических соединениях атомы разных элементов находятся в определенных числовых соотношениях. От чего зависят эти соотношения?
Рассмотрим химические формулы нескольких соединений водорода с атомами других элементов:

Нетрудно заметить, что атом хлора связан с одним атомом водорода, атом кислорода — с двумя, атом азота — с тремя, а атом углерода — с четырьмя атомами водорода. В то же время в молекуле углекислого газа СО2 атом углерода связан с двумя атомами кислорода. Из этих примеров видно, что атомы обладают разной способностью соединяться с другими атомами. Такая способность атомов выражается с помощью численной характеристики, называемой валентностью.
Валентность — численная характеристика способности атомов данного элемента соединяться с другими атомами.
Поскольку один атом водорода может соединиться только с одним атомом другого элемента, валентность атома водорода принята равной единице. Иначе говорят, что атом водорода обладает одной единицей валентности, т. е. он одновалентен.
Валентность атома какого-либо другого элемента равна числу соединившихся с ним атомов водорода. Поэтому в молекуле HCl у атома хлора валентность равна единице, а в молекуле h3O у атома кислорода валентность равна двум. По той же причине в молекуле Nh4 валентность атома азота равна трем, а в молекуле Ch5 валентность атома углерода равна четырем. Если условно обозначить единицу валентности черточкой |, вышесказанное можно изобразить схематически:
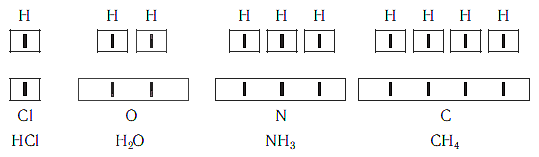
Следовательно, валентность атома любого элемента есть число, которое показывает, со сколькими атомами одновалентного элемента связан данный атом в химическом соединении.
Численные значения валентности обозначают римскими цифрами над символами химических элементов:

Определение валентности
Однако водород образует соединения далеко не со всеми элементами, а вот кислородные соединения есть почти у всех элементов. И во всех таких соединениях атомы кислорода проявляют валентность, равную двум. Зная это, можно определять валентности атомов других элементов в их бинарных соединениях с кислородом. (Бинарными называются соединения, состоящие из атомов двух химических элементов.)
Чтобы это сделать, необходимо соблюдать простое правило: в химической формуле вещества суммарные числа единиц валентности атомов каждого элемента должны быть одинаковыми.
Так, в молекуле воды h3O общее число единиц валентности двух атомов водорода равно произведению валентности одного атома на соответствующий числовой индекс в формуле:
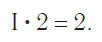
Так же определяют число единиц валентности атома кислорода:
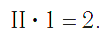
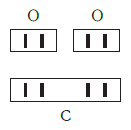
По величине валентности атомов одного элемента можно определить валентность атомов другого элемента. Например, определим валентность атома углерода в молекуле углекислого газа СО2:
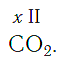
Согласно вышеприведенному правилу х·1 = II·2, откуда х = IV.
Существует и другое соединение углерода с кислородом — угарный газ СО, в молекуле которого атом углерода соединен только с одним атомом кислорода:
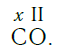
В этом веществе валентность углерода равна II, так как х·1 = II·1, откуда х = II:
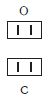
Постоянная и переменная валентность
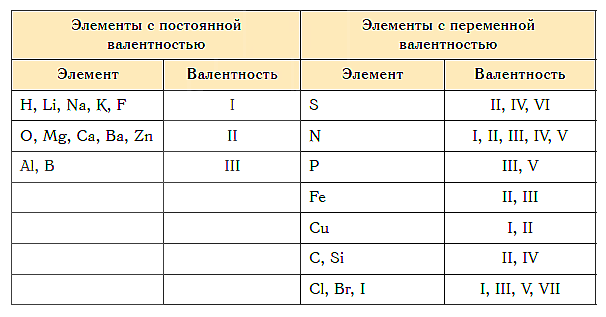
Как видим, углерод соединяется с разным числом атомов кислорода, т. е. имеет переменную валентность. У большинства элементов валентность — величина переменная. Только у водорода, кислорода и еще нескольких элементов она постоянна (см. таблицу).
Составление химических формул по валентности
Зная валентность элементов, можно составлять формулы их бинарных соединений. Например, необходимо записать формулу кислородного соединения хлора, в котором валентность хлора равна семи. Порядок действий здесь таков.

Еще один пример. Составим формулу соединения кремния с азотом, если валентность кремния равна IV, а азота — III.
Записываем рядом символы элементов в следующем виде:
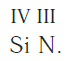
Затем находим НОК валентностей обоих элементов. Оно равно 12 (IV·III).
Определяем индексы каждого элемента:
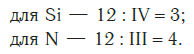
Записываем формулу соединения: Si3N4.
В дальнейшем при составлении формул веществ не обязательно указывать цифрами значения валентностей, а необходимые несложные вычисления можно выполнять в уме.
Краткие выводы урока:
- Численной характеристикой способности атомов данного элемента соединяться с другими атомами является валентность.
- Валентность водорода постоянна и равна единице. Валентность кислорода также постоянна и равна двум.
- Валентность большинства остальных элементов не является постоянной. Ее можно определить по формулам их бинарных соединений с водородом или кислородом.
Надеюсь урок 6 «Валентность» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Урок 6. Валентность
4.9 (98.57%) 14 voteshimi4ka.ru
Урок №12. Валентность химических элементов.
Валентность – это способность атомов присоединять к себе определенное число других атомов.
С одним атомом одновалентного элемента соединяется один атом другого одновалентного элемента (HСl). С атомом двухвалентного элемента соединяются два атома одновалентного (h3O) или один атом двухвалентного (CaO). Значит, валентность элемента можно представить как число, которое показывает, со сколькими атомами одновалентного элемента может соединяться атом данного элемента. Валентность элемента – это число связей, которое образует атом:

Na – одновалентен (одна связь)
H – одновалентен (одна связь)
O – двухвалентен (две связи у каждого атома)
S – шестивалентна (образует шесть связей с соседними атомами)
Правила определения валентностиэлементов в соединениях
1. Валентность водорода принимают за I (единицу). Тогда в соответствии с формулой воды Н2О к одному атому кислорода присоединено два атома водорода.
2. Кислород в своих соединениях всегда проявляет валентность II. Поэтому углерод в соединении СО2 (углекислый газ) имеет валентность IV.
3. Высшая валентность равна номеру группы.
4. Низшая валентность равна разности между числом 8 (количество групп в таблице) и номером группы, в которой находится данный элемент, т.е. 8 - N группы.
5. У металлов, находящихся в «А» подгруппах, валентность равна номеру группы.
6. У неметаллов в основном проявляются две валентности: высшая и низшая.
Например: сера имеет высшую валентность VI и низшую (8 – 6), равную II; фосфор проявляет валентности V и III.
7. Валентность может быть постоянной или переменной.

Валентность элементов необходимо знать, чтобы составлять химические формулы соединений.

Алгоритм составления формулы соединения оксида фосфора
| Последовательность действий | Составление формулы оксида фосфора |
| 1. Написать символы элементов | Р О |
| 2. Определить валентности элементов | V IIP O |
| 3. Найти наименьшее общее кратное численных значений валентностей | 5•2 = 10 |
| 4. Найти соотношения между атомами элементов путем деления найденного наименьшего кратного на соответствующие валентности элементов | 10 : 5 = 2, 10 : 2 = 5; P : О = 2 : 5 |
| 5. Записать индексы при символах элементов | Р2 О5 |
| 6. Формула соединения (оксида) | Р2О5 |
Особенности составления химических формул соединений.
1) Низшую валентность проявляет тот элемент, который находится в таблице Д.И.Менделеева правее и выше, а высшую валентность – элемент, расположенный левее и ниже.
Например, в соединении с кислородом сера проявляет высшую валентность VI, а кислород – низшую II. Таким образом, формула оксида серы будет SO3.
В соединении кремния с углеродом первый проявляет высшую валентность IV, а второй – низшую IV. Значит, формула – SiC. Это карбид кремния, основа огнеупорных и абразивных материалов.
2) Атом металла стоит в формуле на первом месте.
2) В формулах соединений атом неметалла, проявляющий низшую валентность, всегда стоит на втором месте, а название такого соединения оканчивается на «ид».
Например, СаО – оксид кальция, NaCl – хлорид натрия, PbS – сульфид свинца.
Теперь вы сами можете написать формулы любых соединений металлов с неметаллами.
sites.google.com
Валентность химических элементов – как определить, таблица валентности (8 класс)
При рассмотрении химических элементов можно заметить, что количество атомов у одного и того же элемента в разных веществах разнится. Каким же образом правильно записать формулу и не ошибиться в индексе химического элемента? Это легко сделать, если иметь представление, что такое валентность.

Для чего нужна валентность?
Валентность химических элементов – это способность атомов элемента образовывать химические связи, то есть присоединять к себе другие атомы. Количественной мерой валентности является число связей, которые образует данный атом с другими атомами или атомными группами.
В настоящее время валентность представляет собой число ковалентных связей (в том числе возникших и по донорно-акцепторному механизму), которыми данный атом соединен с другими. При этом не учитывается полярность связей, а значит, валентность не имеет знака и не может быть равной нулю.
Ковалентная химическая связь – это связь, осуществляемая за счет образования общих (связывающих) электронных пар. Если между двумя атомами имеется одна общая электронная пара, то такая связь называется одинарной, если две – двойной, если три – тройной.
Как находить валентность?
Первый вопрос, который волнует учеников 8 класса, начавших изучать химию – как определить валентность химических элементов? Валентность химического элемента можно посмотреть в специальной таблице валентности химических элементов
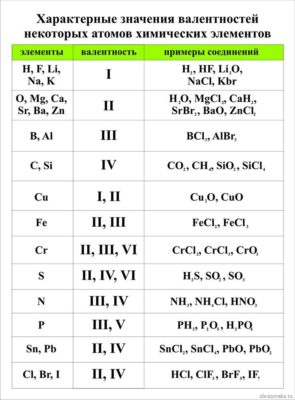
Рис. 1. Таблица валентности химических элементов
Валентность водорода принята за единицу, так как атом водорода может образовывать с другими атомами одну связь. Валентность других элементов выражаем числом, которое показывает, сколько атомов водорода может присоединить к себе атом данного элемента. Например, валентность хлора в молекуле хлористого водорода равна единице. Следовательно формула хлористого водорода будет выглядеть так: HCl. Так как и у хлора и у водорода валентность равна единице, никакой индекс не используется. И хлор и водород являются одновалентными, так как одному атому водорода соответствует один атом хлора.
Рассмотрим другой пример: валентность углерода в метане равна четырем, валентность водорода – всегда единица. Следовательно, рядом с водородом следует поставить индекс 4. Таким образом формула метана выглядит так: Ch5 .
Очень многие элементы образуют соединения с кислородом. Кислород всегда является двухвалентным. Поэтому в формуле воды h3O, где встречаются всегда одновалентный водород и двухвалентный кислород, рядом с водородом ставится индекс 2. Это значит, что молекула воды состоит из двух атомов водорода и одного атома кислорода.
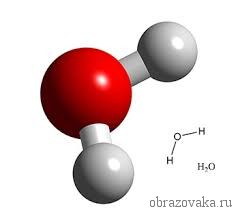
Рис. 2. Графическая формула воды
Не все химические элементы имеют постоянную валентность, у некоторых она может изменяться в зависимости от соединений, где используется данный элемент. К элементам с постоянной валентностью относятся водород и кислород, к элементам с переменной валентностью относятся, например, железо, сера, углерод.
Как определить валентность по формуле?
Если у вас перед глазами нет таблицы валентности, но есть формула химического соединения, то возможно определение валентности по формуле. Возьмем для примера формулу оксид марганца – Mn2O7
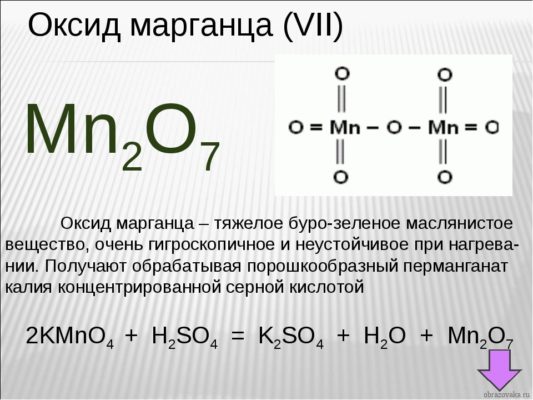
Рис. 3. Оксид марганца
Как известно, кислород является двухвалентным. Чтобы выяснить, какой валентностью обладает марганец, необходимо валентность кислорода умножить на число атомов газа в этом соединении:
2*7=14
Получившееся число делим на количество атомов марганца в соединении. Получается:
14:2=7
7 (VII) – валентность марганца в данном соединении
Что мы узнали?
В данной теме раскрывается информация о том, что такое валентность. Валентность – способность образовывать химические соединения посредством присоединения к атомам одного элемента атомов другого элемента. Валентность бывает постоянная и переменная. Зная валентность того или иного элемента, можно легко научиться записывать формулы соединений.
Тест по теме
obrazovaka.ru
Валентность. Определение валентности. - Ида Тен
Валентность элементов
До сих пор вы пользовались химическими формулами веществ, приведенными в учебнике, или теми, которые вам называл учитель. Как же правильно составлять химические формулы?
Химические формулы веществ составляются на основе знания качественного и количественного состава вещества. Веществ существует гигантское количество, естественно запомнить все формулы невозможно. Это и не нужно! Важно знать определенную закономерность, согласно которой атомы способны соединяться друг с другом с образованием новых химических соединений. Такая способность называется валентностью.
Валентность – свойство атомов элементов присоединять определенное число атомов других элементов
Рассмотрим модели молекул некоторых веществ, таких, как вода, метан и углекислый газ.

Видно, что в молекуле воды атом кислорода присоединяет два атома водорода. Следовательно, его валентность равна двум. В молекуле метана атом углерода присоединяет четыре атома водорода, его валентность в данном веществе равна четырем. Валентность водорода в обоих случаях равна одному. Такую же валентность углерод проявляет и в углекислом газе, но в отличие от метана, атом углерода присоединяет два атома кислорода, так как валентность кислорода равна двум.
Существуют элементы, валентность которых не меняется в соединениях. О таких элементах говорят, что они обладают постоянной валентностью. Если же валентность элемента может быть различной – это элементы с переменной валентностью. Валентность некоторых химических элементов приведена в таблице 2. Валентность принято обозначать римскими числами.
Таблица 2. Валентность некоторых химических элементов
| Символ элемента | Валентность | Символ элемента | Валентность |
| H, Li, Na, K, F, Ag | I | C, Si, Sn, Pb | II, IV |
| Be, Mg, Ca, Ba, Zn, O | II | N | I, II, III, IV |
| Al, B | III | P, As, Sb | III, V |
| S | II, IV, VI | Cl | I, II,III, IV,V, VII |
| Br, I | I, III, V | Ti | II, III, IV |
Стоит отметить, что высшая валентность элемента численно совпадает с порядковым номером группы Периодической Системы, в которой он находится. Например, углерод находиться в IV группе, его высшая валентность равна IV.
Исключение составляют три элемента:
- азот – находится в V группе, но его высшая валентность IV;
- кислород – находится в VI группе, но его высшая валентность II;
- фтор – находится в VII группе, но его высшая валентность – I.
Исходя из того, что все элементы расположены в восьми группах Периодической Системы, валентность может принимать значения от I до VIII.
Составление формул веществ при помощи валентности
Для составления формул веществ при помощи валентности воспользуемся определенным алгоритмом:
| Алгоритм | Пример |
| Записать химические формулы элементов | |
| Вверху, над символами элементов записать значение их валентности. Для элементов с переменной валентностью конкретная валентность указана в условии | |
| Найти наименьшее общее кратное (НОК) значений валентности, записать его вверху | |
| Поделить НОК на значения валентностей элементов – это индексы, выражающие число атомов | 10:V=2(P)10:II=5(O)P2O5 |
Определение валентности по формуле вещества
Чтобы определить валентность элементов по формуле вещества, необходим обратный порядок действий. Рассмотрим его также при помощи алгоритма:
| Алгоритм | Пример |
| Записать формулу вещества | |
| Указать известную валентность элемента (для элементов с постоянной валентностью) | |
| Найти наименьшее общее кратное (НОК) валентности и индекса элемента | |
| Поделить значение НОК на индекс элемента, валентность которого неизвестна |
При изучении данного параграфа были рассмотрены сложные вещества, в состав которых входят только два вида атомов химических элементов. Формулы более сложных веществ составляются иначе.
Бинарные соединения – соединения, в состав которых входит два вида атомов элементов
Для определения порядка последовательности соединения атомов используют структурные (графические) формулы веществ. В таких формулах валентности элементов обозначают валентными штрихами (черточками). Например, молекулу воды можно изобразить как
Н─О─Н
Графическая формула изображает только порядок соединения атомов, но не структуру молекул. В пространстве такие молекулы могут выглядеть иначе. Так, молекула воды имеет угловую структурную формулу:

- Валентность – способность атомов элементов присоединять определенное число атомов других химических элементов
- Существуют элементы с постоянной и переменной валентностью
- Высшая валентность химического элемента совпадает с его номером группы в Периодической Системе химических элементов Д.И. Менделеева. Исключения: азот, кислород, фтор
- Бинарные соединения – соединения, в состав которых входит два вида атомов химических элементов
- Графические формулы отражают порядок связей атомов в молекуле при помощи валентных штрихов
- Структурная формула отражает реальную форму молекулы в пространстве
idaten.ru
Урок №54. Валентность и степень окисления. Правила определения степеней окисления элементов
I. Валентность (повторение)
Валентность – это способность атомов присоединять к себе определенное число других атомов.

Правила определения валентностиэлементов в соединениях
1. Валентность водорода принимают за I (единицу). Тогда в соответствии с формулой воды Н2О к одному атому кислорода присоединено два атома водорода.
2. Кислород в своих соединениях всегда проявляет валентность II. Поэтому углерод в соединении СО2 (углекислый газ) имеет валентность IV.
3. Высшая валентность равна номеру группы.
4. Низшая валентность равна разности между числом 8 (количество групп в таблице) и номером группы, в которой находится данный элемент, т.е. 8 - Nгруппы.
5. У металлов, находящихся в «А» подгруппах, валентность равна номеру группы.
6. У неметаллов в основном проявляются две валентности: высшая и низшая.
Например: сера имеет высшую валентность VI и низшую (8 – 6), равную II; фосфор проявляет валентности V и III.
7. Валентность может быть постоянной или переменной.

Валентность элементов необходимо знать, чтобы составлять химические формулы соединений.

Запомните!
Особенности составления химических формул соединений.
1) Низшую валентность проявляет тот элемент, который находится в таблице Д.И.Менделеева правее и выше, а высшую валентность – элемент, расположенный левее и ниже.
Например, в соединении с кислородом сера проявляет высшую валентность VI, а кислород – низшую II. Таким образом, формула оксида серы будет SO3.
В соединении кремния с углеродом первый проявляет высшую валентность IV, а второй – низшую IV. Значит, формула – SiC. Это карбид кремния, основа огнеупорных и абразивных материалов.
2) Атом металла стоит в формуле на первое место.
2) В формулах соединений атом неметалла, проявляющий низшую валентность, всегда стоит на втором месте, а название такого соединения оканчивается на «ид».
Например, СаО – оксид кальция, NaCl – хлорид натрия, PbS – сульфид свинца.
Теперь вы сами можете написать формулы любых соединений металлов с неметаллами.
3) Атом металла ставится в формуле на первое место.
II. Степень окисления (новый материал)
Степень окисления – это условный заряд, который получает атом в результате полной отдачи (принятия) электронов, исходя из условия, что все связи в соединении ионные.
Рассмотрим строение атомов фтора и натрия:
F +9 )2)7
Na +11 )2)8)1
- Что можно сказать о завершённости внешнего уровня атомов фтора и натрия?
- Какому атому легче принять, а какому легче отдать валентные электроны с целью завершения внешнего уровня?
- Оба атома имеют незавершённый внешний уровень?
- Атому натрия легче отдавать электроны, фтору – принять электроны до завершения внешнего уровня.
F0 + 1ē → F-1 (нейтральный атом принимает один отрицательный электрон и приобретает степень окисления «-1», превращаясь в отрицательно заряженный ион - анион)
Na0 – 1ē → Na+1 (нейтральный атом отдаёт один отрицательный электрон и приобретает степень окисления «+1», превращаясь в положительно заряженный ион - катион)

| - Процесс отдачи электронов атомом, называется окислением. - Атом, отдающий электроны и повышающий свою степень окисления, окисляется и называется восстановителем. - Процесс принятия электронов атомом, называется восстановлением. - Атом, принимающий электроны и понижающий свою степень окисления, восстанавливается и называется окислителем. |
Как определить степень окисления атома в ПСХЭ Д.И. Менделеева?
Правила определения степени окисления атома в ПСХЭ Д.И. Менделеева:
1. Водород обычно проявляет степень окисления (СО) +1 (исключение, соединения с металлами (гидриды) – у водорода СО равна (-1) Me+nHn-1)
2. Кислород обычно проявляет СО -2 (исключения: О+2F2, h3O2-1 – перекись водорода)
3. Металлы проявляют только +n положительную СО
4. Фтор проявляет всегда СО равную -1 (F-1)
5. Для элементов главных подгрупп:
Высшая СО (+) = номеру группы Nгруппы
Низшая СО (-) = Nгруппы–8
Правила определения степени окисления атома в соединении:
I. Степень окисления свободных атомов и атомов в молекулах простых веществ равна нулю - Na0, P40, O20
II. В сложном веществе алгебраическая сумма СО всех атомов с учётом их индексов равна нулю = 0, а в сложном ионе его заряду.
Например, H+1N+5O3-2: (+1)*1+(+5)*1+(-2)*3 = 0
[S+6O4 -2]2-: (+6)*1+(-2)*4 = -2
Задание 1 – определите степени окисления всех атомов в формуле серной кислоты h3SO4?
1. Проставим известные степени окисления у водорода и кислорода, а СО серы примем за «х»
H+1SxO4-2
2. Составим и решим уравнение, согласно правилу (II):
(+1)*1+(х)*1+(-2)*4=0
Х=6 или (+6), следовательно, у серы CО +6, т.е. S+6
Задание 2 – определите степени окисления всех атомов в формуле фосфорной кислоты h4PO4?
1. Проставим известные степени окисления у водорода и кислорода, а СО фосфора примем за «х»
h4+1PxO4-2
2. Составим и решим уравнение, согласно правилу (II):
(+1)*3+(х)*1+(-2)*4=0
Х=5 или (+5), следовательно, у фосфора CО +5, т.е. P+5
Задание 3– определите степени окисления всех атомов в формуле иона аммония (Nh5)+?
1. Проставим известную степень окисления у водорода, а СО азота примем за «х»
(Nхh5+1)+
2. Составим и решим уравнение, согласно правилу (II):
(х)*1+(+1)*4=+1
Х=-3, следовательно, у азота CО -3, т.е. N-3
Алгоритм составления формулы по степени окисления
Составление названий бинарных соединений
Сравним понятия «валентность» и «степень окисления»:
ЗАКРЕПЛЕНИЕ
Определите степени окисления атомов в формулах веществ:Br2, CaO , SiO2, h3CO3 , CuO , Cu2O , Н2, KNO3 , FeO , Fe , Fe2O3, Fe(OH)2, Fe2(SO4)3, N2, HClO4
sites.google.com
Валентность железа. Какая валентность у железа?
Трудно переоценить роль железа для человеческого организма, ведь именно оно способствует «творению» крови, его содержание влияет на уровень гемоглобина и миоглобина, железо нормализует работу ферментной системы. Но что это за элемент с точки зрения химии? Какая валентность железа? Об этом будет рассказано в данной статье.

Немного истории
Человечество знало об этом химическом элементе и даже владело изделиями из него еще в IV веке до нашей эры. Это были народы Древнего Египта и Шумеры. Именно они первые начали изготавливать украшения, оружие из сплава железа и никеля, которые были найдены при археологических раскопках и тщательно исследованы химиками.
Немного позже, племена арийцев, переселившиеся в Азию, научилось добывать твердое железо из руды. Оно было настолько ценным для людей того времени, что изделия покрывали золотом!
Характеристика железа
Железо (Fe) стоит на четвертом месте по содержанию его в недрах земной коры. Оно занимает место в 7 группе 4 периода и имеет номер 26 в химической таблице элементов Менделеева. Валентность железа имеет прямую зависимость от своего положения в таблице. Но об этом позже.

Данный металл наиболее всего распространен в природе в виде руды, встречается в воде как минерал, а также в различных соединениях.
Наибольшее количество запасов железа в виде руды, находится в России, Австралии, Украине, Бразилии, США, Индии, Канаде.
Физические свойства
Прежде чем переходить к валентности железа, необходимо подробнее рассмотреть его физические свойства, так сказать, приглядеться к нему поближе.
Этот металл имеет серебристый цвет, достаточно пластичный, но способен к увеличению твердости путем его взаимодействия с другими элементами (например, с углеродом). Также он обладает магнитными свойствами.
Во влажной среде железо может корродировать, то есть ржаветь. Хотя абсолютно чистый металл устойчивее к влаге, но если в нем есть примеси, именно они провоцируют коррозию.

Железо хорошо взаимодействует с кислотной средой, даже может образовывать соли железной кислоты (при условии сильного окислителя).
В воздушной среде быстро покрывается оксидной пленкой, которая защищает его от взаимодействий.
Химические свойства
Также этот элемент обладает рядом химических свойств. Железо, как и остальные элементы таблицы Менделеева, имеет заряд атомного ядра, который соответствует порядковому номеру +26. А возле ядра вращается 26 электронов.
А вообще, если рассматривать свойства железа – химического элемента, то он является металлом с невысокой активной способностью.
Взаимодействуя с окислителями более слабыми, железо образует соединения, где оно двухвалентно (то есть его степень окисления +2). А если с сильными окислителями, то степень окисления железа достигает +3 (то есть валентность его становится равной 3).
При взаимодействии с химическими элементами, которые не являются металлами, Fe выступает по отношению к ним восстановителем, при этом степень окисления его становиться, кроме +2 и +3, даже +4, +5, +6. Такие соединения имеют очень сильные окислительные свойства.
Как уже отмечалось выше, железо в воздушной среде покрывается оксидной пленкой. А при нагревании скорость реакции повышается и может образоваться оксид железа с валентностью 2 (температура менее 570 градусов по Цельсию) или оксид с валентностью 3 (температурный показатель более 570 градусов).

Взаимодействие Fe с галогенами, приводит к образованию солей. Элементы фтор и хлор окисляют его до +3. Бром же – до +2 или +3 (все зависит от того, какие условия осуществления химического превращения при взаимодействии с железом).
Вступая во взаимодействия с йодом, элемент окисляется до +2.
Нагревая железо и серу, получается сульфид железа с валентностью 2.
Если феррум расплавить и соединить его с углеродом, фосфором, кремнием, бором, азотом, то получатся соединения называемые сплавами.
Железо является металлом, поэтому оно вступает во взаимодействие и с кислотами (об этом кратко также говорилось чуть выше). Например, кислоты серная и азотная, имеющие высокую концентрацию, в среде с пониженной температурой, на железо не оказывают воздействия. Но стоит ей повысится, как происходит реакция, в результате которой железо окисляется до +3.
Чем выше концентрация кислоты, тем большую температуру необходимо дать.
Нагревая 2-х валентное железо в воде, получим его оксид и водород.
Также Fe обладает способностью вытеснять из водных растворов солей металлы, которые имеют пониженную активность. При этом он окисляется до +2.
При повышении температуры, железо восстанавливает металлы из оксидов.

Что такое валентность
Уже в предыдущем разделе немного встречалось понятие валентности, а также степени окисления. Пришло время рассмотреть валентность железа.
Но для начала необходимо понять, что это вообще за такое свойство химических элементов.
Химические вещества почти всегда постоянны в своем составе. Например, в формуле воды Н2О – 1 атом кислорода и 2 атома водорода. То же самое и с другими соединениями, в которых задействованы два химических элемента, один из которых водород: к 1 атому химического элемента может добавиться 1-4 атома водорода. Но никак не наоборот! А потому, видно, что водород присоединяет к себе всего 1 атом другого вещества. И именно это явление называют валентностью – способностью атомов химического элемента присоединять конкретное количество атомов других элементов.
Значение валентности и графическая формула
Есть элементы таблицы Менделеева, которые обладают постоянной валентностью – это кислород и водород.
А есть такие химические элементы, у которых она изменяется. Например, железо чаще 2-х и 3-х валентно, сера 2, 4, 6-ти, углерод 2 и 4-х. Это элементы с переменной валентностью.
Далее, понимая, что такое валентность, можно правильно написать графическую формулу соединений. Она отображает последовательность соединения атомов в молекуле.
Также, зная валентность одного из элементов в соединении, можно определить валентность другого.
Валентность железа
Как было отмечено, железо относится к элементам с переменной валентностью. И она может колебаться не только между показателями 2 и 3, но и достигать 4, 5 и даже 6.
Конечно, более подробно изучает валентность железа неорганическая химия. Рассмотрим этот механизм кратко на уровне простейших частиц.
Железо является д-элементом, к которому причисляется еще 31 элемент таблицы Менделеева (это 4-7 периоды). С возрастанием порядкового номера, свойства д-элементов приобретают небольшие изменения. Атомный радиус у этих веществ также медленно возрастает. Они обладают переменной валентностью, которая зависит от того, что предвнешний д-электронный подуровень является незавершенным.
Потому для железа валентными есть не только с-электроны, находящиеся во внешнем слое, но и неспаренные 3д-электроны предвнешнего слоя. И, как следствие, валентность Fe в химических соединениях может равнятся 2, 3, 4, 5, 6. В основном, она равна 2 и 3 – это более устойчивые соединения железа с другими веществами. В менее устойчивых - он проявляет валентность 4, 5, 6. Но, такие соединения встречаются реже.

Двухвалентный феррум
При взаимодействии 2 валентного железа с водой получается оксид железа (2). Такое соединение обладает черным цветом. Достаточно легко взаимодействует с соляной (малой концентрации) и азотной (высокой концентрации) кислотами.
Если такому оксиду 2-х валентного железа провзаимодействовать или с водородом (температура 350 градусов по Цельсию), или с углеродом (коксом) при 1000 градусов, то оно восстанавливается до чистого состояния.
Добывают оксид железа 2-х валентного такими способами:
- через соединение оксида 3-х валентного железа с угарным газом;
- при нагревании чистого Fe, при этом низкое давление кислорода;
- при раскладывании оксалата 2-х валентного железа в вакуумной среде;
- при взаимодействии чистого железа с его оксидами, температура при этом 900-1000 градусов по Цельсию.
Что касается природной среды, то оксид железа 2-х валентного, присутствует в виде минерала вюстита.
Есть еще способ, как в растворе определить валентность железа – в данном случае, имеющего ее показатель 2. Необходимо провести реакции с красной солью (гексацианоферрат калия) и с щелочью. В первом случае наблюдается получение осадка темно-синего цвета – комплексной соли железа 2-х валентного. Во втором – получение темного серо-зеленого осадка – гидроксида железа также 2-х валентного, в то время, как гидроксид железа 3-х валентного имеет цвет в растворе темно-бурый.

Трехвалентное железо
Оксид 3-х валентного феррума имеет порошкообразную структуру, цвет которой красно-коричневый. Имеет также наименования: окись железа, железный сурик, красный пигмент, пищевой краситель, крокус.
В природе это вещество встречается в виде минерала – гематита.
Оксид такого железа с водой уже не взаимодействует. Но соединяется с кислотами и щелочами.
Применяется оксид железа (3) для окрашивания материалов, применяемых в строительстве:
- кирпичей;
- цемента;
- керамических изделий;
- бетона;
- тротуарной плитки;
- напольных покрытий (линолеум).
Железо в организме человека
Как отмечалось в начале статьи, вещество железо является важной составляющей человеческого организма.
Когда этого элемента является недостаточно, то могут возникнуть следующие последствия:
- повышенная усталость и чувствительность к холоду;
- сухость кожи;
- снижение мозговой деятельности;
- ухудшение прочности ногтевой пластины;
- головокружение;
- проблемы с пищеварением;
- седина и выпадение волос.
Накапливается железо, как правило, в селезенке и печени, а также почках и поджелудочной железе.
В рационе человека должны быть продукты, содержащие железо:
- говяжья печень;
- гречневая каша;
- арахис;
- фисташки;
- зеленый горошек консервированный;
- сушенные белые грибы;
- куриные яйца;
- шпинат;
- кизил;
- яблоки;
- груши;
- персики;
- свекла;
- морепродукты.
Недостаток железа в крови, приводит к снижению гемоглобина и развитию такого заболевания, как железодефицитная анемия.
fb.ru
Валентность элементов | Путешествие в мир химии
 В настоящее время известно около 120 химических элементов, причём несколько самых тяжёлых ещё не получили даже своего названия. Реально же окружающий человека мир, включая его самого, построен примерно из 85 элементов.
В настоящее время известно около 120 химических элементов, причём несколько самых тяжёлых ещё не получили даже своего названия. Реально же окружающий человека мир, включая его самого, построен примерно из 85 элементов.
Как же эти несколько десятков разновидностей атомов создают всё многообразие растительного и животного мира, а также все материки и моря, горы и пустыни, песок и глину, нефть и уголь?
Дело в том, что элементы могут соединяться, связываться друг с другом в самых разнообразных сочетаниях.
И этим процессом управляют строгие законы. Один из самых важных связан с понятием валентности элементов.
Когда Дальтон формулировал свой закон кратных отношений, он опирался на данные химического анализа разных веществ, построенных из одних и тех же элементов.
Постепенно таких примеров становилось всё больше, и химики стремились понять, существуют ли какие-то закономерности в числе атомов, соединяющихся друг с другом.
Когда к середине XIX века были правильно определены формулы большинства известных к тому времени веществ, оказалось, что атомы в них могут связываться друг с другом не в любых, а только во вполне определённых соотношениях.
Так, атомы водорода любят связываться с одним атомом какого-нибудь элемента (включая и сам водород). Например, были известны такие соединения, как хлороводород НС1, бромоводород НВг, йодоводород HI, молекулярный водород Н2 и т. п. Но не было случая, чтобы получилось вещество состава, положим, НС12.
Другие атомы могут связываться с несколькими атомами водорода, но тоже с определённым их числом. Например, в уже знакомой нам молекуле воды один атом кислорода связывается с двумя атомами водорода.
Поэтому формулу молекулы воды можно записать так: Н-О-Н (чёрточка показывает, что два атома связаны друг с другом) или, сокращённо, Н2О. Атомы серы тоже могут связываться с двумя атомами водорода, образуя сероводород h3S. Атомы азота и фосфора могут связываться с тремя атомами водорода, образуя аммиак Nh4 и фосфин PHV Атомы углерода могут связываться с четырьмя атомами водорода, образуя метан СН4. Такое свойство атомов связываться с определённым числом других атомов назвали валентностью.
Зная валентность одних атомов, можно определить валентность других, связанных с ними. Скажем, водород в своих соединениях одновалентен, то есть образует одну связь с другими атомами.
Поэтому хлор (С1), бром (Вг) и йод (I) в соединениях с водородом тоже одновалентны: это можно изобразить с помощью «формул с чёрточками», Н-CI, Н-Вг и H-I, в которых одна чёрточка обозначает одну валентность.
Валентность, равную единице, имеет также натрий (и все другие щелочные металлы, например литий и калий).
Это проявляется, например, в формуле хлорида натрия NaCl — той самой поваренной соли, которую синтезировал и съел в молодости академик Н. Н. Семёнов: натрий одновалентен, хлор одновалентен, вот они и соединились в таком соотношении.
А атом кислорода двухвалентен, именно поэтому он и связывается с двумя одновалентными атомами водорода в молекуле воды. Если же двухвалентные атомы кислорода связываются друг с другом (в газообразном кислороде), то между этими атомами образуется двойная связь, которая изображается двумя чёрточками: О=О (а в молекуле газообразного азота N2 между атомами образуется тройная связь N=N). Характерные валентности, которыми может обладать каждый элемент, помогли в своё время Д. И. Менделееву открыть знаменитый периодический закон и составить не менее знаменитую периодическую таблицу химических элементов.
Как устанавливали валентность разных элементов с помощью одновалентного водорода, понятно. Но многие элементы, например серебро, с водородом не соединяются.
Как узнать их валентность? На помощь пришёл кислород, который соединяется почти со всеми элементами.
А кислород, как известно, двухвалентен. Значит, чтобы узнать валентность серебра, нужно получить его соединение с кислородом.
Такое соединение (оксид серебра) было известно, его формула Ag2О.
А так как кислород двухвалентен, значит, серебро, как и водород, — одновалентно!
Если оксид магния имеет формулу MgO, значит, магний двухвалентен.
Если оксид алюминия имеет формулу А12О3, значит, алюминий трёхвалентен (три атома кислорода имеют суммарную валентность шесть, значит, на каждый из двух атомов алюминия приходится валентность три). Теперь, зная, что водород одновалентен, а кислород двухвалентен, можно было установить валентность в разных соединениях для атомов элементов, которые образуют химические соединения с водородом или с кислородом.
Например, из формулы диоксида кремния SiО2 (такую формулу имеет, например, кварц) следует, что кремний четырёхвалентен.
Читайте так же:
cgz.sumy.ua


















