Свойства и структура воды (стр. 1 из 5). Структура воды
Структура воды: новые экспериментальные данные
Воде дана таинственная власть Быть соком жизни на Земле.Леонардо да Винчи
Рис. 1. Структура воды при температуре 20<sup>о</sup>С, размер по горизонтали — 400 мкм. Белые пятна — это эмулоны.<br><br>

Рис. 2. Структура водных растворов при 20<sup>о</sup>С: А — дистиллированная вода; Б — дегазированная минеральная вода боржоми; В — спиртовая настойка 70%.

Рис. 3. Эмулоны в бидистиллированной воде при температурах 4<sup>о</sup>С (А), 20<sup>о</sup>С (Б), 80<sup>о</sup>С (В). Размеры снимков 1,5 × 1,5 мм.
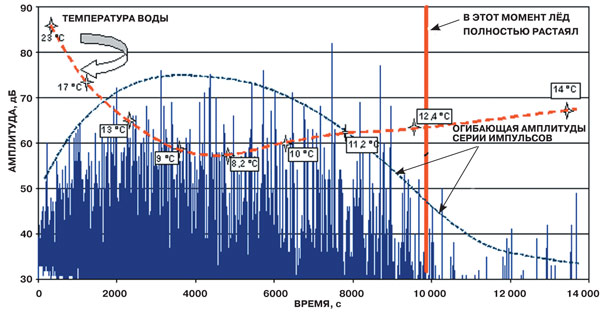
Рис. 4. Изменение амплитуды сигналов акустической эмиссии и температуры воды в процессе таяния льда.
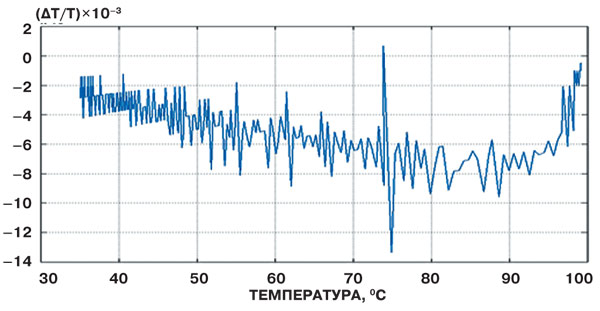
Рис. 5. Относительное изменение температуры при нагревании воды.
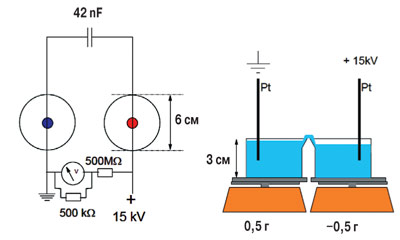
Подробности для любознательных. Схема опыта. За короткое время из стаканчика с положительным электродом (анодом) через «мостик» утекло 0,5 грамма воды.

«Парящий водяной мостик» длиной около 3 сантиметров.

Наэлектризованная стеклянная палочка искажает форму «мостика» и разбивает его на струйки.
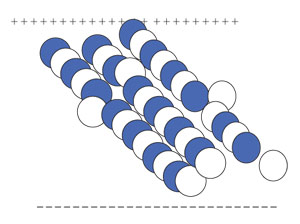
Так могут выглядеть эмулоны, образующие нитевидную структуру «мостика».
‹
›
Воду принято рассматривать и как практически нейтральный растворитель, в котором протекают биохимические реакции, и как субстанцию, разносящую по телу живых организмов различные вещества. Вместе с тем вода — непременный участник всех физико-химических процессов и, в силу своей огромной важности, самое изучаемое вещество. Изучение свойств воды не раз приводило к неожиданным результатам. Казалось бы, какие неожиданности может таить в себе несложная реакция окисления водорода 2h3 + O2 → 2h3O? Но работы академика Н. Н. Семёнова показали, что реакция эта — разветвлённая, цепная. Было это более семидесяти лет назад, и про цепную реакцию деления урана ещё не знали. Вода в стакане, реке или озере не просто огромные количества отдельных молекул, а их объединения, надмолекулярные структуры — кластеры. Для описания структуры воды предложен ряд моделей, которые более или менее правильно объясняют только некоторые её свойства, а в отношении других противоречат эксперименту.

теоретически кластеры рассчитывают обычно только для нескольких сотен молекул или для слоёв вблизи межфазной границы. Однако ряд экспериментальных фактов свидетельствует, что в воде могут существовать гигантские, по молекулярным масштабам, структуры (работы члена-корреспондента РАН Е. Е. Фесенко).
В тщательно очищенной дважды дистиллированной воде и некоторых растворах нам удалось методом акустической эмиссии обнаружить и с помощью лазерной интерферометрии визуализировать структурные образования, состоящие из пяти фракций размерами от 1 до 100 мкм. Эксперименты позволили установить, что каждый раствор имеет свою, присущую только ему структуру (рис. 1, 2).
Надмолекулярные комплексы образованы сотнями тысяч молекул воды, сгруппированных вокруг ионов водорода и гидроксила в виде ионных пар. Для этих надмолекулярных комплексов мы предлагаем название «эмулоны», чтобы подчеркнуть их сходство с частицами, образующими эмульсию. Комплексы состоят из отдельных фракций размерами от 1 до 100 мкм, причём фракций, имеющих размеры 30, 70 и 100 мкм, значительно больше остальных.
Содержание отдельных фракций эмулонов зависит от концентрации ионов водорода, температуры, концентрации раствора и предыстории образца (рис. 3). В бидистиллированной воде при 4оС комплексы плотно упакованы и образуют текстуру, напоминающую паркет. Как известно, вода при этой температуре имеет максимальную плотность. При повышении температуры до 20оС в структуре воды происходят существенные изменения: количество свободных эмулонов становится наибольшим. При дальнейшем нагреве они постепенно разрушаются, число их уменьшается, и этот процесс в основном заканчивается при 75оС, когда скорость звука в воде достигает максимума.
За счёт дальнодействия электростатических сил эмулоны в воде образуют довольно стабильную сверхрешётку, которая, однако, чутко реагирует на электромагнитные, акустические, тепловые и другие внешние воздействия.
Обнаруженные надмолекулярные комплексы непротиворечиво включают в себя все ранее полученные сведения об организации воды в нанообъёмах и позволяют объяснить многие экспериментальные факты, которые не имели стройного, логичного обоснования. К ним относится, например, образование «парящего водяного мостика», описанного в ряде работ.
Суть эксперимента заключается в том, что если поставить рядом два небольших химических стакана с водой, опустить в них платиновые электроды под постоянным напряжением 15—30 кВ, то между сосудами образуется водяная перемычка диаметром 3 мм и длиной до 25 мм. «Мостик» парит длительное время, имеет слоистую структуру, и по нему происходит перенос воды от анода к катоду. Этот феномен и все его свойства — следствие наличия в воде эмулонов, которые, по-видимому, обладают дипольным моментом. Можно предсказать и ещё одно свойство явления: при температуре воды выше 75оС «мостик» не возникнет.
Легко объясняются и аномальные свойства талой воды. Как отмечалось в литературе, многие свойства талой воды — плотность, вязкость, электропроводность, показатель преломления, растворяющая способность и другие — отличаются от равновесных параметров. Сведéние этих эффектов к удалению из воды дейтерия в результате фазового перехода (температура плавления «тяжёлого льда» D2O 3,82оС) несостоятельно, поскольку концентрация дейтерия крайне незначительна — один атом дейтерия на 5—7 тыс. атомов водорода.
Изучение плавления льда методом акустической эмиссии позволило впервые установить, что после полного расплавления льда талая вода, находящаяся в метастабильном состоянии, становится источником акустических импульсов, что служит экспериментальным подтверждением образования в воде надмолекулярных комплексов (рис. 4).
Эксперименты показывают, что талая вода на протяжении почти 17 часов может находиться в активном метастабильном состоянии (после плавления льда его микрокристаллики сохраняются только доли секунды и совсем не определяют свойства талой воды). Это загадочное явление объясняется тем, что при разрушении гексагональной кристаллической решётки льда резко меняется структура вещества. Кристаллы льда разрушаются быстрее, чем перестраивается в устойчивое равновесное состояние образовавшаяся из него вода.
Уникальность фазового перехода лёд↔вода заключается в том, что в талой воде концентрация ионов водорода H+ и гидроксила OH– непродолжительное время сохраняется неравновесной, какой она была во льду, то есть в тысячу раз меньшей, чем в обычной воде. Через некоторое время концентрация ионов H+ и OH– в воде принимает своё равновесное значение. Поскольку ионы водорода и гидроксила играют решающую роль в формировании надмолекулярных комплексов воды (эмулонов), вода на некоторое время остаётся в метастабильном состоянии. Реакция её диссоциации h3O → H+ + OH– требует значительной затраты энергии и протекает очень медленно. Константа скорости этой реакции составляет всего 2,5∙10–5 c–1 при 20оС. Поэтому время возвращения талой воды в равновесное состояние теоретически должно составлять 10—17 часов, что и наблюдается на практике. Исследования динамики изменения концентрации ионов водорода в талой воде во времени подтверждают это. Необычные свойства талой воды служат причиной разговоров о «памяти» воды. Но под «памятью» воды следует понимать зависимость её свойств от предыстории и ничего больше. Можно разными способами — замораживанием, нагреванием, кипячением, обработкой ультразвуком, воздействием различных полей и др. — перевести воду в метастабильное состояние, но оно будет неустойчивым, недолго сохраняющим свои свойства. Оптическим методом мы обнаружили в талой воде присутствие лишь одной фракции надмолекулярных образований с размерами 1—3 мкм. Возможно, что пониженная вязкость и более редкая пространственная сетка из эмулонов в талой воде увеличивают растворяющую способность и скорость диффузии.
Реальность существования эмулонов подтверждает классический метод термического анализа (рис. 5). На графике наблюдаются чётко выраженные пики, свидетельствующие о структурных перестройках в воде. Наиболее значимые соответствуют 36оC — температуре минимальной теплоёмкости, 63оC — температуре минимальной сжимаемости, и особенно характерен пик при 75оC — температуре максимальной скорости звука в воде. Их можно трактовать как своеобразные фазовые переходы, связанные с разрушением эмулонов. Это позволяет сделать вывод: жидкая вода — очень своеобразная дисперсная система, включающая как минимум пять структурных образований с различными свойствами. Каждая структура существует в определённом, характерном для неё температурном интервале. Превышение температуры над пороговым уровнем, критичным для данной структуры, приводит к её распаду.
Литература
Зацепина Г. Л. Физические свойства и структура воды. — М.: Изд-во Московского университета. — 1998. — 185 с.
Кузнецов Д. М., Гапонов В. Л., Смирнов А. Н. О возможности исследования кинетики фазовых переходов в жидкой среде методом акустической эмиссии // Инженерная физика, 2008, № 1, с. 16—20.
Кузнецов Д. М., Смирнов А. Н., Сыроешкин А. В. Акустическая эмиссия при фазовых превращениях в водной среде // Российский химический журнал — М.: Рос. хим. об-во им. Д. И. Менделеева, 2008, т. 52, № 1, с. 114—121.
Смирнов А. Н. Структура воды: новые экспериментальные данные. // Наука и технологии в промышленности, 2010, № 4, с. 41—45.
Смирнов А. Н. Акустическая эмиссия при протекании химической реакции и физико-химических процессов // Российский химический журнал. — М.: Рос. хим. об-во им. Д. И. Менделеева, 2001, т. 45, с. 29—34.
Смирнов А. Н., Сыроешкин А. В. Супранадмолекулярные комплексы воды // Российский химический журнал. — М.: Рос. хим. об-во им. Д. И. Менделеева, 2004, т. 48, № 2, с. 125—135.
***
Подробности для любознательных
Как возникает «мостик»
Образование «водяного мостика» описано в работах нидерландского физика Элмара Фукса с коллегами[1, 2].
В две стоящие рядом небольшие ёмкости с водой погружают платиновые электроды и подают на них постоянное напряжение 15—20 кВ. На фотографиях из [1] отчётливо видно, что вначале в анодном стакане, а затем и в катодном на поверхности воды возникают возвышения, которые сливаются, образуя между ёмкостями водяную перемычку круглого сечения диаметром 2—4 мм. После этого стаканы можно отодвинуть один от другого на 20—25 мм. Перемычка существует довольно долго, образуя «парящий водяной мостик». Вдоль «мостика» перетекает вода. Концы «мостика» разноимённо заряжены, поэтому вода в ёмкостях приобретает различные значения рН: 9 и 4. «Мостик» состоит из тонких струек; при поднесении к нему заряженной стеклянной палочки он расщепляется на несколько рукавов. Высокая техника эксперимента позволила зарегистрировать движение шаровидных образований по поверхности «водяного мостика» [2].
Объяснить этот эффект доктор Э. Фукс не смог, но ряд наблюдавших его исследователей склонны считать эффект следствием возникновения сверхтекучести, изменения соотношений количеств орто- и парамолекул воды (с параллельными и антипараллельными спинами соответственно) или притяжения дипольных молекул воды. Но ни один из этих вариантов объяснений не представляется убедительным. А обнаруженные гигантские надмолекулярные комплексы размерами до 100 мкм — эмулоны — вполне подходят на роль элементов «мостика». Возникновение на нём сферических образований, например, можно объяснить потерей устойчивости нитями из эмулонов и выталкиванием некоторых из них на поверхность «мостика», по которой они станут перемещаться к одному из электродов.
Литература
1. Elmar C. Fuchs et al. The floating water bridge, J. Phys. D: Appl. Phis. 40 (2007) 6112 — 4.
2. Elmar C. Fuchs et al. Dynamic of the floating water bridge, J. Phys. D: Appl. Phis. 41 (2008) 185502 (5pp).
www.nkj.ru
Структура жидкой воды
Под структурой воды понимается конкретное расположение в пространстве составляющих структуру частиц – молекул воды.
Представим себе ситуацию, что мы имеем идеально чистую воду, из которой образовался лед с идеальной кристаллической, т.е. плотнейшей структурой. Диаметр молекулы воды во льду, определенный методами кристаллографии, равен 2,76 Å (0,276 нм). Если бы жидкая вода обладала идеальной, т.е. плотнейшей упаковкой молекул, напоминающей размещение бильярдных шаров в ящике, то в 1 см3объема поместилось бы 1/√16dчастиц, плотность воды была бы 1,74 г/см3, а координационное число, т.е. количество контактирующих соседей, равнялось бы 12. В действительности же структура воды ажурная, т.е. в ней имеется множество пустот, координационное число 4-5, а плотность близка к 1 г/см3(см.рис.1.5)
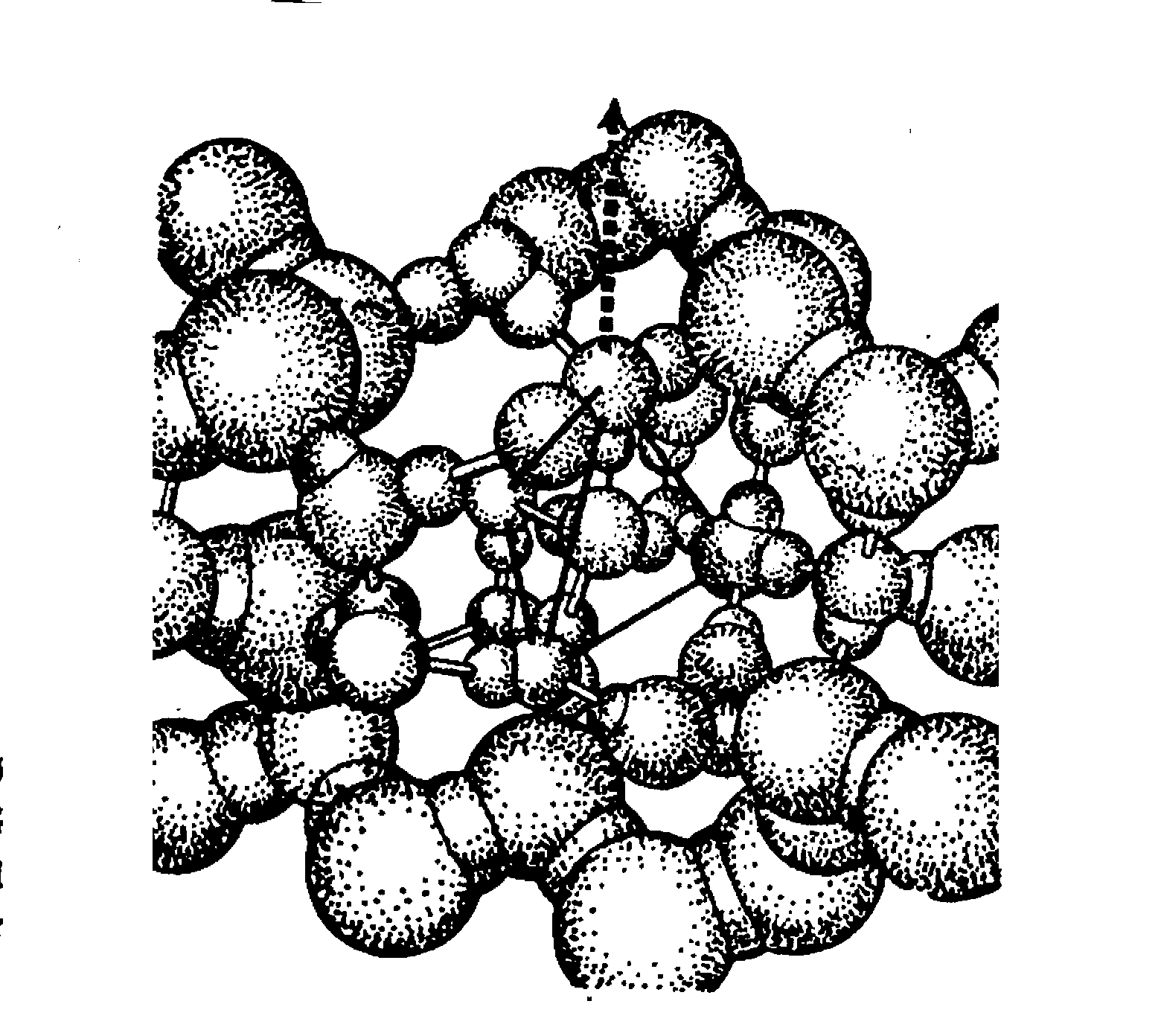
Рис.1.5. Кристаллическая структура воды
В жидкой воды молекулы не реализуют полностью свои водородные связи, существуют свободные молекулы, способные проникать в пустоты ажурного каркаса. Все это называется дефектами кристаллической решетки, причина возникновения которых до сих пор выясняется. Одной из причин называют наличие тяжелой воды D2О, искажающей кристаллическую решетку.
Таким образом, в жидкой воде существует ближний порядок, т.е. сохранение кристаллической структуры на некотором небольшом расстоянии. За счет теплового движения молекул часть их отрывается от ассоциата и становится свободной, другая их часть, оставаясь в структуре ассоциата, искажает кристаллический порядок. Схематично это показано на рис.1.6.
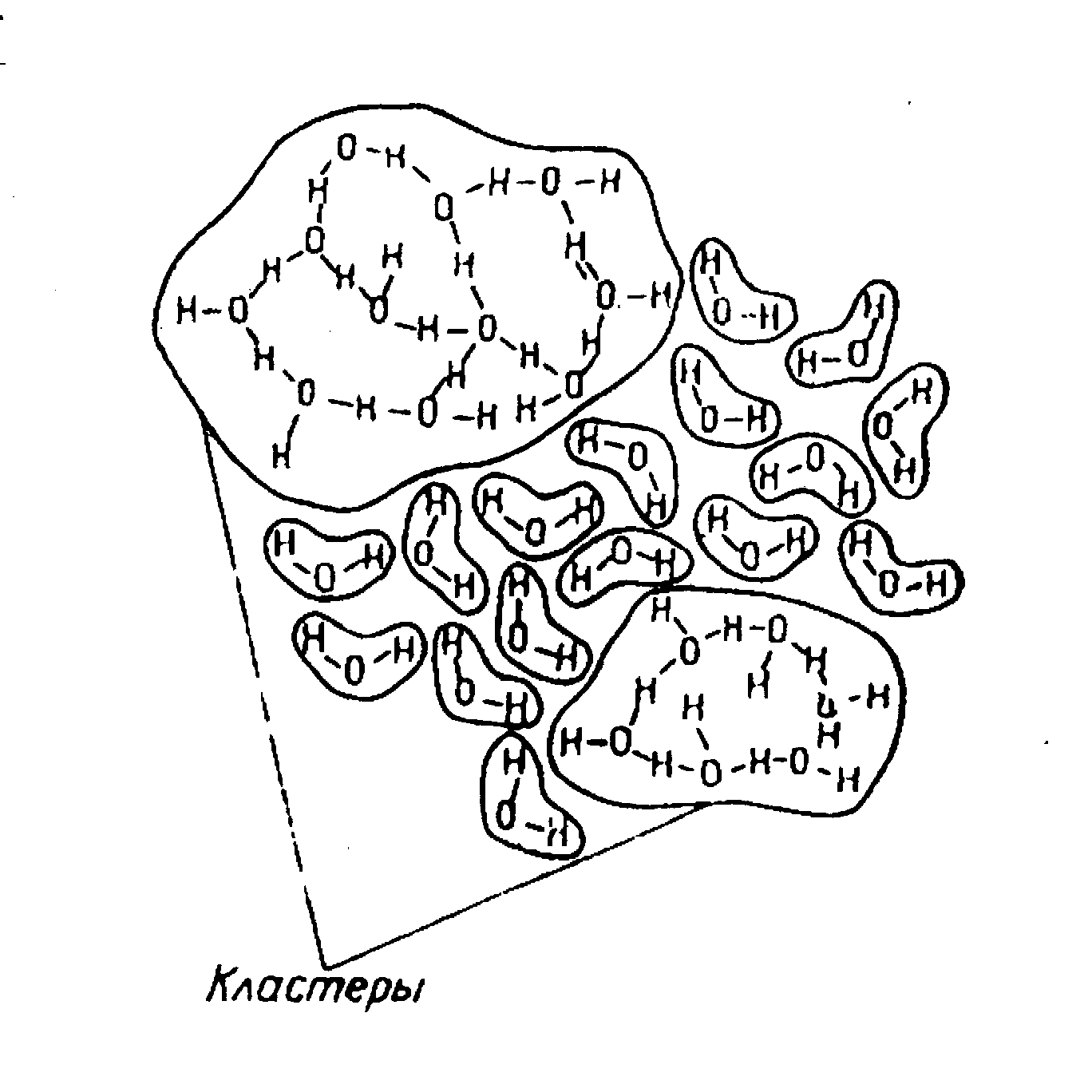
Рис.1.6. Схематическое изображение структуры жидкой воды (кластерная модель)
Сохранившие структуру ассоциаты получили название «кластеры».
Если для наглядности каждую молекулу воды представить в виде шара, а связи между ними – в виде пружинок, то каждый шар окажется связанным с четырьмя соседними, образуя элементарную ячейку-тетраэдр. Множество тетраэдров объединяются в некую колеблющуюся, но упорядоченную систему. Часть шаров отрываются, свободно перемещаются среди кластеров, могут проникать внутрь ажурной структуры.
Пока вода существует в форме льда, шары колеблются и перемещаются в пределах тех степеней свободы, которые дают им упругие связи – пружинки, т.е. они могут колебаться и поворачиваться вокруг своей оси. В объеме существует дальний порядок.
При повышении температуры движение шаров усиливается, плавление льда сопровождается разрывом связей. После завершения процесса плавления устанавливается равновесие для данной температуры, когда разорванными сохраняется определенная доля связей. При нормальной температуре разрываются 9-10% всех водородных связей.
Плотность воды в твердом состоянии 0,9168, а в жидком – 0,9998 г/см3, т.е. вода при плавлении сжимается на 8,3%. Это близко и к доле разорванных водородных связей.
Посмотрим, что происходит внутри кластера. Элементарная ячейка – тетраэдр – имеет возможность присоединить еще двенадцать молекул воды (рисунок 1.7).
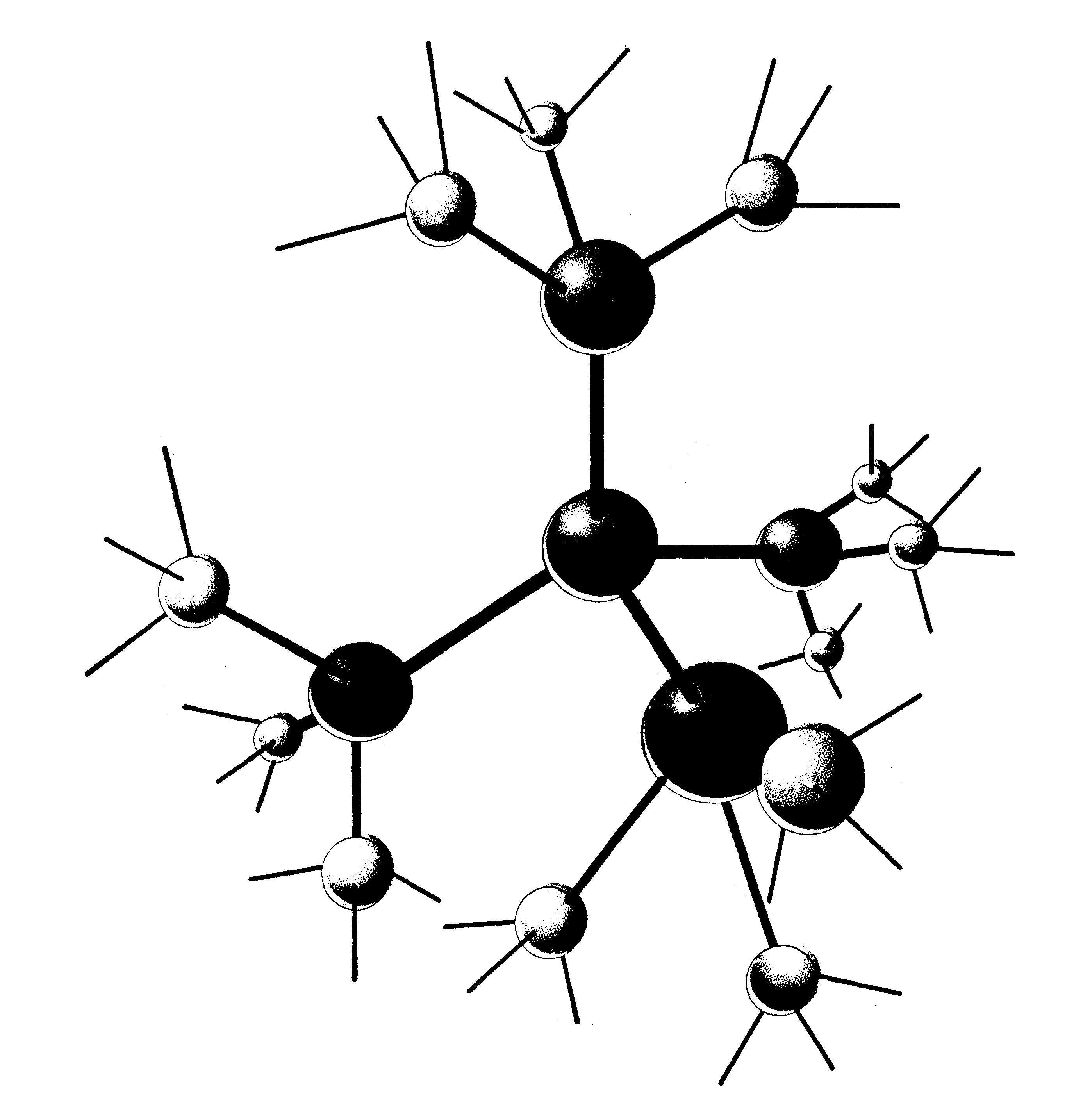
Рис. 1.7. Пятимолекулярный ассоциат рисунка 2 с полностью реализованными двенадцатью центрами образования водородных связей
Можно дальше представить следующую сферу структуры, но вероятность существования семнадцатимолекулярного ассоциата очень мала из-за нарушений дальнего порядка. Вместе с тем появляется возможность зацикливания концевых кислородов в пятичленные циклы, что понижает общую энергию ассоциата и стабилизирует его (рисунок 1.8).
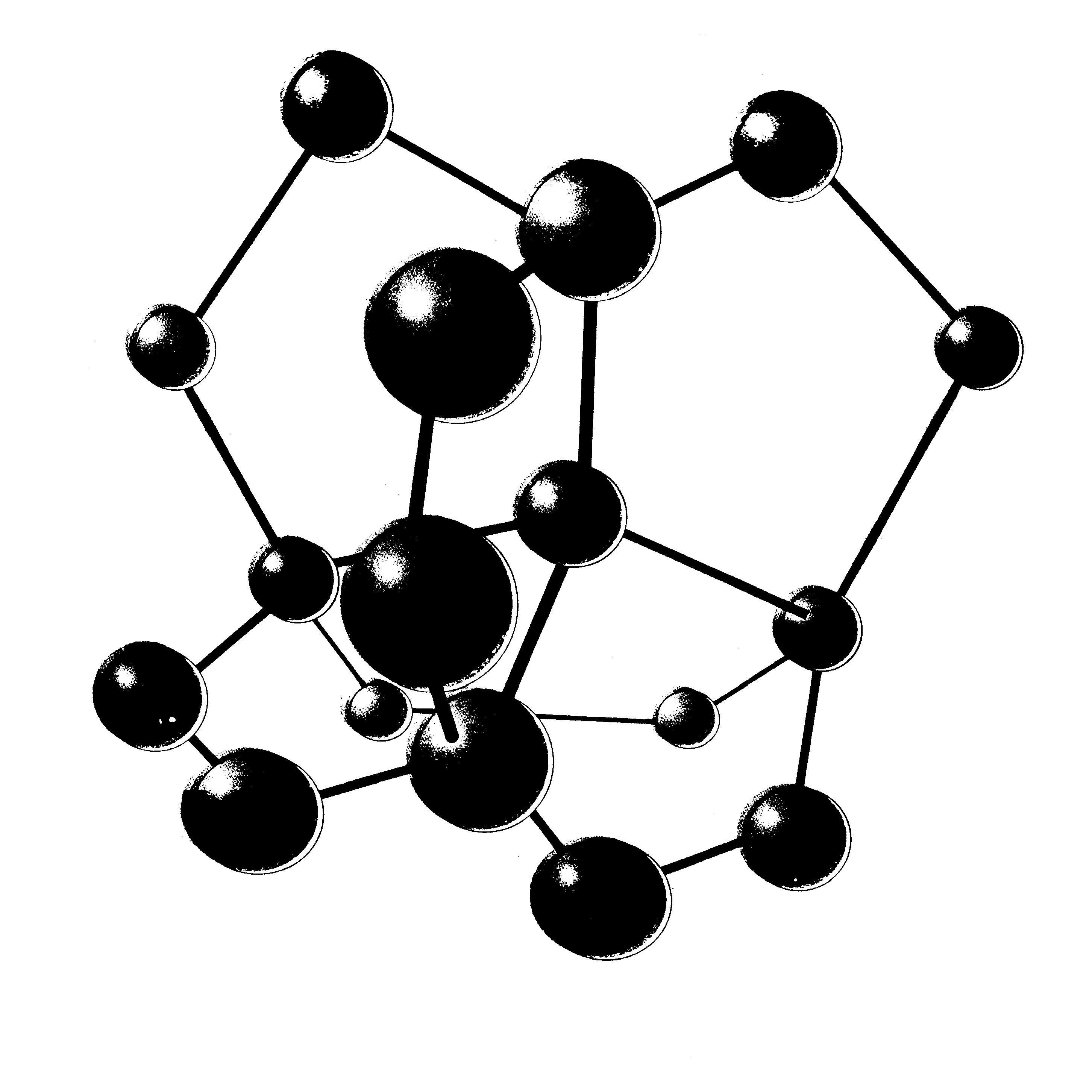
Рис.1.8. Семнадцатимолекулярный ассоциат рисунка 7 с шестью образовавшимися циклами
На следующем этапе рассматриваются ассоциаты воды, составленные из таких стабильных комплексов (рисунок 1.9).
Рис.1.9. Модель ассоциата воды из 57-и молекул.
Тетраэдр из четырех додекаэдров («квант»). Каждый из додекаэдров имеет 12 пятиугольных граней, 30 ребер, 20 вершин (в каждой соединяются три ребра, вершинами являются атомы кислорода, ребром служит водородная связь О-Н…О).
Естественно, что у таких ассоциатов-кластеров существует некоторый порог стабильности и при любом энергетическом воздействии на воду будут происходить некие перестройки во взаимном расположении структурных единиц. Виды и способы таких воздействий разнообразны – электрические и магнитные поля, ультразвуковая и гидродинамическая кавитация. Уровень энергетического воздействия можно охарактеризовать производимым результатом: разрушение структуры или перестройка структуры. Изменить некоторые свойства воды можно и сверхслабыми внешними воздействиями, правда, эти изменения пока не идентифицируются физико-химическими методами, а фиксируются лишь косвенными проявлениями на живых биологических системах.
studfiles.net
Что такое структура воды?, раздел Статьи профессора К.Г. Короткова, Статьи по темам
Коротков К.Г., 2008
В последнее время возникает много разговоров по поводу структур в воде. Сторонники этих представлений утверждают, что в воде формируются ажурные конструкции, подобные кристаллам, противники называют это лженаукой и ссылаются на известные всем сведения из учебников физики. Кто же прав, и что об этом говорит современная наука? Прежде всего, введем описание, что же мы понимаем под самим термином «структура».
Структура - это локализованный в определенных участках среды процесс. Иначе говоря, это - процесс, имеющий определенную геометрическую форму, способный к тому же перестраиваться и перемещаться в этой среде.
Даже в относительно простых математических моделях возникает идея фундаментальной общности различных структур и среды, их порождающей: любая среда содержит в потенциальной форме разные пути развития, разные виды локализации процессов, то есть разные виды структур. Это вывод из математических моделей, который в полной мере применим к воде и к характерным для нее процессам структурообразования. Водяные кластеры – это не застывшие в граните монументы, но динамические процессы, постоянно меняющиеся и постоянно воспроизводящие сами себя в бесконечном многообразии своих элементов.
Структура в применении к жидкостям имеет другой смысл по сравнению со структурой твердых тел [1]. В жидкостях молекулы должны постоянно двигаться, но они могут при этом сохранять некоторую упорядоченность, связываясь группами в так называемые некристаллические кластеры. В процессе теплового движения при комнатных температурах эти кластеры в течение длительного времени ведут себя как единое целое, перемещаясь по объему жидкости. Хотя это приводит к потере порядка на больших расстояниях, порядок на малых расстояниях все еще сохраняется. Как было показано методом дифракции медленных нейтронов, такой порядок на коротких расстояниях простирается, по крайней мере, на 10 Ангстрем, и до 15 Ангстрем в более упорядоченной переохлажденной тяжелой воде (D2O) [2]. Расстояние, на которое простирается ближний порядок, оказываются больше, когда имеется обширное водородное связывание.
При растворении веществ в воде вокруг их частиц: ионов, молекул, мелких ассоциатов, мицелл (крупных ассоциатов) образуются гидратные оболочки. Вокруг ионов, полярных молекул и мицелл возникает двухслойная гидратная оболочка, состоящая из плотного слоя молекул воды и рыхлого слоя. Плотный слой гидратной оболочки, можно считать, состоящим из связанных между собой водородными связями водных кластеров, структура которых специфична в зависимости от природы гидратируемой частицы. Среднее время жизни молекул воды в гидратной оболочке зависит от природы частицы, концентрации растворенных веществ и температуры. В частности, было показано, что пристеночная вода обладает другой структурой по сравнению с объемной водой, что дает дополнительный вклад в особенности движения воды по трубопроводам.
Кластеры, ассоциаты, илатраты являются элементами структурной организации воды. Предполагается, что из этих элементов путем самоорганизации возникают структуры, захватывающие всю толщу воды, и возникает процесс, аналогичный формированию решетки льда. В тоже время возможен другой взгляд на эту проблему. В течение многих лет группа итальянских физиков под руководством Джулио Препарата и Дель Гиудичи развивают представления о воде, как о квантовой кооперативной структуре. При этом основной упор делается не на геометрию отдельных кластеров, а на коллективные свойства воды, как единого целого. На основании строгих квантовомеханических расчетов показано, что при определенных условиях вода ведет себя как единая система, в которой все молекулы настраиваются на резонансную частоту и начинают вести себя как «организованная структура». По модели Препарата-Дель Гиудичи при комнатной температуре в воде присутствует «нормальная вода» + «организованная вода», причем последняя образует макроскопическую молекулярную структуру. Эта модель была экспериментально подтверждена при помощи спектров ядерного магнитного резонанса (ЯМР при В=3Тесла и tимп 2*10мс).
В настоящее время разрабатываются новые информативные методы исследования структурированной воды. Одним из перспективных является метод Газоразрядной Визуализации (ГРВ). Информативность метода ГРВ для исследования жидкофазных объектов была продемонстрирована при изучении свечения микробиологических культур [3], крови здоровых людей и онкологических больных [4], реакции крови на аллергены [5], гомеопатических препаратов 30С потенции [6] и цветочных эссенций [7], сверхмалых концентраций различных солей [8]. Большой интерес вызвали работы по выявлению различий в свечении натуральных и синтетических эфирных масел, имеющих одинаковый химический состав [9], а также натуральной и синтетической питьевой воды.
Литература
1. Martynov G. A., Structure of fluids from the statistical mechanics point of view, J. Mol. Liquids. 106, 2003, 123. 2. Dore J. C., Sufi M. A. and Bellissent-Funel M.C., Structural change in D2O water as a function of temperature; the isochoric temperature derivative function for neutron diffraction, Phys. Chem. Chem. Phys.2, 2000, 1599-1602. 3. Гудакова Г.З., Галынкин В.А., Коротков К.Г. Исследование фаз роста культур грибов рода CANDIDA методом газоразрядной визуализации (эффект Кирлиан). Микология и фитология. 1990. Т.24, N 2. С. 174. 4. Коротков К.Г., Гурвиц Б.Я., Крылов Б.А. Новый концептуальный подход к ранней диагностике рака. Сознание и физ. реальность. 1998. Т. 3, № 1, С. 51-58. 5. Л.П. Свиридов, А.В. Степанов, О.В. Хлопунова, К.Г. Коротков, Г.Г. Ахметели, С.А. Короткина, Э.В. Крыжановский. Регистрация реакции агглютинации с помощью метода газоразрядной визуализации. Современная микробиология – клинической медицине и эпидемиологии: материалы научной конференции, г. С.-Петерб., 21 мая 2003 г. СПб.: ВМедА., 2003, С. 32-33. 6. Bell I., Lewis D.A., Brooks A.J., Lewis S.E., Schwartz G.E. Gas Discharge Visualisation Evaluation of Ultramolecular Doses of Homeopathic Medicines Under Blinded, Controlled Conditions. J of Alternative and Complementary Medicine, 2003, 9, №1, рр. 25-37. 7. Коротков К. Загадки живого свечения. СПб. Издательство «Весь». 2003. 157 с. 8. К.Г Коротков Э.В. Крыжановский, С.А. Короткина, М.Б. Борисова, А. Вайншельбойм, П. Матраверс, К. Момох, М. Хайес, Н. Шаас. Исследование временных рядов характеристик газоразрядного свечения жидкофазных объектов. Изв. вузов. Приборостроение. 2003. Т45. N6. C.18-24. 9. Korotkov K., Krizhanovsky E., Borisova M., Hayes M., Matravers P., Momoh K.S., Peterson P., Shiozawa K., and Vainshelboim A. The Research of the Time Dynamics of the Gas Discharge Around Drops of Liquids. J of Applied Physics. 2004, v. 95, N 7, pp. 3334-3338.
www.finer.ru
Свойства и структура воды
Санкт-Петербургский государственный архитектурно-строительный университет
Кафедра химии
РЕФЕРАТ
Свойства и структура воды
Выполнил студент
группы 2-В-1
Горохов М. В.
Принял
доцент
Л. И. Акимов
Санкт-Петербург
1999
Содержание :
1. Введение. Вода в природе ............................................ 3
2. Структура воды ............................................................ 5
3. Свойства воды .............................................................. 11
4. Серебряная и талая вода ............................................. 20
5. Заключение .................................................................. 22
6. Литература .................................................................. 23
Введение. Вода в природе.
Самое важное для жизни – вода.
Вода имеет первостепенное значение при большинстве химических реакций, в частности и биохимических. Древнее положение алхимиков – «тела не действуют, пока не растворены» – в значительной степени справедливо.
Человеческий зародыш содержит воды, %: трехдневный - 97, трехмесячный - 91, восьмимесячный - 81. У взрослого человека доля воды в организме составляет 65%.
Человек и животные могут в своем организме синтезировать первичную ("ювенильную") воду, образовывать ее при сгорании пищевых продуктов и самих тканей. У верблюда, например, жир содержащийся в горбу, может путем окисления дать 40 л воды.
Связь между водой и жизнью столь велика, что даже позволила В. И. Вернадскому «рассматривать жизнь, как особую коллоидальную водную систему... как особое царство природных вод».
Количество воды, содержащейся в живых существа составляет в каждый данный момент громадную величину. Силами жизни в течение одного года перемещаются десятые доли процента всего океана, а в немногие сотни лет через живое вещество проходят массы воды, превышающие массу Мирового океана.
Геохимический состав океанической воды близок к составу крови животных и человека (см табл.).
Сравнительное содержание элементов в крови человека и в Мировом океане, %
Вода — весьма распространенное в природе вещество. 71 % поверхности земного шара покрыт водой, о бразующей океаны, моря, реки и озера. Много воды находится в газообразном состоянии в виде паров в атмосфере; в виде огромных масс снега и льда лежит она круглый год на вершинах высоких гор и в полярных странах. В недрах земли также находится вода, пропитывающая почву и горные породы. Общие запасы воды на Земле составляют 1454,3 млн. км3 (из них менее 2% относится к пресным водам, а доступны для использования 0,3%).
Природная вода не бывает совершенно чистой. Наиболее чис той является дождевая вода, но и она содержит незначительные к оличества различных примесей, которые захватывает из воздуха.
Количество примесей в пресных водах обычно лежит в пределах от 0,01 до 0,1% (масс.). Морская вода содержит 3,5% (масс.) рас творенных веществ, главную массу которых составляет хлорид натрия (поваренная соль).
Вода, содержащая значительное количество солей кальция и магния, называется жесткой в отличие от мягкой воды, например дождевой. Жесткая вода дает мало пены с мылом, а на стенках котлов образует накипь.
Чтобы освободить природную воду от взвешенных в ней частиц, е е фильтруют сквозь слой пористого вещества, например, угля, обожженной глины и т. п.
Фильтрованием можно удалить из воды только нерастворимые п римеси. Растворенные вещества удаляют из нее путем перегонки (дис тилляции) или ионного обмена.
Вода имеет очень большое значение в жизни растений, животн ых и человека. Во всяком организме вода представляе т собой среду, в которой протекают химические процессы, обеспечивающие жизнедеятельность организма; кроме т ого, она сама принимает участие в целом ряде биохимических реакций.
Вода - обязательный компонент практически всех технологических процессов как промышленного, так и сельскохозяйственного производства.
Структура воды
Английский физик Генри Кавендиш обнаружил, что водород Н и кислород О образуют воду. В 1785 г. французскими химиками Лавуазье и Менье было установлено, что вода состоит из двух весовых частей водорода и шестнадцати весовых частей кислорода.
Однако нельзя думать, что это представление, выражающееся химической формулой Н2 О, строго говоря, верно. Атомы водорода и кислорода, из которых состоит природная вода, или, точнее, окись водорода, могут иметь различный атомный вес и значительно отличаться друг от друга по своим физическим и химическим свойствам, хотя и занимают в периодической системе элементов одно и то же место.
Это так называемые изотопы. Известны пять различных водородов с атомными весами 1, 2, 3, 4, 5 и три различных кислорода с атомными весами 16, 17 и 18. В природном кислороде на 3150 атомов изотопа О16 приходится 5 атомов изотопа кислорода О17 и 1 атом изотопа кислорода О18 . В природном газообразном водороде на 5,5 тыс. атомов легкого водорода Н (протия) приходится 1 атом Н2 (дейтерия). Что касается Н3 (трития), а также Н4 и Н5 , то их в природной воде на Земле ничтожно мало, но участие их в космических процессах при низких температурах в межпланетном пространстве, в телах комет и т п. весьма вероятно.
Ядра атомов изотопов содержат одинаковое число протонов, но разное число нейтронов. Атомные массы изотопов различны.
Вокруг ядра атома водорода вращается один единственный электрон, поэтому атомный номер водорода равен единице. Этот электрон вращается по круговым орбитам, в совокупности образующим сферу. Орбит множество, и в зависимости от нахождения электрона на или иной круговой орбите у атома водорода может существовать множество энергетических состояний электрона, т. е. он может быть в спокойном или более или менее возбужденном состояниях.
У атома кислорода 8 электронов (атомный номер 8), 6 из которых движутся по наружным орбитам, представляющим форму восьмерки или гантели, и 2 по внутренней круговой орбите. В соответствии с количеством электронов в ядре атома кислорода 8 протонов, таким образом, сам атом в целом нейтрален.
Наиболее устойчивой наружной орбитой атома является состоящая из 8 электронов, а у кислорода их 6, т, е., не хватает 2 электронов. В то же время водород, как и кислород, существует в молекулах, содержащих 2 атома (Н2 ), связанных между собой двумя электронами, которые легко замещают вакансию двух электронов наружной орбиты атома кислорода, образуя в совокупности молекулу воды, с полной устойчивой восьмиэлектронной наружной
 орбитой (см рис 1.).
орбитой (см рис 1.). Рис 1. Схема образования молекулы воды (б) из 1 атома кислорода и 2 атомов водорода (а).
Можно привести много различных схем образования молекулы воды, основанных на представлениях разных физиков. По существу в них нет никаких противоречий и принципиальных различий. Ведь в действительности ни строения атомов, ни строения молекулы никто не видел, поэтому гипотетические схемы строятся лишь на основе косвенных наблюдаемых приборами признаков, позволяющих предположить как поведение, так и свойства атомов и молекул.
Размеры атомов различных элементов колеблются примерно от 0,6 до 2,6 А, а величины длины световой волны – в несколько тысяч раз больше: (4,5-7,7)*10-5 см. К тому же и атомы, и молекулы не имеют четких границ, чем и объясняется существующий разнобой вычисленных радиусов.
 При нормальных условиях следовало бы ожидать, что связи атома кислорода с обоими водородными атомами в молекуле Н2 О образуют у центрального атома кислорода очень тупой угол, близкий к 180°. Однако совершенно неожиданно этот угол равен не 180°, а всего лишь 104°31'. Вследствие этого внутримолекулярные силы компенсируются не полностью и их избыток проявляется вне молекулы. На рис. 2 показаны основные размеры молекулы воды.
При нормальных условиях следовало бы ожидать, что связи атома кислорода с обоими водородными атомами в молекуле Н2 О образуют у центрального атома кислорода очень тупой угол, близкий к 180°. Однако совершенно неожиданно этот угол равен не 180°, а всего лишь 104°31'. Вследствие этого внутримолекулярные силы компенсируются не полностью и их избыток проявляется вне молекулы. На рис. 2 показаны основные размеры молекулы воды. Рис 2. Молекула воды и ее размеры.
В молекуле воды положительные и отрицательные заряды распределены неравномерно, асимметрично. Такое расположение зарядов создает полярность молекулы. Хотя молекула воды нейтральна, но в силу своей полярности она ориентируется в пространстве с учетом тяготения своего отрицательно заряженного полюса к положительному заряду и положительно заряженного полюса к отрицательному заряду.
Внутри молекулы воды это разделение зарядов по сравнению с разделением зарядов у других веществ очень велико. Это явление называют дипольным моментом. Эти свойства молекул воды (называемые также диэлектрической проницаемостью, которая у Н2 О очень велика) имеют очень большое значение, например в процессах растворения различных веществ.
Способность воды растворять твердые тела определяется ее диэлектрической проницаемостью e, которая у воды при 0° С равна 87,7; при 50° С – 69,9; при 100° С - 55,7. При комнатной температуре диэлектрическая проницаемость равна 80. Это значит, что два противоположных электрических заряда взаимно притягиваются в воде, с силой, равной 1/80 силы их взаимодействия в воздухе. Таким образом, отделение ионов от кристалла какой-либо соли в воде в 80 раз легче, чем в воздухе.
Но вода состоит не только из одних молекул. Дело в том, что молекула воды может диссоциировать (расщепляться) на заряженный положительно ион водорода Н+ и на заряженный отрицательно гидроксильный ион ОН- . В обычных условиях чистая вода диссоциирована очень слабо: только одна молекула из 10 млн. молекул воды распадается на ион водорода и ион гидроксила. Однако с повышением температуры и изменением других условий диссоциация может быть значительно большей.
mirznanii.com
здоровье и процветание - Структура воды
Структурированная вода – это вода, имеющая структуру схожую со структурой воды в плазме крови или внутриклеточной жидкости. Такая вода обладает повышенной жизненной силой и энергией. Очищение не только воды, но и питательных растворов, поступающих в клетку, производится клеточными мембранами. Мембрана клетки не пропускает все подряд. Обычная вода усваивается лишь на 1%.В настоящее время доказано, что вода живой и мертвой клетки неодинакова. Лишь часть клеточной воды подвижна., а остальная ее часть “структурирована”. Клеточная цитоплазма похожа на желе, которое начинает “дрожать” в ответ на внешние воздействия.
Сейчас все более убедительна гипотеза С. В. Зинина, что вода представляет собой иерархию правильных объемных структур, в основе которых лежит кристаллоподобный “квант воды”, состоящий из 57 молекул. Такая структура энергетически выгодна и разрушается с освобождением свободных молекул лишь при определенных условиях.
“Кванты воды” могут взаимодействовать друг с другом за счет свободных водородных связей, как бы “торчащих” наружу из вершин кванта своими гранями. При этом возможно образование уже двух типов структур более высокого - уже второго порядка. Их взаимодействие друг с другом приводит к появлению структур высшего порядка. Последние состоят из 912 молекул воды и уже не способны к взаимодействию за счет образования водородных связей..
Этим и объясняется высокая текучесть жидкости, состоящей из громадных полимеров. Таким образом, водная среда представляет собой как бы иерархически организованный “жидкий кристалл”. За счет структуры подобного кристалла происходит запись на воду биополевой информации. Это один из самых важных параметров воды, имеющий большое
Современными методами исследований установлено, что в контакте с биологическими молекулами вода находится в особом состоянии и имеет структуру, аналогичную структуре льда. Именно такая структура воды дает возможность для протекания важнейших биофизических и биохимических реакций, т.к. живые молекулы организма находятся внутри такой структурированной воды..
В то же время обыкновенная питьевая вода представляет собой хаотическое скопление молекул, биологические молекулы сами непрочно расположены между молекулами такой воды и поэтому удерживают ее плохо. На необходимое структурирование обычной воды, для усвоения на клеточном уровне, организм тратит свою энергию. Достоверно установлено, что вода обладает памятью. При этом оказывается, что информация о пребывании в воде вредных ядовитых примесей не стирается при обычной угольной фильтрации и вода остается, по сути, “больной”.
Но идеальная структурированная вода есть в природе в родниках или талой воде.
Что касается минеральной воды, целебна она не только составом растворенных веществ, а в большей степени информацией, которую вода вобрала в себя, проходя через толщу земли. Выходя на поверхность, такая вода, ранее не имевшая контакта с солнечным светом резко активизируется. Слабое световое воздействие становится катализатором естественного природного процесса завершающего многоуровневое информационное структурирование воды на выходе из источника. Происходит эффективная комплексная многоуровневая запись положительной информации, что ведет к резкому усилению эффекта природного структурирования воды. Получающаяся вода становится индивидуально настроенной на человеческий организм. Исследования показали, что, радиус биополя для структурированной воды составляет 21 метр, и замеры в течение одного года показали его неизменность.
Издавна считалось, что употребление талой воды способствует омоложению организма. Талая вода отличается от обычной своей структурой, более сходной со структурой протоплазмы наших клеток. Свойства талой воды сохраняются до 12 часов. Получить талую воду можно, замораживая очищенную водопроводную воду в морозильной камере холодильника. Тем, кто страдает от головных болей, гипертонии, гастритами, колитами, излишним весом, а также всем, кто хочет продлить молодость и сохранить здоровье, рекомендую ежедневно пить талую воду или очищенную структурированную воду.
Существует много технологий получения структурированной воды: омагничивание, замораживание с последующим оттаиванием, процесс электролитического разделения воды на анолит («мертвая» вода) и католит («живая» вода), после чего образуется вода с новыми для нее свойствами, которые появляются не за счет химических воздействий, а за счет изменения волновых характеристик.
help-in-health.ru





















