Содержание
Температура кипения воды в обычных условиях, в горах при низком давлении, вакууме
Температуру кипения необходимо знать, потому что при ее достижении вода превращается в пар, то есть переходит из одного агрегатного состояния в другое.
Мы привыкли к тому, что в кипящей воде можно дезинфицировать посуду, варить продукты, но это не всегда так. В некоторых условиях температура жидкости будет слишком низкой для всего этого.
Не забудь поделиться с друзьями!
Содержание статьи
- Суть процесса
- Различные условия
- Кипение при повышенном давлении
- Кипение в вакууме
Суть процесса
Прежде всего надо определиться с понятием кипения. Что это такое? Это процесс, при котором вещество превращается в пар. Причем процесс этот происходит не только на поверхности, но и по всему объему вещества.
При кипении начинают образовываться пузырьки, внутри которых находится воздух и насыщенный пар. Шум закипающего чайника, кастрюли указывает на то, что пузырьки воздуха начали всплывать, затем опускаться и лопаться. Когда емкость хорошо прогреется со всех сторон, шум прекратится, значит, жидкость полностью закипела.
Шум закипающего чайника, кастрюли указывает на то, что пузырьки воздуха начали всплывать, затем опускаться и лопаться. Когда емкость хорошо прогреется со всех сторон, шум прекратится, значит, жидкость полностью закипела.
Процесс проходит при определенной температуре и давлении и является с точки зрения физики фазовым переходом первого рода.
Обратите внимание! Испарение может происходить при любой температуре, кипение же – при строго определенной.
В таблицах температура кипения воды или другой жидкости при нормальном атмосферном давлении приводится как одна из основных физических характеристик. Температура кипения (Тк) на самом деле равняется температуре пара, который находится в насыщенном состоянии прямо на границе между водой и воздухом. Сама вода, если быть точным, нагрета чуть-чуть больше.
На процесс кипения также ощутимо влияют:
- наличие в воде примесей газа;
- звуковые волны;
- ионизация.

Есть и другие факторы, заставляющие образовываться пузырьки быстрее или медленнее. Следует также отметить, что у каждых веществ своя Тк. Бытует мнение, что если добавить в воду соль, то она закипит быстрее. Это действительно так, но время изменится совсем немного. Для ощутимых результатов придется добавить очень много соли, что полностью испортит блюдо.
Различные условия
При нормальном атмосферном давлении (760 мм рт. ст., или 101 кПа, 1 атм.) вода начинает кипеть, нагревшись до 100 ℃. Это знают все.
Важно! Если внешнее давление увеличивать, то температура кипения тоже возрастет, а если уменьшать, то станет меньше.
Уравнение зависимости температуры кипения воды от давления довольно сложное. Зависимость эта не линейная. Иногда пользуются барометрической формулой для расчета, делая некоторые приближения, и уравнением Клапейрона-Клаузиуса.
Удобнее воспользоваться таблицами из справочников, в которых приведены данные, полученные экспериментальным путем. По ним можно построить график и, проведя экстраполяцию, вычислить требуемое значение.
В горах вода закипит, не успев нагреться до 100 ℃. На самой высокой вершине мира Джомолунгме (Эверест, высота над уровнем моря 8848 м) температура закипания воды равняется приблизительно 69 ℃. Но даже если опуститься немного ниже, то все равно вода будет кипеть не при ста градусах, пока мы не достигнем давления в 101 к Па. На Эльбрусе, который ниже Эвереста, чайник с водой закипит при 82 ℃ – там давление равно 0,5 атм.
Поэтому в горных условиях для приготовления пищи потребуется значительно больше времени, а некоторые продукты вообще не сварятся в воде, их придется готовить другим способом. Иногда неопытные туристы удивляются, почему яйца так долго варятся, а кипяток не обжигает. Все дело в том, что этот кипяток недостаточно нагрет.
В автоклавах и скороварках, наоборот, давление увеличивают. Это заставляет воду кипеть при более высокой температуре. Пища сильнее разогревается, и готовка происходит быстрее. Поэтому скороварки так и назвали. Нагрев до высокой температуры полезен еще и тем, что происходит дезинфекция жидкости, в ней погибают микробы.
Это заставляет воду кипеть при более высокой температуре. Пища сильнее разогревается, и готовка происходит быстрее. Поэтому скороварки так и назвали. Нагрев до высокой температуры полезен еще и тем, что происходит дезинфекция жидкости, в ней погибают микробы.
Кипение при повышенном давлении
Повышение давления приведет к увеличению Тк воды. При 15 атмосферах кипение начнется только при 200 градусах, при 80 атм. – 300 градусов. В дальнейшем рост температуры будет очень медленным. Максимальное значение стремится к 374,15 ℃, что соответствует 218,4 атмосферам.
Кипение в вакууме
Что будет, если воздух начнет все более и более разряжаться, стремясь к вакууму? Понятно, что температура кипения тоже начнет уменьшаться. И когда же сможет закипеть вода?
Если понизить давление до 10–15 мм рт. ст. (в 50–70 раз), то температура кипения уменьшится до 10–15 ℃. Такой водой можно охладиться.
Такой водой можно охладиться.
При дальнейшем снижении давления Тк будет уменьшаться и может достигнуть температуры замерзания. В этом случае в жидком состоянии вода просто не сможет существовать. Она будет переходить изо льда сразу в газ. Это случится примерно при 4,6 мм рт. ст.
Достичь абсолютного вакуума невозможно, но сильно разряженную атмосферу можно получить, если откачивать из сосуда с водой воздух. В результате такого эксперимента можно увидеть, когда именно закипает жидкость.
Давление понижается не только при откачке воздуха. Оно снижается возле быстро вращающегося винта, например, корабельного. В этом случае возле его поверхности тоже начинается кипение. Такой процесс назвали кавитацией. Во многих случаях такое явление нежелательно, но иногда оно приносит пользу. Так, кавитацию используют в биомедицине, промышленности и при очистке поверхностей ультразвуком.
что это такое, чему равна, от чего зависит, может ли закипеть при нагреве более или менее 100 градусов?
Содержание
- Что это такое?
- От чего зависит?
- Чему равна в нормальных условиях?
- Почему h3O закипает именно при 100 градусах?
- Может ли кипеть при нагреве более или менее 100С?
- Заключение
Что это такое?
Температура кипения воды – это граница ее фазового перехода из жидкого состояния в газообразное (пар). Причем в этот момент все тепло поглощается этим пограничным процессом, не позволяя воде продолжать греться. Она не нагревается выше 100С, в отличие от пара.
От чего зависит?
Это параметр зависим от следующих факторов:
- Нагрев. Он заставляет молекулы воды двигаться быстрее, постепенно уравнивая давление ее насыщенного пара с атмосферным.
При достаточном нагревании их значения выравниваются. В этот момент вода начинает кипеть.
- Давление окружающей среды – второй по значимости фактор после нагрева.
 Его сокращение снижает порог закипания.
Его сокращение снижает порог закипания. - Чистота воды незначительно, но влияет на ее закипание. Частицы посторонних включений тяжелее водяных, и для их разгона нужно больший разогрев. Поэтому чем сильнее загрязнение воды, тем выше граница ее закипания.
Чему равна в нормальных условиях?
Состояние, при котором давление составляет 760 мм. рт. ст (101,325 кПа) при 0С, принимают нормальным. Чистая вода в таком состоянии закипает при 100С.
Если выразить температуру кипения воды в этих системах, то она будет равна или 100С, или 475,15 оK или 212 оF. Эти величины равнозначны.
Почему h3O закипает именно при 100 градусах?
Нагрев приводит к отделению растворенного воздуха от h3O и образованию микроскопических пузырей. Чем горячее она становится, тем больше вырастает их объем и количество. При этом их пространство заполняется паром, давление которого также растет.
Постепенно пар становится насыщенным. Пузыри укрупняются и, ускоряясь, покидают воду.
Этому процессу свойственны следующие этапы:
- образование мелких пузырьков и их группировка на дне и стенках емкости;
- рост количества и объема пузырей, а также скорости их подъема на поверхность, что сопровождается характерным звуком;
- массовое всплытие и ускорение движения пузырьков вызывает усиление звука бурления и изменение его тональности.
На последней стадии объем паровых пузырей максимален. Давление пара и атмосферы соизмеримы, что и провоцирует фазовый переход и сильное бурление. Если значение давления атмосферы близко к нормальному, то описанный процесс протекает именно при 100С.
Может ли кипеть при нагреве более или менее 100С?
Из вышесказанного следует утвердительный ответ. Достаточно искусственно повысить давление, окружающее воду, или растворить в ней какое-нибудь вещество. Опыт показывает, что температура кипения воды повысится на 1С при добавлении в ее состав 40 граммов пищевой соли.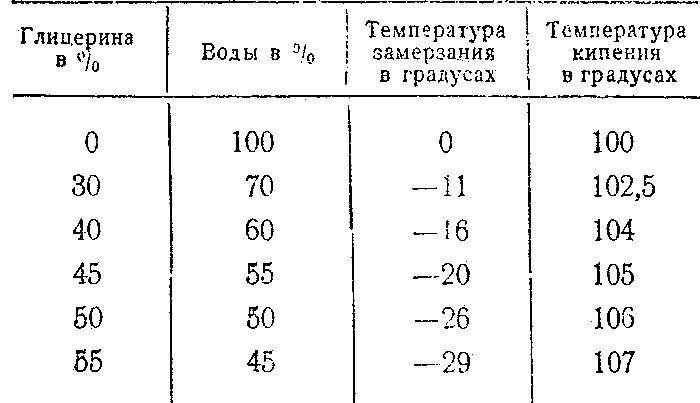
Напротив, в разряженном воздухе температура закипания снижается (ориентировочно около 0,2С на каждые 5 мм. рт. ст.).
Так на высоте 4000 м. над уровнем моря вода закипит при 80С. На этом уровне разреженность атмосферы составляет 357 мм. рт. ст. или 47,6 кПа.
Заключение
Теперь можно утверждать, что температура кипения воды не является незыблемой константой. Поэтому неудивительно, что на Эвересте она составляет порядка 69 градусов. Напротив, океаническая вода закипает только при 101С по причине своей солености.
Каноническое же значение, равное 100С, подразумевает проведение измерения с кристально чистой h3O и нормальным давлением. Разумеется, соблюсти оба требования на практике принципиально невозможно.
А какова Ваша оценка данной статье?
Загрузка…
точка кипения воды против высоты
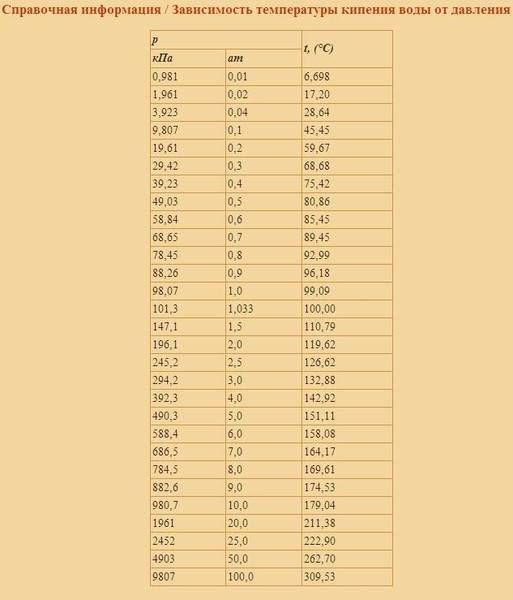
Точка кипения воды уменьшается с высотой:
| Высота — по сравнению с уровнем моря | . (m) (m) | ( o F) | ( o C) | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| -1000 | -305 | 213.9 | 101.1 | ||||||||||
| -750 | -229 | 213.5 | 100.8 | ||||||||||
| -500 | -152 | 213.0 | 100.5 | ||||||||||
| -250 | -76 | 212.5 | 100.3 | ||||||||||
| 0 | 0 | 212.0 | 100.0 | ||||||||||
| 250 | 76 | 211.5 | 99.7 | ||||||||||
| 500 | 152 | 211.0 | 99.5 | ||||||||||
| 750 | 229 | 210.5 | 99.2 | ||||||||||
| 1000 | 305 | 210.1 | 98.9 | ||||||||||
| 1250 | 381 | 209.6 | 98.6 | ||||||||||
| 1500 | 457 | 209. 1 1 | 98,4 | ||||||||||
| 1750 | 533 | 208.6 | 98.1 | ||||||||||
| 98.1 | |||||||||||||
| 98.1 | |||||||||||||
| 98.1 | |||||||||||||
| 98.1 | |||||||||||||
| 98.1 | |||||||||||||
| 610 | 208.1 | 97.8 | |||||||||||
| 2250 | 686 | 207.6 | 97.6 | ||||||||||
| 2500 | 762 | 207.2 | 97.3 | ||||||||||
| 2750 | 838 | 206.7 | 97.1 | ||||||||||
| 3000 | 914 | 206.2 | 96.8 | ||||||||||
| 3250 | 991 | 205.7 | 96.5 | ||||||||||
| 3500 | 1067 | 205.3 | 96.3 | ||||||||||
| 3750 | 1143 | 204.8 | 96.0 | ||||||||||
| 4000 | 1219 | 204. 3 3 | 95.7 | ||||||||||
| 4250 | 1295 | 203,8 | 95,5 | ||||||||||
| 4500 | 1372 | 203,4 | 95.2 | ||||||||||
| 4750 | 202.9 | 94.9 | |||||||||||
| 5000 | 1524 | 202.4 | 94.7 | ||||||||||
| 5250 | 1600 | 202.0 | 94.4 | ||||||||||
| 5500 | 1676 | 201.5 | 94.2 | ||||||||||
| 5750 | 1753 | 201.0 | 93.9 | ||||||||||
| 6000 | 1829 | 200.6 | 200.6 | 200.6 | 200.6 | 200.6 | |||||||
| 6250 | 1905 | 200.1 | 93.4 | ||||||||||
| 6500 | 1981 | 199.6 | 93.1 | ||||||||||
| 6750 | 2057 | 199. 2 2 | 92.9 | ||||||||||
| 7000 | 2134 | 198,7 | 92,6 | ||||||||||
| 7250 | 2210 | 198,2 | 92,4 | ||||||||||
| 7500 | 2286 | ||||||||||||
| 7500 | 2286 | ||||||||||||
| 7500 | 2286 | ||||||||||||
| 7500 | 2286 | ||||||||||||
| 7500 | 2286 | ||||||||||||
| 7500 | 2286 | ||||||||||||
| 7500 | 2286 | 197.8 | 92.1 | ||||||||||
| 7750 | 2362 | 197.3 | 91.8 | ||||||||||
| 8000 | 2438 | 196.9 | 91.6 | ||||||||||
| 8250 | 2515 | 196.4 | 91.3 | ||||||||||
| 8500 | 2591 | 196.0 | 91.1 | ||||||||||
| 8750 | 2667 | 195.5 | 90.8 | 195.5 | 90.8 | ||||||||
| 9000 | 2743 | 195.0 | 90.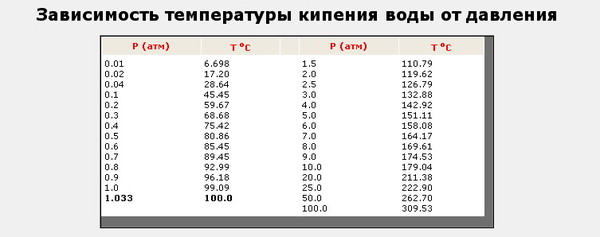 6 6 | ||||||||||
| 9250 | 2819 | 194.6 | 90.3 | ||||||||||
| 9500 | 2896 | 194.1 | 90.1 | ||||||||||
| 9750 | 2972 | 193,7 | 89,8 | ||||||||||
| 10000 | 3048 | 193,2 | 89,6 | ||||||||||
| 10250 | 3124 | ||||||||||||
| 10250 | 3124 | 192.8 | 89.3 | ||||||||||
| 10500 | 3200 | 192.3 | 89.1 | ||||||||||
| 10750 | 3277 | 191.9 | 88.8 | ||||||||||
| 11000 | 3353 | 191.4 | 88.6 | ||||||||||
| 11250 | 3429 | 191.0 | 88,3 | ||||||||||
| 11500 | 3505 | 190,5 | 88.1 | 190,5 | 88.1 | 190,5 | 88.1 | 0016 | |||||
| 11750 | 3581 | 190. 1 1 | 87.8 | ||||||||||
| 12000 | 3658 | 189.7 | 87.6 | ||||||||||
| 12250 | 3734 | 189.2 | 87.3 | ||||||||||
| 12500 | 3810 | 188,8 | 87,1 | ||||||||||
| 12750 | 3886 | 188,3 | 86,8 | ||||||||||
| 13000 | 3962 | 187.9 | 86.6 | ||||||||||
| 13250 | 4037 | 187.4 | 86.4 | ||||||||||
| 13500 | 4115 | 187.0 | 86.1 | ||||||||||
| 13750 | 4191 | 186.6 | 85.9 | ||||||||||
| 14000 | 4267 | 186.1 | 85,6 | ||||||||||
| 14250 | 4343 | 185,7 | 85,4 9 | 185,7 | 85,4 9 9930043 | ||||||||
| 14500 | 4420 | 185.3 | 85.1 | ||||||||||
| 14750 | 4496 | 184. 8 8 | 84.9 | ||||||||||
| 15000 | 4572 | 184.4 | 84.7 | ||||||||||
| 15250 | 4648 | 184.0 | 84,4 | ||||||||||
| 15500 | 4724 | 183,5 | 84,2 | ||||||||||
| 15750 | |||||||||||||
| 15750 | 15750 | 15750 | 0042 4801 | 183.1 | 83.9 | ||||||||
| 16000 | 4877 | 182.7 | 83.7 | ||||||||||
| 16250 | 4953 | 182.2 | 83.5 | ||||||||||
| 16500 | 5029 | 181.8 | 83.2 | ||||||||||
| 16750 | 5105 | 181.4 | 83.0 | ||||||||||
| 17000 | 5182 | 180.9 | 82.7 | 180.9 | 82.7 | 180.9 | 82.7 | 180.9 | 82.0043 | ||||
| 17250 | 5258 | 180. 5 5 | 82.5 | ||||||||||
| 17500 | 5334 | 180.1 | 82.3 | ||||||||||
| 17750 | 5410 | 179.7 | 82.0 | ||||||||||
| 18000 | 5486 | 179,2 | 81,8 | ||||||||||
| 18250 | 5563 | 178,8 | 81,6 | ||||||||||
| 18500 | 178.4 | 81.3 | |||||||||||
| 18750 | 5715 | 178.0 | 81.1 | ||||||||||
| 19000 | 5791 | 177.6 | 80.9 | ||||||||||
| 19250 | 5867 | 177.1 | 80.6 | ||||||||||
| 19500 | 5944 | 176.7 | 80.4 | ||||||||||
| 19750 | 6020 | 176.3 | 80.2 | ||||||||||
| 20000 | 6096 | 175.9 | 79.9 | ||||||||||
| 20250 | 6172 | 175. 5 5 | 79.7 | ||||||||||
| 20500 | 6248 | 175.1 | 79.5 | ||||||||||
| 20750 | 6325 | 174,7 | 79,3 | ||||||||||
| 21000 | 6401 | 174.2 | 79,0 | ||||||||||
| 21250 | 173.8 | 78.8 | |||||||||||
| 21500 | 6553 | 173.4 | 78.6 | ||||||||||
| 21750 | 6629 | 173.0 | 78.3 | ||||||||||
| 22000 | 6706 | 172.6 | 78.1 | ||||||||||
| 22250 | 6782 | 172.2 | 77,9 | ||||||||||
| 22500 | 6858 | 171.8 | 77.7 977 9008 | 171.8 | 77.7 97.7 977.7 977 977 977 977 | 171.8 | 77.7 77.7 977 977.7 | ||||||
| 22750 | 6934 | 171.4 | 77.4 | ||||||||||
| 23000 | 7010 | 171. 0 0 | 77.2 | ||||||||||
| 23250 | 7087 | 170.6 | 77.0 | ||||||||||
| 23500 | 7163 | 170,2 | 76,8 | ||||||||||
| 23750 | 7239 | 169,8 | 76,5 | ||||||||||
| 24000 | 169.4 | 76.3 | |||||||||||
| 24250 | 7391 | 169.0 | 76.1 | ||||||||||
| 24500 | 7468 | 168.6 | 75.9 | ||||||||||
| 24750 | 7544 | 168.2 | 75.6 | ||||||||||
| 25000 | 7620 | 167,8 | 75,4 | ||||||||||
| 25250 | 7696 | 167.4 | 75,2 | 167.4 | 75,2 | 167.4 | 75,2 | 167.4 | 75,2 | ||||
| 25500 | 7772 | 167.0 | 75.0 | ||||||||||
| 25750 | 7849 | 166. 6 6 | 74.8 | ||||||||||
| 26000 | 7925 | 166.2 | 74.5 | ||||||||||
| 26250 | 8001 | 165,8 | 74,3 | ||||||||||
| 26500 | 8077 | 165,4 | 74,1 | ||||||||||
| 26750 | |||||||||||||
| 26750 | 8153 | 165.0 | 73.9 | ||||||||||
| 27000 | 8230 | 164.6 | 73.7 | ||||||||||
| 27250 | 8306 | 164.2 | 73.5 | ||||||||||
| 27500 | 8382 | 163.8 | 73.2 | ||||||||||
| 27750 | 8458 | 163.4 | 73.0 | ||||||||||
| 28000 | 8534 | 163.1 | 72.8 | 163.1 | 72.8 | 163.1 | 72.8 | 163.1 | 720043 | ||||
| 28250 | 8611 | 162.7 | 72.6 | ||||||||||
| 28500 | 8687 | 162. 3 3 | 72.4 | ||||||||||
| 28750 | 8763 | 161.9 | 72.2 | ||||||||||
| 29000 | 8839 | 161,5 | 72,0 | ||||||||||
| 29250 | 8916 | 161,1 | 71,7 | ||||||||||
| 29500 | |||||||||||||
| 29500 | 160.7 | 71.5 | |||||||||||
| 29750 | 9068 | 160.4 | 71.3 | ||||||||||
| 30000 | 9144 | 160.0 | 71.1 | ||||||||||
Example — Boiling Point of Water at the вершина горы Эверест
Высота горы Эверест в Непале составляет 8848 м .
Согласно приведенной выше таблице температура кипения воды составляет ок. 72 о С (161,5 или F) .
Температура кипения и замерзания чистой и соленой воды | Физика Фургон
Категория
Выберите категориюО фургоне физикиЭлектричество и магнитыВсе остальноеСвет и звукДвижение вещейНовая и захватывающая физикаСостояния материи и энергииКосмосПод водой и в воздухе
Подкатегория
Поиск
Задайте вопрос
Последний ответ: 22.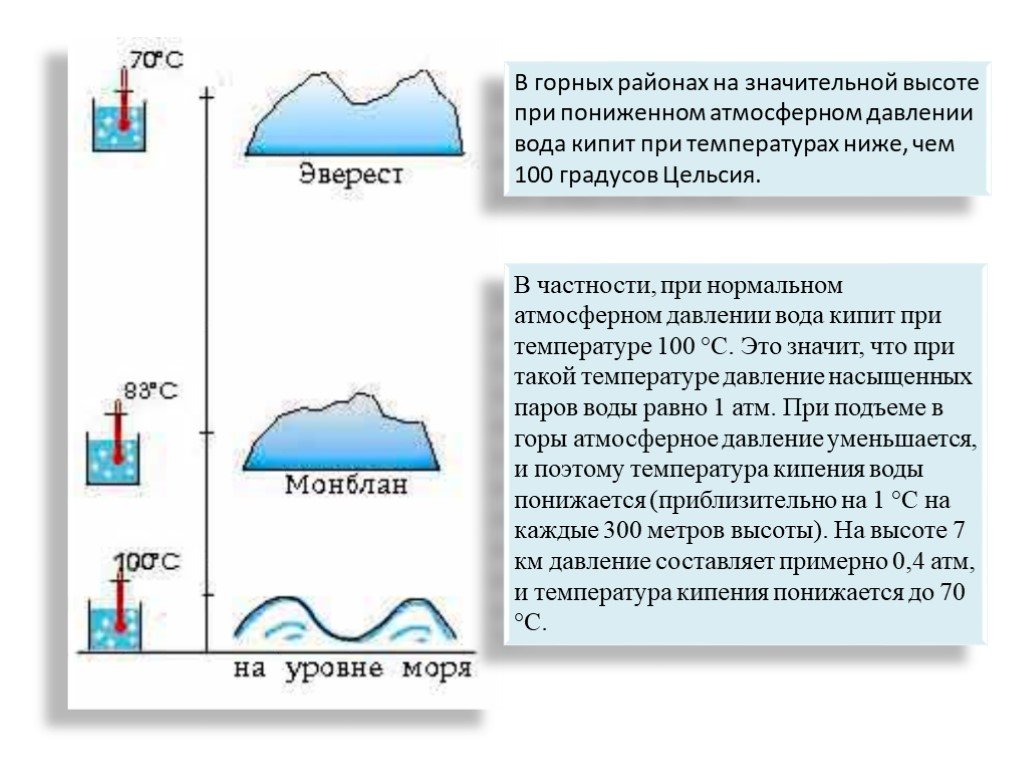 10.2007
10.2007
Q:
Какова температура кипения и замерзания пресной и морской воды?
— мария (13 лет)
конгресс мидл, лейк ворт, Флорида
A:
Привет, Мария,
Температура кипения чистой воды составляет 100 градусов по Цельсию (212 по Фаренгейту) при давлении в одну атмосферу, и температура плавления составляет 0 градусов Цельсия (32 градуса по Фаренгейту) при давлении в одну атмосферу. На больших высотах более низкое давление снижает температуру кипения на несколько градусов. Например, в Денвере, штат Колорадо, температура кипения составляет около 95°C или 203°F.
Для соленой воды температура кипения повышается, а температура плавления понижается. На сколько зависит от того, сколько там соли. Я предполагаю, что соль представляет собой хлорид натрия, NaCl (поваренная соль). Температура плавления понижается на 1,85 градуса Цельсия, если 29,2 г соли растворяются в каждом кг воды (так называемый «0,5-моляльный раствор» соли). соли, имеется 1,0 молярная концентрация ионов).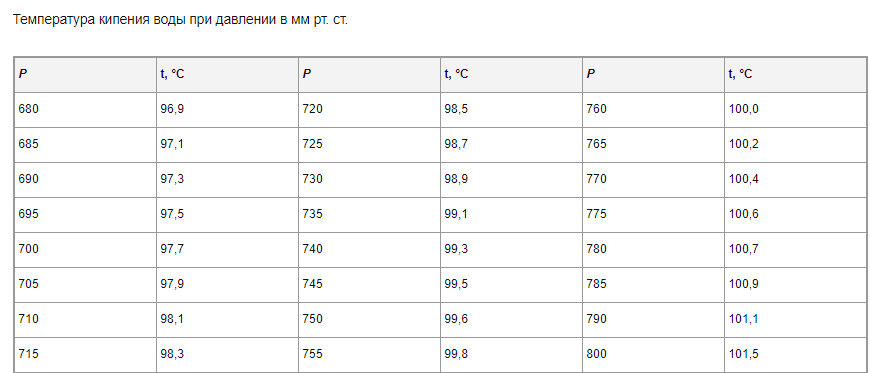 Температура кипения повышается на 0,5 градуса Цельсия у воды с 29.2 грамма соли растворено в каждом кг воды.
Температура кипения повышается на 0,5 градуса Цельсия у воды с 29.2 грамма соли растворено в каждом кг воды.
Если у вас разные концентрации соли, то вы можете масштабировать предсказания повышения точки кипения и понижения точки плавления непосредственно с концентрацией.
Эти номера взяты из CRC Handbook of Chemistry and Physics.
Том
(опубликовано 22.10.2007)
Дополнение №1: давление и замерзание
Вопрос:
Повышение давления воды повышает ее температуру кипения повышает ли она температуру замерзания
— Гарри
Масуэллбрук, Новый Южный Уэльс, Австралия
A:
Повышение давления на самом деле немного снижает температуру замерзания воды. Это связано с тем, что лед занимает больший объем, чем жидкая вода, поэтому при сжатии он становится жидким.
Это довольно необычно для точек замерзания, поскольку для большинства веществ твердое тело занимает меньше места, чем жидкость.
Майк В.
(опубликовано 22.10.2007)
Дополнение №2: эффективное соление воды
Q:
Итак, после вывода о том, что соленая вода имеет более высокую температуру кипения, чем пресная вода, возникает вопрос;
С точки зрения энергопотребления, когда добавлять соль в воду при тушении спагетти?
то есть; если я добавлю соль в воду, пока она еще холодная, потребуется больше энергии, чтобы заставить ее закипеть?
Если я добавлю его, когда вода закипит при 100 ° C, вода перестанет кипеть, и ей нужно будет потреблять больше энергии, чтобы достичь новой точки кипения?
В конце концов, такая же энергия требуется для приготовления порции спагетти, как я полагаю? 🙂
— Джейкоб Хансен (39 лет)
Нествед, Дания
A:
Вы в основном правы. В любом случае вы начинаете с простой воды и соли комнатной температуры. Лапша идет, когда у вас есть соленая вода в ее точке кипения. Разница в энергии между этим и начальной точкой не зависит от того, когда вы добавляете соль.
Однако по дороге на испарение теряется немного энергии. Если вы подождете, пока вода закипит, затем добавите соль, а затем снова закипите, вода будет находиться на грани кипения немного дольше, чем если бы вы сначала добавили соль. Таким образом, вы теряете немного больше энергии. Немного эффективнее сначала добавить соль.
Mike W.
(опубликовано 18.06.2009)
Дополнение №3: кипячение соленой воды литр кухонной водопроводной воды, чтобы температура кипения увеличилась выше 100 градусов по Цельсию?
*******
Я отчаянно нуждаюсь в ответе, потому что это задание
если вы не можете дать ответ, у вас есть идеи о некоторых полезных веб-сайтах, которые могут мне помочь?
С уважением
аноним
— анонимно
Австралия
A:
Я отметил ваш вопрос как продолжение вопроса, на который уже был ответ. Любое количество соли повысит температуру кипения выше 100°C. Вопрос в том, насколько выше того, что вы хотите получить. Ответ выше должен помочь в этом.
Ответ выше должен помочь в этом.
Mike W.
(опубликовано 21.04.2011)
Дополнение №4: соль, образующая пар
Q:
Теперь я в замешательстве. Всякий раз, когда я кипятлю воду для макарон, я добавляю соль, когда с нетерпением жду, пока она закипит. Когда я добавляю соль, когда она близка к кипению, она мгновенно закипает. Это полная противоположность тогдашней физике, описываемой здесь. Это из-за другой фуномины? Обеспечивает ли соль точку для образования ядра пара?
— Люк (30 лет)
Бостон
A:
Точно, вы догадались.
Mike W.
(опубликовано 17.01.2012)
Дополнение №5: Использование соли в увлажнителях
Вопрос:
поместите как можно больше воды в воздух. Это один из дешевых увлажнителей, который кипятит воду и производит пар. Кажется, я читал в инструкциях, что если добавить щепотку соли, в воздухе будет больше воды. Как это сработает? Я имею в виду, что это повысит температуру кипения, поэтому, возможно, вода станет горячее, например, 103 градуса по Цельсию, но похоже, что кипятить придется дольше. Как только он достигает 103, почему выходит больше пара, чем при 100?
Как только он достигает 103, почему выходит больше пара, чем при 100?
— Джон (45 лет)
Оверленд Парк Канзас, США
Ответ:
Я пользуюсь таким увлажнителем. Добавление соли работает. Нагрев происходит за счет электрического тока, протекающего через воду. Водопроводная вода имеет довольно низкую проводимость, поэтому по ней течет не так много тока. Добавление соли повышает проводимость, поскольку ионы электрически заряжены. На самом деле вам нужно быть немного осторожным, чтобы не добавить слишком много соли, так как вы не хотите перегореть.
Влияние на температуру кипения очень незначительно по сравнению с влиянием на проводимость.
Кстати, несмотря на то, что эти увлажнители дешевы, у них есть приятное преимущество: поскольку они выпускают водяной пар, а не капли, вам не нужно беспокоиться о попадании бактерий и т. д. в воздух.
Майк В.
(опубликовано 24.02.2014)
Дополнение №6: высота над уровнем моря и точка кипения
Вопрос:
«на пару градусов» ниже в таких городах, как Денвер (который находится на той же высоте, что и мой город, Альбукерке).

 Его сокращение снижает порог закипания.
Его сокращение снижает порог закипания.