5. Требования к воде очищенной, регламентируемые различными фармакопеями. Фармакопейная вода
ФС.2.2.0019.15 Вода для инъекций | Фармакопея.рф
Содержимое (Table of Contents)
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФАРМАКОПЕЙНАЯ СТАТЬЯ
Вода для инъекций ФС.2.2.0019.15
Вода для инъекций Взамен ГФ Х, ст. 74;
Aqua per injectionis взамен ФС 42-2620-97
Н2О М. м. 18,02
Настоящая фармакопейная статья распространяется на нефасованную воду для инъекций, получаемую из воды питьевой методами дистилляции, ионного обмена, обратного осмоса, комбинацией этих методов или другим способом, или из воды, очищенной методом дистилляции, и предназначенную для производства или изготовления парентеральных и других лекарственных средств.
При использовании воды для инъекций в технологии парентеральных и других лекарственных средств, получаемых непосредственно перед применением, в условиях, исключающих последующую стерилизацию лекарственных препаратов, вода для инъекций должна быть стерильной.
Вода для инъекций должна быть апирогенной и не должна содержать антимикробных консервантов или других добавок.
Описание
Бесцветная прозрачная жидкость без запаха.
рН
От 5,0 до 7,0 (ОФС «Ионометрия», метод 3). К 100 мл воды очищенной прибавляют 0,3 мл насыщенного раствора калия хлорида.
Кислотность или щелочность
К 20 мл воды для инъекций прибавляют 0,05 мл 0,1 % раствора фенолового красного. При появлении желтого окрашивания оно должно измениться на красное от прибавления не более 0,1 мл 0,01 М раствора натрия гидроксида. При появлении красного окрашивания оно должно измениться на желтое от прибавления не более 0,15 мл 0,01 М раствора хлористоводородной кислоты.
Электропроводность
Определение проводят в соответствии с ОФС «Электропроводность» с помощью оборудования – кондуктометров, внесенных в Государственный реестр средств измерений.
Оборудование
Кондуктометрическая ячейка:
— электроды из подходящего материала, такого как нержавеющая сталь;
— константа ячейки обычно устанавливается поставщиком и впоследствии проверяется через соответствующие интервалы времени с использованием сертифицированного стандартного раствора с электропроводностью менее 1500 мкСм/см или путем сравнения с ячейкой, имеющей аттестованную константу ячейки. Константа ячейки считается подтвержденной, если найденное значение находится в пределах 2 % от значения, указанного в сертификате; в противном случае должна быть проведена повторная калибровка.
Кондуктометр. Точность измерения должна быть не менее 0,1 мкСм/см в низшем диапазоне.
Калибровка системы (ячейки электропроводности и кондуктометра). Калибровка должна проводиться с использованием одного или более соответствующих стандартных растворов (ОФС «Электропроводность»). Допустимое отклонение должно составлять не более 3 % от измеренного значения электропроводности.
Калибровка кондуктометра. Калибровку кондуктометра проводят с использованием сопротивлений высокой точности или эквивалентным прибором после отсоединения ячейки электропроводности для всех интервалов, использующихся для измерения электропроводности и калибровки ячейки, с погрешностью не более 0,1 % от сертифицированной величины.
В случае невозможности отсоединения ячейки электропроводности, вмонтированной в производственную линию, калибровка может быть проведена относительно предварительно калиброванной ячейки электропроводности, помещенной в поток воды рядом с калибруемой ячейкой.
Методика
Стадия 1
Измеряют электропроводность без температурной компенсации с одновременной регистрацией температуры. Измерение электропроводности с помощью кондуктометров с температурной компенсацией возможно только после соответствующей валидации.
Находят ближайшее значение температуры (табл. 1), меньше измеренного. Соответствующая величина электропроводности является предельно допустимой.
Вода для инъекций соответствует требованиям, если измеренное значение электропроводности не превышает найденного по табл. 1 предельно допустимого значения.
Таблица 1 – Предельно допустимые значения электропроводности воды для инъекций в зависимости от температуры
| Температура, ºС | Электропроводность, мкСм/см | Температура, ºС | Электропроводность, мкСм/см |
| 0 | 0,6 | 55 | 2,1 |
| 5 | 0,8 | 60 | 2,2 |
| 10 | 0,9 | 65 | 2,4 |
| 15 | 1,0 | 70 | 2,5 |
| 20 | 1,1 | 75 | 2,7 |
| 25 | 1,3 | 80 | 2,7 |
| 30 | 1,4 | 85 | 2,7 |
| 35 | 1,5 | 90 | 2,7 |
| 40 | 1,7 | 95 | 2,9 |
| 45 | 1,8 | 100 | 3,1 |
| 50 | 1,9 |
Для значений температур, не представленных в табл. 1, рассчитывают максимально допустимое значение электропроводности путем интерполяции ближайших к полученному верхнему и нижнему значениям, приведенным в табл. 1.
Если величина электропроводности превышает приведенное в табл. 1 значение, продолжают испытания в соответствии с требованиями стадии 2.
Стадия 2
Не менее 100 мл воды для инъекций помещают в сосуд и перемешивают. При постоянном перемешивании устанавливают температуру в пределах 25 ± 1 ºС и измеряют электропроводность через каждые 5 мин до тех пор, пока изменение электропроводности за 5 мин не составит менее0,1 мкСм/см. Фиксируют это значение электропроводности.
Вода для инъекций удовлетворяет требованиям, если полученное значение электропроводности составляет не более 2,1 мкСм/см.
Если значение электропроводности более 2,1 мкСм/см, проводят испытания в соответствии с требованиями стадии 3.
Стадия 3
Испытание выполняют в течение приблизительно 5 мин после проведения испытания по стадии 2, поддерживая температуру в пределах25 ± 1 ºС. Прибавляют свежеприготовленный насыщенный раствор калия хлорида к воде для инъекций (0,3 мл на 100 мл воды для инъекций) и определяют pH с точностью до 0,1.
Определяют предельное значение электропроводности (табл. 2) для данного рН.
Вода для инъекций удовлетворяет требованиям по электропроводности, если величина электропроводности, полученная на стадии 2, не превышает значения, приведенного в табл. 2. Если полученная на стадии 2 величина электропроводности превышает значение, приведенное в табл. 2, или значение рН находится за пределами диапазона 5,0–7,0, то вода для инъекций не соответствует требованиям по показателю «Электропроводность».
Таблица 2 – Предельно допустимые значения электропроводности воды для инъекций в зависимости от рН
| рН | Электропроводность, мкСм/см | рН | Электропроводность, мкСм/см |
| 5,0 | 4,7 | 6,1 | 2,4 |
| 5,1 | 4,1 | 6,2 | 2,5 |
| 5,2 | 3,6 | 6,3 | 2,4 |
| 5,3 | 3,3 | 6,4 | 2,3 |
| 5,4 | 3,0 | 6,5 | 2,2 |
| 5,5 | 2,8 | 6,6 | 2,1 |
| 5,6 | 2,6 | 6,7 | 2,6 |
| 5,7 | 2,5 | 6,8 | 3,1 |
| 5,8 | 2,4 | 6,9 | 3,8 |
| 5,9 | 2,4 | 7,0 | 4,6 |
| 6,0 | 2,4 |
Сухой остаток
Не более 0,001 %. 100 мл воды для инъекций выпаривают досуха и сушат при температуре от 100 до 105 ºС до постоянной массы.
Восстанавливающие вещества
100 мл воды для инъекций доводят до кипения, прибавляют 0,1 мл 0,02 М раствора калия перманганата и 2 мл серной кислоты разведенной 16 %, кипятят 10 мин; розовое окрашивание должно сохраниться.
Углерода диоксид
При взбалтывании воды для инъекций с равным объемом раствора кальция гидроксида (известковой воды) в наполненном доверху и хорошо закрытом сосуде не должно быть помутнения в течение 1 ч.
Нитраты и нитриты
К 5 мл воды для инъекций осторожно прибавляют 0,1 мл свежеприготовленного раствора дифениламина; не должно появляться голубое окрашивание.
Аммоний
Не более 0,00002 % (ОФС «Аммоний»). Определение проводят с использованием эталонного раствора, содержащего 1 мл стандартного раствора аммоний-иона (2 мкг/мл) и 9 мл воды, свободной от аммиака. Для определения отбирают 10 мл испытуемой пробы.
Примечание. Стандартный раствор аммоний-иона (2 мкг/мл) готовят разбавлением стандартного раствора аммоний-иона (200 мкг/мл) водой, свободной от аммиака.
Хлориды
К 10 мл воды для инъекций прибавляют 0,5 мл азотной кислоты, 0,5 мл 2 % раствора серебра нитрата, перемешивают и оставляют на5 мин. Не должно быть опалесценции.
Сульфаты
К 10 мл воды для инъекций прибавляют 0,5 мл хлористоводородной кислоты разведенной 8,3 % и 0,1 мл 5 % раствора бария хлорида, перемешивают и оставляют на 10 мин. Не должно быть помутнения.
Кальций и магний
К 100 мл воды для инъекций прибавляют 2 мл буферного раствора аммония хлорида, рН 10,0, 50 мг индикаторной смеси протравного черного 11 и 0,5 мл 0,01 М раствора натрия эдетата; должно наблюдаться чисто синее окрашивание раствора (без фиолетового оттенка).
Алюминий
Не более 0,000001 % (ОФС «Алюминий», метод 1).
Испытуемый раствор. К 400 мл воды очищенной прибавляют 10 мл ацетатного буферного раствора, рН 6,0 и 100 мл воды дистиллированной, перемешивают.
Эталонный раствор. К 2 мл стандартного раствора алюминий-иона(2 мкг/мл) прибавляют 10 мл ацетатного буферного раствора, рН 6,0 и 98 мл воды дистиллированной, перемешивают.
Контрольный раствор. К 10 мл ацетатного буферного раствора, рН 6,0 прибавляют 100 мл воды дистиллированной и перемешивают.
Тяжелые металлы
Не более 0,00001 %.
Определение проводят одним из приведенных методов.
Метод 1. В пробирку диаметром около 1,5 см помещают 10 мл испытуемой воды для инъекций, прибавляют 1 мл уксусной кислоты разведенной 30 %, 2 капли 2 % раствора натрия сульфида и перемешивают. Через 1 мин производят наблюдение окраски раствора по оси пробирки, помещенной на белую поверхность. Не должно быть окрашивания.
Метод 2. 120 мл воды для инъекций упаривают до объёма 20 мл. Оставшаяся после упаривания вода в объеме 10 мл должна выдерживать испытание на тяжёлые металлы (ОФС «Тяжелые металлы») с использованием эталонного раствора, содержащего 1 мл стандартного раствора свинец-иона (5 мкг/мл) и 9 мл испытуемой воды для инъекций.
Примечание. Стандартный раствор свинец-иона (5 мкг/мл) готовят разбавлением стандартного раствора свинец-иона (100 мкг/мл) испытуемой водой для инъекций.
Микробиологическая чистота
Общее число аэробных микроорганизмов (бактерий и грибов) не более 10 КОЕ в 100 мл. Не допускается наличие Еscherichia coli, Staphylococcus aureus, Pseudomonas aeruginosa в 100 мл.
Для анализа микробиологической чистоты воды для инъекций отбирают образец в объеме не менее 1000 мл.
Исследование проводят методом мембранной фильтрации в асептических условиях в соответствии с методами ОФС «Микробиологическая чистота», п.12.
Бактериальные эндотоксины
Менее 0,25 ЕЭ/мл (ОФС «Бактериальные эндотоксины»).
Хранение и распределение
Воду для инъекций хранят и распределяют в условиях, предотвращающих рост микроорганизмов и исключающих возможность любой другой контаминации.
Хранение воды для инъекций осуществляют в специальных сборниках при условии постоянной циркуляции при температуре не ниже 85 ºС, в течение не более 1 сут.
Скачать в PDF ФС.2.2.0019.15 Вода для инъекций
Поделиться ссылкой:
pharmacopoeia.ru
16 Июля 1997 г.
N 214
О контроле качества лекарственных средств, изготовляемых в аптечных организациях (аптеках)
В целях повышения эффективности внутриаптечного контроля качества лекарственных средств, изготовляемых в условиях аптечных организаций (аптек),
ПРИКАЗЫВАЮ:
1. Руководителям территориальных органов управления здравоохранением субъектов Российской Федерации:
1.1. Обеспечить во всех аптечных организациях (аптеках) выполнение требований "Инструкции по контролю качества лекарственных средств, изготовляемых в аптечных организациях (аптеках)" (приложение 1).
1.2. Оснастить рабочие места для проведения контроля качества лекарственных средств, изготовляемых в аптеках, приборами, оборудованием и реактивами в соответствии с требованиями Инструкции (приложение А к "Инструкции по контролю качества лекарственных средств, изготовляемых в аптечных организациях (аптеках)").
1.3. Обеспечить в аптечных организациях (аптеках) условия хранения изготовленных лекарственных средств в соответствии с "Условиями хранения и режимом стерилизации лекарственных средств, изготовленных в аптеках" (приложение 2)……………………………………
Инструкция по контролю качества лекарственных средств, изготовляемых в аптечных организациях (аптеках)
VIII. Химический контроль
8.1. Химический контроль заключается в оценке качества изготовления лекарственного средства по показателям: "Подлинность", "Испытания на чистоту и допустимые пределы примесей" (качественный анализ) и "Количественное определение" (количественный анализ) лекарственных веществ, входящих в его состав.
8.2. Качественному анализу подвергаются обязательно:
8.2.1. Вода очищенная, вода для инъекций ежедневно (из каждого баллона, а при подаче воды по трубопроводу на каждом рабочем месте) на отсутствие хлоридов, сульфатов и солей кальция. Вода, предназначенная для изготовления стерильных растворов, кроме указанных выше испытаний должна быть проверена на отсутствие восстанавливающих веществ, солей аммония и углерода диоксида в соответствии с требованиями действующей Государственной Фармакопеи.
Ежеквартально вода очищенная должна направляться в территориальную контрольно - аналитическую лабораторию для полного химического анализа.
Приложение 3
Фармакопейная статья Вода очищенная
Aqua purificata ФС 42-2619-97
Н2O М.м. 18,02
Настоящая фармакопейная статья распространяется на воду очищенную, получаемую дистилляцией, ионным обменом, обратным осмосом, комбинацией этих методов или другим способом, применяемую для приготовления неинъекционных лекарственных средств.
Описание. Бесцветная прозрачная жидкость без запаха и вкуса. РН от 5,0 до 7,0 (к 100 мл воды прибавляют 0,3 мл насыщенного раствора калия хлорида и измеряют рН раствора потенциометрически, (ГФ XI, вып. 1, стр.113).
Сухой остаток. 100 мл воды выпаривают на водяной бане досуха и сушат при (100-105°С) до постоянной массы. Остаток не должен превышать 0,001%.
Восстанавливающие вещества. 100 мл воды доводят до кипения, прибавляют 1мл 0,01 М раствора калия перманганата и 2 мл кислоты серной разведенной, кипятят 10 мин; розовая окраска должна сохраниться.
Диоксид углерода. При взбалтывании воды с равным объемом известковой воды в наполненном доверху и хорошо закрытом сосуде не должно быть помутнения в течение 1 ч.
Нитраты и нитриты. К 5 мл воды осторожно прибавляют 1 мл свежеприготовленного раствора дифениламина; не должно появляться голубого окрашивания.
Аммиак. К 10 мл воды прибавляют 0,15 мл реактива Несслера, перемешивают и через 5 мин сравнивают с раствором, состоящим из смеси 1 мл эталонного раствора Б, содержащего 0,002 мг иона аммония в 1 мл и 9 мл воды, свободной от аммиака, и такого же количества реактива прибавлено к испытуемому раствору. Окраска, появившаяся в испытуемом растворе, не должна превышать эталон (0,00002% в препарате).
Хлориды. К 10 мл воды прибавляют 0,5 мл кислоты азотной,0,5 мл раствора серебра нитрата, перемешивают и оставляют на 5 мин. Не должно быть опалесценции.
Сульфаты. К 10 мл воды прибавляют 0,5 мл кислоты хлористоводородной разведенной и 1 мл раствора бария хлорида, перемешивают и оставляют на 10 мин, Не должно быть помутнения.
Кальций. К 10 мл воды прибавляют 1 мл раствора аммония хлорида, 1 мл раствора аммиака и 1 мл раствора аммония оксалата, перемешивают и оставляют на 10 мин. Не должно быть помутнения.
Тяжелые металлы. К 10 мл воды прибавляют 1 мл кислоты уксусной разведенной, 2 капли раствора натрия сульфида, перемешивают и оставляют на 1 мин. Наблюдение окраски производят по оси пробирки диаметром около 1,5 см, помешенной на белой поверхности. Не должно быть окрашивания.
Микробиологическая чистота. Должна соответствовать требованиям на питьевую воду (не более 100 микроорганизмов в 1 мл) при отсутствии бактерий сем. Enterobacteriaceae. Staphylococcus aureus, Pseudomonas aeruginosa. Испытания проводят в соответствии со статьей «Испытание на микробиологическую чистоту» (ГФ XI, вып.2, стр. 193).
Использование и хранение. Используют свежеприготовленной или хранят в закрытых емкостях, изготовленных из материалов, не изменяющих свойств воды и защищающих ее от инородных частиц и микробиологических загрязнений.
Примечание:
Для приготовления стерильных неинъекционных лекарственных средств, изготовляемых асептически, воду необходимо стерилизовать.
Реактивы, титрованные растворы и индикаторы, приведенные в настоящей Фармакопейной статье, описаны в соответствующих разделах Государственной Фармакопеи СССР XI издания.
studfiles.net
ФС.2.2.0020.15 Вода очищенная | Pharmacopoeia.ru
Содержимое (Table of Contents)
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФАРМАКОПЕЙНАЯ СТАТЬЯ
Вода очищенная ФС.2.2.0020.15
Вода очищенная Взамен ГФ Х, ст. 73;
Aqua purificata взамен ФС 42-2619-97
Н2О М. м. 18,02
Настоящая фармакопейная статья распространяется на нефасованную воду очищенную, получаемую из воды питьевой методами дистилляции, ионного обмена, обратного осмоса, комбинацией этих методов или другим способом, и предназначенную для производства или изготовления лекарственных средств, получения воды для инъекций, а также для проведения испытаний лекарственных средств.
Для приготовления лекарственных средств, изготовляемых в асептических условиях, воду очищенную необходимо подвергать стерилизации.
Вода очищенная не должна содержать антимикробных консервантов или других добавок.
Описание
Бесцветная прозрачная жидкость без запаха.
рН
От 5,0 до 7,0 (ОФС «Ионометрия», метод 3). К 100 мл воды очищенной прибавляют 0,3 мл насыщенного раствора калия хлорида.
Кислотность или щелочность
К 20 мл воды очищенной прибавляют 0,05 мл 0,1 % раствора фенолового красного. При появлении желтого окрашивания оно должно измениться на красное при прибавлении не более 0,1 мл 0,01 М раствора натрия гидроксида. При появлении красного окрашивания оно должно измениться на желтое при прибавлении не более 0,15 мл 0,01 М раствора хлористоводородной кислоты.
Электропроводность
Определение проводят в соответствии с требованиями ОФС «Электропроводность» с помощью оборудования – кондуктометров, внесенных в Государственный реестр средств измерений.
Оборудование
Кондуктометрическая ячейка:
− электроды из подходящего материала, такого как нержавеющая сталь;
− константа ячейки обычно устанавливается поставщиком и впоследствии проверяется через соответствующие интервалы времени с использованием сертифицированного стандартного раствора с электропроводностью менее 1500 мкСм/см или путем сравнения с ячейкой, имеющей аттестованную константу ячейки. Константа ячейки считается подтвержденной, если найденное значение находится в пределах 2 % от значения, указанного в сертификате; в противном случае должна быть проведена повторная калибровка.
Кондуктометр. Точность измерения должна быть не менее 0,1 мкСм/см в низшем диапазоне.
Калибровка системы (ячейки электропроводности и кондуктометра). Калибровка должна проводиться с использованием одного или более соответствующих стандартных растворов (ОФС «Электропроводность»). Допустимое отклонение должно составлять не более 3 % от измеренного значения электропроводности.
Калибровка кондуктометра. Калибровку кондуктометра проводят с использованием сопротивлений высокой точности или эквивалентным прибором после отсоединения ячейки электропроводности для всех интервалов, использующихся для измерения электропроводности и калибровки ячейки, с погрешностью не более 0,1 % от сертифицированной величины.
В случае невозможности отсоединения ячейки электропроводности, вмонтированной в производственную линию, калибровка может быть проведена относительно предварительно калиброванной ячейки электропроводности, помещенной в поток воды рядом с калибруемой ячейкой.
Методика
Измеряют электропроводность без температурной компенсации с одновременной регистрацией температуры. Измерение электропроводности с помощью кондуктометров с температурной компенсацией возможно только после соответствующей валидации.
В табл. 1 находят ближайшее значение температуры, меньше измеренного. Соответствующая величина электропроводности является предельно допустимой.
Вода очищенная соответствует требованиям, если измеренное значение электропроводности не превышает найденного по табл.1 предельно допустимого значения.
Таблица 1 – Предельно допустимые значения электропроводности воды очищенной в зависимости от температуры
| Температура, ºС | Электропроводность, мкСм/см | Температура, ºС | Электропроводность, мкСм/см |
| 0 | 2,4 | 60 | 8,1 |
| 10 | 3,6 | 70 | 9,1 |
| 20 | 4,3 | 75 | 9,7 |
| 25 | 5,1 | 80 | 9,7 |
| 30 | 5,4 | 90 | 9,7 |
| 40 | 6,5 | 100 | 10,2 |
| 50 | 7,1 |
Для значений температур, не представленных в табл. 1, рассчитывают предельно допустимое значение электропроводности путем интерполяции ближайших к полученному верхнему и нижнему значениям, приведенным в табл. 1.
Сухой остаток
Не более 0,001 %. 100 мл воды очищенной выпаривают досуха и сушат при температуре от 100 до 105 ºС до постоянной массы.
Восстанавливающие вещества
100 мл воды очищенной доводят до кипения, прибавляют 0,1 мл 0,02 М раствора калия перманганата и 2 мл серной кислоты разведенной 16 %, кипятят 10 мин; розовое окрашивание должно сохраниться.
Углерода диоксид
При взбалтывании воды очищенной с равным объемом раствора кальция гидроксида (известковой воды) в наполненном доверху и хорошо закрытом сосуде не должно быть помутнения в течение 1 ч.
Нитраты и нитриты
К 5 мл воды очищенной осторожно прибавляют 1 мл свежеприготовленного раствора дифениламина; не должно появляться голубое окрашивание.
Аммоний
Не более 0,00002 % (ОФС «Аммоний»). Определение проводят с использованием эталонного раствора, содержащего 1 мл стандартного раствора аммоний-иона (2 мкг/мл) и 9 мл воды, свободной от аммиака. Для определения отбирают 10 мл испытуемой пробы.
Примечание. Стандартный раствор аммоний-иона (2 мкг/мл) готовят разбавлением стандартного раствора аммоний-иона (200 мкг/мл) водой, свободной от аммиака.
Хлориды
К 10 мл воды очищенной прибавляют 0,5 мл азотной кислоты, 0,5 мл 2 % раствора серебра нитрата, перемешивают и оставляют на 5 мин. Не должно быть опалесценции.
Сульфаты
К 10 мл воды очищенной прибавляют 0,5 мл хлористоводородной кислоты разведенной 8,3 % и 1 мл 5 % раствора бария хлорида, перемешивают и оставляют на 10 мин. Не должно быть помутнения.
Кальций и магний
К 100 мл воды очищенной прибавляют 2 мл буферного раствора аммония хлорида, рН 10,0 50 мг индикаторной смеси протравного черного 11 и 0,5 мл 0,01 М раствора натрия эдетата; должно наблюдаться чисто синее окрашивание раствора (без фиолетового оттенка).
Алюминий
Не более 0,000001 % (ОФС «Алюминий», метод 1). Испытание проводят для воды очищенной, предназначенной для использования в производстве растворов для диализа.
Испытуемый раствор. К 400 мл воды очищенной прибавляют 10 мл ацетатного буферного раствора, рН 6,0 и 100 мл воды дистиллированной, перемешивают.
Эталонный раствор. К 2 мл стандартного раствора алюминий-иона(2 мкг/мл) прибавляют 10 мл ацетатного буферного раствора, рН 6,0 и 98 мл воды дистиллированной, перемешивают.
Контрольный раствор. К 10 мл ацетатного буферного раствора, рН 6,0 прибавляют 100 мл воды дистиллированной и перемешивают.
Тяжелые металлы
Не более 0,00001 %.
Определение проводят одним из приведенных методов.
Метод 1. В пробирку диаметром около 1,5 см помещают 10 мл испытуемой воды очищенной, прибавляют 1 мл уксусной кислоты разведенной 30 %, 2 капли 2 % раствора натрия сульфида и перемешивают. Через 1 мин производят наблюдение за изменением окраски раствора по оси пробирки, помещенной на белую поверхность. Не должно быть окрашивания.
Метод 2. 120 мл воды очищенной упаривают до объёма 20 мл. Оставшеаяся после упаривания вода в объеме 10 мл должна выдерживать испытание на тяжёлые металлы (ОФС «Тяжелые металлы») с использованием эталонного раствора, содержащего 1 мл стандартного раствора свинец-иона (5мкг/мл) и 9 мл испытуемой воды очищенной.
Примечание. Стандартный раствор свинец-иона (5мкг/мл) готовят разбавлением стандартного раствора свинец-иона (100мкг/мл) испытуемой водой очищенной.
Микробиологическая чистота
Общее число аэробных микроорганизмов (бактерий и грибов) не более 100 КОЕ в 1 мл. Не допускается наличие Еscherichia coli, Staphylococcus aureus, Pseudomonas aeruginosa в 100 мл.
Для анализа микробиологической чистоты воды очищенной отбирают образец в объеме не менее 1000 мл.
Исследование проводят методом мембранной фильтрации в асептических условиях в соответствии с методами ОФС «Микробиологическая чистота», п.12.
Бактериальные эндотоксины
Менее 0,25 ЕЭ/мл (ОФС «Бактериальные эндотоксины»).
Испытание проводят для воды очищенной, предназначенной для использования в производстве растворов для диализа.
Хранение и распределение
Вода очищенная хранится и распределяется в условиях, предотвращающих рост микроорганизмов и исключающих возможность любой другой контаминации.
Хранение воды очищенной осуществляют в специальных сборниках, оно не должно превышать 3 сут.
Скачать в PDF ФС.2.2.0020.15 Вода очищеннаяnaya
pharmacopoeia.ru
2.2.20. (ФС.2.2.0020.15)
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФАРМАКОПЕЙНАЯ СТАТЬЯ
Вода очищенная ФС.2.2.0020.15
Вода очищенная Взамен ГФ Х, ст. 73;
Aqua purificata взамен ФС 42-2619-97
Н2ОМ. м. 18,02
Настоящая фармакопейная статья распространяется на нефасованную воду очищенную, получаемую из воды питьевой методами дистилляции, ионного обмена, обратного осмоса, комбинацией этих методов или другим способом, и предназначенную для производства или изготовления лекарственных средств, получения воды для инъекций, а также для проведения испытаний лекарственных средств.
Для приготовления лекарственных средств, изготовляемых в асептических условиях, воду очищенную необходимо подвергать стерилизации.
Вода очищенная не должна содержать антимикробных консервантов или других добавок.
Описание. Бесцветная прозрачная жидкость без запаха.
рН. От 5,0 до 7,0 (ОФС «Ионометрия», метод 3). К 100 мл воды очищенной прибавляют 0,3 мл насыщенного раствора калия хлорида.
Кислотность или щелочность. К 20 мл воды очищенной прибавляют 0,05 мл 0,1 % раствора фенолового красного. При появлении желтого окрашивания оно должно измениться на красное при прибавлении не более 0,1 мл 0,01 М раствора натрия гидроксида. При появлении красного окрашивания оно должно измениться на желтое при прибавлении не более 0,15 мл 0,01 М раствора хлористоводородной кислоты.
Электропроводность. Определение проводят в соответствии с требованиями ОФС «Электропроводность» с помощью оборудования – кондуктометров, внесенных в Государственный реестр средств измерений.
Оборудование
Кондуктометрическая ячейка:
− электроды из подходящего материала, такого как нержавеющая сталь;
− константа ячейки обычно устанавливается поставщиком и впоследствии проверяется через соответствующие интервалы времени с использованием сертифицированного стандартного раствора с электропроводностью менее 1500 мкСм/см или путем сравнения с ячейкой, имеющей аттестованную константу ячейки. Константа ячейки считается подтвержденной, если найденное значение находится в пределах 2 % от значения, указанного в сертификате; в противном случае должна быть проведена повторная калибровка.
Кондуктометр. Точность измерения должна быть не менее 0,1 мкСм/см в низшем диапазоне.
Калибровка системы (ячейки электропроводности и кондуктометра). Калибровка должна проводиться с использованием одного или более соответствующих стандартных растворов (ОФС «Электропроводность»). Допустимое отклонение должно составлять не более 3 % от измеренного значения электропроводности.
Калибровка кондуктометра. Калибровку кондуктометра проводят с использованием сопротивлений высокой точности или эквивалентным прибором после отсоединения ячейки электропроводности для всех интервалов, использующихся для измерения электропроводности и калибровки ячейки, с погрешностью не более 0,1 % от сертифицированной величины.
В случае невозможности отсоединения ячейки электропроводности, вмонтированной в производственную линию, калибровка может быть проведена относительно предварительно калиброванной ячейки электропроводности, помещенной в поток воды рядом с калибруемой ячейкой.
Методика
Измеряют электропроводность без температурной компенсации с одновременной регистрацией температуры. Измерение электропроводности с помощью кондуктометров с температурной компенсацией возможно только после соответствующей валидации.
В табл. 1 находят ближайшее значение температуры, меньше измеренного. Соответствующая величина электропроводности является предельно допустимой.
Вода очищенная соответствует требованиям, если измеренное значение электропроводности не превышает найденного по табл.1 предельно допустимого значения.
Таблица 1 – Предельно допустимые значения электропроводности воды очищенной в зависимости от температуры
| Температура, ºС | Электропроводность, мкСм/см | Температура, ºС | Электропроводность, мкСм/см |
| 0 | 2,4 | 60 | 8,1 |
| 10 | 3,6 | 70 | 9,1 |
| 20 | 4,3 | 75 | 9,7 |
| 25 | 5,1 | 80 | 9,7 |
| 30 | 5,4 | 90 | 9,7 |
| 40 | 6,5 | 100 | 10,2 |
| 50 | 7,1 |
Для значений температур, не представленных в табл. 1, рассчитывают предельно допустимое значение электропроводности путем интерполяции ближайших к полученному верхнему и нижнему значениям, приведенным в табл. 1.
Сухой остаток. Не более 0,001 %. 100 мл воды очищенной выпаривают досуха и сушат при температуре от 100 до 105 ºС до постоянной массы.
Восстанавливающие вещества. 100 мл воды очищенной доводят до кипения, прибавляют 0,1 мл 0,02 М раствора калия перманганата и 2 мл серной кислоты разведенной 16 %, кипятят 10 мин; розовое окрашивание должно сохраниться.
Углерода диоксид. При взбалтывании воды очищенной с равным объемом раствора кальция гидроксида (известковой воды) в наполненном доверху и хорошо закрытом сосуде не должно быть помутнения в течение 1 ч.
Нитраты и нитриты. К 5 мл воды очищенной осторожно прибавляют 1 мл свежеприготовленного раствора дифениламина; не должно появляться голубое окрашивание.
Аммоний. Не более 0,00002 % (ОФС «Аммоний»). Определение проводят с использованием эталонного раствора, содержащего 1 мл стандартного раствора аммоний-иона (2 мкг/мл) и 9 мл воды, свободной от аммиака. Для определения отбирают 10 мл испытуемой пробы.
Примечание. Стандартный раствор аммоний-иона (2 мкг/мл) готовят разбавлением стандартного раствора аммоний-иона (200 мкг/мл) водой, свободной от аммиака.
Хлориды. К 10 мл воды очищенной прибавляют 0,5 мл азотной кислоты, 0,5 мл 2 % раствора серебра нитрата, перемешивают и оставляют на 5 мин. Не должно быть опалесценции.
Сульфаты. К 10 мл воды очищенной прибавляют 0,5 мл хлористоводородной кислоты разведенной 8,3 % и 1 мл 5 % раствора бария хлорида, перемешивают и оставляют на 10 мин. Не должно быть помутнения.
Кальций и магний. К 100 мл воды очищенной прибавляют 2 мл буферного раствора аммония хлорида, рН 10,0 50 мг индикаторной смеси протравного черного 11 и 0,5 мл 0,01 М раствора натрия эдетата; должно наблюдаться чисто синее окрашивание раствора (без фиолетового оттенка).
Алюминий. Не более 0,000001 % (ОФС «Алюминий», метод 1). Испытание проводят для воды очищенной, предназначенной для использования в производстве растворов для диализа.
Испытуемый раствор. К 400 мл воды очищенной прибавляют 10 мл ацетатного буферного раствора, рН 6,0 и 100 мл воды дистиллированной, перемешивают.
Эталонный раствор. К 2 мл стандартного раствора алюминий-иона (2 мкг/мл) прибавляют 10 мл ацетатного буферного раствора, рН 6,0 и 98 мл воды дистиллированной, перемешивают.
Контрольный раствор. К 10 мл ацетатного буферного раствора, рН 6,0 прибавляют 100 мл воды дистиллированной и перемешивают.
Тяжелые металлы. Не более 0,00001 %.
Определение проводят одним из приведенных методов.
Метод 1. В пробирку диаметром около 1,5 см помещают 10 мл испытуемой воды очищенной, прибавляют 1 мл уксусной кислоты разведенной 30 %, 2 капли 2 % раствора натрия сульфида и перемешивают. Через 1 мин производят наблюдение за изменением окраски раствора по оси пробирки, помещенной на белую поверхность. Не должно быть окрашивания.
Метод 2. 120 мл воды очищенной упаривают до объёма 20 мл. Оставшеаяся после упаривания вода в объеме 10 мл должна выдерживать испытание на тяжёлые металлы (ОФС «Тяжелые металлы») с использованием эталонного раствора, содержащего 1 мл стандартного раствора свинец-иона (5мкг/мл) и 9 мл испытуемой воды очищенной.
Примечание. Стандартный раствор свинец-иона (5мкг/мл) готовят разбавлением стандартного раствора свинец-иона (100мкг/мл) испытуемой водой очищенной.
Микробиологическая чистота
Общее число аэробных микроорганизмов (бактерий и грибов) не более 100 КОЕ в 1 мл. Не допускается наличие Еscherichia coli, Staphylococcus aureus, Pseudomonas aeruginosa в 100 мл.
Для анализа микробиологической чистоты воды очищенной отбирают образец в объеме не менее 1000 мл.
Исследование проводят методом мембранной фильтрации в асептических условиях в соответствии с методами ОФС «Микробиологическая чистота», п.12.
Бактериальные эндотоксины. Менее 0,25 ЕЭ/мл (ОФС «Бактериальные эндотоксины»).
Испытание проводят для воды очищенной, предназначенной для использования в производстве растворов для диализа.
Хранение и распределение. Вода очищенная хранится и распределяется в условиях, предотвращающих рост микроорганизмов и исключающих возможность любой другой контаминации.
Хранение воды очищенной осуществляют в специальных сборниках, оно не должно превышать 3 сут.
studfiles.net
Фармакопейная статья Вода для инъекций
Aqua pro injectionibus ФС 42- 2620-97
Настоящая фармакопейная статья распространяется на воду очищенную, получаемую дистилляцией, ионным обменом, обратным осмосом, комбинацией этих методов или другим способом, применяемую для приготовления неинъекционных лекарственных средств.
Вода для инъекции должна выдерживать испытания, приведенные в статье «вода очищенная», должна быть апирогенной, не содержать антимикробных веществ и других добавок.
Для инъекционных лекарственных средств, которые изготавливаются в асептических условиях и не подвергают последующей стерилизации, используют стерильную воду для инъекции.
Пирогенность. Испытание проводят в соответствии со статьей «Испытание на пирогенность» (ГФ XI. вып.2, стр.183).
Использование и хранение. Используют свежеприготовленной или хранят при температуре от 5°С до 10°С или от 80°С до 95°С в закрытых емкостях, изготовленных из материалов, не изменяющих свойств воды, защищающих воду тот попадания механических включений и микробиологических загрязнений, но не более 24 ч.
Приложение 4
к "Инструкции по контролю качества лекарственных средств,
изготовляемых в аптечных организациях (аптеках)",
утвержденной приказом Министерства здравоохранения
Российской Федерации от 16.07.1997 г. N 214
ЖУРНАЛ РЕГИСТРАЦИИ РЕЗУЛЬТАТОВ КОНТРОЛЯ "ВОДЫ ОЧИЩЕННОЙ", "ВОДЫ ДЛЯ ИНЪЕКЦИЙ"
| Дата получения (отгонки воды) | Дата контроля | № п/п (он же № анализа) | № баллона или бюретки | Результаты контроля на отсутствие примесей* | Заключение (удовл. или не удовл. ФС) | Подпись проверив-шего | |||||||
| хлорид-иона | сульфат-иона | солей кальция | солей аммония | восстанавливающих веществ | углерода диоксида | ||||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | ||
* – В графах с 5 по 10 результаты контроля при отсутствии примесей отмечаются знаком минус(-).
12
studfiles.net
5. Требования к воде очищенной, регламентируемые различными фармакопеями. Сравнительная оценка требований к воде очищенной и к воде для инъекций отечественных и зарубежных фармакопейных статей
Похожие главы из других работ:
Ассоциации иммуногенетической системы HLA с развитием туберкулеза
Глава 2. Ассоциация туберкулёза с различными генетическими факторами
Туберкулез вызывается микобактериями туберкулеза, медленно растущими кислотоустойчивыми бациллами. Воскоподобная клеточная стенка микобактерий, которая состоит из нескольких гликолипидов...
Вода и здоровье
О воде вообще
О воде много говорилось, но мало сказано. Поэтому фраза “Вода - это жизнь" для многих из нас ровным сетом ничего не значит. И за беспечное отношение к ней вода жестоко мстит нам. Задумайтесь, что вы знаете о воде? Как ни удивительно...
Вода очищенная
4. Системы распределения воды очищенной
Системы хранения и распределения воды очищенной представляют собой циркуляционный контур, в который включена емкость для хранения. Все поверхности, находящиеся в контакте с водой, должны быть выполнены из материалов...
Вода очищенная
4.1 Состав и организация системы распределения воды очищенной
В системе распределения воды очищенной поддерживается температура в пределах 15-30°С. Для поддержания микробиологической чистоты в циркуляционном контуре устанавливается ультрафиолетовый стерилизатор...
Водоподготовка на фармацевтическом предприятии
Требования к воде в фармацевтической промышленности
Вода, которая используется в производстве, должна быть чистой и контролироваться как на содержание примесей, так и по микробиологическим показателям. Поскольку вода может использоваться на разных стадиях производства и в различных целях...
Гигиенический (оздоровительный) массаж
4. Ручной массаж в воде (ванне, бассейне)
Массаж в воде активизирует обменные процессы, улучшает крово- и лимфообращение в тканях и органах. Его влияние обусловлено не только механическим воздействием на поверхностные ткани...
Гидрореабилитация при нарушении осанки
Глава 1. Влияние занятий плаванием на организм человека, страдающего различными заболеваниями
Условия организации воспитания и образования детей в Российской Федерации в семье, проживающей летом в городе, на даче или загородном участке при расположенном рядом водоеме, свидетельствует о том...
Голодание по Полю Брэгу
4. Однодневное лечебное голодание на воде
Однодневное оздоровительное голодание по Брэггу наиболее приемлемо для проведения в домашних условиях. Лечебное голодание, которое длится от 7 до 10 суток, проводить следует только под контролем врача...
Заболевания, обусловленные химическим составом воды
3. Токсиканты в воде, имеющие глобальный характер распространения
Загрязнение водного бассейна можно считать наиболее ощутимым и достаточно хорошо изученным проявлением глобального экологического кризиса...
Медицинские растворы заводского производства. Интенсификация процесса растворения. Способы очистки
2.1 Контроль качества раствора натрия бромида 6,0, магния сульфата 6,0, глюкозы 25,0, воды очищенной до 100,0 мл
Особенности химического контроля. Качественный и количественный анализы проводят без предварительного разделения ингредиентов. Наиболее экспрессным методом определения глюкозы в жидких лекарственных формах является метод рефрактометрии...
Приготовление гипертонического раствора и контроль его качества
2.3.2 Анализ воды очищенной
1.Описание. Бесцветная прозрачная жидкость без запаха и вкуса. рН. от 5,0 до 7,0 (к 100 мл воды прибавляют 0,3 мл насыщенного раствора калия хлорида и измеряют рН раствора потенциометрически. 2.Сухой остаток...
Применение волоконных штифтов в стоматологии
7.3 Изучение предела прочности на разрыв с различными композитными цементами
Цель проведения этого теста - проверить качество влияния PVD покрытия на эффективность прочности соединения штифта с различными композитными цементами, чтобы доктор мог пользоваться любым материалом по своему выбору...
Сравнительная оценка требований к воде очищенной и к воде для инъекций отечественных и зарубежных фармакопейных статей
6. Требования к воде для инъекций, регламентируемые различными фармакопеями
Вода для инъекций используется для производства и/или изготовления стерильных ЛС, финишного ополаскивания тары и укупорки, обработки систем приготовления, хранения и распределения...
Сравнительная оценка требований к воде очищенной и к воде для инъекций отечественных и зарубежных фармакопейных статей
5. Требования к воде очищенной, регламентируемые различными фармакопеями
Вода очищенная используется для производства и/или изготовления нестерильных ЛС, а также для получения пара, санитарной обработки...
Сравнительная оценка требований к воде очищенной и к воде для инъекций отечественных и зарубежных фармакопейных статей
6. Требования к воде для инъекций, регламентируемые различными фармакопеями
Вода для инъекций используется для производства и/или изготовления стерильных ЛС, финишного ополаскивания тары и укупорки, обработки систем приготовления, хранения и распределения...
med.bobrodobro.ru
Очистка и подготовка воды для фармацевтики | ООО "УниВОД"

Безопасность технологических процессов.
Высокое качество продукции.
Вода для фармацевтических целей относится к одному из самых важных элементов, обеспечивающих безопасность и качество производимых лекарственных средств. Ввиду особенностей продукта вода широко используется в качестве вспомогательного вещества в составе лекарственных средств, самого лекарственного средства, а также при различных технологических нуждах, например, мойка флаконов, ампул, уборка помещений и приготовление дезинфицирующих растворов и т.д. Поскольку вода может использоваться на разных стадиях производства и в различных целях, существует несколько типов воды, отличающихся по требованиям к ее чистоте. Требования к качеству воды для различных применений в фармацевтических производствах регламентируются фармакопейными статьями.
Действующие в России фармакопейные статьи:
Производители большинства стран мира и в частности - России, одновременно с национальными фармакопеями для оценки качества воды для фармацевтических целей также учитывают требования USP и Европейской Фармакопеи, поскольку они содержат более жесткие требования к качеству воды.
В Европейской Фармакопее существуют статьи:
До настоящего времени отечественные регуляторы принимали стандарты Европейской фармакопеи в качестве основного ориентира, что нашло свое отражение в государственной фармакопее, а также в фармакопейных статьях предприятий на отечественные препараты. Явно или косвенно принята на вооружение Европейская фармакопея и в ряде стран бывшего СССР. Европейская фармакопея имеет классическую структуру: содержит общую фармакопейную статью и собственно фармакопейные статьи. Но ее особенностью является то, что она не содержит фармакопейных статьей на препараты. В ней имеются фармакопейные статьи только на субстанции.
В соответствии с современными требованиями, изложенными в Фармакопее США (USP) вода для фармацевтических целей делиться на следующие ее виды:
Фармакопея США – Национальный формуляр выпускается единственной в мире негосударственной фармакопейной организацией – Фармакопейной конвенцией США. Однако требования этого стандарта признаются на государственном уровне и определяют минимальный уровень качества, обязательный для организаций, производящих или поставляющих лекарственных средства в США. Не будет преувеличением сказать, что Фармакопейная конвенция США является одной из самых влиятельных фармакопейных организаций в мире. Ее стандарты качества действуют не только в США и Канаде, но и принимаются на вооружение в ряде других стран, активно производящих лекарственные средства. Принимая во внимание процесс гармонизации фармакопейных требований, большое значение имеет выход русскоязычного издания Фармакопеи США. Переводное издание USP не имеет законодательного значения в РФ, однако значительное число воспроизведенных лекарственных средств анализируется по методикам, описанным, в частности, в USP. И производители дженериков часто ориентируются на этот документ при разработке фармакопейных статей предприятия или других нормативных документов.
Дженерик - лекарственное средство, продающееся под международным непатентованным названием либо под патентованным названием, отличающимся от фирменного названия разработчика препарата. После вступления в действие соглашения по торговым аспектам прав интеллектуальной собственности (ТРИПС) дженериками обычно называют лекарственные средства, на действующее вещество которого истёк срок патентной защиты либо защищенные патентами препараты, выпускающиеся по принудительной лицензии. Как правило, дженерики по своей эффективности не отличаются от «оригинальных» препаратов, однако значительно дешевле их. Поддержка производства дженериков, их использования в медицинской практике и замещение ими «оригинальных» брендированных препаратов является одной из стратегических целей Всемирной организации здравоохранения при обеспечении доступа к медицинской помощи.
Соответствие фармакопейных статей типам воды для фармацевтических целей:
| ТИПЫ ВОДЫ | ГФ РФ | EP | USP |
| Вода для инъекций (ангро) | + | + | + |
| Стерильная вода для инъекций (в упаковке) | + | + | + |
| Бактериостатическая вода для инъекций (в упаковке) | - | - | + |
| Высокоочищенная вода (ангро) | - | + | - |
| Вода очищенная (ангро) | + | + | + |
| Вода очищенная (в упаковке) | - | + | - |
| Стерильная вода очищенная (в упаковке) | - | - | + |
| Стерильная вода для ингаляций (в упаковке) | - | - | + |
| Стерильная вода для ирригаций (в упаковке) | - | - | + |
| Вода для диализа (ангро и в упаковке) | - | + | - |
| Вода для фармацевтических целей (ОФС) | - | - | + |
ВОДА, ОЧИЩЕННАЯ используется для производства и (или) изготовления нестерильных лекарственных средств, а также для получения пара, санитарной обработки, мытья тары и укупорки (за исключением финишного ополаскивания при производстве и/или изготовлении стерильных лекарственных средств), в лабораторной практике. На фармацевтическом производстве она является исходной при получении воды для инъекций. Вода очищенная, удовлетворительно прошедшая испытание на эндотоксины, может быть использована при производстве растворов для диализа.
Методы получения и хранения Воды очищенной:
| ТИПЫ ВОДЫ | ФС 42-2619-97 | EP | USP |
| Методы получения | Дистилляция, ионный обмен, обратный осмос, комбинация этих методов или другим способом | Дистилляция, ионный обмен или другие подходящие методы | Любым подходящим методом |
| Качество исходной воды | - | Вода, соответствующая требованиям на воду питьевую, установленным соответствующим уполномоченным органом власти | Вода, соответствующая требованиям на питьевую воду Американского Национального ведомства по защите окружающей среды, или аналогичным требованиям на питьевую воду Европейского Союза или Японии |
| Использование и хранение | Используют свежеприготовленной или хранят в закрытых емкостях, изготовленных из материалов, не изменяющих свойств воды и защищающих ее от инородных частиц и микробиологических загрязнений | Хранится и распределяется в условиях, предотвращающих рост микроорганизмов и попадание других видов загрязнений | В системах получения, хранения и распределения холодной Воды Очищенной возможно образование биопленок из микроорганизмов, которые могут стать источником микробиологического загрязнения и бактериальных эндотоксинов, поэтому необходимо обеспечить периодическую санитарную обработку и микробиологический контроль |
В случае использования ионного обмена как финишного этапа, обеспечить надлежащую микробиологическую чистоту, либо использовать для удаления или разрушения бактерий дополнительный метод.
Требования по физико-химическим показателям и микробиологической чистоте, предъявляемые к Воде очищенной различными фармакопеями:
| ТИПЫ ВОДЫ | ФС 42-2619-97 | EP | USP |
| pH | 5,0-7,0 | - | - |
| Сухой остаток | 0,001% | - | - |
| Восстанавливающие вещества | 1мл 0,01 KMnO4/100 мл | Альтернативный ООУ 0,1мл 0,02 KMnO4/100 мл | - |
| Диоксид углерода | Отсутствие | - | - |
| Аммоний | 0,00002% (в препарате) | - | - |
| Нитриты | Отсутствие | - | - |
| Нитраты | Отсутствие | - | - |
| Хлориды | Отсутствие | - | - |
| Сульфаты | Отсутствие | - | - |
| Кальций | Отсутствие | - | - |
| Тяжёлые металлы | Отсутствие | - | - |
| Алюминий | - | 10 мкг/л (для гемодиализа) | - |
| Общий органический углерод (ООУ) | Отсутствие | 0,5 мг/л | 0,5 мг/л |
| Удельная электропроводность | - | 4,3 ?S* см-1(20OС) в линии или в лаборатории | 1,3 ?S* см-1(25OС) в линии; 2,1 ?S* см-1(25OС) в лаборатории |
| Микробиологическая чистота | 100 м.о/мл при отсутствии Entero-bacteriaceae, Staphylococcusaureus, Pseudomonasaeruginosa | 100 м.о/ мл | 100 м.о/ мл |
| Бактериальные эндотоксины | - | 0,25 ЕЭ/мл (для гемодиализа) | - |
Под понятием «Отсутствие» подразумевается отсутствие заметной разницы между испытуемым раствором и раствором без добавления основного реактива, открывающего данную примесь (например, …не должно быть помутнения…, …не должно быть опалесценции…, … не должно появляться окрашивания… и т.п.).
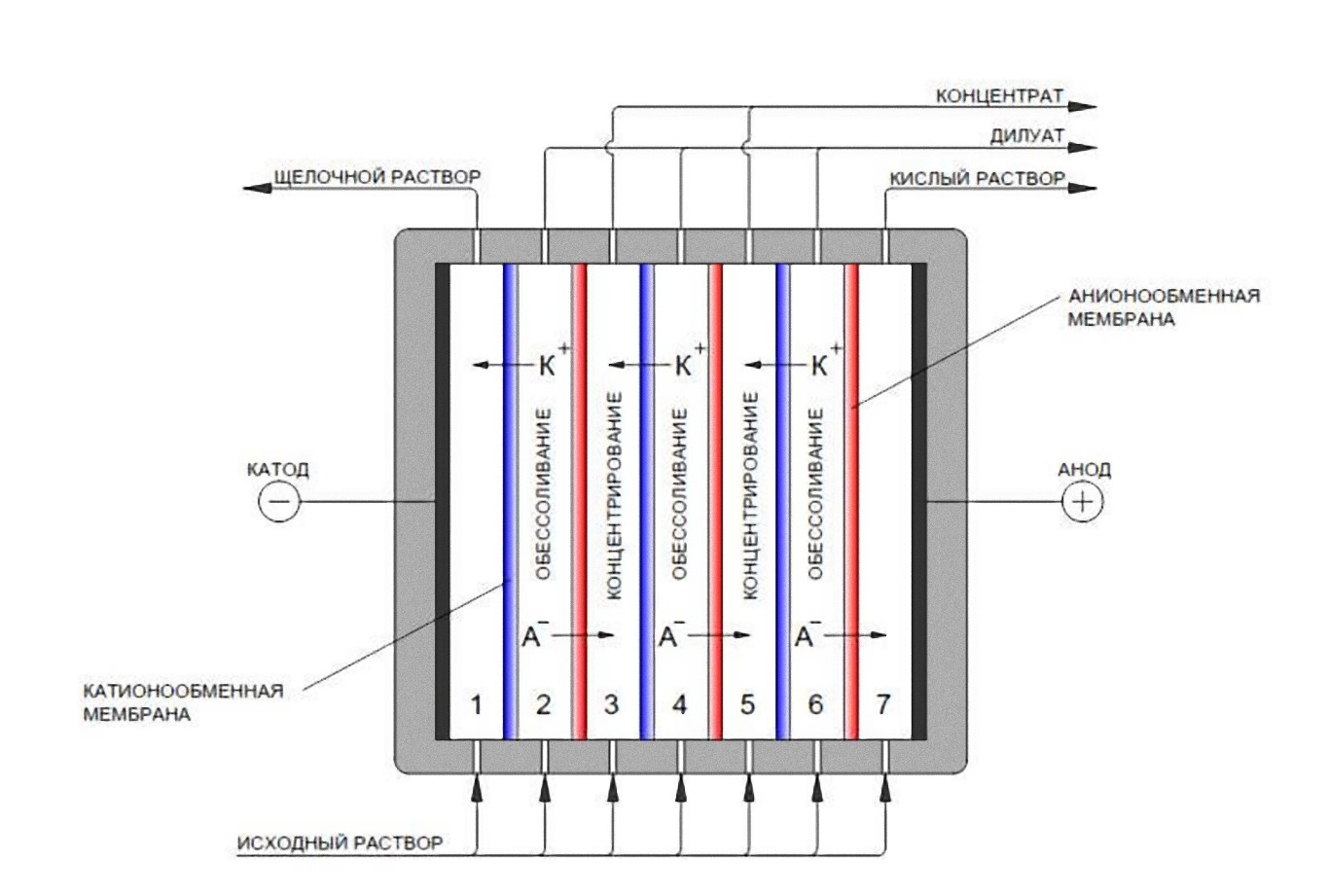
В последнее время для получения воды очищенной часто используют одноступенчатый обратный осмос в комплексе с модулем электродеонизации или двухступенчатый обратный осмос. Данные методы эффективны и энергетически выгодны. Дистилляция для получения воды очищенной применяется достаточно редко.
ВОДА ДЛЯ ИНЪЕКЦИЙ - это вода для приготовления лекарств для парентерального введения, если вода используется в качестве носителя (вода для инъекций ангро или вода для инъекций нерасфасованная) и для растворения или разведения субстанций перед применением препаратов для парентерального введения (вода для инъекций стерилизованная). Вода для инъекций используется для производства и/или изготовления стерильных лекарственных средств, финишного ополаскивания тары и укупорки, обработки систем приготовления, хранения и распределения, непосредственно контактирующих с конечной продукцией.
Вода для инъекций должна выдерживать испытания, приведенные в ФС 42-2619-97 «Вода очищенная», быть апирогенной, не содержать антимикробных веществ и других добавок.
Методы получения и хранения Воды для инъекций:
| ТИПЫ ВОДЫ | ФС 42-2620-97 | EP | USP |
| Методы получения | Дистилляция, обратный осмос | Дистилляция | Дистилляция или метод, эквивалентный или превосходящий дистилляцию по удалению химических примесей и микроорганизмов |
| Качество исходной воды | - | Вода, соответствующая требованиям на воду питьевую, установленным соответствующим уполномоченным органом власти либо вода очищенная | Вода, соответствующая требованиям на питьевую воду Американского Национального ведомства по защите окружающей среды, или аналогичным требованиям на питьевую воду Европейского Союза или Японии |
| Использование и хранение | Используют свежеприготовленной или хранят при температуре от 5OС до 10OС или от 80OС до 95OС в закрытых емкостях, изготовленных из материалов, не изменяющих свойств воды, защищающих воду от попадания механических включений и микробиологических загрязнений, но не более 24 часов | Хранится и распределяется в условиях, предотвращающих рост микроорганизмов и попадание других видов загрязнений | Хранится и распределяется в условиях, предотвращающих микробиологический рост и образование БЭ |
Требования по физико-химическим показателям и микробиологической чистоте, предъявляемые к Воде для инъекций различными фармакопеями:
| ТИПЫ ВОДЫ | ФС 42-2620-97 | EP | USP |
| Удельная электропроводность (УЭ) | - | 1,3 ?S*см-1(25OС) в линии; 2,1 ?S*см-1(25OС) в лаборатории | 1,3 ?S*см-1(25OС) в линии; 2,1 ?S*см-1(25OС) в лаборатории |
| Общий органический углерод (ООУ) | - | 0,5 мг/л | 0,5 мг/л |
| Микробиологическая чистота | 100 м.о./мл при отсутствии сем. Enterobacteriaceae, Staphylococcus aureus, Pseudomonas aeruginosa | 10 КОЕ/100 мл | 10 КОЕ/100 мл |
| Пирогенность | Апирогенна (биологический метод) | - | - |
| Бактериальные эндотоксины (БЭ) | 0,25 БЭ/мл | 0,25 БЭ/мл | 0,25 БЭ/мл |
На протяжении многих лет, применение обратного осмоса для получения воды для инъекций является предметом дискуссии в рамках Европейской фармакопейной комиссии. Но поскольку на сегодняшний день, нет достаточного количества аргументов в пользу применения обратного осмоса для производства воды для инъекций, а также исходя из требований к безопасности, вода для инъекций может производиться только методом дистилляции, как это предусмотрено в Европейской Фармакопее. Однако это достаточно дорогой метод, который требует высоких капитальных и эксплуатационных затрат, поэтому необходимо тщательно проводить предварительную подготовку подаваемой воды.
Следует отметить, что по требованиям USP и Государственной Фармакопее РФ допускается использование обратного осмоса для получения воды для инъекций.
ВОДА ВЫСОКООЧИЩЕННАЯ имеет такие же показатели качества, как и вода для инъекций, различие заключается, только в методах, которые допущены для приготовления воды высокоочищенной и воды для инъекций. Вода высокоочищенная готовится мембранными методами и может применяться, в основном для мытья контейнеров и поверхностей, соприкасающихся с парентеральными продуктами при условии проведения депирогенизации контейнеров и поверхностей. Воду для фармацевтических целей получают из воды питьевого качества, которая должна соответствовать локальным требованиям России - по санитарным нормам и правилам СанПин 2.1.4.1074-01 «Питьевая вода. Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения. Контроль качества». Источником воды питьевого качества является городской водопровод или природная вода. Важным моментом является доведение природной воды до воды питьевого качества путем фильтрации, умягчения и т.п. Питьевая вода, в фармацевтическом производстве, зачастую используется для мойки неклассифицированных помещений и оборудования, которое находится в этих помещениях, на ранних стадиях производства.
Накопленный практический опыт производителей лекарственных препаратов (особенно растворов для парентерального применения большого объема (инфузионных растворов)) в России и за рубежом показывает, что причиной отзыва продукции и источником ее загрязнения является в большинстве случаев используемая вода неудовлетворительного качества. В связи с вышесказанным, подготовка и получение воды относятся к наиболее ответственным и сложным, так называемым критическим стадиям технологического процесса на любом фармацевтическом предприятии. Поэтому, для оценки и анализа существующей или проектируемой системы водоподготовки, безусловно, необходимо знать современные требования к качеству воды и понимать, в каком месте для каких целей и какой тип воды необходимо использовать.
univod.ru