Содержание
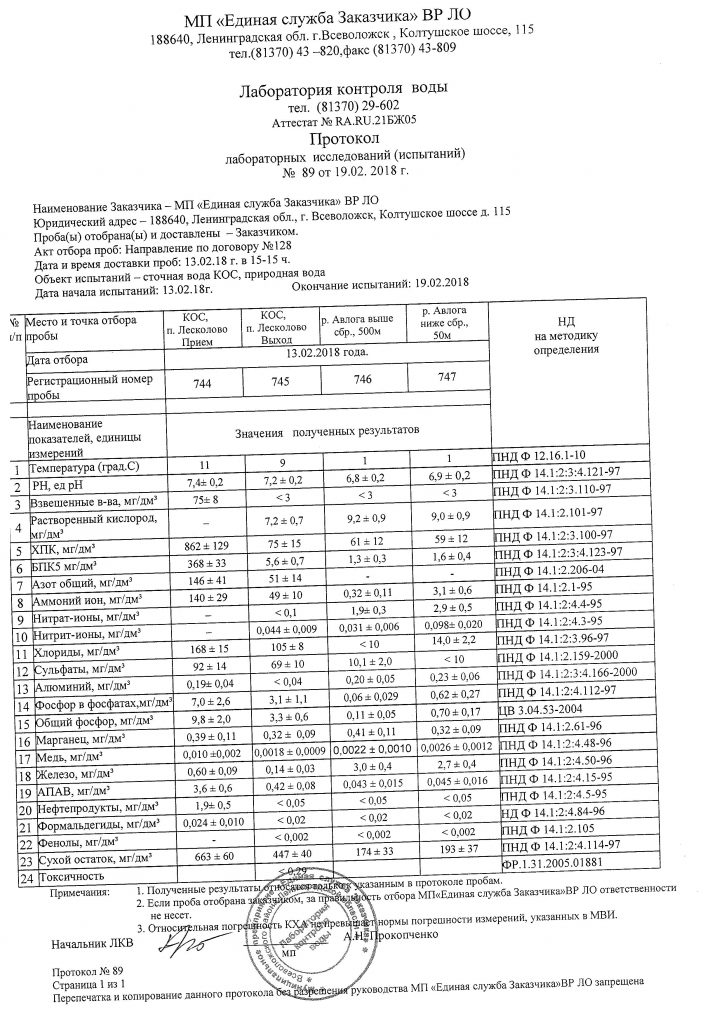
Анализ воды очищенной после очистных сооружений.
В современных условиях экономического кризиса большинство промышленных предприятий испытывают дефицит средства для эксплуатации, модернизации, а тем более для строительства новых высокотехнологичных очистных сооружении для очистки сточных вод. Многие предприятий направляют производственные стоки на городские канализационные станции механической и биологической очистки, которые не обеспечивают необходимую степень очистки из-за разнородности присутствующих в сточных водах токсичных веществ.
Биологическая очистка в типовых аэротенках, даже в режиме продленной аэрации, не всегда приводит к снижению содержания биогенных элементов в очищенной воде до допустимых уровней при сбросе в природные водоемы. Удаление азота из сточной воды связано с чередованием аэробного процесса нитрификации и анаэробного (аноксидного) процесса денитрификации, заканчивающегося образованием газообразного азота и его выходом в атмосферу. Процесс удаления фосфора в аэротенке основан на его выведении с избыточным активным илом при создании благоприятных условий для развития в активном иле гетеротрофных бактерий, склонных к повышенному накоплению фосфора в биомассе (почти в 4-5 раз больше обычного). Это достигается последовательным проведением двух стадий: сначала в анаэробной зоне (со специальной организованной подачей в нее легко окисляемой органики), в которой фосфатаккумулирующие бактерии запасают углерод и высвобождают фосфор, и затем в следующей за ней аэробной (либо аноксидной) зоне, в которой эти бактерии используют запасенный углерод для интенсивного роста, сопровождающегося значительно большим изъятием фосфора из воды и накоплением его в биомассе бактерий.
Процесс удаления фосфора в аэротенке основан на его выведении с избыточным активным илом при создании благоприятных условий для развития в активном иле гетеротрофных бактерий, склонных к повышенному накоплению фосфора в биомассе (почти в 4-5 раз больше обычного). Это достигается последовательным проведением двух стадий: сначала в анаэробной зоне (со специальной организованной подачей в нее легко окисляемой органики), в которой фосфатаккумулирующие бактерии запасают углерод и высвобождают фосфор, и затем в следующей за ней аэробной (либо аноксидной) зоне, в которой эти бактерии используют запасенный углерод для интенсивного роста, сопровождающегося значительно большим изъятием фосфора из воды и накоплением его в биомассе бактерий.
Осуществление совместных процессов очистки сточных вод и биологического удаления биогенных элементов путем нитрификации-денитрификации и дефосфатации требует создания в аэротенке последовательно расположенных в определенном порядке анаэробных, аноксидных и аэробных зон со специально организованными рециркуляционными потоками активного ила и нитрифицированной воды. Однако, имеющиеся сложности, связанные с одновременным проведением этих процессов в одном рабочем объеме аэротенка, в том числе необходимостью одновременного обеспечения большого возраста активного ила, оптимального для прохождения нитрификации, и малого возраста, требуемого для удаления фосфора, на практике привело к появлению большого числа вариантов и схем расположения зон, различных конфигураций аэротенков. Несмотря на общие черты наиболее перспективных схем, существующие различия указывают на отсутствие в настоящее время общепринятых окончательных технических решений получения очищенной воды. Концентрацию аммонийного азота, нитратов, нитритов, фосфора в очищенной воде, необходимо контролировать, проводя лабораторное исследование воды. Химический анализ проб очищенной воды заключается в определении концентрации иона аммония фотометрическим методом с реактивом Несслера, концентрации нитрат-ионов фотометрическим методом с салициловой кислотой. При необходимости проводится полный химический анализ воды, для того, чтобы убедиться в ее безопасности.
Однако, имеющиеся сложности, связанные с одновременным проведением этих процессов в одном рабочем объеме аэротенка, в том числе необходимостью одновременного обеспечения большого возраста активного ила, оптимального для прохождения нитрификации, и малого возраста, требуемого для удаления фосфора, на практике привело к появлению большого числа вариантов и схем расположения зон, различных конфигураций аэротенков. Несмотря на общие черты наиболее перспективных схем, существующие различия указывают на отсутствие в настоящее время общепринятых окончательных технических решений получения очищенной воды. Концентрацию аммонийного азота, нитратов, нитритов, фосфора в очищенной воде, необходимо контролировать, проводя лабораторное исследование воды. Химический анализ проб очищенной воды заключается в определении концентрации иона аммония фотометрическим методом с реактивом Несслера, концентрации нитрат-ионов фотометрическим методом с салициловой кислотой. При необходимости проводится полный химический анализ воды, для того, чтобы убедиться в ее безопасности.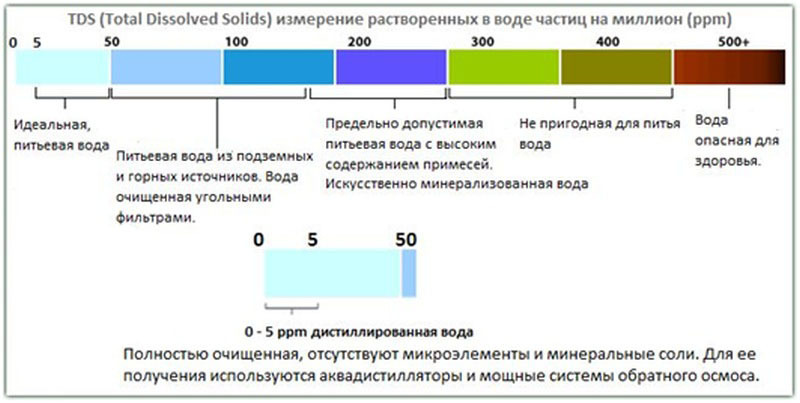
Основными критериями, определяющими перспективы использования очищенных сточных вод, является их количество и качество. Наиболее перспективным является использование очищенной воды для целей орошения в сельском хозяйстве. Объемы поливной воды должны быть постоянны и не зависеть от погодных условий, для обеспечения проведения поливов в вегетационный период. Учитывая рост численности населения и увеличивающиеся темпы урбанизации, основным поставщиком альтернативного водного ресурса будет коммунальное хозяйство. Очищенные сточные воды канализационно-очистных сооружений населенных пунктов, могут быть использованы для целей орошения кормовых, технических и древесно-кустарниковых культур.
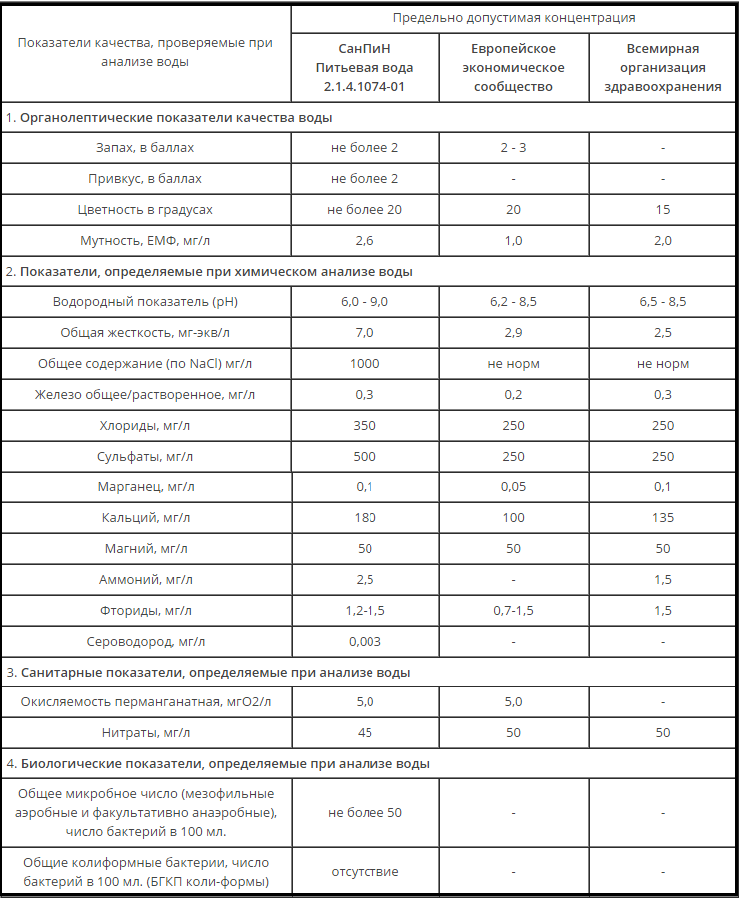
Лабораторное исследования очищенных сточных вод с целью оценки их пригодности для орошения должно включать: отбор проб очищенных стоков для определения их химического состава а также изучение их токсичности на основании лабораторных опытов с использованием метода биотестирования. Для определения качества прошедших очистку сточных вод проводят химический анализ воды очищенной по следующему перечню показателей: минерализация, Са2+, Mg2+, Na+ , K+ , НСО3 — , СО32- , SO42- , Cl— , рН в лаборатории воды.
Ключевые слова:качественный анализ воды очищенной,анализ воды очищенной после очистных сооружений, анализ воды после очистных сооружений когда необходимо производить,отбор проб анализ работы очистных сооружений,очищенные стоки после очистных сооружений анализ воды очищенной,общие сроки контроля очистных сооружений сточных вод анализ очищенной воды лаборатория, сброс в водные объекты после очистных сооружений как надо проводить анализ воды очищенной,проверка эффективности работы очистных сооружений куда сдать очищенную воду на анализ сроки цена периодичность отбора воды после очистных сооружений.
Лаборатории МАГАТЭ проводят анализ проб очищенной воды с АЭС «Фукусима-дайити»
16.09.2022
Джоанн Лю, Бюро общественной информации и коммуникации МАГАТЭ
Целевая группа МАГАТЭ посетила подземную счетную лабораторию в составе Лаборатории радиометрии МАГАТЭ в Монако. Этот подземный объект создан для ограничения помех от фонового излучения, благодаря чему исследователи могут обнаруживать очень низкие уровни радиоактивности в различных пробах окружающей среды, включая морскую воду.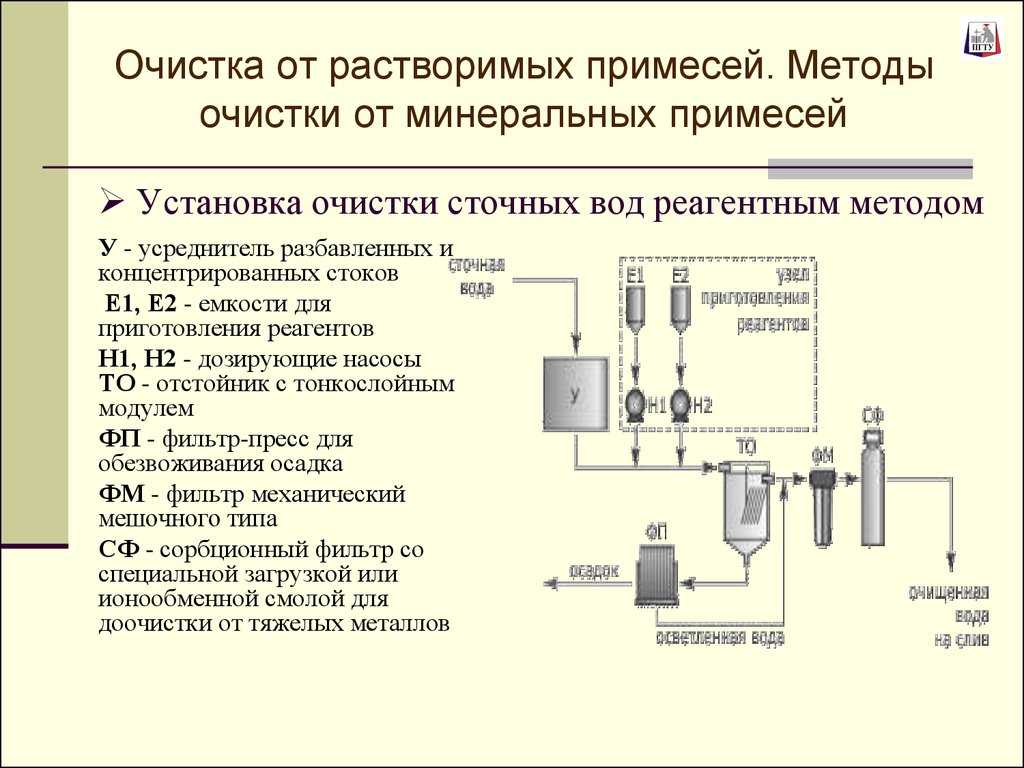 (Фото: МАГАТЭ)
(Фото: МАГАТЭ)
Для проверки представленных Японией данных МАГАТЭ выполняет независимый анализ и подтверждение данных, касающихся сброса очищенной воды с АЭС «Фукусима-дайити». Эта деятельность представляет собой одно из направлений экспертной работы по рассмотрению трех основных аспектов безопасности, проводимой целевой группой МАГАТЭ, которая была учреждена Генеральным директором Рафаэлем Мариано Гросси в 2021 году и включает в свой состав 11 международных экспертов из разных стран мира, а также сотрудников МАГАТЭ. Два других направления — техническая оценка мер по обеспечению безопасности и защите населения и рассмотрение деятельности и процессов регулирующего органа; в данный момент по ним также ведется работа, которую планируется завершить выпуском всеобъемлющего доклада в 2023 году, перед тем как будет начат сброс очищенной воды.
Проводимый в настоящее время анализ очищенной воды призван подтвердить радиологические характеристики, представленные оператором АЭС «Фукусима-дайити» — Токийской электроэнергетической компанией (ТЕПКО). ТЕПКО отвечает за определение того, пригодна ли вода, прошедшая очистку с целью удаления из нее 62 различных радионуклидов, для сброса в окружающую морскую акваторию. После аварии на АЭС «Фукусима-дайити» в 2011 году вода, используемая для охлаждения расплавленного топлива и обломков топлива, очищалась и хранилась на площадке. Работа МАГАТЭ по подтверждению данных будет продолжаться и после начала запланированного на 2023 год сброса очищенной воды, что является частью обязательства Генерального директора Гросси поддерживать сотрудничество на всех этапах до, во время и после сброса очищенной воды.
ТЕПКО отвечает за определение того, пригодна ли вода, прошедшая очистку с целью удаления из нее 62 различных радионуклидов, для сброса в окружающую морскую акваторию. После аварии на АЭС «Фукусима-дайити» в 2011 году вода, используемая для охлаждения расплавленного топлива и обломков топлива, очищалась и хранилась на площадке. Работа МАГАТЭ по подтверждению данных будет продолжаться и после начала запланированного на 2023 год сброса очищенной воды, что является частью обязательства Генерального директора Гросси поддерживать сотрудничество на всех этапах до, во время и после сброса очищенной воды.
«В рамках рассмотрения аспектов безопасности МАГАТЭ опирается на мощный потенциал наших лабораторий, что обеспечивает высокую степень прозрачности и дает уверенность международному сообществу», — сказал Густаво Карузо, директор одного из подразделений МАГАТЭ и председатель целевой группы.
Лаборатории МАГАТЭ обеспечивают всесторонний анализ
Во время посещения целевой группой МАГАТЭ Лаборатории радиохимии наземной среды в Зайберсдорфе поступила партия проб очищенной воды с АЭС «Фукусима-дайити». (Фото: МАГАТЭ)
(Фото: МАГАТЭ)
Три из четырех участвующих в этой работе лабораторий МАГАТЭ являются лабораториями изучения окружающей среды, в том числе Лаборатория изотопной гидрологии в Вене, Лаборатория радиохимии наземной среды в Зайберсдорфе, который находится в 35 км к югу от Вены, и Лаборатория радиометрии в Монако. Последняя из упомянутых лабораторий — это Лаборатория технических служб по обеспечению радиационной безопасности в Вене.
В период с 29 августа по 2 сентября целевая группа провела заседание в Вене и совершила поездки в Зайберсдорф и Монако для посещения всех четырех лабораторий. Члены группы обсудили аналитические методы оценки содержания радионуклидов в пробах, график работы и будущие потребности в анализе дополнительных проб.
Эксперты МАГАТЭ проинформировали целевую группу о подготовительных операциях, которые требуются для анализа более 30 различных радиоизотопов в каждой пробе воды с помощью современных приборов. Эксперты объяснили различия в том, как производятся измерения по каждому радиоизотопу и как подготавливаются пробы. Использование совместных технических разработок в лабораториях в сочетании с раздельным анализом единичных проб позволяет получить наиболее точные результаты даже в сложных случаях анализа на редкие радионуклиды. «Лаборатории МАГАТЭ работают совместно, чтобы обеспечить всеобъемлющий и научно обоснованный характер анализа и подтвердить данные ТЕПКО. Мы прилагаем все усилия к тому, чтобы первые результаты были представлены международному сообществу до начала сброса воды в 2023 году», — резюмировал Карузо.
Использование совместных технических разработок в лабораториях в сочетании с раздельным анализом единичных проб позволяет получить наиболее точные результаты даже в сложных случаях анализа на редкие радионуклиды. «Лаборатории МАГАТЭ работают совместно, чтобы обеспечить всеобъемлющий и научно обоснованный характер анализа и подтвердить данные ТЕПКО. Мы прилагаем все усилия к тому, чтобы первые результаты были представлены международному сообществу до начала сброса воды в 2023 году», — резюмировал Карузо.
Целевая группа обсудила также методы, позволяющие подтвердить потенциал ТЕПКО и АЭС «Фукусима-дайити» в области радиационной защиты при профессиональным облучении, и ход подготовки к этой работе. Предложенное техническое рассмотрение и оценка основываются на требованиях к оценке профессионального облучения, изложенных в Общем руководстве по безопасности № GSG-7.
В начале этого года МАГАТЭ содействовало проведению двух кампаний по отбору проб очищенной воды на АЭС «Фукусима-дайити» для их анализа Агентством и сторонними лабораториями.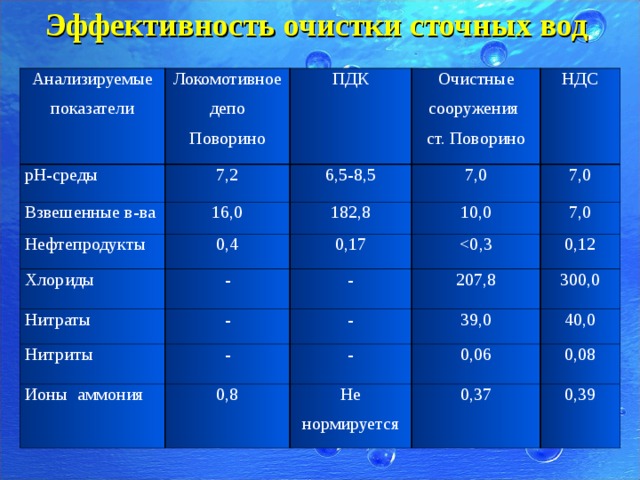 В предстоящие месяцы и годы планируется проведение дополнительных кампаний по отбору проб как на площадке «Фукусима-дайити», так и в окружающей акватории. МАГАТЭ ежегодно организует регулярные аттестационные испытания для примерно 500 лабораторий, занимающихся измерениями содержания радионуклидов в окружающей среде, которые служат отправной точкой для оценки качества и возможностей участвующих лабораторий.
В предстоящие месяцы и годы планируется проведение дополнительных кампаний по отбору проб как на площадке «Фукусима-дайити», так и в окружающей акватории. МАГАТЭ ежегодно организует регулярные аттестационные испытания для примерно 500 лабораторий, занимающихся измерениями содержания радионуклидов в окружающей среде, которые служат отправной точкой для оценки качества и возможностей участвующих лабораторий.
Подробнее об очищенной воде на АЭС «Фукусима-дайити» и работе МАГАТЭ по рассмотрению аспектов безопасности
В апреле 2021 года Япония обнародовала базовую политику обращения с очищенной водой, хранящейся на площадке АЭС «Фукусима-дайити», которая предусматривает постепенный сброс очищенной воды в море рядом со станцией, при условии получения разрешений национального регулирующего органа. Собираемая на площадке после аварии 2011 года вода подвергается очистке с помощью процесса фильтрации через так называемую усовершенствованную систему водоочистки (ALPS), в которой используется серия химических реакций для удаления из воды 62 радионуклидов.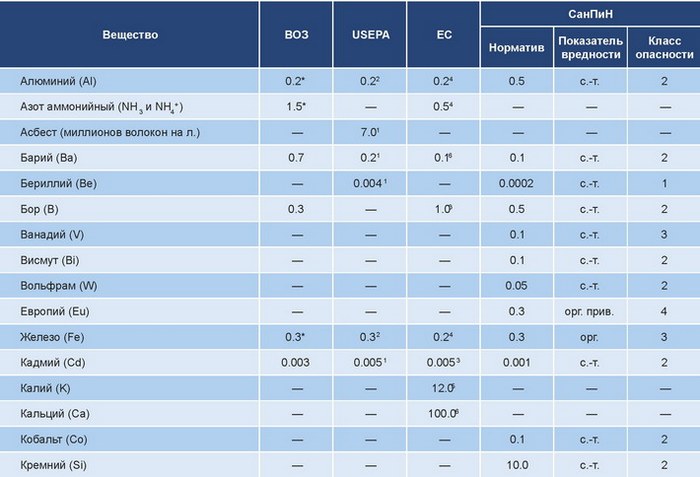 Однако ALPS не позволяет удалить из загрязненной воды тритий (см. дополнение «Наука»). Вскоре после этого власти страны обратились к МАГАТЭ с просьбой организовать мониторинг и рассмотрение планов и мероприятий, связанных со сбросом очищенной воды, в целях обеспечения безопасности и прозрачности их реализации. В 2021 году Генеральный директор Гросси учредил целевую группу для проведения в интересах Японии и международного сообщества объективного и научно обоснованного рассмотрения безопасности операций по сбросу воды на площадке. С тех пор группа в составе более 25 экспертов, в том числе из стран региона, провела восемь заседаний и совершила пять выездов на площадку АЭС «Фукусима-дайити».
Однако ALPS не позволяет удалить из загрязненной воды тритий (см. дополнение «Наука»). Вскоре после этого власти страны обратились к МАГАТЭ с просьбой организовать мониторинг и рассмотрение планов и мероприятий, связанных со сбросом очищенной воды, в целях обеспечения безопасности и прозрачности их реализации. В 2021 году Генеральный директор Гросси учредил целевую группу для проведения в интересах Японии и международного сообщества объективного и научно обоснованного рассмотрения безопасности операций по сбросу воды на площадке. С тех пор группа в составе более 25 экспертов, в том числе из стран региона, провела восемь заседаний и совершила пять выездов на площадку АЭС «Фукусима-дайити».
В начале этого года целевая группа МАГАТЭ выпустила свой первый доклад о безопасности планируемого сброса воды, а в июне был выпущен второй доклад, касающийся аспектов регулирования. Третий доклад, который, как ожидается, будет опубликован позднее в этом году, будет включать всеобъемлющий обзор планируемой МАГАТЭ деятельности по подтверждению соответствующих радиологических данных в рамках проводимого им более широкого рассмотрения аспектов безопасности.
Узнайте больше о сбросе очищенной воды на АЭС «Фукусима-дайити».
Ресурсы по теме
16.09.2022
Очищенная вода – Процедура отбора проб и испытаний
Очищенная вода – Процедура отбора проб и испытаний
- Автор сообщения: pharmabeginers
- Сообщение опубликовано: 23 мая 2020 г.
- Категория поста: cGMP / контрольный список / форматы / GLP / Micro Sop / Microbiology / SOPs
Стандартная операционная процедура (СОП) для отбора проб из разных точек и микробиологического анализа/тестирования проб очищенной воды на фармацевтических предприятиях.
Отбор проб и анализ очищенной воды в микробиологии
1.0 НАЗНАЧЕНИЕ:
- Установить процедуру отбора проб и испытаний очищенной воды.
2.
 0 ОБЛАСТЬ ПРИМЕНЕНИЯ:
0 ОБЛАСТЬ ПРИМЕНЕНИЯ:
- Настоящая стандартная операционная процедура применима к отделению микробиологии.
3.0 ССЫЛКА:
- Асептическая методика микробиологического тестирования.
- Мониторинг качества воды для фармацевтических целей.
- СОП по анализу проб воды.
- IP/BP/USP
4.0 ОТВЕТСТВЕННОСТЬ:
- Сотрудник или руководитель отдела микробиологии несет ответственность за подготовку новых или пересмотр существующих СОП.
- За рассмотрение СОП отвечает руководитель отдела/должностное лицо, ответственное за соответствующие области и отдел обеспечения качества.
- Руководитель отдела обеспечения качества несет ответственность за утверждение СОП.

- Руководитель отдела обеспечения качества несет ответственность за утверждение СОП.
5.0 СПИСОК СОКРАЩЕНИЙ:
- CCR: изменение контрольной записи
- КОЕ: колониеобразующая единица
- Сертификат подлинности: Сертификат анализа
- °C: Градусы Цельсия
- HCL: соляная кислота
- ИПС: Изопропиловый спирт
- мл: миллилитр
- ppb: миллиардная часть
- TOC: Общий органический углерод
6.0 ОПРЕДЕЛЕНИЕ:
Предел предупреждений:
- Превышение микробных уровней, указанных в стандартной рабочей процедуре или спецификациях, должно привести к расследованию, чтобы убедиться, что процесс все еще находится под контролем.

- Превышение микробных уровней, указанных в стандартной рабочей процедуре или спецификациях, должно привести к расследованию, чтобы убедиться, что процесс все еще находится под контролем.
- Уровни тревоги специфичны для данного объекта и устанавливаются на основе исходного уровня, разработанного в рамках программы мониторинга деятельности.
- Эти уровни предупреждений могут быть изменены в зависимости от анализа тенденций, выполненного в программе мониторинга. Уровни предупреждений всегда ниже уровней действий.
7.0 ПРОЦЕДУРА ОТБОРА ПРОБ И ИСПЫТАНИЙ ОЧИЩЕННОЙ ВОДЫ
:
- Для химического анализа:
- Чистые бутылки из прозрачного стекла объемом 1000 мл с крышкой. Промойте очищенной водой.
- Для анализа TOC:
- Бутыли из янтарного стекла объемом 125 мл или подходящие бутылки с пробкой промыть 2,0 М HCl или 2,0% азотной кислотой, промыть очищенной водой и высушить бутылки при 105 ºC не менее одного часа.

- Бутыли из янтарного стекла объемом 125 мл или подходящие бутылки с пробкой промыть 2,0 М HCl или 2,0% азотной кислотой, промыть очищенной водой и высушить бутылки при 105 ºC не менее одного часа.
- Для микробиологического анализа:
- Clean 250 мл Прозрачные стеклянные бутылки с крышкой для метода мембранной фильтрации или метода наливной пластины и ополаскивания очищенной водой.
- Закройте бутыль крышкой, оберните горлышко алюминиевой фольгой и стерилизуйте бутыль при температуре 121 ºC (15 фунтов) в течение установленного времени.
- См. Приложение-2 для подготовки Графика отбора проб. составьте график таким образом, чтобы точка генерации (для химического и микробиологического анализа) и обратная петля (только для микробиологического анализа) покрывались ежедневно, а другие полезные точки (только для микробиологического анализа) поочередно в течение месяца.
- Подготовьте график отбора проб (ориентировочный) к первому рабочему дню каждого Нового года.

- Подготовьте график отбора проб (ориентировочный) к первому рабочему дню каждого Нового года.
- Напишите детали отбора проб или наклейте этикетку на бутылку в соответствии с Приложением-3.
- Доставить контейнеры для отбора проб к месту отбора проб в соответствии с графиком отбора проб.
- Продезинфицируйте руки 70 % об./об. изопропиловым спиртом. Перед отбором проб наденьте перчатки и маску для носа.
- Промойте контейнер не менее одного-двух раз очищенной водой из точки отбора проб.
- Наполните контейнеры 1000 мл и 125 мл или до горлышка очищенной водой для химического анализа и анализа TOC соответственно и немедленно закройте крышку.
- Проанализируйте образец ТОС как можно быстрее по прибытии в лабораторию.
- Если немедленный анализ невозможен, подкислите образец 2-3 каплями 2,0 М HCl и храните образец в холодильнике при температуре от 2 до 8ºC.

- Если немедленный анализ невозможен, подкислите образец 2-3 каплями 2,0 М HCl и храните образец в холодильнике при температуре от 2 до 8ºC.
- Эти сохраненные образцы должны быть проанализированы в течение 6 часов.
- Держите стерильный контейнер рядом с точкой отбора проб.
- Разверните алюминиевую фольгу и откройте бутылку, стараясь не касаться внутренней поверхности и горлышка бутылки.
- Соберите образец очищенной воды (см. таблицу 1) без ополаскивания и немедленно закройте его пробкой.
- Не наполняйте флакон до горлышка.
- Оберните горловину алюминиевой фольгой, чтобы избежать загрязнения во время транспортировки.
- Закройте вентиль и отнесите пробы в лабораторию и сделайте запись в журнале поступления очищенной воды.
- Выполните анализ в соответствии с текущей версией спецификации очищенной воды.

- Выполните анализ в соответствии с текущей версией спецификации очищенной воды.
- Как можно быстрее проанализируйте образец по прибытии в лабораторию.
- Если немедленный анализ невозможен, храните образец в холодильнике при температуре от 2 до 8ºC.
- Эти сохраненные образцы должны быть проанализированы в течение 6 часов.
Таблица 1
| Параметры испытаний | Количество проб | Бутыль для проб |
| Химический анализ | 1000 мл | Нестерильный |
| Анализ ТОС | 125 мл | Нестерильный |
| Микробиологический анализ | 250 мл | Стерильный |
- Перед анализом зарегистрируйте/зарегистрируйте образец и сгенерируйте/выпустите рабочий лист или шаблон.

- Перед анализом зарегистрируйте/зарегистрируйте образец и сгенерируйте/выпустите рабочий лист или шаблон.
- Назначенное лицо выдает шаблон/рабочий лист.
- Проанализируйте образец очищенной воды на общее количество жизнеспособных организмов, используя метод фильтрации в соответствии с текущими спецификациями очищенной воды.
- Проанализируйте образец очищенной воды на наличие патогенов с помощью метода фильтрации/Прямого в соответствии с действующими техническими условиями очищенной воды.
- Провести химический анализ проб в соответствии с действующей версией технических условий на воду очищенную.
- Отбор проб из коммунальных систем требует особой осторожности, так как пробы отбираются в контролируемых и неконтролируемых зонах предприятия.
- Персонал, занимающийся отбором проб, должен надевать чистые халаты или халаты и стерильные перчатки перед отбором любой пробы (в соответствии с требованиями зоны).

- Персонал, занимающийся отбором проб, должен надевать чистые халаты или халаты и стерильные перчатки перед отбором любой пробы (в соответствии с требованиями зоны).
- Пробоотборники и контейнеры должны быть чистыми, стерильными и/или свободными от эндотоксинов в соответствии с требованиями испытаний.
- Сотрите всю видимую пыль с внешней стороны порта пробы или клапана с помощью безворсовой салфетки/ткани, смоченной утвержденным дезинфицирующим средством – не распыляйте и не протирайте внутреннюю часть порта или клапана.
- Убедитесь, что достигнуто необходимое время контакта дезинфицирующего средства.
- Если шланг уже подсоединен к порту или клапану, возьмите образец непосредственно из этого шланга.
- Если шланг не подключен, но имеется, подсоедините шланг, используя процедуры, применимые для данной системы.
- Замените использованный шланг на прилагаемый зажим после отбора проб, чтобы он полностью стекал.

- Замените использованный шланг на прилагаемый зажим после отбора проб, чтобы он полностью стекал.
- Если шланг отсутствует, можно использовать стерилизованный адаптер и шланг для отбора проб непосредственно из клапана/порта.
- Промойте порт/клапан пробы в течение установленного времени или объема и немедленно откройте маркированный контейнер для проб и соберите пробу.
- Немедленно закройте контейнер и запишите время отбора проб.
| Места отбора проб | Тип анализа | Частота |
| Точка генерации | Химическая промышленность TOC/Окисляемое вещество Общее количество микробов Наличие патогенов | Ежедневно |
| Обратный контур | Общее количество микробов Наличие патогенов | Ежедневно |
| Пользовательские баллы | Общее количество микробов Наличие патогенов | Ежемесячно |
- Ограничение: Общее количество микробов не должно превышать 100 КОЕ/мл, патогены должны отсутствовать.
 Общий органический углерод не должен превышать 500 частей на миллиард.
Общий органический углерод не должен превышать 500 частей на миллиард.
| Наименование испытания | Предел предупреждений | Ограничение действия | Ограничение спецификации |
| рН | 6,5 | 6,8 | 5-7 |
| Электропроводность (мк/С) | 3,5 | 4,4 | 5,1 |
| ROE (%) | 0,0008 | 0,0009 | 0,001 |
| TOC (ppb) | 400 | 450 | 500 |
| ТМС (КОЕ/мл) | 65 | 83 | 100 |
- После завершения аналитического отчета проверяется и утверждается назначенным лицом, после чего создается сертификат подлинности (при необходимости).
Связанный: Контрольный список для обзора данных микробиологии
- Если какой-либо химический параметр превышает предел, немедленно сообщите об этом в тот же отдел обеспечения качества, производственный и технический отдел.

- Если какой-либо химический параметр превышает предел, немедленно сообщите об этом в тот же отдел обеспечения качества, производственный и технический отдел.
- Если общее количество бактерий превышает предел предупреждения/предел действия, немедленно сообщите об этом отделу обеспечения качества и инженерному персоналу, и должно быть проведено расследование в соответствии с СОП «Обработка микробной экскурсии в воде и окружающей среде».
- Фаза 1 посвящена методу и аналитику; цель этапа 1 состоит в том, чтобы проверить достоверность данных. Ошибка аналитика должна быть редкостью. Необходимо выполнить немедленную повторную выборку конкретного места, где произошло OOT/OOS, чтобы быстро оценить состояние системы.
- Этап 2 следует за определением достоверности данных и исследует систему водоснабжения и все потенциально затронутые партии продуктов.
- Этап 2 требует анализа основных причин и корректирующих действий.
Связанный: СОП по корректирующим и предупреждающим действиям (CAPA)
- Анализ динамики параметров качества очищенной воды Ежемесячно, анализ трендовых графиков и заключение (при необходимости).

- Анализ динамики параметров качества очищенной воды Ежемесячно, анализ трендовых графиков и заключение (при необходимости).
- Важно регулярно выявлять организмы, извлеченные из водных систем, когда:
- Переносимые водой организмы могут быть вредными для готовой продукции или процессов, в которых используется вода.
- Необходимо установить источник загрязнения.
- Методы санитарной обработки системы водоснабжения требуют оценки.
- Важно отметить, что вам не нужно превышать спецификацию, чтобы отправить результат на идентификацию, рекомендуется документировать, выбирать и идентифицировать репрезентативную флору из системы.
8.0 ПРИЛОЖЕНИЯ – ОЧИЩЕННАЯ ВОДА:
| Старший № | Название места | Идентификационный № образца |
1. | Этаж обслуживания резервуара для хранения PW | Пароль 01 |
| 2. | После УФ-обработки | PW 02 |
| 3. | Блендер Granulation-III | Пароль 03 |
| 4. | Грануляция сухой мельницы-III | PW 04 |
| 5. | Грануляция FBD-III | Пароль 05 |
| 6. | Приготовление пасты Грануляция-III | PW06 |
| 7. | Грануляция RMG-III | Пароль 07 |
| 8. | Miller and Sifter Granulation-III | Пароль 08 |
| 9. | Блендер Granulation-IV | Пароль 09 |
| 10. | Грануляция сухой мельницы-IV | Пароль 10 |
| 11. | Грануляция RMG-IV | Пароль 11 |
| 12. | Miller and Sifter Granulation-IV | Пароль 12 |
13. | Приготовление пасты Грануляция-IV | Пароль 13 |
| 14. | Мойка Второй этаж | № 14 |
| 15. | Очистка оборудования второго этажа | № 15 |
| 16. | Зона приготовления раствора для покрытия II | № 16 |
| 17. | Зона подготовки раствора для покрытия I | № 17 |
| 18. | Капсула III | № 18 |
| 19. | Среднеквадратичная стирка | № 19 |
| 20. | Покрытие I | № 20 |
| 21. | Покрытие II | PW21 |
| 22. | Покрытие III | № 22 |
| 23. | Покрытие IV | № 23 |
S. № | Название места | Идентификационный номер образца |
24. | Покрытие V | № 24 |
| 25. | Покрытие VI | № 25 |
| 26. | Зона промывки покрытия | № 26 |
| 27. | Блендер Грануляция II | № 27 |
| 28. | Грануляция для сухого помола II | № 28 |
| 29. | Упаковка зоны мойки | № 29 |
| 30. | Грануляция FBD II | № 30 |
| 31. | Грануляция RMG II | № 31 |
| 32. | Просеивание и измельчение Грануляция II | № 32 |
| 33. | Просеивание и измельчение I Грануляция I | № 33 |
| 34. | Грануляция RMG I | № 34 |
| 35. | Грануляция FBD I | ПВ 35 |
| 36. | Грануляция сухой мельницы I | № 36 |
37. | Смешивание гранул I | № 37 |
| 38. | Приготовление пасты I | № 38 |
| 39. | Приготовление пасты II | Пароль 39 |
| 40. | Сжатие зоны мойки | номер 40 |
| 41. | Компрессия-17 | № 41 |
| 42. | IPQC I | номер 42 |
| 43. | Покрытие IX | № 43 |
| 44. | Покрытие VIII | № 44 |
| 45. | Подготовка раствора для покрытия III | номер 45 |
| 46. | Покрытие VII | № 46 |
С. № | Название места | Идентификационный номер образца |
| 47. | IPQC II | № 47 |
48. | Контроль качества | № 48 |
| 49. | Впускной патрубок УФ после смесительного слоя | PW49 |
| 50. | Выход УФ-излучения после смешения | PW50 |
| 51. | Возвратный контур резервуара для хранения PW | № 51 |
| 52. | Переключение гр.V | PW52 |
| 53. | РМГ гр.V | PW53 |
| 54. | ФБД гр.V | ПВ54 |
| 55. | Сухое фрезерование гр. V | ПВ55 |
| 56. | Блендер гр.V | PW56 |
| 57. | Мойка гр.V | PW57 |
| 58. | Блендер гр.VI | PW58 |
| 59. | РМГ гр.VI | PW59 |
| 60. | Миллер и Шифтер гр.VI | PW60 |
61. | Мойка гр.VI | PW61 |
| 62. | IPQC III | PW62 |
| 63. | Покрытие Х | PW63 |
| 64. | Покрытие XI | PW64 |
| 65. | Покрытие XII | PW65 |
| 66. | Помещение для приготовления пасты гр.VI | PW66 |
| 67. | Моечная (новый RMS) | PW67 |
| 68. | Зона подготовки подвески IV | PW68 |
| 69. | Грануляция VII | PW69 |
S. № | Название места | Идентификационный номер образца |
| 70. | Грануляция VIII | PW70 |
| 71. | УФ-вход | ПВШ01 |
72. | УФ-выход | ПВШ02 |
| 73. | SH покрытие | ПВШ03 |
| 74. | Помещение для подготовки подвески | ПВШ04 |
| 75. | IPQC | ПВШ05 |
| 76. | Зона мойки SH | ПВШ06 |
| 77. | SH грануляция | ПВШ07 |
| 78. | SH грануляция | ПВШ08 |
| 79. | Дозирование | ПВШ09 |
| 80. | Кладовая | ПВШ20 |
| 81. | Дренаж обратной линии | ПВШ21 |
Теги: Частота отбора проб очищенной воды, Идентификация микроорганизмов (водные изоляты), Меры предосторожности при отборе проб очищенной воды, Тенденции результатов очищенной воды
фармацевты
Янки Сингх имеет опыт работы в области фармацевтики, автор и основатель Pharma Beginners, передовой платформы для ведения фармацевтических блогов.
Электронная почта: [email protected]
Фармацевтические испытания воды | CPT℠ Labs
Pharmaceutical Water Testing
Можно с уверенностью сказать, что вода является наиболее часто используемым материалом в фармацевтической промышленности. Он используется в качестве вспомогательного ингредиента в лекарственных препаратах, для очистки технологического оборудования и при тестировании лекарственных препаратов и связанных с ними материалов. Поскольку лекарственные препараты изначально разрабатываются и создаются для улучшения здоровья, вода, используемая при их производстве и тестировании, должна иметь соответствующий уровень чистоты. Чтобы определить пригодность воды для любого фармацевтического применения, она должна быть проверена на наличие загрязнителей, включая, помимо прочего, органический углерод, электролитические материалы и микробиологические организмы.
Фармакопея США (или просто «USP») содержит свод методов испытаний, спецификации и общую информацию, касающуюся фармацевтической воды в США. USFDA признает USP официальным «Стандартом» для фармацевтических продуктов и связанных с ними материалов, методологий тестирования и спецификаций. В результате FDA основывает свои инспекционные ожидания для фармацевтической воды на методах и спецификациях USP. Другие юрисдикции имеют аналогичные сборники, такие как Британская фармакопея (или «BP»), Европейская фармакопея (или «EP») и Японская фармакопея (или «JP»). Следует отметить, что существуют различия между различными сборниками, поэтому важно сверяться с официальными справочниками юрисдикции, в которой будет производиться и/или распространяться фармацевтический продукт, чтобы обеспечить соответствие этого продукта нормативным требованиям.
USFDA признает USP официальным «Стандартом» для фармацевтических продуктов и связанных с ними материалов, методологий тестирования и спецификаций. В результате FDA основывает свои инспекционные ожидания для фармацевтической воды на методах и спецификациях USP. Другие юрисдикции имеют аналогичные сборники, такие как Британская фармакопея (или «BP»), Европейская фармакопея (или «EP») и Японская фармакопея (или «JP»). Следует отметить, что существуют различия между различными сборниками, поэтому важно сверяться с официальными справочниками юрисдикции, в которой будет производиться и/или распространяться фармацевтический продукт, чтобы обеспечить соответствие этого продукта нормативным требованиям.
Варианты тестирования
Фармакопея США устанавливает спецификации для каждого из различных типов воды, которые используются фармацевтической промышленностью в США. Наиболее распространенным типом является очищенная вода , которую можно использовать в качестве ингредиента в нестерильных/непарентеральных лекарственных препаратах, в качестве средства для очистки технологического оборудования, а также при тестировании лекарственных препаратов и связанных с ними материалов.
Спецификации для различных типов фармацевтической воды будут различаться в зависимости от области применения. Таким образом, требования к тестированию для Вода для инъекций или Вода для гемодиализа будет отличаться от требований к очищенной воде . Монография USP для каждого типа фармацевтической воды включает требования к тестированию, которые специально разработаны для типа лекарственного препарата или применения, в котором будет использоваться вода.
- Общий органический углерод: Хотя некоторые тесты проводятся только для определенного типа фармацевтической воды, существуют и другие тесты более общего характера, применимые к большинству, если не ко всем типам воды. Первым из этих «общих» тестов воды является общий органический углерод (или «TOC»). Этот тест требуется почти для всех типов фармацевтической воды здесь, в США, и в юрисдикциях по всему миру. Фармацевтическая вода должна быть относительно бесплатной ( < 500 частей на миллиард здесь, в США) органических углеродсодержащих соединений, что свидетельствует о наличии в воде химических и/или микробиологических примесей.
 Примеры химических загрязнителей, которые обнаруживаются при тестировании TOC, включают, помимо прочего, ацетон, метилэтилкетон и бензин. Поскольку все микробиологические организмы состоят в основном из молекул углерода, они также могут быть обнаружены с помощью тестирования TOC, примеры которого включают pseudomonas aeruginosa 9.0217 и кишечная палочка.
Примеры химических загрязнителей, которые обнаруживаются при тестировании TOC, включают, помимо прочего, ацетон, метилэтилкетон и бензин. Поскольку все микробиологические организмы состоят в основном из молекул углерода, они также могут быть обнаружены с помощью тестирования TOC, примеры которого включают pseudomonas aeruginosa 9.0217 и кишечная палочка. - Проводимость воды: Другим распространенным тестом, который проводится с фармацевтической водой, является проводимость воды. Электропроводность в воде определяется USP как «мера потока электронов, облегчаемого ионами, через нее». Следовательно, присутствие ионов в воде позволит протекать через нее электрическому току, тогда как полное отсутствие таких ионов не будет способствовать протеканию электрического тока. Тест на проводимость воды используется для обнаружения присутствия в воде посторонних ионов, которые облегчают протекание электрического тока через воду. Примеры посторонних ионов включают, помимо прочего, катионы металлов (Fe +3 или Mg +2 ) и специфические анионы, такие как фосфат (PO 4 -3 ), хлорид (Cl –) и аммоний (NH 4 + ).
 Поскольку чрезвычайно низкие уровни ионов облегчают электрический ток, USP предоставляет спецификацию для приемлемого уровня, выраженного в микросименсах, которые являются минутными единицами электрического тока.
Поскольку чрезвычайно низкие уровни ионов облегчают электрический ток, USP предоставляет спецификацию для приемлемого уровня, выраженного в микросименсах, которые являются минутными единицами электрического тока. - Окисляемые вещества и Твердые частицы в инъекциях: Другие фармацевтические тесты воды включают окисляемые вещества и твердые частицы в инъекциях. Окисляемые вещества тестируют на наличие молекул, которые легко соединяются с кислородом. Перманганат калия, сильный и ярко окрашенный окислитель, используется для обозначения присутствия в воде окисляемых веществ. Примеры загрязняющих веществ, которые обнаруживаются с помощью этого теста, включают, помимо прочего, микробиологические организмы, биологические соединения и соединения, содержащие металлы. Что касается твердых частиц в инъекциях, как следует из названия, этот тест используется для определения присутствия твердых частиц, которые могут присутствовать в фармацевтической воде.
 Твердые частицы вызывают большую озабоченность, если вода используется для офтальмологических или инъекционных препаратов.
Твердые частицы вызывают большую озабоченность, если вода используется для офтальмологических или инъекционных препаратов. - Микробиологические испытания: Хотя микробиологические испытания не включены в монографии Фармакопеи США для каждого типа фармацевтической воды, FDA рассматривает отдельные монографии как содержащие только «минимальные» требования к качеству и полностью ожидает, что все типы фармацевтической воды, которые производятся из системы очистки на участке их использования («наливные» воды) для регулярного контроля на предмет микробиологического загрязнения. В Общей главе Фармакопеи США <1231>, озаглавленной «Вода для фармацевтических целей», указаны методы испытаний, адаптированные из Фармакопеи США <61>, озаглавленной «Тесты для подсчета микробов», и Фармакопеи США <62>, «Тест на определенные организмы», которые подходят для контроля качества фармацевтической продукции. Вода.
- Биопленки: Одной из самых серьезных проблем, связанных с системами очистки воды, является образование биопленок.
 Общая глава USP <1231> Раздел 8.2 определяет биопленку как «трехмерное структурированное сообщество неподвижных микробных клеток, встроенных в матрицу внеклеточных полимерных веществ (EPS)». Биопленки образуются, когда бактерии прикрепляются к поверхностям во влажной среде и производят слизистое, похожее на клей вещество, матрицу EPS, при этом размножаясь в этом месте. После закрепления другие микроорганизмы могут прикрепляться к матрице ЭПС, создавая таким образом микробное «сообщество». Трехмерная структура биопленок объясняет их устойчивость к большинству химических дезинфицирующих средств, которые с трудом проникают через ЭПС. Наиболее эффективным методом удаления биопленки из системы водоснабжения является термическая дезинфекция.
Общая глава USP <1231> Раздел 8.2 определяет биопленку как «трехмерное структурированное сообщество неподвижных микробных клеток, встроенных в матрицу внеклеточных полимерных веществ (EPS)». Биопленки образуются, когда бактерии прикрепляются к поверхностям во влажной среде и производят слизистое, похожее на клей вещество, матрицу EPS, при этом размножаясь в этом месте. После закрепления другие микроорганизмы могут прикрепляться к матрице ЭПС, создавая таким образом микробное «сообщество». Трехмерная структура биопленок объясняет их устойчивость к большинству химических дезинфицирующих средств, которые с трудом проникают через ЭПС. Наиболее эффективным методом удаления биопленки из системы водоснабжения является термическая дезинфекция. - Проект системы очистки воды: Важно понимать, что вода и любая система очистки, которая используется для производства фармацевтической воды, обеспечивает прекрасную среду для роста микробов. Таким образом, проектирование системы очистки воды является важным вопросом.
 Плохо спроектированная система может привести к загрязнению воды, которую она производит. При принятии решения о проектировании системы очистки воды есть много вариантов на выбор. Наиболее распространенные методы производства фармацевтической воды включают деионизацию, обратный осмос, фильтрацию и дистилляцию. Существуют также «горячие» системы, предназначенные для поддержания температуры воды при микробиологической «убийственной» температуре (минимум 80°С).1641 или С). Выбор конструкции должен основываться на конкретных потребностях производственной площадки, которые должна поддерживать система очистки воды. Качество воды, скорость производства, потребности в хранении и распределении, простота обслуживания и стоимость – все это играет важную роль при проектировании системы водоснабжения.
Плохо спроектированная система может привести к загрязнению воды, которую она производит. При принятии решения о проектировании системы очистки воды есть много вариантов на выбор. Наиболее распространенные методы производства фармацевтической воды включают деионизацию, обратный осмос, фильтрацию и дистилляцию. Существуют также «горячие» системы, предназначенные для поддержания температуры воды при микробиологической «убийственной» температуре (минимум 80°С).1641 или С). Выбор конструкции должен основываться на конкретных потребностях производственной площадки, которые должна поддерживать система очистки воды. Качество воды, скорость производства, потребности в хранении и распределении, простота обслуживания и стоимость – все это играет важную роль при проектировании системы водоснабжения. - Валидация и Квалификация: Независимо от того, какой дизайн выбран, в конечном итоге каждая система должна пройти Валидацию и Квалификацию Очистки воды , Хранение и Распределение частей , из которых он состоит .
 Действия по валидации и квалификации устанавливают надежность всей системы, демонстрируя контроль над процессом в течение соответствующего периода мониторинга и наблюдения. В разделе 4.2 USP <1231> говорится: «Валидация — это программа документирования с высоким уровнем уверенности в том, что конкретный процесс способен стабильно поставлять продукт, соответствующий установленному набору атрибутов качества».
Действия по валидации и квалификации устанавливают надежность всей системы, демонстрируя контроль над процессом в течение соответствующего периода мониторинга и наблюдения. В разделе 4.2 USP <1231> говорится: «Валидация — это программа документирования с высоким уровнем уверенности в том, что конкретный процесс способен стабильно поставлять продукт, соответствующий установленному набору атрибутов качества». - Отбор проб и тестирование: Мониторинг системы очищенной воды требует отбора и тестирования фармацевтической воды из различных мест внутри системы, включая систему производства воды, резервуар(ы) для хранения и распределительную сеть (точки использовать). Несмотря на то, что многие системы оснащены «встроенными» устройствами мониторинга, такими как анализаторы общего органического углерода и измерители проводимости, всегда существует необходимость физического отбора проб системы для проведения «автономных» испытаний. Всякий раз, когда физически отбираются пробы воды из систем, необходимо принимать меры предосторожности, чтобы предотвратить попадание загрязняющих веществ в отбираемую воду.
 Клапаны для отбора проб следует продезинфицировать и дать им высохнуть перед отбором проб. Подходящие объемы промывки должны быть установлены до отбора пробы. Пробоотборник должен быть обучен отбору проб из систем водоснабжения и должен носить стерильные перчатки и любую другую одежду/устройства, которые он сочтет необходимыми. Для сбора образцов следует использовать стерильные контейнеры. Образцы для определения ТОС следует отбирать в специально подготовленные флаконы. После того, как образцы собраны, их следует как можно быстрее протестировать. Если тестирование не может быть начато в течение нескольких часов, образцы следует хранить в холодильнике до начала тестирования. Даже пробы охлажденной воды имеют короткую продолжительность жизни, максимум несколько дней.
Клапаны для отбора проб следует продезинфицировать и дать им высохнуть перед отбором проб. Подходящие объемы промывки должны быть установлены до отбора пробы. Пробоотборник должен быть обучен отбору проб из систем водоснабжения и должен носить стерильные перчатки и любую другую одежду/устройства, которые он сочтет необходимыми. Для сбора образцов следует использовать стерильные контейнеры. Образцы для определения ТОС следует отбирать в специально подготовленные флаконы. После того, как образцы собраны, их следует как можно быстрее протестировать. Если тестирование не может быть начато в течение нескольких часов, образцы следует хранить в холодильнике до начала тестирования. Даже пробы охлажденной воды имеют короткую продолжительность жизни, максимум несколько дней.
Почему стоит выбрать CPT℠ для тестирования фармацевтической воды?
Когда речь идет о фармацевтической воде любого типа, CPT℠ может удовлетворить ваши потребности в тестировании. Наша команда опытных химиков и микробиологов может обеспечить точное тестирование, будь то рутинный мониторинг или тестирование для поддержки деятельности по валидации.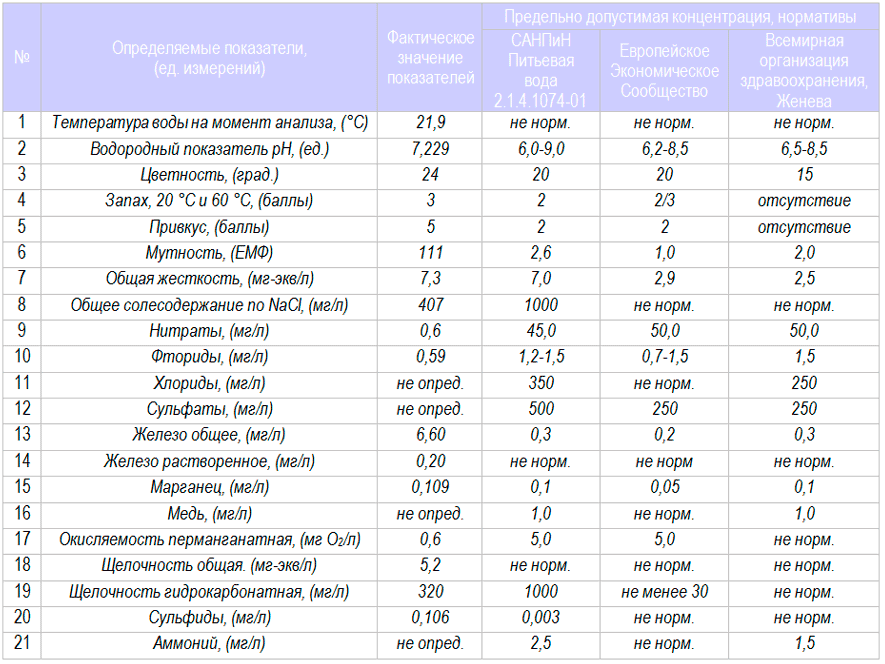 Консультационные услуги также доступны, чтобы помочь вам в выявлении проблем в вашей системе очистки воды. Независимо от ваших потребностей в тестировании воды, CPT℠ готова оказать помощь.
Консультационные услуги также доступны, чтобы помочь вам в выявлении проблем в вашей системе очистки воды. Независимо от ваших потребностей в тестировании воды, CPT℠ готова оказать помощь.
Думайте о CPT℠ как о расширении вашей группы контроля качества. Точное тестирование, проведенное в среде тестирования с высокими требованиями. Испытывать сырье самого высокого значения. Свяжитесь с нами при первой возможности.
Наши отделы
Основываясь на индивидуальных потребностях наших клиентов, мы предлагаем широкий спектр поддержки в различных отделах. Поскольку первоначальное тестирование продукта может быть довольно сложным с точки зрения высококачественного, безопасного и надежного продукта, наши клиенты обычно изучают преимущества многочисленных отделов и областей знаний, в том числе:
- Клинические испытания — могут проводиться испытания эффективности для обеспечения безопасности, использования потребителем, а также для подтверждения утверждений, таких как «протестировано дерматологами» и «проверено офтальмологами».





 Общий органический углерод не должен превышать 500 частей на миллиард.
Общий органический углерод не должен превышать 500 частей на миллиард.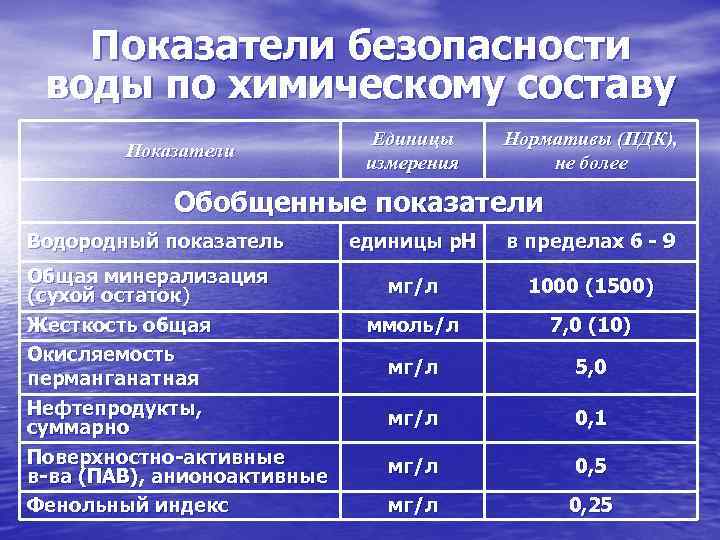

 Примеры химических загрязнителей, которые обнаруживаются при тестировании TOC, включают, помимо прочего, ацетон, метилэтилкетон и бензин. Поскольку все микробиологические организмы состоят в основном из молекул углерода, они также могут быть обнаружены с помощью тестирования TOC, примеры которого включают pseudomonas aeruginosa 9.0217 и кишечная палочка.
Примеры химических загрязнителей, которые обнаруживаются при тестировании TOC, включают, помимо прочего, ацетон, метилэтилкетон и бензин. Поскольку все микробиологические организмы состоят в основном из молекул углерода, они также могут быть обнаружены с помощью тестирования TOC, примеры которого включают pseudomonas aeruginosa 9.0217 и кишечная палочка.  Поскольку чрезвычайно низкие уровни ионов облегчают электрический ток, USP предоставляет спецификацию для приемлемого уровня, выраженного в микросименсах, которые являются минутными единицами электрического тока.
Поскольку чрезвычайно низкие уровни ионов облегчают электрический ток, USP предоставляет спецификацию для приемлемого уровня, выраженного в микросименсах, которые являются минутными единицами электрического тока. Твердые частицы вызывают большую озабоченность, если вода используется для офтальмологических или инъекционных препаратов.
Твердые частицы вызывают большую озабоченность, если вода используется для офтальмологических или инъекционных препаратов. Общая глава USP <1231> Раздел 8.2 определяет биопленку как «трехмерное структурированное сообщество неподвижных микробных клеток, встроенных в матрицу внеклеточных полимерных веществ (EPS)». Биопленки образуются, когда бактерии прикрепляются к поверхностям во влажной среде и производят слизистое, похожее на клей вещество, матрицу EPS, при этом размножаясь в этом месте. После закрепления другие микроорганизмы могут прикрепляться к матрице ЭПС, создавая таким образом микробное «сообщество». Трехмерная структура биопленок объясняет их устойчивость к большинству химических дезинфицирующих средств, которые с трудом проникают через ЭПС. Наиболее эффективным методом удаления биопленки из системы водоснабжения является термическая дезинфекция.
Общая глава USP <1231> Раздел 8.2 определяет биопленку как «трехмерное структурированное сообщество неподвижных микробных клеток, встроенных в матрицу внеклеточных полимерных веществ (EPS)». Биопленки образуются, когда бактерии прикрепляются к поверхностям во влажной среде и производят слизистое, похожее на клей вещество, матрицу EPS, при этом размножаясь в этом месте. После закрепления другие микроорганизмы могут прикрепляться к матрице ЭПС, создавая таким образом микробное «сообщество». Трехмерная структура биопленок объясняет их устойчивость к большинству химических дезинфицирующих средств, которые с трудом проникают через ЭПС. Наиболее эффективным методом удаления биопленки из системы водоснабжения является термическая дезинфекция. Плохо спроектированная система может привести к загрязнению воды, которую она производит. При принятии решения о проектировании системы очистки воды есть много вариантов на выбор. Наиболее распространенные методы производства фармацевтической воды включают деионизацию, обратный осмос, фильтрацию и дистилляцию. Существуют также «горячие» системы, предназначенные для поддержания температуры воды при микробиологической «убийственной» температуре (минимум 80°С).1641 или С). Выбор конструкции должен основываться на конкретных потребностях производственной площадки, которые должна поддерживать система очистки воды. Качество воды, скорость производства, потребности в хранении и распределении, простота обслуживания и стоимость – все это играет важную роль при проектировании системы водоснабжения.
Плохо спроектированная система может привести к загрязнению воды, которую она производит. При принятии решения о проектировании системы очистки воды есть много вариантов на выбор. Наиболее распространенные методы производства фармацевтической воды включают деионизацию, обратный осмос, фильтрацию и дистилляцию. Существуют также «горячие» системы, предназначенные для поддержания температуры воды при микробиологической «убийственной» температуре (минимум 80°С).1641 или С). Выбор конструкции должен основываться на конкретных потребностях производственной площадки, которые должна поддерживать система очистки воды. Качество воды, скорость производства, потребности в хранении и распределении, простота обслуживания и стоимость – все это играет важную роль при проектировании системы водоснабжения. Действия по валидации и квалификации устанавливают надежность всей системы, демонстрируя контроль над процессом в течение соответствующего периода мониторинга и наблюдения. В разделе 4.2 USP <1231> говорится: «Валидация — это программа документирования с высоким уровнем уверенности в том, что конкретный процесс способен стабильно поставлять продукт, соответствующий установленному набору атрибутов качества».
Действия по валидации и квалификации устанавливают надежность всей системы, демонстрируя контроль над процессом в течение соответствующего периода мониторинга и наблюдения. В разделе 4.2 USP <1231> говорится: «Валидация — это программа документирования с высоким уровнем уверенности в том, что конкретный процесс способен стабильно поставлять продукт, соответствующий установленному набору атрибутов качества».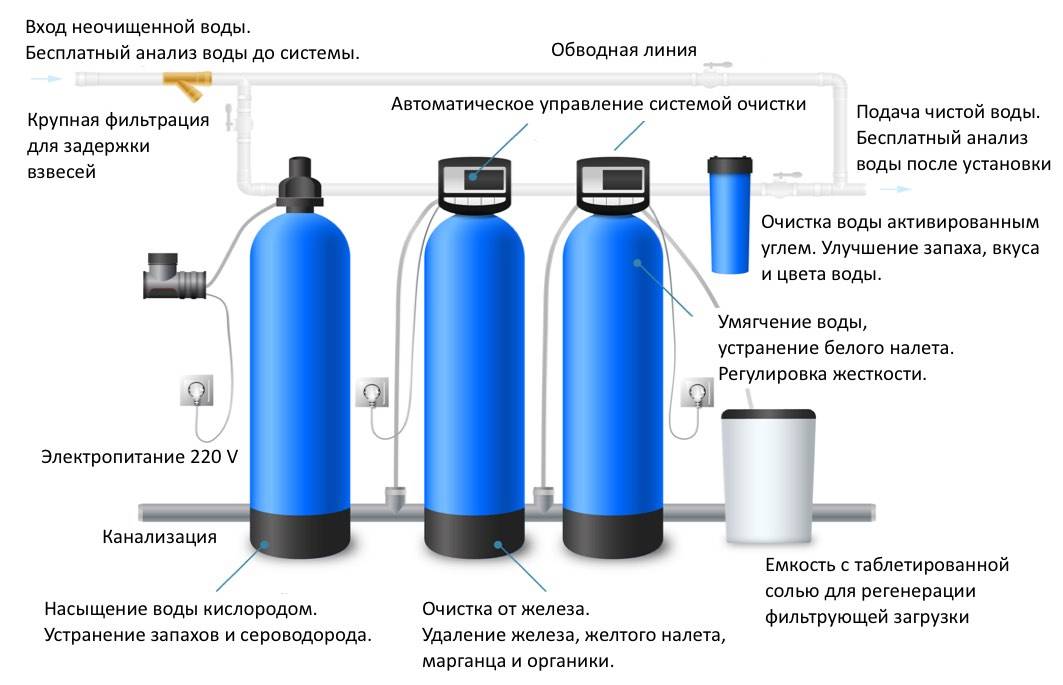 Клапаны для отбора проб следует продезинфицировать и дать им высохнуть перед отбором проб. Подходящие объемы промывки должны быть установлены до отбора пробы. Пробоотборник должен быть обучен отбору проб из систем водоснабжения и должен носить стерильные перчатки и любую другую одежду/устройства, которые он сочтет необходимыми. Для сбора образцов следует использовать стерильные контейнеры. Образцы для определения ТОС следует отбирать в специально подготовленные флаконы. После того, как образцы собраны, их следует как можно быстрее протестировать. Если тестирование не может быть начато в течение нескольких часов, образцы следует хранить в холодильнике до начала тестирования. Даже пробы охлажденной воды имеют короткую продолжительность жизни, максимум несколько дней.
Клапаны для отбора проб следует продезинфицировать и дать им высохнуть перед отбором проб. Подходящие объемы промывки должны быть установлены до отбора пробы. Пробоотборник должен быть обучен отбору проб из систем водоснабжения и должен носить стерильные перчатки и любую другую одежду/устройства, которые он сочтет необходимыми. Для сбора образцов следует использовать стерильные контейнеры. Образцы для определения ТОС следует отбирать в специально подготовленные флаконы. После того, как образцы собраны, их следует как можно быстрее протестировать. Если тестирование не может быть начато в течение нескольких часов, образцы следует хранить в холодильнике до начала тестирования. Даже пробы охлажденной воды имеют короткую продолжительность жизни, максимум несколько дней.