Содержание
Свойства воды | Обучонок
Руководитель проекта:
Филиппова Наталья Валерьевна
Учреждение:
МБОУ «СОШ № 3» г. Сосновый Бор
Данная исследовательская работа на тему «Свойства воды» ученицы 4 класса начальной школы посвящена изучению физических свойств воды и их применения в повседневной жизни. Автор проекта проводит эксперименты с водой с целью выяснить, является ли она универсальным растворителем.
Подробнее о работе:
В ученической исследовательской работе по окружающему миру «Свойства воды» автор рассматривает теорию о воде, ее свойствах и месте в жизни человека. В исследовательском проекте о воде учащаяся начальной школы проводит опыты по растворению в воде различных веществ, узнает, как можно использовать свойства воды в повседневной жизни?
Результатом исследовательского проекта по окружающему миру о свойствах воды, стала практическая работа, наблюдение за степенью растворения в воде сахара, соли, песка, земли и масла. Данная работа будет полезна при изучении предмета окружающий мир в начальной школе, в качества образца выполнения проекта о свойствах воды.
Данная работа будет полезна при изучении предмета окружающий мир в начальной школе, в качества образца выполнения проекта о свойствах воды.
Оглавление
Введение
1. Физические свойства воды.
2. Опыты с водой. Как можно использовать свойства воды в повседневной жизни?
Вывод
Литература
Введение
Вода- это жизнь, а значит без воды не будет жизни на Земле.
Загадка:
В морях и реках обитает,
Но часто по небу летает.
А как наскучит ей летать
На землю падает опять.
(вода)
Вода — это вещество прозрачное, без цвета и запаха. В повседневной жизни воду мы можем увидеть в морях, океанах, реках, родниках. Вода течет из крана. Воду широко используют в быту. Она содержится во всех растениях.
В химии вода — это растворитель. Вода «добывает» электрический ток, работая на гидроэлектростанциях. В медицине вода- это растворитель и лекарственное средство, средство санитарии и гигиены.
Цель проекта: Узнать физические свойства воды.
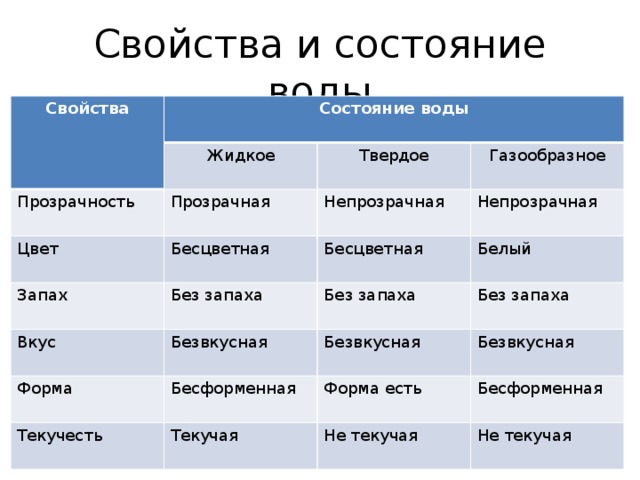
В окружающем нас мире вода существует в трех состояниях: твердом (лед на реках, сосульки, снег), жидком (моря, океаны, реки, озера), газообразном (туман, пар)
Гипотеза: выяснить, можно ли применить эти знания в нашей жизни?
Физические свойства воды
Вода играет важную роль в нашей жизни. Узнав лучше свойства воды, можно применять эти знания в жизни. Оказывается, что водоемы, при наступлении морозов, не промерзают до дна благодаря особенностям смешивания воды. Образовавшийся лед не дает воде остывать, сохраняя ее температуру.
Еще это свойство воды активно используется человеком в повседневной жизни, например, в системе отопления. Свойства воды растворять в себе разные вещества используются в быту, например, при приготовлении пищи, в медицине и химии, как растворитель.
Впитывание воды растениями можно наблюдать у каждого из нас дома на подоконнике с цветочными горшками, когда поливаем цветы.
Опыты с водой. Как можно использовать свойства воды в повседневной жизни.
ОПЫТ 1. Как пьет дерево?
Понадобится блюдце, вода, краситель, спичка. Растворяем краситель в воде и ставим спичку вертикально. Через некоторое время увидим, что окрашенная вода поднимается вверх по спичке. Таким образом мы доказали, как дерево, даже мертвое, пьет воду.
ОПЫТ 2. Почему насекомые могут бегать по воде?
Понадобится тарелка, кусочек бумаги, иголка, вода. В тарелку с водой положить бумагу с иголкой. Намокшая бумага опустится на дно, а иголка останется плавать. Вывод: поверхность воды обладает особыми свойствами. Частички воды плотно прилегают друг к другу и создают невидимую пленку, по которой могут двигаться насекомые.
ОПЫТ 3. Вода растворяет разные вещества.
Понадобится: стакан, вода, сахар или соль, песок или земля, растительное масло.
Вода растворяет соль и сахар.
Вода не растворяет песок, землю.
Вода не растворяет масло, оно остается плавать.
ОПЫТ 4. Вода течет.
Если вылить воду на плоскую поверхность- она растекается в лужу. Происходит это потому, что вода состоит из частиц- молекул, которые движутся. А зависит ли движение частиц от ее температуры?
ОПЫТ 5.
Понадобится два стакана и два листа бумаги, свернутые конусом. Конусы ставим вниз в стаканы острым концом. Наливаем в один конус холодную, в другой горячую воду одинаковое количество.
Вывод: в горячей воде молекулы движутся быстрее, чем в холодной, поэтому горячая вода течет быстрее.
ОПЫТ 6. Смешивание горячей и холодной воды.
Мы узнали, что вода состоит из молекул, которые движутся. А что произойдет с частицами горячей и холодной воды, если их смешать?
Понадобятся два стакана, красители, лист картона. В одном стакане смешиваем синий краситель с холодной водой, в другом- красный с горячей водой.
В одном стакане смешиваем синий краситель с холодной водой, в другом- красный с горячей водой.
1) Стакан с холодной водой накрываем картоном, переворачиваем и ставим на стакан с горячей водой, вытаскиваем картон. Красная вода поднимается в стакан с синей водой, смешивается и становится фиолетовой.
2) Стакан с горячей водой накрываем и переворачиваем на стакан с холодной водой. Видим, что вода не смешивается.
Вывод: холодная вода тяжелее.
Выводы
Вода — одно из главных богатств на Земле. Человеку нужно выпивать в день около двух литров воды. И примерно в 20 раз больше ежедневно требуется каждому из нас для мытья, приготовления пищи. Без воды невозможно растениеводство, животноводство, все отрасли промышленности. Без воды невозможна жизнь на Земле.
Информационные источники
- Энциклопедия для детей.
- Научные эксперименты/ Пер. с англ. А. Филоновой.
- Интернет ресурсы.

Если страница Вам понравилась, поделитесь в социальных сетях:
Необычные свойства воды
Проектная деятельность учащихся на уроках по окружающему миру
Беляева Ольга Александровна
В настоящее время преподавание в школе должно соответствовать требованиям ФГОС второго поколения. Это предполагает использование разнообразных новых методов и приемов работы. Один из них это — проектная деятельность учащихся. Данная деятельность используется как в старшей, так и в начальной школе. Проектная деятельность может использоваться и в урочное время , и во внеурочной работе. Создание проектов — это увлекательная, но трудоемкая работа, которая предполагает постановку целей, выдвижение гипотезы, доказательство или исследование и выводы.
Проект « Необычные свойства воды» разработан по теме « Вода» 3 класс УМК « Школа 21 00. В данном проекте учащиеся рассматривали те свойства воды, которые не описываются в учебнике. При работе над проектом в течении нескольких месяцев учащиеся класса доказывали необычные свойства воды, проводя различные опыты, изучая дополнительную литературу. Данный проект дети с успехом защитили на школьной научной конференции.
При работе над проектом в течении нескольких месяцев учащиеся класса доказывали необычные свойства воды, проводя различные опыты, изучая дополнительную литературу. Данный проект дети с успехом защитили на школьной научной конференции.
Содержание
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Тема: Необычные свойства воды.
Обоснование выбора темы. С водой мы сталкиваемся ежедневно и она занимает важнейшее место в жизни всего живого. С одной стороны- нет ничего более простого и доступного на планете, как вода, с другой – более загадочного и уникального.
Гипотеза— предположим, что вода обладает уникальными свойствами.
Объект- вода.
Цель исследования— доказать, что вода необычное вещество.
Задачи исследования:
-
проанализировать литературу и информацию в Интернете по данной проблеме; -
провести наблюдения за основными состояниями воды, её физическими свойствами; -
определить и выделить удивительные свойства воды; -
провести эксперименты, доказывающие её уникальность; -
понаблюдать, как человек использует необычные свойства воды; -
сделать выводы.
Методы исследования: анализ, наблюдение, эксперимент(опыт).
Введение
«Вода! У тебя нет ни вкуса, ни запаха, тебя не опишешь, тобой наслаждаешься, не понимая, что ты такое. Ты просто необходима для жизни, ты есть сама жизнь. Ты величайшее в мире богатство, но и самое непрочное. Ты не терпишь примесей, не выносишь ничего чужеродного. Ты божество, которое так легко спугнуть» .
(французский писатель Антуан де Сент- Экзюпери).
Что такое вода? Разве она только та бесцветная жидкость, что налита в стакан? Океан, покрывающий почти всю нашу планету — это вода. В нём миллионы лет назад зародилась жизнь. Тучи, облака, туманы, несущие влагу всему живому на земной поверхности, — это ведь тоже вода. Бескрайние ледяные пустыни полярных областей, снеговые покровы, застилающие почти половину планеты, — и это вода. Без неё не возможна жизнь и деятельность человека. Вода- наиболее распространенное, доступное и дешевое вещество. Она и дорога, и среда обитания животных, и «добытчик» электрического тока, и «транспортное средство» питательных веществ к клеткам растений и животных. И наконец, без неё не обойтись в быту. Вода- это чудо природы. (приложение рис.1)
Вода- наиболее распространенное, доступное и дешевое вещество. Она и дорога, и среда обитания животных, и «добытчик» электрического тока, и «транспортное средство» питательных веществ к клеткам растений и животных. И наконец, без неё не обойтись в быту. Вода- это чудо природы. (приложение рис.1)
Нынешняя наука, с легкостью рассуждает о галактиках и черных дырах, но не всегда может пояснить, как «работает» элементарная вода.
В своей исследовательской работе мы собрали информацию о воде из разных источников- из книг, научно- популярных фильмов и Инетернета. Проанализировали её и выделили свойства воды, которые придают ей уникальность.
1 глава
Основные физические свойства воды
Мы провели наблюдения и доказали, что объект нашего исследования уникален по сравнению с другими веществами на Земле. Не одно вещество не может «похвастаться» таким количеством свойств, которые делают его незаменимым в нашей жизни. Выделим некоторые из них:
Выделим некоторые из них:
-
не имеет запаха, вкуса и формы; -
текучее; -
прозрачное и бесцветное; -
растворяет другие вещества. (приложение рис. 2)
Единственное вещество на планете, которое может находится в 3х состояниях:
-
жидком- вода; -
твердом- лед; -
газообразном- пар; (приложение рис. 3)
Ученым известно, что тело человека почти на 2/3 состоит из воды.
Человек может прожить без воды не более восьми дней, а в пустыне смертельное обезвоживание организма наступает уже через сутки. Потеря 6-8% воды от общего веса тела приводит к обмороку. Потеря же 25% жидкости смертельна для человека. Учеными подсчитано, что для того чтобы себя хорошо чувствовать, взрослому жителю умеренных широт необходимо выпивать от двух до трёх литров воды в сутки, а человеку, живущему в пустыне — семь с половиной литров. Можно рассчитать необходимое количество воды для себя. Это 40 граммов на килограмм массы тела. Т.е. если участник проекта Рита весит 30 кг, то ей нужно выпить 1,2 литра в день, а участник Рома -40кг соответственно – 1,6 литра в день. Если не придерживаться этих норм, то снижается работоспособность, появляется усталость.
Можно рассчитать необходимое количество воды для себя. Это 40 граммов на килограмм массы тела. Т.е. если участник проекта Рита весит 30 кг, то ей нужно выпить 1,2 литра в день, а участник Рома -40кг соответственно – 1,6 литра в день. Если не придерживаться этих норм, то снижается работоспособность, появляется усталость.
Вода занимает 3/4 поверхности земного шара
Из воды состоит 4/5 растения.
Докажем, что вода находится в растениях. Для этого проведем опыт.
Опыт №1.
Выделим из свежей древесины воду. Мы поместим кусочек в сухую банку, закроем крышкой и поставим на горячую батарею.
Результат: при нагревании на стенках банки образовались мелкие капельки воды. (приложение рис. 4)
Вывод: вода содержится в растениях.
Докажем, что вода «нужна всем».
Опыт №2.
Возьмём две фасолины, одну положим на сухую ватку, другую на мокрую.
Результат: через 3 дня на мокрой ватке у фасоли появился росток, а на сухой фасоль засохла. (приложение рис. 5)
Вывод: вода необходима для начала и продолжения жизни.
Мы рассмотрели основные физические свойства воды, всем известные. Но есть и удивительные. Мы их используем в повседневной жизни, не замечая их уникальность. Эти свойства и представляют для нашего проекта наибольший интерес.
2 глава
Удивительные свойства воды
-
Хотите получить награду в 1 тысячу фунтов стерлингов от Британского Королевского химического общества? Надо всего лишь объяснить с научной точки зрения, почему в некоторых случаях горячая вода замерзает быстрее, чем холодная!
Еще в древности Аристотель обращал внимание на это. В средние века ученые пытались объяснить данный феномен. Затем об этом неудобном факте забыли. И только в 1968 году «вспомнили» благодаря школьнику Эрасто Мпембе из далекой от всякой науки Танзании, который случайно заметил этот факт.
В средние века ученые пытались объяснить данный феномен. Затем об этом неудобном факте забыли. И только в 1968 году «вспомнили» благодаря школьнику Эрасто Мпембе из далекой от всякой науки Танзании, который случайно заметил этот факт.
Проведем эсперимент и понаблюдаем за горячей и холодной водой в морозильной камере.
Опыт № 3.
В ячейки для льда нальём теплую воду 35 ° С и поставим в морозильную камеру, засечем время превращения воды в лёд.
Тоже самое проделаем с холодной водой-0,5 ° С.
Результат: тёплая вода превратилась в лед через 20 минут;
холодная вода превратилась в лед через 25 минут;
Для опыта необходима вода пределенной температуры.
Вывод: горячая вода замерзает быстрее, чем холодная при определенных условиях. (приложение рис. 6)
Производители мороженого и бармены используют этот эффект в своей повседневной работе, но никто в действительности не знает, почему это работает.
-
В ходе работы над проектом мы обратили внимание, что вода может перемещаться самостоятельно.
Опыт №4.
Возьмем 3 стакана, в два из них нальём воду. Третий оставим пустым и к нему перекинем «мостики» из бумажных салфеток.
Результат: вода по «мостикам» « перешла» в пустой стакан, уровень воды в 3х стаканах стал почти одинаковый.
Вывод:вода может подниматься вверх без посторонней помощи. (приложение рис. 7)
Это удивительное свойство помогает растениям получать влагу из почвы и перемещать от корней по стеблям к листьям. Зная такую способность воды, можно домашние растения надолго оставлять без полива. Для этого необходимо сделать нехитрое устройство. (приложение рис. 8)
-
Мы задумались, а какая вода быстрее будет подниматься вверх?
Опыт №5.
Возьмет 2 стакана: №1- с теплой водой и №2 -с холодной водой;
две полоски картона, один конец которых окрашен в разные цвета маркерами;
опустим концы полосок картона в стаканы;
Результат: краски маркера на полоске в тёплой воде поднялись вверх быстрее и выше, чем в холодной. (приложение рис. 9)
(приложение рис. 9)
Вывод: теплая вода поднимается вверх быстрее холодной.
Теперь нам понятно почему растения нужно поливать теплой водой. Не потому что от холодной они могут «простудиться» и «заболеть», а потому что теплая вода доставит необходимые питательные вещества из почвы и живительную влагу быстрее.
-
Когда мы любуемся рыбками в аквариуме, они всегда кажутся нам больше, чем есть на самом деле. Выясним почему?
Опыт №6.
В один прозрачный стакан нальём воду, другой оставим пустым. Поставим игрушечную фигурку сначала за пустой, затем за наполненный водой.
Результат: за пустым стаканом размеры фигурки не изменились, а за стаканом с водой значительно увеличились. (приложение рис.10)
Вывод: вода зрительно увеличивает предметы.
-
В холодное время года наши квартиры теплые благодаря паровому отоплению. А почему именно вода в батареях?
А почему именно вода в батареях?
Опыт №7.
Поставим металлический ковшик на плиту.Через 10 секунд его нельзя взять в руки-он раскален. В этот же ковшик нальем стакан воды и поставим на плиту. Доводим до кипения, на это нужно уже больше времени. Переливаем горячую воду из ковша в стакан с ложкой.
Результат: Через десять минут ковш остыл, а стакан нельзя взять в руки. Вода нагрела ложку и стенки стакана.(приложение рис.11 )
Вывод: У воды есть свойство долго удерживать тепло. Оно и самое доступное текучее вещество. Поэтому именно вода в наших батареях.
-
Всем известно, что зимой необходимо поддерживать паровое отопление. Иначе вода остынет, замерзнет и батареи лопнут.
Опыт № 8.
Возмём бутылку, нальём воду и поместим её в морозильную камеру холодильника.
Результат: вода замерзла и расширилась, её объём увеличился и бутылка треснула. (приложение рис.12)
(приложение рис.12)
Вывод:
1. вода при низких температурах превращается в лед;
2. вода при замерзании расширяется.
-
Многие ученые, изучающие воду, утверждают, что она способна менять свою структуру под воздействием любой информации. Даже эмоции человека оказывают сильное влияние на воду.
Опыт №9.
Возьмем три горшка, поместим их в одинаковые условия и посадим фасоль. Возьмем 3 банки с одинаковой водой. Каждой горшок поливаем «своей» водой. Поливая фасоль, будем передавать воде информацию разного характера:
№1 -добрые, хвалебные слова, петь песни, читать стихи;
№2- молчим;
№3- ругаем воду;
Результат: росток фасоли пророс в горшке
№1- на 3-й день,
№2- на 4-й день,
№3- на 5-й день.
Вывод: вода способна накапливать, передавать информацию другим объектам, состоящим из воды .
(приложение рис. 13)
Объект нашего исследования кажется будничным и естественным только на первый взгляд. Опытным путем мы убедились в необычности многих его свойств. Эти свойства- подарок всему живому на Земле.
ВЫВОДЫ:
В таблице представлены удивительные свойства воды, которые мы доказали опытами.
Таблица № 1.
Свойства воды.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Список литературы и источников.
-
«Тайная жизнь воды» ЭмотоМасару. -
«Тайны воды» Олег Арсенов. -
Журнал «GEO. -
«Наука и жизнь».Электронное издание. http://www.nkj.ru/ -
«Знание-сила»-научно-популярный журнал http://www.znanie-sila.ru/
Фильмы:
«Необычные свойства воды»
http://www.youtube.com/watch?v=NQQbrgjGukI
«Великая тайна воды»
http://www.youtube.com/watch?v=YuyQiBBGxvs
«Вода. Новое измерение» http://www.youtube.com/watch?v=u4y1mNHW8is
Список
5.1 Свойства воды. Введение в океанографию
Наиболее очевидной особенностью океанов является то, что они содержат воду. Вода настолько вездесуща, что может показаться не очень интересным веществом, но она обладает многими уникальными свойствами, влияющими на глобальные океанографические и климатологические процессы. Многие из этих процессов связаны с образованием между молекулами воды.
Многие из этих процессов связаны с образованием между молекулами воды.
Рисунок 5.1.1 Водородные связи (штриховые линии) между молекулами воды. Атомы кислорода показаны красным, атомы водорода — белым (общественное достояние, через Wikimedia Commons).
Молекула воды состоит из двух атомов водорода и одного атома кислорода. Электроны, ответственные за связи между атомами, распределены по всей молекуле неравномерно, так что водородные концы молекул воды имеют небольшой положительный заряд, а кислородный конец имеет небольшой отрицательный заряд, что делает воду . Отрицательная кислородная сторона молекулы образует притяжение к положительному водородному концу соседней молекулы. Эта довольно слабая сила притяжения называется водородной связью (рис. 5.1.1). Если бы не водородные связи, вода испарялась бы при -68 o C, что означает, что жидкая вода (и, следовательно, жизнь) не может существовать на Земле. Эти водородные связи ответственны за некоторые уникальные свойства воды:
1. Вода – это единственное вещество, существующее в природе в твердом, жидком и газообразном состояниях при обычных для Земли диапазонах температур и давлений. Это связано с относительно высокими температурами замерзания и испарения воды (см. ниже).
Вода – это единственное вещество, существующее в природе в твердом, жидком и газообразном состояниях при обычных для Земли диапазонах температур и давлений. Это связано с относительно высокими температурами замерзания и испарения воды (см. ниже).
2. Вода имеет высокое , которое представляет собой количество тепла, которое необходимо добавить, чтобы повысить ее температуру. это теплота, необходимая для повышения температуры 1 г вещества на 1 o C. Вода имеет самую высокую удельную теплоемкость из всех жидкостей, кроме аммиака (табл. 5.1.1).
Таблица 5.1.1 Удельная теплоемкость ряда обычных веществ
| Удельная теплоемкость (калории/г/C o ) | |
|---|---|
| Аммиак | 1,13 |
| Вода | 1,00 |
| Ацетон | 0,51 |
| Зерновой спирт | 0,23 |
| Алюминий | 0,22 |
| Медь | 0,09 |
| Серебро | 0,06 |
Таким образом, вода является одной из самых трудных для нагревания или охлаждения жидкостей; он может поглощать большое количество тепла без повышения его температуры. Помните, что температура отражает среднее количество молекул внутри вещества; чем энергичнее движение, тем выше температура. В воде молекулы удерживаются вместе водородными связями, и эти связи необходимо преодолеть, чтобы позволить молекулам свободно двигаться. Когда к воде добавляется тепло, энергия должна сначала пойти на разрыв водородных связей, прежде чем температура начнет повышаться. Следовательно, большая часть добавочного тепла поглощается за счет разрыва Н-связей, а не за счет повышения температуры, что придает воде высокую теплоемкость.
Помните, что температура отражает среднее количество молекул внутри вещества; чем энергичнее движение, тем выше температура. В воде молекулы удерживаются вместе водородными связями, и эти связи необходимо преодолеть, чтобы позволить молекулам свободно двигаться. Когда к воде добавляется тепло, энергия должна сначала пойти на разрыв водородных связей, прежде чем температура начнет повышаться. Следовательно, большая часть добавочного тепла поглощается за счет разрыва Н-связей, а не за счет повышения температуры, что придает воде высокую теплоемкость.
Водородные связи также придают воде высокую скрытую теплоту; теплота, необходимая для перехода из твердого состояния в жидкое или из жидкого в газообразное. — это количество тепла, необходимое для перехода из твердого состояния в жидкое; 80 кал/г в случае таяния льда в воду. Лед является твердым телом, потому что водородные связи удерживают молекулы воды в твердой кристаллической решетке (см. ниже). При нагревании льда температура поднимается до 0, o С. В этот момент любое дополнительное тепло идет на плавление льда за счет разрыва водородных связей, а не на повышение температуры. Так что пока есть лед, температура воды не повысится. Вот почему ваш напиток останется холодным, пока в нем есть лед; любое поглощенное тепло идет на таяние льда, а не на подогрев напитка.
В этот момент любое дополнительное тепло идет на плавление льда за счет разрыва водородных связей, а не на повышение температуры. Так что пока есть лед, температура воды не повысится. Вот почему ваш напиток останется холодным, пока в нем есть лед; любое поглощенное тепло идет на таяние льда, а не на подогрев напитка.
Когда весь лед растает, дополнительное тепло повысит температуру воды на 1 o C на каждую добавленную калорию тепла, пока она не достигнет 100 o C. В этот момент любое дополнительное тепло идет на преодоление водородные связи и превращение жидкой воды в водяной пар, а не повышение температуры воды. Теплота, необходимая для испарения жидкой воды в водяной пар, равна , что имеет значение 540 кал/г (рис. 5.1.2).
Рисунок 5.1.2 Скрытая теплота, необходимая для фазовых переходов в воде. Скрытая теплота плавления — это теплота, необходимая для таяния льда (80 кал/г), а скрытая теплота парообразования — это теплота, необходимая для превращения жидкой воды в водяной пар (540 кал/г) (PW).
Высокий уровень воды помогает регулировать глобальный климат, поскольку океаны медленно поглощают и выделяют тепло, предотвращая резкие колебания температуры (см. раздел 8.1). Это также означает, что водные организмы не так подвержены таким быстрым изменениям температуры, как наземные организмы. Глубоководный организм может испытывать не более 0,5 o C изменение температуры в течение всей жизни, в то время как наземные виды могут столкнуться с изменениями более чем на 20 o C за один день!
3. Вода растворяет больше веществ, чем любая другая жидкость; это «универсальный растворитель» , поэтому в океане растворено так много веществ. Вода особенно хорошо растворяет ионные соли; молекулы, состоящие из противоположно заряженных частиц, таких как NaCl (Na + и Cl – ). В воде заряженные ионы притягивают молекулы воды. Ионы окружаются слоем молекул воды, ослабляя связь между ионами до 80 раз. При ослаблении связей между ионами вещество растворяется (рис. 5.1.3).
5.1.3).
Рисунок 5.1.3 Притяжение между полярными молекулами воды и заряженными ионами (например, в NaCl) больше, чем притяжение между заряженными ионами, вызывая диссоциацию ионов и растворение соли (PW).
4. Твердая фаза менее плотна, чем жидкая фаза . Другими словами, лед плавает. Большинство веществ более плотные в твердом состоянии, чем в жидком, поскольку их молекулы более плотно упакованы в твердом состоянии. Исключение составляет вода: плотность пресной воды составляет 1,0 г/см 9 .0011 3 , а плотность льда 0,92 г/см 3 , и опять же это связано с действием водородных связей.
По мере снижения температуры воды молекулы замедляются, в конечном итоге замедляясь настолько, что могут образовываться водородные связи и удерживать молекулы воды в кристаллической решетке. Молекулы в решетке расположены дальше друг от друга, чем молекулы в жидкой воде, что делает лед менее плотным, чем жидкая вода (рис. 5.1.4). Это знакомо каждому, кто когда-либо оставлял полную бутылку с водой в морозильной камере только для того, чтобы она лопнула, когда вода замерзнет и расширится.
Рисунок 5.1.4 Структура кристаллической решетки льда, показывающая молекулы воды, удерживаемые вместе водородными связями (автор Adam001d (собственная работа) [CC BY-SA 3.0], через Wikimedia Commons).
Но зависимость между температурой и плотностью воды не является простой линейной. Когда вода охлаждается, ее плотность, как и ожидалось, увеличивается, так как молекулы воды замедляются и сближаются. Однако пресная вода достигает максимальной плотности при температуре 4 o C, а по мере охлаждения выше этой точки ее плотность снижается, поскольку начинают формироваться водородные связи и увеличивается межмолекулярное расстояние (рис. 5.1.5, вставка). Плотность продолжает снижаться, пока температура не достигнет 0, o C и образуются кристаллы льда, резко снижающие плотность (рис. 5.1.5).
Рисунок 5.1.5 По мере снижения температуры плотность воды увеличивается, пока не достигнет максимальной плотности при 4 o C (врезка). Затем плотность немного снижается до 0 o C, где она резко снижается по мере образования кристаллов льда (Клаус-Дитер Келлер, [CC BY-SA 3.0], через Wikimedia Commons).
Затем плотность немного снижается до 0 o C, где она резко снижается по мере образования кристаллов льда (Клаус-Дитер Келлер, [CC BY-SA 3.0], через Wikimedia Commons).
То, что лед менее плотный, чем вода, имеет ряд важных последствий. Лед, плавающий на поверхности океана, помогает регулировать температуру океана и, следовательно, глобальный климат, влияя на количество солнечного света, который отражается, а не поглощается (см. раздел 8.1). В меньших масштабах поверхностный лед может предотвратить замерзание озер и прудов зимой. По мере того как пресная поверхностная вода охлаждается, она становится более плотной и опускается на дно. Затем новая поверхностная вода охлаждается и опускается, и процесс повторяется в так называемом , где более плотная вода тонет, а менее плотная вода поднимается на поверхность только для того, чтобы охладиться и опуститься. Таким образом, весь водоем охлаждается несколько равномерно. Этот процесс продолжается до тех пор, пока поверхностная вода не остынет ниже 4 o C. Ниже 4 o C вода по мере охлаждения становится менее плотной, поэтому она больше не тонет. Вместо этого он остается на поверхности, становясь все холоднее и менее плотным, пока не замерзнет при температуре 0, o C. Как только пресная вода замерзает, лед всплывает и изолирует остальную воду под ним, уменьшая дальнейшее охлаждение. Самая плотная придонная вода по-прежнему находится на уровне 4 o C, поэтому он не замерзает, позволяя дну озера или пруда оставаться незамерзшим (что является хорошей новостью для живущих там животных), независимо от того, насколько холодно на улице.
Ниже 4 o C вода по мере охлаждения становится менее плотной, поэтому она больше не тонет. Вместо этого он остается на поверхности, становясь все холоднее и менее плотным, пока не замерзнет при температуре 0, o C. Как только пресная вода замерзает, лед всплывает и изолирует остальную воду под ним, уменьшая дальнейшее охлаждение. Самая плотная придонная вода по-прежнему находится на уровне 4 o C, поэтому он не замерзает, позволяя дну озера или пруда оставаться незамерзшим (что является хорошей новостью для живущих там животных), независимо от того, насколько холодно на улице.
Растворенные в морской воде соли препятствуют образованию кристаллической решетки и, следовательно, затрудняют образование льда. Таким образом, морская вода имеет точку замерзания около -2 o C (в зависимости от солености) и замерзает до достижения температуры максимальной плотности. Таким образом, морская вода будет продолжать тонуть по мере того, как становится холоднее, пока, наконец, не замерзнет.
5. Вода имеет очень высокое , самое высокое из всех жидкостей, кроме ртути (Таблица 5.1.2). Молекулы воды притягиваются друг к другу водородными связями. Молекулы, не находящиеся на поверхности воды, окружены другими молекулами воды во всех направлениях, поэтому силы притяжения равномерно распределяются во всех направлениях. Но для молекул на поверхности над ними мало соседних молекул, только внизу, поэтому все силы притяжения направлены внутрь, от поверхности (рис. 5.1.6). Эта внутренняя сила заставляет капли воды принимать сферическую форму, а вода собирается на поверхности, поскольку сферическая форма обеспечивает минимально возможную площадь поверхности. Эти силы притяжения также заставляют поверхность воды действовать как эластичная «кожа», которая позволяет таким вещам, как насекомые, сидеть на поверхности воды и не тонуть.
Рисунок 5.1.6 Чистая сила притяжения между молекулами на поверхности направлена внутрь, что приводит к поверхностному натяжению. Для молекул в центре сила одинакова во всех направлениях (PW).
Для молекул в центре сила одинакова во всех направлениях (PW).
Таблица 5.1.2 Поверхностное натяжение различных жидкостей
| Жидкость | Поверхностное натяжение (миллиньютон/метр) | Температура o С |
|---|---|---|
| Меркурий | 487,00 | 15 |
| Вода | 71,97 | 25 |
| Глицерин | 63,00 | 20 |
| Ацетон | 23,70 | 20 |
| Этанол | 22,27 | 20 |
Свойства воды и ее значение для жизни
РЕКЛАМА:
1. Вода обладает высокой когезивностью и клейкостью:
Благодаря водородным связям между молекулами воды возникает сильное межмолекулярное притяжение. Это называется сплоченностью.
Когда вода образует водородные связи с другим веществом, притяжение называется адгезией. Благодаря когезии и адгезии семена набухают и прорастают; происходит подъем сока и капиллярное движение воды.
Благодаря когезии и адгезии семена набухают и прорастают; происходит подъем сока и капиллярное движение воды.
ОБЪЯВЛЕНИЯ:
2. Вода высокого напряжения:
Это происходит из-за когезии молекул воды. Благодаря этому свойству мелкие организмы плавают или ходят по поверхности воды.
3. Вода имеет высокую удельную теплоемкость и высокую теплоту парообразования:
Оба этих свойства обусловлены тем, что для разрыва водородных связей требуется больше энергии. Удельная теплоемкость означает количество тепла, поглощаемое или теряемое 1 г. вещества изменить свою температуру на 1°С. Удельная теплоемкость воды высокая (1 калория/г/°С). Это свойство обеспечивает медленный нагрев воды; поддерживать постоянную температуру живых организмов и окружающей среды.
ОБЪЯВЛЕНИЯ:
Вода имеет высокую теплоту парообразования (540 кал грамм-1), т.е. около 540 кал тепла требуется для превращения 1 г жидкой воды в газ. Таким образом, испарение воды с поверхности отводит избыточную тепловую энергию. Это обусловливает охлаждающий эффект листьев, отводит тепло тела через потоотделение и защищает организм от теплового удара.
Это обусловливает охлаждающий эффект листьев, отводит тепло тела через потоотделение и защищает организм от теплового удара.
4. Вода имеет высокую температуру кипения и высокую теплопроводность:
Благодаря этим свойствам вода сохраняет и распространяет тепло и предотвращает перегрев
5. Вода с высокой теплотой плавления:
Для замерзания воды требуется много тепла. Это предотвращает замерзание и образование льда в протоплазме даже при воздействии очень низкой температуры.
6. Вода имеет меньшую плотность при замерзании:
Вода имеет максимальную плотность при 4°C. Но ниже 4 ° C вода становится менее плотной, потому что из-за этого они раздвинуты, поэтому лед менее плотный, чем жидкая вода, и плавает на поверхности воды, лед изолирует подводную пленку от замерзания и защищает водную жизнь.
7. Вода прозрачная:
Позволяет свету проникать в море и озера на глубину до 200 м. Таким образом, растения осуществляют фотосинтез в условиях погружения.
ОБЪЯВЛЕНИЯ:
8. Вода имеет высокую диэлектрическую проницаемость:
Противодействует притяжению противоположных зарядов ионов. Из-за этого вода действует как мощный растворитель для солей и многих неионизируемых органических молекул.
9. Вода несжимаемая:
Помогает организмам переносить давление и сжатие. Из-за этого в дождевых червях вода действует как гидрокаркас. Потеря или приток воды вызывает различные движения растений, такие как движение устьиц, сейсмонастия листьев мимозы и т. д.
ОБЪЯВЛЕНИЯ:
10. Канистра для ионизации воды:
Небольшое количество воды самопроизвольно диссоциирует на ион водорода (H + ) и ион гидроксила (OH – ), что зависит от температуры. Это называется ионизацией.
Н 2 О ⇋ Н + ОН –
При 25°C из 550 миллионов молекул воды только одна подвергается ионизации. В воде H + не существует стабильно и встречается в ассоциации с другой молекулой воды с образованием иона гидроксония (H 3 O + ).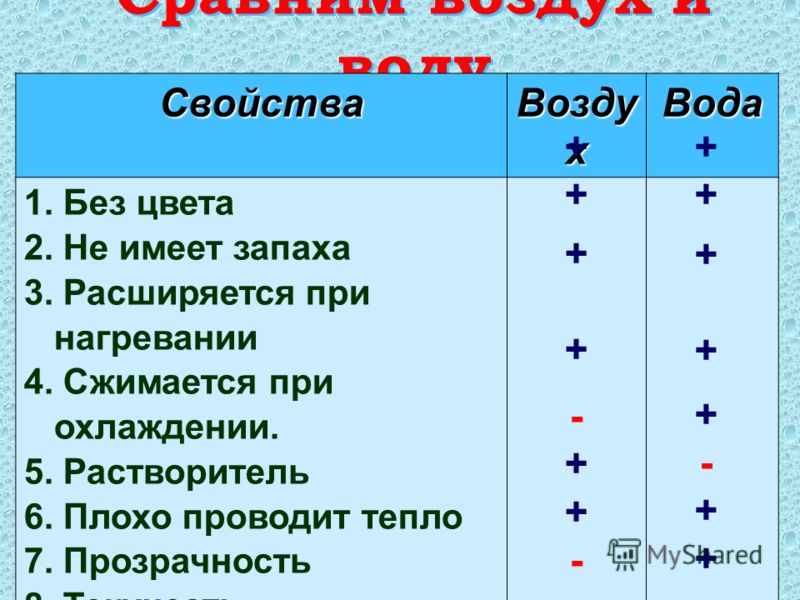


 А почему именно вода в батареях?
А почему именно вода в батареях?