Содержание
Как две молекулы воды танцуют вместе In-chemistry.ru
Владелец: CC0 Public Domain
Международная исследовательская группа открыла новое понимание того, как взаимодействуют молекулы воды. Для экспериментов потребовался лазер с особенно высокой яркостью, который имеется в лаборатории FELIX в Университете Радбуда. Их результаты помогут лучше понять странные свойства воды и опубликованы в Angewandte Chemie.
Хотя вода есть везде, взаимодействие между отдельными молекулами воды еще не полностью понято. Впервые исследователи смогли полностью наблюдать все движения между молекулами воды, известные как межмолекулярные колебания. Определенное движение отдельных молекул воды друг напротив друга, называемое затрудненным вращением, является особенно важным.
Неизвестные взаимодействия
Вода является наиболее важным растворителем в химии и биологии и обладает множеством странных свойств — например, она достигает своей максимальной плотности при четырех градусах Цельсия. Это связано с особыми взаимодействиями между молекулами воды. «Описание этих взаимодействий создавало проблемы для исследований на протяжении десятилетий», — говорит Мартина Хэвенит из Рурского университета Бохума.
«Описание этих взаимодействий создавало проблемы для исследований на протяжении десятилетий», — говорит Мартина Хэвенит из Рурского университета Бохума.
Эксперименты при экстремально низких температурах
Команда исследовала простейшее мыслимое взаимодействие, а именно между двумя отдельными молекулами воды, используя терагерцовую спектроскопию. Исследователи посылают короткие импульсы излучения в терагерцовом диапазоне через образец, который поглощает часть излучения. Картина поглощения раскрывает информацию об интересующих взаимодействиях между молекулами. Для экспериментов был необходим лазер с особенно высокой яркостью, который имеется в лаборатории университета Радбуда FELIX.
Исследователи проанализировали молекулы воды при экстремально низких температурах. Для этого они последовательно помещали отдельные молекулы воды в крошечную каплю сверхтекучего гелия, который имеет температуру 0.4 Кельвина (или -272.75 градуса Цельсия). Капли работают как пылесос, который захватывает отдельные молекулы воды. Из-за низкой температуры между двумя молекулами воды возникает стабильная связь, которая при комнатной температуре не будет стабильной.
Из-за низкой температуры между двумя молекулами воды возникает стабильная связь, которая при комнатной температуре не будет стабильной.
Эта экспериментальная установка позволила группе впервые записать спектр затрудненных вращений двух молекул воды. «Молекулы воды постоянно движутся», — объясняет Мартина Хавенит. «Они вращаются, открываются и закрываются». Однако молекула воды, в непосредственной близости от которой находится вторая молекула воды, не может свободно вращаться, поэтому ее называют препятствующей вращению.
Многомерная энергетическая карта
Взаимодействие молекул воды также может быть представлено в форме так называемого водного потенциала. «Это своего рода многомерная карта, которая отмечает, как изменяется энергия молекул воды при изменении расстояний или углов между молекулами», — объясняет Мартина Хавенит. Все свойства, такие как плотность, проводимость или температура испарения, могут быть получены из водного потенциала. «Наши измерения теперь позволяют провести наилучшую возможную проверку всех потенциалов, разработанных на сегодняшний день», — говорит исследователь.
Узнать больше: Martina Havenith-Newen et al. Observation of the low frequency spectrum of water dimer as a sensitive test of the water dimer potential and dipole moment surfaces, Angewandte Chemie International Edition (2019). DOI: 10.1002/anie.201906048
Два водорода и один кислорода – Наука – Коммерсантъ
4K
2 мин.
…
В начале своей научной карьеры Авогадро занимался в первую очередь физикой. В 1804 году он был удостоен звания члена-корреспондента, представив исследование, посвященное поведению проводников и диэлектриков в электрическом поле. В дальнейшем Авогадро регулярно публиковал свои работы, посвященные электрическим явлениям. Некоторые открытия Авогадро повлияли на других знаменитых физиков, среди которых был, например, Анри-Мари Ампер, которого Авогадро в дальнейшем назвал «одним из самых искусных физиков наших дней».
В 1804 году он был удостоен звания члена-корреспондента, представив исследование, посвященное поведению проводников и диэлектриков в электрическом поле. В дальнейшем Авогадро регулярно публиковал свои работы, посвященные электрическим явлениям. Некоторые открытия Авогадро повлияли на других знаменитых физиков, среди которых был, например, Анри-Мари Ампер, которого Авогадро в дальнейшем назвал «одним из самых искусных физиков наших дней».
Фото: Wikipedia
Авогадро также занимался выявлением связи между электрическими и химическими явлениями, вопросами теплового расширения тел и теплоемкости. В молодости он испытал влияние французского ученого Жозефа-Луи Гей-Люссака, известного своими экспериментами в области изучения газов и бесчисленными своими полетами на воздушном шаре. В 1808 году Гей-Люссак сформулировал уравнение идеального газа, которое устанавливало зависимость межу давлением, объемом и абсолютной температурой идеального газа. После серии экспериментов Гей-Люссак обнаружил, что 100 объемных частей кислорода и 200 объемных частей водорода образуют воду.
После серии экспериментов Гей-Люссак обнаружил, что 100 объемных частей кислорода и 200 объемных частей водорода образуют воду.
Хорошо знакомый с исследованиями Гей-Люссака и активно занимающийся собственными, Авогадро в 1811 году публикует «Очерк метода определения относительных масс элементарных молекул тел и пропорций, согласно которым они входят в соединения». В этой работе ученый делает вывод: поскольку объемы водорода и кислорода, образуя при соединении друг с другом воду, находятся в соотношении 2 к 1, то молекула водорода состоит из двух атомов, а не из одного, а значит, формула воды — Н2О, а не HO, как было принято считать раньше. Кроме того, Авогадро установил, что равные объемы любых газов при одинаковой температуре и давлении содержат равное число молекул. Как правильно полагал Авогадро, только тогда, когда в опытах Гей-Люссака газы занимали одинаковый объем, молекулы одного газа и молекулы другого газа реагировали между собой без остатка. Впоследствии гипотеза о равном числе молекул в одинаковых объемах газов подтвердилась многочисленными экспериментами. Так был сформулирован закон, справедливо названный впоследствии законом Авогадро.
Так был сформулирован закон, справедливо названный впоследствии законом Авогадро.
Авогадро понимал, что для идеального соотношения газов важен еще и фактор массы веществ, которые вступают в соединение друг с другом. Авогадро был одним из первых, кто стал проводить различие между молекулами и атомами вещества, между молекулярной и атомной массой. Так как масса мельчайших неделимых частиц чрезвычайно мала, то легче измерять массу атомов не в граммах, а в своеобразных «атомных упаковках» – молях (устаревшее название – «грамм-молекула»). Так же, как при одинаковых температуре-давлении газы имеют один и тот же объем, в котором содержится одно и то же число молекул, один моль вещества при равнозначных температуре-давлении имеет один и тот же объем и количество молекул. Ученый эмпирически установил, что моль одного вещества составляет 22,4 литра, а количество молекул в моле любого вещества составляет 6,02 * 10 (в степени 23). Если представить атом вещества в виде горошины, то можно представить, что количества молекул, содержащихся в одном моле, достаточно для того, чтобы покрыть всю поверхность Земли 100-метровым слоем этих горошин.
Увы, результаты работ Авогадро по молекулярной теории не были оценены при жизни ученого, а были признаны лишь в 1860 г. на I Международном конгрессе химиков в Карлсруэ.
Даниил Казбеков
Картина дня
Вся лента
SCIRP Открытый доступ
Издательство научных исследований
Журналы от A до Z
Журналы по темам
- Биомедицинские и биологические науки.
- Бизнес и экономика
- Химия и материаловедение.

- Информатика. и общ.
- Науки о Земле и окружающей среде.
- Машиностроение
- Медицина и здравоохранение
- Физика и математика
- Социальные науки. и гуманитарные науки
Журналы по тематике
- Биомедицина и науки о жизни
- Бизнес и экономика
- Химия и материаловедение
- Информатика и связь
- Науки о Земле и окружающей среде
- Машиностроение
- Медицина и здравоохранение
- Физика и математика
- Социальные и гуманитарные науки
Публикация у нас
- Представление статьи
- Информация для авторов
- Ресурсы для экспертной оценки
- Открытые специальные выпуски
- Заявление об открытом доступе
- Часто задаваемые вопросы
Публикуйте у нас
- Представление статьи
- Информация для авторов
- Ресурсы для экспертной оценки
- Открытые специальные выпуски
- Заявление об открытом доступе
- Часто задаваемые вопросы
Подпишитесь на SCIRP
Свяжитесь с нами
клиент@scirp. org org | |
| +86 18163351462 (WhatsApp) | |
| 1655362766 | |
| Публикация бумаги WeChat |
| Недавно опубликованные статьи |
| Недавно опубликованные статьи |
Европа может иметь устойчивые поставки газа из средиземноморских газовых запасов()
Ихаб Элокда, Сайед Камран Али
Журнал библиотеки открытого доступа Том 9 №12, 27 декабря 2022 г.

DOI: 10.4236/oalib.1109498
12 загрузок 143 просмотраРоль исходной функциональной МРТ как предиктора эффективности постинсультной реабилитации у пациентов с умеренной и тяжелой дисфункцией верхних конечностей (9)0003
Реза Алмаси Галех, Сарвеназ Рахимибаргани, Нилуфар Ширзад, Айлар Ахангари, Мохаммад-Реза Назем-Заде, Аболфазл Махмуди Акил Абади, Аббас Тафахори, Хамид Р. Фатех
Journal of Behavioral and Brain Science Vol.12 No.12, 27 декабря 2022 г.
DOI: 10.4236/jbbs.2022.1212039
9 загрузок 62 просмотровСравнительная эффективность микроскопии и гнездовой ПЦР для обнаружения видов Cryptosporidium у пациентов, живущих с ВИЧ/СПИДом, в Абиджане (Кот-д’Ивуар)()
Н’Дочо Асси Фиакре-Танги, Гонеделе Би Сери Эрнест, Туо Карим, Бьяле Марина Даниэль Дачо-Гуэне Аяуд, Н’Гессан Тиако Ландри, Коффи Аттоунгбре Клеман, Коффи Давид, Ако Ако Аристид Беранже, Ванга Боссон Або Генриетта, Туре Оффиан Андре
Американский журнал молекулярной биологии Том 13 № 1, 27 декабря 2022 г.

DOI: 10.4236/ajmb.2023.131002
7 загрузок 39 просмотровМелатонин улучшает память распознавания объектов посредством мелатонина MT1 и MT2 рецептор-опосредованных и нерецептор-опосредованных механизмов у самцов мышей ()
Масахиро Сано, Хикару Ивасита, Ацухико Хаттори, Ацухико Чиба
Journal of Behavioral and Brain Science Vol.12 No.12, 27 декабря 2022 г.
DOI: 10.4236/jbbs.2022.1212038
3 загрузки 26 просмотровЯвляется ли Национальный промышленный суд (NIC) по-прежнему специальным судом? Обзор дополнительного багажа дополнительной юрисдикции NIC как медвежья услуга трудовому правосудию ()
Браун Э.
 Умукоро, Питер А. Оборех
Умукоро, Питер А. ОборехBeijing Law Review Vol.13 No.4, 27 декабря 2022 г.
DOI: 10.4236/blr.2022.134061
3 загрузки 25 просмотровПринятие решений на будущее в глобализованном обществе с непредсказуемыми обстоятельствами, коллективными действиями и трансформационными путями для улучшения человеческого развития: оценка ()
Говиндхарадж Йоганандхам
Journal of Human Resource and Sustainability Studies Vol.10 No.4, 27 декабря 2022 г.
DOI: 10.4236/jhrss.2022.104050
5 загрузок 32 просмотров
Подпишитесь на SCIRP
Свяжитесь с нами
клиент@scirp. org org | |
| +86 18163351462 (WhatsApp) | |
| 1655362766 | |
| Публикация бумаги WeChat |
Бесплатные информационные бюллетени SCIRP
Copyright © 2006-2022 Scientific Research Publishing Inc. Все права защищены.
Вершина
Задачи:
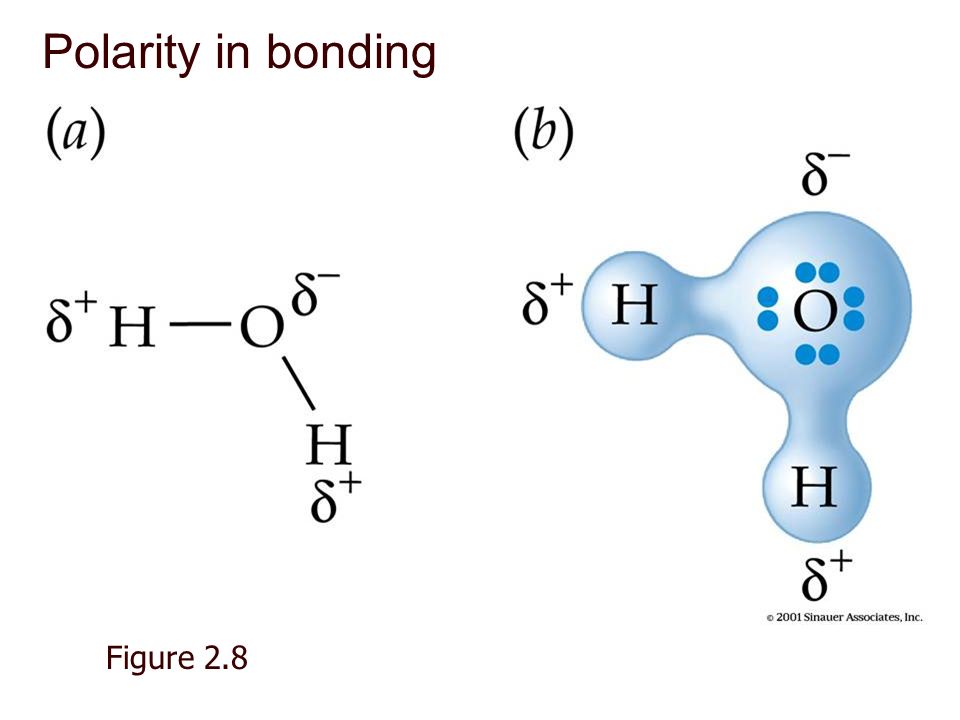
Полярность — это термин, описывающий разделение электрического заряда, приводящее к образованию молекулы, имеющей электрический диполь. Это происходит из-за неравномерного распределения частичных зарядов между атомами в молекуле. В таком соединении, как вода, электроны не распределяются поровну между двумя связанными атомами, водородом и кислородом, что приводит к частичным положительным и отрицательным зарядам. Это разделение зарядов создает диполь , то есть два полюса. Таким образом, когда молекула содержит полярные связи как таковые, молекула называется полярной. Вот почему молекула воды полярна, и это неравномерное распределение электронной плотности позволяет кислороду одной молекулы воды притягиваться к атому водорода другой молекулы и образовывать связи, называемые водородные связи . Когда многие молекулы воды образуют водородные связи с другими молекулами воды, они образуют прочную и гибкую решетку из молекул воды. Это создает высокое поверхностное натяжение. Силы, действующие на молекулу воды на поверхности и в объеме жидкости, различны, и именно так работает поверхностное натяжение. Молекула воды на поверхности притягивается к соседним молекулам воды, в том числе к тем, которые находятся ниже и по бокам, но нет других молекул воды, с которыми она могла бы взаимодействовать над поверхностью. В результате эта молекула на поверхности имеет тенденцию втягиваться в объем жидкости и, таким образом, сводит к минимуму площадь поверхности жидкости. Моющее средство , напротив, разрушает поверхностное натяжение воды. Мыло — это молекула, у которой один конец полярен, а другой — неполярен, что означает, что один конец притягивается к воде, а другой — к маслу или жиру, и именно так мыло заставляет масло и воду смешиваться и очищать жир. блюда. Это происходит потому, что моющее средство буквально физически взаимодействует с молекулами воды и ослабляет водородные связи между ними. Молекулы детергента выстраиваются в шарообразные клетки, называемые мицеллы в воде. «Водолюбивая» внешняя часть мицеллы сильно взаимодействует с водой, что снижает взаимодействие вода-вода на поверхности. Аналогичное влияние на поверхностное натяжение оказывают и другие вещества, сильно взаимодействующие с водой.
Молекулы воды — это мельчайшие частицы вещества, которые ведут себя как вода. Как вы думаете, вода на поверхности ведет себя иначе, чем вода в середине жидкости? Что делает моющее средство с водой на поверхности? Сегодня мы собираемся исследовать некоторые свойства воды на поверхности. Важно наблюдать и делать тщательные наблюдения в своем лабораторном листе.
 Деятельность 1Наполните чашку доверху водой. Как вы думаете, что произойдет, если вы добавите к нему копейки? Попробуйте добавлять монеты по одной. Что происходит с водой в стакане? Сколько пенни вы можете добавить, чтобы вода не перелилась через край? Деятельность 2
Деятельность 3
|



 Умукоро, Питер А. Оборех
Умукоро, Питер А. Оборех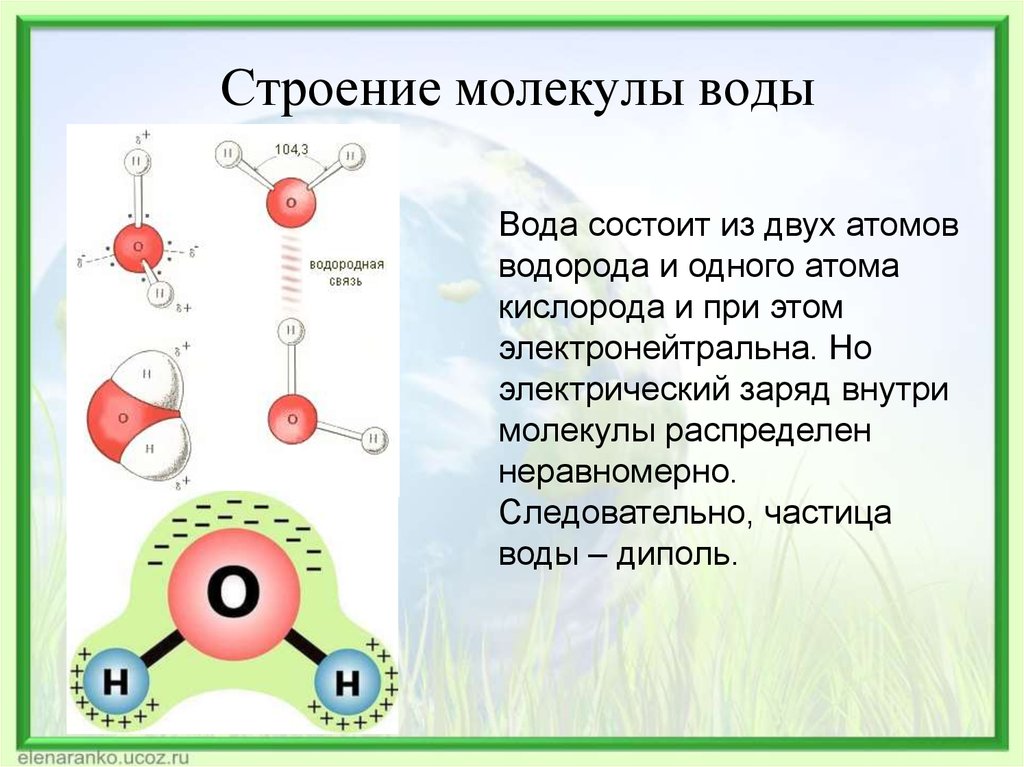 Они увидят, что некоторые вещества сильно взаимодействуют с водой и уменьшают взаимодействие между молекулами воды.
Они увидят, что некоторые вещества сильно взаимодействуют с водой и уменьшают взаимодействие между молекулами воды.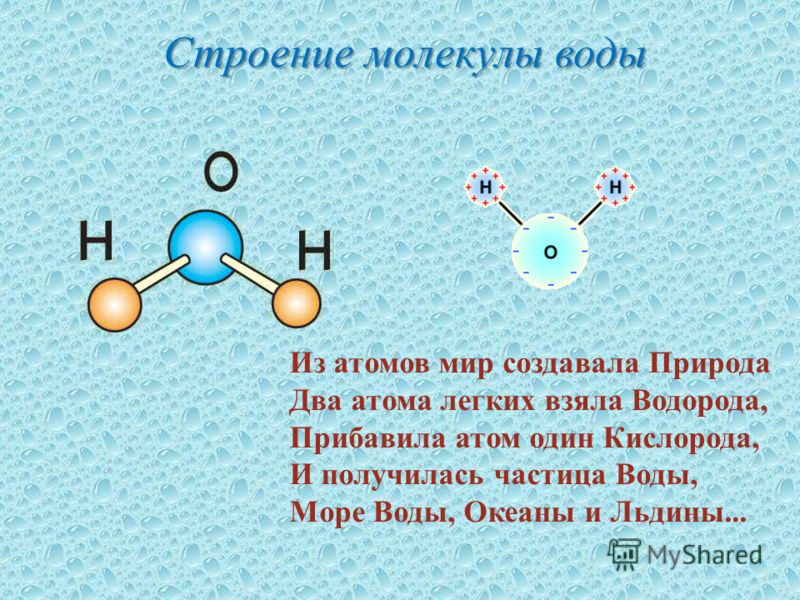 Атомы, такие как азот, кислород и галогены, как правило, имеют частичные отрицательные заряды, потому что они более электроотрицательны, способность атома притягивать к себе электроны.
Атомы, такие как азот, кислород и галогены, как правило, имеют частичные отрицательные заряды, потому что они более электроотрицательны, способность атома притягивать к себе электроны.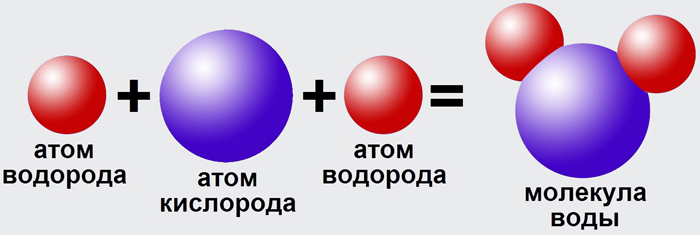 Поверхностное натяжение — это то, что позволяет водомеркам ходить по поверхности воды. Молекулы воды на поверхности не имеют других молекул воды для образования водородных связей, как другие молекулы воды, которые водородно связываются с другими молекулами воды со всех сторон, поэтому они сильнее притягиваются к молекулам воды вокруг них. Другими словами, вода имеет тенденцию иметь наименьшую возможную поверхность, чтобы стать более стабильной, пытаясь находиться внутри жидкости. Поверхностное натяжение создает поверхностную пленку и отвечает за пузырьки, капли воды и капиллярное действие.
Поверхностное натяжение — это то, что позволяет водомеркам ходить по поверхности воды. Молекулы воды на поверхности не имеют других молекул воды для образования водородных связей, как другие молекулы воды, которые водородно связываются с другими молекулами воды со всех сторон, поэтому они сильнее притягиваются к молекулам воды вокруг них. Другими словами, вода имеет тенденцию иметь наименьшую возможную поверхность, чтобы стать более стабильной, пытаясь находиться внутри жидкости. Поверхностное натяжение создает поверхностную пленку и отвечает за пузырьки, капли воды и капиллярное действие.
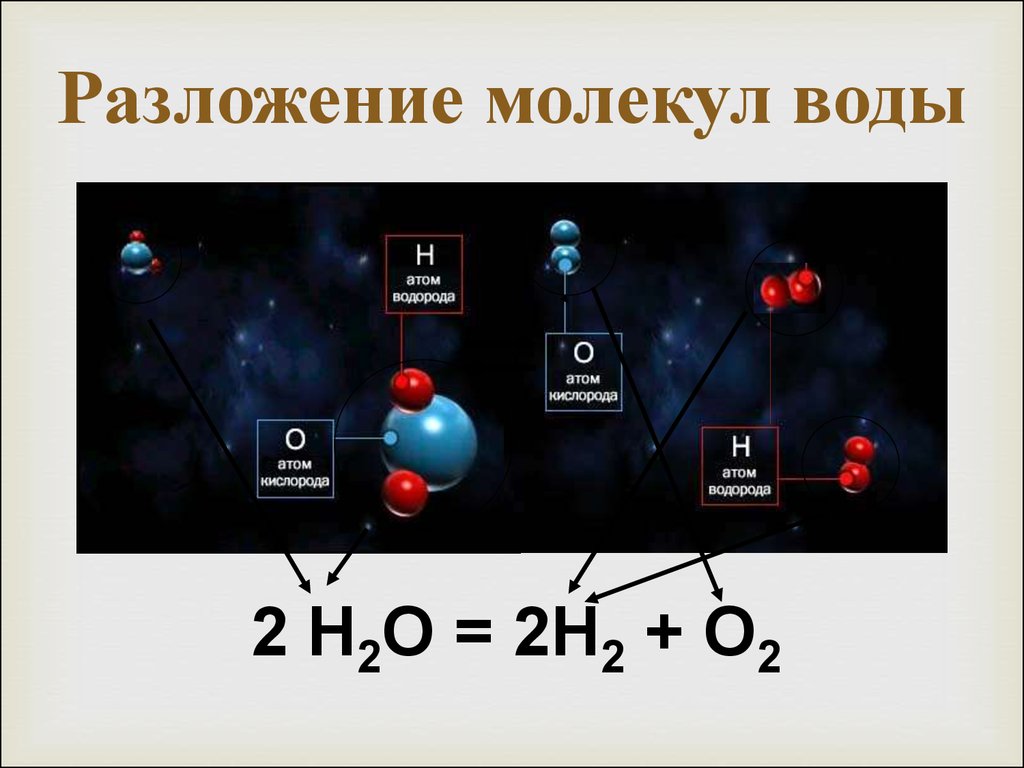
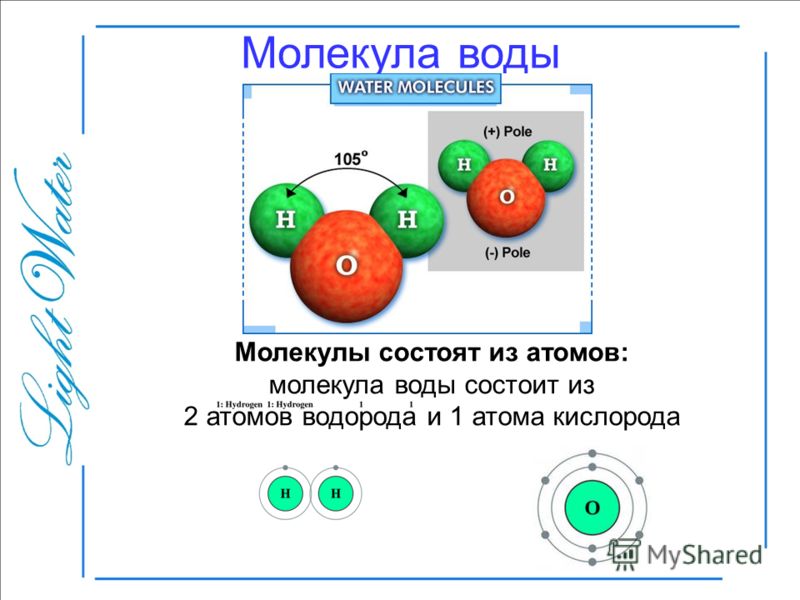 В водяном паре или паре есть отдельные молекулы воды, которые движутся сами по себе. Однако в жидкой воде молекулы воды прочно связаны с другими молекулами воды во всех направлениях. На поверхности воды вода связана с другими молекулами воды в жидкости и вдоль поверхности, но над поверхностью не может быть никаких связей.
В водяном паре или паре есть отдельные молекулы воды, которые движутся сами по себе. Однако в жидкой воде молекулы воды прочно связаны с другими молекулами воды во всех направлениях. На поверхности воды вода связана с другими молекулами воды в жидкости и вдоль поверхности, но над поверхностью не может быть никаких связей.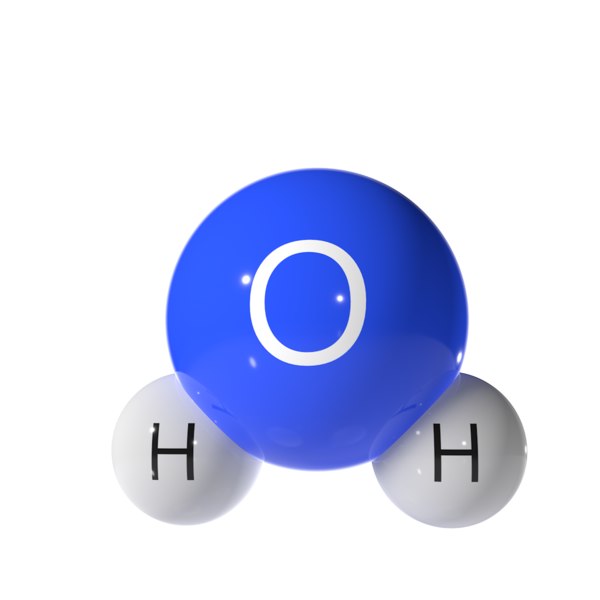 Что делает перец? Запишите свои наблюдения.
Что делает перец? Запишите свои наблюдения.