Роль свойств воды в биологических процессах и явлениях. Биологические свойства воды
Биологические свойства воды :: Живая вода
Вода как растворительВода - превосходный растворитель для полярных веществ. К ним относятся ионные соединения, такие как соли, у которых заряженные частицы (ионы) диссоцииируют в воде, когда вещество растворяется, а также некоторые неионные соединения, например сахара и простые спирты, в молекуле которых присутствуют заряженные (полярные) группы (-OH).
Гидратация ионов в водеРезультаты многочисленных исследований строения растворов электролитов свидетельствуют, что при гидратации ионов в водных растворах основную роль играет ближняя гидратация - взаимодействие ионов с ближайшими к ним молекулами воды. Большой интерес представляет выяснение индивидуальных характеристик ближней гидратации различных ионов, как степени связывания молекул воды в гидратных оболочках, так и степени искажения в этих оболочках тетраэдрической льдоподобной структуры чистой воды - связи в молекуле изменяются на неполный угол. Величина угла зависит от иона.
Что происходит с растворенными в воде веществами?Когда вещество растворяется, его молекулы или ионы получают возможность двигаться более свободно и, соответственно, его реакционная способность возрастает. По этой причине в клетке большая часть химических реакций протекает в водных растворах. Неполярные вещества, например липиды, не смешиваются с водой и потому могут разделять водные растворы на отдельные компартаменты, подобно тому, как их разделяют мембраны. Неполярные части молекул отталкиваются водой и в её присутствии притягиваются друг к другу, как это бывает, например, когда капельки масла сливаются в более крупные капли; иначе говоря, неполярные молекулы гидрофобны. Подобные гидрофобные взаимодействия играют важную роль в обеспечении стабильности мембран, а также многих белковых молекул, нуклеиновых кислот и других субклеточных структур.
Вода - транспортПрисущие воде свойства растворителя означают также, что вода служит средой для транспорта различных веществ. Эту роль она выполняет в крови, в лимфатической и экскреторных системах, в пищеварительном тракте и во флоэме и ксилеме растений.
Теплоемкость водыБольшая теплоёмкость. Удельной теплоёмкостью воды называют количество теплоты в джоулях, которое необходимо, чтобы поднять температуру 1 кг воды на 1° C. Вода обладает большой теплоёмкостью (4,184 Дж/г). Это значит, что существенное увеличение тепловой энергии вызывает лишь сравнительно небольшое повышение её температуры. Объясняется такое явление тем, что значительная часть этой энергии расходуется на разрыв водородных связей, ограничивающих подвижность молекул воды.
Большая теплоёмкость воды сводит к минимуму происходящие в ней температурные изменения. Благодаря этому биохимические процессы протекают в меньшем интервале температур, с более постоянной скоростью и опасность нарушения этих процессов от резких отклонений температуры грозит им не столь сильно. Вода служит для многих клеток и организмов средой обитания, для которой характерно довольно значительное постоянство условий.
Теплота испарения водыБольшая теплота испарения. Скрытая теплота испарения есть мера количества тепловой энергии, которую необходимо сообщить жидкости для её перехода в пар, то есть для преодоления сил молекулярного сцепления в жидкости. Испарение воды требует довольно значительных количеств энергии (2494 Дж/г). Это объясняется существованием водородных связей между молекулами воды. Именно в силу этого температура кипения воды - вещества со столь малыми молекулами - необычно высока.
Энергия, необходимая молекулам воды для испарения, черпается из их окружения. Таким образом, испарение сопровождается охлаждением. Это явление используется у животных при потоотделении, при тепловой одышке у млекопитающих или у некоторых рептилий (например, у крокодилов), которые на солнцепёке сидят с открытым ртом; возможно, оно играет заметную роль и в охлаждении транспирирующих листьев.
Теплота плавления водыБольшая теплота плавления. Скрытая теплота плавления есть мера тепловой энергии, необходимой для расплавления твёрдого вещества (льда). Воде для плавления (таяния) необходимо сравнительно большое количество энергии. Справедливо и обратное: при замерзании вода должна отдать большое количество тепловой энергии. Это уменьшает вероятность замерзания содержимого клеток и окружающей их жидкости. Кристаллы льда особенно губительны для живого, когда они образуются внутри клеток.
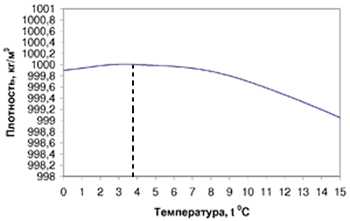
Плотность водыПлотность и поведение воды вблизи точки замерзания. Плотность воды (максимальна при +4° С) от +4 до 0° С понижается, поэтому лёд легче воды и в воде не тонет. Вода - единственное вещество, обладающее в жидком состоянии большей плотностью, чем в твёрдом, так как структура льда более рыхлая, чем структура жидкой воды. Это - одно из аномальных свойств воды.
Поскольку лёд плавает в воде, он образуется при замерзании сначала на её поверхности и лишь под конец в придонных слоях. Если бы замерзание прудов шло в обратном порядке, снизу вверх, то в областях с умеренным или холодным климатом жизнь в пресноводных водоёмах вообще не могла бы существовать. То обстоятельство, что слои воды, температура которых упала ниже 4° С, поднимаются вверх, обусловливает перемешивание воды в больших водоёмах. Вместе с водой циркулируют и находящиеся в ней питательные вещества, благодаря чему водоёмы заселяются живыми организмами на большую глубину.
После проведения ряда экспериментов было установлено, что связанная вода при температуре ниже точки замерзания не переходит в кристаллическую решётку льда. Это энергетически невыгодно, так как вода достаточно прочно связана с гидрофильными участками растворённых молекул. Это находит применение в криомедицине.
Поверхностное натяжение воды и когезияБольшое поверхностное натяжение и когезия. Когезия - это сцепление молекул физического тела друг с другом под действием сил притяжения. На поверхности жидкости существует поверхностное натяжение - результат действующих между молекулами сил когезии, направленных внутрь. Благодаря поверхностному натяжению жидкость стремится принять такую форму, чтобы площадь её поверхности была минимальной (в идеале - форму шара). Из всех жидкостей самое большое поверхностное натяжение у воды (7,6 · 10-4 Н/м). Значительная когезия, характерная для молекул воды, играет важную роль в живых клетках, а также при движении воды по сосудам ксилемы в растениях. Многие мелкие организмы извлекают для себя пользу из поверхностного натяжения: оно позволяет им удерживаться на воде или скользить по её поверхности.
Вода как реагентБиологическое значение воды определяется и тем, что она представляет собой один из необходимых метаболитов, то есть участвует в метаболических реакциях. Вода используется, например, в качестве источника водорода в процессе фотосинтеза, а также участвует в реакциях гидролиза.
zhivaja-voda.webnode.cz
Биологические свойства воды
Как растительные, так и животные микро- и макроорганизмы, населяющие водоемы, называются биоценозом. Кроме рыб, речных и морских животных, относящихся к так называемому нектону, все водные организмы разделяются на планктон и бентос. Организмы, которые, находясь во взвешенном состоянии, самостоятельно или пассивно перемещаются в воде, называются планктоном, а организмы, связанные с дном водоема и с поверхностью различных подводных предметов (камней, свай и пр.), называются бентосом. По населяющим воду видам организмов можно судить о санитарных свойствах воды. В зависимости от качества водной среды в ней живут определенные, более или менее типичные (индикаторные) представители зоопланктона и фитопланктона.
Всех водных организмов по степени приспособленности их к загрязнению воды делят на полисапробов, мезосапробов, олигосапробов и катаробов.
Полисапробная группа организмов развивается в коде, сильно загрязненной органическими веществами, и не нуждается в свободном кислороде. Представители этой группы: бесцветные жгутиковые, инфузории и огромное количество бактерий, особенно анаэробов и серных.
Альфа-мезосапробная группа организмов обитает в воде, загрязненной органическими веществами, в которой уже идут окислительные процессы и присутствует кислород. Количество микроорганизмов в 1 мл поды составляет сотни тысяч. Это бактерии, грибы, простейшие и водоросли (диатомовые и сине-зеленые).
Бета-мезосапробная группа организмов обитает в водах, в которых протекают окислительные процессы; эти организмы питаются минеральными веществами и нуждаются в свободном кислороде. Количество микроорганизмов в 1 мл такой воды исчисляется десятками тысяч. Эту группу составляют бактерии, инфузории, жгутиковые, водоросли различных видов, ракообразные, коловратки и рыбы.
Олигосапробная группа организмов характерна для чистой воды, пригодной для водоснабжения, свободной от загрязнения и богатой кислородом. Количество микроорганизмов исчисляется тысячами в 1 мл вода. Представители данной группы: водоросли зеленые, диатомовые, коловратки, губки, ракообразные, рыбы и водяные цветковые растения.
Катаробкая группа организмов — показатель совершенно чистой воды.
Таким образом, представители планктона и бентоса, очищая водоемы от органических веществ, являются в то же время показателями степени загрязнения воды. Определенные заключения могут быть сделаны и по выживаемости в водоеме некоторых пород рыб, из которых особенно чувствительны к загрязнению форель, стерлядь и др., а наиболее выносливые — тука, окунь, плотва, линь, карась и карп.
Во всех природных водах, за исключением глубоких подземных, имеется большое количество микроорганизмов как свойственных воде (водных), так и случайных, пребывающих в ней временно. В незагрязненной органическими веществами воде содержится много кислорода, а потому населяют ее аэробные микроорганизмы. В воде, загрязненной органическими веществами, бедной кислородом, находятся анаэробные микроорганизмы. Однако количество микроорганизмов имеет общеориентирующее значение для характеристики качества воды. Согласно ГОСТ, в 1 мл хорошей воды допустимо не более 100-1000 бактерий.
При загрязнении водоемов отбросами животного происхождения (навозом, мочой, сточными водами промышленных предприятий, перерабатывающих животное сырье) не исключена возможность заражения воды патогенными микроорганизмами и яйцами гельминтов. В этих случаях вода может явиться источником заражения животных инфекционными и инвазионными болезнями.
К таким инфекциям в первую очередь можно отнести сибирскую язву, паратиф, туберкулез, бруцеллез, туляремию, рожу, листереллез, инфекционную анемию, инфекционный гепатит утят и некоторые другие.
Известно также, что через воду могут передаваться холера, брюшной тиф, паратиф, дизентерия, лептоспироз, туляремия, полиомиелит и некоторые другие инфекционные болезни человека (Л. В. Громашевский).
Данные разных исследований о сроках возможного выживания патогенных бактерий в воде довольно противоречивы. Так, в экспериментальных условиях возбудители разных инфекционных болезней могут проявлять жизнеспособность и вирулентность в течение недель, нескольких месяцев и больше (П. А. Муханцев, В. И. Полтев, И. А. Каркалиновская, П. Ф. Милявская и др.). В естественных условиях поступающие в водоемы патогенные бактерии подвергаются большому разведению, противоставляются огромному числу их антагонистов — сапрофитов и скоро погибают. Последнее, однако, не снимает опасности воды в возникновении инфекционных заболеваний животных в результате постоянного или значительного инфицирования водоисточников.
При бактериологическом исследовании воды наиболее важным было бы непосредственное определение в ней наличия патогенных микробов. Однако выявить в воде патогенные микроорганизмы весьма трудно. Иногда заведомо в инфицированной воде их не удается обнаружить, поэтому при бактериологическом контроле за качеством воды обычно пользуются косвенным методом, при котором определяют показатели фекального загрязнения. Основным показателем фекального загрязнения воды служит кишечная палочка (В. coli) — постоянный обитатель кишечника животных и человека. Чем больше вода загрязнена кишечной палочкой, тем больше вероятности встретить патогенных микроорганизмов и зародышей гельминтов, так как путь их попадания в воду один и тот же. При сильных загрязнениях воды отбросами животного происхождения кишечная палочка обнаруживается в небольших объемах ее, а в чистой воде кишечную палочку удается найти лишь в большом объеме воды.
Поэтому по степени загрязненности воды и пригодности ее для поения животных судят также по коли-титру (титру кишечной палочки) и коли-индексу.
Коли-титром называется тот наименьший объем исследуемой воды в миллилитрах, в котором обнаруживается кишечная палочка. Хорошая питьевая вода по стандарту должна иметь коли-титр не ниже 200—300 мл.
Коли-индексом называется число кишечных палочек, содержащихся в 1 л исследуемой воды.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
www.activestudy.info
""Биологические свойства воды" - Биология

Тема урока: «Биологические свойства воды»
Цель урока : Расширить представление о воде как универсальном веществе на Земле.
Тип урока : Обобщить полученные знания по теме: «Биологические свойства
воды».
Оборудование урока: тесты , тетрадные листы,ручки , презентация, компьютер , интерактивная доска, кристаллизатор с водой и льдом.
Вид урока : Деловая игра (пресс-конференция).
Задачи урока:
1) Обобщить знания о биологических свойствах воды.
2) Выяснить значение воды в природе и в жизни живых организмов.
3) Выяснить аномальные свойства воды.

План урока.
1. Организационный момент.
2. Вступительное слово учителя.
3. Работа исследовательских групп:
А) Группа «Биохимики».
Б) Группа «Биофизики».
В) Представители СЭС.
4. Рефлексия.
5. Подведение итогов урока.
6.Домашнее задание

Биологическая функция воды в природе состоит в том, что она:
1. Обеспечивает поддержание структуры организмов.
2. Служит растворителем и средой для диффузии.
3. Участвует в реакциях гидролиза.
4. Среда для оплодотворения.
5. Обеспечивает распространение семян, гамет, личиночных стадий водных животных.

Главными биологическими функциями воды для растительных организмов являются следующие:
1. Поддержание осмотического и тургорного давления.
2. Участвует в процессе фотосинтеза.
3. Обеспечивает транспирацию.
4. Обеспечивает прорастание семян.

Не менее важны биологические функции воды для животных и человека. Наиболее значимые из них такие:
1. Обеспечивают транспорт веществ.
2. Способствуют охлаждению тела.
3. Обеспечивают осморегуляцию.
4. Выполняет защитную функцию (слезы).
5. Способствует миграции (морские течения).

Тесты с выбором одного или нескольких правильных ответов из трех предложенных:
1. Воды больше в клетках организма:
а) мужского;
б) женского;
в) одинаковое количество.
2. В образовании молекулы воды участвуют связи:
а) ковалентные и водородные;
б) только ковалентные;
в) только водородные.
3. Живые организмы не могут долго существовать без воды, так как :
а) организм обезвоживается;
б) нарушается обмен веществ;
в) нарушается гомеостаз.
4. В молекулах воды могут растворятся молекулы :
а) полярные;
б) полярные и неполярные;
в) неполярные.
5. К гидрофильным веществам относятся :
а) фруктоза;
б) инулин;
в) камедь.
6. К гидрофобным веществам относятся :
а) триглицериды;
б) тетрозы;
в) гексозы.
7. Для воды характерны агрегатные состояния :
а) твердое, жидкое, газообразное;
б) твердое, жидкое, коллоидное;
в) твердое, коллоидное, жидкое, газообразное.
8. Молекулы воды взаимодействуют с химическими веществами, элементы в которых имеют связи:
а) электростатические;
б) дисульфидные;
в) гидрофобные.
2 этап урока.

В 1783 коду выдающиеся экспериментаторы Генри Кавендиш и Антуан Лавуазье установили, что вода состоит из двух газов: водорода и кислорода, соотношение которых выражается формулой Н 2 О
Антуан Лавуазье
Генри Кавендиш
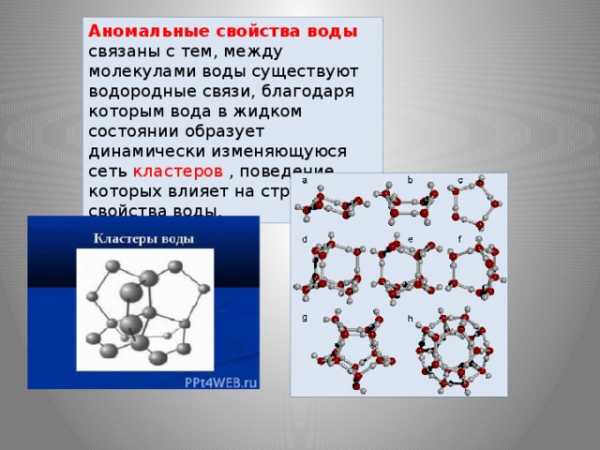
Аномальные свойства воды связаны с тем, между молекулами воды существуют водородные связи, благодаря которым вода в жидком состоянии образует динамически изменяющуюся сеть кластеров , поведение которых влияет на структуру и свойства воды.

Уникальным свойством воды является то, что вода имеет непостоянную плотность при определенных температурных режимах :
1. При охлаждении от + 100 о С до – 4 о С вода сжимается увеличивая свою плотность.
2. При температуре + 4 о С – она имеет найбольшую плотность. Но при охлаждении вода вновь начинает расширяться, а ее плотность уменьшается.
3. При 0 о С вода переходит в твердое агрегатное состояние.

Удивительные свойства приобретает вода в нанотрубках , диаметр которых 1х10 -9 м: резко увеличивается ее вязкость и вода не замерзает при температурах близких к абсолютному нулю. Молекулы воды в нанотрубках при температуре -23 о С и давлении 40 тысяч атмосфер самостоятельно выстраивает спиральные лесенки, в том числе и двойные спирали, которые напоминают структуру ДНК.
Рис. Внутренняя стенка структуры воды (изображение New Scientist)

Существует мнение о том, что кристаллы воды реагируют на звуки музыки, отдельные фразы, слова:
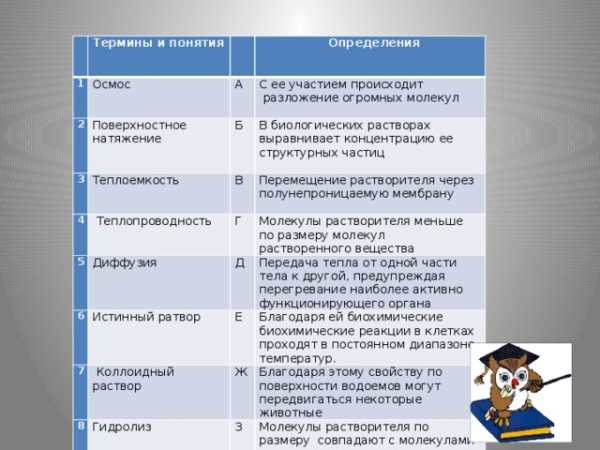
Термины и понятия
1
Осмос
2
Определения
А
Поверхностное натяжение
3
Теплоемкость
С ее участием происходит
Б
4
5
В
Теплопроводность
разложение огромных молекул
В биологических растворах выравнивает концентрацию ее структурных частиц
Г
Диффузия
6
Перемещение растворителя через полунепроницаемую мембрану
7
Молекулы растворителя меньше по размеру молекул растворенного вещества
Д
Истинный ратвор
8
Коллоидный раствор
Е
Передача тепла от одной части тела к другой, предупреждая перегревание наиболее активно функционирующего органа
Благодаря ей биохимические биохимические реакции в клетках проходят в постоянном диапазоне температур.
Ж
Гидролиз
Благодаря этому свойству по поверхности водоемов могут передвигаться некоторые животные
З
Молекулы растворителя по размеру совпадают с молекулами растворенного вещества

« Живительная» влага может быть опасной !
Например, в воде, которая поступает в кран, может содержаться до 700 вредных веществ и не только:
1. Болезнетворные бактерии (холерный вибрион, кишечная и дизентирийная палочка, сальмонелла и др.).
2 Вирусы (например, вирус гепатита).
3. Нитраты (уменьшают содержание кислорода в крови, вызывая кислородное голодание, а также приводящее к раку желудочно – кишечного тракта).
4.Хлор ( приводит к образованию опухолей прямой кишки, простаты, мочевого пузыря)
5.Соли тяжелых металлов ( вызывают мутации и зашлаковывание организма).
6. Избыток алюминия (способствует развитию болезни Альцгеймера).
7. Свинец (замедляет физическое и психическое развитие у детей, у взрослых повышает давление крови, вызывает проблемы с почками).
8 Повышенное содержание солей кальция и магния, разные формы железа – неблагоприятно воздействуют на сердечно – сосудистую систему.

Правилами «здорового потребления воды» :
1. Выпивайте в день, как минимум, 8 стаканов воды.
2. Равномерно распределите потребление питьевой воды в течении дня.
3. Питьевую воду не заменять чай, кофе или безалкогольные напитки.
4. Питьевую воду пкйте перед, во время и после тяжелой работы.
5. Стаканом воды начинайте и заканчивайте свой день.
Учитель благодарит выступающих.

Задача.
Общее количество воды в организме человека составляет от 44% до 70% массы человека.
Посчитайте:
а) сколько литров воды содержится в вашем теле;
б) суточную потребность вашего организма в воде;
в) сколько воды из выше посчитанного количества поступает вместе с пищей;
г) сколько воды вы должны выпивать еще ( кроме воды, поступающей с пищей), чтобы удовлетворить суточную потребность в воде?

Рефлексия
Вопросы:
1. Вам понравился урок?
2. Что нового для себя вы узнали?
3. Каков ваш личный вклад на уроке?

Урок окончен. До свидания!
multiurok.ru
Вода в жизни человека. Биологическое и экологическое значение воды :: SYL.ru
Вода – источник жизни на Земле, великая природная ценность, покрывающая 71% поверхности нашей планеты, самое распространенное химическое соединение и необходимая основа для существования всего живого на планете. Высокое содержание в растениях (до 90%) и в теле человека (около 70%) лишь подтверждает важность этого компонента, не имеющего вкуса, запаха и цвета.
Вода – это жизнь!
Роль воды в жизни человека неоценима: она используется для питья, пищи, умывания, различных хозяйственных и промышленных нужд. Вода – это жизнь!  Роль воды в жизни человека можно определить по занимаемой ею доле в теле и органах, каждая клетка которых богата водным раствором из необходимых питательных веществ. Вода – одно из эффективных средств физического воспитания, широко использующееся для личной гигиены, оздоровительной физкультуры, закаливания, водных видов спорта.
Роль воды в жизни человека можно определить по занимаемой ею доле в теле и органах, каждая клетка которых богата водным раствором из необходимых питательных веществ. Вода – одно из эффективных средств физического воспитания, широко использующееся для личной гигиены, оздоровительной физкультуры, закаливания, водных видов спорта.
Биохимические свойства воды
Сохранение упругости и объема живой клетки было бы невозможным без воды, равно как и значительная часть химических реакций организма, протекающих именно в водных растворах. Незаменимой столь ценную жидкость делает ее теплопроводность и теплоемкость, обеспечивающая терморегуляцию и защищающая от температурных перепадов.  Вода в жизни человека способна растворять некоторые кислоты, основания и соли, представляющие ионные соединения и некоторые полярные неионные образования (простые спирты, аминокислоты, сахара), называемые гидрофильными (с греч. дословно – склонность к влаге). Не под силу жидкости нуклеиновые кислоты, жиры, белки и некоторые полисахариды - гидрофобные вещества (с греч. – страх влаги).
Вода в жизни человека способна растворять некоторые кислоты, основания и соли, представляющие ионные соединения и некоторые полярные неионные образования (простые спирты, аминокислоты, сахара), называемые гидрофильными (с греч. дословно – склонность к влаге). Не под силу жидкости нуклеиновые кислоты, жиры, белки и некоторые полисахариды - гидрофобные вещества (с греч. – страх влаги).
Биологическое значение воды достаточно велико, так как эта бесценная жидкость является основной средой при протекающих в организме внутренних процессах. В процентном соотношении наличие воды в организме выглядит следующим образом:
Системы организма | Содержание, % |
Жировые ткани | 25 |
Кости | До 28 |
Печень | До 69 |
Мышцы | 75 |
Почки | До 82 |
Мозг | До 85 |
Кровь | 92 |
Интересные высказывания о воде
Интересно по этому поводу высказывание фантаста В. Савченко, одной фразой раскрывшего значение воды: у человека имеется значительно больше мотивов считать себя жидкостью в отличие, к примеру, от 40%-го раствора натрия. А среди биологов популярна шутка, что в качестве средства собственного передвижения вода «изобрела» человека, основным компонентом организма которого она является. 2/3 ее общего количества содержится внутри клеток и именуется «внутриклеточной», или «структурируемой» жидкостью, которая способна обеспечивать устойчивость организма к влиянию отрицательных факторов внешней среды. Третья часть воды находится вне клеток, причем 20% этого количества составляет сама межклеточная жидкость, 2% и 8% - соответственно, вода лимфы и плазмы крови.
Значение воды в жизни человека
Значение природного компонента в жизни и быту просто неоценимо, так как без него невозможно существование в принципе.
Вода необходима для жизни потому, что:
- увлажняет вдыхаемый кислород;
- помогает организму в качественном усвоении питательных веществ;
- способствует превращению пищи в энергию и нормальному пищеварению;
- участвует в проходящем обмене веществ и химических реакциях;
- выводит излишки солей, шлаки и токсины;
- отлаживает температуру тела;
- обеспечивает упругость кожи;
- регулирует кровяное давление;
- препятствует возникновению камней в почках;
- является своего рода «смазкой» для суставов и амортизатором для спинного мозга;
- оберегает жизненно важные органы.
Круговорот воды в организме
Одно из условий существования всего живого – постоянное содержание воды, количество поступления которой в организм зависит от образа жизни человека, его возраста, физического здоровья, факторов внешней среды. В течение суток до 6% имеющейся в организме воды подвергается обмену; в течение 10 дней обновляется половина ее общего количества. Так, в сутки организм теряет воды примерно 150 мл с калом, около 500 мл с выдыхаемым воздухом и столько же с потом и 1,5 литра выводится с мочой. Примерно такое же количество воды (около 3 литров в сутки) человек получает обратно. Из них треть литра образуется в самом организме во время биохимических процессов, а около 2 литров потребляется с пищей и напитками, причем суточная потребность в исключительно питьевой воде составляет где-то 1,5 литра.
В последнее время специалисты подсчитали, что человек все-таки должен выпивать воды в чистом виде около 2 литров в день, чтобы не допустить даже малейшего обезвоживания организма. Такое же количество рекомендуют потреблять йоги, знающие истинное значение воздуха и воды. Абсолютно здоровый человеческий организм в идеале должен иметь состояние водного равновесия, называемое иначе водным балансом.
К слову, немецкие ученые после ряда проведенных на студентах экспериментов выяснили, что большую выдержанность и склонность к творчеству проявляют те из них, кто больше остальных пьет воду и напитки. Вода в жизни человека играет побудительную роль, наполняя энергией и жизненными силами.
По некоторым подсчетам за 60 лет жизни человек в среднем выпивает около 50 тонн воды, что соизмеримо практически с целой цистерной. Интересно знать, что обычная пища наполовину состоит из воды: в мясе ее – до 67%, в кашах – 80%, овощи и фрукты содержат до 90%, хлеб – около 50%.
Ситуации повышенного потребления воды
Обычно человек в день получает около 2-3 литров воды, но существуют ситуации, при которых потребность в ней увеличивается. Это:
- Повышенная температура тела (более 37°C). С каждым возрастающим градусом воды требуется на 10% больше от общего количества.
- Тяжелая физическая работа на свежем воздухе, при которой жидкости нужно выпивать 5 – 6 литров.
- Работа в горячих цехах – до 15 литров.
Дефицит ценной жидкости является причиной возникновения многих заболеваний: аллергии, астмы, избыточного веса, повышенного артериального давления, эмоциональных проблем (депрессии в том числе), а ее отсутствие приводит к нарушению выполнения всех функций организма, подрывая здоровье и делая уязвимым для болезней.
Потеря воды до 2% от общей массы тела (1 – 1,5 литра) вызовет у человека чувство жажды; утрата 6 – 8% приведет к полуобморочному состоянию; 10% обусловят появление галлюцинаций и нарушение глотательной функции. Лишение 12% воды от общей массы тела приведет к гибели. Если без пищи человек способен просуществовать около 50 дней при условии потребления питьевой воды, то без нее - максимум 5 дней.
В действительности большая часть людей выпивает воды меньше рекомендуемого количества: всего лишь третью часть, причем появляющиеся недомогания нисколько не связываются с недостатком жидкости.
Признаки недостатка воды в организме
Первые признаки обезвоживания:
- головокружение;
- шелушение и сухость кожи;
- усталость и вялость;
- боли в суставах и спине;
- снижение работоспособности;
- нарушение пищеварительных и кровообразовательных процессов,
- увеличение вязкости крови и, как следствие, повышение риска тромбообразования.

Стабильное поступление воды в организм в необходимом количестве способствует обеспечению жизненного тонуса, избавлению от недомоганий и многих серьезных заболеваний, улучшению мышления и координационных действий мозга. Поэтому появляющуюся жажду всегда нужно стараться утолить. Лучше при этом пить часто и понемногу, так как большое количество жидкости с целью разового пополнения ежедневной нормы полностью впитается в кровь, что даст ощутимую нагрузку на сердце до момента выведения воды из организма почками.
Водный баланс организма – прямой путь к здоровью
Иными словами, вода в жизни человека при правильно организованном питьевом режиме способна создать приемлемые условия для сохранения необходимого водного баланса. Важно, чтобы жидкость при этом была высокого качества, с наличием необходимых минеральных веществ. Парадоксальной является ситуация современного мира: вода, источник жизни на Земле, может быть опасна для самой жизни, неся практически с каждой каплей разнообразные инфекции. То есть полезной для организма может быть только чистая вода, проблема качества которой в современном мире очень актуальна.
Дефицит воды – страшное будущее планеты
Вернее, жизненно важной становится сама проблема наличия питьевой воды, с каждым днем превращающейся во все более дефицитный продукт. Причем значение воды на Земле и ее недостаток в международных отношениях обсуждаются на высшем уровне и часто конфликтным способом.  Сейчас более 40 стран испытывают недостаток воды по причине засушливости многих регионов. Через 15 – 20 лет, даже по самым оптимистичным прогнозам, значение воды на Земле поймет каждый человек, так как проблема ее нехватки затронет 60 – 70% населения планеты. В развивающихся странах водный дефицит вырастет на 50%, в развитых – на 18%. Как следствие, усилится международная напряженность вокруг темы нехватки водных ресурсов.
Сейчас более 40 стран испытывают недостаток воды по причине засушливости многих регионов. Через 15 – 20 лет, даже по самым оптимистичным прогнозам, значение воды на Земле поймет каждый человек, так как проблема ее нехватки затронет 60 – 70% населения планеты. В развивающихся странах водный дефицит вырастет на 50%, в развитых – на 18%. Как следствие, усилится международная напряженность вокруг темы нехватки водных ресурсов.
Загрязненная вода как результат деятельности человека
Связано это с геофизическими условиями, хозяйственной деятельностью человека, часто непродуманной и безответственной, что значительно увеличивает нагрузку на водные ресурсы и приводит к их загрязнению. Огромное количество воды уходит на нужды городов и промышленности, которые не только потребляют, но и загрязняют воду, сбрасывая в водоемы ежедневно около 2 млн тонн отходов. То же самое касается сельского хозяйства, у которого миллионы тонн продуктов жизнедеятельности и удобрений стекают в водоемы с ферм и полей. В Европе из 55 рек только 5 считаются чистыми, в то время как в Азии все реки чрезвычайно засорены отходами сельскохозяйственного производства и металлами. В Китае недостаток воды испытывают 550 городов из 600; из-за сильного загрязнения в водоемах не выживает рыба, а некоторые реки, впадающие в океан, просто до него не дотекают.
Что течет из кранов
Да и зачем далеко ходить, если качество воды, оставляющее желать лучшего, касается практически каждого человека. Значение воды в жизни человека велико, особенно актуально это ощущается при ее потреблении, когда санитарные нормы идут вразрез с качеством потребляемой жидкости, в которой присутствуют вредные для здоровья пестициды, нитриты, нефтепродукты, соли тяжелых металлов. Половина населения получает опасную для здоровья воду, вызывающую около 80% всех известных болезней.
Хлор – опасно!
Для избежания возможного заражения какой-либо инфекцией вода хлорируется, что нисколько не умаляет опасность. Наоборот, хлор, уничтожающий множество опасных микробов, образует вредные для здоровья химические соединения и провоцирует такие заболевания, как гастрит, пневмония, онкология. При кипячении он не успевает раствориться полностью и соединяется с всегда присутствующими в воде органическими веществами. При этом образуются диоксины – очень опасные яды, превосходящие по своей силе даже цианистый калий.  Водное отравление намного страшнее пищевого, потому как вода в жизни человека, в отличие от пищи, принимает участие во всех биохимических процессах организма. Диоксины, накапливаемые в организме, разлагаются очень медленно, практически десятки лет. Вызывая нарушения эндокринной системы, репродуктивных функций, они разрушают иммунитет, обуславливают раковые заболевания и генетические аномалии. Хлор является самым опасным убийцей современности: убивая одну болезнь, он порождает другую, еще страшнее. После того как в 1944 году началось глобальное хлорирование воды, стали массово проявляться эпидемии сердечных заболеваний, слабоумия и рака. Риск заболевания раком на 93% больше, чем у тех, кто пьет воду нехлорированную. Вывод один: воду из-под крана ни в коем случае пить нельзя. Экологическое значение воды – проблема №1 в мире, так как не будет воды – не будет жизни на Земле. Поэтому непременным условием сохранения здоровья является ее очистка и соответствие санитарно-эпидемиологическим нормам.
Водное отравление намного страшнее пищевого, потому как вода в жизни человека, в отличие от пищи, принимает участие во всех биохимических процессах организма. Диоксины, накапливаемые в организме, разлагаются очень медленно, практически десятки лет. Вызывая нарушения эндокринной системы, репродуктивных функций, они разрушают иммунитет, обуславливают раковые заболевания и генетические аномалии. Хлор является самым опасным убийцей современности: убивая одну болезнь, он порождает другую, еще страшнее. После того как в 1944 году началось глобальное хлорирование воды, стали массово проявляться эпидемии сердечных заболеваний, слабоумия и рака. Риск заболевания раком на 93% больше, чем у тех, кто пьет воду нехлорированную. Вывод один: воду из-под крана ни в коем случае пить нельзя. Экологическое значение воды – проблема №1 в мире, так как не будет воды – не будет жизни на Земле. Поэтому непременным условием сохранения здоровья является ее очистка и соответствие санитарно-эпидемиологическим нормам.
www.syl.ru
Роль свойств воды в биологических процессах и явлениях.
| Свойства воды. | Значение |
| Высокая теплоемкость и скрытая теплота парообразования | Поддержание теплового баланса растений |
| Высокое поверхностное натяжение | Определяет передвижение воды по капиллярам |
| Высокая растворяющая способность | Важна для корневого питания растений, передвижения продуктов фотосинтеза, транспорта 02 и СО2 |
| Структурированность, обусловленная водородными связями | Обусловливает аномальные свойства воды, делает воду структурным компонентом цитоплазмы, играет роль в процессах анестезии |
| Взаимодействие с биополимерами | Влияет на конформацию биополимеров и активность ферментов, определяет степень устойчивости растения к неблагоприятным условиям |
| Диссоциация на высокоактивные фотоионы | Участвует в химических реакциях (синтез, дыхание, гидролиз) |
| Поглощает инфракрасную радиацию, сравнительно прозрачна для видимой части спектра | Обеспечивает способность водных растений поглощать фотосинтетически активную радиацию (ФАР), прозрачные клетки эпидермиса наземных растений пропускают ФАР к мезофиллу и в какой-то мере предотвращают его перегрев |
Состояние и роль воды в растении. Для функционирования живых организмов важна не только их общая оводненность, но и состояние, в котором находится содержащаяся в них вода (ее концентрация, энергетический уровень, подвижность, реакционная способность и т. д.)
Состояние воды характеризуется её структурой, соотношением свободной (с неизменными физико-химическими свойствами) и связанной (с измененными физико-химическими свойствами вследствие взаимодействия с неводными компонентами) воды. Ведь вода не может сохранять в неизменном виде все свои свойства, находясь в такой сложнейшей гетерогенной среде, как клетка, где неизбежны самые разнообразные взаимодействия с ионами, молекулами других веществ, где действуют векторные факторы внутриклеточных полей, вдоль силовых линий которых могут ориентироваться диполи воды.
Вода в биологических объектах существует в таких условиях, которые пока невозможно корректно и полностью воспроизвести вне клетки.
С введением физических методов исследования - ядерного магнитного резонанса (ЯМР), электронного парамагнитного резонанса (ЭПР), диэлектрической спектроскопии (ДС), инфракрасной спектроскопии (ИКС) - появилась возможность характеризовать состояние воды подвижностью ее молекул (трансляционной, вращательно-колебательной), энергией и числом водородных связей. Для лучшего представления рассмотрим разные уровни изменения состояния воды в клетке.
Влияние ионов на состояние воды. При взаимодействии ионов с молекулами воды происходит ориентация диполей воды в электрическом поле иона. Исследованиями 0.Я.Самойлова (1957) было показано, что одни ионы понижают трансляционное движение воды, другие, наоборот, его усиливают. В первом случае говорят о положительной гидратации, во втором - об отрицательной. Положительную гидратацию вызывают ионы Mg2+, Ca2+, Li+, Na+, SO42-, отрицательную- ионы K+, Cs+, Nh5+, Cl-, I-, NO3-. Катионы взаимодействуют с отрицательно заряженными атомами кислорода молекул воды, тогда как анионы - с положительными зарядами диполя воды. Электрические взаимодействия между ионами и молекулами воды экранируют локальные электрические поля, образуемые ионами, и позволяют им оставаться в растворе. Воду, связанную ионами и низкомолекулярными соединениями, называют осмотически связанной.
Уровень макромолекул. Взаимодействие высокополимерных веществ с водой включает следующие способы:
гидратацию ионизированных и полярных групп;
стабилизацию структуры воды около неполярных групп («гидрофобная гидратация) иммобилизацию воды.
Гидратация ионизированных (-Nh4+, -СОО-) и гетерополярных групп (-СООН, -ОН, -СОН, > С = О, > NH, -Nh3, -CONh3, -SH) состоит в электростатическом притяжении молекул воды. Между этими двумя видами гидратации существуют только количественные различия. Степень гидратации зависит от количества этих групп на поверхности макромолекул, характера их расположения и соответствия структуре воды. Этим определяется связь степени гидратации с конформационными изменениями макромолекул. Гидратная вода располагается около гидрофильных радикалов в виде сферы, состоящей из нескольких слоев молекул.
В основе полимолекулярной гидратации лежит кооперативный характер образования водородных связей. Определенная ориентация монослоя молекул воды около полярных групп макромолекул создает благоприятные условия для возникновения других водородных связей с соседними молекулами воды, вследствие чего ее структура упрочняется в более широкой области. Данные ЯМР и ЭПР показывают, что существуют 2-3 слоя воды с ограниченной подвижностью около поверхности макромолекулы, помимо воды, непосредственно взаимодействующей с полярными группами. Различают две категории связанной воды: невращательно связанная - монослой гидратной оболочки, где подвижность молекул по сравнению с чистой водой снижена на 3-4 порядка; менее прочно связанная вода двух следующих слоев молекул, где подвижность воды снижена на 2 порядка. Для сравнения отметим, что у льда подвижность воды снижена на 6 порядков.
Количество гидратной воды у белков составляет около 0,3 г на 1 г белка. В пересчете на молярные соотношения эта величина означает, что одной молекулой белка связывается 850-1000 молекул воды, т. е. в среднем менее 1 моль на аминокислотный остаток. На гидратацию высокополимерных веществ большое влияние оказывает рН среды, который предопределяет количество ионизированных групп. В изоэлектрической точке степень гидратации будет наименьшей. Отнятие у белков связанной воды сопровождается изменениями третичной структуры макромолекул, определяющей индивидуальность и функционирование белка. Более чувствительны к дегидратации белки с высокоразвитой третичной структурой, т. е. ферменты и другие активные белки мембран.
Взаимодействие гидрофобных групп белка, например остатков аланина (-СН3), валина (-С3Н7), фенилаланина (-С7Н7), сопровождается ослаблением их взаимодействия с водой. Молекулы воды как бы выталкиваются из той сферы, в которой возникает сближение неполярных частей полипептидных цепочек, что также стабилизирует структуру воды и называется гидрофобной гидратацией.
Особое положение занимает иммобилизованная макромолекулами вода. Иммобилизация представляет собой механический захват воды при конформационных изменениях макромолекул или их комплексов. При этом вода оказывается заключенной в замкнутом пространстве внутри макромолекулы или между макромолекулами. Количество иммобилизованной воды не поддается точному учету. Считается, что белки могут иммобилизовать воды в 30 раз больше, чем весят сами.
Уровень мембран. Возможности взаимодействия воды с неводными компонентами расширяются при переходе к более сложным структурам. Мембраны содержат 25-30 % воды, причем она связана не только с белками, но и с полярными частями липоидов. Не вызывает сомнения структурообразующая роль воды в формировании мембран, так как строго ориентированные липоидные мицеллы образуются только в ее присутствии в результате гидрофобных взаимодействий неполярных частей молекул. Существует модель строения мембраны, где поверхностный слой представлен структурированной водой (См. рисунок! 70). При обезвоживании происходят изменение структуры мембраны, закрывание гидрофильных пор и снижение проницаемости.
Клеточный уровень. Все сказанное ранее относится и к клетке в целом. В зрелой растительной клетке можно выделить три основных компартмента, различающихся по состоянию воды: клеточные стенки, протоплазма, вакуоль.
Клеточные стенки составляют около 13 %, объем воды в них примерно 10 % объема ткани. Состояние воды в клеточных стенках неодинаковое. Примерно 1/3 часть ее гидратирует вещества и имеет сниженную подвижность, 2/3 представляет воду с такой же подвижностью молекул, как у обычной воды. Это наиболее лабильная, легко обмениваемая вода клетки.
Протоплазма занимает около 10 % объема клетки, оводненность органелл составляет 65 %, гиалоплазмы -95 -98 %. На долю протопласта приходится около 8 % внутриклеточной воды. Это в основном коллоидно-связанная вода. Причем в ядре содержится 20-30 %, в хлоропластах - 14-20, в митохондриях - 5-7 % воды протоплазмы. Автономность водообмена органелл клетки давно является установленным фактом. Убедительно показаны набухание митохондрий при нарушении окислительного фосфорилирования, при снижении оводненности клеток узлов кущения озимых во время второй фазы закаливания, набухание хлоропластов при обезвоживании клеток листа.
Клеточный сок вакуолей занимает 80-90 % объема клетки и содержит осмотически связанную воду.
Оставшуюся в клетках после воздействия гипертонического раствора воду нельзя считать «связанной» в точном физическом смысле, т. е. водой, взаимодействующей с неводными компонентами и вследствие этого имеющей пониженную подвижность молекул, так как часть её удерживается мембранами. Тем не менее водоудерживающую способность можно использовать как физиологическую характеристику подвижности воды: ее способность выходить за пределы определенных, разграниченных мембранами компартментов, участвовать в физиолого-биохимических процессах за пределами этого пространства.
Обширный экспериментальный материал, накопленный к настоящему временя, свидетельствует о тесной связи между интенсивностью и направленностью физиологических процессов и оводненностью растительных тканей. Убедительно показана зависимость активности ферментов дыхания, фотосинтеза, азотного и фосфорного обмена от содержания и состояния воды. С оводненностью тканей также связана устойчивость растений к различным неблагоприятным факторам: морозу, жаре, засухе, засолению и т.д. А. М. Алексеев (1969) ввел понятие о протоплазме как целостной системе, структура которой определяется взаимодействием находящихся в ней воды и белков. Эти компоненты протоплазмы взаимосвязаны и взаимообусловлены, так что нарушение одного из них вызывает нарушение структуры всей системы. Гидратная вода влияет на активность белков-ферментов, состояние мембран, их устойчивость.
Несмотря на важную роль связанной воды, количество ее не так велико. Согласно современным данным гидратная вода составляет 0,13-0,55 г/г сухого вещества, что не превышает 10-15 % водного запаса листа.
Уровень целостного растения. Вода в растении существует и форме
конституционной (химически связанной),
гидратационной,
резервной, заполняющей водосборные полости в вакуолях и др. клеточных компартментах,
интерстициальной, которая выполняет транспортные функции в апопласте и проводящих путях.
Роль воды в растительном организме заключается в следующем:
Вода - структурообразователь протоплазмы. Макромолекулы белков, нуклеиновых кислот, мембраны могут сохранять свою структуру и функциональную активность только при наличии водородных связей с водным матриксом. При повышении температуры водородные связи рвутся и стабилизирующее действие воды на структуру протоплазмы снижается. Поэтому жизнь может существовать в относительно таких пределах температур.
Вода - растворитель разнообразных веществ, обеспечивает транспорт минеральных, органических веществ и газов (СО2 , О2) по растению.
Вода - активный участник биохимических превращений, принимает участие в фотосинтезе, дыхании, гидролитических процессах.
Вода способствует стабилизации температуры растений.
Поддерживает тургесцентное состояние растении, что обеспечивает сохранение формы травянистых растений, определенную ориентацию органов в пространстве.
Обеспечивает связь органов друг с другом. Пронизывая все ткани растения, вода создает в нем непрерывною фазу и осуществляет координацию деятельности органов в целостном растении.
studfiles.net
Биологическое значение воды, её физические свойства
Вода является основным компонентом большинства растительных клеток и тканей. Содержание воды в клетках варьирует в зависимости от типа клеток и физиологических условий. Например, в корне моркови содержится около 85 % воды, тогда как молодые листья салата на 95 % состоят из воды.
В некоторых сухих семенах и спорах содержание воды составляет всего лишь 10 %; однако, для того чтобы они стали метаболически активными, содержание воды в них должно существенно увеличиться.
Вода является средой, в которой происходит диффузия растворенных соединений по клеткам растения; представляет собой вещество, необычайно удобное для регуляции температуры; служит растворителем необходимым для протекания многих биохимических реакций; наконец, вода довольно мало сжимаема при давлениях, существующих в организме, что подчеркивает ее роль в поддержании структуры растения.
Минеральные вещества, необходимые для роста, и органические соединения, синтезируемые в ходе фотосинтеза – все они транспортируются по растению в виде водных растворов. У активно растущих растений существует непрерывный водный поток из почвы через тело растения к листьям, где вода испаряется в основном через устьица.
Вода представляет собой один из необходимых метаболитов, т.е. непосредственно участвует в метаболизме. Она служит источником кислорода, выделяемого в ходе фотосинтеза, и водорода, используемого для восстановления углекислого газа. При образовании АТФ – важного макроэргического соединения – из АДФ и фосфата происходит отщепление воды, иными словами, подобное фосфорилирование есть не что иное, как процесс дегидратации, происходящий в водном растворе в биологических условиях; вода участвует в реакциях гидролиза. Таким образом, знание уникальных свойств воды имеет громадное значение для общего понимания физиологии растений.
Если оба атома водорода заменить на атомы дейтерия (2Н), то мы получим тяжелую воду, или окись дейтерия с молекулярной массой 20.
В воду можно также ввести атом трития (3Н), который радиоактивен и имеет период полураспада 12,4 г. Такая вода оказалась полезным инструментом в изучении скорости ее диффузии в тканях растений. Возможно пометить воду замещая обычный изотоп воды 16О на тяжелый изотоп 18О. Этот тип метки был использован для доказательства того, что кислород, выделяемый в ходе фотосинтеза, происходит из воды, а не из углекислого газа.
Физические свойства воды
Без воды жизнь на нашей планете не могла бы существовать. Вода не только необходимый компонент живых клеток, но для многих еще и среда обитания.
Важное свойство воды – ее полная прозрачность для лучей видимой части спектра, что позволяет солнечным лучам достигать хлоропластов, находящихся в клетках листьев, а также растений погруженных в толщу воды.
Свойства воды необычны и связаны главным образом с малыми размерами молекул, с полярностью и со способностью последних соединяться друг с другом водородными связями. Под полярностью подразумевают неравномерное распределение зарядов в молекуле. У воды один конец молекулы несет небольшой положительный заряд, а другой – отрицательный. Такую молекулу называют диполем.
Сильные взаимодействия между молекулами воды обусловлены структурой молекул этого соединения. Расстояние между ядром кислорода и ядрами одного из двух атомов водорода равно примерно 0,099 нм, а угол между связями Н-О-Н равен примерно 105о. Атом кислорода обладает сильной электроотрицательностью и стремиться оттянуть электроны от атомов водорода. Благодаря этому на атоме кислорода возникает частично отрицательный заряд (d –) в то время как два атома водорода приобретают положительный заряд (d+). Несущие положительный заряд атомы водорода испытывают электростатическое притяжение со стороны отрицательно заряженных атомов кислорода соседних молекул воды (рис. 4.1).
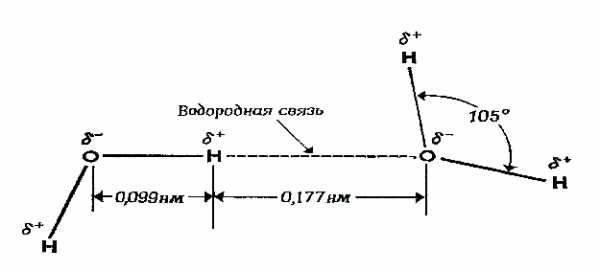
Рис. 4.1. Водородная связь между двумя полярными молекулами воды: δ+ –очень маленький положительный заряд; δ – – очень маленький отрицательный заряд
Это приводит к возникновению водородных связей между молекулами воды, энергия которых составляет около 4,8 ккал/моль.
В результате такого связывания молекул воды друг с другом возникает большая упорядоченность в водных растворах. Действительно, на отдельных участках жидкая вода приобретает почти кристаллическую структуру, что чрезвычайно важно, поскольку может играть определенную роль во взаимодействиях и ориентации молекул в водных растворах.
Учитывая данную особенность воды, мы можем теперь перейти к рассмотрению других физико-химических свойств, важных с биологической точки зрения.
Вода обладает большой теплоемкостью. Удельной теплоемкостью воды называют количество теплоты, которое необходимо, чтобы поднять температуру 1 кг воды на 1о С. Большая теплоемкость означает, что существенное увеличение тепловой энергии вызывает лишь сравнительно небольшое повышение ее температуры. Объясняется это тем, что значительная часть энергии расходуется на разрыв водородных связей, ограничивающих подвижность молекул воды.
Большая теплоемкость воды сводит к минимуму происходящие в ней температурные изменения. Благодаря этому биохимические процессы протекают в меньшем интервале температур, с более постоянной скоростью и опасность нарушения этих процессов от резких отклонений температур грозит им столь сильно. Это очень важно, поскольку вода служит для многих клеток и организмов средой обитания и в этом случае необходимо сохранение постоянства условий произрастания.
Испарение воды требует довольно значительных количеств энергии. Это опять таки объясняется наличием водородных связей. Именно в силу этого температура кипения воды – вещества со столь малыми молекулами – необычайно высока.
Энергия, необходимая молекулам воды для испарения черпается из их окружения. Таким образом, испарение сопровождается охлаждением. Потери тепла при испарении воды являются одним из основных приемов регуляции температуры у наземных растений.
Как известно, вода при температуре 0 оС и ниже переходит в твердое состояние – образуется лед. При этом выделяется значительное количество энергии. Это уменьшает вероятность замерзания содержащей клетками жидкости. С другой стороны, для плавления (таяния) льда необходимо сравнительно большое количество энергии (скрытая теплота плавления есть мера тепловой энергии, необходимая для расплавления твердого вещества). Кристаллики льда весьма пагубны для живых систем, если они образуются внутри клетки.
Плотность воды от +4 до 0 оС понижается, поэтому лед легче воды и в воде не тонет. Вода – единственное вещество, обладающее в жидком состоянии большей плотностью, чем в твердом.
Поскольку лед плавает в воде, он образуется при замерзании сначала на ее поверхности и лишь под конец в придонных слоях. Если бы замерзание шло в обратном порядке, то жизнь в пресноводных водоемах вообще не могла бы существовать.
Еще одной важной физической характеристикой воды является необычайно высокая диэлектрическая проницаемость (D), что является следствием молекулярной структуры. Высокая диэлектрическая проницаемость воды делает электрические силы между растворенными в ней заряженными веществами относительно слабыми.
Диэлектрическая проницаемость воды равна 80,2 при 20 оС и 78,4 при 25 оС. Для неполярной жидкости – гексана D = 1,87. Следовательно, электрическое притяжение для таких ионов, как Na+ и Cl –, в гексане больше (80,2/1,7) в 43 раза, чем в воде. Значительно более сильное притяжение в гексане, чем в воде, уменьшает степень ионизации NaCl по сравнению с диссоциацией этой соли в водном растворе, т. е. вода является хорошим растворителем для заряженных частиц.
Из всех жидкостей самое большое поверхностное натяжение у воды (поверхностное натяжение – результат действующих между молекулами сил на поверхности раздела фаз).
Притяжение между молекулами воды, наблюдаемое в жидкой фазе, обычна называют когезией, и притяжение между жидкой водой и твердой фазой, например стенками тонкой трубочки или капилляра – адгезией. Когда взаимодействие вода – стенка оказывается значительным, говорят, что стенки смачиваются. Напротив, когда межмолекулярные когезионные силы внутри жидкости значительно больше, чем адгезия между жидкостью и материалом стенки, верхний уровень жидкости в капилляре оказывается ниже уровня поверхности свободного раствора. Такое понижение уровня характерно для жидкой ртути в стеклянном капилляре. В случае воды в стеклянных капиллярах или в сосудах ксилемы притяжение между молекулами воды и стенками велико и поэтому жидкость поднимается.
Капиллярное поднятие имеет важное значение для физиологии водообмена растений. Тем не менее, количественные характеристики этого процесса показали, что для поднятия воды до вершины дерева высотой 30 м за счет капиллярной силы, сосуды должны иметь радиус 0,5 · 10-4 см. Эти размеры значительно меньше, чем в действительности. Более того, элементы проводящей системы не соприкасаются с воздушной средой своим верхним концом, и поэтому сосуды ксилемы не подобны капилляру.
Большое количество пор в стенках сосудов ксилемы образуют сетку маленьких извилистых капилляров, которые не только способствуют поднятию воды, но и способствуют поддержанию воды в просветах сосуда. Следовательно, клеточная стенка могла бы действовать как эффективный фитиль, поднимая воду за счет множества пор, хотя фактическая скорость такого движения вверх далеко недостаточна для восполнения воды, которая теряется в процессе испарения.
Значительные величины когезии и адгезии, характерные для молекул воды, играют важную роль в живых клетках, а также, при движении воды по сосудам ксилемы.
Как мы уже отметили в разделе физико-химические свойства протоплазмы, вода в клетке находится в двух состояниях: свободной и связанной (4,5 % от всей воды), причем последняя может быть нескольких видов. В вакуолях вода удерживается относительно низкомолекулярными соединениями (осмотически связанная) и большая часть воды находиться в свободном состоянии. В клеточной стенке часть молекул воды находиться в адсорбированном состоянии на поверхности фибрилл клеточной стенки. Вода тут связывается, главным образом, целлюлозой, гемицеллюлозой, пектиновыми веществами, т. е. коллоидно-связанная вода. Кроме того, в клеточной стенке есть свободная вода (в порах). В цитоплазме имеется свободная, коллоидно- и осмотически связанная вода. Вода, которая находится на расстоянии 1 нм от поверхности белковой молекулы связана сильно. Осмотически связанная вода цитоплазмы – это вода связанная с ионами.
Физиологическое значение свободной и связанной воды разное. С одной стороны, интенсивность физиологических процессов зависит в первую очередь от содержания свободной воды. С другой стороны, наблюдается положительная корреляция между содержанием связанной воды и устойчивостью клеток к неблагоприятным факторам.
На уровне целого растения выделяют конституционную воду(химически связанная), гидрационную, резервную, заполняющую водосборные полости (вакуоли и др. клеточные компартменты) и интерстициальную, которая выполняет транспортные функции в апопласте и проводящих путях.
Одним из главных факторов естественного отбора, влияющих на видообразование, является недостаток воды. С этим фактором связано распространение некоторых растений, имеющих подвижные гаметы. Все наземные растения приспособлены к тому, чтобы добывать и сберегать воду; в крайних своих проявлениях – у ксерофитов – такого рода приспособления представляются подлинным чудом «изобретательности» природы.
Вкратце важные биологические функции воды можно свести к следующим (табл. 1.4).
Таблица 4.1. Биологические функции воды
|
Для всех организмов |
Для растений |
|
Обеспечивает поддержание структуры (высокое содержание
воды в протоплазме). Служит растворителем и средой для диффузии. Участвуют в реакциях гидролиза. Служит средой, в которой происходит оплодотворение. Обеспечивает распространение семян, гамет и т. д. |
Обуславливает осмос и тургесцентность (от которых зависит: рост, поддержание структуры, движения устьиц и т. п.). Обеспечивает транспирацию, а также транспорт неорганических ионов и органических молекул. Обеспечивает прорастание семян – набухание, разрыв семенной кожуры и дальнейшее развитие. |
biofile.ru
Биологические свойства воды - Свойства воды - Статьи о воде - структура воды, память воды, свойства воды
Вода как растворитель Вода - превосходный растворитель для полярных веществ. К ним относятся ионные соединения, такие как соли, у которых заряженные частицы (ионы) диссоцииируют в воде, когда вещество растворяется, а также некоторые неионные соединения, например сахара и простые спирты, в молекуле которых присутствуют заряженные (полярные) группы (-OH).Гидратация ионов в водеРезультаты многочисленных исследований строения растворов электролитов свидетельствуют, что при гидратации ионов в водных растворах основную роль играет ближняя гидратация - взаимодействие ионов с ближайшими к ним молекулами воды. Большой интерес представляет выяснение индивидуальных характеристик ближней гидратации различных ионов, как степени связывания молекул воды в гидратных оболочках, так и степени искажения в этих оболочках тетраэдрической льдоподобной структуры чистой воды - связи в молекуле изменяются на неполный угол. Величина угла зависит от иона.
Что происходит с растворенными в воде веществами?Когда вещество растворяется, его молекулы или ионы получают возможность двигаться более свободно и, соответственно, его реакционная способность возрастает. По этой причине в клетке большая часть химических реакций протекает в водных растворах. Неполярные вещества, например липиды, не смешиваются с водой и потому могут разделять водные растворы на отдельные компартаменты, подобно тому, как их разделяют мембраны. Неполярные части молекул отталкиваются водой и в её присутствии притягиваются друг к другу, как это бывает, например, когда капельки масла сливаются в более крупные капли; иначе говоря, неполярные молекулы гидрофобны. Подобные гидрофобные взаимодействия играют важную роль в обеспечении стабильности мембран, а также многих белковых молекул, нуклеиновых кислот и других субклеточных структур.
Вода - транспортПрисущие воде свойства растворителя означают также, что вода служит средой для транспорта различных веществ. Эту роль она выполняет в крови, в лимфатической и экскреторных системах, в пищеварительном тракте и во флоэме и ксилеме растений.
Теплоемкость водыБольшая теплоёмкость. Удельной теплоёмкостью воды называют количество теплоты в джоулях, которое необходимо, чтобы поднять температуру 1 кг воды на 1° C. Вода обладает большой теплоёмкостью (4,184 Дж/г). Это значит, что существенное увеличение тепловой энергии вызывает лишь сравнительно небольшое повышение её температуры. Объясняется такое явление тем, что значительная часть этой энергии расходуется на разрыв водородных связей, ограничивающих подвижность молекул воды.
Большая теплоёмкость воды сводит к минимуму происходящие в ней температурные изменения. Благодаря этому биохимические процессы протекают в меньшем интервале температур, с более постоянной скоростью и опасность нарушения этих процессов от резких отклонений температуры грозит им не столь сильно. Вода служит для многих клеток и организмов средой обитания, для которой характерно довольно значительное постоянство условий.
Теплота испарения водыБольшая теплота испарения. Скрытая теплота испарения есть мера количества тепловой энергии, которую необходимо сообщить жидкости для её перехода в пар, то есть для преодоления сил молекулярного сцепления в жидкости. Испарение воды требует довольно значительных количеств энергии (2494 Дж/г). Это объясняется существованием водородных связей между молекулами воды. Именно в силу этого температура кипения воды - вещества со столь малыми молекулами - необычно высока.
Энергия, необходимая молекулам воды для испарения, черпается из их окружения. Таким образом, испарение сопровождается охлаждением. Это явление используется у животных при потоотделении, при тепловой одышке у млекопитающих или у некоторых рептилий (например, у крокодилов), которые на солнцепёке сидят с открытым ртом; возможно, оно играет заметную роль и в охлаждении транспирирующих листьев.
Теплота плавления водыБольшая теплота плавления. Скрытая теплота плавления есть мера тепловой энергии, необходимой для расплавления твёрдого вещества (льда). Воде для плавления (таяния) необходимо сравнительно большое количество энергии. Справедливо и обратное: при замерзании вода должна отдать большое количество тепловой энергии. Это уменьшает вероятность замерзания содержимого клеток и окружающей их жидкости. Кристаллы льда особенно губительны для живого, когда они образуются внутри клеток.
Плотность водыПлотность и поведение воды вблизи точки замерзания. Плотность воды (максимальна при +4° С) от +4 до 0° С понижается, поэтому лёд легче воды и в воде не тонет. Вода - единственное вещество, обладающее в жидком состоянии большей плотностью, чем в твёрдом, так как структура льда более рыхлая, чем структура жидкой воды. Это - одно из аномальных свойств воды.
Поскольку лёд плавает в воде, он образуется при замерзании сначала на её поверхности и лишь под конец в придонных слоях. Если бы замерзание прудов шло в обратном порядке, снизу вверх, то в областях с умеренным или холодным климатом жизнь в пресноводных водоёмах вообще не могла бы существовать. То обстоятельство, что слои воды, температура которых упала ниже 4° С, поднимаются вверх, обусловливает перемешивание воды в больших водоёмах. Вместе с водой циркулируют и находящиеся в ней питательные вещества, благодаря чему водоёмы заселяются живыми организмами на большую глубину.
После проведения ряда экспериментов было установлено, что связанная вода при температуре ниже точки замерзания не переходит в кристаллическую решётку льда. Это энергетически невыгодно, так как вода достаточно прочно связана с гидрофильными участками растворённых молекул. Это находит применение в криомедицине.
Поверхностное натяжение воды и когезияБольшое поверхностное натяжение и когезия. Когезия - это сцепление молекул физического тела друг с другом под действием сил притяжения. На поверхности жидкости существует поверхностное натяжение - результат действующих между молекулами сил когезии, направленных внутрь. Благодаря поверхностному натяжению жидкость стремится принять такую форму, чтобы площадь её поверхности была минимальной (в идеале - форму шара). Из всех жидкостей самое большое поверхностное натяжение у воды (7,6 · 10-4 Н/м). Значительная когезия, характерная для молекул воды, играет важную роль в живых клетках, а также при движении воды по сосудам ксилемы в растениях. Многие мелкие организмы извлекают для себя пользу из поверхностного натяжения: оно позволяет им удерживаться на воде или скользить по её поверхности.
Вода как реагент Биологическое значение воды определяется и тем, что она представляет собой один из необходимых метаболитов, то есть участвует в метаболических реакциях. Вода используется, например, в качестве источника водорода в процессе фотосинтеза, а также участвует в реакциях гидролиза.
alka-mine.at.ua