Окисляемость или Редокс-потенциал. Вода редокс
Редокс потенциал воды и дезинфекция озоном
Окислительно-восстановительный или редокс потенциал (ORP) отражает количество окислителя в воде. Отметим, что он не является мерой концентрации самого окислителя, однако используется как надежный и универсальный показатель окислительного потенциала воды в точке измерения. Окислителями выступают кислород, хлор, перекиси, озон и другие вещества.
Единицей измерения редокс потенциала являются милливольты. Полный диапазон измерений составляет от -2000 до +2000 мВ. Большинство ORP-метров работают в диапазоне от -1200 до +1200 мВ, и этого достаточно в области обработки воды. Значения выше 0 мВ свидетельствуют о доступной энергии для окисления молекулы или связывания её с атомом кислорода.
В природе редокс потенциал является мерой того, насколько озеро и реки способны самоочищаться и расщеплять различные продукты, загрязнения и омертвевшие части растений и животных. Когда значения потенциала высокие, в воде избыток кислорода. Это означает, что аэробные бактерии, перерабатывающие мертвые ткани и загрязнения, работают более эффективно. В общем, более высокие значения потенциала свидетельствуют о здоровом состоянии водоемов. Однако, даже благополучные озера и реки около дна и донных отложений имеют более низкие концентрации кислорода и, соответственно, значения ORP. Это связано с большим количеством бактерий, которые напряженно разлагают органику и потребляют много кислорода. Фактически, кислород быстро исчезает в грязи на дне (часто на глубине 1-2 см), и ORP также падает. Регистрация окислительно-восстановительного потенциала, помимо измерения концентрации растворенного кислорода, дает более полную информацию о качестве воды и степени загрязнения. Кроме того, существуют другие элементы, которые подобно кислороду, вносят вклад в повышение ORP.
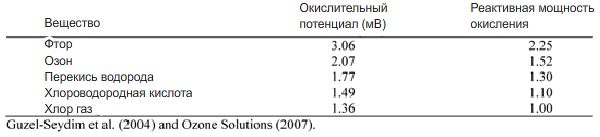 Окислительный потенциал ряда веществ
Окислительный потенциал ряда веществБиологическое значение редокс потенциала воды
Окислительно-восстановительный потенциал природных водоемов, в значительной степени, зависит от концентрации растворенного в воде кислорода, а также количества других элементов, функционально схожих с кислородом. Говоря проще, кислород и другие элементы, повышающие ORP, помогают утилизировать нежелательные загрязнения и органику в воде. Когда окислительно-восстановительный потенциал низкий, концентрация кислорода низкая, возрастает токсичность определенных металлов и загрязнений, и большинство омертвевшей, гниющей материи нельзя переработать. Очевидно, загрязненная среда вредна для рыб и насекомых. В благополучной среде значение ORP находится в диапазоне 300-500 мВ.
Озон как средство дезинфекции
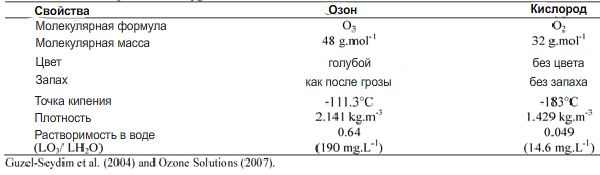 Свойства кислорода и озона. Сравнительная таблица
Свойства кислорода и озона. Сравнительная таблицаОзон в воде реагирует с загрязнением и микроорганизмами, либо переходит обратно в кислород. Если озон встречает микроорганизм прежде, чем окисляет загрязнение, он убивает патоген и, соответственно, выступает дезинфектором. С другими химическими веществами, например, хлором, ситуация сложнее и менее предсказуема. Эти химикаты реагируют с микроорганизмами гораздо медленнее озона и чаще окисляют загрязнения. Кроме того, на эффективность многих окисляющих агентов влияет pH среды.
 Свойства хлора и озона. Сравнение в области дезинфекции
Свойства хлора и озона. Сравнение в области дезинфекции
Использование хлора для дезинфекции зависит от pH среды. Традиционные системы мониторинга измеряют потенциал в частях на миллион с использованием титрования или тест-полосок. Однако эти методы нужно совмещать с измерением pH и концентрации хлорноватистой кислоты (HClO). Значение pH важная переменная, потому что тестовые полоски в равной степени определяют кислоту HClO и ионы (OCl-). При pH 7.5 соотношение недиссоциированной кислоты HClO и ионов (OCl-) эквивалентно (50:50). Снижение pH приводит к возрастанию HClO и редокс потенциала, что свидетельствует об окислительном потенциале. Недавние исследования в коммерческих и модельных водных системах «после сбора урожая» показал, что если необходимо, ORP критерий может использоваться для определения потенциала уничтожения бактерий. Иными словами, среда ORP 700 мВ при pH 6.5 имеет такой же потенциал дезинфекции, что и среда ORP 700 мВ при pH 8.5. Хотя для достижения такого же значения ORP при pH 8.5 требуется гораздо больше гипохлорита. Это связано с тем, что доля хлорноватистой кислоты (HClO) составляет всего 15% от общего свободного хлора. Измерения свободного хлора (частей на миллион) при двух данных значениях pH (при постоянной концентрации гипохлорита) покажут одинаковые результаты, что дает ошибочное представление о высоком потенциале дезинфекции при pH 8.5.
Когда в воде присутствуют окисляющие агенты (ORP положительный), при достаточном времени и области контакта, они реагируют с какими-либо веществами или распадаются. Конечно, более высокая концентрация этих агентов приводит к более активному окислению и эффективной дезинфекции. Прогнозирование результата дезинфекции зависит от равномерного перемешивания воды и температуры, потому что в теплой среде молекулы взаимодействуют быстрее. Существуют и другие факторы, такие как тип окислителя, течение, световой режим и т.д..
Преимуществом озона является переход его в форму свободного радикала и кислород. Этот свободный радикал обладает потрясающим потенциалом дезинфекции. Распад озона на кислород и радикал ускоряется при посредничестве энергии УФ-излучения, либо добавлением перекиси водорода в раствор.
В муниципальных водах редокс потенциал составляет 200-300 мВ. Эта вода подверглась дезинфекции, но её потенциал дезинфекции невысок. Значение 650 мВ воды в очистных сооружениях свидетельствует о том, что любой окисляемый объект будет уничтожен. Задачей дезинфекции является достижение точки реакции, когда обработанная вода безопасна для потребления растениями, человеком и животными.
Большинство коммерческих моделей генерируют озон под воздействием коронного разряда или ультрафиолета. В первом случае коронный разряд порождает высокоэнергетическое поле между двумя металлическими пластинами, через которое проходит сухой воздух, при этом образуется озон. Ультрафиолетовое излучение (140-190 нм) используется для распада молекул кислорода и образования озона. Излучение дешевле коронного разряда, но менее эффективный.
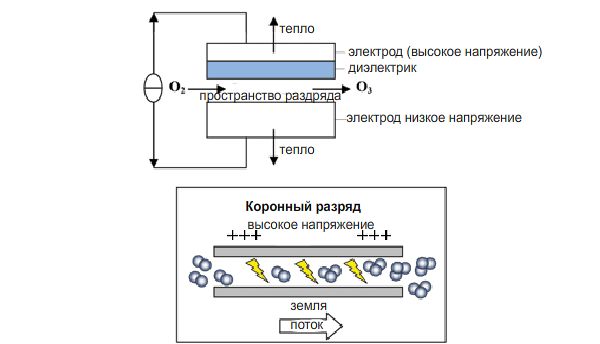 Генератор озона с коронным разрядом
Генератор озона с коронным разрядом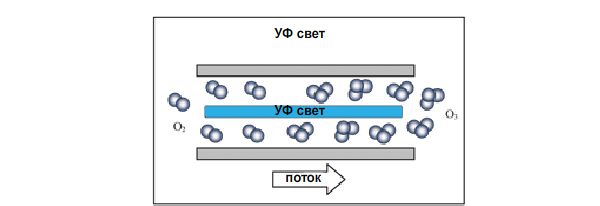 Генератор озона с УФ-излучателем
Генератор озона с УФ-излучателемКонструкция реактора и контактной камеры озонатора очень важно для успеха дезинфекции. Тип реакторов разнообразен, например, распылитель пузырьков, турбинная контактная камера, инъектор, глубокие u-трубчатые реакторы, статические смесители камеры с распылителем.
Важны эффективность переноса озона, конструкция без утечки озона, стойкий к окислению материал озонатора.
Материалы должны инертны к этому газу. Долговременное использование некоторых пластиков, например, ПВХ и поликарбонатов, и гальванической стали не рекомендовано.
В качестве материала контактной камеры и труб подойдет нержавеющая сталь. Краны изготавливаются из нержавеющей стали с мембранами из тефлона.
Режимы обработки озонированием
Озон применяют непрерывно, сериями, одиночно. В большинстве случаев, выбор режима обусловлен стратегиями кормления в системе культивирования. От трех до четырех часов после кормления рыбы концентрация аммония, растворенных органических веществ достигает максимума. Если рыбу кормят несколько раз в день, после каждого кормления запускают озонирование. Если кормление ведется непрерывно, качество воды ухудшается непрерывно, и озон необходимо вводить непрерывно. Одиночное озонирование применяется для планового снижения загрязнений в системе, связанных с умеренным кормлением, либо для обработки вносимой в систему свежей воды.
Непрерывное введение озона предпочтительно, потому что качество воды остается стабильным.
Концентрация необходимого озона рассчитывается на основе норм кормления. Обычно с целью снижения органических загрязнений рекомендуют вносить 10-15 г газа на 1 кг корма.
С другой стороны, дезинфекция воды требует более высоких концентраций озона, с учетом её загрязнения органическими веществами. В грязной воде остаточная концентрация O3 — 0.01-0.1 мг/л в течение 15 секунд достаточна для эффективного снижения бактериальной нагрузки. Однако в среде с высокой органической нагрузкой остаточная концентрация и/или время контакта с газом должно возрастать. Для дезинфекции, сопровождаемой окислением органических веществ, естественных вод (морская, солоноватая и пресная) обычно требуется остаточной концентрации 0.1-0.2 мг/л и время контакта 1-5 минут.
Оптимальные дозы O3 для дезинфекции изменчивы и представляют совокупность его затрат на окисление органических веществ, коллоидных частиц, нитратов и саму дезинфекцию. Как правило, в условиях УЗВ стоимость озонирования для полной дезинфекции слишком высока. Тем не менее, некоторое снижение нагрузки патогенных организмов и улучшения качества воды достигают умеренным использованием озона.
Дезинфекция вносимой воды и стоков более целесообразна, чем обработка всей системы. Озонирование источника воды в совокупности с карантинными мероприятиями поступающего посадочного материала, существенно снижают риск возникновения инфекции.
Место приложения
Озон в остаточной концентрации 0.01-0.1 мг/л токсичен для большинства пресноводных и морских организмов. Точка его приложения должна выбираться аккуратно. Существует несколько мест УЗВ, где вводят озон:
— Место подачи кислорода. Традиционно озон вносят в систему оксигенатор, после биофильтра, но перед культуральным бассейном. Вследствие близости бассейна, этот метод создает умеренный риск отравления рыб остаточным озоном. Его снижают удержанием газа в течение нескольких минут в контактной камере. Преимуществами метода являются дезинфекция и снижение нитрита.
— Место перед биофильтром. Озон вводят перед биофильтром. Этот метод сравнительно безопасен для рыб. Любые остаточные концентрации газа вначале проходят через биофильтр и используются для окисления биопленок. Таким образом, фильтр становится эффективным буфером пред бассейнами с рыбой. Однако слишком высокая остаточная концентрация озона снизит скорость нитрификации. Преимуществом такого озонирования является повышение концентрации кислорода в биофильтре, что особенно актуально для погруженного неорошаемого биофильтра. В свою очередь, в орошаемом аппарате любые формы кислорода улетучиваются в атмосферу.
— Обработка поступающей воды. Для УЗВ, использующих поверхностные воды, эта мера обязательна.
— Обработка стоков. Проводится с целью охраны окружающей среды от инфекций и загрязнений. Более эффективно накапливать сточные воды в емкости и затем озонировать их.
Не рекомендуется:
— Обрабатывать воду до этапа грубой механической очистки. Это ведет к необоснованному расходу озона.
— Обрабатывать культуральные бассейны. Опасно для рыб.
Озонирование солоноватой и морской воды ведет к появлению побочных продуктов. Озон реагирует с хлором, бромом и образует стабильные окислы, токсичные для гидробионтов. Применение озонатора в морской системе обычно ограничивается обработкой в ваннах, обособленных от основного потока. Активированный уголь эффективно удаляет остаточный озон из морской воды.
Измерение концентрации озона в УЗВ
Обычно прямое измерение озона в воде проводят колориметрическим методом или спектрофотометрией. Однако эти методы слишком грубые для регистрации низких остаточных концентраций озона, летальных для рыб, и непригодны для непрерывного мониторинга. Традиционно для этих целей используют ORP-датчики. Они не измеряют напрямую уровень газа, а регистрируют общую способность раствора окислять электрод (мВ). Таким образом, можно контролировать уровень окислителей и, соответственно, косвенно контролировать уровень озона. Для пресноводной УЗВ безопасно значение редокс потенциала 300 мВ.
Многие озонаторы связаны с датчиками и автоматически прекращают подачу озона. Как только его уровень вышел за допустимые пределы. Стоит отметить, что ORP датчики делают измерения несколько минут, поэтому концентрацию озона можно контролировать приблизительно. Параллельно с измерением озона необходимо поводить мониторинг других параметров, особенно, нитрита.
Риски озонирования воды
Озон очень эффективный окислитель. Именно это создает большие риски для систем УЗВ:
— Снижение нитрита в ходе его окисления озоном и перехода в нитрат приводит к нехватке нитрита в биофильтре. Количество нитрифицирующих бактерий снижается. После прекращения подачи озона может наступить подъем уровня нитрита.
— Высокая остаточная концентрация озона создает риск рыбе, вызывает серьезные повреждения тканей и смертность.
— Высокая остаточная концентрация озона создает риск бактериальной пленке биофильтра. Нарушается функция фильтра, что ведет к повышению аммония и нитрита. Это отражается на рыбе, снижает темпы роста, ухудшает здоровье.
Рекомендуется устанавливать деозонаторы для удаления остаточного озона. Простейшая конструкция включает камеру, в которой задерживается вода и где улетучивается озон. В капельных фильтрах этот газ также активно улетучивается.
Для человека безопасна концентрация озона в воздухе 0.05-0.1 мг/л в течение 8 часов, 0.3 мг/л в течение 10 минут.
Электроды для регистрации редокс потенциала
ORP-электроды аналитические датчики для измерения окислительно-восстановительного потенциала. Они входят в состав ORP-метра.
Окислительно-восстановительные реакции являются типом химической реакции, когда электроны от одного атома переходят к другому. Окисленный атом теряет электроны, а восстановленный – приобретает. Редокс реакция сопровождается обменом электронов. Окисление связано с потерей электронов, поэтому раствор положительный. Восстановление сопровождается приобретением электронов, поэтому раствор имеет отрицательный заряд. Для протекания реакции должны присутствовать оба участника. Скорость реакции, происходящая на электроде ORP-метра, напрямую связана с плотностью тока обмена, производного от концентрации раствора, окислительно-восстановительной системы и электрода. Скорость снижается, когда редокс потенциал образца подобен редокс потенциалу на электроде ORP-метра. Кроме того, излишний ток обмена также является проблемой при проверке сильных окислителей и восстановителей. Последнее решается ополаскиванием электродов перед замерами.
ORP-метр нельзя использовать как непосредственный индикатор остаточного окислителя или восстановителя, потому что в системе наблюдаются флуктуации, вследствие влияния pH и температуры. Тем не менее, прибор можно привести в соответствие с измеряемой средой за счет регистрации потенциала в спокойном состоянии. Состояние покоя достигается замерами pH и другими тестами. Таким образом, можно добиться высокой степени корреляции показаний ORP-метра и состояния системы.
Когда измерительный электрод находится в контакте с окислителями или восстановителями, электроны непрерывно перемещаются навстречу или прочь от его поверхности, что порождает крошечное напряжение. Измерительный электрод сделан из платины, золота или графита. Электрод сравнения связан с солевым водным раствором, с заданным потенциалом полуэлемента – 0.0 мВ. Этот электрод сделан их хлорида серебра или растворенного хлорида ртути (каломельный электрод), которые обеспечивают стабильные и надежные показатели. ORP электроды регистрируют напряжение в цепи, состоящей из двух электродов. Это напряжение можно измерить интерфейсом милливольтметра или pH метра. Положительные значения указывают на присутствие окислителя, тогда как негативные значения — восстановителя.
Регистрация ORP должна проводиться в нескольких точках, а не фиксированной точке. В реальной системе датчики редко устанавливают в фиксированной точке. Различия значений у датчика, в зависимости от того, подвижен он или в стационарном положении, могут превышать 25 мВ, особенно, портативных приборов. Размер проверяемой поверхности также влияет на флуктуации считывания: лучшие датчики имеют большую зону считывания. Хорошей практикой является стандартизация измерений и установка порогов окна считывания, что обеспечит удовлетворительное снижение концентрации бактерий. Для портативных приборов рекомендуют погружать датчик в проточную воду на 30 секунд. Если вода имеет сильное течение, образец набирают в чистый стакан (предварительно дважды ополаскивают дистиллированной водой). Аккуратно в течение 30 секунд размешивают содержимое стакана датчиком, а затем измеряют 30 секунд.
——
www.dramm.com/media/DRAMMwater/Understanding%20ORP%20&%20Ozone.pdf
www.globalspec.com/learnmore/sensors_transducers_detectors/chemical_sensors/oxidation_reduction_potential_orp_electrodes
www.dpi.nsw.gov.au/fishing/aquaculture/publications/water-quality-management/ozone-in-recirculating-aquaculture-systems
aquavitro.org
Окисляемость или Редокс-потенциал аквариумной воды
Оба термина употребляются в равной степени и означают на сколько активно расходуется кислород биосистемой аквариума. Редокс-потенциал позволять оценить степень загрязнённости воды органическими отходами: экскременты, не съеденные остатки пищи и прочие продукты разложения. Чем выше показатель окисляемости, тем меньше кислорода остаётся в воде, а к чему приводит недостаток O2 пояснений не требует.
Окисляемость измеряется в объёме (в мл.) расходуемого кислорода на один литр воды. Для большинства видов рыб не желательно превышать средний уровень, лишь самые выносливые, такие как Гуппи и Золотые рыбки, будут чувствовать себя нормально при повышенном уровне.
- Малый уровень — до 4 мл. на 1 л.
- Средний уровень — 4–10 мл. на 1 л.
- Повышенный уровень — 10–15 мл. на 1 л.
- Опасный — более 15 мл. на 1 л.
Для аквариумиста это один из важнейших показателей, причём довольно универсальный, а главное простой в измерениях, не требующих дорогостоящих препаратов и больших временных затрат.
Способ проверки окисляемости воды в домашних условиях
Простым и одновременно эффективным методом определения редокс-потенциала воды в аквариуме служит Перманганатная окисляемость. Метод основан на использовании раствора марганцовки (перманганат калия), который добавляют в пробу воды из аквариума. В марганцовке содержится много кислорода, который вступает в реакцию с примесями в воде.
Суть метода проста — если в пробе воды кислорода много, марганцовка окрасит её в розовый цвет, если мало — в оттенки жёлтого.
Шаг № 1. Приготовить концентрированный раствор марганцовки
Возьмите небольшую ёмкость, объёма в 100 мл. более чем достаточно (такой объём имеет самая маленькая баночка детского питания). Наберите в неё менее половины чистой кипячёной остывшей воды и добавьте марганцовку. Её следует насыпать до тех пор, пока раствор не станет на столько насыщенным, что крупицы перестанут растворяться. Например, для объёма в 20–25 мл. это чайная ложка марганцовки.Получившегося раствора хватит на множество тестов. Храните его в плотно закрытой баночке в тёмном месте.
Шаг № 2. Тестирование пробы воды
Для работы понадобится одноразовый пластиковый прозрачный стаканчик и шприц. С помощью шприца наберите в стаканчик 50 мл. воды из аквариума и добавьте в неё одну каплю раствора. В этом случае шприц также служит прекрасным дозатором.Будьте внимательны — набирайте в шприц только с поверхности раствора, чтобы не растворённые крупицы не попали внутрь, иначе результат получится недостоверным.
Шаг № 3. Проверка результатов
Пробу воды с каплей марганцовки оставляют на 40–50 минут при комнатной температуре, избегайте попадания на стаканчик прямых солнечных лучей. В результате вода должна окрасится в один из цветов красного спектра от розового до жёлтого, иногда возможно выпадение осадка.Сопоставьте получившийся цвет с эталонной картой, представленной ниже. Однако, виду многочисленных нюансов в передаче цвета на экранах компьютеров и мобильных устройств, карту рекомендуется использовать только в качестве уточняющего материала. Свой эталон можно сделать самостоятельно, в другой стаканчик вместо аквариумной наберите 50 мл чистой кипячёной воды и добавьте туда каплю раствора марганцовки. Вода окрасится в красивый розовый цвет и сохранит его на протяжении длительного времени.
Цветовая шкала определения редокс-потенциала
 Определение степени окисляемости (редокс-потенциала) посредством соответствия раствора аквариумной воды цветовым индикаторам
Определение степени окисляемости (редокс-потенциала) посредством соответствия раствора аквариумной воды цветовым индикаторам Высокая окисляемость может быть связана с перенаселением аквариума, избыточным рационом питания, когда рыбки не успевают съесть всю еду, нерегулярным обслуживанием (очистка грунта, подмена части воды) или же совокупность всех факторов.Кроме того, вещества и реагенты, используемые для понижения показателя pH, также оказывают влияние на редокс-потенциал, повышая его.
www.aqvium.ru
Химические характеристики воды: вопросы и ответы
Что такое минерализация?Зачем измерять уровень минерализации в вашей воде?Как влияют растворенные в воде вещества на организм человека?Где рекомендуется измерять уровень минерализации?Что такое кондуктометр и для чего он нужен?Что такое pH?Для чего нужно измерять pH?Что такое RedOx окислительно-восстановительный потенциал?Где рекомендуется измерять RedOx потенциал?Что такое минерализация?
Минерализация - это суммарный количественный показатель содержания растворенных в воде веществ. Этот параметр также называют содержанием растворимых твердых веществ или общим солесодержанием, так как растворенные в воде вещества находятся именно в виде солей. К числу наиболее распространенных относятся неорганические соли (в основном бикарбонаты, хлориды и сульфаты кальция, магния, калия и натрия) и небольшое количество органических веществ, растворимых в воде.За рубежом минерализацию еще называют как общее количество растворенных частиц - Total Dissolved Solids (TDS), что по сути, то же самое. За единицу уровня минерализации приняты миллиграмм на литр (мг/л). Это означает вес растворенных веществ в граммах, растовренных в 1 литре воды. Также уровень минерализации может выражаться в частицах на миллион частиц воды - сокращенно ppm (parts per million - частиц на миллион). Такую аббревиатуру можно встретить в зарубежных источниках. Это означает количество частиц растворенных в 1 миллионе частиц воды. Соотношение между единицами измерения мг/л и ppm практически равное - 1 мг/л = 1 ppm.
Зачем измерять уровень минерализации в вашей воде?
Согласно требованиям Управления по охране окружающей среды (EPA) максимально допустимый уровень загрязнения воды является 500 мг/литр или 500 частиц на миллион (parts per million, ppm) к общему количеству растворенных в воде твердых частиц.Когда уровень минерализации превышает 1000 мг/литр, считается, что такая вода не пригодна для потребления человеком. Высокий уровень минерализации является индикатором потенциальной опасности, а также подтверждает необходимость проведения лабораторных исследований. В большинстве случаев высокий уровень минерализации вызван содержанием калия, солей хлористоводородной кислоты и натрия, ионы которых имеют небольшой или краткосрочный эффект. Однако помимо этого в воде могут содержаться токсичные ионы (арсенат свинца, кадмий, нитрат и другие), представляющие опасность для живых организмов.
Даже самые лучшие очистительные системы, представленные на рынке, требуют слежения за уровнем минерализации для того, чтобы быть уверенными, что фильтры и/или мембраны эффективно удаляют нежелательные элементы и бактерии из вашей воды.
Как влияют растворенные в воде вещества на организм человека?
Содержащиеся в воде органические соединения и их воздействие на организм человекаВсе органические соединения, находящиеся в воде, можно условно разделить на мелкие (размер молекулы - меньше 100 килодальтон) и крупные (размер молекулы - от 100 килодальтон). Наиболее опасны для человека крупные органические соединения, которые на 90% являются канцерогенами или мутагенами. Наиболее опасны хлорорганические соединения, образующиеся при кипячении хлорированной воды, т.к. они являются сильными канцерогенами, мутагенами и токсинами. Остальные 10% крупной органики в лучшем случае нейтральны в отношении организма. Полезных для человека крупных органических соединений, растворенных в воде, всего 2-3 (это ферменты, необходимые в очень малых дозах). Воздействие органики начинается непосредственно после питья. В зависимости от дозы это может быть 18-20 дней или, если доза большая, 8-12 месяцев.
Содержащиеся в воде ионы тяжелых металлов и их воздействие на организм человека
Тяжелые металлы, попадая в наш организм, остаются там навсегда, вывести их можно только с помощью белков молока и белых грибов. Достигая определенной концентрации в организме, они начинают свое губительное воздействие - вызывают отравления, мутации. Кроме того, что сами они отравляют организм человека, они еще и чисто механически засоряют его - ионы тяжелых металлов оседают на стенках тончайших систем организма и засоряют почечные каналы, каналы печени, таким образом снижая фильтрационную способность этих органов. Соответственно, это приводит к накоплению токсинов и продуктов жизнедеятельности клеток нашего организма, т.е. самоотравление организма, т.к. именно печень отвечает за переработку ядовитых веществ, попадающих в наш организм, и продуктов жизнедеятельности организма, а почки - за их выведение наружу. К тяжелым металлам относятся Pb (свинец), Al (алюминий), Mn (марганец), Si (кремний), Fe (железо), Se (селен), Zn (цинк), Hg (ртуть), Cd (кадмий).
Марганец забивает канальцы нервных клеток. Снижается проводимость нервного импульса, как следствие повышается утомляемость, сонливость, снижается быстрота реакции, работоспособность, появляются головокружение, депрессивные, подавленные состояния. Особенно опасны отравления марганцем у детей и эмбрионов (когда женщина беременна) - приводит к идиотии. Из 100 детей, матери которых во время беременности подверглись отравлению марганцем, 96-98 рождаются идиотами. Есть также теория, что токсикозы на ранних и поздних сроках беременности вызываются марганцем. В водопроводной воде - избыток марганца. Кроме воды марганец содержится в воздухе из-за производственных выбросов. В природе марганец затем накапливается в грибах и растениях, попадая таким образом в пищу. Марганец почти невозможно вывести из организма; очень тяжело диагностировать отравление марганцем, т.к. симптомы очень общие и присущи многим заболеваниям, чаще же всего человек просто не обращает на них внимания.
Алюминий так же оказывает общее отравляющее и засоряющее действие на организм человека. В водопроводной воде его избыток связан с тем, что излишки железа на водозаборе удаляют сульфатом алюминия. Реагируя с ионами железа, сульфат алюминия дает нерастворимый осадок, в который выпадает, в принципе и железо, и алюминий, но в реальности в воде остается и железо, и алюминий.
Селен не содержится в природной воде Новосибирска. Селен необходим человеку в очень малых дозах, при малейшем превышении дозы он превращается в канцероген, мутаген и токсин. Человеку можно безопасно восполнить недостаток селена с помощью специальных минеральных комплексов; селен также содержится в морской капусте.
Железо бывает в природе в трех состояниях - молекулярное железо F0(когда оно куском), Fe2+ - необходимо в организме человека как переносчик кислорода (в молекуле гемоглобина 4 иона F2+) и F3+ - вредное для человека - оно и есть ржавчина. Железо необходимо организму человека, но только в определенной пропорции и в виде иона F2+. В водопроводной воде большой избыток железа, т.к. в природной воде Новосибирска его много, плюс ржавые трубы, по которым течет вода к потребителям.
Кальций необходим в организме человека для строения костной ткани (зубы, кости), мышечной ткани (мышцы, мышца сердца), поддержания проводящей функции нервной ткани. При избытке кальций нейтрален по отношению к организму человека, однако, это снижает качество воды - соли кальция образуют накипь и мутность воды.
Магний необходим для нормальной деятельности нервных клеток. Однако, его количество в воде должно быть ограниченно, т.к. при избытке он действует на подобие марганца - засоряет канальцы нервных клеток, только он менее активен и проще выводится из организма.
Калий также необходим для нормальной жизнедеятельности организма, т.к. является компонентом калий-натриевого насоса. Калий-натриевый насос - это структура на мембране каждой клетки, благодаря которой в клетку проникают вещества из межклеточной жидкости, а из клетки выводятся продукты ее жизнедеятельности. Кроме того, особенно важен калий для сердечно-сосудистой деятельности, т.к. он нормализует давление крови и работу сердца.
Где рекомендуется измерять уровень минерализации?
В быту:- при анализе качества питьевой водыВысокий уровень минерализации проявляется в неприятном привкусе воды, которая может быть соленой, горькой или с металлическим привкусом. Это также может означать присутствие токсичных минералов. Рекомендуемый уровень минерализации в воде согласно сведениям Управления по охране окружающей среды (EPA) США должен составлять 500 мг/литр (500ppm). Проверить это нетрудно с помощью TDS Meter.
- при выборе бытовой системы очистки водыПеред покупкой системы очистки для воды (фильтра) Вам необходимо знать характеристики Вашей воды, чтобы подобрать наиболее эффективную систему очистки. Решить этот вопрос Вам поможет TDS Meter.
- при проверке эффективности работы Вашей системы очистки водыДля того чтобы быть уверенным, что фильтр эффективно удаляет нежелательные элементы и бактерии из вашей воды. Даже самые лучшие очистительные системы, представленные на рынке, требуют наблюдение за уровнем минерализации. С помощью анализатора Clean Tap Monitor, который устанавливается непосредственно в магистраль фильтрующей системы, Вы всегда сможете вовремя определить время замены картриджа с фильтром или мембраны.
- в аквариумахПостоянный уровень содержания минералов необходим для водной флоры и фауны. Вода в аквариуме должна содержать одинаковый уровень минерализации, жесткости и pH так же как и в естественной природной среде обитания населения аквариума (рыб или кораллов). Создать подобную среду Вам поможет анализатор TDS Meter.
- в бассейнахВысокий уровень минерализации определяет твердую воду, которая образует наросты и отложения в трубах и клапанах. Во избежание проблем с обслуживанием бассейнов рекомендуется измерять уровень с помощью TDS Meter.
- при производстве продуктов питания
- при производстве косметических средств
- при производстве лекарственных препаратов
Что такое кондуктометр и для чего он нужен?
КОНДУКТОМЕТРИЯ - (от англ . conductivity - электропроводность и ...метрия), электрохимический метод анализа, основанный на измерении электрической проводимости растворов.Применяют для определения концентрации растворов солей, кислот, оснований, контроля состава некоторых промышленных растворов.
Кондуктометры используются для:
- оценки качества дистиллированной воды;
- оценки засоления почв;
- кондуктометрического титрования - это постепенное прибавление контролируемого количества реагента (напр., кислоты) к анализируемому раствору (напр., щелочи).
Что такое pH?
pH - это водородный показатель, характеризующий концентрацию свободных ионов водорода в воде. Для удобства отображения был введен специальный показатель, названный рН и представляющий собой логарифм концентрации ионов водорода, взятый с обратным знаком, т.е pH = -log[H+].Если говорить проще, то величина рН определяется количественным соотношением в воде ионов Н+ и ОН-, образующихся при диссоциации воды. Если в воде пониженное содержание свободных ионов водорода (рН>7) по сравнению с ионами ОН-, то вода будет иметь щелочную реакцию, а при повышенном содержании ионов Н+ (рН<7)- кислую. В идеально чистой дистиллированной воде эти ионы будут уравновешивать друг друга. В таких случаях вода нейтральна и рН=7. При растворении в воде различных химических веществ этот баланс может быть нарушен, что приводит к изменению уровня рН.
Очень часто показатель рН путают с такими параметрами, как кислотность и щелочность воды. Важно понимать разницу между ними. Главное заключается в том, что рН - это показатель интенсивности, но не количества. То есть, рН отражает степень кислотности или щелочности среды, в то время как кислотность и щелочность характеризуют количественное содержание в воде веществ, способных нейтрализовывать соответственно щелочи и кислоты. В качестве аналогии можно привести пример с температурой, которая характеризует степень нагрева вещества, но не количество тепла. Например, опустив руку в воду, мы можем сказать какая вода - прохладная или теплая, но при этом не сможем определить сколько в ней тепла (т.е. условно говоря, как долго эта вода будет остывать).
Для чего нужно измерять pH?
pH воды - один из важнейших рабочих показателей качества воды, во многом определяющих характер химических и биологических процессов, происходящих в воде.В зависимости от величины pH может изменяться скорость протекания химических реакций, степень коррозионной агрессивности воды, токсичность загрязняющих веществ и т.д.
Контроль за уровнем рН особенно важен на всех стадиях водоочистки, так как его "уход" в ту или иную сторону может не только существенно сказаться на запахе, привкусе и внешнем виде воды, но и повлиять на эффективность водоочистных мероприятий.
Оптимальная требуемая величина рН варьируется для различных систем водоочистки в соответствии с составом воды, характером материалов, применяемых в системе распределения, а также в зависимости от применяемых методов водообработки. Обычно уровень рН находится в пределах, при которых он непосредственно не влияет на потребительские качества воды. Так, в речных водах pH обычно находится в пределах 6.5-8.5, в атмосферных осадках 4.6-6.1, в болотах 5.5-6.0, в морских водах 7.9-8.3.
Известно, что при низком рН вода обладает высокой коррозионной активностью, а при высоких уровнях (рН>11) вода приобретает характерную мылкость, неприятный запах, способна вызывать раздражение глаз и кожи. Именно поэтому для питьевой и хозяйственно-бытовой воды оптимальным считается уровень рН в диапазоне от 6 до 9.
Что такое RedOx окислительно-восстановительный потенциал?
Окислительно-восстановительный потенциал (ОВП), называемый также редокс-потенциал (от английского RedOx - Reduction/Oxidation), характеризует степень активности электронов в окислительно-восстановительных реакциях, т.е. реакциях, связанных с присоединением или передачей электронов.Значение окислительно-восстановительного потенциала для каждой окислительно-восстановительной реакции вычисляется по довольно сложной формуле, выражается в милливольтах и может иметь как положительное, так и отрицательное значение. В природной воде значение Eh колеблется от - 400 до + 700 мВ, что определяется всей совокупностью происходящих в ней окислительных и восстановительных процессов. В условиях равновесия значение ОВП определенным образом характеризует водную среду, и его величина позволяет делать некоторые общие выводы о химическом составе воды. В зависимости от значения ОВП различают несколько основных ситуаций, встречающихся в природных водах:
- Окислительная:Характеризуется значениями Еh > + (100 - 150) мВ, присутствием в воде свободного кислорода, а также целого ряда элементов в высшей форме своей валентности (Fe3+, Mo6+, As5-, V5+, U6+, Sr4+, Cu2+, Pb2+). Ситуация, наиболее часто встречающаяся в поверхностных водах.
- Переходная окислительно-восстановительная:Определяется величинами Еh от 0 до + 100 мВ, неустойчивым геохимическим режимом и переменным содержанием сероводорода и кислорода. В этих условиях протекает как слабое окисление, так и слабое восстановление целого ряда металлов.
- Восстановительная:Характеризуется значениями Еh < 0. Типична для подземных вод, где присутствуют металлы низких степеней валентности (Fe2+, Mn2+, Mo4+, V4+, U4+), а также сероводород.
Где рекомендуется измерять RedOx потенциал?
Окислительно-восстановительный потенциал зависит от температуры и взаимосвязан с рН. В некоторых применениях (например, в обработке воды для бассейнов) ОВП является одним из основных параметров контроля качества воды. В частности потому, что позволяет оценить эффективность обеззараживания воды. В частности, при обслуживании бассейнов, используется таблица зависимости продолжительности жизни типичных микроорганизмов (E-Coli) от величины редокс-потенциала.aquacomplex.livejournal.com
Все о воде в аквариуме - химия ph экстракт торфа промилле редокс-потенциал
В литературе по аквариумистике нередко используются формулировки: «жесткая вода», «мягкая вода». Так что же это означает?
Жесткость воды — это доля содержащихся в ней минеральных солей, как правило солей кальция и магния. Определяют общую, или карбонатную, жесткость, и постоянную, или некарбонатную. Общая жесткость — это сумма временной и постоянной жесткости. Единица измерения — градусы. В отечественных источниках по аквариумистике используют немецкие градусы жесткости dH. Очень мягкая вода — это вода с жесткостью от 0 до 4°, мягкая — от 5 до 8°, средней жесткости — от 9 до 16°, жесткая — от 16 до 30° и свыше 30° — очень жесткая. Как правило аквариумисты пользуются водой из водопровода, жесткость которой изменчива и определяется временем года, количеством осадков и географией места проживания. Например, жесткость воды в Москве от 4 до 12°, 2-3° в Санкт-Петербурге, 12° и выше в Одессе.
Постоянная и временная жесткость. Что это такое?
Постоянная или некарбонатная жесткость воды зависит от растворенных в воде сульфатов, хлоридов кальция и магния и . Этот устраняется только дистилляцией воды или химическим путем. В то время как временная или карбонатная жесткость определяется содержанием бикарбонатов кальция и магния.
Каким образом повысить жесткость воды?
Небольшого увеличения жесткости воды в аквариуме можно добиться положив в воду кусочки мрамора или ракушки. В данном случае она повышается не сразу. Отметим, что чем мягче вода, тем быстрее увеличивается ее жесткость.
Более быстрый метод — добавление растворов хлористого кальция и сульфата магния (магнезии), продающихся в аптеках. Так добавление 1 миллиграмма 10-процентного раствора хлористого кальция повышает жесткость 1 литра воды где-то на 3°, а 1 миллиграмма 25-процентного раствора сульфата магния увеличит жесткость на 4°. Одновременное использование хлористого кальция и магнезии даст более близкое к природному соотношению ионов кальция и магния в воде аквариума.
Каким образом понизить жесткость воды?
Есть несколько методов уменьшения жесткости воды. Самый простой — кипячение и вымораживание. Чтобы понизить жесткость вдвое, необходимо кипячение воды в течение 30 минут. Еще сильнее она снизится при вымораживании. Процедура вымораживания включает следующее. Воду наливают в неглубокую емкость. После того как половина объема воды замерзнет, остаток, в котором остались растворенные соли, сливают. А лед, практически не содержащий солей, растапливают. Полученная вода будет иметь значительно меньшую жесткость.
Что такое рН?
Активная реакция водородных ионов (рН) — одна из основных характеристик физико-химического состояния воды. Она обусловливается числом содержащихся в воде водородных (Н’1′) и гидроксильных (ОН~) ионов. Среда считается нейтральной, если рН равен 7, кислой — ниже 7 и щелочной — больше 7.
Как правило, растворенные соли, определяющие жесткость воды, наряду с этим делают ее щелочной. В то же время органические вещества (отходы жизнедеятельности рыб и растений) и растворенная двуокись углерода оказывают на воду окисляющее действие.
Кислотность воды в аквариуме должна соответствовать потребностям содержащихся в нем рыб и растений. От правильного значения показателя кислотности зависит здоровье и даже жизнь аквариумных обитателей. Как правило, этот показатель бывает от 6 до 9. Родина большинства аквариумных рыб водоемы, где кислотность воды нейтральная или слабокислая (pH 6 — 7). В то же время, цихлиды африканских озер Малави и Танганьика предпочитают слабощелочную воду (pH 7.5 — 8.0). В морских аквариумах лучшей является щелочная кислотность в пределах 8.2 — 8.4 pH. Некоторые рыбы выдерживают большие колебания значений рН, другие — могут обитать только в воде с довольно устойчивой кислотностью. В аквариуме величина рН может колебаться даже в течение суток. Это связано с биологическими и химическими процессами, происходящими в аквариуме. Водопроводная вода, отстоянная в течение суток, как правило, имеет величину рН близкую к нейтральной.
Как изменить рН воды в аквариуме?
Чтобы изменить рН в воду добавляют кислоту или щелочь. Но не всякая кислота и щелочь подходит для этой цели. Для подкисления воды в аквариуме предпочтительней всего применять ортофосфорную кислоту (серная и соляная непригодны ;-)). Сперва кислоту разводят водой (прибавляя кислоту к воде, а не наоборот), а после этого по каплям добавляют в аквариум, наблюдая уровень рН.
Воду в аквариуме можно подкислять и с помощью экстракта торфа или отвара ольховых шишек. Для приготовления отвара ольховых шишек одну столовую ложку шишек заливают стаканом кипятка и держат на огне 5-7 минут. Остывший отвар доливают в аквариум из расчета 1 стакан на 10 литров воды.
Обычно воду в аквариуме подкисляют только при разведении некоторых видов рыб. В декоративном аквариуме изменять рН не требуется.
Для подщелачивания воды могут использоваться разные щелочи, но лучше применять питьевую соду (гидрокарбонат натрия) из расчета 0,2 — 0,5 грамма на 1 литр воды. Соду необходимо растворить в отдельной емкости, а затем добавлять в аквариум. Ощелачивание мягкой и очень мягкой воды не дает постоянного результата. В аквариумах, где часть воды систематически подменяют, величина рН обычно больше 7, и производить подщелачивание не требуется.
Как приготовить экстракт торфа?
Для приготовления торфяного экстракта несколько кусков торфа вываривают в эмалированной посуде. Количество торфа и объем воды, в которой он будет вывариваться, не имеют значения. Затем, остудив, процеживают полученный отвар через вату 2-3 раза. Торфяной настой готовят так же, как отвар, но торф не вываривают, а настаивают. На каждые 100 литров воды нужно вносить 0,5-1 литр отвара или настоя. Чтобы местный торф соответствовал тропическому, некоторые аквариумисты добавляют несколько зерен кофе, щепотку чая, лист эвкалипта, а также несколько ольховых шишки и немного дубовой коры.
Отвар или настой добавляют в воду до тех пор, пока она не приобретет светло — янтарный оттенок.
Что такое промилле?
Соленость, или минерализация, воды выражается долей растворенных в ней солей. Их концентрация в граммах на 1 литр называется промилле (°/оо).
Что такое редокс-потенциал?
Редокс-потенциал, или окислительно-восстановительный потенциал — характеристика химической и биологической активности воды. В аквариуме он имеет значимость как характеристика насыщенности воды органическими веществами, той есть загрязненности аквариума. Измеряют редокс-потенциал при помощи особого электронного прибора — рН-метра. Редокс-потенциал определяется в условных единицах от 0 до 42. Измерить его в домашних условиях, обычно, нельзя.
В заново оборудованном аквариуме он имеет величину 30 — 34. При этом хорошо развиваются большинство плавающих в толще воды, а также мелколистных растений со слабой корневой системой (перистолистник, гигрофила, кабомба и др.). Это может говорить о высоком значении редокс-потенциала. Далее понемногу величина редокс-потенциал снижается. Показатель этого — хороший рост эхинодорусов и апоногетонов. В более старом аквариуме, когда редокс-потенциал еще меньше, превосходно растут криптокорины. Когда и криптокорины начинают хуже развиваться, значит пришло время чистить грунт, подменить частично воду. Возможно, необходимо улучшить фильтрацию, установив донный фильтр.
системой (перистолистник, гигрофила, кабомба и др.). Это может говорить о высоком значении редокс-потенциала. Далее понемногу величина редокс-потенциал снижается. Показатель этого — хороший рост эхинодорусов и апоногетонов. В более старом аквариуме, когда редокс-потенциал еще меньше, превосходно растут криптокорины. Когда и криптокорины начинают хуже развиваться, значит пришло время чистить грунт, подменить частично воду. Возможно, необходимо улучшить фильтрацию, установив донный фильтр.
Что такое «старая вода»?
В аквариуме со временем скапливаются продукты жизнедеятельности рыб и растений, которые, разлагаясь, обогащают воду органическими кислотами. При отсутствии фильтра или редкой подмене воды этот процесс ускоряется. Вода приобретает желтоватый цвет и имеет кислую реакцию. Такая вода и называется «старой».
ИНТЕРЕСНЫЕ СТАТЬИ:
 Январь 13, 2017 Коридорас нанус содержание описание уход
Январь 13, 2017 Коридорас нанус содержание описание уход Январь 11, 2017 Коридорас-пигмей содержание и уход разведение
Январь 11, 2017 Коридорас-пигмей содержание и уход разведение Сентябрь 8, 2016 Барбус алый содержание разведение совместимость кормление фото.
Сентябрь 8, 2016 Барбус алый содержание разведение совместимость кормление фото. Сентябрь 12, 2016 Барбус латеристрига: содержание совместимость разведение фото
Сентябрь 12, 2016 Барбус латеристрига: содержание совместимость разведение фото Февраль 16, 2017 Жесткость воды в аквариуме
Февраль 16, 2017 Жесткость воды в аквариуме Февраль 9, 2017 Чешутся рыбы в аквариуме что делать — описание
Февраль 9, 2017 Чешутся рыбы в аквариуме что делать — описание Февраль 16, 2017 Карликовые цихлиды фото и описание
Февраль 16, 2017 Карликовые цихлиды фото и описание Июль 9, 2017 Разновидности барбусов
Июль 9, 2017 Разновидности барбусов Февраль 16, 2017 Аквариум Амано Такаши — удивительный подводный мир
Февраль 16, 2017 Аквариум Амано Такаши — удивительный подводный мир Февраль 8, 2017 Таймер для аквариума — описание фото видео обзор
Февраль 8, 2017 Таймер для аквариума — описание фото видео обзор
aquarium-fish-home.ru