Чем отличаются молекулы воды. Вода молекулы
Чем отличаются молекулы воды и молекулы льда?
Понятие молекулы ( и производные от него представления о молекулярном строении вещества, структуры собственно молекулы) позволяет понимать свойства веществ создающих мир. Современные, как и ранние, физико-химические исследования опираются и базируются на грандиозном открытие об атомно-молекулярном строении вещества. Молекула – единая «деталь» всех веществ, существование которой предположил ещё Демокрит. Потому именно её структура и взаимосвязь с другими молекулами (образуя определенное строение и состав) и определяет/объясняет все различия между веществами, их видом и свойствами.
Сама молекула, будучи не самой мельчайшей составной частью вещества (коей является атом) имеет определенную структуру, свойства. Определяется структура молекулы числом вхожих в неё определенных атомов и характером связи (ковалентной) между ними. Состав этот неизменен, даже если вещество преобразуется в другое состояние(как примеру, происходит с водой – об этом пойдет речь дальше).
Молекулярное строение вещества фиксируется формулой, которая сообщает информацию об атомах, их количестве. Кроме того, молекулы составляющие вещество/тело не статичны: и сами являются подвижными – атомы вращаются, взаимодействуя между собой (притягиваются/отталкиваются).
Характеристики воды, её состояния
Состав такого вещества, как вода (равно как и её химическая формула) знаком каждому. Каждую её молекулу составляют три атома: атом кислорода, обозначающийся буквой «О», и атомы водорода – латинская «Н», в количестве 2-х. Форма молекулы воды не симметрична (схожа с равнобедренным треугольником).
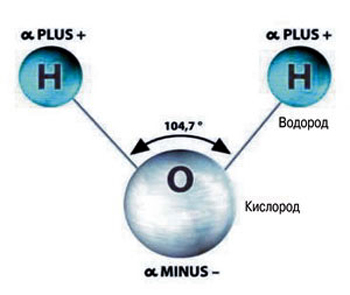
Молекула воды
Вода, как вещество, составляющие её молекулы, реагирует на внешнюю «обстановку», показатели окружающей среды — температуру, давление. Зависимо от последних вода способна изменять состояние, которых три:
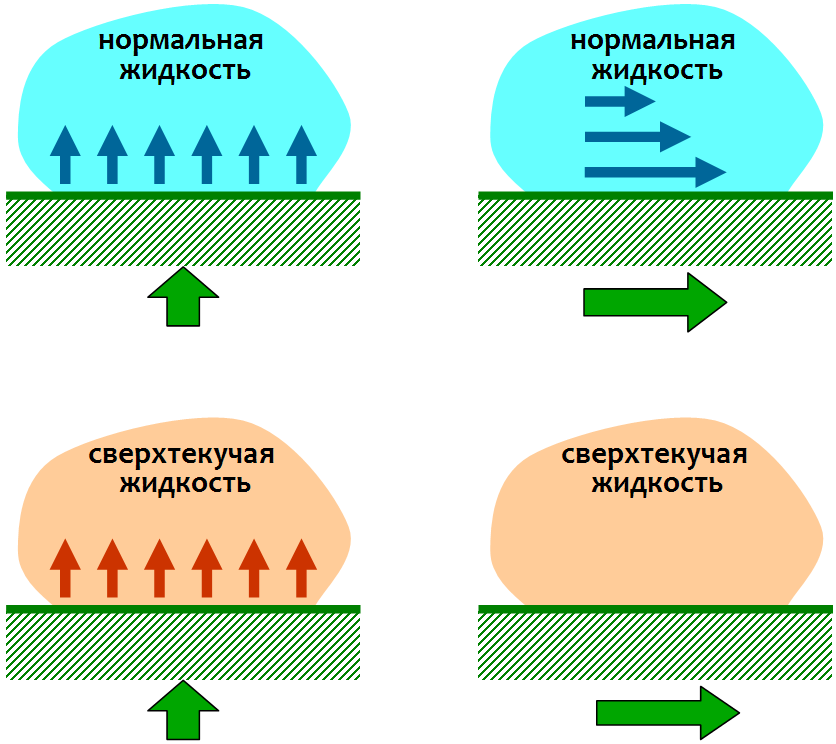
- Наиболее привычное, естественное для воды состояние жидкое. Молекулярная структура (дигидроль) своеобразного порядка, при котором одиночные молекулы заполняют (водородными связями) пустоты.
- Состояние пара, при котором молекулярная структура (гидроль) представлена одиночными молекулами между которыми не образуются водородные связи.
- Твердое состояние (собственно лед), имеет молекулярную структуру (тригидроль) с прочными и устойчивыми водородными связями.
Помимо данных различий, естественно, разнятся и способы «перехода» вещества из одного состояния (жидкого) в другие. Эти переходы и трансформируют вещество, и провоцируют передачу энергии (выделение/поглощение). Среди них есть процессы прямые – преобразование жидкой воды в пар (испарение), в лед (замерзание) и обратные – в жидкость из пара (конденсация), из льда (таяние). Также и состояния воды — парообразное и лед — могут трансформироваться друг в друга: возгонка – лед в пар, сублимация – обратный процесс.
Специфичность льда как состояния воды
Широко известно, что лед замерзает ( трансформируется из воды) при пересечении температурой в сторону уменьшения границы в ноль градусов. Хотя, в этом всем понятном явлении, есть свои нюансы. К примеру, состояние льда неоднозначно, различны его виды, модификации. Отличаются они первоочередно условиями, при которых возникают – температурой, давлением. Таких модификаций насчитывается аж пятнадцать.
Лед в разных своих видах имеет различное молекулярное строение (молекулы же неотличимы от молекул воды). Природный и естественный лед, в научной терминологии обозначающийся как лед Ih — вещество с кристаллической структурой. То есть, каждая молекула с четырьмя окружающими её «соседками» (расстояние между всеми равное) создают геометрическую фигуру тетраэдр. Другие фазы льда обладают более сложной структурой, к примеру высокоупорядоченная структура тригонального, кубического или моноклинного льда.
Основные отличия льда от воды на молекулярном уровне
Первое и напрямую не относящееся к молекулярному строению воды и льда различие между ними – показатель плотности вещества. Кристаллическая структура, присущая льду, образовываясь, способствует одновременному уменьшению плотности (с показателя почти в 1000 кг/м³ до 916,7 кг/м³). А это стимулирует увеличение объема на 10%.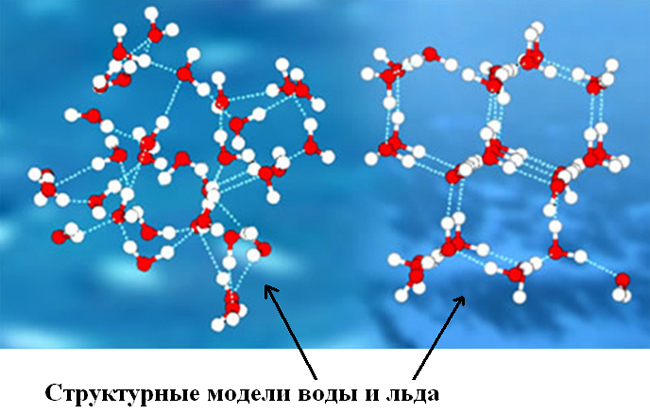 Основное же отличие в молекулярном строении этих агрегатных состояний воды (жидкого и твердого) в количестве, виде и силе водородных связей между молекулами. Во льду же (твердом состоянии) ими объединены пять молекул, а собственно связи водородные прочнее.
Основное же отличие в молекулярном строении этих агрегатных состояний воды (жидкого и твердого) в количестве, виде и силе водородных связей между молекулами. Во льду же (твердом состоянии) ими объединены пять молекул, а собственно связи водородные прочнее.
Сами молекулы веществ воды и льда, как упоминалось ранее, одинаковы. Но в молекулах льда атом кислорода (для создания кристаллической «решетки» вещества) образовывает водородные связи (две) с молекулами-«соседками».
Отличает вещество воды в разных её состояниях (агрегатных) не только структура расположения молекул (молекулярное строение), но и движение их, сила взаимосвязи/притяжения между ними. Молекулы воды в жидком состоянии достаточно слабо притягиваются, обеспечивая текучесть воды. В твердом же льду наиболее сильно притяжение молекул, потому и мала их двигательная активность (она обеспечивает постоянство формы льда).
vchemraznica.ru
Структура молекул воды - Новости

Если посмотреть на каплю воды невооружейным глазом, то она выглядит просто как капля воды. Но микроскоп открывает нам гораздо большее видение. Точно так же, если вы смотрите на ночное небо невооруженным глазом, вы видите только звезды. Но телескоп открывает нам планеты, туманности, кометы - самые невообразимые объекты.
 Давайте посмотрим в микроскоп: как организованы молекулы воды. Молекула воды состоит из одного атома кислорода, связанного с двумя атомами водорода h3O . Вблизи атома кислорода скапливается избыточный отрицательный заряд, а у атомов водорода - положительный. Атомы водорода имея одинаковый по полярности заряд отталкиваются друг от друга образуя угол химической связи с кислородом 104,5 градусов.
Давайте посмотрим в микроскоп: как организованы молекулы воды. Молекула воды состоит из одного атома кислорода, связанного с двумя атомами водорода h3O . Вблизи атома кислорода скапливается избыточный отрицательный заряд, а у атомов водорода - положительный. Атомы водорода имея одинаковый по полярности заряд отталкиваются друг от друга образуя угол химической связи с кислородом 104,5 градусов.

Молекулы воды Н2О объединяются в группы – кластеры. Кластеры, объединяясь, образуют ячейки памяти воды. Современные приборы зафиксировали, что в каждой ячейке памяти воды находятся тысячи информационных панелей. Вода – это природный компьютер. Устойчивость кластерной структуры подтвердила гипотезу о способности воды запоминать и сохранять информацию. Например, вода, над которой прочитали молитву, сохраняет ее энергетический посыл, выстраиваясь в определенную кластерную форму.
Рустум Рой Доктор наук, заслуженный профессор Государственного университета,  штат Пенсильвания; профессор материаловедения Государственного университета, штат Аризона, США, член Академии наук Швеции, Индии, Японии, России, США.
штат Пенсильвания; профессор материаловедения Государственного университета, штат Аризона, США, член Академии наук Швеции, Индии, Японии, России, США.
«…Молекулярная структура - алфавит воды. Если я вам дам алфавит, а вы не знаете ни слов, ни букв, ни предложений, то вы не сможете ими воспользоваться. Химики, используют крайне элементарный способ, когда говорят о воде. По сути, они говорят о буквах алфавита. Но знание букв недостаточно, чтобы говорить о Пушкине или о Шекспире. Химический состав воды был господствующий точкой зрения у химиков. Так вот, сенсационная новость заключается в том, что все это чепуха. Структура воды намного более важна, чем ее химический состав…»
 Сегодня существует метод определения качества структуры воды по замороженным кристаллам льда. Статистика, которая продолжается более 10 лет по разным водам: природным, водопроводным, бутилированным, прошедшим различную фильтрацию, активацию и пр. пр. пр. показала, что в природной горной воде или в структурированной воде будут образовываться симметричные шестилучиковые снежинки, а в воде, прошедшей техногенную обработку, будут изломанные деформированные кристаллы воды. Смотрите на фото замороженные образцы горной воды и водопроводной.
Сегодня существует метод определения качества структуры воды по замороженным кристаллам льда. Статистика, которая продолжается более 10 лет по разным водам: природным, водопроводным, бутилированным, прошедшим различную фильтрацию, активацию и пр. пр. пр. показала, что в природной горной воде или в структурированной воде будут образовываться симметричные шестилучиковые снежинки, а в воде, прошедшей техногенную обработку, будут изломанные деформированные кристаллы воды. Смотрите на фото замороженные образцы горной воды и водопроводной.
Если говорить о «правильной» качественной, например, хорошей горной воде, то в такой воде кластеры будут упорядочены, а, например, в водопроводной воде кластеры будут расположены хаотично. И это доказано экспериментально!
После замораживания воды образуются кристаллы льда. Это стоп-кадр организации – структуры воды. В качественной воде будет много симметричных шестилучиковых кристаллов воды, а вот в воде, прошедшей ту или иную техногенную обработку будет мало или совсем не будет. Кристаллы воды говорят об активности воды, о ее внутренней энергии, то есть при замораживании воде хватило энергии вырастить симметричный красивый кристал-снежинку.
Структура воды это не застывшие кластеры. Структура воды может меняться под любым воздействием: температура, давление, электромагнитные поля, микроволновое воздействие, грязные трубы, телевизор, ругательства, крики, пение, молитвы, добрые слова и прочее. Ученые доказали, что это влияние может быть направлено, как в положительную, так и в отрицательную сторону по отношению к здоровью человека.
 Научно доказано, что вода может пагубно влиять на любой живой организм в случае если ее кристаллы займут хаотичную позицию. К примеру, воду в бутылках разгружали в магазине и матерились грузчики. Покупая такую бутилированную воду, мы надеемся на ее чистоту, и она может быть будет чистой с точки зрения химии, но вот с точки зрения биоэнергии, био полезности это будет вода, разрушающая здоровье!
Научно доказано, что вода может пагубно влиять на любой живой организм в случае если ее кристаллы займут хаотичную позицию. К примеру, воду в бутылках разгружали в магазине и матерились грузчики. Покупая такую бутилированную воду, мы надеемся на ее чистоту, и она может быть будет чистой с точки зрения химии, но вот с точки зрения биоэнергии, био полезности это будет вода, разрушающая здоровье!
Для того, чтобы очищенная вода, бутилированная или фильтрованная, стала полезной для клеток, необходимо обязательно восстановить ее природную структуру! Этот процесс возможен в случае использования специальных устройств, максимально приближенных к природному процессу формирования горной чистой структурированной воды.
Преобразователи воды от Biocera, помогут восстановить структуру вашей воды, с помощью специальных природных минералов таким образом, что она станет структурной, то есть Живой!
bio-aqua-holding.com
Чем отличаются молекулы воды
Вода – это бесцветная жидкость без запаха и вкуса. Данное вещество играет важнейшую роль в геологической истории нашей планеты и возникновении жизни, в формировании физической и химической среды, климата и погоды. Вода может находиться в одном из трех состояний: жидком, твердом (лёд) и газообразном (пар). Чем же отличаются молекулы воды в разных состояниях?

Вода – окись водорода имеет химическую формулу h3O. Она входит в состав всех живых организмов нашей планеты и составляет свыше 60% от их общей массы. Гидросфера Земли включает в себя все водоемы, океаны, моря, реки, подземные источники и почвенную влагу. Здесь вода присутствует в качестве простейшего химического соединения. В атмосфере вода находится в виде пара, тумана и облаков, капель дождя и кристаллов снега. В литосфере вода входит в состав некоторых минералов и горных пород. Переход воды из одного агрегатного состояния в другое обусловлен изменением температуры и давления.
Вода - сложное вещество, основной структурной единицей которого является молекула, состоящая из двух атомов водорода и одного атома кислорода. Спектрографические исследования показали, что молекула воды имеет строение равнобедренного треугольника, в вершине которого расположен атом кислорода, а в основаниях – атомы водорода. Угол при вершине составляет 104°27, а длина стороны — 0,096 нм. Эти параметры относятся к гипотетическому равновесному состоянию молекулы без ее колебаний и вращений.
В настоящее время существует два научных подхода к изучению структуры воды. Первый был предложен в 19 веке и получил название гидрольной теории. Согласно данной гипотезе, основной строительной единицей водяного пара является молекула h3O, называемая гидроль, или моногидроль. Основной строительной единицей воды является двойная молекула воды (h3O)2—дигидроль; лед же состоит из тройных молекул (h3O)3 — тригидроль.
Водяной пар состоит из собрания простейших молекул моногидроля и их ассоциаций, а также из незначительного количества молекул дигидроля. Вода в жидком виде представляет собой смесь молекул моногидроля, дигидроля и тригидроля. Соотношение числа этих молекул в воде различно и зависит от температуры.
Современная гипотеза строения воды основана на представлении, что лед, вода и водяной пар состоят из молекул h3O, объединенных в группы с помощью водородных связей, возникающих в результате взаимодействия атомов водорода одной молекулы с атомом кислорода соседней молекулы. Плотные водородные связи характерны для воды в замерзшем состоянии, что объясняет ее кристаллическую структуру. Повышение температуры льда до его плавления и выше приводит к разрыву водородных связей и разрушению групп молекул, вплоть до отдельных молекул, что характерно для пара.
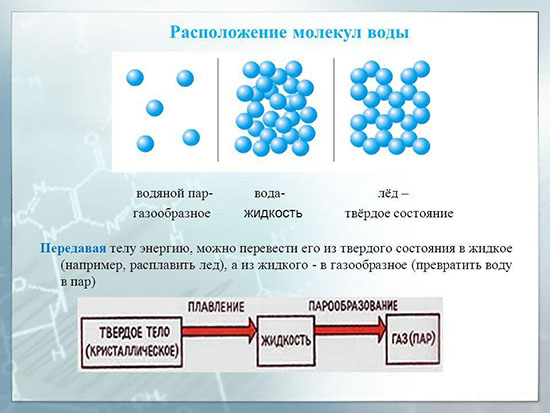
Обе гипотезы обосновывают ключевое различие в строении воды в разных состояниях – расположение молекул. Расстояния между молекулами пара в десятки раз больше размеров самих молекул, поэтому притяжение между ними очень слабое. По этой причине водяной пар не имеет собственной формы и постоянного объема. Расстояние между молекулами воды меньше, чем размер самих молекул, поэтому в жидком состоянии сохраняется объем, но изменяется форма вещества. Молекулы льда расположены в определенном порядке, что позволяет веществу сохранять форму и объем.
Выводы:
- Вода – окись водорода имеет химическую формулу h3O.
- Вода может находиться в одном из трех состояний: жидком, твердом (лёд) и газообразном (пар).
- Согласно гидрольной теории, водяной пар состоит из гидролей, непосредственно вода – из дигидролей, лёд – из тригидролей.
- Современная гипотеза строения воды основана на представлении, что лед, вода и водяной пар состоят из молекул h3O, объединенных в группы с помощью водородных связей.
- Молекулы воды идентичны во всех агрегатных состояниях.
- Разница свойств воды, пара и льда объясняется расстоянием и силой притяжения между молекулами вещества.
thedb.ru