Модель молекулы воды. Вода модель
Модели воды
Это продолжение статьи, начало - на предыдущих страницах данного раздела.
В настоящее время существуют и другие модели воды, объясняющие её аномальные свойства. Так, профессор Мартин Чаплин из Лондонского университета (Martin Chaplin Professor of Applied Science Water and Aqueous Systems Research of the London South Bank University) рассчитал и предположил иную структуру воды, в основе которой лежит икосаэдр (рис. 32).
Рис. 32. Формирование икосаэдра воды. Модель М. Чаплина.
Согласно этой модели вода состоит из 1820 молекул воды - это в два раза больше, чем в модели Зенина. Гигантский икосаэдр в свою очередь состоит из 13 более мелких структурных элементов. Причем, так же как и у Зенина, структура гигантского ассоциата базируется на более мелких образованиях.
См. ссылку: /article/learn/mathmodel.htm
В Черном море наблюдается другой интересный феномен. На глубинах в воде присутствует сероуглерод (h3S), концентрации которого настолько высоки, что ниже 120-200 метров в Чёрном море жизни почти нет. Причиной наличия таких высоких концентраций сероводорода в водах Черного моря является деятельность особых бактерий Bacterium hydrosuifureurn Penticum, Vibro sulfureus и Microspira aestuaria, способных выделять сероводород при восстановлении сульфатов, солей, растворенных в морской воде. В начале эволюции некоторые хемосинтетические бактерии использовали и энергию, полученную в результате окисления сероводорода (h3S) до серы (S).
В разные геологические эпохи сероводородные зоны занимали различную площадь. Около 3,5 — 3,7 миллиарда лет назад (самый ранний докембрий), когда атмосфера Земли содержала крайне мало кислорода, причем небиологического происхождения (образовывавшегося, например, при остывании базальтовой магмы, по гипотезе геохимика В.И. Вгатова), воды океана были полностью сероводородными. И первая жизнь в океане тоже была анаэробной. Первые живые простейшие, вероятно, мало отличались от современных нам анаэробных бактерий. Даже при отсутствии или малом количестве органического вещества, как это было в первичном океане, анаэробные бактерии могли выделять сероводород. Потом, по мере того как состав атмосферы изменялся, в ней скапливался кислород, сероводородные зоны уменьшались. Этот процесс продолжался сотни миллионов лет. Вероятно, вода Черного моря “сохранила” память о том первичном океане.
Биогенное происхождение имеет также и кислород атмосферы Земли, который образовался за счет процесса фотосинтеза зелеными растениями. Жизнь на Земле, как подтверждают данные палеогеологии, возникла в докембрийскую эпоху. Так, в научной литературе сообщалось о находках ископаемых водорослей в Южной Африке, возраст которых 2,7 млрд. лет. Обнаружены также остатки органического происхождения в южноафриканской формации Фиг-Три, возраст которой приблизительно 3,5 млрд. лет. Академик Б.С. Соколов на основе имеющихся сведений о развитии жизни на нашей планете в раннем докембрии сделал вывод, что биогенные накопления кислорода в океане начались 3,0 — 3,5 млрд. лет назад, а в атмосфере - 2 млрд. лет тому назад.
По мере того как атмосфера Земли в процессе её эволюции эволюционировала из восстановительной в окислительную, постепенно стало происходить „очищение” водной среды – гидросферы от дейтерия. По мнению Мосина, в те времена существовало два очень важных процесса. В первичной атмосфере Земли не было защитного кислородно-озонового слоя, защищающего поверхность Земли от жёсткого коротковолнового излучения Солнца. Поэтому, вследствие вулканических геотермальных и электрических процессов могло происходить обогащение гидросферы Земли дейтерием. Кроме того под действием излучения мог происходить фотолиз воды (Мосин, 1996).
На более позднем этапе вода могла очищаться от дейтерия при помощи горных пород. Большую роль в этом процессе, по-видимому, играли карстовые породы. В настоящее время содержание дейтерия в карстовых источниках равняется 30-35 г/тонна. В морской воде его содержание 130-150 г/тонна. Очевидно, что когда в воде меньше дейтерия, эволюция происходит быстрее. Если на Земле не начался бы природный процесс очищения от дейтерия, эволюция могла „застыть” на очень низком уровне.
С годами температура Земли понижалась. На определенном этапе эволюции Земли, температура воды была на10-15°C выше теперешней. А когда температура снизилась до 3,8 °C, в первую очередь замерзала тяжёлая вода. Это означает, что лед сначала встраивает в свою кристаллическую решётку атомы дейтерия (Д-р Игнатов, 2010). При этом природный лёд обычно значительно чище, чем вода, так как при кристаллизации воды в кристаллическую решётку встраиваются молекулы воды, а примеси вытесняются в жидкость. Растущий кристалл льда, тем самым, всегда стремится создать идеальную кристаллическую решетку и вытесняет посторонние вещества. В планетарном масштабе именно замечательный феномен замерзания и таяния воды играет роль гигантского очистительного процесса - вода на Земле постоянно очищает сама себя.
www.o8ode.ru
Модель - вода - Большая Энциклопедия Нефти и Газа, статья, страница 2
Модель - вода
Cтраница 2
Мы выдвигаем другое универсальное объяснение, основанное на учете структуры воды и водных растворов, в рамках двухструктур-ной модели воды. [16]
В табл. 7.1 приводятся результаты расчета методами вычислительного эксперимента фактора сжимаемости и средней од-ночастичной потенциальной энергии для двух описанных выше моделей воды. [18]
Кроме моделей воды с льдоподобным тетраэдрическим каркасом и находящимися в равновесии с ним мономерными молекулами воды, были предложены модели, в соответствии с которыми тетраэдрически связанные молекулы воды образуют рои определенных размеров. Рои отделены друг от друга пространствами, заполненными мономерными молекулами воды. [20]
Первая обстоятельная попытка подсчета величины энергии гидратации ионов принадлежит Берналу и Фаулеру. Они исходили из кристаллической модели воды, считая на основании рентгеновского анализа, что-при низких температурах вода имеет кристаллическую решетку типа кварца, а структура воды, деформированная под влиянием ионов солей, имеет тетраэдри-ческую структуру ( см. рис. 41 и 42, стр. [21]
Выше представленные данные показывают, что в настоящий момент мы располагаем достаточно точными результатами зависимости вязкости от давления и температуры Аномалии вязкости воды состоят в существовании отрицательного коэффициента в зависимости вязкость - давление и в наличии минимума в изотермах вязкости при низких температурах. Теория вязкости, которая описывала бы эти аномалии, исходя из одной какой-либо модели воды, не существует. [22]
В основе всех рассмотренных моделей лежит представление о подобии структуры жидкой воды тетраэдрической структуре льда. Однако, несмотря на то, что существование такого подобия подтверждено экспериментально [12], основанные на нем модели воды не в состоянии объяснить многих опытных данных. [24]
Были взяты два девонских песчаника длиной Ю см и диаметром 5 см с проницаемостью по воздуху 260 и 1600 мд. В качестве вытесняемой и вытесняющей жидкости была применена трапная туймазинская нефть, изовискозная нефть в пластовых условиях и модель пластовой туймазинской воды соответственно. [25]
Точно такой же раствор солей и в той же концентрации добавляли в контрольные пробы для питания аборигенных бактерий, причем концентрация солей в моделях воды была в 10 раз ниже как в контрольных пробах, так и в опыте. [26]
Для спектров HOD в области 7200 - 6200 см 1 при температурах ниже 150 С наблюдается характерная изопиестическая точка [6 - 8, 16, 17], что позволяет отнести участок 7100 см - v / 6800 CM-J к колебаниям свободных или слабосвязанных ОН-групп, а участок 6800см 1 66200 см - к колебаниям ОН-групп, участвующих в образовании водородных связей. Результаты, представленные на рис. 3.2, во-первых, свидетельствуют о смещении равновесия между свободными и связанными группами под действием температуры, а во-вторых, дают с учетом уравнения ( 1) количественную основу для построения модели воды как среды, где реализуется равновесие между ОН-группами и неподеленными электронными парами. [27]
Таким образом, для воды характерна трехмерная льдопо-добная или квазикристаллическая структура. Такие льдоподоб-ные структуры названы кластерами. В соответствии с двух-структурной моделью воды кластеры плавают в среде свободных молекул, образующих вторую структуру - плотную кубическую упаковку ( рис. VII. Обе структуры находятся между собой в равновесии. Двухструктурная модель удовлетворительно объясняет аномальные свойства воды. [29]
Во-первых, согласие результатов расчета каких-либо свойств с экспериментом не доказывает адекватность модели, поскольку такое же хорошее совпадение может быть достигнуто и с помощью другой модели, зачастую несовместимой с первой. Во-вторых, ни одна модель воды, предложенная до сих пор, не в состоянии одинаково хорошо воспроизвести все ее свойства. В-третьих, ( и это, пожалуй, главное) даже если получено прекрасное совпадение расчета по модели с экспериментом, мы не получаем новой информации, поскольку параметры модели оцениваются по экспериментальным данным и, следовательно, никакой независимой информации о V-струк-туре модель не дает. [30]
Страницы: 1 2 3
www.ngpedia.ru
Модель молекулы воды
СОСТОЯНИЕ ВОДЫ В ОРГАНИЧЕСКИХ И НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЯХ
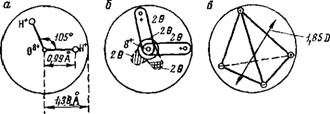
Геометрия молекулы воды в настоящее время изучена достаточно хорошо. Из десяти электронов молекулы воды два находятся вблизи атома кислорода (Is2), четыре участвуют в образовании двух о-связей с протонами, четыре несвязывающих электрона располагаются попарно на гибридных орбитах. Расстояние между ядром кислорода (центром молекулы) и протоном составляет 0,99 А, радиус молекулы (радиус электронной сферы иона кислорода) равен 1,38 А {1—5]. Угол между двумя протонами и центром близок к тетраэдрическому. Его величина в среднем составляет 105°.
В молекуле воды кроме направлений ОН (две наи^ более вытянутые орбиты) выделяют направления орбит двух неподеленных пар электронов атома кислорода (менее вытянутые орбиты), которые расположены в плоскости, перпендикулярной плоскости протонов и кислородного ядра (НОН). Имеются предположения о том, что угол между последними из указанных орбит также близок к тетраэдрическому [6, 7]. Тетраэдрическую модель молекулы воды впервые предложил Бьеррум [5]. Впоследствии она не претерпела существенных изменений, что видно из общепринятой в настоящее время плоскостной и пространственной моделей молекулы воды, которые представлены на рис. 1.
Работами Бернала и Фаулера [1, 8] было установлено, что молекулы жидкой воды, как и в структуре льда, четырежды координированы, что позволяет предположить тетраэдрический характер структуры воды. Обсуждение проблемы структуры воды было начато еще в 1933 г., однако и сейчас она еще далека от своего завершения.
Несмотря на различия в высказываниях ряда автороь по поводу структуры воды, все они сводятся к двум основным положениям: Структура воды может бЫть либо Гомогенной, либо гЕтеРогеНной Цервой точки зрёния~при Дёщкппаются ТГопл (вода--Смесь однородных, четырежДы коордИнированных молекул с иЗогнУтыми водород - Ными г-мзями^ [6], Икин [9]. Форшлинд ПО]. БолЬшее
|
Рис. 1. Модель молекулы воды А — плоскостная; б — пространственная; в — тетраэдрическое распределение двух отрицательных и двух положительных зарядов и результирующий ди - польиый момент |
Распространение получила вторая точкА зрения — Бери Нала и Фаулера Наулинга и ТЙача [11], Франка. и_ Вена [12], Иринга [13ТГ"согласно которой вода представ-
ЛяетСоБой либо полиэдрические клатраты с распределенНыми внутри них свободными молекулами, Либо льдо - подобную структуру, сОстоящую из двух форм — кварца Итдид^митя, либо, наконец, соВокупность ^ласхедши 7с]вяЗанных водородными~связями 'молеКул2_и_СВДб одных Молекул воды.
В последнее время наибольшее распространение получила идея Самойлова [14—17], согласно которой в воде сохраняется «ближнее упорядочение» льдоподобного каркаса, а часть его пустот заполняется молекулами воды, ушедшими вследствие трансляционного движения из положений равновесий, соответствующих узлам кристаллической решетки в тетраэдрической структуре. При этом в воде ближняя упорядоченность выражена сильнее, чем в других жидкостях [18—20].
Это свойство обусловлено тем, что каждая молекула воды способна образовать четыре водородные связи, геометрия которых приводит к существованию тетраэдриче - ского каркаса [21]. Ажурность каркаса позволяет предположить, что движение молекул воды происходит в основном по пустотам, что существенно не сказывается на разупорядочении ее структуры.
Представление о заполнении молекулами воды полостей льдоподобного каркаса экспериментально подтвердили Денфорд и Леви [22], которые нашли, что количество подобного рода молекул воды составляет около 20%.
Переход части молекул воды в полости структуры сопровождается разрывом водородных связей, но взаимодействие между ними и молекулами окружения сохраняется [23, 24]. Подтверждением этому является тот факт, что молекулы воды в пустотах оказываются смещенными относительно центра пустот [22]. Модель тетраэдрической структуры воды с частично заполненными пустотами была разработана позднее Михайловым и Сырникоьым [25].
Представления о структуре воды, развитые Самойловым, нашли подтверждение в результатах ряда экспериментальных работ [22, 26—28].
Существование в воде двух разновидностей молекул, одна из которых образует тетраэдрический каркас, а другая заполняет полости каркаса, представляет собой важнейшую особенность структуры воды. V
Своеобразие структуры воды с тетраэдрической координацией соседних молекул обусловлено не только существованием в ней водородной связи, обладающей резко выраженной направленностью, но и электронным строением молекулы воды.
Квантовомеханический расчет показал, что распределение электронной плотности в молекуле воды в значительной степени определяется влиянием двух пар не - поделенных электронов атома кислорода [26] и обладает тетраэдрической симметрией.
В связи с тем, что полярность связи О — Н довольно мала (дипольный момент равен 0,16 D [29]), было сделано предположение о том, что поляризация О — Н происходит в процессе образования водородной связи [30] При этом эффективный заряд на протоне молекулы воды, участвующей в водородной связи с соседними молекулами воды, оказался равным 0,16 е [22]. Это значение согласуется с величиной 0,17 е, предложенной в [5], и 0,15 е, полученной методом протонного резонанса [30]. Это означает, что практически весь наблюдаемый дипольный момент, равный 1,84 D [31], обусловлен атомным диполь - ным моментом кислорода, точнее, его неподеленной парой электронов.
Использование значения <7 = 0,16 е для расчета собственного дипольного момента водородной связи позволило оценить величину последнего. Она оказалась равной 0,83 D.
Безусловно, специфика структуры воды должна найти отражение в ее колебательном спектре, который является ценным источником информации о структуре молекул, связи их между собой.
Как показано в § 3, присутствующие в системе ионы по - разному влияют на структуру воды. В результате упоря - дочивающе-разупорядочивающего действия ионов на структуру воды при введении неэлектролита должны …
Выяснение механизма экстракции сильных кислот — одна из наиболее интересных и наиболее сложных задач теории экстракции. К сожалению, ценное для своего времени представление об оксониевом механизме экстракции таких соединений в …
Изучение взаимодействия воды с органическими и неорганическими соединениями и расчет энергии такого взаимодействия позволили с совершенно новой точки зрения рассмотреть механизм взаимодействия воды с силаноль - ными группами при ее …
msd.com.ua
Модели состояния воды - Справочник химика 21
Структура жидкой воды. Для объяснения аномальных свойств воды в жидком состоянии учеными созданы различные модели ее структуры. В основе многочисленных моделей жидкая вода рассматривается как кристаллическое вещество (жидкие кристаллы). Упорядоченное (кристаллическое) расположение частиц воды в жидком состоянии доказано экспериментально. Полагают, что прн плавлении льда его решетка частично разрушается и эти пустоты и ажурная структура льда заполняются освободившимися молекулами воды. Плотность жидкой воды вследствие этого увеличивается. Учеными подсчитано, что в жидкой фазе при 0°С несвязанные, заполняющие пустоты молекулы составляют около 16% от их общего количества. [c.9]| Рис. 4.3. Модель состояния воды в поле нона по Фрэнку. |  |
Диаграмма состояния воды имеет такой простой вид только в области не слишком высоких давлений. Начиная же примерно с 2000 бар она усложняется вследствие образования других модификаций льда. На рис. 121 изображена пространственная модель состояния воды, охватывающая давления до 10 000 бар. Кроме осей температуры и давления, в этой модели введена также третья — ось объемов. Каждое поле модели отвечает области существования одной определенной фазы, т. е. двухвариантной системе. Площадки, связывающие различные поля, отвечают равновесию между этими двумя фазами (система одновариантна). Эти площадки соответствуют линиям рис. 120 и ширина их характеризует изменение объема при данном фазовом переходе. Наибольшим объемом (наименьшей плотностью) обладает обычный лед, устойчивый при невысоких давлениях (лед /). Меньшим объемом (большей плотностью) обладает жидкая вода. Далее следует лед JII, лед II, лед V и лед VI. Так как эти модификации льда обладают большей плотностью, чем жидкая вода, то равновесию воды с каждой из них [c.332]
Указанное выше противоречие может быть объяснено с использованием формализма простейшей качественной модели жидкой воды — модели двух состояний (см., например, [187]). [c.57]
Для этого модели пластовой воды вводились в контакт при нормальной температуре и периодическом перемешивании с мелкораздробленным карбонатом кальция, приготовленным по ГОСТ 3313-46. Так как растворение связано с поглощением углекислоты из воздуха, то достижение состояния равновесия требует весьма длительного времени. Для выбранных условий эксперимента оно составляет 3,5 месяца (рис. 1) и находится в хорошем соответствии с исследованиями, проведенными в аналогичных условиях 5]. [c.92]
Указанное выше противоречие может быть объяснено с использованием формализма простейшей качественной модели жидкой воды — модели двух состояний (см., например, [187]). В работе [161] показано, что при неглубоком смещении равновесия в сторону состояния с пониженной плотностью и пониженной энтальпией есть такая область концентрации двух структур, в пределах которой увеличение второй производной объема воды соответствует уменьшению второй производной сжимаемости до нуля и меньше. На структурном уровне понижению энтальпии соответствует упрочнение водородной связи, что согласуется со спектроскопическими данными [189] и результатами машинных расчетов [166, 167]. [c.57]Попытки определения энергии водородной связи в воде были предприняты давно и небезуспешно. Однако значения, полученные различными авторами, не совпадали между собой, хотя и имели один и тот же порядок. Они находятся в интервале от 1,3 до 8,1 ккал моль [6, 52, 85, 87, 103, ИЗ—115]. Расхождение возникает,очевидно, потому, что авторы исходят из различных представлений понятия водородной связи, структурной модели воды, состояния воды, при котором производится расчет. В настоящее время наиболее достоверным, приемлемым и часто используемым значением является 4,5—5,0 ккал моль [15, 84, 116]. [c.20]
В проекции пространственной модели фазового состояния воды на плоскость р/, наиболее удобной для пользования, отражены три обширные области, в которых три фазы существуют каждая в отдельности. В таких однокомпонентных однофазных системах число степеней свободы равно двум (бивариантные системы) и для их описания должны быть известны температура и давление. Границами, разделяющими области на этой диаграмме, являются линии (следы проекций, соответствующих плоскостям объемной модели), и поэтому точкам, лежащим на них, соответствует равновесие двух фаз вода—пар (АВ), вода— лед (АО), лед — пар АС). Как уже отмечалось, для характеристики таких систем достаточно указать лишь температуру или давление, так как они имеют только одну степень свободы. [c.8]
В соответствии с современными представлениями [14, 15] ближняя гидратация однозарядных и крупных двухзарядных ионов имеет скорее кинетический, чем термодинамический характер, в связи с чем попытки точного определения числа молекул воды, занятых в гидратных оболочках, весьма затруднены. Учитьшая указанные обстоятельства и разработанную Г.А. Крестовым модель состояния ионов в растворе [3], представляется возможным в качестве первого приближения оценивать количество молей свободного растворителя по разности между общим числом молей растворителя и электролита в данном количестве раствора и числом молей растворенной соли [16]. Формула (28) может быть записана в более общем виде [c.106]
В качестве одного из исходных положений принята модель молекулы воды, также рассчитанная методом МО ЛКАО, и обладающая следующей электронной конфигурацией в исходном состоянии [c.100]К сожалению, сорбционная теория, разработка которой осуществлена известным цитологом Д. Н. Насоновым, содержит ряд неизвестных или трудно определяемых параметров, например, упорядоченность воды как функция состояния белка, растворимость тех или иных веществ как функция упорядоченности воды и т. д. Поэтому в настоящее время всеобщее признание получила мембранная теория , согласно которой транспорт обменных веществ в клетку и из клетки осуществляется особыми мембранными насосами , причем внутриклеточная вода в мембранной теории играет роль растворителя со свойствами обычной воды. Отсюда видно, что модель диффузии воды в коллагене согласуется с представлениями мембранной теории о роли воды, в то время как теория анизотропного вращения молекул воды согласуется с адсорбционной теорией. На основе сказанного экспериментальное доказательство справедливости диффузионной модели имеет принципиальное значение. [c.138]
Предложено много различных моделей состояния воды, но во всех этих моделях признается образование льдоподобной ажурной тетраэдрической структуры — каркаса, в котором молекулы воды соединены друг с другом водородными связями. В такой струкхуре каждая молекула воды в среднем окружена четырьмя другими молекулами воды. Наличие тетраэдрической структуры воды было впервые предсказано в классической работе Бернала и Фаулера и подтверждено позже рентгенографическими исследованиями. Наряду с молекулами, входящими в каркас, существуют свободные молекулы воды, не связанные водородными мостиками. Эти молекулы частично заполняют области неплотной упаковки внутри структуры воды, перемещаясь в них. В результате теплового движения между молекулами каркаса и свободными молекулами происходит постоянный тепловой обмен. Понижение температуры приводит к уменьшению числа свободных молекул, т. е. к упрочнению, или иначе, к стабилизации структуры воды. Повышение температуры дает обратный эффект — уменьшается число молекул, входящих в каркас, и тетраэдрическая структура воды ослабляется. [c.406]
В связи с приведенными термодинамическими результатами следует заметить, что на любой гидрофильной поверхности молекулы воды адсорбируются локализованно. Постулируемая в работе [98] нелокализованная модель адсорбции воды в межслоевых промежутках монтмориллонита объясняется [85] некорректностью использования обычного термодинамического подхода для анализа состояния связанной набухающими сорбентами воды. [c.37]
Полинг считал, что клатратные клетки в структуре воды также представляют собой пентагональные додекаэдры [И], однако рентгепоструктурные исследования не подтвердили этих предположений. Данные рентгеноструктурпых изменений жидкой воды скорее согласуются со структурой, предложенной для объяснения свойств воды О. Я. Самойловым [18]. В структуре модели жидкой воды О. Я. Самойлова предполагается, что равновесная взаимная ориентация молекул воды, связанных водородными связями, существующая в структуре льда I, при плавлении частично разрушается. Молекулы воды, обладающие избытком энергии, при этом мигрируют в полости льдоподобной структуры, заполняя в ней около 50% объема всех пустот. Стесненность движения этих молекул в пустотах деформированной льдоподобной структуры отличает его от движения изолированных молекул в газообразном состоянии. Близкие представления развиваются также в работе Грётхейма и Крог-Му [19]. Г. А. Крестов [2] считает, что модель О. Я. Самойлова наиболее близко отражает реальную структуру жидкой воды. [c.11]
В последние годы становится все более популярной идея о существенной роли димерных молекул в формировании структуры жидкой воды. Так, Викке [26] считает, что димерные молекулы воды являются третьим состоянием воды. Количество таких димеров с повышением температуры растет за счет разрушения тетраэдрических Н-связей, что, возможно, и является причиной увеличения растворяющей способности воды с ростом температуры [27]. Идею о существовании димеров в равновесии с водой, тет-раэдрически связанной в структурные образования, использует и Ю. В. Гуриков [25]. Сложность его двухструктурной модели, однако, едва ли делает ее более совершенной, чем модели О. Я. Самойлова и Фрэнка и Вина, а экспериментальных прямых доказательств эта теория, как и другие, по существу не имеет. [c.14]
Большой практический интерес вызывают модели качества воды в реках. Предложенная в [Цхай, 1995] модель воспроизводит пространственное распределение, содержания в реке двадцати видов химических показателей (БПК5, взвешенные вещества, нефтепродукты, фенолы, железо, фосфаты и др.). Уравнения модели представляют собой вариант одномерной системы для установившегося неравномерного движения воды с учетом боковой приточности в непризматическом русле реки. Задача прогноза решается для восемнадцати периодов в течение расчетного года для паводка (апрель-июнь) — ежедекадно, для остального времени — ежемесячно. Решение уравнений модели осуществляется численно модифицированным методом прогонки с организацией нескольких итерационных процессов. В указанной работе предложена также технология построения математических моделей биогеохимического цикла азота и фосфора, которые могут быть использованы для оценки и прогноза состояния экосистемы водоема. Модели ориентированы на стандартную входную информацию, получаемую от Государственной службы наблюдения. [c.291]
Двоякое поведение жидкой воды следует также из большого числа других экспериментальных данных. Так, зависимость плотности воды от температуры и понижение температуры максимальной плотности жидкости с возрастанием давления можно хорошо объяснить, если учесть возможность самоперехода объемной структуры воды в более плотную форму. Таким же образом вызываемые давлением разрушения объемной структуры с образованием в жидкости менее плотных компонентов можно объяснить влиянием температуры на вязкость воды, находящейся под высоким давлением [33]. Данные по поглощению ультразвука водой также согласуются с развитыми представлениями о пребывании воды в виде двух отличающихся по состоянию жидкостей. Минимум, наблюдаемый при 55° на кривой поляризуемость электрона — температура, объясняется термическим разрушением структурных пустот и степенью заполнения этих пустот ближайшими молекулами воды [35]. Кроме этого, близкие значения энергии активации диэлектрической релаксации, ламинарного потока и самодиффузии (4,6 ккал/люль) также позволяют предположить, что лимитирующей стадией для всех этих процессов является разрушение структуры [36]. Количественная обработка такого двойственного поведения воды дает возможность определить степень разрушения водородных связей, которая меняется в зависимости от выбранной модели от 0,1 до 70% при 0° [37]. Очевидно, эти величины относятся к различным моделям или к различным степеням разрушения водородных связей. Как следует из данных по дисперсии рентгеновских лучей, многие физические свойства воды, которые свидетельствуют о ее существовании в двух жидких состояниях, можно объяснить, используя существенно отличающиеся друг от друга модели [29, 38]. Следовательно, точное определение природы менее связанного плотного состояния воды представляет значительную трудность, [c.15]
Наиболее подробным и отвечающим современному состоянию проблемы является обзор О. Я. Самойлова и Т. А. Носовой [14]. Вместе с цитированной выше статьей Г. Френка [11] он дает объективную картину довольно сложного состояния вопроса об однозначном выборе модели строения воды и водных растворов электролитов. По нашему мнению, наиболее аргументирована в настоящее время экспериментальными фактами модель, впервые предложенная [c.27]
По крайней мере со времен Рентгена [301] выдвигались гипотезы о структуре жидкой воды. Попытки проверить или отвергнуть эти гипотезы затруднялись отсутствием общей теории жидкого состояния воды. По этой же причине теории о структуре воды основывались на двух подходах, ни один нз которых не был достаточно строгим. Первый подход состоял в формулировке модели жидкой воды, трактовке модели некоторым способом, обычно требовавшем большого количества допущений, с помощью методов статистической механики, и сравнении теоретических значений микроскопических свойств с экспериментальными величинами. Совпадение теоретических величин с опытными данными рассматривалось как показатель соответствия модели действительности (см. раздел 5). Второй подход, принятый в этой главе, состоит в установлении аспектов структуры жидкости на основе макроскопических свойств воды. Свойства воды исследованы настолько широко и детально, что даже если какое-либо из них и может быть связано только качественным или полуколичествепным образом с некоторой особенностью жидкой структуры, приемлемая картина воды создается только при рассмотрении многих ее свойств. [c.154]
Все предложенные различными исследователями модели структуры воды в жидком состоянии должны отвечать результатам измерений малоуглового рассеяния рентгеновских лучей и медленных нейтронов в воде, согласовываться с результатами, полученными другими методами исследования, и объяснять не только физические свойства воды (плотность, вязкость, диэлектрическую проницаемость и др.), но и ее растворяющую способность. К таким моделям относятся различные варианты кластерных структур, предложенные Немети и Шерага [3], Френком И Веном [4] и другими, модель льдоподобных пустот Самойлову [5], а также модели, учитывающие аналогию между составом тазогидратов и клатратов ряда органических молекул в вод-/йых растворах. [c.9]
В терминах простой модели адсорбированной воды [8] вода, находящаяся в окружении В (псевдообъемная вода), первой удаляется из пор в ходе дегидратации. При этом в порах остается вода в двух связанных состояниях А1 и Аг (или в комбинированном состоянии А). Предполагается, что комбинированное состояние А охватывает два слоя воды и что оно не зависит от величины диаметра пор пористого стекла (см. табл. 2 в работе [8]). [c.321]
Вполне логичное объяснение упрочнения структуры воды при добавках к ней спиртов дано О. Я. Самойловым [443] на основе предложенной им модели структуры воды (см. подробнее гл. И), в которой ближняя упорядоченность может быть охарактеризована как нарушенный тепловым движением льдоподобный каркас, пустоты которого частично заполнены перемещающимися по ним молекулами воды. М. Н. Буслаева и О. Я- Самойлов [443] объясняют появление экстремума на кривых зависимости теплот смешения от состава системы НгО—СН3ОН максимальной стабилизацией структуры воды в этой зоне. Такая стабилизация, по их мнению, наступает, когда все пустоты в ажурной структуре воды заполнены молекулами спирта. В таком состоянии молекулы СН,,ОН связаны с водой наиболее прочно, и смешанный растворитель представляет собою еди- [c.256]
При рассмотрении строения молекулы аммиака было обращено внимание на то, что угол HNH равный 107°, очень близок к тетраэдрическому углу 109 28. Это дало повод считать участие неразделенной пары электронов у атома азота молекулы Nh4 в формировании трех связей N—Н иначе говоря, в формировании связей участвуют 5-электроны в гибридных состояниях. Таким образом, геометрическую модель молекулы аммиака следует считать тетраэдрической при наличии одной неразделенной пары электронов в одной из вершин тетраэдра. Модель молекулы воды также следует считать тетраэдрической (в двух вершинах тетраэдра расп0.[10жены две неразделенные пары электронов). Некоторым подтверждением сказанному может служить сопоставление углов между связями у изоэлектронных молекул СН4, Nh4 и Н2О НСН= 109 28, HNH= 107°47, НОН= 104°31. [c.77]
Вопрос о справедливости той или иной модели движения воды в коллагене имеет принципиальное значение, поскольку его решение связано с важными особенностями биологической роли воды, как отмечено в предисловии к настоящей главе. В частности, основные функции живого — мембранная проницаемость, молекулярная и ионная селективность клеток, мускульная активность, проводимость нервных импульсов и другие — по одной из гипотез ( адсорбционная теория ) определяются наличием особого, упорядоченного или структурированного состояния во всей гидратной оболочке белка. Согласно этой теории, вся или почти вся внутриклеточная вода связана или структурирована и растворимость данного вещества в ней является функцией степени структурной организации гидратной оболочки белка. В свою очередь, степень структурной организации водпо11 оболочки зависит от состояния самой белковой молекулы. Изменение состояния белка иод влиянием внешнего воздействия (например, нервного импульса) приводит в описываемой модели к очень сложной последовательности химических ре- [c.137]
В терминах диаграммы переходного состояния (рис. 18) энтропию активации можно рассматривать как меру ширины участка энергетической седловины, через которую реагирующие молекулы переходят при достижении активированного состояния. Энтальпия активации является мерой высоты энергетического барьера, который должны преодолеть реагирующие молекулы, в то время как энтропия активации является мерой того, сколько молекул, достигших этой энергии, фактически реагируют. Энтропия активации отра-я ает стерические и ориентационные требования, энтропию разбавления, концентрационные эффекты (зависящие от выбора некоторого стандартного состояния, в котором выражаются равновесные константы и константы скорости) и эффекты растворителя. При эквивалентности остальных особенностей мономолекз лярные реакции будут иметь энтронии активации, близкие к нулю, поскольку для таких реакций обычно не существует концентрационных или ориентационных требований. Бимолекулярные реакции, которые описываются константами скоростей с размерностями, содержащими л/моль, будут иметь отрицательную энтропию активации в результате объединения двух молекул реагентов, находящихся в концентрациях 1 моль/л, в активированный комплекс и, вероятно, должны иметь еще большие отрицательные энтропии в результате стерических и ориентационных требований, включающих потерю поступательных и вращательных степеней свободы в переходном состоянии. Энтропия равновесной гидратации альдегида, которую можно рассматривать как модель взаимодействия воды и карбонильного соединения с образованием переходного состояния, составляет около —18 энтр. ед. (—75,6 Д/к/моль-К). Это заметно более отрицательная величина, чем энтропия, равная —8 энтр. ед. (—31,6 Дж/моль-К), которая требовалась бы для ассоциации молекул реагента в стандартном молярном растворе. [c.448]
В настоящее время предложены различные модели структуры воды, которые можно разбить на две большие группы структурно однородные и структурно неоднородные (в смысле ближней упорядоченности). Последние, по Гурикову [225 стр. 5], подразделяются на мозаичные модели и модели двух состояний. [c.162]
Океан служит областью седиментации карбонатов. В осадках развивается микрофлора донных отложений, образующая восстановленные газы (газогенерирующий этап), прежде всего НзЗ с доминированием сульфатредукции как заключительного этапа анаэробной деградации мортмассы и развитием на поверхности ила организмов, окисляющих соединения серы (сообщество сульфуреты), и даже придонные воды обычно оксигенированы. Благодаря высокому слою оксигенированной воды донные выделения из океана не достигают поверхности, даже в случае Черного моря - модели состояния древнего стратифицированного океана. Особый случай представляет локальное просачивание метана, наподобие грязевого вулканизма на суше (холодные метановые сипы ). Источником этого метана, помимо деятельности метаногенов, может служить разложение газогидратов метана. На дне океана в области спрединга на выходе эндогенных газов, образующихся при контакте морской воды с перегретыми породами базальтов океанической коры, развиваются особые микробные сообщества подводных гидротерм (термальные глубоководные оазисы ), в которых продукция органического вещества осуществляется за счет хемосинтеза и окисления газов кислородом фотосинтетического происхождения, приносимого в глубину холодными океаническими водами. [c.104]
Д. Поланд и Г. Шерага [46, 47] предприняли попытку построить количественную теорию гидрофобных взаимодействий, основанную на трактовке У. Козмана и разработанных Г. Немети и Г. Шерагой [44, 48, 49] моделях структуры воды. Г. Немети и Г. Шерагой в 1962 г. была предложена статистическая модель воды, учитывающая пять ее состояний без водородных связей, с одной, двумя, тремя и четырьмя водородными связями. Введение гидрофобной молекулы увеличивает координационное число льдоподобной структуры (четыре водородные связи) и, следовательно, понижает энергию молекулы. Энергия остальных четырех состояний, напротив, повышается предположительно на одну и ту же величину. В результате из полуэмпирического выражения статистической суммы рассчитываются ДО, АНиАЗ, отвечающие контактам любых пар неполярных боковых групп белковой молекулы. Найденные значения для разных групп при 25° варьируют для АС от -0,2 до -0,5 ккал/моль, АН - от 0,4 до 1,8 ккал/моль и Д8 - от 1,7 до 10 кал/(моль град). Эти количественные оценки согласуются с качественными представлениями, но не более того. Сама структурная теория воды, основанная на модели смеси четко различающихся видов структур, не согласуется с рядом спектроскопических данных, 240 [c.240]
С этой целью па основе разработанной Г. А. Крестовым [9, 15] модели состояния ионов в растворе и экспериментальных данных по растворимости благородных газов в воде различной степени дейтернро-ванности [16] были вычислены изменения энтропии воды и [c.77]
chem21.info