Большая Энциклопедия Нефти и Газа. Вода борная
Чудо целитель вода Мазнев Н. И.
Золото является одним из старейших медикаментов в истории человечества. Целители, назначали препараты с содержанием золота своим пациентам на протяжении тысячелетий из-за обеззараживающего свойства губительно действующего на болезнетворные микробы. Препараты из золота обладают множеством других лечебных свойств. Древние лекари рекомендовали употреблять золотую воду при болезни сердца, связанной с нарушением ритма (аритмии, ишемической болезни, стенокардии). В конце XIX века золото также прописывалось для лечения сифилиса и туберкулеза. С 20-х годов прошлого века повязки с содержанием золота использовались при лечении ревматических заболеваний.
Золотые украшения благотворно действуют на нервную систему и психику. Золотая цепочка на шее ребенка будет успокаивать его, золотое кольцо, носимое на мизинце левой руки женщиной и правой руки мужчиной, активизирует работу сердца, а на среднем пальце — укрепляет иммунную систему. И сегодня золото используется при лечении ревматизма, а чаще всего — в гомеопатии, как средство от депрессий, фобий и хронической усталости.
Практика показала, что золотая вода облегчает приступы эпилепсии и истерии, улучшает память и интеллект. Хорошие результаты получены также при лечении и профилактике варикозного расширения вен, возбуждении центральной нервной системы. Препараты с содержанием золота в малых дозах оказывают регулирующее влияние на иммунную систему человека.
Для получения лечебного средства из золота налить в эмалированную кастрюлю пол-литра отфильтрованной воды, положить туда несколько золотых украшений высокой пробы (без камней), поставить кастрюлю на огонь и греть до тех пор, пока не выкипит половина всего объема воды.
1 При ослабленной памяти или угнетенном психическом j состоянии пить золотую воду по 1 ч. л. за 30 мин до еды 3 раза в день. Курс лечения не больше 1 недели (в зависимости от самочувствия), потому что золотая вода является сильным тонизирующим средством. Перерыв между курсами лечения— 1 месяц. Специалисты утверждают, что золотое украшение должно принадлежать именно тому человеку, для которого приготавливают лечебную воду. ; Для разглаживания морщин и придания коже лица \ свежести делать компрессы на лицо (на 10-15 мин 2 раза i в неделю) из ткани, смоченной в золотой воде. Экстракт | золота препятствует потере коллагена и эластина и под-I держивает эластичность и упругость кожи.
Кремниевая вода
Специалисты-медики напрямую связывают такие заболевания, как сахарный диабет, проказа, гепатит, гипертония, дизентерия, катаракта, артриты, язва желудка, рак и ревматизм или с пониженным содержанием кремния в крови, тканях и органах человека, или же с нарушением обмена соединений кремния. В результате контакта воды с кремнием она очищается от болезнетворных микробов и многих химических соединений. Замечено, что в помещении, где стоит банка с кремниевой водой, очищается воздух. Активированная присутствием
92 ? Я. -УС. Мунев кремния вода улучшает самочувствие, нормализует обмен ве- i ществ, повышает сопротивляемость организма. Кремниевая вода:
— помогает при расстройствах желудка и кишечника;
— уменьшает содержание сахара в крови у диабетиков;
— улучшает деятельность почек и печени;
— помогает при желчнокаменной и почечно-каменной i болезнях;
— останавливает кровотечения, в том числе и при кровоточивости десен; — помогает при кожных болезнях;
— действует тонизирующе на кожные ранки;
— успокаивает зубную боль,
— уничтожает вирус гриппа;
— лечит ангины и насморк;
— помогает в лечении туберкулеза и атеросклероза;
— способствует росту волос (смачивать волосы и массировать кожу головы).
| При пародонтозе полоскание рта и массирование десен \ кремниевой водой в течение 5-6 дней значительно улуч-j шает, а при длительном применении даже полностью | излечивает от этой болезни.
Приготовление кремниевой воды
Несколько небольших кусочков кремния положить на дно банки из прозрачного стекла, залить обычной водой и настаивать от 2 до 6 суток (не на солнце и не в темноте) при открытой крышке банки и температуре не ниже 4 °С. Полученную воду* можно разлить в бутылки, закупорить и хранить продолжительное время, она сохраняет приобретенные свойства и не портится. Специалисты утверждают, что кремний может легко» заменить любой домашний фильтр. Камешек величиной в один кубический сантиметр может очистить 1 литр воды. Кремниевые камешки можно использовать продолжительное; время, если каждый раз перед применением промывать их; проточной водой. Однако для получения кремниевой во; подходят не всякие кремни. Для этой цели необходим толы кремний сероватого или темного оттенка. Но не красно-ке* ричневый, в котором могут содержаться примеси вредных (му| тагенных) для организма металлов — бериллия, свинца. Кремний продается также под названием «опал халцедоновый» — живой камень.
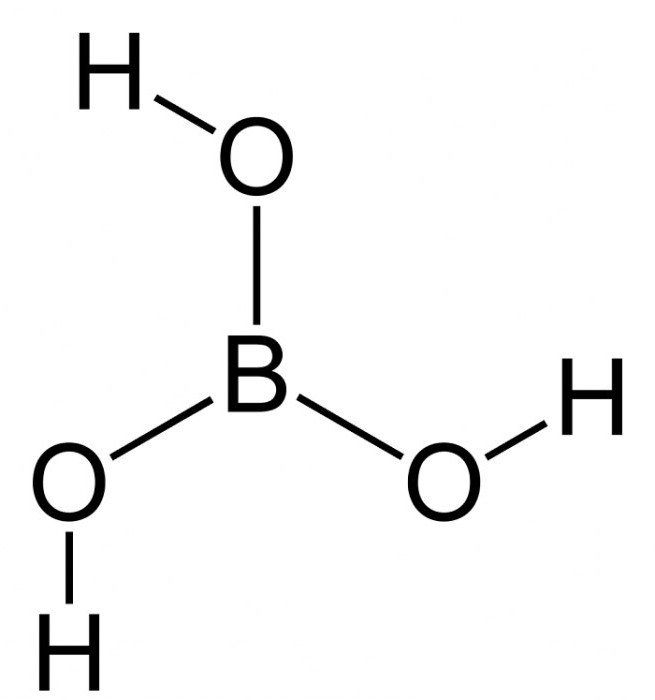
Борная вода
Борную воду получают из борной кислоты, которая легко растворяется в воде. Растворимость борной кислоты в 100 мл воды: 1,95 г при 0 'С и 39,1 г при 100 °С. В минеральных кислотах растворяется хуже, чем в воде, а в растворах солей лучше. В природе борная кислота встречается в виде минерала сассоли-на, а также в термальных водах и природных рассолах, из которых ее экстрагируют спиртами или смесью полиолов. Срок хранения борной кислоты — 2 года со дня изготовления.
Борная вода — это 2-4%-й водный раствор борной кислоты (1 ч. л. борной кислоты на стакан воды). Применяется наружно для полосканий рта, зева и для промывания глаз, компрессов на веки, подглазные «мешки», используется при кровотечениях из уха, а также в косметических целях.
| Стягивающая маска для лица: взбить в крепкую пену I яичный белок, добавить 3 чайные ложки борной водыина-! нести на лицо на 20 минут.
Чтобы улучшить состояние кожи косметологи рекомендуют после традиционного утреннего умывания или даже вместо него протирать лицо и шею тонизирующим раствором. Это может быть борная вода (приготовленная из расчета: 2 г борной кислоты на 100 мл кипяченой воды), укропная вода, айвовая вода или огуречный сок. Лицо полезно протирать и укропным лосьоном. Для его приготовления смешать настой укропа с глицерином, 2%-й борной водой, одеколоном или спиртом в соотношении 6:1:7:6. Протирать нужно ватнымтампоном, обильно смоченным подготовленной жидкостью, очень осторожными движениями: лицо — от середины лба к уху, от кончика носа и середины подбородка в стороны, а шею — вниз и в стороны. После обтирания рекомендуется нанести крем.
Одновременно с маской, наносимой на лицо, рекомендуется делать и глазные примочки, которые оказывают на глаза прекрасное успокаивающее действие. Два кусочка ваты намочить в борной воде для глаз, и приложить к глазам на 20 минут.
Затем на кожу вокруг глаз поколачивающими движениями подушечек пальцев нанести жирный, питательный или витаминизированный крем или же туалетное молоко; при этом необходимо следить за тем, чтобы ни крем, ни туалетное молочко не попадали в глаза.
При покраснении и раздражении век имеется самое простое средство: примочки из чуть теплой борной воды. Примочки накладывают на закрытые глаза, лежа на высокой подушке. Затем после остывания примочки следует повторно намочить в теплом растворе, повторив 2-3 раза.
) Также полезно промывать глаза. Промывания глаз снимает усталость, ощущение рези, устраняет и другие неприят-
\ ные явления. Для промывания глаз можно использовать
| чистую воду, лучше кипяченую, комнатной температуры с различными добавками, например: 1 чайная ложка борной
I кислоты на 1 стакан кипяченой воды.
I Борную воду закапывают в ухо при его воспалении, экзе-
\ ме слухового прохода.
Началом эпохи антисептики в хирургии считается 1865 год, когда английский хирург Джозеф Листер опубликовал в журнале «Ланцет» статью о новом методе обработки хирургических ран с помощью карболовой кислоты (в просторечии — карболка). Карболка эффективно убивала микробы, но обладала множеством недостатков, худшим из которых была ее ядовитость. Вскоре за этим событием французский химик Жан Батист Дюма обнаружил антисептические свойства у борной кислоты, которая не раздражала раны, не пачкала белье, не пахла дурно, как карболка, даже вкуса не имела. По этой причине многие из известных в то время «домашних» и клинических антисептиков, как перекись водорода, марганцовка и карболка, стали все чаще и чаще заменять борной кислотой. Однако токсикологи доказали, что микроэлемент бор относится к группе так называемых общеклеточных ядов. Только высокая стабильность борной кислоты в организме человека делает ее относительно безвредной. Но небольшое количество борной кислоты все же расщепляется. При остром отравлении людей она поражает мозг, слизистые оболочки и кожу, а при хроническом — кроветворные и половые клетки. Особенно опасна борная кислота для развивающихся эмбрионов. Даже поступление однократной нетоксической дозы в организм матери может вызвать патологические изменения плода. Отравления наблюдались в результате самых, казалось бы, невинных действий родителей и врачей: обтирания сосков матери раствором кислоты перед кормлением, присыпания мокнущих поверхностей кожи, обработки слизистой рта. Смертельная доза борной кислоты для взрослого — 5—20 граммов. Большой разброс мнений получается из-за того, что кислота выделяется через почки в неизменном виде. Хорошо они работают — отравление переносится легко, плохо — спасти от него крайне трудно. У детей имеется относительная недоразвитость почечных функций — это чисто физиологическая закономерность. И чем ребенок младше, тем эта недоразвитость выражена сильнее. Из этого следует, что борная кислота опасней всего для новорожденных, а с возрастом риск отравления постепенно снижается. Поэтому применение борной кислоты для лечения новорожденных больше приносит вреда, нежели пользы. Для грудных детей она может использоваться лишь в стационаре при обязательном контроле за ее содержанием в крови. При больных почках борную кислоту нельзя давать ни детям, ни взрослым. Для детей старше года возможно употребление борной кислоты в виде растворов и мазей, но с учетом того, чтобы общая доза, независимо от длительности применения, не превышала двух граммов. Например, в одной капле ее 2%-го раствора содержится один миллиграмм вещества. По две капли в оба глаза пять раз в день — 20 мг, а за 10 дней лечения организм ребенка получает токсическую дозу.
продолжениеwww.coolreferat.com
Борная кислота для растений применение
Борная кислота для растений применение. Применение борной кислоты в саду и на огороде. Аптечная борная кислота на приусадебной участке.
Польза борной кислоты для сада и огорода огромна и разнообразна. Борную кислоту можно использовать практически на любой почве, особенно она необходима на почвах с повышенной кислотностью. Бор помогает увеличивать число завязей, помогает росту растений, увеличивает количество сахара и повышает качества вкуса плодов.
Но переизбыток бора может и навредить. Различные садовые культуры нуждаются в боре в разных количествах. Наибольшая потребность в борной кислоте у плодовых деревьев, капусты и свеклы. Менее требовательны к бору: морковь, томаты, салаты и все косточковые культуры. Наименьшая потребность в борной кислоте у картофеля, бобовых и клубники.
Как приготовить раствор борной кислоты. Нужно учитывать, что борная кислота легко растворяется только в горячей воде. Поэтому сначала разводим необходимое количество порошка в 1 литре горячей воды, а затем добавляем нужное количество воды комнатной температуры.
Какие признаки нехватки бора у растений:
- у яблони и груши: листья утолщаются, коробятся, происходит опробковение и потемнение жилок; при остром голодании листья опадают. Наблюдается розеточность листьев – мелкие листья на концах побегов собраны в виде розетки. В запущенных случаях у деревьев отмирают верхушки.
- у земляники (клубники): искривление листьев и некроз краев.
- у винограда: появление хлоротичных пятен между жилками листовых пластинок, которые постепенно разрастаются, отсутствие нормальных завязей на кистях (измельчение). Новый саженец погибает в течение года или через 1–2 года после высадки на постоянное место.
- у томатов: почернение и отмирание точки роста стебля, бурный рост новых побегов от корня, при этом черешки молодых листьев становятся очень ломкими. На плодах, обычно в области вершинки, образуются бурые пятна отмершей ткани.
- у картофеля: заболевание грибной паршой, общая задержка развития. Угнетается точка роста, что сопровождается пожелтением листьев, черешки краснеют, становятся ломкими.
- у свеклы: загнивает сердечко корнеплода, что вызвано грибным заболеванием – фомозом. На листьях образуются концентрические светло-бурые пятна с черными точками в центре, затем болезнь переходит на корнеплод, загнивает его сердцевина. Ткани на разрезе на начальном этапе имеют темно-коричневый, почти черный цвет, в дальнейшем усыхают, становятся пожухлыми, трухлявыми.
Используя борную кислоту в саду и на огороде, необходимо применять её правильно и соблюдая дозировку.
Вот некоторые советы по применению борной кислоты на дачных участках:
Борная кислота для растений:
- Для стимуляции прорастания семян используют следующий раствор: 0,2 гр борной кислоты разводят в 1 литре воды. Семена свеклы, моркови, лука и томатов замачивают на сутки, а семена тыквы, капусты, огурцов, кабачков – на 12 часов.
- Для подготовки почвы к посеву и посадке используют следующий раствор: 0,2 гр борной кислоты разводят в 1 литре воды. Почву поливают данным раствором перед посевом семян или высадкой рассады, расходуя ведро раствора на 10 м2.
- Для внекорневой подкормки (опрыскивания) приготавливают следующий раствор: 0,1 гр борной кислоты разводят в 1 литре воды. Проводят три опрыскивания (во время бутонизации, цветения и в период плодоношения растений). Проводить лучше в пасмурную погоду или под вечер, чтобы избежать солнечного ожога. При использовании с другими микроэлементами концентрацию борной кислоты снижают до 0,05–0,06 гр на 1 литр воды.
- Для корневой подкормки приготавливают следующий раствор: 0,1–0,2 гр борной кислоты разводят в 1 литре воды. Чтобы корням растений не нести химического ожога, растения предварительно поливают обычной водой. Подкормка проводится если бора в почве недостаточно.
- Для увеличения урожайности клубники. Для стимуляции роста ранней весной клубнику (землянику) проливаем раствором борной кислоты с добавлением марганцовокислого калия (1 гр марганцовки и 1 гр борной кислоты разводим в 10 литрах воды). Затем перед цветением проводим внекорневую подкормку следующим раствором (2 гр борной кислоты, 2 гр марганца, 1 стакан просеянной золы разводим в 10 литрах воды).
- Для улучшения плодоношения деревьев проводим внекорневые подкормки следующим раствором: 10–20 гр борной кислоты разводим в 10 литрах воды. Первоначально опрыскиваем всю доступную крону – в начале появления бутонов, через неделю опрыскивание повторяем. Проводить лучше в пасмурную погоду или под вечер, чтобы избежать солнечного ожога. Такая обработка сокращает количество опавших завязей, увеличивает устойчивость деревьев к неблагоприятным условиям, повышает лежкость плодов.
- Для повышения урожайности винограда проводим обработку в период бутонизации следующим раствором: к борной кислоте добавляем соли цинка (в 10 литрах воды разводим 5 гр борной кислоты и 5 гр сернокислого цинка) — это помогает сохранению цветков и уменьшению осыпания завязей. А появление качественных цветков у винограда помогает избежать проблемы горошения винограда (измельчение ягод).
- Для повышения урожайности томатов первоначально замачиваем семена перед посевом в борном растворе, затем раствором борной кислоты проливаем грядки для высадки рассады. А перед началом цветения кусты помидоров опрыскиваем следующим раствором: в 10 литрах воды разводим 10 гр борной кислоты. Во время жары в теплице помидоры освежаем опрыскиванием следующим раствором: 2 гр борной кислоты разводим в 10 литрах воды.
- Для снижения нехватки бора для картофеля (при профилактике заболевания паршой). Первоначально опрыскиваем клубни картофеля при яровизации следующим раствором: 10–15 гр борной кислоты разводим в 10 литрах воды и расходуем примерно 50 мл на 1 кг клубней. Затем проводим подкормку кустов картофеля следующим раствором: 6 гр борной кислоты разводим в 10 литрах воды и расходуем на 10 м2 посадок. Бор лучше использовать в сочетании с другими удобрениями (фосфором), а при их отсутствии можно использовать золу. В 1 кг золы содержится от 200 до 700 мг бора.
- Для получения здоровой и вкусной свеклы (для профилактики фомоза у свеклы) перед посадкой выдерживаем семена 10–12 часов в 0,1%-ном растворе борной кислоты. В стадии 4–5 листьев проводим одну внекорневую подкормку следующим раствором: 5 гр борной кислоты разводим в 10 литрах воды.
- Для увеличения завязей огурцов, баклажан, кабачков и перцев, опрыскивание растений следующим раствором: 2 гр борной кислоты разводим в 10 литрах воды. Данный раствор используем так же при загнивании плодов данных плодов.
Борная кислота для борьбы с муравьями и другими насекомыми:
Борная кислота эффективна против муравьев, тараканов и других насекомых. С помощью борной кислоты готовят различные приманки, которые выкладывают в местах наибольшего скопления вредителей, но недоступных для домашних животных.
Вот некоторые варианты приманок из борной кислоты:
- Рассыпать порошок борной кислоты в тех массовых местах где бывают муравьи — самый простой вариант, но менее эффективный.
- В полстакана горячей воды насыпать 5 гр борной кислоты, растворить, добавить к раствору чайную ложку меда и 2 стол. ложки сахара. Все перемешать, а полученную смесь вылить в плоскую посуду, которую лучше разместить вблизи муравьиных троп.
- 2 яичных желтка растереть с 0,5 чайн. лож. борной кислоты. Из полученной массы сделать маленькие горошинки и разложить в проблемных местах.
- 1 стол. ложку воды смешать с 2 сто. ложками глицерина, добавить 1 чайн. ложку меда, 0,5 чайн. ложки борной кислоты и 1,5 стол. ложки сахара. Все перемешать, скатать маленькие шарики-приманки. Этот рецепт хорош тем, что приманка долго остается влажной и мягкой.
- 3 очищенных средних отваренных в мундире картофелины, 3 вареных желтка,10 гр борной кислоты, 1 чайн. ложка сахара. Все перетереть и тщательно перемешать, скатать шарики-приманки.
Пользуйтесь полезными советами про борную кислоту.
Как можно обойтись без химии с помощью других простых подручных средств читайте здесь: Сад и огород без химии.
Удачи вам!
(Visited 13 707 times, 8 visits today)
zagorod1.ru
Растворимость - борная кислота - Большая Энциклопедия Нефти и Газа, статья, страница 1
Растворимость - борная кислота
Cтраница 1
Растворимость борной кислоты при 0 - 2 г в 100 мл дистиллированной воды; при 20 - 5 г и при 100 - 40 г. Для получения перекристаллизованной борной кислоты в достаточном для приготовления стандартного раствора количестве следует отвесить на технических весах 10 - 12 г борной кислоты, растворить при нагревании и постоянном помешивании в 100 мл дистиллированной воды. [1]
Растворимость борной кислоты Н3ВО3 в воде при 13 С равна 38 5 г на I л раствора и 49 1 г на 20 С. [2]
Растворимость борной кислоты Н3ВО3 в воде при 13 С равна 38 5 г в 1 л раствора и 49 1 г при 20 С. [3]
Растворимость борной кислоты в присутствии моно-кальцийфосфата изучена в пределах концентраций СаО от 0 до 4.4 % в растворе; Н3В03 во всех пробах была в твердой фазе. Полученные результаты приведены в таблице. [4]
Растворимость борной кислоты Н3ВО3 в воде при 13 С равна 38 5 г в 1 л раствора и 49 1 г при 20 С. [5]
Увеличение растворимости борной кислоты с повышением тем-пературы до 25 свидетельствует о том, что наиболее благоприятными условиями для получения растворов, богатых содержанием борной кислоты, будут являться более высокие температуры. [6]
Данных о растворимости борной кислоты в присутствии фосфатов магния в литературе пет. [7]
Так как растворимость борной кислоты с повышением температуры сильно повышается ( при 0 С-1947 г, при 20 С - 39 92 г, при 102 С - насыщенный раствор - 291 2 г в 1 л), то при охлаждении она выделяется в виде характерных кристаллов. [8]
Снижение концентрации сульфата магния увеличивает растворимость борной кислоты и содержание ее в маточнике, а повышение концентрации MgSO4 снижает растворимость борной кислоты. Очистку борной кислоты производят перекристаллизацией из воды при 85 - 90J в присутствии активированного угля. Технический и экономический интерес представляет процесс возгонки борной кислоты при помощи пара. Для этого пульпу из боратовой руды и серной кислоты нагревают в печах в присутствии водяного пара при 400 - 500 - при этом борная кислота возгоняется и возгон конденсируется при охлаждении в чистом виде, не требуя перекристаллизации. [9]
Выделение борной кислоты из раствора основано на различной растворимости борной кислоты и сернокислого магния при различных температурах: растворимость борной кислоты резко повышается с повышением температуры, а растворимость сернокислого магния повышается мало. [11]
Сопоставляя полученные изотермы для 0, 15 и 25, можно отметить, что с повышением температуры увеличивается растворимость борной кислоты, что на диаграмме соответствует уменьшению области кристаллизации. [13]
Снижение концентрации сульфата магния увеличивает растворимость борной кислоты и содержание ее в маточнике, а повышение концентрации MgSO4 снижает растворимость борной кислоты. Очистку борной кислоты производят перекристаллизацией из воды при 85 - 90J в присутствии активированного угля. Технический и экономический интерес представляет процесс возгонки борной кислоты при помощи пара. Для этого пульпу из боратовой руды и серной кислоты нагревают в печах в присутствии водяного пара при 400 - 500 - при этом борная кислота возгоняется и возгон конденсируется при охлаждении в чистом виде, не требуя перекристаллизации. [14]
Были предложены также различные способы извлечения из маточных растворов товарной борной кислоты и сульфата магния, например раздельное получение борной кислоты и сульфата магния, основанное на повышении растворимости борной кислоты при введении в раствор некоторого количества окиси магния. Проверка этого способа, названного биборацией, в производственных условиях, проведенная совместно с Научно-исследовательским институтом химической промышленности Министерства местной и топливной промышленности РСФСР, показала его неэкономичность. [15]
Страницы: 1 2
www.ngpedia.ru
Борная кислота в природной воде
Открытие борной кислоты (или буры) в почвенной влаге или в природной воде [c.400]Изучалось поглощение бора на анионитах и селективных сорбентах из чистых растворов борной кислоты, природных вод и их модельных растворов, а также из борсодержащих растворов, в которые для повышения обменной емкости анионитов по бору были добавлены вещества, образующие комплексные анионы с бором. В качестве таких веществ применялись фтористоводородная кислота и фториды, винная кислота, поливиниловый спирт, фосфорная кислота. [c.314]
Важнейшие природные соединения бора бура ЫагВ407 ЮНгО и другие бораты, борная кислота Н3ВО3 (в воде некоторых минеральных источников) и силикаты бора. Значительные месторождения бора встречаются сравнительно редко. [c.74]Товарными продуктами являются декагидрат и безводная соль. При получении буры из борной кислоты или природных боратов из реакционного раствора выкристаллизовывают декагидрат тетрабората натрия. Его высушивают при низких температурах. Для получения безводной соли обезвоживание ведут во вращающихся барабанах, подобно тому, как обезвоживают мирабилит. При подаче в сушилку водного раствора тетрабората натрия, распыляемого над движущимся и перемешивающимся слоем безводного продукта, нагретого до 450—650 °С, вода испаряется из капель раствора, и частицы оседают на слой продукт не агломерируется. [c.363]
Опыты для чистых растворов борной кислоты позволили сделать предсказание о характере поглощения бора из природных вод и предложить метод извлечения этого элемента, суть которого заключается в поглощении его анионитом ЭДЭ-ЮП в ОН-форме при pH 8—9 и последующем вымывании раствором щелочи. Для того чтобы выяснить, в какой мере ка по- [c.316]
С другой стороны, фотометрические методы определения бора настолько специфичны и точны, что их можно использовать для. определения борной кислоты не только в очень малых ее концентрациях, но и в относительно больших после соответствующего разбавления пробы. Определению бора всеми методами мешает присутствие фторидных ионов. (Совместное присутствие боратов и фторидов наблюдается в некоторых природных водах, особенна в минеральных.) В таких случаях можно рекомендовать добавление в пробу фторида натрия или калия и определение образующихся фторборатных ионов Вр4 в виде ионных ассоциатов этих ионов с бриллиантовой зеленой, метиленовой синей или другим подобным красителем , - [c.172]
Обогащённый бором-10 пентаборат натрия используется при эксплуатации реакторов на кипящей воде в системах контроля протечек. Использование пентабората натрия в системах борного регулирования ядерных реакторов позволяет избежать дорогостоящего и сложного процесса смешивания обогащённой бором-10 борной кислоты с природной бурой непосредственно на площадке реактора. [c.197]
Различают два вида вазелина натуральный и искусственный. Натуральный (природный) вазелин получают из остатков от разгонки парафиновых нефтей с последующей очисткой серной кислотой и отбелкой адсорбентами. Природный вазелин обладает асептическими и гидрофильными свойствами и способностью (особенно в смеси с ланолином) поглощать и удерживать значительное количество воды. В чистом виде в промышленности используется натуральный вазелин не как самостоятельный продукт, а как сырье для приготовления искусственных вазелинов. Искусственный вазелин представляет собой ароматизированную смесь из церезина, парафина и парфюмерного масла в различной пропорции в зависимости от точки Ш1авления первых двух компонентов. В состав вазелина могут входить также естественный вазелин белого цвета и отбеленный петролатум, предназначенный для повышения вязкости и предохранения от выстуш1ения влаги на поверхности кожи. В борный вазелин добавляют в качестве дезинфицирующего средства борную кислоту. Вследствие того что вазелин при нагревании полностью смешивается с жирами, маслами и восками, он является хорошей основой для приготовления жировых защитных кремов. [c.215]
Серная кислота, благодаря большой активности и связыванию ею кальция, оказалась наиболее эффективным реагентом при переработке природных боратов. Однако, сернокислотный процесс в его современном виде не может считаться достаточно совершенным. Он связан с большими потерями борной кислоты и его аппаратурное оформление нуждается в улучшении (переход на непрерывную схему). Наряду с его усовершенствованием целесообразна разработка новых технологических процессов, которые должны комплексно использовать сырье и устранить отходы, дать возможность использовать низкопроцентные и трудно разлагаемые виды сырья, бедные глинистые бораты, буровые нефтяные воды, рапу некоторых озер, а в дальнейшем возможно, — датолиты, турмалины и др. [c.253]
Природные ресурсы. Содержание бора в земной коре со ставляет 3-10 %. В свободном состоянии бор не встречается, он находится в основном в виде кальциевых и магниевых солей поли-борных кислот (В20з)п(Н20)т, режб — Б виде буры и борной кислоты (растворены в воде некоторых озер и источников). [c.326]
Методика обработки пробы воды. В платиновую чащку вливают 50 мл воды, если анализу подвергают конденсат, обескремненную ионитным способом воду, питательную воду парогенераторов высокого давления илн дистиллят испарителей. При определении общего содержания кремниевой кислоты во всех других случаях (вода котловая, природная, известково-коагулироваи-ная, обескремненная магнезиальным способом, умягченная) в чащку помещают такое их количество, чтобы содержание кремниевом кислоты не превышало 50 мкг 5Юз (см. примечание на стр. 398). В чашку вводят 1 мл 0,3 н. раствора плавиковой кислоты и 1 мл 4%-ного раствора хлористого натрия. Жидкость выпаривают досуха на слабо кипящей водяной бане. Сухой остаток обрабатывают 15—20 мл обескремненной дистиллированной воды, нагревая чашку с водой на кипящей водяной бане в течение 5—7 мин. Охладив жидкость, вводят в иее 2,5 мл 3%-ного раствора борной кислоты и вливают в мерную колбу емкостью 50 мл. Б чашку вновь наливают 15—20 мл обескремненной дистиллированной воды нагревают 5—7 мин иа кипящей водяной бане, дают затем остыть и переливают в ту же мерную колбу. При обработке содержимого чашки водой стремятся смочить всю ее внутреннюю поверхность, чтобы полностью растворить образовавшийся кремнефторид натрия. [c.399]
Благодаря тому, что в природных водах бор находится в ничтожных количествах (0,002—0,1% ВдОд) при высокой общей минерализации и многокомпонентности воды, извлечение бора представляет сложнейшую задачу, которая может быть в общем виде решена только при наличии высокоселективных сорбентов. Такими оказались гидроксилсодержащие полимеры, исследованные в настоящей работе. Анионообменные смолы для поглощения бора и исследования растворов борной кислоты были применены А. Д. Кешаном с сотр. [8], Эверестом и Попилем [9]. Кешан сопоставил поглощение бора на анионитах отечественных марок (МГ, ММГ-1, НО, ДН, Н) из раствора чистой борной кислоты, содержащего [c.312]
Максимальная сорбция бора анионитами из борсодержащих растворов и природных вод происходит при рн 8—Ю. Однако полифункциональ-ные аниониты, к которым относится и наиболее избирательный к бору анионит ЭДЭ-ЮП, обладают наибольшей обменной емкостью в кислой среде. Сорбция бора анионитами из кислых растворов возможна, если бор связать в прочный комплекс, обладающий свойствами сильной кислоты. Такими свойствами обладают комплексные соединения борной кислоты с фтористоводородной и винной кислотами. Результаты исследования статическим методом поглощения бора из фторборных и тартратборных растворов на ЭДЭ-10П (СГ-форма) в зависимости от pH приведены в табл. 6. Соответствующие растворы были получены смешением фтористоводородной и борной кислот в стехиометрическом соотношении (0,0156 М. НВР ) и равных объемов 0,05 М Н3ВО3 и 0,05 М НзТ (Н2Т — винная кислота). [c.318]
Полевая лаборатория для экспедиций ТУ 25-11-1118—75 ЛНБ-2 Определение брома, иода, борной и нафтеновых кислот в природных водах. Оборудование и реактивы рассчитаны на 400 определений. Основной комплект 503X310X390 мм 11,35 кг запасной комплект 7,2 кг [c.333]
Антропогенные источники поступления в окружаюи ую среду. Сточные воды производств металлургического, машиностроительного, текстильного, стекольного, керамического, кожевенного, а также бытовые сточные воды, насыщенные стиральными порошками [12]. Содержание Б. в сточных водах может достигать 15 мг/кг сухого осадка, тогда как вода для орошения сельскохозяйственных культур не должна содержать больше 0,75 мг/л Б. (Перелыгин). Локальное загрязнение почвы возможно при разработке борсодержаш,их руд и внесении в нее борсодержащих удобрений. Опасность для животных и человека представляют природные воды с высоким содержанием Б. и его соединений. В воздух рабочей зоны Б. и его соединения попадают при разработке руд, при производстве и использовании удобрений, производстве борной кислоты, при обработке и использовании борсодержащих материалов. [c.192]
Такие методы основаны на значительной разнице в силе самой борной кислоты и кислоты, образуемой борной кислотой с мапнитом. Борная кислота является настолько слабой кислотой, что соли ее почти полностью гидролизуются при значении pH = 7,3 тогда как соли маннитоборной кислоты вполне устойчивы. Ошибка, вводимая за счет частичной нейтрализации борной кислоты при pH = 7,3 (около 12%), может быть устранена установкой титра едкой щелочи по таким же количествам борной кислоты, проведенным через все стадии анализа. Необходимо, естественно, чтобы раствор не был заметно буферирован и чтобы в нем не содержались основания или другие кислоты, реагирующие с маннитом. Этим условиям отвечает большинство природных вод и вытяжек из почв. Поведение фторидов и значительных количеств кремнекислоты или фосфатов не изучалось. [c.844]
Ионообменный метод с последующим алкалиметрическим титрованием применялся для определения бора в никелевых и цинковых электролитах для гальванонокрытий [1, 25, 63, 124, 137], в железе и стали [9, 94, 152, 196], в титановых сплавах [150], силикатах [108], природных водах [185] и дезодорантах [32], а также в три-бромиде бора и его продуктах присоединения [189]. Я. А. Дегтя-ренко [41 ] применил этот метод в несколько измененном виде для анализа фтороборатов. В этом анализе вытекающий раствор кипятят с хлоридом кальция, чтобы разложить фтороборную кислоту, затем осаждают фторид кальция и определяют борную кислоту титрованием. Недавно были разработаны методики определения бора [c.257]
Элементарный бор получают нз природного сырья в несколько стадий, Сначала бораты подвергают разложению горячей водой или серной кислотой, получая борную кислоту, а затем обезвоживанием получают борный ангндрнд. Восстановление ангидрида В2О3 металлическим маг- [c.147]
В природе борная кислота встречается как в свободном состоянии, так и в виде солей. В Италии есть такие местности, где протекают теплые ручьи, в воде которых содержится борная кислота, или она выделяется из трещин в земле вместе в водяными парами. Такие выделения называются фумаролами. Природные растворы, в которых содержание борной кислоты бывает весьма незначительно, сгущают посредством выпаривания, пользуясь для нагревания ТсПЛОш тех же ксточкикоб, к по Олляждспии полу-чают продукт в твердом виде. [c.142]
Природные растворы, несмотря на то, что они содержат бор в небольших концентрациях, являются мощным потенциальным источником борного сырья, разработке методов использования которого уделяется все большее внимание Трудность извлечения бора обусловлена крайне низкими концентрациями бора при значительном содержании других веществ, мешающих его выделению. Рапы некоторых солевых озер и некоторые буровые воды являются концентрированными растворами хлоридов натрия, калия, магния и содержат всего около 0,02% В2О3. В рассоле многих озер содержится 0,01—0,06% В2О3В сухом остатке морской воды 0,05% ВгОз . Промышленные отходы — растворы от производства борной кислоты и буры гораздо богаче бором — они содержат около 1,5% В20з. [c.351]
Бура или прямо извлекается из озер, или чрез нагревание природной борноизвестковонатровой соли с содою, или получается из тосканской неочищенной борной кислоты и соды (СО выделяется). Бура относительно легко дает пересыщенные растворы (Жернез), из которых кристаллизуется в октаэдрических формах, как при обыкновенной температуре, так и при нагревании, содержа Ка ВЮ 5№0. Уд. вес 1,81. Если же кристаллизация происходит в открытых сосудах, то при температуре ниже 56° получается обыкновенный призматический кристаллогидрат В Ыа О ЮН О, уд веса 1,71, выветривающийся в сухом воздухе при обыкновенной температуре. 100 ч. воды при 0° растворяют около 3 ч. этого кристаллогидрата, при 50° 27 ч., при 100° 201 ч. Бура при нагревании плавится, теряет воду и дает безводную соль, которая в краснокалильном жару плавится в подвижную жидкость, застывающую в прозрачное аморфное стекло, которое (уд. вес 2,37) пред застыванием приобретает вязкость, свойственную обыкновенному расплавленному стеклу. Расплавленная бура растворяет многие окислы, и от содержания их застывшее борное стекло приобретает характерные оттенки от окиси Со — темносиний, N1 — желтый, Сг — зеленый, Мп — аметистовый, и — светложелтый и т. д. Вс. едствие легкоплавкости и способности растворять окислы, бура употребляется при спаивании и сваривании металлов. В состав страз и других легкоплавких стекол часто вводят буру, и вообще многие виды стекол, приготовляемых ныне для специальных целей (напр., для термометров), часто содержат буру. [c.414]
Недостатком этого метода определения двуокиси углерода является то обстоятельство, что одновременно с СО2 титруются присутствующие органические кислоты преимущественно гумусового происхождения, а также другие слабые кислоты (борная, кремневая). Поэтому справедливо назвать это определение кислотностью воды, выражая ее в миллиграмм-эквивалентах (мг-экв). Однако для большинства природных вод содержание СО2 является основной составной частью кислотнос ги, что позволяет с некоторой условностью выражать результат этого определения в виде СО2. Недостатком данного метода является также и затруднение, возникающее из-за осаждения щелочью некоторых катионов (Са2+, М82+, Ре) при значительном содержании последних. Все эти недостатки, а также небольшой объем раствора щелочи, обычно расходуемый при титровании (десятые доли миллилитра), делают определение СО2 (путем титрования щелочью) весьма приближенным его погрешность может достигать 10% и выше. Особенно увеличивается погрешность данного метода при pH около 8,0. Однако быстрота и легкость этого определения способствуют тому, что данный метод является распространенным при анализе воды. [c.33]
Вместе с ионами угольной кислоты в данном случае титруются и ионы прочих слабых кислот, находящихся в природной воде (фосфорной, борной, кремневой, гумусовых). Поэтому принципиально правильнее определение НСОз данным методом называть, как это часто и делают, определением щелочности воды. Щелочность принято выражать в мг-экв на 1 л исследуемой воды. Однако для большинства природных вод карбонатная часть щелочности настолько велика относительно других кислот, что практически может быть принята равной общей щелочности, вследствие чего ее можно выражать не только в мг-экв, но и в виде НСОГ, т. е. в мг/л, при условии отсутствия ионов СОз -. Бели последние присутствуют, надо из найденного титрованием количества мг-экв карбонатной щелочности вЫчесть полученное специальным определением (см. определение СОз ) содержание СОз - в мг-экв. [c.110]
Среди микроудобрений борные удобрения являются самыми распространенными. Наиболее концентрированные борные удобрения — это борная кислота Н3ВО3 и бура N326407 IOh3O, но обычно в качестве удобрений используют промышленные отходы, содержащие небольшие количества бора, некоторые природные бораты или продукты их простейшей переработки. Для получения борных удобрений могут быть использованы и менее богатые бором материалы, такие как природные растворы — рапы некоторых солевых озер и нефтяные буровые воды, а также отходы от обогащения борных руд и др. Местные удобрения— зола, торф, навоз — также содержат бор 1 кг древесной золы содержит 200—700 мг бора, 1 кг сухого вещества навоза и торфа — около 20 мг. Небольшие количества бора имеются в сырых калийных солях (4—8 мг кг). [c.314]
Бура, а иногда и борная кислота, содержатся во многих минеральных водах Кавказа и Крыма, в нефтяных водах района Баку, в рапе многих озер Казахстана, Сибири, Украины, Крыма. На Северном Кавказе находятся залежи датолитов, содержащие 8—9% В2О3. Природная бура содержится в выделениях грязевых вулканов (на Таманском полуострове и в Крыму). В 1 г сопочной грязи содержится от 1,5 до 4 кг В2О3. [c.242]
Природная борная кислота. В Тоскане (Италия) ежегодно добывается 2—3 тыс. тонн борной кислоты, выделяющейся с водными парами из земных расщелин (фурмарол). Пары направляют для конденсации в бассейны с водой. При испарении из них воды на дно выпадают кристаллы борной кислоты. Оставшийся раствор медленно испаряют при 85° в железных чренах — желобах, обогреваемых топочными газами до начала выпадения кристаллов. После этого при медленном охлаждении раствора в течение 3—4 суток из него кристаллизуется борная кислота. [c.245]
В Западной Европе промышленная добыча борного сырья ведется лишь в Италии — в провинции Тоскана — извлекают борную кислоту из паров вод горячих источников (соффионов), содержащих несколько десятых долей процента Н3ВО3. Природные скважины дают пар с температурой около 100° и давлением 3 ат, а пробуренные— 145° и 6 ат. Суммарный дебит скважин составляет (1965 г.) 3000 т пара в 1 ч. Пары и воды источников, кроме борной кислоты, содержат СО2, h3S, СН4, Nh4, Не, Аг, Ne. [c.321]
Бораты натрия. Наиболее важным является тетраборат (тетраборат динатрия, очищенная бура) (Ма2В407). Получается кристаллизацией растворов природных боратов или обработкой природных боратов кальция или борной кислоты карбонатом натрия. Его производят безводным или гидратированным 5 или 10 молекулами воды. При нагревании и последующем охлаждении он образует стеклоподобную массу (плавленная бура, борное стекло, гранулированная бура). Используется для придания жесткости льняному полотну или бумаге для пайки металлов (флюс для твердого припоя) как флюс для эмалей для изготовления стеклующихся красок, специального стекла (оптическое стекло, стекло для электрических лампочек), клея или лака для очистки золота для получения боратов и антрахиноновых красителей. [c.107]
chem21.info