Классификация подземных вод. Классификация вод
Классификация подземных вод
В земной коре находится большое количество воды — физически и химически связанной, свободной гравитационной, капиллярной, в виде водяного пара и льда. Подземными водами как объектом гидрологии будем называть лишь те содержащиеся в земной коре воды, которые находятся в активном взаимодействии с атмосферой и поверхностными водами (океанами и морями, реками, озерами и болотами) и участвуют в круговороте воды на земном шаре. Подземные воды в таком понимании представлены в основном свободной (гравитационной) и капиллярной водой, а также перемещающимся в порах грунта водяным паром.
Экзогенныеподземные воды попадают в горные породы либо при процессах просачивания (инфильтрации) поверхностных вод и конденсации водяного пара, либо в результате седиментации (осадко- накопления). Эти воды часто называют соответственно инфильтра- ционными, конденсационными и седиментационными.
Инфильтрационныеподземные воды проникают в горные породы путем просачивания атмосферных, речных, морских и озерных вод. Основную роль при этом играет проникновение в грунт через поры и трещины практически пресной атмосферной воды. Конденсационные подземные воды образуются при конденсации в порах грунта водяного пара, перемещающегося в грунте под влиянием разности давления. Считают, что вклад этого вида питания подземных вод невелик, однако в некоторых физико-географических условиях, например пустынях, может иметь существенное значение. Седиментационные подземные воды образуются из вод того водного объекта, где происходил процесс седиментации, т. е. отложения наносов. Воды такого типа распространены в осадочных породах и в ложах океанов и морей, где образуют так называемые «иловые растворы».
Эндогенныеподземные воды образуются в горных породах в результате дегидратации минералов (такие воды называют дегидратационными или «возрожденными») или поступают из магматических очагов, в частности в районах современного вулканизма (их называют «ювенильными» водами).
Инфильтрационные, конденсационные, седиментационные, де- гидратационные и «ювенильные» воды при своем перемещении в горных породах смешиваются, образуя смешанные по происхождению подземные воды.
Подземные воды (главным образом — инфильтрационные) являются важным компонентом материкового звена круговорота воды на земном шаре и играют заметную роль в балансе и режиме природных вод и растворенных в них веществ.
По характеру залегания.
Верхнюю часть земной коры в отношении распределения в ней подземных вод принято делить на две зоны: зону аэрации и зону насыщения.
1. В зоне аэрации образуется верховодка. Это почвенная влага. Мощность этой зоны составляет 2-3 м в таежной зоне, 50 см под саваннами, 20-30 см в степной зоне. В зоне аэрации не все поры заняты водой, часть пор заполнены воздухом.
2. В зоне насыщения все поры и пустоты заполнены водой; здесь формируются несколько горизонтов подземных вод:
■ Грунтовые воды. Это первый от поверхности водоносный горизонт, залегающий на водонепроницаемых горных породах. Грунтовые воды распространены преимущественно в рыхлых четвертичных отложениях. Они в значительной степени загрязнены.
■ Межпластовые воды. Они встречаются в более глубоких пластах Земли и залегают между двумя водоупорными слоями в водопроницаемой толще. Эти воды не соприкасаются с зоной аэрации. Количество горизонтов межпластовых вод и глубина их залегания определяется геологическим строением конкретных территорий. Грунтовые и межпластовые воды являются ненапорными.
■ Артезианские воды. Они приурочены к геологическим отрицательным структурам (синеклизам), заполненными осадочными горными породами при соответствующем напластовании водопроницаемых и водоупорных слоев, а также к сложной системе тектонических трещин и сбросов.
В зависимости от физического состояния, подвижности и характера связи с грунтом выделяют несколько видов воды в грунтах: химически и физически связанная, капиллярная, свободная (гравитационная), вода в твердом и парообразном состоянии.
Химически связанная водавходит в состав некоторых минералов, например гипса CaSO4• 2Н2O, мирабилита Na2SO4• 10Н2O, медного купороса CuS04- 5Н2O. Вода из таких минералов может быть удалена в большинстве случаев лишь при нагревании до 300—400 °С.
Физически связанная водаудерживается на поверхности минералов и частиц грунта молекулярными силами и может быть удалена из грунта только при температуре не менее 90—120 °С. Этот вид воды подразделяют на прочносвязанную (гигроскопическую) и рыхлосвязанную (пленочную).
Гигроскопическая вода образуется вследствие адсорбции частицами грунта молекул воды. На поверхности частиц гигроскопическая вода удерживается молекулярными и электрическими силами. Пленочная вода образует пленку поверх гигроскопической воды, когда влажность грунта становится выше его максимальной гигроскопичности. Эта вода может передвигаться от одной частицы грунта к другой: от мест, где толщина пленки больше, к местам, где ее толщина меньше.
Физически связанная вода (за исключением некоторого количества пленочной воды), как и химически связанная, в круговороте воды в природе практически участия не принимает, и поэтому в состав подземных вод, которые изучает гидрология, не включается.
Капиллярная водаобразуется в порах грунта после насыщения их пленочной водой, заполняет поры и тонкие трещины и перемещается в них под действием капиллярных сил. Капиллярная вода через поверхность почвы или листья растений испаряется, поэтому она участвует в круговороте воды в природе и ее следует включать в состав подземных вод, изучаемых гидрологией.
Свободная, или гравитационная, вода— наиболее подвижный и важный компонент подземных вод. Эта вода в жидком виде находится в порах и трещинах грунта и перемещается под влиянием силы тяжести и градиентов гидростатического давления. Объем свободной (гравитационной) воды в насыщенном водой грунте зависит от его скважности, гранулометрического состава, количества и размера пор.
Вода в твердом состоянии (лед)находится в грунте в виде кристаллов, прослоек и линз льда. В районах сезонного промерзания грунта эта вода периодически участвует в круговороте воды.
Вода в парообразном состоянии (водяной пар)заполняет вместе с воздухом не занятые водой пустоты в грунтах. Водяной пар в фунтах обладает большой подвижностью и перемещается от мест с большей к местам с меньшей упругостью (меньшим давлением). Парообразная вода в грунтах активно участвует в круговороте воды в природе.
По температуре(в °С) подземные воды разделяются (по А.М.Овчинникову) на:
1. весьма холодные - ниже -4° (области многолетней мерзлоты)
2. холодные - -4; +20 (неглубокие воды средних широт)
3. теплые - +20;+37
4. горячие - +37; +42
5. очень горячие - +42;+100
6. исключительно горячие (термы) - выше 100°
(на глубине 3-4 км)
Температура зависит от геологического строения и истории геологического развития структур, физико-географических условий и режима питания. Питьевая вода является наиболее вкусной и освежающей при температуре +7°, +11°. Для лечебных целей (принятия ванн) наиболее ценная вода с температурой +35°, +37°. Температуру измеряют родниковым термометром с ценой деления 0,2°С.
По минерализации.
Минерализация - это сумма всех найденных при химическом анализе воды минеральных веществ. О величине минерализации судят по сухому остатку, полученному при выпаривании определенного объема воды и высушивании остатка при температуре 110°С. Выражается сухой остаток в мг/л (мг/кг) или г/л (г/кг). По величине сухого остатка выделяют 6 групп ( по П.П.Климентьеву):
1. сверхпресные до 0,2 г/л
2. пресные 0,2 - 1 г/л
3. слабосолоноватые 1 - 3 г/л
4. сильносолоноватые 3-10 г/л
5. соленые 10 - 35 г/л
6. рассолы более 35 г/л
Общая минерализация подземных вод изменяется в широких пределах; от нескольких десятков мг/л до 600 г/л и выше.
По химическому составу
Первую классификацию дал В.И.Вернадский. По В.И.Вернадскому подземные воды разделяют на : кислородные, сероводородные, азотные, углекислые, хлоридно-натриевые, хлоридно-кальциевые, радоновые. В настоящее время разработано много схем применительно к разным районам. Остановимся на классификации О.А. Алекина, которая сочетает принцип деления по преобладающему аниону или катиону. За основу взято шесть главных ионов. Выделены 3 класса по преобладающему аниону: гидрокарбонатные (НСО3 +СО3), сульфатные (S04), хлоридные (С1). В каждом из классов по 3 группы по преобладающему катиону: кальциевые (Са), магниевые (Mg), натриево-калиевые (Nа+К).
В зависимости от происхождения различают атмосферные, поверхностные и подземные воды, которые принимают участие в общем, круговороте воды.
а) Атмосферные воды выпадают на поверхность Земли в виде дождя, града, снега, росы и тумана. Они отличаются высоким содержанием газов (азота, кислорода и двуокиси углерода). Эти воды из-за содержания в них двуокиси углерода имеют, кислую реакцию, что придает им неприятный вкус. Атмосферные воды для поения животных и хозяйственных нужд используются крайне редко и только в безводных районах. Качество их невысокое, они слабо минерализованы, содержат большое количество пыли, микроорганизмов.
b) Поверхностные воды – это атмосферные и отчасти грунтовые воды, которые переместились к пониженным частям рельефа местности (лужи, пруды, реки, озера, моря). Из-за возможности загрязнения они далеко не всегда пригодны для питья в сыром виде. Использовать такую воду для питья можно лишь после предварительной обработки.
с) Подземные воды (рис.2) образуются главным образом из атмосферных вод, которые проникают в нижележащие слои почвы и накапливаются там, в виде подземных водотоков или водохранилищ. Эти воды концентрируются над водонепроницаемым слоем в порах грунта, образуя водоносный горизонт. Если водоносный горизонт находится между первым водонепроницаемым слоем и почвой и расположен близко к поверхности Земли, он находится под атмосферным давлением. Если же водоносный горизонт расположен между водонепроницаемыми пластами, то вода может подвергаться гидростатическому давлению (артезианская вода). С санитарной точки зрения подземные воды делятся на верховодку, грунтовые и артезианские. Верховодка находится обычно в верхнем (2-3 м) слое Земли, накапливаясь над первым водонепроницаемым слоем. Ее глубина зависит от глубины залегания этого слоя. В зависимости от времени года эти воды находятся на разной глубине от поверхности Земли. Во время засухи они могут совсем исчезать. Они играют большую роль в развитии растений на полях, оставленных под пар. Часть этих вод образует так называемый почвенный раствор, который заполняет капиллярные пространства между частицами почвы, создавая гидратационный слой. Из-за легкости загрязнения верховодка в большинстве случаев непригодна для питья, даже если по вкусу она отвечает всем требованиям. Грунтовые воды находятся под первым водонепроницаемым слоем, залегающим на глубине не менее 7 м и до 2-3 км, иногда даже до 6,5 км. Они могут, находится в нескольких водоносных горизонтах, быть безнапорными или находиться под давлением. Воды, находящиеся на глубине до 15 м, называют мелкими грунтовыми водами. Они служат главным источником водоснабжения для людей. Воды, залегающие на глубине более 15 м (на третьем или еще более глубоком водонепроницаемым слоем), называются глубокими грунтовыми водами. Грунтовые воды, содержащие не менее 1000 мг /л растворенных солей или СО2 или одного из редко встречающихся в пресной воде элементов, например брома, йода, фтора, железа, радия, называются минеральными водами. В зависимости от преобладания в их составе того или иного химического соединения различают следующие виды минеральных вод: хлоридные, содержащие большое количество хлористого натрия; сульфидные, содержащие сероводород; углекислые, содержащие карбонаты и свободный СО2; горькие воды, содержащие главным образом сернокислый магний; воды, носящие название одного из главных компонентов (йодные, радоновые или радиоактивные) и другие минеральные воды. Артезианские воды особенно ценятся за их гигиенические свойства. Они полностью свободны от микроорганизмов, в связи, с чем они пригодны для питья без очистки и обеззараживания.
studfiles.net
Классификация вод по их химическому составу — КиберПедия
(классификация О.А. Алекина).
Большое разнообразие химического состава природных вод вынуждает тем или иным образом систематизировать их. До сих пор было предложено немало классификаций природных вод по их химическому составу, но вместе с тем пока еще нет простой классификации, учитывающей все особенности условий формирования химического состава всех вод и учитывающей весь комплекс растворенных веществ.
Рассмотрим только некоторые из предложенных классификаций.
Классификация вод по величине их минерализации, т. е. суммы найденных в воде ионов. Округляя различные существующие пределы, в данной классификации можно наметить следующее деление вод по величине минерализации:
пресные до 1,0 г/кг
солоноватые 1—25
воды с морской соленостью 25—50
воды соленые (с соленостью выше морской) выше 50
Область пресных вод, установленная до 1 г/кг, основана на восприятии человеком вкуса солености при наличии ионов свыше 1 г/кг. Граница в 25 г/кг между солоноватыми водами и водами с морской соленостью установлена на том основании, что примерно при этой минерализации (24,695) температуры замерзания и максимальной плотности воды равны между собой. А эти характеристики весьма важны для гидрологии. Граница между водами с морской соленостью и солеными водами установлена потому, что в морях не наблюдается минерализации свыше 50 г/кг, более высокие ее величины характерны только для соляных озер и сильно минерализованных подземных вод.
Классификация вод по их минерализации дает подразделение вод только в общих чертах и не учитывает особенностей содержания отдельных ионов и газов.
Классификация О.А. Алекина(рис.4) сочетает принцип деления по преобладающим анионам и катионам с делением по соотношениям между ионами. Все природные ионы делятся по преобладающему аниону (по эквивалентам) на 3 класса: гидрокарбонатных (и карбонатных) (НСО3 + СО3), сульфатных (S04) и хлоридных (Сl) вод. Каждый класс по преобладающему катиону подразделяется на 3 группы: кальциевую, магниевую и натриевую. В свою очередь каждая группа подразделяется на 3 типа вод, определяемых соотношением между ионами в мг-экв.(рис.4)
Первый тип характеризуется соотношением НСО3> Са + Мg. Воды этого типа образуются при значительном участии изверженных пород, содержащих
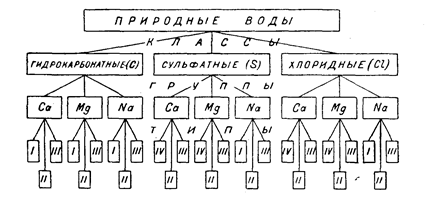
Рис.4. Классификация природных вод по их химическому составу
По О. А. Алекину.
большие количества Na и К - в результате чего в воде появляются ионы Na и НСО3. Могут они образовываться в некоторых случаях и при обмене Са на Nа, содержащийся в почвах или породах (например, глауконитах, щелочных глинах). Воды первого типа чаще всего мало минерализованы, но питаемые этими водами бессточные озера накапливают НСО3 и СО3 в очень больших количествах.
Второй тип характеризуется соотношением НСО3 < Са + Мg < НСО3 + S04. Генетически воды этого типа связаны с различными осадочными породами и продуктами выветривания коренных пород, являясь преимущественно смешанными водами. К этому типу относится большинство рек, озер и подземных вод малой и умеренной минерализации.
Третий тип характеризуется соотношением НСО3 + SO4< Са + Мg, или, что то же самое, Cl > Na. Генетически эти воды являются смешанными и подвергнувшимися значительным изменениям из-за катионного обмена, обычно Nа из раствора на Са или Мg из почв и пород. К этому типу принадлежат воды океана, морей, лиманов, реликтовых водоемов и многих сильно минерализованных подземных вод.
Четвертый тип характеризуется соотношением НСО3 = 0 т.е. воды этого типа кислые. Поэтому в класс карбонатных вод этот тип не входит, а его воды находятся только в сульфатном и хлоридном классах, в группах Са и Мg, где нет первого типа.
Для обозначения в данной классификации существуют символы. Класс обозначается символом, выводимым из названия соответствующего аниона (С, S, Сl), а группа - своим химическим символом, который пишется в виде степени к символу класса. Принадлежность к типу обозначается римской цифрой внизу символа класса. Таким образом, в целом символы пишутся следующим образом: СCaII (гидрокарбонатный класс, группа кальция, тип второй).
cyberpedia.su
Состав природных вод-ликбез 6
Таблица 1.12. Классификация вод по степени минерализации
| Наименование вод | Минерализация, г/кг |
| Пресные | 1,0 |
| Солоноватые | 1,0 - 25,0 |
| С морской соленостью | 25,0 - 50,0 |
| Рассолы | 50,0 и свыше |
Классификация по химическому составу
В
подавляющем большинстве случаев солевой состав природных вод определяется
катионами Са2+, Мg2+, Nа+,
К+ и анионами НСO3-, Сl- , SO42-.
Эти ионы называются главными ионами воды или макрокомпонентами;
они определяют химический тип воды. Остальные ионы присутствуют в значительно
меньших количествах и называются микрокомпонентами; они не определяют
химический тип воды.
Классификация природных вод по химическому составу, предложенная О.
А. Алекиным (рис. 1.13), считается наиболее приемлемой для вод, используемых
в питьевых и хозяйственно-бытовых целях. В ее основу положены два принципа:
преобладающих ионов и соотношения между ними. Рис.
1.13. Классификация природных вод по химическому составу По
преобладающему аниону воды делятся на три класса: гидрокарбонатные,
сульфатные и хлоридные. Воды каждого класса делятся, в свою очередь,
по преобладающему катиону на три группы: кальциевую, магниевую и натриевую.
Каждая группа подразделяется на 4 типа по соотношению содержащихся в
воде ионов (в эквивалентах). При этом класс природных вод обозначается
символом соответствующего аниона: С НСО3-,
S SO42-, Сl
Сl-; группа: символом катиона: К+, Na+, Са2+, Мg2+; тип - римской цифрой.
Формула воды записывается следующим образом. К символу класса добавляется
нижний индекс - значение минерализации (с точностью до 0,1 г/л ), к
символу группы - верхний индекс - значение общего катионного состава
(с точностью до целых единиц вещества в ммоль/л),
например: С1,2 Nа0,5 - гидрокарбонатно-натриевая
вода с общей минерализацией 1,2 г/л и преобладающей концентрацией гидрокарбонатных
ионов и ионов натрия.
В природных водах присутствуют также растворенные газы. В основном это
газы, которые диффундируют в воды из атмосферы воздуха, такие как кислород,
углекислый газ, азот. Но в то же время в подземных водах или водах нецентрализованных
источников водоснабжения, в минеральных и термальных водах могут присутствовать
сер водород, радиоактивный газ радон, а также инертные и другие газы.
В табл. 1.13 представлены ионы, наиболее часто встречающиеся в природных
водах.
По
преобладающему аниону воды делятся на три класса: гидрокарбонатные,
сульфатные и хлоридные. Воды каждого класса делятся, в свою очередь,
по преобладающему катиону на три группы: кальциевую, магниевую и натриевую.
Каждая группа подразделяется на 4 типа по соотношению содержащихся в
воде ионов (в эквивалентах). При этом класс природных вод обозначается
символом соответствующего аниона: С НСО3-,
S SO42-, Сl
Сl-; группа: символом катиона: К+, Na+, Са2+, Мg2+; тип - римской цифрой.
Формула воды записывается следующим образом. К символу класса добавляется
нижний индекс - значение минерализации (с точностью до 0,1 г/л ), к
символу группы - верхний индекс - значение общего катионного состава
(с точностью до целых единиц вещества в ммоль/л),
например: С1,2 Nа0,5 - гидрокарбонатно-натриевая
вода с общей минерализацией 1,2 г/л и преобладающей концентрацией гидрокарбонатных
ионов и ионов натрия.
В природных водах присутствуют также растворенные газы. В основном это
газы, которые диффундируют в воды из атмосферы воздуха, такие как кислород,
углекислый газ, азот. Но в то же время в подземных водах или водах нецентрализованных
источников водоснабжения, в минеральных и термальных водах могут присутствовать
сер водород, радиоактивный газ радон, а также инертные и другие газы.
В табл. 1.13 представлены ионы, наиболее часто встречающиеся в природных
водах.
Таблица 1.13. Ионы, наиболее часто встречающиеся в природных водах
|
Катион |
Анион |
||
|
Наименование |
Обозначение |
Наименование |
Обозначение |
| Водород |
H+ |
Гидроксильный |
OH- |
| Натрий |
Na+ |
Бикарбонатный |
HCO3- |
| Аммоний |
Nh5+ |
Хлоридный |
Cl- |
| Кальций |
Ca2+ |
Сульфатный |
SO42- |
| Магний |
Mg2+ |
Нитритный |
NO2- |
| Железо (двух- и трехвалентное) |
Fe2+, Fe3+ |
Нитратный |
NO3- |
| Барий |
Ba2+ |
Силикатный |
SiO32- |
| Алюминий |
Al3+ |
Ортофосфорный |
PO43- |
| Калий |
K+ |
Фторидный |
F- |
Растворимые и слаборастворимые соли в природных вода
Возвращаясь
к главным ионам пресных вод, необходимо отметить, что их катионный и
анионный состав определяется наличием в осадочных породах хорошо растворимых
минералов. Поэтому в воде присутствуют катионы К+ и Nа+
и анионы Сl-; и SO42-. Ионы кальция
и магния с карбонатным ионом CO32- (продукт второй
ступени диссоциации угольной кислоты) образуют малорастворимые соединения
- так называемые соли жесткости. Эти соединения представлены в природе
в виде известняков, мелов, мраморов, кальцитов, доломитов и других минералов,
содержащих карбонаты кальция и магния. В то же время бикарбонатные ионы
HCO3-(продукт первой ступени диссоциации угольной кислоты) образуют хорошо
растворимые соединения с ионами кальция и магния. Карбонатные ионы
присоединяют ион водорода и превращаются в бикарбонатный ион:
СО32- + Н+
НСО3-.
При высоких концентрациях водородных ионов (высокой кислотности соответствует
низкое значение рН - меньше 6) происходит растворение карбонатов, поэтому
в природных водах могут присутствовать бикарбонатные ионы , карбонатные
ионы , а также катионы жесткости Са2+ и Мg2+ .
Между этими составляющими существует строгое равновесие, которое связано
с содержанием в воде углекислого газа, катионов жесткости и бикарбонатных
ионов.
Угольная кислота имеет две ступени диссоциации:
Н2СО3
Н+ + НСО3-;
НСО
Н+ + СО32-.
и существует, в основном, в виде углекислого газа, концентрация которого
определяется парциальным давлением СО2 в атмосфере и его растворимостью
в соответствии с таблицей растворимости газов.
В зависимости от содержания в природной воде различных форм угольной
кислоты природная вода имеет различное значение водородного показателя
(рис. 1.14).
Правильно также и другое положение: концентрация водородных ионов определяет
соотношение между бикарбонатными HCO32- и карбонатными CO32- ионами. Рис.
1.14. Соотношение форм угольной кислоты в воде при различных значениях
рН Динамическое
равновесие между углекислым газом, анионами угольной кислоты, ионами
кальция и нерастворимым карбонат кальция в какой-то степени может быть
пояснено рис. 1.15.Рис.
1.15. Образование карбоната кальция
Динамическое
равновесие между углекислым газом, анионами угольной кислоты, ионами
кальция и нерастворимым карбонат кальция в какой-то степени может быть
пояснено рис. 1.15.Рис.
1.15. Образование карбоната кальция
 Из рисунка видно, что при снижении кислотности раствора концентрация
водородных ионов снижается, рН раствора повышается и ( приобретает щелочную
реакцию, бикарбонаты переходят в карбонаты, которые после взаимодействия
с ионами кальция образуют растворимый карбонат кальция. Происходит осаждение
кристаллической фазы карбоната кальция. И, наоборот, при повышенной
кислотности воды карбонатные ионы переходят в бикарбонатные, что приводит
к растворению карбоната кальция СаСО3. Кстати, приблизительно по такой
же схеме происходит вымывание кальция из костей скелета и зубов.
Из рисунка видно, что при снижении кислотности раствора концентрация
водородных ионов снижается, рН раствора повышается и ( приобретает щелочную
реакцию, бикарбонаты переходят в карбонаты, которые после взаимодействия
с ионами кальция образуют растворимый карбонат кальция. Происходит осаждение
кристаллической фазы карбоната кальция. И, наоборот, при повышенной
кислотности воды карбонатные ионы переходят в бикарбонатные, что приводит
к растворению карбоната кальция СаСО3. Кстати, приблизительно по такой
же схеме происходит вымывание кальция из костей скелета и зубов.
Примеси, встречающиеся в воде
Вода
является великолепным растворителем, в котором могут растворяться минеральные
и органические вещества, созданные как природой, так и человеком. Говорят,
что «вода камень точит». И в то время в ней могут присутствовать вещества
во взвешенном состоянии: частицы песка и глины, коллоидные и механические
примеси и живые существа различных форм и размеров. Исходная, чистая
вод попадающая на землю в виде дождя, снега, града, росы, изморози и
тумана, насыщаясь различными веществами и организмами, загрязняется
и, как правило, становится непригодной для питья или использования в
быту без предварительной очистки.
Источниками загрязнения природных вод могут быть как природные объекты,
так и объекты, созданные руками человека (рис. 1.16).
Значительное воздействие на природные водные объекты оказывает сельскохозяйственное
производство. Интенсификация оросительного земледелия приводит к поднятию
уровня грунтовых вод и усилению; засоленности почв с последующим исключением
их из сельскохозяйственного оборота. Рис.
1.16. Источники загрязнения природных вод В
природные водные объекты поступают канцерогенные и другие вредные для
здоровья людей вещества. Многие природные вещества в процессе подготовки
воды для питьевого водоснабжения могут стать канцерогенными - это вторичное
загрязнение природных вод. Водные объекты могут быть загрязнены в результате
судоходства, сброса хозяйственно-бытовых и сельскохозяйственных сточных
вод. При этом происходит и термическое загрязнение водных объектов.
Присутствующие в сточных водах фосфор и азот (температура этих вод,
как правило, выше температуры природных вод) способствуют развитию сине-зеленых
водорослей. Интенсивное использование воды для охлаждения оборудования
также ведет к термическому загрязнению вод, в результате чего повышается
их температура, снижается содержание кислорода и, соответственно, способность
водоемов к самоочищению.
К антропогенным источникам поступления канцерогенных веществ в природные
воды относятся производственные и природные сточные воды, ливневые и
талые воды, протекающие по загрязненной территории, хранилища нефтепродуктов,
свалки и захоронения твердых и жидких отходов, отвалы шлаков и пепла,
хранилища минеральных удобрений, животноводческие комплексы, пыль и
стоки автомобильных дорог и т. д.
К числу природных источников канцерогенных веществ необходимо отнести
залежи горючих ископаемых (сланцы, полиметаллические, асбестосодержашие,
селитровые и мышьяковистые руды), геотермальные и минеральные воды.
Вещества, поступающие в водные объекты, насчитывают десятки и сотни
тысяч наименований. Для того чтобы признать эти загрязнения или вещества,
в которые они могут трансформироваться, потенциально опасными для здоровья
человека, необходимо проведение специальных исследований. Для всего
спектра загрязнений такие исследования провести невозможно.
На территории РФ действует утвержденный Минздравом СССР «Перечень веществ,
продуктов, производственных процессов и бытовых факторов, канцерогенных
для человека». К их числу отнесены асбесты, бенз(а)пирен(1,2,3), винилхлорид(1,2),
неочищенные минеральные масла, мышьяк и его соединения и многие другие
вещества.
Санитарные правила и нормы, определяющие гигиенические требования к
питьевой воде источников централизованного и нецентрализованного водоснабжения,
содержат нормативы предельно допустимых концентраций веществ, которые
могут оказать канцерогенное или иное вредное воздействие на организм
человека.
Канцерогенное воздействие полиароматических (циклических) углеводородов
(ПАУ), к числу которых относится и бенз(а)пирен, наиболее изучено. Опасность
поступления их с водой сравнительно невелика. Многие ароматические углеводороды
могут накапливать в организмах гидробионтов, которые в свою очередь
являются пищей для человека.
Опасны для человека и хлорорганические соединения, присутствующие в
воде. Это, в первую очередь, полихлордифенилы (ПХД) и дельные пестициды
(ДДТ, ГХЦГ и гексахлорбензол). Строение некоторых
циклических углеводородов представлено на рис. 1.17. Эти соединения
обладают высокой стабильностью в условиях окружающей среды.
В
природные водные объекты поступают канцерогенные и другие вредные для
здоровья людей вещества. Многие природные вещества в процессе подготовки
воды для питьевого водоснабжения могут стать канцерогенными - это вторичное
загрязнение природных вод. Водные объекты могут быть загрязнены в результате
судоходства, сброса хозяйственно-бытовых и сельскохозяйственных сточных
вод. При этом происходит и термическое загрязнение водных объектов.
Присутствующие в сточных водах фосфор и азот (температура этих вод,
как правило, выше температуры природных вод) способствуют развитию сине-зеленых
водорослей. Интенсивное использование воды для охлаждения оборудования
также ведет к термическому загрязнению вод, в результате чего повышается
их температура, снижается содержание кислорода и, соответственно, способность
водоемов к самоочищению.
К антропогенным источникам поступления канцерогенных веществ в природные
воды относятся производственные и природные сточные воды, ливневые и
талые воды, протекающие по загрязненной территории, хранилища нефтепродуктов,
свалки и захоронения твердых и жидких отходов, отвалы шлаков и пепла,
хранилища минеральных удобрений, животноводческие комплексы, пыль и
стоки автомобильных дорог и т. д.
К числу природных источников канцерогенных веществ необходимо отнести
залежи горючих ископаемых (сланцы, полиметаллические, асбестосодержашие,
селитровые и мышьяковистые руды), геотермальные и минеральные воды.
Вещества, поступающие в водные объекты, насчитывают десятки и сотни
тысяч наименований. Для того чтобы признать эти загрязнения или вещества,
в которые они могут трансформироваться, потенциально опасными для здоровья
человека, необходимо проведение специальных исследований. Для всего
спектра загрязнений такие исследования провести невозможно.
На территории РФ действует утвержденный Минздравом СССР «Перечень веществ,
продуктов, производственных процессов и бытовых факторов, канцерогенных
для человека». К их числу отнесены асбесты, бенз(а)пирен(1,2,3), винилхлорид(1,2),
неочищенные минеральные масла, мышьяк и его соединения и многие другие
вещества.
Санитарные правила и нормы, определяющие гигиенические требования к
питьевой воде источников централизованного и нецентрализованного водоснабжения,
содержат нормативы предельно допустимых концентраций веществ, которые
могут оказать канцерогенное или иное вредное воздействие на организм
человека.
Канцерогенное воздействие полиароматических (циклических) углеводородов
(ПАУ), к числу которых относится и бенз(а)пирен, наиболее изучено. Опасность
поступления их с водой сравнительно невелика. Многие ароматические углеводороды
могут накапливать в организмах гидробионтов, которые в свою очередь
являются пищей для человека.
Опасны для человека и хлорорганические соединения, присутствующие в
воде. Это, в первую очередь, полихлордифенилы (ПХД) и дельные пестициды
(ДДТ, ГХЦГ и гексахлорбензол). Строение некоторых
циклических углеводородов представлено на рис. 1.17. Эти соединения
обладают высокой стабильностью в условиях окружающей среды. При обработке природных вод хлорированием из неканцерогенных «предшественников»
могут образовываться опасные в канцероген» отношении галогенсодержащие
соединения (ГСС). В питьевой воде может содержаться до 100 ГСС, среди
них наиболее часто и в небольшем количестве встречаются хлороформ, дихлорбромметан,
дибромхлорметан, бромоформ, 4-хлористый углерод, дихлорэтан, трихлорэтан,
тетрахлорэтан и др. Причем в нехлорированной воде эти вещества, по мнению
ряда исследователей, не встречаются или встречаются в минимальном количестве.
Наибольшее количество ГСС образуется при хлорировании природных компонентов,
таких как гуминовые кислоты, дубильные вещества, винилиновая и галловая
кислоты, а также фульвокислоты, метаболиты водорослей - всего более
80 веществ.
При обработке природных вод хлорированием из неканцерогенных «предшественников»
могут образовываться опасные в канцероген» отношении галогенсодержащие
соединения (ГСС). В питьевой воде может содержаться до 100 ГСС, среди
них наиболее часто и в небольшем количестве встречаются хлороформ, дихлорбромметан,
дибромхлорметан, бромоформ, 4-хлористый углерод, дихлорэтан, трихлорэтан,
тетрахлорэтан и др. Причем в нехлорированной воде эти вещества, по мнению
ряда исследователей, не встречаются или встречаются в минимальном количестве.
Наибольшее количество ГСС образуется при хлорировании природных компонентов,
таких как гуминовые кислоты, дубильные вещества, винилиновая и галловая
кислоты, а также фульвокислоты, метаболиты водорослей - всего более
80 веществ.
Микроорганизмы и паразиты, присутствующие в воде
В
природных водах присутствуют и размножаются микроорганизмы, водоросли,
ракообразные, рыбы, земноводные, в толще воды развиваются личинки комара,
на поверхности воды живут водомерки. Многие из этих организмов, называемых
гидробионтами, являются опасными для здоровья и жизни человека, например,
огромные морские хищники - акулы - или небольшие хищные рыбы пираньи.
Но и небольшие микроорганизмы - микробы - могут нанести непоправимый
вред здоровью человека.
В воде могут присутствовать также микроскопические личинки паразитов,
амебные цисты, бактерии в споровой форме и другие патогенные формы.
Основным источником патогенных организмов, распространяемых водой, являются
фекалии человека и теплокровных животных, а также фекально-бытовые сточные
воды. Фекальные загрязнения воды ухудшают ее качество, а патогенные
микроорганизмы, попадающие в воду с выделениями теплокровных животных
и человека, могут явиться причиной заболеваемости кишечными инфекциями.
Среди патогенных микроорганизмов чаще других обнаруживаются в загрязненных
водах сальмонеллы, шигеллы, пастереллы, вибрионы, микобактерии, энтеровирусы
человека, амебные цисты, личинки нематод, энтеропатогенные Е.Соli и
др.Сальмонеллы (Salmonellа) - это представители
рода сальмонелл, в который входит около 2000 различных грамм-отрицательных
микроорганизмов, похожих друг на друга по внешнему строению и воздействию
на человека. Эти микробы вызывают заболевание желудочно-кишечного тракта,
называемое сальмонеллезом. В воде сальмонеллы сохраняются до 120 дней;
эффективно дезинфицируются раствором хлорной извести.Шигеллы (Shigеllа) - это дизентерийные
микробы, поражающие отдел толстой кишки человека; вызывают дизентерию
(шигеллез) с признаками интоксикации. Они хорошо сохраняются в воде
и даже могут размножаться. На них губительно действуют высокая температура
и дезинфицирующие средства.Амебные цисты, попадающие в организм
человека с загрязненной водой, вызывают амебиаз - болезнь кишечника,
иногда осложняющаяся абсцессами печени, головного мозга, поражением
Легких и др гих органов. Возбудитель относится к классу простейших
(Епtamoeba histolitiса), размер ее может достигать 20-30
мкм.Лептоспироз - острое инфекционное
заболевание, передающееся человеку от животных. Однако возможен и водный
путь передачи инфекции. Болезнь характеризуется поражением почек, печени,
центральной нервной системы и мышц, сопровождается интоксикацией и лихорадкой.
Возбудителем лептоспироза являются лептоспиры
(Leptospirа interrogans) - спиралевидные организмы, приспособлений
для жизни в воде. Ежегодная заболеваемость во всем мире составляет 1%,
но при контакте с домашними животными может достигать В литературе описана
вспышка лептоспироза у 50 человек, которые купались в реке, протекавшей
вблизи пастбища для коров и свиней.
В этом ряду инфекционных заболеваний, водный путь возникновения которых
является наиболее вероятным, необходимо отметить холеру.
Эта болезнь в XIX в. вызывала в Европе пандемии. Заболевания холерой
были отмечены в 1947 г. в Египте, в 1964 г. - в Иране и Ираке, в 1970
г. - в Советском Союзе (Одесса и Астрахань). В последние годы вибрионы
холеры были обнаружены в водоемах Москвы, Санкт-Петербурга,
Тамбова. Не исключена возможность их появления
и в водоемах других регионов России. Распространение холеры связано
с нарушениями карантинов, усилением миграции людей - носителей холерного
вибриона, а также с перевозкой загрязненных продуктов и воды кораблями
и самолетами.
Возбудителем холеры являются вибрионы (Vibrio
cholerae). Холерный вибрион хорошо переносит низкие температуры
и даже замораживание. При кипячении погибает через 1 мин, при воздействии
дезинфицирующих средств - почти сразу.
Некоторые вирусы человека могут передаваться через воду при ее загрязнении
фекалиями. К ним относятся возбудители инфекционного гепатита, полиомиелита,
энтеровирусных инфекций, вызывающих поражение центральной нервной системы,
мышц, миокарда и кожных покровов.
Возможность передачи вирусов водным путем можно продемонстрировать на
примере вирусного гепатита. Самая
большая вспышка вирусного гепатита отмечена в 1955-1956 гг. в Дели.
Несколько тысяч человек были инфицированы в результате употребления
воды из централизованной системы водоснабжения. Дело в том, что в природной
воде присутствовали возбудители кишечных заболеваний, вирус гепатита
и другие патогенные формы. Обработка воды хлорированием привела к подавлению
возбудителей кишечных инфекций, но не смогла подавить вирус гепатита.
Этому препятствовала высокая мутность исходной воды: вирусы как бы прятались
во взвешенных частицах. В 1996 г. инфицирование вирусным гепатитом при
употреблении питьевой воды было отмечено и в России.
Независимо от происхождения присутствующие в природных водах примеси
можно объединить в группы по размеру и физико-химическому состоянию.
В соответствии с классификацией, разработанной Л. А. Кульским, примеси
(загрязнения) природного и антропогенного происхождения подразделяются
на 4 группы. Первые две группы относятся к гетерогенным (неоднородным),
другие две - к гомогенным (однородным). В
зависимости от принадлежности примеси к определенной группе и производится
выбор способа очистки природных вод. К первой группе примесей относятся кинетически неустойчивые взвеси.
Это водоросли, бактерии, суспензоиды, эмульсоиды и др., снижающие прозрачность
воды (увеличивающие ее мутность). Более крупные примеси удаляются фильтрованием,
микропроцеживанием или центрифугированием, остальные удаляются механическим
путем, коагулированием, флотацией, адгезией на высокодисперсных и зернистых
материалах, агрегированием при помощи флокулянтов,
электрофильтрацией. Воздействие на бактерии тяжелых металлов (серебра
и др.), окислителей, ультразвука и ультрафиолета способствует подавлению
их жизнедеятельности.Ко второй группе относятся агрегативноустойчивые
примеси - вещества, находящиеся в коллоидной форме. Эти примеси могут
быть удалены ультрафильтрацией, окислением, адсорбцией, коагулированием.
К третьей группе относятся молекулярно-растворенные примеси, такие кие
как газы и органические вещества биологического происхождения. Для удаления
этих примесей используют аэрацию, нагревание, окисление, экстракцию,
адсорбцию на активированном угле и биохимический распад.
И наконец, четвертая группа примесей - электролиты. Их удаляют из природной
воды гиперфильтрацией (обратным осмосом), переводом в малорастворимые
соединения, сепарацией при помощи фазовых переходов, фильтрованием через
ионообменные материалы, а также с помощью электродиализа.
Как следует из данной классификации, нет абсолютно надежно способа очистки
воды от содержащихся в ней примесей, кроме, может быть, дистилляции.
К первой группе примесей относятся кинетически неустойчивые взвеси.
Это водоросли, бактерии, суспензоиды, эмульсоиды и др., снижающие прозрачность
воды (увеличивающие ее мутность). Более крупные примеси удаляются фильтрованием,
микропроцеживанием или центрифугированием, остальные удаляются механическим
путем, коагулированием, флотацией, адгезией на высокодисперсных и зернистых
материалах, агрегированием при помощи флокулянтов,
электрофильтрацией. Воздействие на бактерии тяжелых металлов (серебра
и др.), окислителей, ультразвука и ультрафиолета способствует подавлению
их жизнедеятельности.Ко второй группе относятся агрегативноустойчивые
примеси - вещества, находящиеся в коллоидной форме. Эти примеси могут
быть удалены ультрафильтрацией, окислением, адсорбцией, коагулированием.
К третьей группе относятся молекулярно-растворенные примеси, такие кие
как газы и органические вещества биологического происхождения. Для удаления
этих примесей используют аэрацию, нагревание, окисление, экстракцию,
адсорбцию на активированном угле и биохимический распад.
И наконец, четвертая группа примесей - электролиты. Их удаляют из природной
воды гиперфильтрацией (обратным осмосом), переводом в малорастворимые
соединения, сепарацией при помощи фазовых переходов, фильтрованием через
ионообменные материалы, а также с помощью электродиализа.
Как следует из данной классификации, нет абсолютно надежно способа очистки
воды от содержащихся в ней примесей, кроме, может быть, дистилляции.
Из книги "Чистая вода"Миклашевский Н.В. Королькова С.В.
ecoflash.narod.ru


















