Испарения воды растениями. Листопад. Испарения воды
Kvant. Испарение — PhysBook
Черноуцан А.И., Анфимов М. Пока вода испаряется... //Квант. — 1991. — № 11. — С. 31-33.
По специальной договоренности с редколлегией и редакцией журнала "Квант"
Понаблюдаем за испарением воды в сосуде. Наполним водой небольшую кастрюльку или стакан и будем в течение дня следить за понижением ее уровня. Процесс этот достаточно медленный, и есть время поразмышлять и сделать некоторые оценки. В частности, попробуем оценить скорость испарения и сравним ее с нашими наблюдениями.
Каков же механизм процесса испарения? Вспомним, что для превращения некоторого количества воды в пар при неизменной температуре необходимо передать воде определенное количество теплоты — так называемую теплоту парообразования. Например, при комнатной температуре (Т = 290 К) теплота парообразования составляет 2,46 кДж на каждый грамм испаренной воды. Так как в 1 г воды содержится 1/18 NA молекул, где NA = 6,02·1023 моль-1 — число Авогадро, то получаем, что для удаления из жидкости одной молекулы надо затратить энергию E1 = 7,35·10-20 Дж. В атомных расчетах принято выражать энергию в электронвольтах (эВ). Так как 1 эВ = 1,6·10-19 Дж, то E1 = 0,46 эВ.
На что же идет затраченная энергия? Ответ почти очевидный — на преодоление силы притяжения, которая действует со стороны жидкости на вылетающую молекулу. Каждая молекула взаимодействует с окружающими ее другими молекулами. Сила взаимодействия на малых расстояниях (r < r0 ~ 10-8 см) имеет характер отталкивания, а на больших (r > r0) — притяжения. В толще жидкости каждая молекула окружена другими такими же молекулами со всех сторон, и средняя результирующая сила равна нулю. В другом положении оказывается молекула, которая пытается покинуть поверхность воды и улететь в свободное пространство. Она притягивается к молекулам, расположенным на поверхности, и эта сила ничем не скомпенсирована. Поэтому, чтобы преодолеть притяжение и окончательно покинуть поверхность воды, молекула должна обладать достаточно большой кинетической энергией. Сравните: средняя кинетическая энергия поступательного движения молекул воды, равная \(~\frac 32 kT\), где k = 1,38·10-23 Дж/К — постоянная Больцмана, при T = 290 К составляет 0,038 эВ, что на порядок меньше энергии E1, которую необходимо сообщить молекуле для ее удаления из жидкости. Значит, покинуть поверхность могут лишь те немногочисленные молекулы, которые, находясь вблизи поверхности, в результате случайных столкновений приобрели энергию, на порядок большую среднего значения.
Мы теперь можем несколько иначе взглянуть на теплоту парообразования. Конечно, поглощаемое водой тепло не передается непосредственно тем молекулам, которые вылетают с поверхности. Эти молекулы получают избыточную энергию случайным образом от своего окружения. Однако в результате того, что жидкость покидают не любые, а только самые «энергичные» молекулы, на каждую оставшуюся молекулу приходится уже несколько меньшая энергетическая норма. Если жидкость не «скомпенсирует» эту потерю, поглотив из окружающей среды достаточное количество теплоты, то ее температура будет уменьшаться. Чтобы этого не произошло, к жидкости надо подвести количество теплоты, как раз равное ее теплоте парообразования.
- Иногда у школьников возникает неправильное представление о том, что вылетевшие быстрые молекулы обладают аномально большой энергией и поэтому пар должен быть горячей жидкости. Это, конечно, не так. Только в начале своего «свободного» движения молекула обладает избыточной энергией. Преодолевая силу притяжения, она теряет часть своей избыточной энергии, и средняя энергия вылетевших молекул оказывается равной средней энергии пара той же температуры.
Все это хорошо, скажете вы, но мы пока ни на шаг не продвинулись в оценке того, как быстро должна испаряться вода. Более того, стало понятно, что для проведения сколь-нибудь разумных оценок необходимо иметь гораздо более ясное количественное представление об «устройстве» жидкости и характере движения ее молекул. Но все же нам удастся проделать необходимые расчеты. И вот каким образом.
Оказывается, достаточно... мысленно поместить наш стакан с водой в закрытую банку. Через некоторое время в этой банке образуется насыщенный водяной пар, и процесс испарения прекратится. Точнее (и в этом суть!), испарение будет происходить так же, как и раньше, но количество вылетающих из жидкости молекул будет равно количеству молекул, попадающих в жидкость из пара. В таком случае говорят, что между жидкостью и паром установилось динамическое равновесие. Появляется возможность оценить интенсивность испарения косвенным путем, рассматривая не саму жидкость, а ее насыщенный пар. Выигрыш же состоит в том, что жидкость — объект очень сложный, а пар — достаточно простой. Во всяком случае, при проведении оценок насыщенный пар можно с хорошей точностью считать идеальным газом.
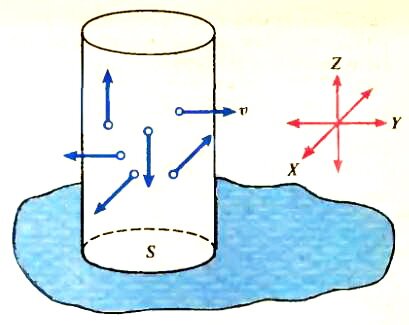
Проведем оценку, сделав некоторые упрощающие предположения. Будем считать, в частности, что все молекулы имеют одинаковую скорость υ и что они могут двигаться не в произвольном направлении, а только в одном из шести направлений, задаваемых координатными осями (одна из осей вертикальна). За одну секунду на участок поверхности жидкости площадью S попадет 1/6 часть молекул, находящихся в цилиндре высотой υ (см. рисунок):
\(~\frac{\Delta N}{\Delta t} = \frac 16 n \upsilon S\) ,где n — концентрация молекул (более детальный расчет дает множитель 1/4 вместо 1/6). Для оценки скорости υ используем известное выражение для средней квадратичной скорости \(~\upsilon_{cp} = \sqrt{\frac{3kT}{m}}\) (здесь m — масса одной молекулы), концентрацию насыщенного пара n выразим через его давление pn с помощью уравнения состояния идеального газа \(~p_n = nkT\). Тогда для массы воды, «выпадающей» из насыщенного пара на площадку S поверхности за 1 с, получаем
\(~\frac{\Delta m}{\Delta t} = \frac 16 m n \upsilon_{cp} S = \frac 16 p_n S \sqrt{\frac{M}{3RT}}\) ,где М — молярная масса воды, R — универсальная газовая постоянная. Подставляя численные данные (pn при 17 °С составляет 0,02·105 Па), получим, что за 1 с на 1 см2 поверхности из насыщенного пара поступает 0,16 г воды. Если предположить, что с такой же скоростью происходит испарение, то уровень воды в сосуде должен был бы опускаться на 1 см каждые 6 секунд!
Ясно, что это совсем не похоже на реальную картину. Мы потерпели очень поучительное поражение, и теперь необходимо разобраться в его причинах. Обсудим некоторые из них.
Первая причина кроется в самом эксперименте. Реальный процесс испарения существенно замедляется из-за того, что воздух в комнате не сухой, а влажный. Причем сама по себе влажность порядка 60—80 % приводила бы к замедлению процесса испарения всего в 3—4 раза. Но если не создавать потока воздуха возле поверхности воды (например, включив вентилятор), то влажность непосредственно возле поверхности оказывается достаточно близкой к 100 % и процесс испарения замедляется еще во много раз. Наша же оценка скорости испарения относится к идеальному случаю, когда обратное поступление молекул на поверхность полностью отсутствует.
Оказывается, однако, что и в этом идеальном случае мы ошибаемся примерно в 30 раз, но эта ошибка связана уже с самим расчетом. Дело в том, что только 3—4 % молекул, подлетающих к поверхности, захватываются этой поверхностью («прилипают») и попадают внутрь жидкости. Остальные же молекулы отражаются обратно.
Подведем окончательный итог. Если бы абсолютно сухой поток воздуха подхватывал все вылетевшие молекулы, поверхность воды в сосуде опускалась бы на 1 см не за 6 секунд, а за 3 минуты. Но все равно куда быстрее, чем можно было ожидать. Не правда ли?
www.physbook.ru
Испарения воды растениями. Листопад. | Биология
Вода всегда присутствует в клетке. Она обеспечивает сложные процессы жизнедеятельности. Без воды клетка погибает.
Испарение воды листьями
Вода поступает в растение из почвы в больших количествах, но для фотосинтеза ее надо совсем немного. Большая часть воды испаряется. Доказать процесс испарения и роль листьев в нем можно опытным путем. Для этого необходимо срезать два одинаковых побега с листьями. У одного из них листья удалить. Побеги поместить в две пробирки, заполненные водой до одинакового уровня. Добавить несколько капель растительного масла (чтобы исключить испарение с поверхности воды). Третью пробирку с таким же количеством воды и масла оставить без побега, используя в качестве контроля. Уже на следующие сутки будет получен результат: уровень воды в пробирке с побегом, несущим листья, понизится значительно сильнее, чем в пробирке с безлистным побегом. Очевидно, что побег с листьями испаряет воды больше, чем побег без листьев, значит, большая часть воды, поступающей в растение, испаряется листьями.

Водяной пар образуется на поверхности клеток мякоти листа, скапливается в межклетниках и выходит через устьичные щели. Открывая или уменьшая устьичные щели, растение увеличивает или уменьшает скорость испарения. При закрытых устьицах пар не выходит наружу, а накапливается в межклетниках.

Условия, влияющие на испарения
Интенсивность испарения зависит от условий обитания растений: силы ветра, температуры и влажности. При высокой температуре, ярком освещении, небольшой влажности, ветре испарение сильнее, чем в тихую пасмурную погоду. У растений, испытывающих недостаток влаги, небольшие листовые пластинки и, соответственно, небольшое число устьиц.
Значение испарения для растений
Испарение поддерживает непрерывный ток воды с растворенными минеральными веществами по растению в восходящем направлении. Чем интенсивнее испарение, тем быстрее передача воды от корней к листьям. При испарении происходит охлаждение организма, что особенно важно для растений жарких и солнечных мест обитания. Если нарушен процесс испарения, растение на солнце страдает от ожогов.
Листопад
Листопадом называют естественное отделение листьев от стебля при их отмирании. На стебле в безлистном состоянии остаются почки. Многолетние растения, которые какой-то отрезок времени в году лишены листьев, называют листопадными (липа, береза, лиственница). Растения, у которых листья сохраняются в течение всего года, называют вечнозелеными (ель, сосна, можжевельник, брусника). С листопадом прекращается испарение. Если бы зимой сохранялись листья у листопадных деревьев и кустарников, то растения погибли бы от иссушения. Игольчатые листья хвойных растений приспособлены к уменьшению испарения: имеют небольшую поверхность хвоинок, толстые оболочки клеток кожицы, мощный восковой налет. Название «вечнозеленые» не означает, что растения сохраняют листья в течение всей жизни. Листопад у таких растений происходит, но опадают только старые листья, а молодые сохраняются. Например, листья у ели сохраняются 5—7 лет, у сосны — 3—4 года, у брусники — больше года.

ebiology.ru
Вода испарение - Справочник химика 21
Химические явления с точки зрения атомно-молекулярной теории. Элементы входят в состав различных сложных веществ в форме отдельных атомов, но не целых молекул. Например, молекула воды хотя и содержит два атома водорода, но в ней нет ни одной молекулы этого вещества (газа водорода вода не содержит), точно так же, как нет ни одной молекулы газа водорода и в молекуле сахара, содержащей 22 атома водорода. При замерзании воды, испарении ее, конденсации паров в жидкую воду состав этого вещества не изменяется. Подобные явления относятся к разряду физических. Однако, если бросить на воду кусочек металлического натрия, наблюдается явление совсем иного рода атомы натрия вытесняют из молекул воды атомы водорода и сами становятся на их место. В результате образуются молекулы едкого натра, имеющие иной атомный состав, чем молекулы воды молекула воды состоит из двух атомов водорода и одного атома кислорода, а молекула едкого натра содержит по одному атому натрия, водорода и кислорода. Действие натрия на воду—явление химическое. Следовательно [c.33] Испарение воды прн нагревании пробы масла осуществляют в приборе Дина—Старка смесь обводненного масла с растворителем нагревают на песчаной бане, а сконденсировавшуюся воду собирают в ловушке. При этом методе возможны значительные ошибки, связанные с потерями части воды при анализе, а чувствительность составляет 0,025% (масс.) воды. Испарение воды осуществляют и при анализе масел с помощью лабораторного влагомера ВМЛ-2. Принцип его действия основан на измерении парциального давления паров воды, образующихся при нагреванип пробы масла, помещенной в испарительную камеру прибора. Давление паров передается через разделительную камеру на манометр, шкала которого градуирована в объемных процентах влажности. На таком же принципе основан зарубежный прибор [10], в котором для создания вакуума (с целью удаления растворенных в масле газов) и для компенсации теплового расширения масла прн нагревании применяют подвижный поршень. [c.36]Прочный незакрепленный слой полиамидного сорбента можно получить, если полиамид растворить в 75%-ной муравьиной кислоте при перемешивании. Полученный вязкий раствор (20 г полиамида в 100 мл кислоты) намазывают на пластинку слоем определенной толщины. Затем пластинку помещают в горизонтальном положении в камеру, насыщенную парами воды. Испарение кислоты продолжается в течение 48 ч при 26—29° С. После этого пластинку прогревают 15 мин при 100° С. Получаются прочные непористые слои, пригодные для длительного хранения. [c.138]
После загрузки катализатора установку герметизируют и опрессовывают в атмосфере азота. Убедившись в герметичности установки, начинают нагревание катализатора. Удобно, если температура каждого следующего реактора выше, чем предыдущего, причем разница температур между первым и последним реакторами составляет 28 °С. Это предотвращает конденсацию воды, испаренной в предыдущих по ходу потока реакторах. После достижения температур 370—430 °С поток азота заменяют на водород высокой чистоты и начинают восстановление оксидной формы катализатора. [c.151]
Первичная переработка нефти включает процессы ее очистки от солей и воды, испарения основных фракций в трубчатых печах и разделения на фракции в ректификационных колоннах. Наиболее часто крекингу подвергают фракции нефти, конденсирующиеся при 300—500 °С. Широко применяемый в крекинге алюмосиликатный катализатор (см. стр. 105) отравляется примесями, которые могут находиться в крекируемом нефтепродукте [19, 20, 21]. Сильное, но обратимое отравление алюмосиликатного катализатора происходит при наличии в сырье азотистых соединений. Необратимо отравляется катализатор соединениями щелочных металлов. Снижают активность катализатора соединения никеля, железа, ванадия и других тяжелых металлов. Нарущается работа катализатора при значительном содержании водяных паров. Для крекинга применяют дистиллаты нефти, не содержащей значительных количеств катализаторных ядов, или же подвергают нефть (или крекируемый дистиллат) очистке от сернистых соединений гидрированием. [c.15]
Нет. При испарении воды с ней не происходит никаких химических изменений. Пары воды как химическое вещество представляют собой ту же самую воду. Испарение воды является чисто физическим процессом. [c.65]
Абсорбция NHg серной кислотой Абсорбция паров HjO серной кислотой Испарение HjO Абсорбция Nh4 водой Испарение HjO То же [c.571]
Нефтешламы, образующиеся при добыче нефти, представляют собой аномально устойчивые эмульсии, постоянно изменяющиеся под воздействием атмосферы и различных процессов, протекающих в них. С течением времени происходит естественное старение эмульсий за счет уплотнения и упрочнения бронирующих оболочек на каплях воды, испарения легких фракций, окисления и осмоления нефти, перехода асфальтенов и смол в другое качество, образования коллоидно-мицеллярных конгломератов, попадания дополнительных механических примесей неорганического происхождения. [c.7]
Количество воды, испаренной в аппарате 2.6 1,16 1,15 1,20 2,12 2,0 1.0 1,00 [c.70]
Исходное сырье с массовым содержанием н-бутиленов = 78% поступает в трубное пространство испарителя 1 и отбойника-перегревателя 2, обогреваемых горячей водой. Испарение происходит при 50 °С и избыточном давлении 0,5 МПа. Затем пары н-бутиленов поступают в первый змеевик трубчатой двухпоточной печи 3, где они перегреваются топливным газом до 430—440 °С. Во втором змеевике перегревается водяной пар до 750—780 °С. [c.40]
Попавшая в воду океана нефть подвергается воздействию природных факторов (ветер, течения, приливы и отливы), происходят испарение, растворение, эмульгирование, усвоение живыми организмами, химические и фотохимические превращения. Скорость распространения нефти на поверхности моря составляет 60 % от скорости течения и 2-4 % от скорости ветра. При дрейфе нефтяного пятна загрязняются все новые порции воды. Испарение интенсивно в течение первого получаса после разлива, когда нефть можно поджечь, позже на поверхности моря остается мало летучих соединений. К концу 1 суток испаряется 50 % соединений с С13-С14, к концу 3-ей недели — 50 % соединений с С17. [c.625]
По характеру выбросы можно разделить на организованные и неорганизованные. К организованным относятся выбросы, которые отводятся в атмосферу, водоемы и в почву с помощью специальных сооружений это — очистные сооружения, дымовые трубы и трубы газомоторных компрессоров, заводские факелы,, печи сжигания шламов и других отходов, патрубки вентиляционных систем, шламовые площадки и илонакопители и т. д. К неорганизованным относятся выбросы, которые невозможно-объединить и отвести в ту или иную среду. Например, утечки через неплотности в аппаратах и арматуре, испарение с поверхности сточной жидкости в системах канализации и очистки сточных вод, испарение продуктов из резервуаров и хранилищ, розливы и залповые выбросы нефтепродуктов при авариях и пожарах, а также выбросы нефтепродуктов в атмосферу при продувках и пропаривании аппаратов и при спусках нефтепродуктов в. канализацию перед проведением ремонтных работ и т. д. [c.14]
Точно определить количество свободной и связанной воды невозможно. В одном из методов определения условно свободной считают воду, которая выделяется из осадка под действием силы тяжести при длительном его фильтровании. Другой метод определения количества свободной воды, тоже условный, заключается в сушке осадка при постоянной температуре. За свободную в этом методе принимают воду, испарение которой из осадка происходит с постоянной скоростью. Нагревание осадка приводит к разрушению коллоидных структур и частичному переходу коллоидно-связанной воды в свободную, поэтому при сушке совместно определяют количество свободной воды и часть коллоидно-связанной воды. [c.137]
Воздух — вода (испарение) [c.426]
Рис, VI1-7. Охлаждение воды испарением. [c.476]
До температуры воздуха 100°С — температуры кипения воды — испарение последней с поверхности пластин может происходить только до его насыщения, после этого испарение воды прекращается. Чем выше температура воздуха, тем быстрее и больше испаряется влаги до его насыщения. Обычно параметр влажности воздуха дается относительной влажностью. Под относительной влажностью понимается отношение количества влаги в воздухе в данный момент при данной его температуре к количеству влаги, насыщающей воздух при этой же температуре. Если, к примеру, относительная влажность воздуха ф=20%, то это значит, что воздух сухой и сушка происходит быстро если ф = 90%, то воздух влажный и скорость сушки замедляется. При ф=100% влага не испаряется и сушка не происходит. [c.219]
Следовательно, точки Р п 61 соответствуют тому же значению энтальпии. В действительности вода не подогревается даже до температуры I о пото му, что при этом отсутствовал бы перепад температур, необходимый для теплообмена. Вода можег нагреваться только до температуры по крайней мере на 2° ниже 01, т. е. до tN Это означает, что при возможно минимальной разности температур в скруббере, орошаемом водой при температуре газ достигнет состояния 8, отобрав от воды количество тепла ах = 1в—/л. Ввиду того что удельная энтальпия воды изменяется в зависимости от температуры почти линейно и количество воды, испаренной в скруббере, или количество водяного пара, сконденсировавшегося в предварительном холодильнике, невелико по сравнению с количеством циркулирующей воды, рабочие линии воды для этих аппаратов представляют собой прямые МЫ, параллельные друг другу. Количество циркулирующей воды (в кг,1нм поступающего сухого газа). можно приближенно вычислить по формуле [c.233]
К физико-химическим способам относятся аэрация, экстрак-Ц ИЯ, адсорбция, отгонка с водяным паром, а также очистка сточных вод испарением с выделением примесей в осадок. [c.41]Однако вода не всегда доступна. Например, в районах с жарким климатом часто ощущается острый недостаток в воде. Стоимость воды резко сказывается на эксплуатационных расходах предприятия. Снижение расхода воды на холодильниках дает большую экономию, поэтому весьма целесообразно повторное использование отходящей с конденсатора воды, для чего ее нужно охладить. Охлаждают воду испарением. Интенсивное испарение, а значит и интенсивное охлаждение воды происходит при увеличении поверхности соприкосновения воды с воздухом и скорости циркуляции. [c.165]
Сжигание фенольных вод путем инжектирования их в топки паровых котлов на многих заводах сняло с повестки дня проблему очистки сточных вод. Испарение сточных вод при высоких температурах в топочном пространстве происходит почти мгновенно и органические примеси сточных вод сгорают безостановочно. [c.439]
Чтобы узнать растворимость или коэффициент ее, поступают различно. Или приготовляют заведомо (т.-е. с явным избытком растворяемого тела) насыщенный при данной температуре раствор и в нем определяют количество воды (испарением, сушением или другими способами) и растворенного тела, или, как эго делается для газов, берут определенные количества воды и избыток растворяющегося тела и определяют количество нерастворенного остатка. Растворимость, значит, определяется не иначе, как в присутствии избытка растворяемого вещества, т.-е. отвечает равновесию между раствором, взятым в определенном количестве (это одна фаза , или одно однородное вещество), и растворяющимся телом (другая фаза , как говорят ныне при рассмотрении равновесий соприкасающихся веществ). [c.386]
При разрушении горных пород образуются растворимые соли, которые выносятся дождевой водой в реки, а оттуда — в моря и океаны. Вода океанов постепенно испаряется и содержание растворенных в ней солей увеличивается. Поэтому морская вода содержит наибольшее количество растворенных солей. Среднее содержание этих солей в морской воде составляет около 3,5 /о. В морях, в которых имеется особенно сильное испарение и недостаточно большой приток пресной речной воды, содержание солей превышает среднюю норму. Например, в Средиземном и Красном морях содержание различных солей больше, чем в воде океанов, оно достигает 4 /о. Вода же Балтийского и Белого морей содержит меньшее количество солей, так как все время опресняется речной водой испарение ее значительно меньше, чем в морях южных широт. [c.85]
До температуры воздуха 100° С — температуры кипения воды — испарение последней с поверхности пластин может происходить только до его насыщения, после этого испарение воды прекращается. Чем выше температура воздуха, тем быстрее п больше испаряется влаги до его насыщения. Обычно параметр влажности воздуха дается относительной влажностью. Под относительной влажностью понимается отношение количества влаги в воздухе в данный момент при данной его температуре к коли- [c.224]
Метод очистки воды испарением [c.122]
Тепло, уносимое парами воды, испаренными из масла Q = 1040-656 = 683 ООО ккал ч, [c.197]
Изменение концентрации раствора путем изотермического испарения воды. При удалении воды испарением при постоянной температуре относительное содержание соли в ненасыщенном растворе будет непрерывно увеличиваться и фигуративная точка М будет перемещаться вдоль абсциссы до тех пор,, пока не попадет на кривую насыщения в точке N1. [c.48]
В связи с быстро возрастающим дефицитом воды во всем мире большое значение приобретает использование воздуха как хладагента. Теплофизические свойства воздуха неблагоприятны (малые теплоемкость, теплопроводность и плотность). Поэтому коэффициенты теплоотдачи к воздуху ниже, чем коэффициенты теплоотдачи к воде. Это приводит к увеличению поверхностей теплообмена и, как следствие, к возрастанию металлоемкости оборудования. Для устранения этого недостатка необходимо применять следующие меры повысить скорости движения воздуха, что вызывает увеличение коэффициента теплоотдачи оребрить трубы со стороны воздуха, что даст увеличение эффективной поверхности теплообмена распылять в воздух воду, испарение которой понизит температуру воздуха и увеличит за счет этого движущую силу процесса теплообмена. Во избежание отложения солей на поверхности теплообменника распыляемая вода должна быть чистой. Принципиальная схема воздушного холодильника приведена на рис. IV. 29. Холодильник представляет собой пучок труб 1 с наружным оребрением. Концы труб герметично укреплены в коллекторах 3 и б. Охлаждаемая среда подается в верхний коллектор через штуцер 4, проходит внутри труб и отводится через штуцеры 5. Движение воздуха с большой скоростью вдоль оребренной наружной поверхности труб обеспечивается с помощью осевого вентилятора 7, снабженного электродвигателем 8. В засасываемый вентилятором воздух форсунками 9 распыляется вода. Регулирование процесса осуществляется с помощью жалюзей 2, установленных снаружи. Угол наклона жалюзей регулируется с помощью приводного механизма. Поскольку количество отводимой теплоты пропорционально разности температур, применение атмосферного воздуха в качестве хладагента особенно целесообразно в тех случаях, когда не требуется охлаждения до ннзкой температуры, например в конденсаторах ректификационных установок. [c.364]
Коллоидный раствор кремниевой кислоты в концентрации порядка 200—250 г/л (кремнезоль) применяется для нанесения защитных, а в смеси с молотым кварцевым стеклом, цирконом или другими минеральными зернами — огнеупорных покрытий на различные трубы, сталеразливочные изложнгщы и т. п. При нанесении их путем распыления воздух может загрязняться аэрозольными частицами, которые, после потери части воды испарением, превращаются в частицы, аналогичные силикагелю. [c.378]
Добыча поваренной соли осуществляется главным образом тремя способами 1) горнопромышленной разработкой кажнной соли, 2) растворением каменной соли под землей и выпаривания полученного рассола, отчасти также выпариванием природных рассолов З) из морской воды испарением в так называемых соляных садках , а в условиях холодного климата — вымораживанием. [c.214]
Из недавних исследований можно назвать работу Скрибнера и Котеки [302], в которой проводилась экстракция трифторацетил-ацетонатов двухвалентных металлов хлороформом, содержащим изобутиламин. Чистый хлороформ слабо экстрагирует трифтор-ацетилацетонаты №, 7п, С(1 и Со, поскольку они содержат гидрат-ную воду. Испарением экстрактов выделены соединения ZIlA2 B, РЬАг 4В и МАг 2В, где А — трифторацетилацетон, В — изобутиламин, а М = Си, №, Со, С(1. [c.102]
Испытание на активность образцов катализаторов проводили на лабораторной установке (рис. 3) в проточном интегральном реакторе с неподвижным слоем катализатора. Установка включает электронагревательную печь с реактором из стали Х25Т, узлы дозирования сырья и воды, испарения воды и перегрева водяного пара, конденсации и охлаждения продуктов реакции [c.9]
Пары воды из нижних досушивателей отводятся через патрубки 29, соединяющиеся в общую трубу 30, по которой пары поступают в один из бункеров над верхними досушивателями, т. е. внутрь кожуха сушилки, откуда и отводятся вместе с парами воды, испаренной на валках и в верхних досушивателях. При такой системе отвода паров воды из нижних досушивателей содержащаяся в этих парах пыль высушиваемого красителя оседает в кожухе сушилки и пары выходят из сушилки частично обеспыленными. [c.40]
Для химической механики весьма важно отличить обратимые реакции от необратимых. Вещества, могущие реагировать друг на друга при данной температуре, дают такие тела, которые при той же температуре или могут, или не могут давать первоначальные вещества. Так, напр., соль растворяется в воде при обыкновенной температуре, но получающийся раствор может распадаться при той же температуре, оставляя соль и выделяя воду испарением. Сернистый углерод происходит из серы и угля при такой температуре, при которой может и обратно давать серу и уголь. Железо выделяет при некоторой температуре водород из воды, образуя окись железа, но она при той же температуре с водородом может давать железо и воду. Очевидно, что если тела А и В дают С и В реакция обратима (т.-е. С и 13 дают А и В), то, взяв определенную массу А и В, или им соответственную массу С и В, мы получим в обоих случаях все четыре тела, т.-е. наступит между реагирующими веществами химическое равновесие (или распределение). Увеличивая массу одного из веществ, получим новые условия равновесия, так что обратимые реакции доставляют возможность изучать влиявие массы на ход химических превращений. Примерами необратимых химических реакций могут служить многие из тех, которые происходят с очень сложными соединениями и смесями. Так, многие сложные вещества организмов (растений и животных) в жару распадаются, но ни при этой температуре, ни при других продукты распадения не дают сами по себе первоначального вещества. Порох, как смесь селитры, серы и угля, сгорая, дает газы и пороховой дым, которые ни при какой температуре обратно не дают начальных веществ. Чтобы их получить, необходим обходный путь — соединения по остаткам. Если А прямо ни при каких условиях не соединяется с В, то это еще не значит, что не может быть по.лучено соединение АВ. Часто А можно соеди- [c.45]
Перемена направления течений, характерная для эстуарной циркуляции (протнвоэстуарная циркуляция), ведет к обеднению воды питательными веществами. Примером может служить Средиземное море, которое является наиболее обедненным из крупных водоемов. Проти-ваэстуарная циркуляция происходит в результате того, что в Средиземном море испарение превышает поступление пресной воды примерно на 4% [7]. Следовательно, значительно больший объем воды втекает через Гибралтарский пролив, чем требуется для замены потерь воды испарением. [c.26]
chem21.info
Испарение — Юнциклопедия
Испарение — переход вещества из жидкого состояния в газообразное (парообразное). Оно происходит с открыток, свободной поверхности, отделяющей жидкость от газа, например с поверхности открытого сосуда, с поверхности водоема и т. д. Испарение происходит при любой температуре, но для всякой жидкости с повышением температуры скорость его увеличивается. Объем, занимаемый данной массой вещества, при испарении скачком возрастает.
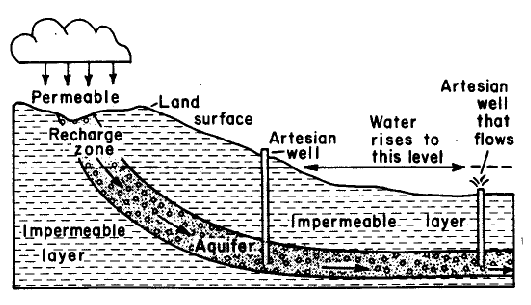
 Облака на небе, иней на деревьях — это все следствия процессов испарения воды и конденсации водяного пара.
Облака на небе, иней на деревьях — это все следствия процессов испарения воды и конденсации водяного пара. 
Следует различать два основных случая. Первый, когда испарение происходит в замкнутом сосуде и температура во всех точках сосуда одинакова. Так, например, испаряется вода внутри парового котла или в чайнике, закрытом крышкой, если температура воды и пара ниже температуры кипения. В этом случае объем образующегося пара ограничен пространством сосуда. Давление пара достигает некоторого предельного значения, при котором он находится в тепловом равновесии с жидкостью; такой пар называется насыщенным, а его давление — упругостью пара. Второй случай, когда пространство над жидкостью незамкнутое; так испаряется вода с поверхности пруда. В этом случае равновесие не достигается практически никогда, и пар ненасыщенный, а скорость испарения зависит от многих факторов.
Мерой скорости испарения является количество вещества, улетающего в единицу времени с единицы свободной поверхности жидкости. Английский физик и химик Д. Дальтон в начале XIX в. нашел, что скорость испарения пропорциональна разности между давлением насыщенного пара при температуре испаряющейся жидкости и действительным давлением того реального пара, который над жидкостью имеется. Если жидкость и пар находятся в равновесии, то скорость испарения равна нулю. Точнее, оно происходит, но с той же скоростью происходит и обратный процесс — конденсация (переход вещества из газообразного или парообразного состояния в жидкое). Скорость испарения зависит также от того, происходит ли оно в спокойной атмосфере или движущейся; скорость его увеличивается, если образующийся пар сдувается потоком воздуха или откачивается насосом.
Если испарение происходит из жидкого раствора, то разные вещества испаряются с разной скоростью. Скорость испарения данного вещества уменьшается с увеличением давления посторонних газов, например воздуха. Поэтому испарение в пустоту происходит с наибольшей скоростью. Напротив, добавляя в сосуд посторонний, инертный газ, можно очень сильно замедлить испарение.
При испарении вылетающие из жидкости молекулы должны преодолеть притяжение соседних молекул и совершить работу против удерживающих их в поверхностном слое сил поверхностного натяжения. Поэтому, чтобы испарение происходило, испаряющемуся веществу надо сообщить тепло, черпая его из запаса внутренней энергии самой жидкости или отбирая у окружающих тел. Количество тепла, которое нужно сообщить жидкости, находящейся при данной температуре и фиксированном давлении, чтобы перевести ее в пар при этой же температуре и давлении, называется теплотой испарения. Упругость пара растет с ростом температуры тем сильнее, чем больше теплота испарения.
Если к испаряющейся жидкости не подводить тепла извне или подводить его недостаточно, то жидкость охлаждается. Вот почему, оставив мокрую руку на воздухе, мы ощущаем холод. Заставляя жидкость, помещенную в сосуд с нетеплопроводными стенками, усиленно испаряться, можно добиться значительного ее охлаждения. Согласно кинетической теории, испаряются наиболее быстрые молекулы, средняя энергия остающихся в жидкости молекул убывает — вот почему жидкость охлаждается.
Иногда испарением называют также сублимацию, или возгонку, т. е. переход твердого вещества в газообразное состояние. Почти все их закономерности действительно похожи. Теплота сублимации больше теплоты испарения приблизительно на теплоту плавления.
При температурах ниже температуры плавления давление насыщенных паров большинства твердых тел очень мало, и их испарение практически отсутствует. Бывают, однако, исключения. Так, вода при 0 °C имеет давление насыщенных паров 4,58 мм рт. ст., а лед при −1 °C — 4,22 мм рт. ст. и даже при −10 °C — всё еще 1,98 мм рт. ст. Этими сравнительно большими упругостями водяного пара объясняется легко наблюдаемое испарение твердого льда, в частности известный всем факт высыхания мокрого белья на морозе.
yunc.org
Испарение - вода - Большая Энциклопедия Нефти и Газа, статья, страница 1
Испарение - вода
Cтраница 1
Испарение воды и создание разности давлений ( движущий напор) вызывают движение среды в контуре. [1]
Испарение воды из жидкого стекла также может вызвать разложение сложных полисиликатов натрия на более простые, сопровождающееся выпадением осадка. В обоих случаях модуль жидкого стекла изменяется. Использование жидкого стекла с изменяющимся модулем в производстве катализатора не рекомендуется, так как это приводит к повышенному растрсскивапию катализатора при сушке. [2]
Испарение воды следует вести нагреванием в струе хлористого водорода, так как иначе произойдет гидролитическое разложение. [3]
Испарение воды по всей длине змеевика увеличивает концентрацию кислоты и этим ускоряет гидролиз пероксомоносерной кислоты до перекиси водорода. Образование перекиси водорода, по-видимому, происходит главным образом у выхода, где находится кислота высокой концентрации. После этого производится разделение жидкости и пара. Жидкость подается на верхнюю часть пасадочной фарфоровой колонны, а в кубовую часть ее поступает пар в противотоке к жидкости. Этот пар дает теплоту, необходимую для гидролиза остаточных пероксосер-ных кислот, одновременно предотвращая образование в жидкости кислоты слишком высокой концентрации. Большая часть остающегося в жидкости активного кислорода при этом превращается в перекись водорода и уходит в виде пара. Жидкость, выходящая из колонны, содержит некоторое количество перекиси водорода и обе пероксосерпые кислоты в количестве, эквивалентном 2 6 г пероксодисерной кислоты па 100 см3 раствора; при протекании этой жидкости через катодные пространства ванн происходит разложение этих соединений за счет электролиза. [4]
Испарение воды листьями растений ( транспирация) хотя и является в своей основе физическим процессом, но осложняется различным ходом биологических процессов. [5]
Испарение воды, находящейся в сосудах 2, приводит к понижению температур косынки и соответственно горячих спаев термобатареи. [7]
Испарение воды в газовую фазу, представленную в основном метаном, по-видимому, может приводить к росту минерализации той части воды, которая остается в жидком виде. Подобные процессы могут играть значительную роль лишь при очень высокой насыщенности водовмещающих толщ углеводородными газами, следовательно, развиты только локально J ( CM. [8]
Испарение воды уменьшается пропорционально количеству растворенных в ней твердых веществ. [9]
Испарение воды кожей является мощным приспособлением, посредством которого человек и теплокровные животные сохраняют постоянную температуру в организме при усиленном образовании тепла в организме или при высокой температуре внешней среды. [10]
Испарение воды кожей является мощным приспособлением, посредством которого человек и теплокровные животные сохраняет постоянную температуру в организме при усиленном образовании тепла в организме или при высокой температуре внешней среды. [11]
Испарение воды указывает на непрерывное движение ее молекул. [12]
Испарение воды из ванны пополняется непрерывным притоком свежей дистиллированной воды, регулируемым так, чтобы уровень раствора в ванне оставался постоянным. [13]
Испарение воды при нагревании пробы масла осуществляют в приборе Дина-Старка; смесь обводненного масла с растворителем нагревают на песчаной бане, а сконденсировавшуюся воду собирают в ловушке. При этом методе возможны значительные ошибки, связанные с потерями части воды при анализе, а чувствительность составляет 0 025 % ( масс.) воды. Испарение воды осуществляют и при анализе масел с помощью лабораторного влагомера ВМЛ-2. Принцип его действия основан на измерении парциального давления паров воды, образующихся при нагревании пробы масла, помещенной в испарительную камеру прибора. Давление паров передается через разделительную камеру на манометр, шкала которого градуирована в объемных процентах влажности. На таком же принципе основан зарубежный прибор [10], в котором для создания вакуума ( с целью удаления растворенных в масле газов) и для компенсации теплового расширения масла при нагревании применяют подвижный поршень. [14]
Испарение воды в объеме испарителя приводит к повышению концентрации примесей, введенных с питательной водой. Часть примесей при этом меняет характер, газообразные примеси десорбируют вместе с паром. Увеличение концентраций примесей приводит к возможности образования твердой фазы в виде накипи на теплообменных поверхностях и в виде шлама в объеме воды. [15]
Страницы: 1 2 3 4
www.ngpedia.ru
2. Физика процесса испарения с поверхности воды.
2.1 Физическое явление - испарение.
Испарение - это процесс, при котором вещество из жидкого или твердого состояния переходит в пар. В случае перехода вещества из твердого состояния непосредственно в парообразное - процесс чаще называют возгонкой. Обратный - переход пара в воду называют конденсацией. Водяной пар, конденсируясь в атмосфере, образует облака, а затем и осадки, выпадающие на землю.
Рассмотрим испарение в замкнутом объеме. Известно, что молекулы жидкости, обладая кинетической энергией, постоянно совершают колебательные движения. Скорость их движения является важным показателем их кинетической энергии. При колебательном движении в пар переходят молекулы воды, обладающие наибольшей скоростью движения по сравнению с другими молекулами. Чтобы оторваться от поверхности воды испаряющаяся молекула должна преодолеть силы притяжения со стороны оставшихся молекул, а также внешнее давление уже образовавшегося пара над этой поверхностью. При испарении температура воды понижается. Объясняется это тем, что жидкость покидают молекулы, обладающие наибольшей энергией по отношению к другим молекулам при данной её температуре. Чтобы температура жидкости не понижалась, её необходимо непрерывно нагревать. Количество теплоты, необходимое для поддержания постоянной температуры называют удельной теплотой испарения. Т.о, испарение воды сопровождается затратой энергии, характеризующейся количеством теплоты, которое нужно сообщить единице её массы, имеющей температуру 1, чтобы превратить её в пар при той же температуре.
Испарение происходит при любой температуре. Но с её возрастанием скорость испарения увеличивается, так как интенсивность теплового движения молекул в этом случае также возрастает. Одновременно с испарением наблюдается процесс конденсации водяного пара, т.е. происходит непрерывный обмен молекулами между этими фазами. В зависимости от преобладания первого или второго процесса над водной поверхностью будет наблюдаться насыщенный водяной пар, динамическое равновесие или перенасыщенный водяной пар. Указанные состояния водяного пара в воздухе можно характеризовать соответствующими разностями давления водяного пара: ℮0 - ℮ > 0, ℮0- ℮ = 0, ℮0- ℮ < 0, где ℮0 - давление насыщенного водяного пара в воздухе, определяемое по температуре поверхности воды; ℮ - парциальное давление водяного пара в воздухе. Разность ℮0- ℮ - дефицит насыщения воздуха.
Итак, в замкнутом объеме интенсивность испарения зависит от температуры поверхности воды, определяющей значение ℮0 , и фактического парциального давления водяного пара ℮ над испаряющей поверхностью. Чем выше температура воды и ниже фактическое парциальное давление водяного пара, тем больше испарение. В естественных условиях температура воды и влажность воздуха непостоянные и зависят от многих факторов: солнечной радиации, радиационного излучения подстилающей поверхности, стратификации атмосферы, скорости воздушного потока и др.
Методы расчета испарения с водной поверхности.
Оценка испарения с водной поверхности может быть произведена с использованием нескольких методов. Большое количество методов вызвано тем, что сложный механизм взаимодействия между водной поверхностью водоема и прилегающей к ней воздушной массой полностью не раскрыт. Более точным из разработанных методов считается инструментальный (прямой) метод, т. е. метод непосредственного измерения слоя испарившейся воды с помощью водных испарителей. К прямому методу относится и пульсационный метод. Однако они не всегда могут быть применены вследствие их трудоемкости и невозможности использования при разработке проекта. Поэтому для определения испарения с поверхности воды применяют косвенные методы, основанные на использовании уравнений водного и теплового балансов, турбулентной диффузии водяного пара в атмосфере, а также производят расчёт по метеорологическим данным с помощью эмпирических формул.
studfiles.net