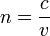Относительная диэлектрическая проницаемость. Диэлектрическая проницаемость воды
Диэлектрическая проницаемость различных веществ, в т.ч. основных диэлектриков.
| ||
Диэлектрическая проницаемость воды, зависимость от концентрации
По мнению Глаубермана и Юхновского правильный учет зависимости диэлектрической проницаемости воды от концентрации раствора, а также учет высших приближений бинарной функции распределения должны привести к еще лучшему согласию теории и эксперимента. [c.439]Рассмотренный метод аналитической экстраполяции имеет некоторые преимущества перед методом, при котором Рох> находится по зависимости Рг от концентрации, так как производимая экстраполяция, во-первых, имеет линейный ход и, во-вторых, позволяет уменьшить ошибки, возникающие в результате загрязнения раствора примесями. Значение диэлектрической проницаемости растворителя может быть найдено путем экстраполяции зависимости диэлектрической проницаемости раствора от концентрации растворенного вещества к Х2=0. Если между значениями диэлектрической проницаемости растворителя, определенной экстраполяцией и непосредственно измеренной, имеется существенная разница, выходящая за пределы ошибок опыта, то надо полагать, что в растворе находятся примеси. В частности, в процессе проведения опыта растворитель может поглотить пары воды, что приведет к увеличению значения диэлектрической проницаемости. [c.51]
Недостаточная общность правила Каблукова — Томсона — Нернста, не учитывающего специфику растворяемого вещества, очевидна, так как в одном и том же растворителе, обладающем вполне определенной диэлектрической проницаемостью (например, в воде), одни вещества диссоциируют полностью (НС1), а другие очень слабо (СНзСООН). Часто наблюдается значительная электропроводность раствора при малом значении диэлектрической проницаемости растворителя. Зависимость электропроводности не- водных растворов электролитов от концентрации нередко носит сложный характер. [c.413]Отметим, что в противоположность подходу Бейтса и Робинсона, в цитированных работах которых игнорируется изменение диэлектрической проницаемости воды в окрестности гидратируемого иона, авторы работ [94, 95, 97] видят основную причину различной зависимости и у от концентрации электролита как раз в различном изменении диэлектрических свойств растворителя вблизи ионов. Именно указывается, что диэлектрическая проницаемость воды, находящейся в непосредственной близости к иону (гидратная оболочка), будет уменьшаться тем сильнее, чем больше заряд иона и меньше его размеры— вплоть до диэлектрического насыщения соответственно будет возрастать напряженность электрического поля в окрестности иона. Поэтому при одинаковых зарядах электростатическое взаимодействие будет наиболее сильным между ионами малого размера, а при одинаковых ионных радиусах — между ионами с наибольшим зарядом. Поскольку анионы, как правило, обладают большими размерами, чем катионы, то взаимное отталкивание катионов ( - — - -взаимодействие) будет проявляться сильнее, а взаимное отталкивание анионов [c.69]
Таким образом, неприложимость уравнения Робинсона — Стокса не может быть оправдана тем, что в неводных растворах эффект сольватации меньше, чем в воде. Отсутствие минимума в неводных растворах с низкой диэлектрической проницаемостью объясняется тем, что наряду с эффектом сольватации наблюдается и эффект ассоциации ионов. Следовательно, с одной стороны, связывание части растворителя в сольватную оболочку ионов и их частичная десольватация с ростом концентрации повышают коэффициенты активности, но, с другой стороны, ассоциация понижает их. Чтобы описать зависимость коэффициентов активности от концентрации, в этих случаях недостаточно учитывать только явление сольватации, необходимо учитывать также и изменение ассоциации ионов. [c.209]Следовательно, наклон зависимости lg V — должен приближаться к — Лг, когда / 2 стремится к нулю. Это предсказание было многократно подтверждено измерениями средних ионных коэффициентов активности и активности растворителя (разд. 2.16), а также влиянием ионной силы на растворимость сильных электролитов и на другие равновесия с участием ионов (см., например, [11 или [21). Установлено, что оно справедливо не только для воды, но и для растворителей со значительно более низкими диэлектрическими проницаемостями. Еще более тщательной проверке было подвергнуто аналогичное предсказание относительно зависимости электропроводности от концентрации (см., например, [31). [c.241]
Введение в раствор воды резко замедляет коррозию циркония. При концентрации воды выше 10 % цирконий не корродирует. Следует отметить, что в некоторых спиртах при содержании воды порядка 10 % пассивное состояние циркония не нарушается даже при анодной поляризации. Параметры анодного растворения циркония в области химической поляризации находятся в линейной зависимости от обратной величины диэлектрической проницаемости растворителя [25]. [c.116]
Кислотно-основные равновесия более чувствительны к изменению диэлектрической проницаемости и основности среды. При уменьшении диэлектрической проницаемости приобретает значение образование ионных пар или ассоциатов более высокого порядка. Кортюм и Андрусов [29] нашли, что относительно неустойчивые ионные пары Бьеррума, присутствующие в метанольных растворах, спектроскопически неразличимы от свободных ионов. В ледяной уксусной кислоте, диэлектрическая проницаемость (6,1) которой значительно меньше, чем у метанола (32,7), цветные реакции индикаторов связаны с ионизацией и с диссоциацией ионных ассоциатов [30, 31]. Для этого растворителя не наблюдается простой зависимости, которая имеет место в воде, между отношением концентраций щелочной и кислой форм индикатора и концентрацией ионов водорода [32]. В апротонном растворителе, например бензоле, свободные ионы, возможно, не играют значительной роли во взаимодействии кислот и оснований, несмотря на перемену окраски индикатора. [c.139]
В растворителе с низкой диэлектрической проницаемостью потенциал средней точки зависит как от концентрации титруемых компонентов, так и от концентрации солей. Однако при постоянных условиях можно получить линейную зависимость между потенциалом средней точки и значениями р/Са в воде для любого класса соединений [c.333]
Подобный же вид зависимости В от состава растворов наблюдается также у растворов вода—перекись водорода [81. Различие состоит лишь в величине отклонений от аддитивности и в концентрациях, при которых имеют место максимальные значения АВ. Нередко встречаются более сложные формы зависимости диэлектрической проницаемости растворов от их состава. На рис.. 36 [c.198]
Падение потенциала в двойном слое такой модели линейно (рис. 1.1). Эта теория в некоторой степени соответствовала опыту. Известно, что экспериментально найденная емкость двойного слоя обычно изменяется в пределах 20—40 мкф/см . Если предположить, что расстояние между обкладками такого конденсатора равно диаметру молекулы воды, а диэлектрическая проницаемость в двойном слое в водных растворах составляет 10, то на основе уравнения для емкости плоского конденсатора можно получить теоретические величины, хорошо совпадающие с экспериментальными результатами. Однако теория Гельмгольца не объясняет зависимости емкости двойного слоя от концентрации электролита и от потенциала. [c.14]
Значения собственной растворимости и констант диссоциации определены -лишь для небольшого числа плохо растворимых веществ, представляющих интерес для аналитиков. Большей частью делается допущение, что диссоциация проходит полностью, а значение 5° настолько мало, что не оказывает никакого влияния на общую растворимость. Это допущение часто необосновано, если дело касается воды, и, по-видимому, мало пригодно в случае органических осадков или растворителей с низкой диэлектрической проницаемостью. Зависимость между диссоциацией, константой диссоциации и концентрацией растворенного вещества типа 1 1 [c.143]
Диэлектрические свойства жидкой фазы — нефти, пресной-воды, электролитов в зависимости от температуры и частоты поляризующего поля изучены рядом авторов [6, 7, 29, 54] Нефть относится к неполярным веществам, поскольку ее диэлектрическая проницаемость колеблется в пределах 2—2,7. Од- нако присутствующие в нефти полярные и неполярные компоненты способствуют приближению ее к слабополярным диэлектрикам. До частоты электрического поля не свыше 50 МГц диэлектрическая проницаемость нефти не зависит от частоты. Исследования Ю. Л. Брылкина и Л. И Дубмана показали, что мезозойские нефти месторождений Западной Сибири имеют диэлектрическую проницаемость 2,2 она остается практически постоянной при изменении температуры от 24 до 100°С и не зависит от частоты внешнего поляризующего поля в пределах 5-10 4-5-10 Гц При повышении температуры от нуля до 100° С диэлектрическая проницаемость воды уменьшается до 40%. С увеличением концентрации солей в воде диэлектрическая проницаемость растворов растет незначительно. [c.109]
Влияние диэлектрической проницаемости на зависимость X от С можно наглядно показать, исследуя растворы какого-либо одного вещества в растворителях с различной е. Были произведены измерения X растворов нитрата тетраизоамиламмония [СНз(СН2)4]4 (N03) в чистой воде и в смесях воды с диокса-ном. Диэлектрическая проницаемость е изменялась при этом от 78,6 до 2,2. Оказалось, что чем меньше е, тем более отчетливо выражен минимум электропроводности и тем больше он сдвинут в сторону малых концентраций, что согласуется с приведенной выше схемой. Если е>10, то минимумов электропроводности в растворах не наблюдается. [c.74]
Если концентрация кислотных форм в органической фазе известна, то график зависимости IgD от IgQ дает сведения об относительной силе кислот в этом растворителе. Тип повеления, иллюстрацией которого служит кривая d на рис. 1, должен быть ожидаемым случаем для кислородсодержащих, не подобных воде (не спиртовых) органических растворителей с умеренной диэлектрической проницаемостью. Если диэлектрическая проницаемость небольшая, ассоциация (объединение ионов в пары) возрастает до тех пор, пока в органической фазе практически существует только НМХг и нет никаких изменений D (правый горизонтальный отрезок на кривой d, рис. 1). Если диэлектрическая проницаемость органического растворителя высока и приближается к диэлектрической проницаемости воды, ассоциация в органической фазе проходит в небольшой степени, а галогеноводородная кислота НХ, присутствующая в водной фазе в гораздо большей концентрации, чем металл, вероятно, довольно хорошо растворима и сильно диссоциирована в органической фазе и таким образом поставляет основную часть водородного иона органической фазы равным образом для всех практически достижимых концентраций металла . Таким образом, D опять становится постоянной величиной (левый горизонтальный отрезок на кривой d, рис. 1). [c.265]
На рис. 1 показана зависимость б от частоты для различных значений проводимости о. При расчетах кривых рис. 1 предполагалось, что параметры электролитов мало отличаются от параметров воды (т == 8- 10 сек, Ец = 80 и 8оо — = 1,8). Следует отметить, что в ряде экспериментальных работ имеются противоречивые данные о диэлектрических параметрах электролитов, свидетельствующие о резком росте [7] или уменьшении [8] диэлектрической проницаемости с повышением концентрации электролигов. Однако, согласно теоретическим предпосылкам [6, 9), диэлектрическая проницаемость электролитов должна мало отличаться от диэлектрической проницаемости воды. Из рис. 1 видно, что малые потери будут происходить только у дистиллированной или очень слабо минерализованной воды (о 10 ) в узком пределе частот. [c.51]
Определения плотности водных растворов сульфата калия при различных повышенных давлениях позволили установить влияние давления на положение минимума кривых зависимости мольных объемов от концентрации. При одной и той же температуре с понижением давления минимумы на кривых мольных объемов становятся более глубокими (рис. 98, в, г и 99). С увеличением давления этот минимум смещается к ординате воды и даже, как, например, на изотерме 300° С при наиболее высоких из исследованных давлений, 1300 и 1500 кПсм , минимум исчезает, т. е. доходит до ординаты воды, и кривая мольного объема приближается к виду кривой при 25° С. Повышение давления производит на контракцию растворов действие, аналогичное понижению температуры. Это обусловлено тем, что с повышением давления сжимаемость растворов значительно уменьшается, как будет показано ниже, а диэлектрическая проницаемость воды,так же как и с понижением температуры,увеличивается [120]. Таким образом, давление приближает свойства растворов, находящихся при высоких температурах, к свойствам их при низких температурах. [c.133]
Для водных растворов электролитов этот максимум (и, соответст-венио, левая ветвь кривой) лежит в зоне значительных разбавлений [2], что обусловлено высокими значениями диэлектрической проницаемости воды. Действительно, в этой области составов зависимость относительной динамической вязкости от молярной концентрации с (моль- л- ) может быть описана уравнением Джонса — Дола [c.8]
При переходе от воды к нeвoдны г растворителям с высокой диэлектрической проницаемостью существенных изменений в зависимости электропроводности от концентрации не наблюдается. Однако в растворах с низкой диэлектрической проницаемостью, например в смеси диоксана с водой, обычный для водных растворов ход кривой молярная электропроводност — концентрация нарушается, и на ней появляются экстремумы. На рис. 4.5 показана зависимость молярной электронроводности от разведения, типичная для таких растворов. [c.113]
Наиболее распространены приборы автоматического действия, основанные на линейной зависимости диэлектрической проницаемости тоилива от содержания в нем воды. Из влагомеров данного типа представляет интерес установка Микроскан , выпускаемая фирмой Миллипор (США) с 1963 г. и предназначенная для непрерывного конт1роля за содержанием воды и механических примесей в потоке реактивных топлив с помощью емкостного датчика. При прохождении механических частиц (или частиц воды) между пластинками конденсатора (детектор Микро-Скан ) его емкость изменяется пропорционально объемной концентрации частиц. Изменение емкости преобразуется в сигнал с постоянной амплитудой и частотой, который усиливается в многокаскадном усилителе и подается на указатель концентрации примесей в топливе. Прибор реагирует на суммарное содержание примесей воды и механических частиц и нечувствителен к воздушным и паровым пузырькам. Установка обладает высокой чувствительностью по воде 0,000001% по механическим примесям 0,02632 мг/л по размеру частиц 5 мкм [149, 154]. Используют установку на автотопливозаправщиках и гидрантных тележках, а также на трубопроводах и стационарных резервуарах. Для отсечения потока топлива при загрязненности его выше установленного уровня предусмотрено использование дополнительного сигнала самописца и автоматических механизмов. [c.176]
Выше теоретически предсказывается, что в эмульсиях М/В может наблюдаться диэлектрическая дисперсия при условии, если масляная фаза имеет высокую диэлектрическую проницаемость. Чтобы обнаружить это явление, Ханаи, Коицуми и Гото (1962а) исследовали диэлектрические свойства эмульсий нитробензола в воде, приготовленные с помощью эмульгатора твин 20. На рис. У.49 показана частотная зависимость е и х этих эмульсий при 70%-ной объемной концентрации. Быстрый рост 6 на частотах электродной поляризации. С увеличением частоты (> 100 кгц) можно [c.379]
Целью настоящей работы является установление характера зависимости удельной электропроводности раствора электролита от концентрации неэлектролита, диэлек рической проницаемости раствора и предельной высокочастотной электропроводности растворителя. Значительный интерес представляет изучение этих зависимостей для водно-органических смесей, диэлектрическая проницаемость которых уменьшается (вода — спирт, вода — ацетон) и увеличивается (вода—мочевина, вода тпомочевина) с ростом крнцентрации неэлектролита. [c.84]Карбоновые кислоты относятся к слабоионизированным средам. Вследствие их низкой диэлектрической проницаемости растворенные в карбоновых кислотах сильные минеральные кислоты и соли находятся в основном в виде ионных пар с низкими константами диссоциации. Поскольку индикаторные основания Гаммета протонируются и протонами, входящими в состав ионных пар, и протонами, находящимися в растворе отдельно, линейную зависимость IgA от Hq раствора следует трактовать как зависимость константы скорости реакции от суммарной прото-нодонорной способности среды. Изменение Яд в изученных растворах достигалось при изменении и концентрации минеральных кислот, и концентрации воды при этом все данные зависимости gk2 от Hq описывались общей прямой линией. Это позволяет сделать вывод, что катализ осуществляется протонированиём одного из реагентов, а не в результате ассоциации его с молекулой катализатора. [c.303]
На основании изучения температурной зависимости электропроводности поливинилацетатных и эпоксидных пленок, погруженных в раствор Na l, и сопоставления энергии активации электропроводности с энергией активации диффузии газов сделан вывод о том, что механизм диффузии газов и ионов идентичны. В обоих случаях имеет место активированная диффузия. Предполагается, что перенос ионов происходит путем перескока из одного элемента объема с высокой диэлектрической проницаемостью (капельки) в другой. Чем больше плотность распределения капелек, тем легче происходит диффузия. Электропроводность покрытий на основе эпоксидной смолы снижается с ростом концентрации контактирующих с ними растворов Na l и почти пропорциональна концентрации воды в пленке т. е. имеет место обратная зависимость между сопротивлениями пленки и раствора. В случае лакокрасочных пленок сложного состава помимо механизма, указаного выше, может иметь место и другой механизм. При большом водопоглощении в пленке образуются каналы. Через них ток переносится так же, как через водный раствор температурный коэффициент при этом мал, а сопротивление пленки меняется симбатно с сопротивлением внешнего раствора. Эти явления уже характерны для переноса электролитов в гидрофильных пленках. [c.217]
В работе [80] рассматривается зависимость ионного обмена в цеолите А на щелочные ионы (литий, натрий и т. д.) в смешанных растворителях (система вода — метанол) от диэлектрической проницаемости раствора. Добавление метанола в раствор повышает кажущуюся константу равновесия для всех катионов, кроме лития. В случае лития константа равновесия снижается с увеличением концентрации метанола, что может быть связано с высокой энергией гидратации ионов лития. Значения исправленных коэффициентов селективности линейно зависят от содержания катиона в обменнике в соответствии с уравнением Килланда — Баррера. Стандартная свободная энергия обмена во всех случаях — величина положительная, как и при обмене натрия в цеолите NaA на другие щелочные катионы в водном растворе. Это позволило сделать вывод, что цеолит А более избирателен по отношению к натрию, "чем к другим щелочным катионам, вне зависимости от того, проводится ли обмен в воде или в смешанном растворителе [80]. [c.602]
В последнее время А. М. Сухотин систематически исследовал проводимость растворов минеральных солей в неводных смешанных растворителях с различной диэлектрической проницаемостью. Исследовалась электропроводность NaJ в смесях этанола с четыреххлористым углеродом (О от 2,3 до 24) и в смесях диоксана с водой, а также проводимость Li l, LiBr, LiJ, (С5Нц)4Ш и H l в смесях бутанола с гексаном D от 2,1 до 19) в широком интервале концентраций. Характер зависимости электропроводности от коицентрации и диэлектрической проницаемости во всех случаях одинаков и подобен зависимости, найденной Сахановым и Фуоссом и Краусом. [c.269]
Можно ожидать, что эффект сольватации в неводных растворах будет сказываться в большей степени, чем в воде. В 1000 г воды находится 55 молей, а в этиловом спирте, молекулярный вес которого равен 46, в 1000 г находится только 22 моля, и сольватация должна сказываться на изменении концентрации в большей степени, чем в воде. Таким образом, неприложимость уравнения Робинсона—Стокса не может быть оправдана тем, что в неводных растворах эффект сольватации меньше, чем в воде. Отсутств.ие минимума в неводных растворах с низкой диэлектрической проницаемостью объясняется тем, что наряду с эффектом сольватации аблю-цается и эффект ассоциации ионов. Следовательно, с одной стороны, связывание части растворителя в сольватную оболочку ионов и их частичная десольватация с ростом концентрации 1т0вышают коэффициенты активности, ио, с другой стороны, ассоциация понижает нх. Чтобы описать ход зависимости коэффициентов активности от концентрации, в этих случаях недостаточно учитывать только явление сольватации необходимо учитывать и изменение ассоциации ионов. [c.392]
Следует упомянуть о методе ван дер Гейджа и Дахмена , который может послужить эмпирическим руководством в вопросе выбора растворителя. Авторы измеряли с помощью стеклянного и каломельного электродов интервал изменения потенциала в каждом растворителе от крайних значений кислотности до крайних значений основности. Они исследовали кислые раство- рители (уксусную и трифторуксуспую кислоты), нейтральные (хлорбензол, ацетонитрил, ацетон, метиловый и изопропиловый спирты,воду) и основные (н-бутиламин, этилендиамин, пиридин, диметилформамид). Пригодность для титрования определялась отношением так называемого потенциала полунейтрализации данной кислоты или основания к крайним величинам потенциалов в данном растворителе. Для смесей разница между потенциалами полунейтрализации в 200—300 мв в большинстве случаев оказывается достаточной для осуществления избирательного титрования. Из соображений, высказанных по поводу кислотно-основного равновесия в уксусной кислоте (раздел 4-5), ясно, что в растворителях с очень низкой диэлектрической проницаемостью потенциал полунейтрализации должен находиться в прямой зависимости от концентрации. Более того, сила основания, очевидно, зависит от силы нейтрализующей его кислоты и наоборот . Поэтому концепция потенциала полунейтрализации может найти лишь ограниченное применение. [c.121]
Систематические исследования влияния изменений характера или концентрации солевого фона на константы устойчивости производятся обычно для нахождения отношения активностей (см. раздел II, 1, А). Изменения термодинамических функций можно рассмотреть с точки зрения конкурируюхцих реакций комплексообразования [240] или изменения коэффициентов активности, входяш их в уравнения (5), (6), (31)— (33). Устойчивости комплексов ионов металлов изучались в смесях водных и неводных ( смешанных ) растворителей главным образом по двум причинам. Во-первых, изменение констант ассоциации в зависимости от диэлектрической проницаемости среды рассматривали как способ проверки представлений Бьеррума—Фуосса об ионных нарах [62]. Во-вторых, многие органические лиганды и их комплексы настолько плохо растворимы в воде, что соответствующие равновесия можно изучать только в смешанных растворителях. [c.69]
Использование смешанных растворителей приводит к появлению двух общих проблем. Если происходит селективная сольватация [11, 181а], то константы ассоциации, полученные в двух разных средах, относятся к разным реакциям. Вероятно, если молярная доля воды больше, чем примерно 0,8, селективной сольватации комплексов металлов не происходит, так как вальденовское произведение предельной электропроводности и вязкости постоянно для ряда систем с большим содержанием воды [75, 148, 149]. В неводных средах ионы металлов и их комплексы не гидратируются и, вероятно, даже не сольватируются, и многие реакции ассоциации были изучены в безводных средах [86, 152, 199, 224, 257, 301]. Стандартное состояние для стехиометрических констант ассоциации выбирается для каждой конкретной среды (растворенные вещества плюс растворители). Предпринимались попытки элиминировать зависимость от концентрации электролита (вторичный эффект среды по Оуэну [123]), с тем чтобы относить стандартное состояние только к смеси растворителей [62, 75, 148, 149], но эти попытки вызывают возражения, изложенные в разделе II, 1, А. За исключением, возможно, амминов металлов, константы ассоциации большого числа разнообразных комплексов металлов, содержащих неорганические [284] и органические [283] лиганды, возрастают при уменьшении диэлектрической проницаемости среды. Это изменение происходит в направлении, ожидаемом на основании электростатических соображений, но влияние органических растворителей (первичный эффект среды по Оуэну [123]) на константы ассоциации не проанализировано. [c.69]
Как видно из табл. 5, зависимость Д// с = f T) для растворов Ка и галогенидов тетраалкиламмония в спиртах носит экстремальный характер. Объяснение этому факту можно дать, рассмотрев основные вклады в процесс растворения от разрушения структуры растворителя ионами электролита и от сольватации (взаимодействия ионов с молекулами растворителя). Следует отметить, что температурная зависимость Д// с Для растворов электролитов в неводных растворителях изучена мало, а имеющиеся немногочисленные данные противоречивы. Так, в работах [18, 19] установлено возрастание экзотермичности при растворении На в метаноле и этаноле при Т > 283 К. Связывается это представление с отсутствием у спиртов такой выраженной структуры, какой обладает вода. Измерения, выполненные Мастрояни и Криссом [20] для ЫаСЮа в метаноле в интервале температур 268—323 К, показали, что для этой соли Д// с увеличиваются с понижением температуры. Отмечена инверсия зависимостей ДЯ с = /("О при разных температурах в области малых концентраций соли ( 0,005 т), которая объясняется авторами сильным влиянием температуры на предельный ограничительный наклон (вследствие изменения с температурой диэлектрической проницаемости растворителя). Обнаруженное увеличение экзотермичности растворения электролитов в метаноле, этаноле и н-пропаноле при пош1женных температурах позволяет предполагать, что разрушение структуры спиртов ионами электролита носит локальный характер. В случае ацетона это выражено более явно. [c.163]
Растворы перекиси водорода в воде не являются идеальными, что обнаруживается при исследовании любым из трех обычно применяемых методов объем раствора меньше, чем сумма объемов составляющих компонентов, смешение происходит с заметным тепловым эффектом и величины давления пара растворов не подчиняются закону Рауля. Дальнейшими доказательствами являются неправилыпзю зависимости между концентрацией раствора и такими свойствами, как вязкость, поверхностное натяжение и диэлектрическая проницаемость. Характер отклонения от идеальности в каждом отдельном случае говор ит об увеличении либо числа молекул, либо сил притяжения между молекулами при образовании растворов, что выражается в уменьшении общего объема и давления пара и выделении тепла при смешении. Аналогия между водой и перекисью водорода в отношении природы и размеров межмолекулярных сил приводит к логическому выводу, что это поведение обусловлено образованием дополнительных водородных связей иначе говоря, можно предполагать, что водородные связи между молекулами воды и перекиси водорода более стабильны, чем сиязи между молекулами каждого из этих веществ в отдельности. Это подтверждают и измерения Уинн-Джонса П171 по изменению основности водных растворов перекиси водорода с концентрацией. [c.292]
В области температуры выше 100 °С температурная зависимость проводимости гораздо сложнее даже для растворов сильных электролитов. Кондратьев и сотр. [11] установили, что в водных растворах хлоридов щелочных и щелочноземельных металлов удельная и эквивалентная проводимости в интервале температур до 300°С (под давлением) максимальны при концентрации 0,5 моль-л и температуре 250 °С, С ростом концентрации раствора максимум проводимости смещается в сторону более низкой температуры. Снижение проводимости после максимального значения объясняется возрастанием с подъемом температуры степени ассоциации, вызванным дегидратацией ионов и соответствующим сокращением их эффективного диаметра. Так как при повышении температуры диэлектрическая проницаемость снижается, создаются условия для более тесного сближения ионов и образования ионных пар. По данным Максимовой и Юшкевич [12], в 20%-ном pa TiBope NaOH проводимость максимальна при 220 °С. В интерпретации этого явления подчеркивается водородные связи в структуре воды вследствие совместного действия высокой температуры и электрического поля ионов раз- [c.395]
Это выражение чисто электростатического характера и оно ограничено в том отношении, что не учитывает ни влияния специфических взаимодействий, ни диэлектрического насыщения. Подобно уравнению Борна, выражение (4-26) может быть использовано лишь для получения приближенных значений величины д. На рис. 4-2 представлена предсказанная линейная зависимость между константой образования соли (определяемой по данным электропроводности) и величиной, обратной диэлектрической проницаемости растворителя [50]. Из рис. 4-2 видно, что в растворителях с низкой диэлектрической проницаемостью константы диссоциации невелики. На практике электролиты типа 1 1 при концентрации М и выше в воде, а в других растворителях с диэлектрической проницаемостью менее 40 при концентрациях выше 10 М диссоциированы не полностью. Даже в воде электролиты типа 2 2 не полностью диссоциированы, несмотря на сильные специфические взаимодействия между растворенным веществом и растворителем и высокую диэлектрическую проницаемость. Согласно представлениям Грюнвальда и Киршенбаума [51], можно считать, что при обычных аналитических концентрациях основные частицы, присутствующие в растворе, — это ионные пары, если константа диссоциации меньше 10 , и свободные ионы, если константа выше 10 . [c.82]
chem21.info
Высокая диэлектрическая проницаемость - вода
Высокая диэлектрическая проницаемость - вода
Cтраница 1
Высокая диэлектрическая проницаемость воды обусловлена тем, что молекулы НгО представляют собой жесткие диполи, обладающие значительным электрическим дипольным моментом. Ближайшие к иону электролита дипольные молекулы воды поворачиваются к нему противоположно заряженными полюсами и притягиваются, образуя вокруг иона своеобразное облако, перемещающееся вместе с ним. Это облако не вполне стабильно; в результате теплового движения отдельные молекулы отрываются от иона, а на их место приходят другие. [1]
Высокая диэлектрическая проницаемость воды обусловлена тем, что молекулы HZO представляют собой жесткие диполи, обладающие значительным электрическим дипольным моментом. Ближайшие к иону электролита дипольные молекулы воды поворачиваются к нему противоположно заряженными полюсами и притягиваются, образуя вокруг иона своеобразное облако, перемещающееся вместе с ним. Это облако не вполне стабильно; в результате теплового движения отдельные молекулы отрываются от иона, а на их место приходят другие. [3]
Высокая диэлектрическая проницаемость воды обусловлена тем, что молекулы Н20 представляют собой жесткие диполи, обладающие значительным электрическим дипольным моментом. Ближайшие к иону электролита дипольные молекулы воды поворачиваются к нему противоположно заряженными полюсами и притягиваются, образуя вокруг иона своеобразное облако, перемещающееся вместе с ним. Это облако не вполне стабильно; в результате теплового движения отдельные молекулы отрываются от иона, а на их место приходят другие. [5]
Высокая диэлектрическая проницаемость воды ( KW 80 4 в ассоциированном состоянии; е 31 - в неассоциированном) позволяет применять метод диэлкометрии для определения содержания воды в бинарных смесях. Определение характеризуется высокой точностью. [6]
Высокая диэлектрическая проницаемость воды ( е2о 80 4 в ассоциированном состоянии; е 31 - в неассоциированном) позволяет применять метод диэлкометрии для определения содержания воды в бинарных смесях. Определение характеризуется высокой точностью. [7]
Высокая диэлектрическая проницаемость воды, обусловливающая поразительную способность воды растворять вещества ионного строения, отчасти является следствием того, что вода способна образовывать водородные связи. Благодаря этим связям молекулы воды располагаются так, чтобы частично нейтрализовать электрическое поле. Водородные связи образуются также и в других жидкостях в перекиси водорода, фтористом водороде, аммиаке ( температура кипения - 33 4 С), цианистом водороде ], которые способны растворять вещества, обладающие ионным строением. [8]
Ниже будет показано, что высокая диэлектрическая проницаемость воды позволяет достаточно просто определять влажность многих веществ путем измерения их диэлектрической проницаемости. В связи с этим приборостроительная промышленность разработала ряд измерительных устройств, специально предназначенных для определения влажности. [10]
Определение содержания влаги путем измерения диэлектрической проницаемости возможно благодаря очень высокой диэлектрической проницаемости воды е 80, во много раз большей, чем у большинства исследуемых веществ. Однако такое предположение правильно только условно. Указанная высокая диэлектрическая проницаемость соответствует только чистой воде, характеризующейся так называемой тридимитной структурой связей. [11]
Отметим, что важную роль в расширении области применимости теории играет высокая диэлектрическая проницаемость воды. [12]
Фактически такая электрическая поляризация воды распространяется на большие расстояния; это и обусловливает высокую диэлектрическую проницаемость воды. [13]
Но почему присутствие влаги резко тормозит скопление молекул в ассоциации. Показано, что тут вступает в роль высокая диэлектрическая проницаемость воды как следствие ее способности образовывать относительно прочные водородные связи между молекулами; в этом отношении вода, наряду с формами-дом и синильной кислотой, занимает одно из первых мест среди жидкостей. Представляется такая картина: электрически весьма асимметричные примесные молекулы воды ( диполи) парализуют проявление электростатических сил притяжения между молекулами основного вещества. [14]
Дипольная поляризация, обусловленная тепловым движением. Механизм тепловой ориентации диполей был предложен Деба-ем для объяснения высокой диэлектрической проницаемости воды и других полярных жидких диэлектриков. Такое различие в е на разных частотах объясняется запаздыванием ориентации полярных молекул во внешнем электрическом поле при частотах выше 109 - 10 Гц. Это равновесие является термодинамическим: за счет тепловых движений ( колебаний, вращений) диполи приобретают благоприятную ориентацию, но те же тепловые колебания препятствуют ориентации всех диполей в электрическом поле. Чем выше напряженность электрического поля, тем большая часть диполей в единице объема ориентирована и тем выше поляризованность. В среднем электрический дипольный момент в расчете на одну молекулу пропорционален напряженности электрического поля ( если поля не слишком велики): р ал. [15]
Страницы: 1 2
www.ngpedia.ru
Диэлектрическая проницаемость
Диэлектрическая проницаемость (ε) характеризует способность вещества изменять напряженность первичного электрического поля вследствие явления поляризации, т.е. упорядоченной ориентировки связанных электрических зарядов. При этом величина ε показывает, во сколько раз в данной среде сила взаимодействия (напряженность электрического поля - Е) между электрическими зарядами уменьшается по сравнению с вакуумом. Это взаимодействие можно выразить через реакцию на электрическое поле:
D= εaE,
где D – электрическая индукция, εa– абсолютная диэлектрическая проницаемость (Ф/м).
Если диэлектрическую проницаемость вакуума обозначить через εо = = 8,854 ×10-12 Ф/м, то относительная диэлектрическая проницаемость среды 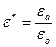 определит одну из электрических характеристик горных пород.
определит одну из электрических характеристик горных пород.
Величина диэлектрической проницаемости горной породы определяется объемом воды в порах. Это связано с тем, что для воды ε*» 80 отн. ед. и на порядок превышает относительную диэлектрическую проницаемость для скелета породы и нефти (ε*= 3÷10).
Возрастание минерализации воды от 1 до 300 г/л приводит к увеличению диэлектрической проницаемости породы на 30-40%.
Вообще применение диэлектрического каротажа целесообразно для разрезов, в которых удельное электрическое сопротивление горных пород превышает 5 Ом∙м при заполнении ствола промывочной жидкостью с удельным электрическим сопротивлением выше 1 Ом∙м.
В процессе обводнения коллекторов нагнетательными водами на величину диэлектрической проницаемости коллекторов влияют в основном те же факторы, что и на сопротивление (r)
· соотношение воды и нефти;
· минерализация смеси остаточной воды с нагнетаемой;
· образование граничных водных слоев с аномальными диэлектрическими свойствами;
· температура пород.
Относительная диэлектрическая проницаемость нефтеносных терригенных коллекторов определяется соотношением:
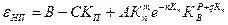 ,
,
где В и С коэффициенты, зависящие от диэлектрических проницаемостей твердой части скелета породы и нефти; А, m, n, p, q – коэффициенты, зависящие от минерализации насыщающнго раствора.
С увеличением минерализации насыщающего раствора величина εНП растет, так же как для дистиллированной воды. Это объясняется следующими факторами:
1. У поверхности твердых минеральных гидрофильных частиц за счет ориентации полярных молекул под влиянием сильного электрического поля формируются граничные слои связанной воды с аномальной диэлектрической проницаемостью значительно меньшей, чем у воды связанной. Так, ε свободной воды при t= 20°С равна 80,3 ед, а интегральное значение пленки связанной воды (εпл. ср) толщиной 0,07 мкм, заключенной между двумя кристаллами слюды, составляет 4,5 отн. ед.
2. Объем связанной воды в порах различен при насыщении пресной и минерализованной водой. Толщина пленки связанной воды, ассоциирующая с двойным электрическим слоем, возрастает с уменьшением минерализации раствора электролита. Замена пресного раствора на минерализованный приводит к уменьшению пленки связанной воды и, следовательно, к уменьшению суммарного объема этой воды с резко заниженным значением ε, что и является причиной роста ε с увеличением минерализации раствора, насыщающего их поровое пространство.
На рис. 8 показана зависимость 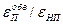 для Усть-Балыкского месторождения с учетом экспериментальных данных для случаев вытеснения нефти пластовой водой и пресной.
для Усть-Балыкского месторождения с учетом экспериментальных данных для случаев вытеснения нефти пластовой водой и пресной.
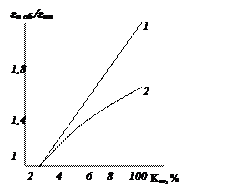
Рис. 8. Зависимости 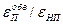 от КВТ.
от КВТ.
Вытеснение нефти водой: 1- пластовой (СВ=15 г/л), 2- пресной (СВ→0)
При выработке нефти из пласта ε может увеличиваться в 2 раза при нагнетании минерализованной водой и в 1,6 раза при нагнетании пресной.
Таким образом, по величине диэлектрической проницаемости можно выделять пласты, обводняющиеся нагнетаемыми пресными и минерализованными водами.
Если определены εп обв, εнп и Кп , то можно определить коэффициент текущей нефтенасыщенности (КНТ).
Контрольные вопросы
1. Какие физические характеристики пластов влияют на изменение диэлектрической проницаемости?
2. Можно ли по данным измерения диэлектрической проницаемости выделять обводненные пласты?
infopedia.su
Относительная диэлектрическая проницаемость — Machinepedia
Относи́тельная диэлектри́ческая проница́емость среды ε — безразмерная физическая величина, характеризующая свойства изолирующей (диэлектрической) среды. Связана с эффектом поляризации диэлектриков под действием электрического поля (и с характеризующей этот эффект величиной диэлектрической восприимчивости среды). Величина ε показывает, во сколько раз сила взаимодействия двух электрических зарядов в среде меньше, чем в вакууме. Относительная диэлектрическая проницаемость воздуха и большинства других газов в нормальных условиях близка к единице (в силу их низкой плотности). Для большинства твёрдых или жидких диэлектриков относительная диэлектрическая проницаемость лежит в диапазоне от 2 до 8 (для статического поля). Диэлектрическая постоянная воды в статическом поле достаточно высока — около 80. Велики её значения для веществ с молекулами, обладающими большим электрическим диполем. Относительная диэлектрическая проницаемость сегнетоэлектриков составляет десятки и сотни тысяч.
Практическое применение
Диэлектрическая проницаемость диэлектриков является одним из основных параметров при разработке электрических конденсаторов. Использование материалов с высокой диэлектрической проницаемостью позволяют существенно снизить физические размеры конденсаторов.
Параметр диэлектрической проницаемости учитывается при разработке печатных плат. Значение диэлектрической проницаемости вещества между слоями в сочетании с его толщиной влияет на величину естественной статической ёмкости слоев питания, а также существенно влияет на волновое сопротивление проводников на плате.
Зависимость от частоты
Следует отметить, что диэлектрическая проницаемость в значительной степени зависит от частоты электромагнитного поля. Это следует всегда учитывать, поскольку таблицы справочников обычно содержат данные для статического поля или малых частот вплоть до нескольких единиц кГц без указания данного факта. В то же время существуют и оптические методы получения относительной диэлектрической проницаемости по коэффициенту преломления при помощи эллипсометров и рефрактометров. Полученное оптическим методом (частота 1014 Гц) значение будет значительно отличаться от данных в таблицах.
Рассмотрим, например, случай воды. В случае статического поля (частота равна нулю), относительная диэлектрическая проницаемость при нормальных условиях приблизительно равна 80. Это имеет место вплоть до инфракрасных частот. Начиная примерно с 2 ГГц εr начинает падать. В оптическом диапазоне εr составляет приблизительно 1,8. Это вполне соответствует факту, что в оптическом диапазоне показатель преломления воды равен 1,33. В узком диапазоне частот, называемом оптическим, диэлектрическое поглощение падает до нуля, что собственно и обеспечивает человеку механизм зрения в земной атмосфере, насыщенной водяным паром. С дальнейшим ростом частоты свойства среды вновь меняются.
Значения диэлектрической проницаемости для некоторых веществ
| Алюминий | Al | 1 кГц | -1300 + 1,3Шаблон:Ei |
| Серебро | Ag | 1 кГц | -85 + 8Шаблон:Ei |
| Вакуум | - | - | 1 |
| Воздух | - | Нормальные условия, 0,9 МГц | 1,00058986 ± 0,00000050 |
| Углекислый газ | CO2 | Нормальные условия | 1,0009 |
| Тефлон | - | - | 2,1 |
| Нейлон | - | - | 3,2 |
| Полиэтилен | [-СН2-СН2-]n | - | 2,25 |
| Полистирол | [-СН2-С(С6Н5)Н-]n | - | 2,4-2,7 |
| Каучук | - | - | 2,4 |
| Битум | - | - | 2,5-3,0 |
| Сероуглерод | CS2 | - | 2,6 |
| Парафин | С18Н38 − С35Н72 | - | 2,0-3,0 |
| Бумага | - | - | 2,0-3,5 |
| Электроактивные полимеры | − | − | 2-12 |
| Эбонит | (C6H9S)2 | − | 2,5-3,0 |
| Плексиглас (оргстекло) | - | - | 3,5 |
| Кварц | SiO2 | - | 3,5-4,5 |
| Диоксид кремния | SiO2 | − | 3,9 |
| Бакелит | - | - | 4,5 |
| Бетон | − | − | 4,5 |
| Фарфор | − | − | 4,5-4,7 |
| Стекло | − | − | 4,7 (3,7-10) |
| Стеклотекстолит FR-4 | - | - | 4,5-5,2 |
| Гетинакс | - | - | 5-6 |
| Слюда | - | - | 7,5 |
| Резина | − | − | 7 |
| Поликор | 98 % Al2O3 | - | 9,7 |
| Алмаз | − | − | 5,5-10 |
| Поваренная соль | NaCl | − | 3-15 |
| Графит | C | − | 10-15 |
| Керамика | − | − | 10-20 |
| Кремний | Si | − | 11.68 |
| Бор | B | − | 2.01 |
| Аммиак | Nh4 | 20 °C | 17 |
| 0 °C | 20 | ||
| −40 °C | 22 | ||
| −80 °C | 26 | ||
| Спирт этиловый | C2H5OH или Ch4-Ch3-OH | − | 27 |
| Метанол | Ch4OH | − | 30 |
| Этиленгликоль | HO—Ch3—Ch3—OH | − | 37 |
| Фурфурол | C5h5O2 | − | 42 |
| Глицерин | HOCh3CH(OH)-Ch3OH или C3H5(OH)3 | 0 °C | 41,2 |
| 20 °C | 47 | ||
| 25 °C | 42,5 | ||
| Вода | h3O | 200 °C | 34,5 |
| 100 °C | 55,3 | ||
| 20 °C | 81 | ||
| 0 °C | 88 | ||
| Плавиковая кислота | HF | 0 °C | 83,6 |
| Формамид | HCONh3 | 20 °C | 84 |
| Серная кислота | h3SO4 | 20-25 °C | 84-100 |
| Перекись водорода | h3O2 | −30 °C — +25 °C | 128 |
| Синильная кислота | HCN | (0-21 °C) | 158 |
| Двуокись титана | TiO2 | - | 86-173 |
| Титанат кальция | CaTiO3 | - | 170 |
| Титанат стронция | SrTiO3 | - | 310 |
| Барий-стронций титанат | - | - | 500 |
| Титанат бария | BaTiO3 | (20-120 °C) | 1250-10000 |
| Цирконат-титанат свинца | (Pb[ZrxTi1-x]O3, 0<x<1) | 500-6000 | |
| Сополимеры | - | - | до 100000 |
machinepedia.org
Диэлектрическая проницаемость - нефть - Большая Энциклопедия Нефти и Газа, статья, страница 2
Диэлектрическая проницаемость - нефть
Cтраница 2
Диэлькометрический метод измерения влажности основан на контроле диэлектрической проницаемости смеси нефти и воды, заполняющей полость между электродами емкостного преобразователя; т.к. диэлектрическая проницаемость нефтей 2 - 2 7, а воды - 80, то результирующая проницаемость смеси зависит от соотношения количества нефти и воды. [16]
Величина емкости той части преобразователя, где в рабочем зазоре имеется только нефть, определяется толщиной зазора и толщиной слоя изоляции 5, а также диэлектрическими проницаемостями нефти и изоляции. [17]
Таким образом, использование диэлькометрического преобразователя при создании влагомеров предусматривает необходимость-корректировки показаний на сорт нефти. Диэлектрическая проницаемость нефтей зависит от температуры. [18]
Если подаваемая в емкостные преобразователи нефть обезвожена, на выходе генератора Г нет напряжения. При наличии в нефти примеси воды диэлектрическая проницаемость нефти изменяется, изменяя емкость емкостного преобразователя ПЕ, что, в свою очередь, вызывает изменение частоты генератора Г автоматического измерителя емкости АИЕ-1. На выходе частотного дискриминатора ЧД возникает электрический сигнал, который усиливается усилителем У и подается на обмотку реверсивного электродвигателя РД. Двигатель начинает вращать конденсатор С, установленный на его валу, до тех пор, пока не будет скомпенсирована частотная расстройка генератора и на выходе частотного дискриминатора не пропадет сигнал. [19]
Од - нако присутствующие в нефти полярные и неполярные компоненты способствуют приближению ее к слабополярным диэлектрикам. До частоты электрического поля не свыше 50 МГц диэлектрическая проницаемость нефти не зависит от частоты. С увеличением концентрации солей в воде диэлектрическая проницаемость растворов растет незначительно. [20]
Анализ экспериментальных результатов ( рис. 1) показывает, что для безводных сырых нефтей диэлектрическая проницаемость зависит от частоты. Эта зависимость обнаруживается в области частот 50кГЦ - 100 МГц, в которой диэлектрическая проницаемость нефтей уменьшается, а затем с частоты 100 МГц остается постоянной, причем для различных нефтей она несколько отличается. Таким образом, в диапазоне частот 50 кГц - 100 МГц для нефтей обнаруживается область дисперсии диэлектрической проницаемости и тангенса угла диэлектрических потерь. Максимальные значения tg6 для различных исследованных нефтей находятся вблизи частоты 10 Гц. Такая зависимость диэлектрической проницаемости и тангенса угла диэлектрических потерь обусловливается до частот 106 Гц наличием сквозной проводимости, а в мегагерцевом диапазоне ( 106 - 108) Гц - явлениями ориентационной поляризации. Поэтому мы считаем, что такая зависимость tg5 от частоты вблизи 107 Гц объясняется наличием в нефти тяжелых полярных компонентов, которые имеют область аномальной дисперсии в этом диапазоне. [22]
Плотность нефтей всех нефтяных месторождений изучена очень тщательно. Рассмотрим, какова же зависимость между плотностью и диэлектрической проницаемостью - нефтей. Миогие авторы [43] утверждают, что диэлектрическая проницаемость нефтей и нефтепродуктов пропорциональна их плотности. [24]
Влагомер ВН-2М состоит из емкостных преобразователей ПЕ и ПЕ-2, устройства подготовки нефти ПН, автоматического измерителя емкости АИЕ-1 и вторичного прибора. Анализируемая жидкость поступает в емкостные преобразователи, установленные на обводной линии в вертикальном положении для соблюдения оди-яаковых температурных условий. Если подаваемая в емкостные преобразователи нефть обезвожена, то на выходе генератора напряжения не будет. При наличии воды диэлектрическая проницаемость нефти изменяется, изменяя емкость преобразователя ПЕ, гчто, в свою очередь, вызывает изменение частоты генератора АИЕ-1. На выходе частотного дискриминатора появляется электрический сигнал, который усиливается и подается на обмотку реверсивного электродвигателя. Двигатель начинает вращать конденсатор, установленный на его валу, до тех пор-пока не будет скомпенсирована частотная расстройка генератора. Угол поворота конденсатора будет пропорционален изменению диэлектрической проницаемости нефти, а следовательно, и ее влажности. Связанная с конденсатором стрелка прибора покажет величину влагосодержания в процентах. [25]
Влагомер ВН-2М состоит из емкостных преобразователей ПЕ и ПЕ-2, устройства подготовки нефти ПН, автоматического измерителя емкости АИЕ-1 и вторичного прибора. Анализируемая жидкость поступает в емкостные преобразователи, установленные на обводной линии в вертикальном положении для соблюдения оди-яаковых температурных условий. Если подаваемая в емкостные преобразователи нефть обезвожена, то на выходе генератора напряжения не будет. При наличии воды диэлектрическая проницаемость нефти изменяется, изменяя емкость преобразователя ПЕ, гчто, в свою очередь, вызывает изменение частоты генератора АИЕ-1. На выходе частотного дискриминатора появляется электрический сигнал, который усиливается и подается на обмотку реверсивного электродвигателя. Двигатель начинает вращать конденсатор, установленный на его валу, до тех пор-пока не будет скомпенсирована частотная расстройка генератора. Угол поворота конденсатора будет пропорционален изменению диэлектрической проницаемости нефти, а следовательно, и ее влажности. Связанная с конденсатором стрелка прибора покажет величину влагосодержания в процентах. [26]
Страницы: 1 2
www.ngpedia.ru